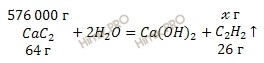Ирина Рудерфер
Высший разум
(120406)
13 лет назад
Уравнение реакции
СаС2 + 2Н2О = С2Н2 + Са (ОН) 2
молярная масса СаС2 = 40 +24 =64
Количество молей ацетилена равно количесвту молей карбида кальция, то есть 10/64, объем одного моля ацетилена равен 22,4 л, а выход равен 60%, то есть нужно брать коэффициент 0,6.
Отсюда объем ацетилена равен 10*22,4*0,6/64 =21,0375 литра
Наталия Емельянова
Высший разум
(169065)
13 лет назад
Помогите решить химию. m(CaC2)=10 г, практический выход (CaC2)=60%. Определить объём C2H2
Решение:
10*0,6—————————-Хл
CaC2+2Н2О==Са (ОН) 2+C2H2
64г——————————-22,4л
Х=10*0,6*22,4/64=2,1(л) это ответ, если условие правильное.
Получение ацетилена
Какой объем ацетилена (C2H2) может быть получен. Если для получения ацетилена (C2H2) было израсходовано 720 килограмм карбида кальция (CaC2), содержащего 20% примесей.
Решение задачи
В лабораториях ацетилен (C2H2) получают путем гидролиза карбида кальция (CaC2). Запишем уравнение реакции получения ацетилена (C2H2):
Учитывая, что карбид кальция (CaC2) содержит 20% примесей, следовательно, в состав карбида кальция (CaC2) входит 80% (если раствор 80-процентный, то массовая доля карбида кальция (CaC2) в нем 0,8.), вычислим, сколько CaC2 кг содержится в 720 кг карбида кальция (CaC2). Расчет проводим по формуле:
Получаем:
m (CaC2) = 720 ∙ 0,8 = 576 (кг) или 576 000 г.
Рассчитаем молярную массу карбида кальция (CaC2) и ацетилена (C2H2):
M (CaC2) = 40 + 2 ∙ 12 = 64 (г/моль),
M (C2H2) =2 ∙ 12 +2 ∙ 1 = 26 (г/моль).
По уравнению реакции найдем массу получения ацетилена (C2H2):
из 64 грамм CaC2 образуется 26 грамм C2H2
из 576 000 грамм CaC2 образуется грамм C2H2
Откуда:
Учитывая, что ацетилен (C2H2) – бесцветный газ, вычислим объем получения ацетилена (C2H2), по формуле перерасчета, устанавливающей связь между массой и объемом газа:
Получаем:
V(C2H2) = 234 000 ∙ 22,4/26 = 201 600 (л) или 201,6 м3.
Ответ:
получение ацетилена 201,6 м3.
Найдите правильный ответ на вопрос ✅ «Дано: CaC2 + H2O = Ca (OH) 2 + C2H2 масса (СaC2) = 128 г. Нужно найти объём (C2H2) …» по предмету 📘 Химия, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Смотреть другие ответы
Главная » Химия » Дано: CaC2 + H2O = Ca (OH) 2 + C2H2 масса (СaC2) = 128 г. Нужно найти объём (C2H2)
Светило науки – 66 ответов – 0 раз оказано помощи
Дано: m смеси (CaC2) = 150 г; w(примесей) = 24% (0,24); w выхода (C2H2) = 90% (0,9).
Найти: V(C2H2) = ?
Решение:
1) Сначала следует написать уравнение реакции:
CaC2 + 2H2O = Ca(OH)2 + C2H2
2) Теперь нужно найти массу чистого карбида кальция (CaC2), так как лишь это вещество будет вступать в реакцию, а его примеси – нет.
3) m чистого (CaC2) = (w (всего вещества, то есть 100%) – w примесей (то есть 24%)) * m смеси (CaC2) = (1 – 0,24) * 150 г = 114 г (100% перевел в 1, а 24% – в 0,24, дабы потом не возиться с тем, чтобы делить это на 100 из-за процентов)
4) Теперь необходимо найти количество вещества карбида кальция (CaC2), то есть количество моль:
Общая формула n = m / M;
M(CaC2) = 40*1 + 12*2 = 64 г/моль
n(CaC2) = 114 г / 64 г/моль = 1,8 моль.
5) Исходя из уравнения реакции видно, что количества вещества карбида кальция (CaC2) и ацетилена (C2H2) равны, так как соотношение в уравнении у них с друг другом равное (то есть 1:1), а значит n(C2H2) = 1,8 моль.
6) Найдем теоретический объем выхода ацетилена (C2H2) по формуле:
Общая формула n = V / Vm
V(C2H2) = n * Vm = 1,8 моль * 22,4 л/моль = 40,32 л.
7) Осталось лишь найти практический объем выхода ацетилена (C2H2) по формуле:
w = V практический / V теоретический * 100%
V практический = w * V теоретический = 0,9 * 40,32 л = 36,288 л. (Здесь также я заранее проценты на сто поделил, дабы потом с этим не возиться, потому умножаю сразу на 0,9 вместо 90%)
Ответ: V практический (C2H2) = 36,288 л.
Какой объём ацетилена (н.у.) образуется в результате гидролиза 320 мг карбида кальция, содержащего 2% примесей?
reshalka.com
ГДЗ учебник по химии 8 класс Габриелян. §34. Вопросы и задания. Номер №2
Решение
Дано:
m (смеси) = 320 мг;
ω (примеси) = 2 %;
Найти:
V (
C
2
H
2
) − ?
Решение:
C
a
C
2
+
2
H
2
O
=
C
a
(
O
H
)
2
+
C
2
H
2
↑
;
ω
ч
и
с
т
(
С
а
С
2
)
=
100
−
ω
(
п
р
и
м
е
с
и
)
=
100
−
2
=
98
% или 0,98;
m (вещ−во) = m (р−ра) * ω;
m (смеси) = 320 * 0,001 = 0,32 г
m
(
С
а
С
2
)
=
m
(
с
м
е
с
и
)
∗
ω
ч
и
с
т
(
С
а
С
2
)
=
0
,
32
∗
0
,
98
=
0
,
314
г;
n
=
m
M
;
M (
С
а
С
2
) = 1 * Ar (Ca) + 2 * Ar (C) = 40 + 2 * 12 = 64 г/моль;
n
(
С
а
С
2
)
=
m
(
С
а
С
2
)
M
(
С
а
С
2
)
=
0
,
314
64
=
0
,
005
моль
Запишем уравнение реакции и составим пропорции:
C
a
C
2
0
,
005
м
о
л
ь
1
м
о
л
ь
+
2
H
2
O
=
C
a
(
O
H
)
2
+
C
2
H
2
x
1
м
о
л
ь
;
x
=
n
(
C
2
H
2
)
=
0
,
005
∗
1
1
=
0
,
005
моль;
V
=
V
m
∗
n
;
V
m
= 22,4 л/моль;
V
(
C
2
H
2
)
=
V
m
∗
n
(
C
2
H
2
)
= 22,4 * 0,005 = 0,112 л = 112 мл.
Ответ. 112 мл.