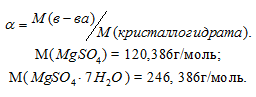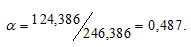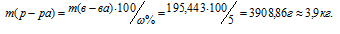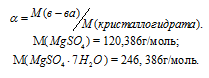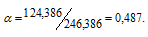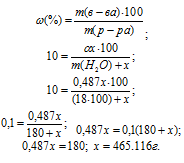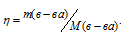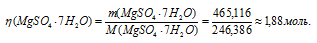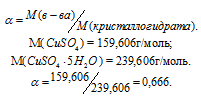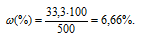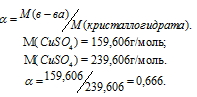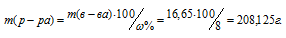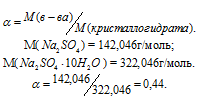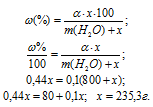определите массу сульфата магния и объём воды
Лилия Иванова
Ученик
(225),
на голосовании
9 лет назад
определите массу сульфата магния и объём воды необходимые для приготовления 200 мл раствора с концентрацией 0,5 моль/л считать плотность раствора 1 г/мл
Голосование за лучший ответ
kot
Гений
(97489)
9 лет назад
0,5 моль/л это 0,5*(24+32+16*4) г/моль = 60 г/л MgSO4
200 мл * 60 г/л * 0,001 л/мл = 12 г MgSO4
200 мл * 1 г/мл = 200 г раствора
200 г – 12 г = 188 г Н2О
Nikolau Gritsiuk
Просветленный
(28868)
9 лет назад
M (MgSO4)=120г/моль
0.5моль= 120*0,5=60г
60—–1000мл
хг——200мл
х=60*200/1000=12г MgSO4)
воды= 200-12=188г
Похожие вопросы
Найдите правильный ответ на вопрос ✅ «Найти количество вещества и объём газа (н. у.) выделившегося при взаимодействии 4,8 г магния с раствором серной кислоты …» по предмету 📘 Химия, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Смотреть другие ответы
Главная » Химия » Найти количество вещества и объём газа (н. у.) выделившегося при взаимодействии 4,8 г магния с раствором серной кислоты
Как приготовить раствор соли из её кристаллогидрата
Задача 406.
Для приготовления 5%-ного (по массе) раствора MgSO4 взято 400 г MgSO4 . 7Н2О. Найти массу полученного раствора.
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) = 
где 
Тогда
Масса MgSO4 в 400г MgSO4 . 7Н2О будет равна:
m(MgSO4) = 
Для расчета массы раствора используем формулу:

где

Отсюда
Ответ: 3,9кг.
Задача 407.
Сколько молей MgSO4 . 7Н2О надо прибавить к 100 молям воды, чтобы получить 10%-ный (по массе) раствор MgSO4?
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) = 
где

Тогда
Для расчета массы кристаллогидрата используем формулу:

где

Обозначим массу кристаллогидрата MgSO4 . 7Н2О через х, а массу MgSO4 через 
Тогда рассчитаем массовую долю MgSO4, подставив соответствующие значения в уравнение, получим
Для расчета количества кристаллогидрата используем формулу:
Отсюда
Ответ: 1,88 моль.
Задача 408.
Определить массовую долю CuSO4 в растворе, полученном при растворении 50г медного купороса CuSO4 . 5H2O в 450г воды
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением: m(в-ва) = 

Тогда
Масса раствора равна:
m(CuSO4) = 
Массовую долю CuSO4 находим из уравнения:

где

Отсюда
Ответ: 6,66%.
Задача 409.
В какой массе воды нужно растворить 25г CuSO4 . 5H2O, чтобы получить 8%-ный (по массе) раствор CuSO4?Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением: m(в-ва) = 

Тогда масса CuSO4, содержащаяся в 25г медного купороса равна:
m(CuSO4) = 
Массу полученного раствора находим из уравнения:

где

Отсюда масса раствора равна:
Тогда масса воды, которую необходимо прибавить к 25 г медного купороса, будет равна:
208,125 – 25 = 183,125г.
Ответ: 183,125г.
Задача 410.
Сколько граммов Na2SO4 . 10H2O надо растворить в 800г воды, чтобы получить 10%-ный (по массе) раствор Na2SO4?
Решение:
Масса растворённого в растворителе вещества и масса кристаллогидрата связаны между собой простым соотношением:
m(в-ва) = 
где 
Для расчета массы кристаллогидрата используем формулу:

где

Обозначим массу кристаллогидрата Na2SO4 . 10H2O через х, а массу Na2SO4 через 
Ответ: 235,3г.
Лучший ответ по мнению автора
|
|||||||||||||||
- Формула: MgO4S или MgSO4
- Относительная молекулярная масса MgO4S: 120.3676
- Молярная масса MgO4S: 120.3676 г/моль (0.12037 кг/моль)
| Элемент | Всего атомов | Атомная масса, а.е.м. | Общая масса атомов, а.е.м. |
|---|---|---|---|
| Mg (магний) | 1 | 24.305 | 24.305 |
| O (кислород) | 4 | 15.9994 | 63.9976 |
| S (сера) | 1 | 32.065 | 32.065 |
| 120.3676 |
Расчёт молярной и относительной молекулярной массы MgO4S
- Mr[MgO4S] = Ar[Mg] + Ar[O] * 4 + Ar[S] = 24.305 + 15.9994 * 4 + 32.065 = 120.3676
- Молярная масса (в кг/моль) = Mr[MgO4S] : 1000 = 120.3676 : 1000 = 0.12037 кг/моль
Расчёт массовых долей элементов в MgO4S
- Массовая доля магния (Mg) = 24.305 : 120.3676 * 100 = 20.192 %
- Массовая доля кислорода (O) = 63.9976 : 120.3676 * 100 = 53.168 %
- Массовая доля серы (S) = 32.065 : 120.3676 * 100 = 26.639 %