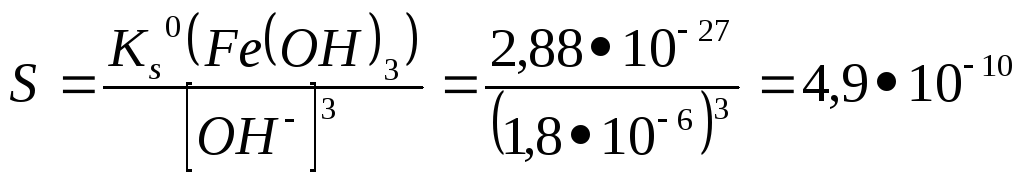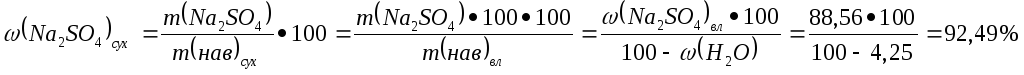Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества
Для расчета массы (объема, количества вещества) продукта реакции, если данные по одному из веществ представлены в виде раствора с определенной массовой долей этого растворенного вещества, следует воспользоваться нижеследующим алгоритмом:
1) Прежде всего следует найти массу растворенного вещества. Возможны две ситуации:
* В условии даны масса раствора и массовая доля растворенного вещества (концентрация). В этом случае масса растворенного вещества рассчитывается по формуле:
* В условии даны объем раствора вещества, плотность этого раствора и массовая доля растворенного вещества в этом растворе. В таком случае следует воспользоваться формулой для расчета массы раствора:
После чего следует рассчитать массу растворенного вещества по формуле 1.
2) Рассчитать количество вещества (моль) участника реакции, масса которого стала известна из расчетов выше. Для этого воспользоваться формулой:
3) Записать уравнение реакции и убедиться в правильности расставленных коэффициентов.
4) Рассчитать количество моль интересующего участника реакции исходя из известного количества другого участника реакции, зная, что количества веществ любых двух участников реакции A и B относятся друг к другу как коэффициенты перед этими же веществами в уравнении реакции, то есть:
Если в условии требовалось рассчитать количество вещества, то действия на этом заканчиваются. Если же требуется найти его массу или объем, следует переходить к следующему пункту.
5) Зная количество вещества, определенное в п.4, мы можем рассчитать его массу по формуле:
Также, если вещество является газообразным и речь идет о нормальных условиях (н.у.), его объем может быть рассчитан по формуле:
Рассмотрим пару примеров расчетных задач по этой теме.
Пример 1
Рассчитайте массу осадка, который образуется при добавлении к 147 г 20%-ного раствора серной кислоты избытка раствора нитрата бария.
Решение:
1) Рассчитаем массу чистой серной кислоты:
m(H2SO4) = w(H2SO4) ∙ m(р-ра H2SO4)/100% = 147 г ∙ 20% /100% = 29,4 г
2) Рассчитаем количество вещества (моль) серной кислоты:
n(H2SO4) = m(H2SO4) / M(H2SO4) = 29,4 г/98 г/моль = 0,3 моль.
3) Запишем уравнение взаимодействия серной кислоты с нитратом бария:
H2SO4 + Ba(NO3)2 = BaSO4↓ + 2HNO3
4) В результате расчетов стало известно количество вещества серной кислоты. Осадок представляет собой сульфат бария. Зная, что:
n(BaSO4)/n(H2SO4) = k(BaSO4)/k(H2SO4), где n — количество вещества, а k — коэффициент в уравнении реакции,
можем записать:
n(BaSO4) = n(H2SO4) ∙ k(H2SO4)/k(BaSO4) = 0,3 моль ∙ 1/1 = 0,3 моль
5) Тогда масса осадка, т.е. сульфата бария, может быть рассчитана следующим образом:
m(BaSO4) = M(BaSO4) ∙ n(BaSO4) = 233 г/моль ∙ 0,3 моль = 69,9 г
Пример 2
Какой объем газа (н.у.) выделится при растворении необходимого количества сульфида железа (II) в 20%-ном растворе соляной кислоты с плотностью 1,1 г/мл и объемом 83 мл.
Решение:
1) Рассчитаем массу раствора соляной кислоты:
m(р-ра HCl) = V(р-ра HCl) ∙ ρ(р-ра HCl) = 83 мл ∙ 1,1 г/мл = 91,3 г
Далее рассчитаем массу чистого хлороводорода, входящего в состав кислоты:
m(HCl) = m(р-ра HCl) ∙ w(HCl)/100% = 91,3 г ∙ 20%/100% = 18,26 г
2) Рассчитаем количество вещества хлороводорода:
n(HCl) = m(HCl)/M(HCl) = 18,26 г/36,5 г/моль = 0,5 моль;
3) Запишем уравнение реакции сульфида железа (II) с соляной кислотой:
FeS + 2HCl = FeCl2 + H2S↑
4) Исходя из уравнения реакции следует, что количество прореагировавшей соляной кислоты с количеством выделившегося сероводорода связано соотношением:
n(HCl)/n(H2S) = 2/1, где 2 и 1 — коэффициенты перед HCl и и H2S соответственно
Следовательно:
n(H2S) = n(HCl)/2 = 0,5/2 = 0,25 моль
5) Объем любого газа, находящегося при нормальных условиях, можно рассчитать по формуле V(газа) = Vm ∙ n(газа), тогда:
V(H2S) = Vm ∙ n(H2S) = 22,4 л/моль ∙ 0,25 моль = 5,6 л
Автор: С.И. Широкопояс https://scienceforyou.ru/
Как найти массу осадка
Часто бывает так, что в ходе химической реакции образуется малорастворимое вещество, выпадающее в осадок (к примеру, сульфат бария, фосфат кальция, хлорид серебра и т.д.). Предположим, химику поставлена задача: определить массу этого осадка. Каким образом можно это сделать?

Инструкция
Если вам неизвестны точные количества исходных веществ, то придется действовать опытным путем. То есть сначала отделите осадок от раствора (путем фильтрования или на обычной воронке, или с использованием воронки Бюхнера). После чего тщательно высушите его и взвесьте на аналитических весах. Так вы получите достаточно точный результат.
Ну а если вам известны точные количества веществ, вступавших в реакцию, то все будет гораздо проще. Например, изначально было 28,4 грамма сульфата натрия и 20,8 грамма хлорида бария. Сколько граммов осадка образовалось?
Напишите правильное уравнение химической реакции: Na2SO4 + BaCl2 = BaSO4 + 2NaCl.В результате этой реакции образуется практически нерастворимое вещество – сульфат бария, мгновенно выпадающий в виде плотного белого осадка.
Вычислите, какое из веществ было взято в недостатке, а какое – в избытке. Для этого подсчитайте молярные массы исходных реагентов:46 + 32 + 64 = 142 г/моль – молярная масса сульфата натрия;
137 + 71 = 208 г/моль – молярная масса хлорида бария.То есть в реакцию вступали 0,2 моля сульфата натрия и 0,1 моля хлорида бария. Сульфат натрия был взят в избытке, следовательно, весь хлорид бария прореагировал.
Подсчитайте количество образовавшегося осадка. Для этого разделите молекулярную массу сульфата бария на молекулярную массу хлорида бария и результат умножьте на количество исходного вещества:20,8 * 233/208 = 23,3 грамма.
А если бы сульфат натрия был в недостатке? Предположим, в реакцию вступило бы не 28,4 грамма этой соли, а в 5 раз меньше – всего 5,68 грамма. И тут нет абсолютно ничего сложного. 5,68 грамма сульфата натрия составляют 0,04 моля. Следовательно, в реакцию с таким количеством этой соли могло вступить также всего 0,04 моля хлорида бария, то есть 0,04 х 208 = 8,32 грамма. Прореагировало только 8,32 грамма из исходных 20,8 граммов.
Умножив эту величину на соотношение молярных масс сульфата бария и хлорида бария, получите ответ: 8,32 * 233/208 = 9,32 грамма осадка.
Источники:
- как найти массу осадка в растворе
- Вычисление молярной массы эквивалента
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Гравиметирическое
определение состоит из ряда этапов:
отбор пробы, растворение пробы, получение
осаждаемой формы, фильтрование осадка
и т.д
На
некоторых этапах определения необходимы
предварительные расчеты. Так следует
рассчитать величину навески или объем
пробы, а так же количество осадителя,
которые необходимо взять для анализа,
объем промывной жидкости, потери при
промывании осадка. Кроме того необходимо
вычислить результат с определенной
точностью.
Основные
виды расчетов приведены в настоящем
разделе.
Расчет
начальной навески или объема пробы.
Масса навески или объем жидкой пробы
для анализа зависят от массовой доли
определяемого компонента, массы
осаждаемой и гравиметрической форм,
чувствительности весов.
При
выполнении одного определения рассчитать
величину навески можно по формуле:
где
– g
– искомая навеска, г.;
m
– масса гравиметрической формы, г.;
p
– массовая доля определяемого компонента,
%;
F
– гравиметрический фактор.
Масса
гравиметрической формы определяется,
с одной стороны погрешностью весов, с
другой стороны оптимальной массой
осаждаемой формы. Погрешность аналитических
весов составляет 1·10-4
г. Относительная погрешность
гравиметрических определений не должна
превышать 0,1 %, погрешность взвешивания
должна составлять не более 0,1 % от
минимальной массы гравиметрической
формы. Отсюда
т.е.
г.
Оптимальная
масса осаждаемой формы в зависимости
от структуры осадка может колебаться
в следующих интервалах:
|
Вид |
Оптимальная |
|
Аморфный |
0,07-0,1 |
|
Кристаллический, |
0,1-0,15 |
|
Кристаллический, |
0,2-0,4 |
|
Кристаллический, |
До |
Расчет
начальной навески или объема пробы
носит приближенный характер, что
обеспечивается численными значениями
величин с двумя значащими цифрами.
Пример
1. Какую
навеску руды, содержащую около 20 % железа,
нужно взять для определения железа в
виде оксида железа.
Решение:
Осаждаемой
формой при определении является гидрат
окиси железа
,
относящийся к аморфным осадкам. Примем
массу осаждаемой формы равной 0,1 г. Масса
гравиметрической формы меньше вследствие
потери воды при прокаливании. Однако
минимальная масса гравиметрической
формы должна быть не менее 0,1 г, поэтому
полагаем m=0,1
г. F
находим по таблицам. (см. Лурье Ю.Ю.
Справочник по аналитической химии. М.:
Химия, 1979. 480 с.)
г.
Пример
2. Рассчитайте
навеску почвы для определения влажности,
если предположительная влажность не
превышает 8 %.
Решение:
Минимальная
потеря массы при высушивании не должна
быть меньше 0,1 г, что составляет 8 %
навески, следовательно
г.
Пример
3. Какой
объем раствора, содержащего 0,9 % (по
массе) хлорида натрия (ρ=1 г/см3),
следует взять для анализа, чтобы масса
весовой формы
составила 0,36 г.
Решение:
Составим
схему определения и найдем стехиометрические
соотношения между элементами схемы
.
Найдем
сколько потребуется хлорида натрия для
получения 0,36 г. хлорида серебра

Учитывая
приближенный характер вычислений примем
плотность раствора равной 1,0 мг/см3
и рассчитаем объем раствора
мл
Расчет
объема раствора осадителя.
Принято считать осаждение практически
полным, если количество осаждаемой
формы, остающейся в растворе, не превышает
погрешности взвешивания (1·10-4
г.). Для
более полного выделения осаждаемого
иона добавляют избыток осадителя по
сравнению с рассчитанной по уравнению
реакции.
Если
осадитель летучий, то рекомендуется
использовать 2-3-кратный избыток, в случае
же нелетучего осадителя ограничиваются
введением 30-50 %-ного избытка.
Пример
4. Сколько
миллилитров 5 %-ного раствора нитрата
серебра необходимо для количественного
осаждения хлорида серебра из 200 мл 0,01
М раствора
соляной кислоты?
Решение:
Рассчитываем стехиометрическое
количество нитрата серебра по уравнению
реакции:
в
200 мл раствора 1·10-2
М раствора соляной кислоты содержится
0,073 г. соляной кислоты, поэтому
Учитывая
приближенный характер вычислений,
принимаем плотность 5%-ного раствора
нитрата серебра равной единице и находим
мл.
Поскольку
нитрат серебра – нелетучие вещество,
для количественного осаждения
холорид-ионов следует взять 30%-ный
избыток осадителя. Следовательно,
мл.
Пример
5. Какой
объем 0,1 М раствора соляной кислоты
необходимо взять для количественного
осаждения хлорида серебра из 200 мл
раствора, содержащего 0,10 г нитрата
серебра.
Решение.
Вычисляем необходимое количество
соляной кислоты по уравнению реакции
осаждения (см. пример 4).
г.
Учитывая
приближенный характер вычислений
принимаем плотность 0,1 М раствора соляной
кислоты равной единице, поэтому
мл.
Поскольку соляная
кислота летучая, для полного осаждения
ионов серебра можно взять ее в 2 раза
больше, т.е. 12 мл.
Расчет
объема промывной жидкости.
Концентрация примесей cn,
остающихся в осадке после n-го промывания,
выражается формулой:
где
– с0–
концентрация примесей в исходном
растворе;
V-
объем одной порции промывной жидкости;
V0
– объем жидкости, удерживаемой осадком;
Зная
с0,
можно
вычислить массу примесей в осадке:
(моль)
или
(мол.
Масса примеси, г.)
Теоретически
рассчитанное количество примеси
несколько меньше действительно
остающегося в осадке, так как примеси
удерживаются осадком и вследствие
окклюзии.
Использовать
большой объем промывной жидкости нельзя,
поскольку потери за счет растворимости
могут превысить погрешность взвешивания.
Можно рассчитать потери при промывании
за счет растворимости осадка, исходя
из произведения растворимости и состава
промывной жидкости.
Пример
6. Сравните
количество примесей, оставшихся в
осадке, при промывании сульфата бария
100 мл воды порциями по 10 мл и по 20 мл, если
объем удерживаемой воды равен 1 мл, а
концентрация примесей в исходном
растворе составляет 1·10-2
М.
Решение.
Находим концентрацию примесей, оставшихся
в осадке после
–
десятикратного промывания:
М
-
пятикратного
промывания:
М
Промывание десятью
порциями, меньшими по объему, эффективнее,
чем промывание пятью порциями большего
объема.
Пример 7. Какое
максимальное количество воды можно
использовать доля промывания осадка
сульфата бария массой 1 г?
Решение:
Погрешность гравиметрического определения
не должна превышать 0,1 %; таким образом,
потеря осадка должна быть не более
1·10–3 г или 4·10-6 М. Рассчитываем
растворимость сульфата бария в воде
(принимая коэффициенты активности
равными единице)
М
следовательно объем
воды для промывания не может быть больше,
чем
л.
Расчет
потерь при промывании осадков.
Этот расчет выполняют на основе закона
действия масс применительно к равновесиям
растворимости осадков в водных растворах.
Обычно применяют допустимую потерю
массы осадка не более 1·10-4
г, чтобы она не сказывалась на результатах
взвешивания. Поскольку численные
значения величины произведений
растворимости (Ks0)
известны с погрешностью 5-10 % (см. Лурье
Ю.Ю. Справочник по аналитической химии.
М.: Химия, 1979. 480 с.) , удовлетворительную
достоверность численных значений в
расчетах получают при использовании
1-2-х значащих цифр.
Пример
8. Сколько
граммов свинца будет потеряно за счет
растворимости сульфата свинца при
осаждении из 100 мл 1,00·10-3
М раствора нитрата свинца эквивалентным,
полуторакратным избытком серной кислоты.
Решение.
Реакция
осаждения свинца:
.
Для расчета воспользуемся произведением
растворимости, пренебрегая изменением
объема раствора при осаждении и реакцией
образования гидросульфат-ионов.
При
добавлении эквивалентного количества
серной кислоты
М.
Это
соответствует содержанию свинца в 100
мл раствора:
г.
В
присутствии избытка осадителя:
Условие
полуторакратного избытка серной кислоты
означает, что концентрация сульфат-иона
в растворе равна 2,5·10-3
М. Следовательно,
М.
Или
в пересчете на 100 мл раствора
г.
Пример
9. Рассчитайте
потери при промывании осадка гидроксида
железа (в граммах) при промывании 0,2 л
аммиачного буферного раствора (0,125 М
аммиака и 1,25 М хлорида аммония).
Решение.
Задача
сводится к расчету растворимости
гидроксида железа при данной концентрации
гидроксид-ионов. Вычисляем концентрацию
гидроксид-ионов при заданных концентрациях
компонентов буферного раствора:
М.
Находим
растворимость гидроксида железа
(принимая коэффициенты активности
равными единице):
М.
С
учетом объема промывной жидкости
рассчитываем потерю осадка:
г.
Пример
10. Сколько
граммов кальция будет потеряно при
промывании моногидрата оксалата кальция
0,2 л воды и таким же объемом 0,1 %-ного
раствора оксалата аммония?
Решение.
Осадок
частично растворяется в промывной
жидкости, поэтому задача сводится к
расчету растворимости осадка в воде в
присутствии одноименного иона.
Пренебрегаем влиянием ионной силы и
протеканием конкурирующих химических
реакций. Если осадок промывают водой
то,
М.
Если
промывают раствором оксалата аммония,
то
М.
С
учетом объема промывной жидкости потери
из-за растворимости при промывании
водой составляют:
г.
Обработка
результатов гравиметрического анализа.
Конечным этапом гравиметрического
анализа является расчет результатов
определения. При этом следует обратить
внимание, что достоверность вычисленного
результата должна соответствовать
наименьшей достоверности измеренных
величин.
Содержание
массовой доли (ω) определяемого компонента
в анализируемом образце рассчитывается
по формуле:
где
– F-
гравиметрический фактор, который
отражает содержание определяемого
компонента
в гравиметрической форме и выражается
формулой:
где
– a,
b
– стехиометрические коэффициенты при
определяемом элементе в
гравиметрической
форме и определяемом компоненте
соответственно.
Пример
11. Рассчитать
гравиметрический фактор при определении
магния в виде фосфата магния-аммония.
Решение.
Гравиметрической формой в данном случае
служит пирофосфат магния
.
Пример
12. Вычислите
гравиметрический фактор при определении
калия по схеме:
.
Решение.
Находим стехиометрические соотношения
между соединениями схемы:
Определяем
гравиметрический фактор:
Пример
13. Каково содержание оксида кальция
в известняке, если при определении
кальция из навески 0,4000 г получено 0,4340
г сульфата кальция?
Решение.
Находим
стехиометрические соотношения:
Находим
гравиметрический
фактор:
Рассчитываем
содержание оксида кальция в изветняке.
Пример
14. Из 25,00
мл раствора сульфата меди получен осадок
массой
0,2144 г. Вычислите массовую концентрацию
ионов в растворе.
Решение.
Находим
стехиометрические соотношения:
Находим
массу ионов меди:
Определяем
массовую концентрацию тонов меди:
г.
Пересчет
результатов анализа на сухое вещество.
Во влажном или воздушно-сухом состоянии
в веществе присутствует внешняя
(гигроскопическая) влага. Удаляя эту
влагу высушиванием при 10-110 ºС получают
сухое (абсолютно сухое) вещество.
Различают
также кристаллизационную (кристаллогидратную,
гидратную) воду, которая входит в состав
химических соединений и удаляется при
более высоких температурах, например
,
Для
вычисления массы компонента в сухом
веществе его массу относя к массе сухой
пробы.
Пример
15.
Для анализа взяли 0,1534 г технического
сульфата натрия и после обработки его
хлоридом бария получили 0,2233 г сульфата
бария. Рассчитайте массовую долю сульфата
натрия во влажной и сухой навеске соли,
если влажность составляет 4,25 %.
Решение.
Определяем массу сульфата натрия по
полученному осадку сульфата бария:
Определяем
массовую долю сульфата во влажной
навеске:
Определяем
массовую долю сульфата в сухой навеске:
Как вычислить массу осадка
В ходе химической реакции могут образоваться самые разные вещества: газообразные, растворимые, малорастворимые. В последнем случае они выпадают в осадок. Часто возникает необходимость узнать, какова точная масса образовавшегося осадка. Каким образом это можно вычислить?
Можете действовать опытным путем. То есть, проведите химическую реакцию, тщательно отделите образовавшийся осадок от фильтрата с помощью обычной стеклянной воронки и бумажного фильтра, например. Более полное отделение достигается с помощью вакуумной фильтрации (на воронке Бюхнера).
После этого осадок высушите – естественным путем или под вакуумом, и взвесьте с возможно большей точностью. Лучше всего, на чувствительных лабораторных весах. Вот так будет решена поставленная задача. К этому методу прибегают, когда неизвестны точные количества исходных веществ, вступивших в реакцию.
Если же вам известны эти количества, тогда задачу можно решить гораздо проще и быстрее. Предположим, необходимо вычислить, сколько хлористого серебра образовалось при взаимодействии 20 грамм хлористого натрия – поваренной соли – и 17 грамм азотнокислого серебра.Прежде всего, напишите уравнение реакции:NaCl+AgNO3 = NaNO3 + AgCl.
В ходе этой реакции образуется очень мало растворимое соединение – хлорид серебра, выпадающий в виде белого осадка.
Подсчитайте молярные массы исходных веществ. Для хлористого натрия она примерно составляет 58,5 г/моль, для азотнокислого серебра – 170 г/моль. То есть, изначально по условиям задачи вы имели 20/58,5 = 0,342 моля хлористого натрия и 17/170 = 0,1 моля азотнокислого серебра.
Таким образом, получается, что хлористый натрий изначально был взят в избытке, то есть, реакция по второму исходному веществу пройдет до конца (прореагируют все 0,1 моля азотнокислого серебра, «связав» те же 0,1 моля поваренной соли). Сколько же образуется хлористого серебра? Для ответа на этот вопрос, найдите молекулярную массу образовавшегося осадка: 108 + 35,5 = 143,5. Умножив изначальное количество азотнокислого серебра (17 грамм) на соотношение молекулярных масс продукта и исходного вещества, получите ответ: 17* 143,5/170 = 14,3 грамма.Вот такова будет точная масса осадка, образовавшегося в ходе реакции.
Как найти массу выпавшего осадка?
Мастер
(1476),
закрыт
10 лет назад
Алекс- 89
Гений
(85771)
10 лет назад
1. Находим количество вещества NaCl:
20 г : 58,5 г/моль = 0,342 моль.
2. Находим количество вещества AgNO3:
20 г : 186 г/моль = 0,108 моль.
3. Теперь мы видим, что хлорид натрия у нас в избытке. Следовательно, полностью он не прореагирует. Нужно вести расчёты по веществу, которое находится в недостатке, а именно по AgNO3.
4. ню (AgCl) = ню (AgNO3) = 0,108 моль.
5. Находим массу AgCl:
0,108 моль * 143,5 г/моль = 15,498 г = примерно 15,5 г.
Ответ: m (AgCl) = 15,5 г.