Максимальное количество воздуха, которое вы вдыхаете и выдыхаете, является жизненной емкостью ваших легких. Существует несколько важных параметров вдоха/выдоха (о них мы обязательно расскажем), которые помогают измерить объем легких даже в домашних условиях.
Источник: https://medvisor.ru/articles/lekarstva-i-protsedury/kak-uznat-svoy-obem-legkikh/
Что такое объем легких?
Так называют количество воздуха, которое проходит через дыхательную систему за один дыхательный цикл. Это очень важный параметр, поскольку от него зависит сатурация – то есть насыщение внутренних органов и тканей кислородом.
В норме взрослый человек делает от 16 до 20 вдохов, при этом средний объем легких у взрослого мужчины может достигать 6 литров (в среднем 4–5 литров), у женщины – 4 литра.
Designed by cookie_studio/freepik
Есть и множество индивидуальных особенностей:
-
Тип телосложения. У худых и высоких объем легких в среднем больше, чем у низкорослых и коренастых;
-
Масса тела. У людей с ожирением, как правило, объем легких на 10–11% ниже. Вероятно, это одна из причин, почему тучные тяжелее переносят COVID-19;
-
Курение. Табачный дым постепенно уменьшает жизненный объем легких;
-
Перенесенные или хронические заболевания дыхательной системы (эмфизема, пневмония, ХОБЛ, туберкулез и т.п.) также уменьшают жизненный объем легких;
-
Проживание в условиях высокогорья. У горцев объем легких выше, чем у живущих на равнине из-за более разреженного воздуха;
-
Пожилой возраст. По мере старения объем легких постепенно уменьшается – это физиологическая норма;
-
Беременность. При вынашивании ребенка матка давит на все внутренние органы, включая диафрагму, объем поступающего воздуха уменьшается. Именно поэтому женщины во время беременности могут страдать от кислородного голодания, приступов головокружения и т.п.
Вопреки общему заблуждению занятия спортом и дыхательная гимнастика НЕ увеличивают физический объем легких. Однако они помогают лучше и эффективнее использовать поступающий кислород за счет укрепления дыхательных мышц и диафрагмы
По этой причине, к примеру, средний пульс у тренированных бегунов ниже, чем у обычных людей, им просто не требуется столько кислорода и дышать можно реже.
Параметры объема легких
Поскольку человек в состоянии покоя почти никогда не дышит полной грудью, в медицине выделяют несколько основных параметров объема легких.
-
Дыхательный объем (ДО, TV) – сколько воздуха проходит через легкие при спокойном ровном дыхании. В среднем у взрослого составляет около 500 см3;
-
Резервный объем вдоха (РОвд, IRV) – то есть, сколько воздуха человек может ещё пустить в легкие после того, как уже вдохнул. В среднем также у взрослого равен 1500 см3;
-
Резервный объем выдоха (РОвыд, ERV) – сколько воздуха человек может выдохнуть ещё после того, как уже сделал выдох. Также как и при Ровд среднее значение – 1500 см3;
-
Остаточный объем легких (ОО, RV) – это объем резервного воздуха, который задерживается в легких, когда человек сделает максимальный выдох. Последний остаточный запас, как правило, не измеряется.
На основе четырех этих параметров врачи оценивают несколько показателей объема легких:
-
Общая емкость легких (ОЕЛ, TLC) – это сумма всех четырех объемов легких;
-
Жизненная емкость легких (ЖЕЛ, VC) – сумма Ровд, РОвыд и дыхательного объема. В сумме она составляет примерно 3500 см3, однако, у спортсменов может быть увеличена на 1000–1500 см³. Самые развитые легкие при этом у пловцов. К примеру, ЖЕЛ олимпийского чемпиона Майкла Фелпса на пике карьеры был равен примерно 6500 см3;
-
Функциональная остаточная емкость (ФОЕЛ, FRC) – объем воздуха в легких после спокойного выдоха. ФОЕ = РОвыд + ОО;
-
Ёмкость вдоха (IC) – сколько воздуха попало в легкие за один вдох. Сумма дыхательного объема и резервного объема вдоха.
Как правило, эти показатели замеряются с помощью специального прибора – спирометра. Однако он позволяет снимать и другие показания, например, пиковую скорость потока в момент выдоха и ещё множество параметров. Это очень важно при оценке поражения легких, например, при раке.
Объем легких: норма у здорового человека (Таблица)
Как уже было сказано, индивидуальный объем легких у людей может быть разным. Однако он должен укладываться в рамки физиологической нормы.
|
Объем |
Средний объем (литры) |
Вычисление |
|
|
мужчины |
женщины |
||
|
Жизненная емкость легких |
4,8 |
3,1 |
IRV + TV + ERV |
|
Емкость вдоха |
3,8 |
2,4 |
IRV + TV |
|
Функциональная остаточная емкость |
2,4 |
1,8 |
ERV + RV |
|
Общая емкость легких |
6,0 |
4,2 |
IRV + TV + ERV + RV |
Как измерить объем легких в домашних условиях с помощью воздушного шарика
Для полноценной проверки здоровья легких вам лучше записаться на обследование к пульмонологу. Если будут показания (одышка, сильный кашель, тахикардия), он направит вас на спирометрию
Designed by standret/freepik
Однако любопытства ради в домашних условиях тоже можно измерить объем легких. Правда, результаты могут быть не совсем точными. Для этого понадобится воздушный шарик круглой формы (это важно!).
Как измерить дыхательный объем (ДО, TV):
-
Перед началом измерений нормализуйте пульс и артериальное давление. То есть за минимум полчаса до замеров нельзя выполнять никаких физических упражнений. Желательно вообще лечь и полежать;
-
Расправьте шарик, чтобы удалить из него весь воздух;
-
Сделайте свой обычный вдох и затем такой же выдох;
-
Завяжите шарик, положите его на ровную поверхность (доска, стол) и поставьте рядом линейку. Замерять нужно по верхней и нижней точкам;
-
Сделайте как минимум три таких замера и затем вычислите среднее арифметическое (складываем три результата и делим на три).
Как измерить жизненную ёмкость лёгких (ЖЁЛ, VC):
-
Подготовка та же самая (отдых, нормализация пульса);
-
Повторите процедуру тем же образом, но на этот раз вдохните максимально глубоко, а затем выдохните как можно сильнее;
-
Также сделайте три таких же замера и вычислите среднее арифметическое.
Как ещё можно измерить объем легких в домашних условиях
Есть и более замороченный способ, требующий некоторых подручных приспособлений. Что вам понадобится:
-
Мерный стакан;
-
Пятилитровая пластиковая бутылка;
-
Ручка или маркер;
-
Длинный резиновый шланг;
-
Емкость с водой (например, таз).
+2
Designed by bbc
Как это работает (см. слайды):
-
Отмерьте 200 мл воды с помощью мерного стакана и поставьте метку на том уровне, на который она поднялась;
-
Далее нужно нарисовать мерную шкалу до самого верха бутылки;
-
Переверните её в таз с водой горлышком вниз, предварительно вставив один конец шланга внутрь. Нужно, чтобы он не поднимался над поверхностью воды;
-
Вдохните полной грудью и со всей силы выдуйте воздух через шланг;
-
Подсчитайте, на сколько линий вверх поднялся уровень воды и умножьте это число на 200;
-
Для надежности сделайте ещё два замера и так же, как в случае с шариком найдите среднее арифметическое. Это и будет ваш показатель ЖЁЛ.
Опять-таки оговоримся, домашние способы измерения объема легких не дают полной картины и не позволяют диагностировать какое-либо заболевание. Однако они дают наглядное представление о том, насколько хорошо функционирует ваша дыхательная система.
Легочные объемы и емкости
Для функциональной
характеристики дыхания принято
использовать различные легочные объемы
и емкости. Легочные объемы подразделяются
на статические и динамические. Первые
измеряют при завершенных дыхательных
движениях. Вторые измеряют при проведении
дыхательных движений и с ограничением
времени на их выполнение. Емкость
включает в себя несколько объемов.
Объем
воздуха в легких и дыхательных путях
зависит от следующих показателей: 1)
антропометрических индивидуальных
характеристик человека и строения
дыхательной системы; 2) свойств легочной
ткани; 3) поверхностного натяжения
альвеол; 4) силы, развиваемой дыхательными
мышцами.
Дыхательный
объем (ДО)
— объем
воздуха, который вдыхает и выдыхает
человек во время спокойного дыхания
(рис. 5). У взрослого человека ДО составляет
примерно
500 мл.
Величина ДО зависит от условий измерения
(покой, нагрузка, положение тела). ДО
рассчитывают как среднюю величину
после измерения примерно шести спокойных
дыхательных движений.
Резервный объем
вдоха (РО вд)
— максимальный
объем воздуха, который способен вдохнуть
испытуемый после спокойного вдоха.
Величина РО вд составляет
1,5—1,8 л.
Резервный объем
выдоха (РО выд)—максимальный
объем воздуха, который человек
дополнительно может выдохнуть после
спокойного выдоха. Величина РО выдоха
ниже в горизонтальном положении, чем
в вертикальном, уменьшается при ожирении.
Она равна в среднем
1,0—1,4 л.
Остаточный объем
(ОО) —
объем воздуха, который остается в легких
после максимального выдоха. Величина
остаточного объема равна
1,0—1,5 л.
Исследование
динамических легочных объемов представляет
научный и клинический интерес, и их
описание выходит за рамки курса нормальной
физиологии,
Легочные емкости.
Жизненная емкость легких (ЖЕЛ) включает
в себя дыхательный объем, резервный
объем вдоха, резервный объем выдоха. У
мужчин среднего возраста ЖЕЛ варьирует
в пределах
3,5—5,0 л и
более. Для женщин типичны более низкие
величины
(3,0—4,0 л).
В зависимости от методики измерения
ЖЕЛ различают ЖЕЛ вдоха, когда после
полного выдоха производится максимально
глубокий вдох и ЖЕЛ выдоха, когда после
полного вдоха производится максимальный
выдох.
Емкость вдоха
(Е вд) равна
сумме дыхательного объема и резервного
объема вдоха. У человека Е вд составляет
в среднем 2,0-2.3
л.
Рисунок 5. Легочные
объемы и емкости
Функциональная
остаточная емкость (ФОЕ)
— объем
воздуха в легких после спокойного
выдоха. ФОЕ является суммой резервного
объема выдоха и остаточного объема. ФОЕ
измеряется методами газовой дилюции,
или «разведения газов» и плетизмографически.
На величину ФОЕ существенно влияет
уровень физической активности человека
и положение тела: ФОЕ меньше в горизонтальном
положении тела, чем в положении сидя
или стоя. ФОЕ уменьшается при ожирении
вследствие уменьшения общей растяжимости
грудной клетки.
Общая емкость
легких (ОЕЛ)
—
объем воздуха в легких по окончании
полного вдоха. ОЕЛ рассчитывают двумя
способами:
ОЕЛ
= 00 + ЖЕЛ
или ОЕЛ
= ФОЕ
+ Евд. ОЕЛ
может быть измерена с помощью плетизмографии
или методом газовой дилюции.
Измерение легочных
объемов и емкостей имеет клиническое
значение при исследовании функции
системы внешнего дыхания у здоровых
людей и при диагностике заболевания
легких.
Соседние файлы в папке Дыхание
- #
- #
Использование метода спирометрии
Утратил силу — Архив
Версия: Клинические рекомендации РФ 2013-2017 (Россия)
Категории МКБ:
Болезни органов дыхания (J00-J99)
Разделы медицины:
Пульмонология
Общая информация
Краткое описание
Российское респираторное общество
ФЕДЕРАЛЬНЫЕ КЛИНИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ИСПОЛЬЗОВАНИЮ МЕТОДА СПИРОМЕТРИИ
ОПРЕДЕЛЕНИЕ
Спирометрия
представляет собой неинвазивный метод измерения воздушных потоков и объемов как функции времени с использованием форсированных маневров [1].
ПОКАЗАНИЯ [2]:
Диагностика:
1) установление причины респираторных жалоб больного, клинических симптомов либо отклонений в лабораторных показателях;
2) оценка влияния болезни на легочную функцию;
3) скрининг популяций людей с высоким риском легочных заболеваний;
4) предоперационная оценка риска;
5) оценка прогноза заболевания;
6) оценка функционального состояния перед участием пациента в программах с физическими нагрузками высокого уровня.
Наблюдение
1) оценка эффективности лечебных мероприятий;
2) мониторирование течения заболевания с нарушением легочной функции;
3) наблюдение за популяциями лиц, подвергающихся воздействию неблагоприятных факторов;
4) мониторирование побочных эффектов лекарств с известной способностью вызывать повреждения легких.
Экспертная оценка нетрудоспособности
1) обследование больного перед началом реабилитации;
2) оценка рисков как части экспертной оценки нетрудоспособности;
3) экспертная оценка состояния здоровья по другим юридическим поводам.
Общественное здоровье
1) эпидемиологические исследования;
2) расчет должных значений спирометрических показателей;
3) клинические исследования .
ПРОТИВОПОКАЗАНИЯ
Спирометрия не имеет абсолютных противопоказаний, но маневр форсированного выдоха следует выполнять с осторожностью:
1) у больных с развившимся пневмотораксом и в течение 2 нед после его разрешения [3];
2) в первые 2 недели после развития инфаркта миокарда, после офтальмологических и полостных операций [3];
3) выраженном продолжающемся кровохарканье [3];
4) тяжелой бронхиальной астме [3].
Лечение
ТЕХНИЧЕСКИЕ УСЛОВИЯ
Все спирометры должны удовлетворять минимальным техническим требованиям, которые достаточны для повседневной клинической практики. Соблюдение этих требований необходимо для точности измерений и минимизации вариабельности результатов. В отдельных ситуациях, например, в некоторых клинических исследованиях, объем технических требований может быть увеличен.
Спирометр должен позволить оценивать объем воздуха в течение ≥15 сек и измерять объемы не менее 8 л с точностью как минимум ± 3%, или ± 0,05 л, а воздушные потоки – от нуля до 14 л/с [2]. Для оптимального контроля за качеством измерений спирометр должен оснащаться дисплеем, на котором отражается кривая поток-объем или объем-время, для визуальной оценки каждого выполненного маневра перед началом следующего. Для оценки воспроизводимости повторных маневров в течение одного исследования желательно, чтобы все кривые в данном исследовании накладывались на дисплее друг на друга.
Калибровка спирометра
Все спирометрические параметры измеряют при условиях окружающей среды ATPS-условиях измерения (ambient temperature pressure saturated = лабораторные условия): температура (Татм.) и давление (Ратм.) окружающей среды, при полном насыщении водяным паром (РН2О = давление насыщенного пара при Tатм.). Далее необходимо преобразовать полученные данные в условия измерения BTPS (body temperature pressure saturated = условия организма): температура тела (37 °С = 310 K), окружающее давление (Pатм.) и полное насыщение водяным паром (РН2О = 6,3 кПа) [2]. При калибровке спирометра должны вноситься соответствующие поправки.
Как правило, все спирометры рассчитаны на работу при температуре окружающего воздуха не менее 17 °С и при снижении температуры ниже этого значения могут искажать результаты измерений. Если спирометр рассчитан на работу при более низких температурах, это должно быть указано в инструкции от производителя [2].
Перед началом работы необходимо калибровать спирометр (табл. 1); это неотъемлемая часть международных требований качественной лабораторной практики.
Калибровка – процедура, во время которой устанавливается взаимосвязь между параметрами потоков и объемов, рассчитанными сенсором, и реальными величинами. Помимо этого, существует процедура проверки калибровки, во время которой исследователь удостоверяется, что спирометр по-прежнему находится в пределах калибровки (±3% от параметров калибровки) [2]. Если спирометр не соответствует параметрам калибровки, выполняют новую калибровку.
Проверка калибровки проводится ежедневно или чаще, если это оговорено в инструкции от производителя.
Объем шприца, используемого для калибровки объема, должен составлять 3 литра и иметь точность ±15 мл, или ±0,5% от всего диапазона измерений [2]. Калибровка самого шприца проводится с периодичностью, указанной в инструкции от производителя. Кроме того, время от времени (например, ежемесячно) шприцы следует проверять на утечку воздуха; для этого надо попытаться опорожнить шприц при закрытом выходном отверстии. Внеплановые калибровки шприца должны проводиться при его повреждении.
Калибровочный шприц должен храниться в помещении с той же температурой и влажностью воздуха, что и в помещении, где проводится спирометрия. Лучше всего хранить калибровочный шприц рядом со спирометром, но вне доступа прямых солнечных лучей и вдали от источников тепла.
Калибровка объема должна выполняться не реже чем 1 раз в день однократным введением в спирометр 3 л воздуха из калибровочного шприца [2]. Благодаря ежедневной калибровке можно выявить нарушение точности измерений в пределах одного дня. В особых ситуациях (при скрининге больших популяций, быстром изменении температуры воздуха и т.д.) требуются более частые калибровки.
Спирометры, измеряющие поток и объем, должны ежедневно проверяться на предмет утечки воздуха. Обнаружить утечку можно, создавая постоянное положительное давление ≥3 см вод.ст. (0,3 кПа) на выходе спирометра (желательно с учетом загубника). При наличии утечки объем через 1 мин снизится более чем на 30 мл через 1 мин [2].
Спирометры, измеряющие объем, не реже 1 раза в 3 мес следует калибровать пошагово на протяжении всего измеряемого диапазона с помощью калибровочного шприца или другого эквивалентного стандартного объема. Измеренный объем должен отличаться от должного не более чем на ±3,5%, или на 65 мл [2].
Спирометры, измеряющие поток, должны калиброваться ежедневно с помощью 3-литрового шприца, который опорожняют как минимум трижды с тем, чтобы получить несколько потоков между 0,5 и 12 л/с. Объем воздуха при каждом потоке должен соответствовать требованиям точности на ±3,5% [2].
Таблица 1. Варианты и периодичность калибровки спирометра [2].
| Параметр | Минимальная периодичность | Действие |
| Объем | Ежедневно | Калибровка 3-литровым калибровочным шприцем |
| Утечка воздуха | Ежедневно | Постоянное давление 3 см вод.ст (0,3 кПа) в течение 1 мин |
| Линейность | Еженедельно | Тестирование как минимум при трех разных диапазонах потока |
| Время | 1 раз в 3 мес | Проверка механического счетчика времени с помощью секундомера |
| Программное обеспечение | Обновление версии | Регистрация данных инсталляции и выполнение теста у «известного» пациента |
МЕТОДИКА ИССЛЕДОВАНИЯ
Объем легких можно измерить двумя способами. В первом случае непосредственно измеряется объем вдыхаемого или выдыхаемого воздуха и время. Строится график зависимости объема легких от времени – кривая объем–время (спирограмма) (рис.1, А). В другом случае измеряется поток и время, а объем рассчитывают, умножая поток на время. Строится график зависимости объемной скорости потока от объема легких – кривая поток–объем (рис.1, Б). Таким образом, обе кривые отражают одинаковые параметры: интегральное выражение скорости воздушного потока дает объем, который, в свою очередь, можно представить как функцию времени. И наоборот, объем выдыхаемого воздуха можно дифференцировать относительно времени, чтобы определить скорость потока. Представление результатов спирометрии в виде кривой поток–объем является наиболее простым для интерпретации и наиболее информативным.
Спирометрическое исследование можно проводить при спокойном и при форсированном дыхании.
При спокойном дыхании необходимо оценить паттерн дыхания, определить жизненную емкость легких (ЖЕЛ) и ее составляющие: резервный объем выдоха (РОвыд) и емкость вдоха (Евд). ЖЕЛ – максимальный объем воздуха, который можно вдохнуть или выдохнуть – является основным показателем, получаемым при спирометрии на фоне спокойного дыхания. Измерение ЖЕЛ может быть проведено одним из нижеследующих способов [4]:
1. ЖЕЛ вдоха (ЖЕЛвд): измерение производится пациенту в расслабленном состоянии без излишней спешки, но в то же время проводящему исследование не следует умышленно сдерживать пациента. После полного выдоха делается максимально глубокий вдох.
2. ЖЕЛ выдоха (ЖЕЛвыд): измерение производится в аналогичной манере из состояния максимально глубокого вдоха до полного выдоха.
3. Двустадийная ЖЕЛ: ЖЕЛ определяется в два этапа как сумма емкости вдоха и резервного объема выдоха.
Для определения жизненной емкости легких рекомендуется измерять ЖЕЛвд; если же это невозможно, то в качестве альтернативы может быть использован показатель ЖЕЛвыд. Двустадийная ЖЕЛ не рекомендуется для рутинного использования; однако ее определение иногда может быть полезным при обследовании больных с тяжелой одышкой.
С помощью маневра форсированного выдоха измеряют форсированную жизненную емкость легких (ФЖЕЛ) и показатели объемной скорости воздушного потока.
Измерение ФЖЕЛ может быть проведено различными способами (максимальный вдох делается после спокойного или после полного выдоха, перед форсированным выдохом делается или нет пауза). Но предшествующий маневру ФЖЕЛ вдох оказывает существенное влияние на экспираторные скоростные показатели, поэтому для получения максимальных результатов исследования мы рекомендуем после спокойного выдоха делать максимально глубокий вдох и сразу же после этого без паузы выдохнуть весь воздух с максимальным усилием. Пауза на высоте вдоха может вызвать «стрессовое расслабление» со снижением эластической тяги и увеличением растяжимости дыхательных путей, что ведет к уменьшению скорости выдоха [4].
Маневр ФЖЕЛ можно разделить на 3 этапа: максимальный вдох, форсированный выдох и продолжение выдоха до конца исследования [2]. Рекомендуется, чтобы исследователь сначала продемонстрировал пациенту правильное выполнение маневра.
Все исследования легочной функции выполняются с носовым зажимом либо зажатием ноздрей пальцами, загубник спирометра следует плотно обхватить губами и зубами. После максимально глубокого вдоха (от уровня функциональной остаточной емкости) пациент должен сделать мощный выдох с максимальным усилием, продолжая его до полного опорожнения легких. Во время маневра рекомендуется словами и жестами поощрять пациента делать максимально мощный выдох и продолжать его максимально долго. В то же время следует внимательно наблюдать за пациентом во избежание нежелательных явлений, связанных с резким и глубоким выдохом (например, синкопальных состояний). Одновременно необходимо следить за графическим отражением результатов теста на дисплее спирометра, что позволяет визуально оценить качественность маневра. Если пациент жалуется на головокружение или другое ухудшение самочувствия, следует сделать паузу до исчезновения нежелательных явлений или прекратить исследование. Уменьшение усилия при форсированном выдохе приводит к завышению спирометрических показателей и неправильной интерпретации результатов исследования [2].
Подготовка к спирометрии
Перед началом исследования рекомендуется:
1) проверить калибровку спирометра;
2) задать пациенту вопросы о недавнем курении перед исследованием, имеющихся заболеваниях, использовании лекарственных препаратов, которые могут повлиять на результаты;
3) измерить рост и вес пациента;
4) внести данные о пациенте в спирометр;
5) правильно усадить пациента перед спирометром: пациент должен сидеть с прямой спиной и слегка приподнятой головой. Спирометрию рекомендуется выполнять в положении пациента сидя в кресле с подлокотниками, но без колесиков. Если особые обстоятельства требуют проведения исследования в положении пациента стоя или каком-либо другом, это должно отражаться в протоколе исследования.
6) объяснить и показать пациенту, как правильно выполнить дыхательный маневр;
7) при наличии у пациента съемных зубных протезов не рекомендуется снимать их перед исследованием, чтобы не нарушать геометрию ротовой полости. Однако иногда плохо установленные протезы не позволяют пациенту герметично обхватывать загубник и становятся причиной утечки воздуха; в этой ситуации рекомендуется повторить дыхательный маневр после снятия протезов [2].
Курение пациента должно быть исключено как минимум за 1 час, употребление алкоголя – за 4 ч до исследования, значительные физические нагрузки – за 30 мин до исследования. Одежда пациента не должна стягивать грудную клетку и живот. В течение 2 ч перед исследованием не рекомендуется обильный прием пищи [3].
Критерии качества спирометрии
Начало исследования. Начало теста (нулевая точка, от которой начинается измерение всех временнЫх параметров спирометрии) определяется методом обратной экстраполяции. Согласно этому методу, нулевая точка – это точка пересечения касательной линии к кривой объем-время до горизонтальной оси (рис. 2). Объем экстраполяции не должен превышать 5% от ФЖЕЛ, или 0,150 л [2]. Увеличение объема экстраполяции происходит при медленном начале маневра форсированного выдоха.
Завершение исследования. Для оценки достаточного экспираторного усилия пациента и определения момента завершения теста рекомендуется использовать 2 критерия:
1) пациент не может продолжать выдох. Несмотря на активную словесную стимуляцию продолжать выдох как можно дольше пациент может прекратить дыхательный маневр в любой момент, особенно при появлении дискомфортных ощущений.
2) объем на кривой объем-время перестает меняться (<0,025 л за ≥1 сек) (кривая достигает плато), при этом длительность выдоха у детй от 5 до 10 лет не менее 3 сек, а у детей старше 10 лет и у взрослых не менее 6 сек. У пожилых пациентов с выраженной бронхиальной обструкцией для достижения плато нередко требуется больше 6 сек, однако даже в этой ситуации не рекомендуется продолжать выдох больше 15 сек. С другой стороны, плато может быть достигнуто слишком рано даже при продолжительности форсированного выдоха более 6 сек, если пациент перекрывает дыхательные пути надгортанником [2].
При несоблюдении критериев завершения теста полученные результаты не могут расцениваться как приемлемые. В то же время раннее завершение теста не является поводом для полного исключения результатов данного маневра из анализа; показатель ОФВ1, полученный в маневре с ранним завершением выдоха, вполне приемлем.
Кашель не должен прерывать дыхательный маневр. Кашель в первую секунду форсированного выдоха влияет на величину объема форсированного выдоха за первую секунду (ОФВ1).
Утечка воздухи из ротовой полости. При неплотном прилегании губ к загубнику возникает утечка воздуха из ротовой полости, что приводит к занижению спирометрических показателей. Некоторым пациентам со слабостью мышц, перенесшим мозговой инсульт или просто пожилого возраста трудно поддерживать герметичный обхват загубника губами в течение всего исследования; в таких ситуациях рекомендуется, чтобы пациент дополнительно фиксировал губы вокруг загубника пальцами рук. Иногда причиной утечки могут быть съемные зубные протезы; в этом случае рекомендуется проводить исследование со снятыми протезами.
Обструкция загубника языком возникает, если язык попадает перед загубником.
Для получения воспроизводимых результатов необходимо получить не менее трех технически удовлетворительных маневра, соответствующих перечисленным критериям приемлемости (рис. 3).
Воспроизводимость дыхательных маневров. Помимо технической приемлемости каждого маневра, необходимо оценить степень вариабельности между ними (воспроизводимость). Критерии воспроизводимости включают [2]:
– разница между двумя наибольшими ФЖЕЛ ≤150 мл;
– разница между двумя наибольшими ОФВ1 ≤150 мл;
Если абсолютные значения ФЖЕЛ не превышают 1 л, допустимая разница между маневрами должна составлять не более 100 мл.
Если разница между выполненными технически приемлемыми маневрами не соответствует этим критериям, рекомендуется провести дополнительные маневры, однако нежелательно выполнять за одно исследование более 8 маневров. Иногда между маневрами пациенту следует дать отдохнуть в течение нескольких минут.
Показатели спирометрии
С помощью маневра форсированного выдоха измеряют ФЖЕЛ и показатели объемной скорости воздушного потока (ОФВ1, отношение ОФВ1/ФЖЕЛ, максимальную усредненную объемная скорость – СОС25-75, максимальные объемные скорости на уровнях 25, 50 и 75% ФЖЕЛ, ПОСвыд) [4].
Форсированная жизненная емкость легких (ФЖЕЛ)
ФЖЕЛ – максимальный объем воздуха, который человек может выдохнуть после максимально глубокого вдоха. ФЖЕЛ снижается при многих видах патологии, а повышается только в одном случае – при акромегалии. При этом заболевании все остальные легочные параметры остаются нормальными.
Причины снижения ФЖЕЛ:
1. Патология легочной ткани (резекция легких, ателектаз); состояния, при которых уменьшается растяжимость легочной ткани (фиброз, застойная сердечная недостаточность). При обструктивных легочных заболеваниях ФЖЕЛ также снижается за счет замедления опорожнения легких.
2. Патология плевры и плевральных полостей (утолщение плевры, плевральный выпот, опухоли плевры с распространением на легочную ткань).
3. Уменьшение размеров грудной клетки. Легкие не могут расправляться и спадаться в полной мере, если движения грудной стенки (в том числе брюшного компонента) ограничены.
4. Нарушение нормальной работы дыхательных мышц, в первую очередь диафрагмы, межреберных мышц и мышц брюшной стенки, которые обеспечивают расправление и опустошение легких.
Таким образом, нетрудно установить причину снижения ФЖЕЛ в каждом конкретном случае.
Следует помнить, что ФЖЕЛ – это максимальная форсированная экспираторная жизненная емкость легких, у больных с обструктивными заболеваниями легких ФЖЕЛ может быть существенно меньше, чем ЖЕЛ, измеренная при спокойном дыхании.
При тяжелых обструктивных заболеваниях легких время выдоха может превышать 15-20 секунд, а экспираторный поток в конце маневра может быть настолько мал, что спирометр с трудом воспринимает его. Выполнение длительного форсированного выдоха может быть затруднительным и вызывать неприятные ощущения у пациента. Во избежание этих явлений вместо ФЖЕЛ в последнее время используют показатель ОФВ6 – объем воздуха, выдыхаемого за 6 секунд. У здоровых лиц ОФВ6 ненамного меньше ФЖЕЛ. Кроме того, ОФВ6 лучше воспроизводим, чем ФЖЕЛ. Отношение ОФВ1/ОФВ6 отражает степень ограничения воздушного экспираторного потока и позволяет прогнозировать снижение ОФВ1 у курильщиков. В отличие от маневра ФЖЕЛ, более короткий маневр ОФВ6, не требующий достижения плато на кривой объем-время, снижает риск развития синкопальных состояний у тяжелых больных во время исследования и уменьшает утомляемость как пациента, так и медицинского персонала. Вместе с тем должные величины ОФВ6 не вполне разработаны, поэтому пока рекомендуется по-прежнему оперировать традиционным ФЖЕЛ.
Объем форсированного выдоха за 1 секунду (ОФВ1)
Из всех показателей наиболее важным является максимальный объем воздуха, который человек может выдохнуть за первую секунду маневра ФЖЕЛ – ОФВ1. Он относительно независим от усилия, приложенного во время маневра выдоха, и отражает свойства легких и дыхательных путей. ОФВ1 – наиболее воспроизводимый, часто используемый и самый информативный показатель спирометрии.
При снижении скорости воздушного потока, например, при эмфиземе, ХОБЛ, бронхиальной астме, муковисцидозе, ОФВ1 снижается соответственно тяжести обструкции. ФЖЕЛ при этом также уменьшается, но, как правило, в меньшей степени. При рестриктивных нарушениях (ограничении расправления легких), например при легочном фиброзе, ОФВ1 также снижается. Возникает вопрос: как различить, что явилось причиной снижения ОФВ1 – рестрикция или обструкция? Для ответа на этот вопрос необходимо вычислить соотношение ОФВ1/ФЖЕЛ.
Соотношение ОФВ1/ФЖЕЛ
Важным спирометрическим показателем является отношение ОФВ1/ФЖЕЛ, которое обычно выражается в процентах и является модификацией индекса Тиффно (ОФВ1/ЖЕЛвд, где ЖЕЛвд – максимальный объем воздуха, который можно вдохнуть после полного спокойного выдоха). Объем воздуха, выдыхаемый за первую секунду, представляет собой достаточно постоянную долю ФЖЕЛ независимо от размера легких. У здорового человека это соотношение составляет 75–85%, но с возрастом скорость выдоха снижается в большей степени, чем объем легких, и отношение несколько уменьшается. У детей, наоборот, скорости воздушных потоков высокие, поэтому соотношение ОФВ1/ФЖЕЛ у них, как правило, выше – около 90%. При обструктивных нарушениях отношение ОФВ1/ФЖЕЛ снижается, поскольку ОФВ1 снижается соответственно тяжести обструкции. ФЖЕЛ при этом также уменьшается, но, как правило, в меньшей степени. При легочной рестрикции без обструктивных изменений ОФВ1 и ФЖЕЛ снижаются пропорционально, следовательно, их соотношение будет в пределах нормальных величин или даже немного выше. Таким образом, при необходимости дифференцировать обструктивные и рестриктивные нарушения оценивают соотношение ОФВ1/ФЖЕЛ.
Другие показатели максимального экспираторного потока
СОС25-75 – средняя объемная скорость в средней части форсированного экспираторного маневра между 25% и 75% ФЖЕЛ. Этот показатель можно измерить непосредственно по спирограмме либо рассчитать по кривой поток–объем. Некоторые исследователи считают, что СОС25-75 более чувствителен, чем ОФВ1, при диагностике ранних стадий бронхиальной обструкции [20], однако он имеет более широкий диапазон нормальных значений.
Максимальные объемные скорости экспираторного потока (МОС25, МОС50 и МОС75) на разных уровнях ФЖЕЛ (25%, 50% и 75%, соответственно) (см. рис. 1, В) не обладают высокой воспроизводимостью, подвержены инструментальной ошибке и зависят от приложенного экспираторного усилия, поэтому не играют существенной роли при определении типа и тяжести нарушений легочной вентиляции.
Пиковая объемная скорость выдоха (ПОСвыд), которая также называется максимальной экспираторной скоростью – показатель, который измеряется в течение короткого отрезка времени сразу после начала выдоха и выражается либо в л/мин, либо в л/сек. ПОСвыд в большей степени, чем другие показатели, зависит от усилия пациента: для получения воспроизводимых данных пациент должен в начале выдоха приложить максимум усилия. Существуют недорогие портативные приборы (пикфлоуметры) для измерения ПОСвыд в домашних условиях и самоконтроля пациентами своего состояния, что получило широкое распространение у больных с бронхиальной астмой.
Все эти показатели, как и ОФВ1, могут снижаться и у больных с рестриктивными нарушениями.
Максимальные инспираторные потоки
Современные спирометры измеряют не только экспираторные, но и инспираторные потоки, в первую очередь, максимальный инспираторный поток (или пиковая объемная скорость вдоха – ПОСвд). При этом испытуемый выполняет маневр ФЖЕЛ и затем делает максимально быстрый и полный вдох, который отражается спирометром в виде инспираторной кривой. Сочетание кривых вдоха и выдоха дает полную петлю поток–объем.
При повышенном сопротивлении дыхательных путей снижаются как экспираторные, так и инспираторные максимальные потоки. Однако в отличие от выдоха, при котором максимальные потоки ограничены, не существует механизмов, ограничивающих максимальные инспираторные потоки. Поэтому ПОСвд в большой степени зависит от приложенного усилия, а ее измерение не получило широкого распространения, за исключением выявления патологии верхних дыхательных путей.
Особенности спирометрии у детей
Спирометрия может выполнять у детей не моложе 5 лет [2]. Большинство детей начиная с возраста 9 лет способны выполнить маневр форсированного выдоха, удовлетворяющий тем же критериям, которые применимы у взрослых пациентов [5], однако для детей до 9 дет необходимо соблюдать некоторые правила. Желательно, чтобы специалист, обследующий ребенка, имел опыт выполнения функциональных исследований у детей. В лаборатории, занимающейся обследованием маленьких детей, должна быть очень доброжелательная атмосфера, можно использовать игрушки, соответствующие возрасту маленьких пациентов. Перед началом исследования ребенку следует объяснить в доступной манере, что он должен делать. Хорошие результаты дает применение визуальной «обратной связи» (изображение свечей или других картинок на дисплее спирометра, меняющихся при выполнении ребенком форсированного выдоха). Даже если первые попытки были неудачными, продолжение исследования в большинстве случаев позволяет ребенку привыкнуть к обстановке и лучше выполнить дыхательный маневр. Не рекомендуется обследовать детей в лабораториях для взрослых пациентов, в которых обстановка не адаптирована к особенностям детей [2].
Во время тестирования исследователь должен внимательно наблюдать за ребенком для своевременного устранения утечки воздуха и контроля за правильностью выполнения дыхательного маневра. [5]. Для оценки качества выполненного маневра, как и у взрослых, используют метод обратной экстраполяции. Если объем обратной экстраполяции превышает 80 мл, или 12,5 % ФЖЕЛ, этот маневр может быть сохранен для дальнейшего анализа при отсутствии других дефектов [5]. Для детей младшего возраста преждевременным завершением маневра форсированного выдоха считается прекращение маневра на уровне более 10% от пиковой скорости выдоха. ФЖЕЛ и форсированные экспираторные потоки, полученные в таком маневре, не должны использоваться для анализа [5].
В идеале, при проведении спирометрии ребенку достаточно получить 2 приемлемых кривых поток-объем, в которых ФЖЕЛ и ОФВ1 отличаются не более чем на 0,1 л, или 10% от максимальных значений. Но даже при получении единственной кривой, удовлетворяющей техническим требованиям, она может использоваться для анализа, однако в протоколе исследования должно быть отражено число технически удовлетворительных маневров и степень воспроизводимости результатов. Как и у взрослых, у детей для анализа выбирают кривую с максимальными значениями ФЖЕЛ и ОФВ1 [5].
У детей моложе 6 лет не должны использоваться должные величины, применяемые у взрослых пациентов. В литературе предложены несколько различных уравнений для расчета должных величин у детей этого возраста [5].
ИНТЕРПРЕТАЦИЯ РЕЗУЛЬТАТОВ
Выбор результата для анализа
ФЖЕЛ и ОФВ1 выбирают не менее чем из трех воспроизводимых технически приемлемых маневров. Результаты исследования анализируют по маневру с максимальными ФЖЕЛ и ОФВ1 [2].
Должные величины
Существуют различные таблицы и формулы для расчета должных величин показателей спирометрии. В большинстве случаев исследования по разработке должных величин ограничиваются уравнениями расчета средних значений, которые получают при обследовании здоровых некурящих людей. Практика использования 80% от должных значений в качестве фиксированного значения для нижней границы нормальных значений (НГН) ФЖЕЛ и ОФВ1 приемлема у детей, но может приводить к существенным ошибкам при интерпретации функции легких у взрослых. Использование 70% в качестве нижней границы нормы для отношения ОФВ1/ФЖЕЛ приводит к значительному числу ложно-положительных результатов (гиподиагностике ХОБЛ) у мужчин в возрасте старше 40 лет и у женщин старше 50 лет и к гипердиагностике ХОБЛ у пожилых лиц, никогда не куривших и не имеющих характерных клинических симптомов. Как известно, с возрастом соотношение ОФВ1/ФЖЕЛ снижается, поэтому некоторые авторы для диагностики ХОБЛ у людей старше 70 лет рекомендуют использовать для ОФВ1/ФЖЕЛ 65% порог нормы.
Для скоростных показателей НГН составляет 60% от должных значений.
При выборе должных значений необходимо сравнить данные, получаемые с помощью выбранных уравнений должных значений, с собственными измерениями, проведенными на репрезентативной выборке здоровых лиц. Следует выбрать те уравнения должных значений, при которых у взрослых разница между измеренными и рассчитанными значениями является минимальной. У детей ориентируются на минимальную разницу логарифмов измеренных и рассчитанных значений. Чтобы быть уверенным, что выбранные должные значения приемлемы, необходимо обследовать достаточно большое число добровольцев (около 100). К сожалению, это трудновыполнимо для большинства лабораторий.
При использовании должных величин следует избегать экстраполяции за указанный диапазон роста и возраста. Если все же возраст или рост пациента выходят за границы популяции, для которой были разработаны должные значения, то в интерпретации необходимо указать, что была проведена экстраполяция.
Должные величины зависят от антропометрических параметров (в основном от роста), пола, возраста, расы. Чем выше человек, тем больше его легкие и протяженность дыхательных путей и, следовательно, максимальная экспираторная скорость. При вычислении нормальных значений для людей с кифосколиозом вместо роста в формулу следует поставить размах рук. У женщин объем легких меньше, чем у мужчин такого же роста. С возрастом эластичность легочной ткани снижается, в результате происходит снижение объема и скорости выдоха. Вместе с тем следует принимать во внимание и индивидуальные вариации нормы. Например, легочные заболевания могут возникать у людей с исходными показателями легочных объемов и потоков выше среднего уровня и, несмотря на снижение их на фоне заболевания относительно исходных значений, они по-прежнему могут оставаться в пределах, нормальных для популяции в целом.
Анализ результатов спирометрии
Интерпретация результатов спирометрии строится на анализе основных спирометрических параметров (ОФВ1, ЖЕЛ, ОФВ1/ЖЕЛ).
Интерпретация результатов функционального исследования должна быть четкой, краткой и информативной. Простая констатация фактов, что какие-то показатели в норме, а какие-то снижены, не годится. В идеале, к интерпретации результатов функционального исследования должны применяться принципы клинического принятия решения, где вероятность болезни после проведения исследования оценивается с учетом вероятности болезни до проведения исследования, качества исследования, вероятности ложно-положительной и ложно-отрицательной интерпретации, и, наконец, непосредственно результатов исследования и должных значений. Это часто невозможно, потому что интерпретация многих, если не большинства, исследований проводится при отсутствии какой-либо клинической информации. Чтобы улучшить ситуацию, по возможности следует спрашивать врачей, направляющих пациента на исследование, на какой клинический вопрос необходимо ответить, а также до исследования поинтересоваться у пациента, почему его направили в лабораторию. В этом отношении также желательно записать респираторные симптомы (например, кашель, мокрота, хрипы и одышка), недавнее использование бронхорасширяющих препаратов, анамнез курения.
Интерпретация будет более точной при учете клинического диагноза, данных рентгенограммы грудной клетки, концентрации гемоглобина и любых подозрений на нейромышечные заболевания или обструкцию верхних дыхательных путей.
Обструктивные вентиляционные нарушения
Наиболее частое показание к проведению спирометрического исследования – выявление обструкции дыхательных путей и оценка ее выраженности. Обструктивный тип вентиляционных нарушений характеризуется снижением соотношения ОФВ1/ФЖЕЛ при нормальной ФЖЕЛ. Патофизиологической основной снижения максимального экспираторного потока при бронхиальной обструкции является повышение сопротивления дыхательных путей, однако при недостаточном усилии, приложенном пациентом во время выполнения маневра ФЖЕЛ, максимальный экспираторный поток также будет снижен. Дифференцировать эти ситуации можно при количественной оценке усилия пациента, измерив плевральное давление (с помощью внутрипищеводного баллона) или компрессионный объем при проведении бодиплетизмографии.
Ранними признаками обструктивных нарушений вентиляции у пациентов без клинических проявлений, возможно, могут служить изменение формы экспираторной кривой поток-объем и снижение скоростных показателей, измеренных при низких легочных объемах во время теста ФЖЕЛ (СОС25-75, МОС50, МОС75) (рис.4), однако в настоящее время не существует убедительных доказательств существования таких корреляционных связей. Более того, значительная вариабельность показателей затрудняет интерпретацию индивидуальных отклонений от должных значений.
При обструктивных нарушениях происходит снижение экспираторных потоков, и кривая пациента располагается под должной кривой (см. рис.4). Кроме того, обычное линейное снижение скорости потока на кривой поток-объем нарушается, ее нисходящее колено приобретает вогнутую форму. Нарушение линейности нижней половины кривой поток-объем является характерной чертой обструктивных нарушений вентиляции и предполагает наличие бронхиальной обструкции, даже когда ФЖЕЛ и ОФВ1 не выходят за пределы нормальных значений. Выраженность изменений формы кривой зависит как от тяжести обструктивных нарушений, так и от нозологической формы. Причиной этого чаще всего является сужение просвета дыхательных путей при бронхиальной астме, ХОБЛ, эмфиземе, муковисцидозе, сдавление крупных бронхов и трахеи опухолью извне, стенозирование эндофитно растущей опухолью, рубцовой тканью, инородным телом. При подозрении на бронхиальную астму следует провести бронходилатационный тест, а при необходимости – бронхоконстрикторный тест. Для оценки выраженности эмфиземы следует исследовать общую емкость легких и диффузионную способность легких.
Особое внимание следует уделить синхронному снижению ОФВ1 и ФЖЕЛ, при котором отношение ОФВ1/ФЖЕЛ остается нормальным или почти нормальным. Такие изменения спирограммы чаще всего наблюдаются, если пациент делает вдох или выдох не полностью или если поток настолько медленный, что для выдыхания всего воздуха из легких требуется слишком большая продолжительность выдоха. В таком случае дистальный отдел кривой поток-объем будет вогнутым (МОС75 снижена). Измерение ЖЕЛ (инспираторной или экспираторной) поможет более точно оценить отношение ОФВ1 к максимальному объему легких. Другая возможная причина одновременного снижения ОФВ1 и ФЖЕЛ – коллапс мелких дыхательных путей в начале выдоха. Если такие изменения наблюдаются при выполнении маневра с максимальным усилием, достоверный прирост ОФВ1 после ингаляции бронхолитика подтвердит наличие экспираторного коллапса. Достоверное увеличение ОФВ1, ФЖЕЛ или обоих параметров после ингаляции бронхолитика свидетельствует об обратимости обструктивных нарушений.
Обструкция верхних дыхательных путей. Форма максимальной кривой поток-объем существенно отличается от должной при обструкции верхних дыхательных путей. Своеобразная форма кривой поток-объем при поражениях верхних дыхательных путей обусловлена различным воздействием динамических факторов на экстра- и интраторакальные дыхательные пути. На экстраторакальные дыхательные пути влияет атмосферное давление, на интраторакальные – внутриплевральное. Разница между внешним давлением (атмосферным или плевральным) и давлением внутри дыхательных путей называется трансмуральным давлением. Положительное трансмуральное давление создает компрессию и уменьшает просвет дыхательных путей. Наоборот, отрицательное трансмуральное давление поддерживает дыхательные пути открытыми, увеличивая их просвет. Если обструкция возникает только во время вдоха либо выдоха, она считается переменной. Если воздушные потоки снижены во время обеих фаз дыхания, обструкция называется фиксированной.
Переменная экстраторакальная обструкция (например, при параличе голосовых связок, увеличении щитовидной железы) вызывает избирательное ограничение воздушного потока при вдохе. Во время выдоха давление внутри дыхательных путей увеличивается и превышает атмосферное, воздействующее на зону поражения снаружи, поэтому экспираторный поток меняется мало. Во время вдоха наблюдается обратная картина: атмосферное давление значительно превышает давление в дыхательных путях, что приводит к снижению инспираторных потоков. Изменения инспираторных потоков хорошо видны на кривой поток–объем (рис. 5, А).
При переменной интраторакальной обструкции (например, при опухоли нижнего отдела трахеи (ниже яремной ямки грудины), трахеомаляции, гранулематозе Вегенера или редицивирующем полихондрите) высокое внутриплевральное давление во время форсированного выдоха превышает давление в дыхательных путях, что приводит к выраженному сужению их просвета с критическим снижением экспираторных потоков. Инспираторные потоки могут мало меняться, если плевральное давление более отрицательное, чем давление в дыхательных путях. Характерная кривая поток–объем представлена на рисунке 5, Б.
При фиксированной обструкции (например, при опухолях на любом уровне верхних дыхательных путей или параличе голосовых связок с фиксированным стенозом, рубцовых стриктурах) инспираторные и экспираторные потоки нарушаются почти в одинаковой степени. Локализация поражения не имеет значения, поскольку размеры трахеи при этом не зависят от давления внутри и снаружи дыхательных путей (рис.5, В).
Для характеристики вышеуказанных поражений верхних дыхательных путей используются различные показатели, например, соотношение инспираторных и экспираторных потоков на уровне 50% жизненной емкости (МОС50вд/МОС50выд, в норме это соотношение приблизительно равно 1,5). Это соотношение наиболее значительно меняется при переменной экстраторакальной обструкции и неспецифично для другой патологии (рис.5). При подозрении на изолированную обструкцию верхних дыхательных путей следует подтвердить диагноз эндоскопически или рентгенологически.
Классификация тяжести обструктивных вентиляционных нарушений
В большинстве случаев функция легких во многом определяет способность больного к повседневной физической активности, качество жизни и прогноз заболевания, в том числе риск летального исхода не только от заболеваний органов дыхания, но и от сердечно-сосудистой патологии. Было показано, что у лиц некоторых профессий ОФВ1 и ОФВ1/ФЖЕЛ являются независимыми факторами риска летального исхода, в том числе от заболеваний органов дыхания. Кроме того, мета-анализ шести обзоров, посвященных смертности в различных профессиональных группах в Великобритании, продемонстрировал, что существует связь между риском смерти от ХОБЛ и ОФВ1. Пациенты, ОФВ1 которых при начальном обследовании был ниже среднего значения более чем на 2 SD, по сравнению с пациентами, ОФВ1 которых был не ниже 1 SD от среднего, имели в 12 раз более высокий риск смерти от ХОБЛ, в 10 раз – от неопухолевых легочных заболеваний и вдвое – от сосудистых заболеваний в течение 20-летнего периода наблюдения. Доказано, что в большинстве случаев ОФВ1 коррелирует с тяжестью симптомов и прогнозом заболевания, тем не менее корреляции не позволяют точно предсказывать тяжесть и течение болезни у конкретного пациента.
Для оценки тяжести обструктивных нарушений в большинстве случаев используют степень отклонения ОФВ1 от должного значения (табл. 2). Эту классификацию не применяют у пациентов с обструкцией верхних дыхательных путей, когда даже слабо выраженная обструкция может быть опасна для жизни.
Для определения тяжести обструктивных нарушений не рекомендуется использовать отношение ОФВ1/ФЖЕЛ, поскольку при прогрессировании заболевания ОФВ1 и ФЖЕЛ могут снижаться синхронно, а их соотношение останется при этом нормальным. Тем не менее, отношение ОФВ1/ФЖЕЛ помогает оценить тяжесть вентиляционных нарушений у людей с исходно большим объемом легких. В этих случаях ОФВ1/ФЖЕЛ может быть очень низким (50 % и менее), а ОФВ1 будет соответствовать обструкции легкой степени.
Таблица 2. Классификация тяжести обструктивных нарушений легочной вентиляции
| ОФВ1, %должн. | |
| Легкие | >70% |
| Умеренные | 60 – 69% |
| Среднетяжелые | 50 – 59% |
| Тяжелые | 35 – 49% |
| Крайне тяжелые | < 35% |
Рестриктивные вентиляционные нарушения
Рестриктивные нарушения вентиляции обусловлены процессами, снижающими растяжимость легких и, следовательно, ограничивающими наполнение легких воздухом. В начале развития патологических нарушений, когда объем легких еще не снижен, скоростные показатели и отношение ОФВ1/ФЖЕЛ могут увеличиваться вследствие того, что паренхима легких оказывает большее растягивающее действие на дыхательные пути: просвет бронхов увеличивается относительно объема легких. При прогрессировании заболевания происходит уменьшение воздушности легочной ткани. Это проявляется снижением ЖЕЛ, кривая поток-объем становится высокой и узкой (рис. 6, А). Пиковая объемная скорость обычно остается нормальной, после пика наблюдается быстрое линейное снижение потока. Форма кривой может и не меняться, а представлять собой пропорционально уменьшенную копию должной кривой, как, например, при пневмонэктомии (рис. 6, Б).
Рестриктивные нарушения могут встречаться при интерстициальных заболеваниях легких, обширной воспалительной инфильтрации легочной ткани, гипоплазии и ателектазах легкого, после резекции легочной ткани. При подозрении на интерстициальные заболевания легких следует измерить диффузионную способность легких и общую емкость легких. К рестрикции также может приводить и внелегочная патология, например, поражение грудного отдела позвоночника, ребер, дыхательной мускулатуры; высокое стояние диафрагмы, что делает невозможным выполнение глубокого полноценного вдоха; нарушение регуляции дыхания при угнетении дыхательного центра наркотическими препаратами или его повреждении опухолью, кровоизлиянием. При подозрении на мышечную слабость как причину рестрикции следует измерить силу дыхательных мышц. Кроме того, у больных с выраженной мышечной слабостью ФЖЕЛ, измеренная в вертикальном положении и в положении лежа, будет существенно различаться из-за воздействия гравитации на органы брюшной полости. В норме ФЖЕЛ в положении лежа на 5-10% меньше, чем в положении сидя. При выраженной диафрагмальной дисфункции эта разница превышает 30%.
Для диагностики рестриктивных нарушений недостаточно спирометрического исследования, а следует выполнить бодиплетизмографию и измерить легочные объемы.
Смешанные вентиляционные нарушения
Смешанные нарушения легочной вентиляции развиваются при сужении просвета дыхательных путей на фоне уменьшения легочных объемов. При этом спирометрия будет регистрировать одновременное снижение ФЖЕЛ, ОФВ1 и ОФВ1/ФЖЕЛ.
Для уточнения характера функциональных нарушений необходимо выполнять бодиплетизмографию с измерением легочных объемов.
БРОНХОДИЛАТАЦИОННЫЙ ТЕСТ
При первичном исследовании функции дыхания почти всегда желательно выполнить бронходилатационный тест (или бронходилатационную пробу), то есть повторить спирометрию после ингаляции бронходилататора.
Показания для проведения бронходилатационного теста:
1. установление обратимости бронхиальной обструкции, включая пациентов с нормальными показателями исходной спирометрии;
2. определение потенциального эффекта бронхолитической терапии;
3. мониторирование динамики легочной функции у больных с хроническими респираторными заболеваниями при длительном (многолетнем) наблюдении.
Противопоказаний к проведению бронходилатационного теста не существует за исключением тех ситуаций, в которых противопоказано выполнение спирометрии, и случаев непереносимости бронхорасширяющих препаратов. Если пациент не переносит β2-агонисты, то в качестве бронходилататора можно использовать М-холинолитик короткого действия.
Методика проведения бронходилатационного теста
Реакция на бронходилататор является интегральной физиологической реакцией, в которую вовлечены эпителий дыхательных путей, нервы, медиаторы и гладкие мышцы.
Если врач ставит задачей исследовать обратимость бронхиальной обструкции, то перед проведением бронходилатационного теста следует прекратить использование любых бронхорасширяющих препаратов на срок, соответствующий длительности их действия. Короткодействующие ингаляционные β2-агонисты (сальбутамол, фенотерол) и антихолинергические препараты (ипратропия бромид) следует отменить за 4-6 ч, пролонгированные β2-агонисты (сальметерол, формотерол) и метилксантины – за 12 ч, пролонгированные холинолитики (тиотропия бромид, гликопиррония бромид) – за 24 ч до исследования [2]. Если препараты отменить нельзя, то в протоколе исследования указывают название препарата, дозу и время последней ингаляции.
Если бронходилатационный тест проводится с целью выявить возможность дополнительного улучшения легочной функции на фоне базисной терапии заболевания, то вся плановая терапия сохраняется перед исследованием в обычном для пациента режиме [2].
Курение не допускается в течение 1 ч до и на протяжении всего тестирования.
Бронходилатационный ответ зависит от многих факторов, определяющих достоверность результатов: выбора бронходилататора и его дозы (чем выше доза, тем больше ответ), времени, прошедшего после ингаляции (как правило, реакция измеряется на пике действия препарата), способа доставки препарата в дыхательные пути (дозированный аэрозоль или небулайзер), соблюдения критериев воспроизводимости как исходной, так и повторной спирометрии и способа расчета бронходилатационного ответа. На сегодняшний день не существует единого стандарта выбора бронходилататора, дозы или способа его применения при проведении бронходилатационного теста. Однако можно минимизировать внутри- и межлабораторные различия при использовании дозированных аэрозольных ингаляторов, если придерживаться стандартных рекомендаций. Для достижения максимально возможной бронходилатации рекомендуется использовать короткодействующие β2-агонисты, например сальбутамол, в виде дозированного аэрозольного ингалятора в максимальной разовой дозе 400 мкг (четыре ингаляции по 100 мкг с интервалом в 30 сек) или фенотерол в максимальной разовой дозе 400 мкг (4 ингаляции по 100 мкг с интервалом в 30 сек) с помощью спейсера, с соблюдением всех правил ингаляционной техники для дозированных аэрозольных ингаляторов (после спокойного неполного выдоха – плавный максимально глубокий вдох с активацией ингалятора (нажатием на клавишу) одновременно с началом вдоха, задержка дыхания на высоте вдоха на 10 сек). Без использования спейсера вдыхаемая фракция аэрозоля меньше и ее величина в значительной степени зависит от синхронизации вдоха с активацией ингалятора. Повторную спирометрию проводят через 15 минут. При использовании М-холинолитика в качестве бронходилататора максимальная разовая доза составляет 160 мкг (4 дозы по 40 мкг) или их комбинации; повторную спирометрию выполняют через 30 мин [2, 7].
Интерпретация результатов бронходилатационного теста
Обратимость бронхиальной обструкции определяется по изменению ОФВ1 или ФЖЕЛ. Другие показатели спирометрии, в том числе потоки, измеренные на разных уровнях ФЖЕЛ (МОС25, МОС50, МОС75, СОС25-75), не используются для оценки обратимости обструкции дыхательных путей в связи с их крайне высокой вариабельностью [7].
Интерпретация результатов бронходилатационного ответа состоит из нескольких этапов. На первом этапе необходимо определить, превышают ли полученные данные вариабельность измерения, которая составляет <8 %, или <150 мл [2, 7]. На сегодняшний день не существует единого мнения о том, как оценивать обратимость бронхиальной обструкции. Разные исследователи используют для вычисления бронходилатационного ответа различные методы и спирометрические показатели. Самым распространенным способом выражения бронходилатационного ответа является абсолютное и относительное (в процентах от исходных значений либо от должных величин) изменение спирометрических показателей. Кроме того, как упоминалось ранее, не существует единого стандарта выбора препарата, дозы и способа введения. Тем не менее, согласно последним рекомендациям ERS и ATS, абсолютное и относительное изменение ОФВ1 и/или ФЖЕЛ (коэффициент бронходилатации – КБД) позволяют достаточно точно определить обратимость обструкции дыхательных путей [2, 7]. Бронходилатационный тест считается положительным, если после ингаляции бронходилататора КБД составляет более 12%, а абсолютный прирост – более 200 мл.
где Показательпосле – значение спирометрического показателя после ингаляции бронходилататора, Показательисх – значение спирометрического показателя до ингаляции бронходилататора [7].
Если изменение ОФВ1 и ФЖЕЛ не значимо, то о положительной реакции на бронходилататор может свидетельствовать уменьшение гиперинфляции легких (снижение общей емкости легких и остаточного объема легких и, как результат, увеличение инспираторной емкости легких) [7]. В отличие от больных с бронхиальной астмой, при ХОБЛ ответ на антихолинергические препараты не менее, а иногда и более выражен, чем при назначении β2-агонистов.
Отсутствие положительной реакции на короткодействующий бронхолитик в условиях бронходилатационного теста не означает нецелесообразности назначения этих препаратов пациенту с терапевтической целью.
Бронходилатационный тест не позволяет дифференцировать бронхиальную астму и хроническую обструктивную болезнь легких, так как при обоих этих заболеваниях могут встречаться больные как с положительной реакцией на бронхолитик, так и ее отсутствием [4].
Информация
Источники и литература
-
Клинические рекомендации Российского респираторного общества
- 1. Ferguson G.T., Enright P.L., Buist A.S., Higgins M.W. Office spirometry for lung health assessment in adults: a consensus statement from the national lung health education program // Chest. 2000;117(4):1146-1161
2. Miller M.R., Hankinson J., Brusasco V. et al. Standardisation of spirometry. Eur. Respir. J. 2005; 26: 319-338.
3. Miller M.R., Crapo R., Hankinson J. et al. General considerations for lung function testing. Eur. Respir. J. 2005; 26 (1):153-161.
4. Чучалин А.Г. (ред.) Функциональная диагностика в пульмонологии. М.: Атмосфера, 2009.
5. Beydon N., Davis S.D., Lombardi E. et al. An official American Thoracic Society/European Respiratory Society statement: pulmonary function testing in preschool children. Am. J. Respir. Crit. Care Med. 2007; 175 (12): 1304-1345.
6. Enright P.L., Studnicka M., Zielinski J. Spirometry to detect and manage chronic obstructive pulmonary disease and asthma in the primary care setting. In: Lung function testing. Eur. Respir. Mon. 2005, 31, 1–14.
7. Pellegrino R., Viegi G., Brusasco V. et al. Interpretative strategies for lung function tests. Eur. Respir. J. 2005; 26: 948-968.
- 1. Ferguson G.T., Enright P.L., Buist A.S., Higgins M.W. Office spirometry for lung health assessment in adults: a consensus statement from the national lung health education program // Chest. 2000;117(4):1146-1161
Информация
КОЛЛЕКТИВ АВТОРОВ
| Чучалин Александр Григорьевич | Директор ФГБУ «НИИ пульмонологии» ФМБА России, Председатель Российского респираторного общества, главный внештатный специалист терапевт-пульмонолог Минздрава РФ, академик РАМН, профессор, д.м.н. |
| Айсанов Заурбек Рамазанович | Заведующий отделом клинической физиологии и клинических исследований ФГБУ «НИИ пульмонологии» ФМБА России, профессор, д.м.н. |
| Чикина Светлана Юрьевна | Старший научный сотрудник лаборатории функциональных и ультразвуковых методов исследования ФГБУ «НИИ пульмонологии» ФМБА России, к.м.н. |
| Черняк Александр Владимирович |
Заведующий лабораторией функциональных и ультразвуковых методов исследования ФГБУ «НИИ пульмонологии» ФМБА России, к.м.н. |
| Калманова Елена Николаевна | Зав. отделением функциональной и ультразвуковой диагностики Городской клинической больницы №57 г. Москвы |
МЕТОДОЛОГИЯ
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Оценка качества и силы доказательств.
Поскольку международные критерии, используемые для оценки качества и силы доказательств, положенных в основу рекомендаций, не применимы к отдельным методам исследования, они не использовались при данных методических рекомендаций.
Описание разработки и валидизации рекомендаций:
Настоящие рекомендации были разработаны на основе международных документов по стандартизации спирометрии и интерпретации ее результатов.
В предварительной версии рекомендации были рецензированы независимыми экспертами, которых попросили прокомментировать прежде всего доступность рекомендаций для понимания практическими врачами.
Получены комментарии врачей первичного звена и участковых терапевтов относительно доступности изложения рекомендаций и оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Обсуждался каждый пункт, регистрировались в изменения, внесенные в рекомендации. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультация и экспертная оценка:
Предварительная версия была выставлена для широкого обсуждения на сайте РРО для того, чтобы лица, не участвовавшие в конгрессе, получили возможность участвовать в обсуждении и совершенствовании рекомендаций.
Проект рекомендаций был рецензирован также независимыми экспертами, которых попросили прокомментировать прежде всего доступность изложения и точность фактического материала, лежащего в основе рекомендаций.
Рабочая группа:
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Рисунок 1. а) Спирограмма форсированного выдоха. ФЖЕЛ – форсированная жизненная емкость легких, ОФВ1 – объем форсированного выдоха за 1 секунду, СОС25-75 – средняя скорость форсированного экспираторного потока на уровне 25-75% ФЖЕЛ. б) Нормальная петля поток-объем, полученная при максимальных вдохе и выдохе. ПОСвыд – пиковая объемная скорость выдоха. равная 10,3 л/сек; МОС25, МОС50 и МОС75 – максимальные объемные скорости, когда пациент выдохнул соответственно 25, 50 и 75% объема ФЖЕЛ, равные 8,8 л/сек, 6,3 л/сек и 3,1 л/сек. МОС50вд – максимальная объемная скорость, когда пациент вдохнул 50% ФЖЕЛ, равная 7,5 л/сек. Обычно МОС50вд в 1,5 раза больше МОС50выд.
Рисунок 2. Расчет объема обратной экстраполяции (Vоэ) = 146 мл, при форсированной емкости легких равной 3 литра, объем обратной экстраполяции=4,9 %.
Рис. 3. Наиболее частые ошибки при выполнении маневра форсированного выдоха
А – медленное начало, Б – недостаточное усилие, В – кашель, Г – ранее завершение выдоха [6].
Рисунок 4. Кривые поток-объем у больных с обструктивными заболеваниями органов дыхания: а)-б) бронхиальной астмой и в) эмфиземой легких.
Рисунок 5. Кривые поток-объем у больных с обструкцией верхних дыхательных путей: а) переменной экстраторакальной обструкцией: МОС50вд/МОС50выд<1, ПОСвыд – снижена или нет, МОС50вд – снижена; б) переменной интраторакальной обструкцией: МОС50вд/МОС50выд>1, ПОСвыд – снижена, МОС50вд – снижена или нет; в) фиксированной обструкцией: МОС50вд/МОС50выд@1, ПОСвыд – снижена, МОС50вд – снижена.
Рисунок 6. Кривые поток-объем у больных с рестриктивными вентиляционными нарушениями: а) фиброзом легких и в) пневмонэктомией.
Прикреплённые файлы
Мобильное приложение “MedElement”

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение “MedElement”

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях “MedElement (МедЭлемент)”, “Lekar Pro”,
“Dariger Pro”, “Заболевания: справочник терапевта”, не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения “MedElement (МедЭлемент)”, “Lekar Pro”,
“Dariger Pro”, “Заболевания: справочник терапевта” являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
From Wikipedia, the free encyclopedia
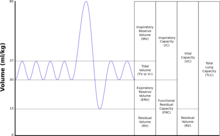 |
|
| TLC | Total lung capacity: the volume in the lungs at maximal inflation, the sum of VC and RV. |
|---|---|
| TV | Tidal volume: that volume of air moved into or out of the lungs during quiet breathing (TV indicates a subdivision of the lung; when tidal volume is precisely measured, as in gas exchange calculation, the symbol TV or VT is used.) |
| RV | Residual volume: the volume of air remaining in the lungs after a maximal exhalation |
| ERV | Expiratory reserve volume: the maximal volume of air that can be exhaled from the end-expiratory position |
| IRV | Inspiratory reserve volume: the maximal volume that can be inhaled from the end-inspiratory level |
| IC | Inspiratory capacity: the sum of IRV and TV |
| IVC | Inspiratory vital capacity: the maximum volume of air inhaled from the point of maximum expiration |
| VC | Vital capacity: the volume of air breathed out after the deepest inhalation. |
| VT | Tidal volume: that volume of air moved into or out of the lungs during quiet breathing (VT indicates a subdivision of the lung; when tidal volume is precisely measured, as in gas exchange calculation, the symbol TV or VT is used.) |
| FRC | Functional residual capacity: the volume in the lungs at the end-expiratory position |
| RV/TLC% | Residual volume expressed as percent of TLC |
| VA | Alveolar gas volume |
| VL | Actual volume of the lung including the volume of the conducting airway. |
| FVC | Forced vital capacity: the determination of the vital capacity from a maximally forced expiratory effort |
| FEVt | Forced expiratory volume (time): a generic term indicating the volume of air exhaled under forced conditions in the first t seconds |
| FEV1 | Volume that has been exhaled at the end of the first second of forced expiration |
| FEFx | Forced expiratory flow related to some portion of the FVC curve; modifiers refer to amount of FVC already exhaled |
| FEFmax | The maximum instantaneous flow achieved during a FVC maneuver |
| FIF | Forced inspiratory flow: (Specific measurement of the forced inspiratory curve is denoted by nomenclature analogous to that for the forced expiratory curve. For example, maximum inspiratory flow is denoted FIFmax. Unless otherwise specified, volume qualifiers indicate the volume inspired from RV at the point of measurement.) |
| PEF | Peak expiratory flow: The highest forced expiratory flow measured with a peak flow meter |
| MVV | Maximal voluntary ventilation: volume of air expired in a specified period during repetitive maximal effort |
|
Lung volumes and lung capacities refer to the volume of air in the lungs at different phases of the respiratory cycle.
The average total lung capacity of an adult human male is about 6 litres of air.[1]
Tidal breathing is normal, resting breathing; the tidal volume is the volume of air that is inhaled or exhaled in only a single such breath.
The average human respiratory rate is 30–60 breaths per minute at birth,[2] decreasing to 12–20 breaths per minute in adults.[3]
Factors affecting volumes[edit]
Several factors affect lung volumes; some can be controlled, and some cannot be controlled. Lung volumes vary with different people as follows:
| Larger volume | Smaller volumes |
|---|---|
| taller people | shorter people |
| people who live at higher altitudes | people who live at lower altitudes |
| fit | obese[4] |
A person who is born and lives at sea level will develop a slightly smaller lung capacity than a person who spends their life at a high altitude. This is because the partial pressure of oxygen is lower at higher altitude which, as a result means that oxygen less readily diffuses into the bloodstream. In response to higher altitude, the body’s diffusing capacity increases in order to process more air. Also, due to the lower environmental air pressure at higher altitudes, the air pressure within the breathing system must be lower in order to inhale; in order to meet this requirement, the thoracic diaphragm has a tendency to lower to a greater extent during inhalation, which in turn causes an increase in lung volume.
When someone living at or near sea level travels to locations at high altitudes (e.g. the Andes; Denver, Colorado; Tibet; the Himalayas) that person can develop a condition called altitude sickness because their lungs remove adequate amounts of carbon dioxide but they do not take in enough oxygen. (In normal individuals, carbon dioxide is the primary determinant of respiratory drive.)
Lung function development is reduced in children who grow up near motorways[5][6] although this seems at least in part reversible.[7] Air pollution exposure affects FEV1 in asthmatics, but also affects FVC and FEV1 in healthy adults even at low concentrations.[8]
Specific changes in lung volumes also occur during pregnancy. Functional residual capacity drops 18–20%,[9] typically falling from 1.7 to 1.35 litres,[citation needed] due to the compression of the diaphragm by the uterus.[citation needed] The compression also causes a decreased total lung capacity (TLC) by 5%[9] and decreased expiratory reserve volume by 20%.[9] Tidal volume increases by 30–40%, from 0.5 to 0.7 litres,[9] and minute ventilation by 30–40%[9][10] giving an increase in pulmonary ventilation. This is necessary to meet the increased oxygen requirement of the body, which reaches 50 ml/min, 20 ml of which goes to reproductive tissues. Overall, the net change in maximum breathing capacity is zero.[9]
Values[edit]
| Volume | Value (litres) | |
|---|---|---|
| In men | In women | |
| Inspiratory reserve volume (IRV) | 3.3 | 1.9 |
| Tidal volume (TV) | 0.5 | 0.5 |
| Expiratory reserve volume (ERV) | 1.1 | 0.7 |
| Residual volume (RV) | 1.2 | 1.1 |
| Volume | Average value (litres) | Derivation | |
|---|---|---|---|
| In men | In women | ||
| Vital capacity | 4.8 | 3.1 | IRV + TV + ERV |
| Inspiratory capacity | 3.8 | 2.4 | IRV + TV |
| Functional residual capacity | 2.4 | 1.8 | ERV + RV |
| Total lung capacity | 6.0 | 4.2 | IRV + TV + ERV + RV |
The tidal volume, vital capacity, inspiratory capacity and expiratory reserve volume can be measured directly with a spirometer. These are the basic elements of a ventilatory pulmonary function test.
Determination of the residual volume is more difficult as it is impossible to “completely” breathe out. Therefore, measurement of the residual volume has to be done via indirect methods such as radiographic planimetry, body plethysmography, closed circuit dilution (including the helium dilution technique) and nitrogen washout.
In absence of such, estimates of residual volume have been prepared as a proportion of body mass for infants (18.1 ml/kg),[12] or as a proportion of vital capacity (0.24 for men and 0.28 for women)[13] or in relation to height and age ((0.0275* Age [Years]+0.0189*Height [cm]−2.6139) litres for normal-mass individuals and (0.0277*Age [Years]+0.0138*Height [cm]−2.3967) litres for overweight individuals).[14] Standard errors in prediction equations for residual volume have been measured at 579 ml for men and 355 ml for women, while the use of 0.24*FVC gave a standard error of 318 ml.[15]
Online calculators are available that can compute predicted lung volumes, and other spirometric parameters based on a patient’s age, height, weight, and ethnic origin for many reference sources.
British rower and three-time Olympic gold medalist Pete Reed is reported to hold the largest recorded lung capacity of 11.68 litres;[16][17][18] US swimmer Michael Phelps is also said to have a lung capacity of around 12 litres.[17][19]
Weight of breath[edit]
The mass of one breath is approximately a gram (0.5-5 g). A litre of air weighs about 1.2 g (1.2 kg/m3).[20] A half litre ordinary tidal breath[11] weighs 0.6 g; a maximal 4.8 litre breath (average vital capacity for males)[11] weighs approximately 5.8 g.
Restrictive and obstructive[edit]
Scheme of changes in lung volumes in restricted and obstructed lung in comparison with healthy lung.
The results (in particular FEV1/FVC and FRC) can be used to distinguish between restrictive and obstructive pulmonary diseases:
| Type | Examples | Description | FEV1/FVC |
| restrictive diseases | pulmonary fibrosis, Infant Respiratory Distress Syndrome, weak respiratory muscles, pneumothorax | volumes are decreased | often in a normal range (0.8–1.0) |
| obstructive diseases | asthma, COPD, emphysema | volumes are essentially normal but flow rates are impeded | often low (asthma can reduce the ratio to 0.6, emphysema can reduce the ratio to 0.78–0.45) |
See also[edit]
- Pulmonary function testing (PFT)
- Spirometry
References[edit]
- ^ “Lung Volumes”. Physiopedia. Retrieved 2023-04-14.
- ^ Scott L. DeBoer (4 November 2004). Emergency Newborn Care. Trafford Publishing. p. 30. ISBN 978-1-4120-3089-2.
- ^ Wilburta Q. Lindh; Marilyn Pooler; Carol Tamparo; Barbara M. Dahl (9 March 2009). Delmar’s Comprehensive Medical Assisting: Administrative and Clinical Competencies. Cengage Learning. p. 573. ISBN 978-1-4354-1914-8.
- ^ Jones RL, Nzekwu MM (2006). “The effects of body mass index on lung volumes”. Chest. 130 (3): 827–33. doi:10.1378/chest.130.3.827. PMID 16963682.
- ^ Reinberg, Steven (2007-01-26). “Living Near Freeways Hurts Kids’ Lungs”. ISSN 0190-8286. Retrieved 2023-04-26.
- ^ Gauderman, W (2007). “Effect of exposure to traffic on lung development from 10 to 18 years of age: a cohort study”. The Lancet. 369 (9561): 571–577. CiteSeerX 10.1.1.541.1258. doi:10.1016/S0140-6736(07)60037-3. PMID 17307103. S2CID 852646.
- ^ “Study Findings – USC Children’s Health Study”.
- ^ Int Panis, L (2017). “Short-term air pollution exposure decreases lung function: a repeated measures study in healthy adults”. Environmental Health. 16 (1): 60. doi:10.1186/s12940-017-0271-z. PMC 5471732. PMID 28615020.
- ^ a b c d e f Simpson, Kathleen Rice; Patricia A Creehan (2007). Perinatal Nursing (3rd ed.). Lippincott Williams & Wilkins. pp. 65–66. ISBN 978-0-7817-6759-0.
- ^ Guyton and hall (2005). Textbook of Medical Physiology (11 ed.). Philadelphia: Saunders. pp. 103g. ISBN 978-81-8147-920-4.
- ^ a b c d Tortora, Gerard J. (2016). Principles of anatomy & physiology. Derrickson, Bryan (15th ed.). Hoboken, NJ. p. 874. ISBN 978-1119447979. OCLC 1020568457.
- ^ Morris, Mohy G. (2010). “Comprehensive integrated spirometry using raised volume passive and forced expirations and multiple-breath nitrogen washout in infants”. Respiratory Physiology & Neurobiology. 170 (2): 123–140. doi:10.1016/j.resp.2009.10.010. ISSN 1569-9048. PMC 2858579. PMID 19897058.
- ^ Wilmore, J. H. (1969). “The use of actual predicted and constant residual volumes in the assessment of body composition by underwater weighing”. Med Sci Sports. 1 (2): 87–90. doi:10.1249/00005768-196906000-00006.
- ^ MILLER, WAYNE C.; SWENSEN, THOMAS; WALLACE, JANET P. (February 1998). “Derivation of prediction equations for RV in overweight men and women”. Medicine & Science in Sports & Exercise. 30 (2): 322–327. doi:10.1097/00005768-199802000-00023. PMID 9502364.
- ^ Morrow JR Jr; Jackson AS; Bradley PW; Hartung GH. (Dec 1986). “Accuracy of measured and predicted residual lung volume on body density measurement”. Med Sci Sports Exerc. 18 (6): 647–52. doi:10.1249/00005768-198612000-00007. PMID 3784877.
- ^ English Institute of Sport, 17 November 2006, test ID 27781
- ^ a b “Making sense of breathing, VO2max and lung capacity”. worldrowing.com. Retrieved 2019-11-28.
- ^ “Pete Reed: Three-time Olympic rowing champion on spinal stroke, paralysis and the future”. 2019-11-28. Retrieved 2019-11-28.
- ^ Smith, Michael Hanlon and Jennifer (2012-08-03). “London 2012 Olympics: Faster. Higher. Longer. Stronger”. Daily Telegraph. ISSN 0307-1235. Retrieved 2019-11-28.
- ^ Atmosphere of Earth#Density and mass
External links[edit]
- Lung function fundamentals (anaesthetist.com)
- Volume of human lungs












