Задачи на выход продукта химической реакции. Как решать задачи на выход продукта реакции. Что такое выход продукта химической реакции. Теоретическое и практическое количество продукта химической реакции.
При решении задач на расчеты по уравнениям химических реакций мы принимаем, что в ходе реакции образуется точно рассчитанное количество продукта, исходя из мольного соотношения реагентов и продуктов. Количество продукта реакции, которое должно получится из реагентов согласно стехиометрическим расчетам — это теоретическое количество (масса, объем) или теоретический выход продукта реакции nтеор.
Однако на практике это соотношение не выполняется, и в большинстве случаев образуется меньшее количество продукта реакции, чем было рассчитано — практическое количество (масса, объем) или практический выход продукта реакции nпр.
Практический и теоретический выход не совпадают в силу разных причин — неэффективные соударения реагирующих частиц, побочные процессы, потери в ходе проведения реакции и т.д.
Обратите внимание! Понятия теоретического или практического количества реагента не существует. Ведь мы всегда берем определенное количество реагентов. А вот вступать в реакцию не полностью реагенты могут.
Массовая (мольная, объемная) доля выхода продукта реакции η или ω — это соотношение массы (количества вещества, объема) продукта, которая практически получена в ходе реакции, mпр., к массе (количеству, объему) продукта, которая рассчитана теоретически, mтеор.:
η = mпр./mтеор.
Массовую (мольную, объемную) долю выхода продукта реакции можно выражать в долях, а можно в процентах:
η = mпр./mтеор.·100%
Рассмотрим несколько задач на определение и использование выхода продукта реакции.
1. Какое количество вещества аммиака получится при действии избытка раствора гидроксида натрия на 500 г сульфата аммония, если выход в данной реакции 70%?
Решение.
2NaOH + (NH4)2SO4 = Na2SO4 + 2NH3 + 2H2O
Количество вещества сульфата аммония:
n((NH4)2SO4) = m/M = 500/132 = 3,79 моль
Теоретическое количество аммиака:
nтеор.(NH3) = 2·n((NH4)2SO4) = 2·3,79 = 7,58 моль
Зная мольную долю выхода продукта реакции, определим практический выход аммиака:
nпр.(NH3) = η·nтеор.(NH3) = 0,7·7,58 = 5,3 моль
Ответ: nпр.(NH3) = 5,3 моль
2. При хлорировании метана объемом 112 л (н. у.) получен дихлорметан массой 255 г. Определите долю выхода дихлорметана.
Решение.
CH4 + 2Cl2 = CH2Cl2 + 2HCl
Количество вещества метана:
n(CH4) = V/Vm = 112/22,4 = 5 моль
Теоретическое количество дихлорметана:
nтеор.(CH2Cl2) = n(CH4) = 5 моль
mтеор.(CH2Cl2) = M·nтеор.(CH2Cl2) = 85 г/моль·5 моль = 425 г
Масса дихлорметана, которая приведена в условии задачи — это практический выход дихлорметана.
Доля выхода дихлорметана:
η = mпр./mтеор. = 255/425 = 0,6 или 60%
Ответ: выход продукта реакции 60%
3. Определите массу оксида меди (II), которая потребуется для получения 500 г нитрата меди, если доля выхода в реакции взаимодействия оксида меди с HNO3 составляет 92%?
4. Определите объем (н.у., л) аммиака, который получится при действии избытка раствора гидроксида натрия на 48 г карбоната аммония, если выход в реакции составляет 70%?
5. Определите массу соли, г, которая образуется при растворении в избытке азотной кислоты 80 г оксида меди (II), если выход в реакции составляет 80%?
6. При термическом разложении 1700 г нитрата натрия было получено 174,4 л кислорода (н.у.). Определите массовую долю выхода в этой реакции.
7. Рассчитайте массу оксида магния, которая образуется при разложении гидроксида магния массой 50 г, если реакция разложений прошла с выходом 95,5%.
8. Какая масса бензола (кг) может получиться из 369,6 м3 (н.у.) ацетилена, если доля выхода бензола составила 65% от теоретически возможного?
9. Определите массу спирта, полученного при гидратации 40 л пропилена (н.у.), если доля выхода продукта реакции составляет 65% от теоретически возможного.
10. Определите долю выхода в реакции каталитического окисления аммиака кислородом, если при окислении 10 моль аммиака образуется 200 л оксида азота (II) при н.у.?
11. Пары брома объемом 20 л смешали с избытком водорода, в результате из смеси выделили 32 л бромоводорода. Определите долю выхода, %, если объемы газов измерялись при одинаковых условиях.
12. Оксид кальция массой 0,64 кг нагрели до 1200° С с достаточной массой оксида кремния (IV). Масса образовавшегося силиката кальция оказалась равной 1,024 кг. Определите выход (%) реакции соединения.
13. Из 36 г метанола было получено 24 г диметилового эфира. Рассчитайте выход реакции дегидратации
14. Углекислый газ объемом 6 л (н.у.) пропустили над раскалённым углем, продукт реакции пропустили через избыток известковой воды, после чего собрали 7,2 л (н.у.) газа. Определите степень превращения углекислого газа, %.
15. Определите массу, г нитрата аммония, которая содержалась в растворе, если при действии на этот раствор избытка гидроксида кальция выделилось 6 г аммиака. Реакция прошла с выходом 88,2 %.
16. При термическом разложении не загрязненного примесями карбоната кальция образовалось 20 г оксида кальция. Известно, что реакция прошла с выходом 85%. Вычислите массу карбоната кальция, взятого для проведения реакции разложений и объем (н.у.) образовавшегося углекислого газа.
17. Какой объем пропана (н.у.) потребуется для получения 42 г пропена, если доля выхода продуктов реакции составляет 60% от теоретически возможного?
18. При бромировании пентена-2 массой 8,4 г получен 2,3-дибромпентан массой 24,3 г. Определите долю выхода продукта реакции.
19. Из 69 г этанола получен бутадиен-1,3 массой 36,85 г. Определите массовую долю выхода продукта реакции.
20. При бромировании 5,4 г дивинила избытком брома образуется 28,2 г 1,2,3,4-тетрабромбутана. Определите выход продукта реакции.
21. Определите, какая масса 2-метилбутана необходима для получения 46,24 г изопрена, если доля выхода продукта реакции составляет 85%?
22. Определите объем метана, который потребуется для получения 63 л ацетилена (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
23. Определите, какую массу уксусного альдегида можно получить по реакции Кучерова из 11,2 л ацетилена (н. у.), если доля выхода продуктов реакции составляет 80% от теоретически возможного?
24. При действии избытка воды на 48 г технического карбида кальция, содержащего 10% примесей, образовался ацетилен объемом 10,08 л (н.у.). Определите долю выхода продукта реакции.
25. Определите массу технического карбида алюминия, содержащего 7% примесей, необходимого для получения 56 л метана (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
26. Из 179,2 л бутана (н.у.) с объемной долей примесей 25% двухстадийным синтезом получен бутанол-2 массой 159,84 г. Доли выхода продуктов на первой и второй стадиях одинаковы. Определите доли выхода продуктов реакций.
27. Циклогексан массой 16 г сожгли в избытке кислорода и полученный углекислый газ пропустили через избыток раствора гидроксида кальция, в результате чего выпал осадок массой 90 г. Определите массовую долю негорючих примесей в циклогексане, если доля выхода продуктов горения составляет 90% от теоретически возможного.
28. При нитровании 46,8 г бензола получен нитробензол массой 66,42 г. Определите выход продуктов реакции.
Расчетные задачи типа «Определение выхода продукта реакции в процентах от теоретического»
Признак
В условии задачи встречается слово «выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём, практическая масса или объём» могут быть использованы только для веществ-продуктов.
Доля выхода продукта обозначается буквой
(эта), измеряется в процентах или долях.
Также для расчётов может использоваться количественный выход:
I. Первый тип задач
Известны масса (объём) исходного вещества и масса (объём) продукта реакции. Необходимо определить выход продукта реакции в %.
Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5, 5 г. Определите выход продукта реакции (%).
| 1. Записываем краткое условие задачи |
Дано: m (Mg) = 1,2 г m практическая(MgSO4) = 5,5 г _____________________ Найти: |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(Mg) = 24 г/моль M(MgSO4) = 24 + 32 + 4 · 16 = 120 г/моль |
|
4. Находим количество вещества реагента по формулам |
ν(Mg) = 1,2 г / 24(г/моль) = 0,05 моль |
| 5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
m = ν · M mтеор (MgSO4) = M(MgSO4) · νтеор (MgSO4) = = 120 г/моль · 0,05 моль = 6 г |
|
6. Находим массовую (объёмную) долю выхода продукта по формуле |
Ответ: Выход сульфата магния составляет 91,7% по сравнению с теоретическим |
II. Второй тип задач
Известны масса (объём) исходного вещества (реагента) и выход (в %) продукта реакции. Необходимо найти практическую массу (объём) продукта реакции.
Задача 2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид кальция массой 16,8 г, если выход составляет 80%.
|
1. Записываем краткое условие задачи |
Дано: m(CaO) = 16,8 г
___________________ Найти: m практ (CaC2) = ? |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
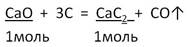 |
|
3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(CaO) = 40 + 16 = 56 г/моль M(CaC2) = 40 + 2 · 12 = 64г/моль |
|
4. Находим количество вещества реагента по формулам |
ν(CaO)=16,8 (г) / 56 (г/моль) = 0,3 моль |
|
5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
|
|
6. Находим массовую (объёмную) долю выхода продукта по формуле |
m практич (CaC2) = 0,8 · 19,2 г = 15,36 г Ответ: m практич (CaC2) = 15,36 г |
III. Третий тип задач
Известны масса (объём) практически полученного вещества и выход этого продукта реакции. Необходимо вычислить массу (объём) исходного вещества.
Задача 3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу карбоната натрия нужно взять для получения оксида углерода (IV) объёмом 28,56 л (н. у.). Практический выход продукта 85%.
| 1. Записываем краткое условие задачи |
Дано: н. у. Vm = 22,4 л/моль Vпрактич(CO2) = 28,56 л = 85% или 0,85 ____________________ Найти: m(Na2CO3) =? |
| 2. Находим по ПСХЭ молярные массы веществ, если это необходимо | M (Na2CO3) =2·23 + 12 + 3·16 = 106 г/моль |
|
3. Вычисляем теоретически полученный объём (массу) и количество вещества продукта реакции, используя формулы: |
Vтеоретич(CO2) = = 28,56 л / 0,85 = 33,6 л ν(CO2) = 33,6 (л) / 22,4 (л/моль) = 1,5 моль |
|
4. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 5. Находим количество вещества реагента по УХР |
По УХР:
ν(Na2CO3) = ν(CO2) = 1,5 моль |
|
6. Определяем массу (объём) реагента по формуле: m = ν · M V = ν · Vm |
m = ν · M m(Na2CO3) = 106 г/моль · 1,5 моль = 159 г |
IV. Решите задачи
Задача №1. При взаимодействии натрия количеством вещества 0, 5 моль с водой получили водород объёмом 4,2 л (н. у.). Вычислите практический выход газа (%).
Задача №2. Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно получить при восстановлении его оксида массой 228 г, если практический выход хрома составляет 95 %.
Задача №3. Определите, какая масса меди вступит в реакцию с концентрированной серной кислотой для получения оксида серы (IV) объёмом 3 л (н.у.), если выход оксида серы (IV) составляет 90%.
Задача №4. К раствору, содержащему хлорид кальция массой 4,1 г, прилили раствор, содержащий фосфат натрия массой 4,1 г. Определите массу полученного осадка, если выход продукта реакции составляет 88 %.
Дорогие друзья продолжаем наши разборы задач и сегодня разберем “Что такое выход продукта химической реакции?” Не всегда в ходе практических опытов мы получаем то количество вещества, на которое изначально рассчитывали. Часть вещества может не прореагировать, часть потеряться. Поэтому, полностью реагенты вряд ли когда-то прореагируют, отсюда возникли понятия практический выход от теоретически возможного
Сначала основные термины:
Количество продукта реакции, которое должно получится из реагентов согласно стехиометрическим расчетам — это теоретическое количество (масса, объем) или теоретический выход продукта реакции nтеор.
Однако на практике это соотношение не выполняется, и в большинстве случаев образуется меньшее количество продукта реакции, чем было рассчитано — практическое количество (масса, объем) или практический выход продукта реакции nпр.
Массовая (мольная, объемная) доля выхода продукта реакции η или ω — это соотношение массы (количества вещества, объема) продукта, которая практически получена в ходе реакции, mпр., к массе (количеству, объему) продукта, которая рассчитана теоретически, mтеор.:
η = mпр./mтеор.
Массовую (мольную, объемную) долю выхода продукта реакции можно выражать в долях, а можно в процентах:
η = mпр./mтеор.·100%
Алгоритм решения задач
1.Записываем условие задачи, определяем известные и не известные данные
2.Составляем уравнение химической реакции (УХР), расставляем коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции.
3.Находим количество вещества известных данных
4.По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции
5.Находим массовую (объёмную) долю выхода продукта по формуле.
6.Если в условии задачи уже дан выход продуктов реакции, следовательно выводим из основной формулы практические или теоретические массы.
Пример 1. При хлорировании метана объемом 112 л (н. у.) получен дихлорметан массой 255 г. Определите долю выхода дихлорметана.
Пример 2. Определите массу осадка (г, н.у.), полученного при сливании двух растворов, один из которых содержит 4,5 г хлорида кальция, а другой 4,1 г ортофосфата натрия. Выход продукта реакции составляет 88%
Пример 3. Рассчитайте выход (%) продукта реакции 43,05 г анилина с избытком бромной воды, если для нейтрализации выделившегося бромоводорода потребовалось 62,5 г 40%-ного раствора гидроксида натрия
Задачи для самоконтроля
1.При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5,5 г. Определите выход продукта реакции (%). (91,67%.)
2.При взаимодействии натрия количеством вещества 0,5 моль с водой получили водород объемом 4,2 л. Вычислите практический выход газа(%). (75%.)
3.Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно получить восстановлением его оксида массой 228 кг, если практический выход хрома составляет 95%. (148,2 кг.)
4.При каталитическом гидрировании формальдегида получили метиловыи спирт, при взаимодейтвии которого с металлическим натрием образовался водород объемом 8,96 л (н. у.). Выход продукта на каждой стадии синтеза составил 80%. Определите исходную массу формальдегида. (37,5 г.)
5.Вычислите, какой объем раствора с массовой долей гидроксида калия 26% (р = 1,24 r/мл) необходим для реакции с алюминием, чтобы получить водород объемом 10,64 л, если выход водорода составляет 95%. (41,35)
Надеюсь, моя статья была для вас полезна. Еще больше интересной информации вы найдете в наших сообществах в ВКонтакте vk.com/biochemschool и Телеграме t.me/biochemschool.

VaVaS
+10
Решено
10 лет назад
Химия
5 – 9 классы
При взаимодействии 6,9 г натрия с водой получили 3 л водорода (н.у.). Вычислите объемную долю выхода газа ( в процентах).
Напишите пожалуйста вместе с дано,найти,решение по пунктам
Смотреть ответ
1
Ответ проверен экспертом
4
(24 оценки)
69
LittleFiend
10 лет назад
Светило науки – 6 ответов – 127 раз оказано помощи
Дано:
m(Na)= 6,9 г
m(H)= 3 л
Найти объм. долю
Решение:
2Na+2H2O=2NAOH+H2O
M(Na)= 23г/моль
Составим пропорцию
2*23=22,4
6,9=x
Теперь методом крест на крест
x=6,9*22,4/2*23= 3,36 л
Составим соотношение:
3/3,36= 0,893=89,3 %
Ответ: Объемная доля газа = 89,3%
(24 оценки)
https://vashotvet.com/task/286091
- Главная
- Химия
- При взаимодей…
-
Предмет:
Химия
-
Автор:
ivoryflynn
-
Создано:
4 года назад
Ответы 1
Дано:
m(Na)= 6,9 г
m(H)= 3 л
Найти объм. долю
Решение:
2Na+2H2O=2NAOH+H2O
M(Na)= 23г/моль
Составим пропорцию
2*23=22,4
6,9=x
Теперь методом крест на крест
x=6,9*22,4/2*23= 3,36 л
Составим соотношение:
3/3,36= 0,893=89,3 %
Ответ: Объемная доля газа = 89,3%
-
Автор:
jaysonhaynes
-
Оценить ответ:
0
Знаешь ответ? Добавь его сюда!
Последние вопросы
-
Экономика2 часа назад
На фото
-
Математика3 часа назад
Спростіть вираз -3(2x-1) і знайдіть його значення, якщо х=-2
-
Математика7 часов назад
Люди помогите!
Постройте треугольник АBC, по данным:
Угол А = 35°
ВС = 5 см
АС = 4 см
Мне не нужен ответ с другого сайта!
Скажите пожалуйста, как сделать это с помощью циркуля, кто учится в 7 классе.
-
Математика8 часов назад
(x-1)^8*(2x+3)^2*(x-7)^4*(3x-5)*(x+6)^3>0
-
Математика13 часов назад
помогите решить пожалуйста задачу
-
Литература15 часов назад
пересказ повести мелентьева одни сутки войны всего текста
-
Право16 часов назад
у rauf.bakirov нет прав
кто тоже так считает +
-
Математика19 часов назад
кто даун?
-
Математика1 день назад
355+360+365+…+505=? Скажите формулу чтоб решать такие задачи
-
Физика1 день назад
176. Каково ускорение свободного падения на высоте, равной Rз /2 от поверхности Земли?
-
Математика1 день назад
помогите пж
даны координаты точек А(1; -1; -4) В(-3; -1; 0) С(-1; 2; 5) D(2; -3; 1). найдите |2АВ + 3СD|
-
Физика1 день назад
Хэппи хэппи гёрл
-
Право1 день назад
я мужлан
“у прав нет мужлан” +100
“у мужлан нет прав” -10004014102402104021042141
-
Математика1 день назад
Помогите решить.
Найти производную второго порядка функции y = x * ln(x+1) при x = 0
-
Геометрия1 день назад
Помогите срочно!! Нужно Дано, Найти и решение(желательно с рисунком)
Прямая аб касается окружности с центром о и радиусом 5 см в точке б. найдите оа если аб 12 см.
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.

