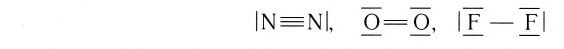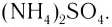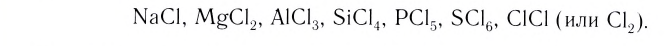Число общих электронных пар между связанными атомами характеризует кратность связи. [2]
По числу общих электронных пар химические связи подразделяются на простые ( одинарные) и кратные – двойные и тройные. [3]
По числу общих электронных пар химические связи подразделяются на простые ( ординарные) и кратные – двойные и тройные. Если между двумя атомами одинаковой или различной химической природы возникает только одна ковалентная связь, то ее называют простой, или ординарной, связью. Сигма-связь образуется в результате взаимодействия двух s – электро-нов, двух / з-элект ронов, а также двух смешанных s – и р-электронов. На рис. 14 изображены о-связи в некоторых элементарных и сложных веществах. [4]
Валентность элемента в соединениях с ковалентной связью определяется числом общих электронных пар, которые атом элемента образует с атомами других элементов. [5]
Валентность элемента в соединениях с ковалентной связью определяется числом общих электронных пар. [6]
В соединениях с ковалентной связью валентность элемента определяется числом общих электронных пар. Атом, к которому смещена электронная пара, обладает отрицательной валентностью, а противоположный атом – положительной валентностью. [7]
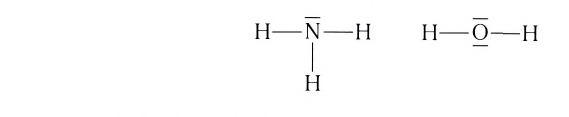
Степень окисления элемента в молекуле с ковалентной связью равна числу общих электронных пар. Так, в молекуле аммиака атом азота образует с атомами воДорода три общие электронные пары, следовательно, валентность азота равна трем. [8]
Для многоатомных частиц типа SO2, СО2, SO, SO и С8Ыв, в которых п-связи предпочтительнее рассматривать как многоцентровые и делокализо-ванные, подсчет числа общих электронных пар для отдельных атомов теряет свой смысл, а число валентностей ничего не говорит о ковалентиости атомов. [9]
Одиночные ( или неспаренные) электроны в электронных оболочках атомов, за счет спаривания которых возникает химическая связь в молекулах, называют валентными. Число общих электронных пар, образующихся при взаимодействии атомов химических элементов, определяет их валентность. [10]
По методу валентных связей, в котором все ковалентные связи рассматриваются как двухцентровые, ковалентность атома – это число общих электронных пар, образуемых данным атомом. [11]
В органических соединениях СН4, С2Н4, С2Н2 атом углерода четырехвалентен. Для многоцентровых частиц, например S02, C02, S047 SO, C6H6 в которых л-связи предпочтительное рассматривать как многоцентровые и делокализованные, подсчет числа общих электронных пар для отдельных атомов теряет свой смысл, и число валентностей ничего не говорят о ковалентности атомов. [12]
Из приведенных схем видно, что каждая электронная пара соответствует одной единице валентности. Химическая связь, осуществляемая парой общих электронов, называется ковалент-ной, или атомной, связью. Валентность элемента в соединениях с ковалентной ( атомной) связью определяется числом общих электронных пар. [13]
Валентность элемента в настоящее время рассматривается как число ковалентных связей его атома в данном соединении, современные синонимы этого термина – ковалентность, связность. Именно в ковалентной химической связи проявляется высокая химическая специфичность каждого элемента и каждого его валентного состояния: специфичность энергии связи, степени полярности и стереометрических характеристик – углов связи, их длин. Ионная связь менее специфична; она собственно становится связью только в конденсированных фазах, главным образом в твердых телах, в которых кристаллические структуры ионных веществ довольно однообразны и определяются зарядами и размерами ионов. Поэтому нельзя априорно определять валентность по числу неспаренных электронов в основном состоянии атома, как это иногда делается; валентность определяется числом общих электронных пар между данным атомом и соединенными с ним атомами.
Теория ковалентной связи
Для
объяснения образования ковалентной
связи применяют два приближенных метода
расчета систем, состоящих из ядер и
электронов:
–
метод валентных связей (ВС),
–
метод молекулярных орбиталей.
Рассмотрим
метод валентных связей (локализованных
электронных пар).
Теория
Гейтлера – Лондона. Метод валентных
связей (МВС).
В
1927 году В.Гейтлер и Ф.Лондон произвели
приближенный расчет молекулы водорода.
Вначале они рассмотрели систему из двух
атомов водорода, находящихся на большом
расстоянии друг от друга и выразили
зависимость волновой функции
рассматриваемой системы от координат.
Далее они предположили, что найденная
зависимость сохраняется и при сближении
атомов водорода. В результате они
получили уравнения, позволяющие найти
зависимость потенциальной энергии
системы, состоящей из двух атомов
водорода, от расстояния r между ядрами
этих атомов. Оказалось, что при совпадающем
направлении спинов сближение атомов
приводит к непрерывному возрастанию
энергии системы, т.е. связь не образуется.
При противоположно направленных спинах
сближение атомов до некоторого расстояния
r0
приводит к снижению энергии системы.
При r = r0
система обладает минимальной потенциальной
энергией, т. е. находится в самом устойчивом
состоянии – образуется связь. Дальнейшее
сближение атомов приводит к возрастанию
энергии. Таким образом, lcв
соответствует длине связи, а выделяющаяся
при этом энергия (Есв
–
энергии связи. Полученные расчетные
значения оказались близки к экспериментально
найденным величинам. Для молекулы
водорода энергия связи составляет 430,9
кДж/моль, а длина связи 0,74Å, что совпадает
с экспериментальными данными.
Рис
1.График изменения энергии системы,
образующейся при сближении двух атомов
водорода
Поскольку
длина связи меньше суммы радиусов двух
атомов водорода (0,53·2=1,06Å). Это
позволяет сделать вывод, что при
возникновении ковалентной связи
происходит перекрывании электронных
облаков с образованием молекулярного
электронного облака, сопровождающееся
уменьшением энергии.
Механизм
образования связей.
Согласно методу ВС химическую связь
образуют два электрона с противоположными
спинами (связь двухцентровая и
двухэлектронная). Например, образование
молекулы F2
по методу ВС представляется следующим
образом:
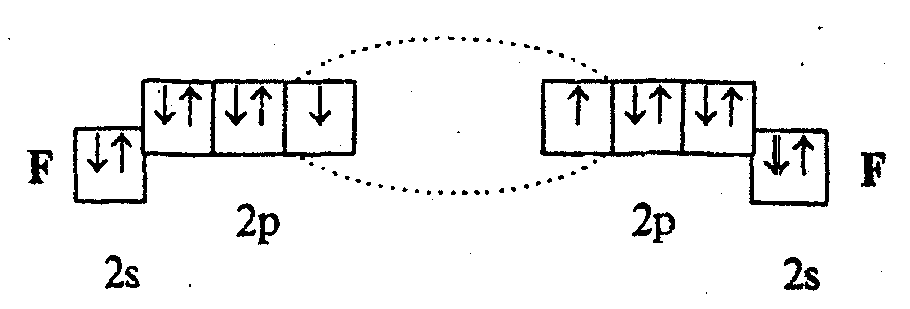
Каждая
пара атомов в молекуле удерживается
при помощи одной или нескольких
электронных пар, образующихся за счет
двух электронов, которые до образования
связи принадлежали разным атомам. В
случае образования нескольких электронных
пар возникают кратные связи. Например,
в молекуле азота осуществляется
трехкратная связь NN,
каждый атом приобретает устойчивую
восьмиэлектронную оболочку.
Возможен
и другой механизм образования ковалентной
связи за счет неподеленных электронных
пар одного атома А (донора) и свободных
орбиталей другого В (акцептора):
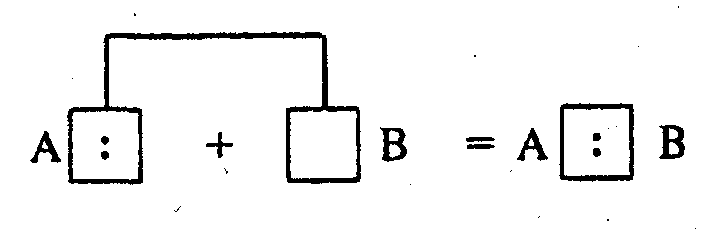
Такая
связь называется донорно-акцепторной
и отличается от обычной ковалентной
связи только происхождением электронной
пары.
Число
общих электронных пар, связывающих атом
данного элемента с другими атомами
(число образуемых атомом ковалентных
связей), называется ковалентностью
элемента в данном соединении. Например,
в молекулах СН4
и СО2
ковалентность углерода равна четырем,
водорода – единице, а кислорода – двум.
Связь
образуется путем перекрывания электронных
облаков взаимодействующих атомов (длина
связи меньше суммы радиусов взаимодействующих
атомов). Чем в большей степени перекрываются
взаимодействующие
электронные облака, тем прочнее
ковалентная связь
Ковалентная
связь насыщаема и направлена.
Насыщаемость
связи
– полное использование валентных
возможностей атома. Количество связей,
которое может образовать атом (его
ковалентность), определяется количеством
неспаренных электронов в основном и
возбужденном состояниях атома.
Ковалентность может быть повышена также
за счет образования дополнительных
донорно-акцепторных связей. Например,
в молекуле СО количество связей равно
трем: две связи образуются за счет
объединения неспаренных р-электронов
углерода и кислорода, а третья – за счет
неподеленной электронной пары кислорода
(донор) и свободной квантовой ячейки
углерода (акцептор).
Валентные
возможности атомов. Нормальное и
возбужденное состояния.(
см. главу «Периодический закон и
периодическая система Д.И.Менделеева»)
Направленность
связи.
Поскольку перекрывающиеся облака
определенным образом направлены в
пространстве, возникающая химическая
связь имеет направленный характер.
Различают -,
-
и
– связи.
–
связи
получаются в результате взаимного
перекрывания орбиталей вдоль
линии, соединяющей центры атомов.
-связи
возникают при перекрывании орбиталей
в направлении, перпендикулярном
линии связи.
-связи
возникают при перекрывании всех четырех
лепестков d-орбиталей
в
параллельных
плоскостях
(рис.
2):
Рис. 2 Схема
перекрывания орбиталей при образовании
-,
-,
-связей
Таким
образом, s-орбитали образуют только
-связи;
р-орбитали -
и
‑связи; а d–орбитали
– -,
-
и -связи.
Эти связи различаются по энергии:
Е-связи>
Е-связи>
Е-связи
Итак,
согласно методу ВС ковалентная химическая
связь – двуцентровая, двухэлектронная,
локализованная, направленная и насыщенная.
Геометрия
и свойства молекул, образующихся из
нормального состояния атомов
Молекулы
типа А2:
H2,
O2,
N2
линейные,
неполярные. Кратность связи равна 1,2,3
соответственно.
Они
образуются двумя одинаковыми атомами,
между которыми могут возникать:
–
одна одинарная σ- связь, за счет
перекрывания двух s-(молекулы
Н2)
или двух р- орбталей (молекулы Cl2),
–
двукратная связь – одна σ- и одна π-
связи (молекулы О2),
–
трехкратная – одна σ- и две π- связи
(молекулы N2).
Рис.3 Формы молекул:
а – линейная (А2,
АВ); б – угловая (АВ2);
в – пирамидальная (АВ3)
Молекулы
типа АВ: HF,
HCl,
HBr,
HI
линейные, полярные.
Свойства
связей в молекулах типа АВ
|
Свойство |
HF |
HCl |
HBr |
HI |
|
Длина, |
0,92 |
1,27 |
1,41 |
1,61 |
|
Энергия, |
565,7 |
431,6 |
364 |
298,3 |
|
Полярность, |
1,91 |
1,03 |
0,79 |
0,42 |
Молекулы
типа А2В:
H2O,
H2S,
H2Se,
H2Te,
H2Po
угловые (α ≥ 90˚), полярные.
На
рисунке 4 представлена схема образования
молекулы Н2Те
– два р-облака теллура перекрываются
s
– орбиталями двух атомов водорода:
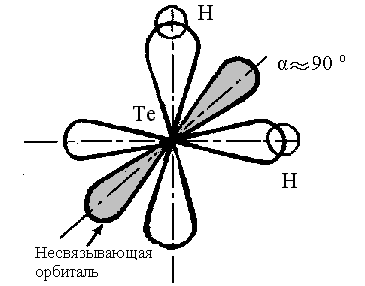
Рис.4
Схема образования связей в молекуле
Н2Tе
В
ряду
: H2O,
H2S,
H2Se,
H2Te,
H2Po
Длина
связи возрастает
Энергия
связи уменьшается
Полярность
связи уменьшается
Угол
между связями уменьшается
Молекулы
типа АВ3:
NH3,
PH3,
AsH3,
SbH3
имеют форму тригональной пирамиды, (α
≥ 90˚), полярные.
На
рисунке представлена схема образования
молекулы SbH3
– три орбитали атома сурьмы перекрываются
с тремя s
– обиталями трех атомов водорода с
образованием полярных σ – связей.
Образующаяся молекула имеет пирамидальное
строение с углом между связями ≈ 900
.
Молекула полярна.
|
|
|
Рис.5
Схема образования связей в молекуле
SbН3
Cвойства
связей в молекулах типа АВ3
|
Свойства |
NH3 |
PH3 |
AsH3 |
SbH3 |
|
Угол |
107 |
94 |
92 |
91 |
|
Длина, |
1,01 |
1,45 |
1,52 |
1,7 |
|
Энергия, |
380 |
323 |
281 |
256 |
Геометрия
и свойства молекул, образующихся из
возбужденного состояния атомов. Теория
гибридизации.
В
рассмотренных примерах химическая
связь образуется электронами одного
энергетического подуровня (р). В
большинстве же случаев в образовании
химической связи участвуют электроны
различных подуровней. Рассмотрим,
например, молекулу SiCl4.
Атом Si
имеет в невозбужденном состоянии два
валентных электрона и, следовательно,
может образовывать только две связи.
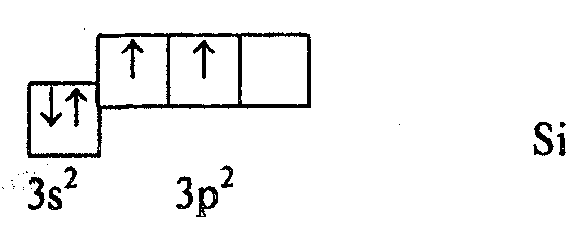
Предположим
теперь, что один из 3s-электронов
в результате возбуждения перешел на
3р-подуровень, теперь атом Si
может образовать четыре связи, причем
выигрыш в энергии при образовании связей
превосходит незначительную энергию
возбуждения. Поскольку теперь у атома
Si
в образовании связи могут участвовать
три р-электрона и один s‑электрон,
логично предположить, что связи в
молекуле SiCl4
должны быть неравноценными.
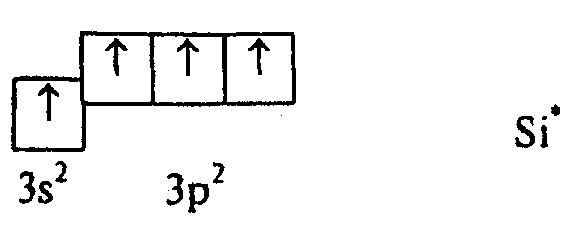
Однако
исследования показывают, что связи в
SiСl4
совершенно одинаковы (имеют одну и ту
же энергию и длину) и направлены
симметрично к вершинам тетраэдра. Этот
факт можно истолковать как гибридизацию,
т.е. смешивание валентных орбиталей
различных подуровней, в результате чего
возникают четыре новые (гибридные)
орбитали, промежуточные по форме и
энергии. В данном случае в гибридизации
участвует одна s-
и три р‑орбитали, поэтому имеет место
sр3-гибридизация
и форма образующейся молекулы
тетраэдрическая.
Основные
положения теории гибридизации:
(Л.Полинг
и Дж.Слейтер, 1931г.).
1.
При гибридизации, т.е. смешивании
валентных орбиталей различных подуровней,
возникают новые (гибридные)
орбитали, промежуточные по форме и
энергии.
2.
Число образующихся гибридных орбиталей
всегда равно числу смешивающихся
орбиталей.
3.
Связи,
возникающие путем перекрывания гибридных
орбиталей,
совершенно одинаковы (имеют одну и ту
же энергию и длину) и направлены
симметрично.
Исходя из этого, образующиеся при этом
молекулы
неполярны
или
малополярны.
4.
Гибридные электронные облака асимметричны
(рис.), поэтому они могут образовывать
только σ-связи; перекрывание орбиталей
происходит в большей степени и химические
связи
обладают
большей прочностью,
чем связи, образованные за счет негибридных
электронных орбиталей.
5.
При образовании кратных связей, π- связи
образуются за счет негибридных орбиталей.
6.
Геометрическую форму молекулы определяют
σ-связи.
7.
Тип гибридизации определяется типом и
количеством смешивающихся орбиталей
(sp-,
sp2-,
sp3-,
dsp2-,
dsp3-,
sp3d2–
).
Рассмотрим
образование химических связей в молекуле
ВеF2:
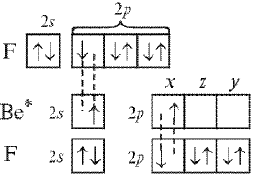
В образовании
связей участвуют 2s–
и 2рх-орбитали
возбужденного атома бериллия (рис. 6, а),
которые должны перекрываться с
соответствующими 2р-орбиталями
атомов фтора. Из характера перекрывания
следует, что связь, образованная
2рх-орбиталью
бериллия, должна быть более прочной,
чем связь, образованная его 2s-орбиталью.
Направление образования первой связи
строго определенное – вдоль оси х.
Перекрывание 2s-орбитали
не имеет преимущества в каком-либо
направлении, поэтому угол между связями
в молекуле ВеF2
может быть переменным.
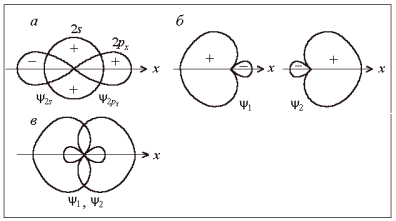
Рис. 6.
Образование гибридных sp-орбиталей ψ1
и ψ2
(плюс
и минус – знаки волновой функции)
Однако эти выводы
противоречат экспериментальным данным,
которые однозначно указывают, что угол
между связями составляет 180° и они
равноценны. Оказалось, что подобное
несоответствие теории и эксперимента
наблюдается там, где связи центрального
атома образованы орбиталями разного
типа симметрии (например, s
и р;
р
и d;
s,
р
и d).
Для объяснения
такого несоответствия Л.Полинг и
Дж.Слейтер разработали теорию гибридизации.
Сущность ее состоит в том, что близкие
по энергии валентные орбитали с различной
симметрией преобразуются в такое же
количество одинаковых гибридных
орбиталей, каждая из которых представляет
собой продукт смешения исходных
орбиталей. Гибридные орбитали более
вытянуты в направлении образования
химической связи и обеспечивают лучшее
перекрывание.
В нашем примере в
гибридизации участвуют одна 2s–
и одна 2р-орбиталь
атома бериллия. Такой случай называется
sp-гибридизацией.
Гибридные орбитали представляют собой
линейные комбинации исходных атомных
орбиталей с учетом знаков их частей –
«лопастей» (для 2s-функции
общепринято выбирать знак плюс):
ψ1
= а1
ψs
+ b1
ψp (1)
ψ2
= а2
ψs
+ b2
ψp (2)
где a1,
a2,
b1,
b2
– нормированные коэффициенты; в данном
случае
a1
= a2
= –b1
= b2
= 1/√2.
На рис. 6, б
показана форма sp-гибридных
орбиталей, графически построенных
согласно формулам (1) и (2). При смешении
волновых функций с одинаковыми знаками
они складываются, а с противоположными
– вычитаются. Поэтому гибридные волновые
функции сильно деформированы вдоль оси
симметрии и ориентированы вдоль нее.
Линейное расположение (рис. 6, в)
обеспечивает их минимальное отталкивание
и минимальную энергию системы.
Отсюда становится
понятным угол между связями (Be–F), равный
180°, и равноценность связей (рис. 7).
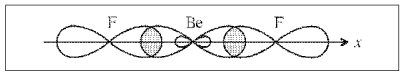
Рис. 7.
Орбитали молекулы BeF2
Гибридные орбитали
ψ1
и ψ2
по энергии занимают промежуточное
положение между исходными атомными
орбиталями (s
и p)
(рис. 8). Суммарная энергия электронов
на гибридных орбиталях даже несколько
больше, чем на исходных. Несмотря на то,
что на гибридизацию затрачивается
энергия, лучшее перекрывание гибридных
орбиталей по сравнению с исходными
атомными не только компенсирует
энергетические затраты, но и обеспечивает
энергетический выигрыш. В противном
случае гибридизация не происходит.
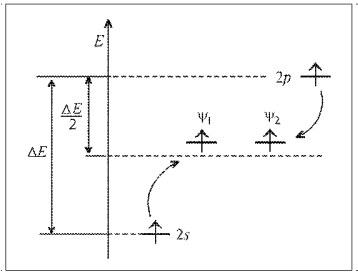
Рис. 8.
Энергетическая диаграмма sp-гибридизации
sp-Гибридизация
характерна для элементов II
группы, но возможна и для атомов других
элементов, образующих две s-связи
с участием одной s–
и одной р-орбиталей.
Участие в образовании
связей одной s–
и двух р-орбиталей
центрального атома приводит к
sp2-гибридизации.
Гибридизация такого типа характерна
для соединений элементов III группы.
Рассмотрим ее на
примере молекулы ВF3.
В возбужденном атоме бора при образовании
связей происходит гибридизация трех
орбиталей – 2s,
2рх,
2рz:
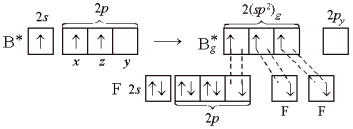
(Здесь у двух атомов
фтора показаны только 2р-электроны,
образующие связи.) Три гибридные орбитали
(sp2)g
в соответствии с принципом наименьшей
энергии ориентируются так, чтобы
отталкивание между ними было минимальным.
Этому отвечают углы между осями гибридных
орбиталей, равные 120° (рис. 9).
Поэтому молекула ВF3
– плоская, связи в ней – равноценные,
направленные по углам правильного
треугольника.
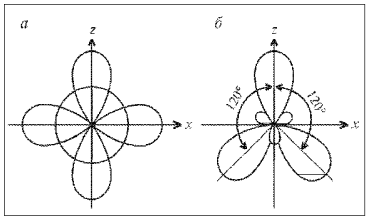
Рис. 9. sp2-Гибридизация:
а – исходные 2s-,
2рx–
и 2рz-орбитали;
б
– гибридные 2(sp2)g-орбитали
sp3-Гибридизация,
в которой участвуют s-орбиталь
и все три p-орбитали,
характерна для соединений элементов
IV группы периодической системы, в
частности для насыщенных углеводородов.
Рассмотрим молекулу метана СН4.
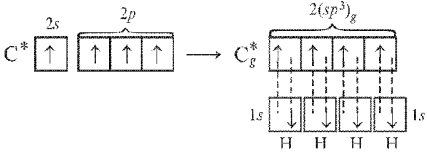
В этом случае (при
sp3-гибридизации)
образуются четыре sp3-гибридные
орбитали, направленные в пространстве
по углам тетраэдра. Углы между осями
гибридных орбиталей составляют 109,46°
(рис. 10).
Рассмотренный ранее ион аммония NH4+
также имеет тетраэдрическое строение
благодаря sp3-гибридизации.
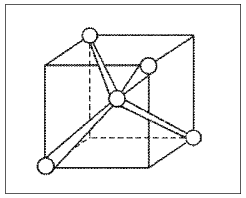
Рис. 10.
Ориентация sp3-гибридных
орбиталей в молекуле СН4
В гибридизации
могут участвовать и d-орбитали
внешнего или предвнешнего квантового
уровня. При образовании комплексного
иона [АlF6]3–
происходит sp3d2-гибридизация,
в которой участвуют вакантные d-орбитали:
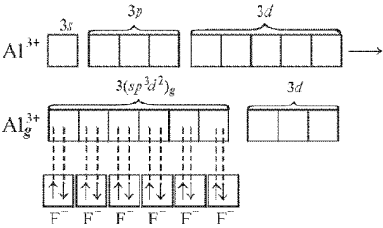
Такие шесть
гибридных орбиталей направлены по углам
октаэдра. Угол между связями 90° (рис.
11).
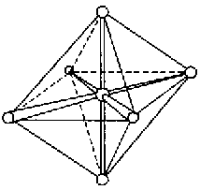
Рис. 11.
Ориентация sp3d2–
и d2sp3-гибридных
орбиталей
В комплексном ионе
[Fе(СN)6]4–
в гибридизации участвуют «внутренние»
d-орбитали
предвнешнего квантового слоя. При
возбуждении иона Fе2+,
входящего в состав комплекса, происходит
спаривание 3d-электронов
и переход в гибридное валентное состояние:
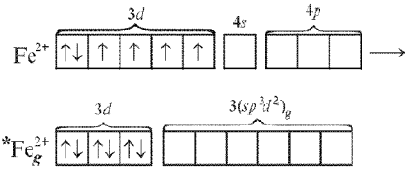
Связи образуются
в результате взаимодействия вакантных
гибридных d2sp3-орбиталей
иона *Feg2+и
неподеленных пар электронов шести ионов
СN–.
Тип гибридизации – d2sp3.
Геометрическая форма комплекса также
октаэдрическая.
Гибридизация с
участием d-орбиталей
дает и другие структуры молекул и сложных
ионов.
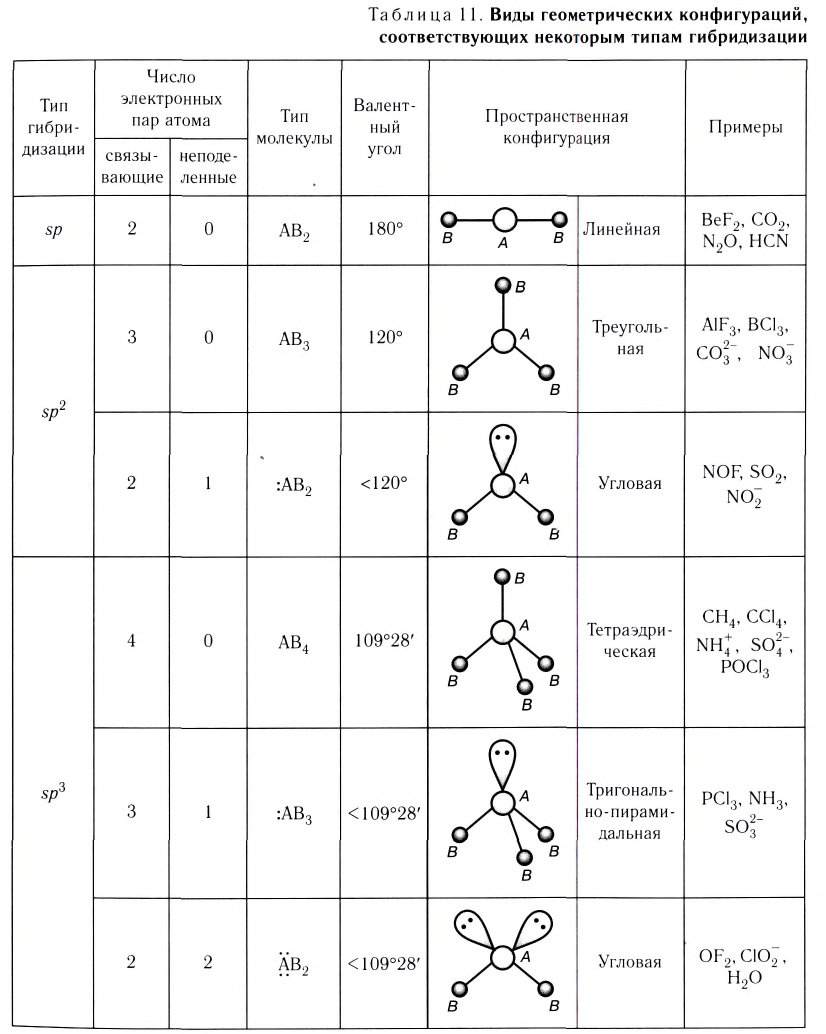
Таким образом,
направленность валентности обусловлена
ориентацией гибридных орбиталей в
пространстве. В обобщенной форме это
представлено в табл. 1.
Таблица 1
Пространственная конфигурация молекул
и ионов
|
Тип гибрдизации |
Валентные углы, форма молекулы |
Примеры |
|
sp |
180°
линейная |
H–Be–H, HC≡CH |
|
sp2 |
120°
плоская тригональная |
H2C=CH2, C6H6, BCl3 |
|
sp3 |
109°28′
тетраэдрическая |
[NH4]+, |
|
sp2d |
90°
квадратная |
[Ni(CN)4]2–, [PtCl4]2– |
|
sp3d или dsp3 |
90°, 120°
тригонально-бипирамидальная |
PCl5 |
|
d2sp3 или sp3d2 |
90°
октаэдрическая |
[Fe(CN)6]3–, [CoF6]3–, |
Гибридизация
с участием орбиталей с неподеленными
электронными парами.
Оказалось, что
конфигурация не всех молекул может быть
объяснена схемой, приведенной в табл.
2. Так, например, можно представить себе,
что в молекуле аммиака NH3
три связи N–H образованы «чистыми» (т.е.
негибридизованными) 2р-орбиталями азота.
Молекула должна
иметь пирамидальную форму: в вершине
пирамиды – атом азота, угол между связями
– 90°. Однако экспериментально измеренный
угол составляет ~107,8°, что значительно
лучше согласуется с тетраэдрической
конфигурацией, характерной для
sp3‑гибридизации.
Это можно объяснить, если предположить,
что в гибридизации принимает участие
орбиталь неподеленной (несвязывающей)
пары электронов:
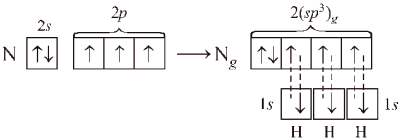
Перекрывание
орбиталей в молекуле NH3
показано на рис. 12.
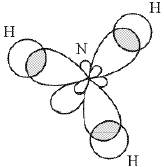
Рисунок 12.
Перекрывание орбиталей в молекуле NH3
С этих же позиций
участием орбиталей двух неподеленных
пар электронов в sp3‑гибридизации
можно объяснить строение молекулы воды,
в которой угол между связями О–Н равен
~104,5°:
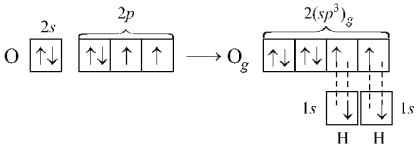
Вследствие более
сильного отталкивающего действия
неподеленных (несвязывающих) электронных
пар валентные углы в молекулах NН3
и Н2О
оказываются несколько меньше
тетраэдрического.
Таблица 2
Изменение угла
между связями Э–Н
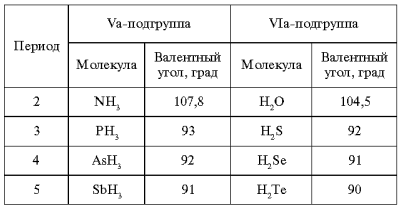
Для третьего и
последующих периодов из-за увеличения
размеров атомов и уменьшения плотности
электронных облаков гибридизация, как
реальное явление не наблюдается, связи
образуются р-орбиталями. Это иллюстрирует
табл. 2
В случае sp,
sp2,
sp3,
sp3d2
гибридизации вершины в многограннике,
описывающем геометрию химической
частицы, равноценны, и поэтому кратные
связи и неподеленные пары электронов
могут занимать любые из них. Однако,
sp3d-гибридизации
отвечает тригональная
бипирамида, в
которой валентные углы для атомов,
расположенных в основании пирамиды
(экваториальной плоскости), равны 120o,
а валентные углы с участием атомов,
расположенных в вершинах бипирамиды,
равны 90o.
Эксперимент показывает, что неподеленные
электронные пары всегда располагаются
в экваториальной плоскости тригональной
бипирамиды. На этом основании делается
вывод, что они требуют больше свободного
пространства, чем пары электронов,
участвующие в образовании связи. Примером
частицы с таким расположением неподеленной
электронной пары является тетрафторид
серы. Если центральный атом одновременно
имеет неподеленные пары электронов и
образует кратные связи (например, в
молекуле XeOF2),
то в случае sp3d-гибридизации
именно они располагаются в экваториальной
плоскости тригональной бипирамиды.
Механизм
образования связи – обменный или
донорно-акцепторный – не
влияет на тип гибридизации электронных
облаков атомов-партнеров. Линейная
молекула ВеСl2
может образоваться в газовой фазе как
из атомов Ве и Сl, так и из ионов Ве2+
и Сl–.
В последнем случае ион Ве2+
(акцептор) предоставляет вакантные 2s–
и 2p-орбитали,
а ионы Сl–
(доноры) – неподеленные электронные
облака связи. Оба механизма в конечном
итоге приводят к одному и тому же
sр-гибридному
состоянию.
В образовании
молекулы CH4
и NH4+
принимают участие электроны 2s-
и 2p-орбиталей.
Общее число валентных электронов
одинаково в обеих частицах. Именно
вследствие sp3-гибридизации
для них характерна одна и та же структура
– правильного тетраэдра, несмотря на
различие в механизме их образования.
Наличие π-связей
также не влияет на тип гибридизации.
Однако наличие дополнительного связывания
может привести к изменению валентных
углов, поскольку электроны кратных
связей сильнее отталкиваются друг от
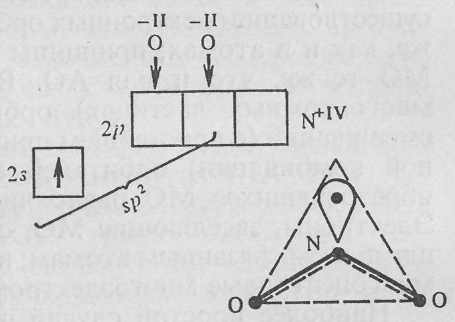
друга. По этой причине, например, валентный
угол в молекуле NO2
(sp2-гибридизация)
увеличивается от 120o
до 134o.
Гибридизация в
молекулах с кратными связями (частичная
гибридизация).
При образовании
кратных связей наряду с σ- образуются
π-связи. В связи с этим можно предположить
частичную гибридизацию, при которой
часть электронов не участвует в
гибридизации, оставаясь на р-орбиталях,
и именно они являются ответственными
за образование π-связей. Так, молекулах
ацетилена С2Н2
и диоксида углерода СО2
каждый атом углерода образует две π- и
две σ- связи, что позволяет предположить
sp
–гибридизацию.
В молекулах этилена С2Н4
и бензола С6Н6
каждый атом углерода образует одну π-
и три σ- связи. Учитывая вышесказанное,
можно предположить, что в этих случаях
имеет место sp2
–гибридизация.
Такие предположения подтверждены
экспериментально – валентные углы в
этих молекулах соответственно 180 и 1200
.
Рис.13 -Связи
в молекуле бензола -Связи
в молекуле бензола
Геометрическая
форма молекул и реакционная способность
веществ
Обычно вещества
с симметричными молекулами химически
более пассивны, чем вещества с
асимметричными молекулами.
Так, реакционная
способность диоксида серы SO2
(незавершенный треугольник) выше, чем
у триоксида серы SO3
(правильный треугольник); сульфаты,
содержащие симметричный анион SO42−
(правильный тетраэдр), химически пассивны
по сравнению с сульфитами, содержащими
несимметричный ион SO32−
(незавершенный тетраэдр).
В молекуле NO2
у атома азота N+IV
(2s12p0)
на одной из sp2-гибридных
орбиталей находится не электронная
пара, а неспаренный электрон. Такие
молекулы особенно реакционноспособны,
их называют радикалами.
В органической
химии радикалами являются метил −CH3,
этил −C2H5
и многие другие.
МЕТОД МОЛЕКУЛЯРНЫХ
ОРБИТАЛЕЙ
(линейная комбинация
атомных орбиталей)
ММО ЛКАО
Метод Валентных
Связей нагляден. Он позволяет теоретически
предсказать форму и полярность молекул,
валентные углы, виды и свойства реализуемых
связей. Однако он не позволяет объяснить
устойчивость частиц с нечетным количеством
электронов, существование и образование
частиц типа Н2+,
Не2+
и т.д., не
объясняет парамагнитные свойства
некоторых молекул, например, кислорода.
Эти трудности позволяет в некоторой
степени преодолеть Метод Молекулярных
Орбиталей.
Основные
положения метода МО:
1)
При образовании молекул все электроны
переходят с атомных орбиталей (АО) на
молекулярные орбитали (МО).
2) Количество МО равно сумме АО
взаимодействующих атомов. Из двух АО
образуется две МО, одна из которых
обладает меньшей энергией и называется
связывающей, другая – большей энергией
и называется разрыхляющей.
Ψ+=
С1
ΨА
+ С2
ΨВ
Ψ–=
С3
ΨА
– С4
ΨВ
,
где
Ψ+
и Ψ–
–
волновые функции связывающей и
разрыхляющей МО, С – доля участия
соответствующих АО в формировании МО.
На рисунках показаны схемы образования
МО из АО различных типов:
Рис. 14 Схема
образования связывающей и разрыхляющей
σs
МО
Рис. 15 Схема
образования молекулы водорода из двух
атомов по методу молекулярных орбиталей
Рис. 16 Схема
образования связывающей и разрыхляющей
σрх
МО
Рис. 17 Схема
образования связывающей и разрыхляющей
πру
и πрz
МО
Схематично
энергетическое распределение молекулярных
орбиталей, образованных атомными
орбиталями 2-го уровня, следующее:
А
В
3) Заполнение МО
происходит по принципу наименьшей
энергии и правилу Хунда. Энергетический
ряд МО:
А) при значительном
энергетическом различии 2s
и 2р орбиталей
σ1s
св
< σ1s
разр
< σ2s
св
< σ2s
разр
< σ2рх св
<π2русв
=π2рzсв<
π2руразр
=π2рzразр<σ2рх
разр
В) при незначительном
энергетическом различии 2s
и 2р орбиталей
σ1s
св
< σ1s
разр
< σ2s
св
< σ2s
разр
<π2русв
=π2р zсв
< σ2рх св
< π2руразр
=π2рzразр<σ2рх
разр
4) кратность связи
равна полуразности количества связывающих
и раэрыхляющих электронов. Образование
молекул или заряженных частиц или
радикалов возможно при условии, что
число электронов на связывающих орбиталях
больше, чем на разрыхляющих.
5) молекулы, имеющие
неспаренные электроны, обладают
парамагнитными свойствами.
Рассмотрим
распределение электронов на МО молекулы
кислорода:
Электронный паспорт
молекулы кислорода запишется так:
(σ1s
св )2(
σ1s
разр)2(
σ2s
св)2(
σ2s
разр)2(
σ2рх
св)2(π2русв)2(π2рzсв)2(π2руразр)1
(π2рzразр)1(σ2рх
разр)0
Кратность связи
равна двум, имеется два неспаренных
электрона, объясняющие парамагнитные
свойства кислорода.
Электронный паспорт
молекулы фтора:
(σ1s
св )2(
σ1s
разр)2(
σ2s
св)2(
σ2s
разр)2(
σ2рх
св)2(π2русв)2(π2рzсв)2(π2руразр)2
(π2рzразр)2(σ2рх
разр)0
Кратность связи
равна единице, все электроны спарены,
что объясняет диамагнитные свойства
фтора.
Распределение
электронов на МО молекулы фтора.
Число общих электронных пар между двумя атомами в молекулах характеризует кратность ковалентной связи: одинарная, двойная или тройная. Какова кратность ковалентной связи в молекулах веществ, формулы которых
H
2
,
C
l
2
,
N
2
?
reshalka.com
ГДЗ Химия 8 класс класс Габриелян. §35. Примените свои знания. Номер №5
Решение
Запишем структурные формулы веществ:
1) H − H: одинарная связь, так как атомы водорода соединяются в молекулу с помощью одной общей электронной пары.
2) Cl − Cl: одинарная связь, так как атомы хлора соединяются в молекулу с помощью одной общей электронной пары.
3) N ≡ N: атомы азота соединяются в молекулу с помощью трёх общих электронных пар.
Содержание:
Ковалентная связь:
Свойство вещества определяется его химическим составом, последовательностью соединения атомов в его молекуле и их взаимодействием. Совокупность сил, связывающих друг с другом атомы в молекуле, называется химической связью. Теория строения атома раскрывает природу химической связи и механизм образования молекулы.
Было установлено, что образование и природа химической связи строение непосредственно связаны со строением наружных электронных слоев взаимодействующих атомов элементов. Имеющиеся к настоящему времени сведения об агомах и молекулах подтверждают электронное происхождение всех химических связей. По правилу октета, при образовании химической связи наружные энергетические уровни завершаются в большинстве случаев образуются восьмиэлектронные октеты …ns2np6, а в некоторых случаях (для атомов и ионов H– , He0, Li+, Be2+, B+3) двухэпектронное дуплетное строение 1s2.
Электроны, участвующие в образовании связи, называются валентными электронами. В различных химических соединениях химические связи по механизму образования и типу отличаются друг от друга. Электроотрицательность элементов влияет на распределение электронов между взаимодействующими друг с другом атомами. По характеру распределения электронов в веществах различают четыре основных типа химической связи.
Химическая связь, возникающая в результате образования общих (связывающих) электронных пар, называется ковалентной связью. Ковалентная связь образуется между атомами неметаллов с одинаковыми или мало отличающимися друг от друга электроотрицательностями. Образование большинства молекул связано с созданием ковалентной связи.
Ковалентная связь это локализованная двухэлектронная связь с двумя центрами. Локализованная связь подразумевает такую связь, которая действует лишь между двумя атомами на ограниченном участке. Одна ковалентная связь образуется одной электронной парой. Т.е. ковалентную связь показывают парными точками или линиями. Эти электроны расположены в наружных электронных слоях обоих атомов.
Ковалентная связь в основном возникает по двум различным механизмам:
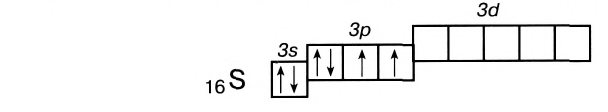
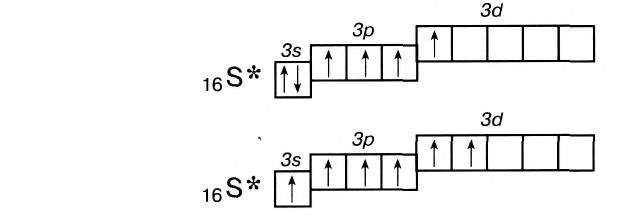
1. Механизм обмена. Каждый атом, образующий ковалентную связь, отдаёт одинаковое количество электронов для образования общей электронной пары. Общую электронную пару образуют неспаренные (одиночные |) электроны атомов, образующих связь. При этом спаренные электроны должны обладать антипараллельными спинами
2. Донорно-акцепторный механизм. Ковалентная связь образуется за счет неподеленной электронной пары одного атома и незаполненных (пустых) орбиталей другого атома. Схематически это выглядит так:
Здесь атом D, предоставляющий свою неподеленную электронную пару для общего пользования, называется донором, а атом А, имеющий свободную орбиталь, акцептором. Образованная таким путем ковалентная связь называется донорно-акцепторной или координативной связью.
 |
Этот механизм химической связи был открыт в 1893 ем году Альфредом Вернером, создавшим координационную теорию комплексных соединений. В связи с этим, донорно акцепторная связь раньше называлась координативной связью. |
Ион аммония (NH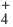
- а) Донорно-акцепторная связь указывается стрелкой, которая всегда направлена от донора (N) в сторону акцептора (H);
- б) При образовании донорно-акцепторной связи валентность атома-донора увеличивается на одну единицу. Степень окисления не меняется.
| Молекулы и ионы | Донор-атом | |
| Валентность | Степень окисления | |
NH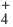 |
4 | -3 |
| NH3 | 3 | -3 |
| H2O | 2 | -2 |
| H3O+ | 3 | -2 |
Установлено, что все связи N H ионе аммония (NH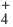
Механизм образования иона аммония
Все кислоты, кроме кремниевой кислоты (H2SiO3), при растворении а воде образуют ион гидроксония (H3O+). Образование иона гидроксония также происходит по донорно акцепторному механизму.
|
Механизм образования иона гидроксония: |
Механизм образования угарного газа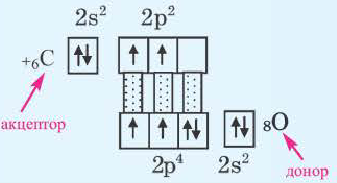 |
| Вещество или ион | Донор | Акцептор | Число электронов, участвующих в образовании связей | |
| у донора | у акцептора | |||
NH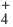 |
N | H | 5 | 3 |
| СО | O | C | 4 | 2 |
| H3O+ | O | H | 4 | 2 |
Виды ковалентной связи
Начертите схему связи и электронов, образующих эту связь.
1. H2S→ 



Какие виды ковалентной связи существуют? Чем они отличаются друг от друга?
Существует два вида ковалентной связи, образованной по механизму обмена:
Неполярная ковалентная связь
Ковалентная связь, образованная между атомами неметаллов одного вида (или между атомами с одинаковой электроотрицательностью), называется неполярной ковалентной связью:
H2, N2, O2, F2, Cl2, Br2,I2, P4, S8
Неполярная ковалентная связь
При образовании ковалентной связи между атомами с одинаковой электроотрицательностью электронные пары между ядрами атомов размещаются симметрично. В образовавшейся в результате
этого молекуле центры положительных и отрицательных зарядов совпадают.
Полярная ковалентная связь
Ковалентная связь, образованная между атомами различных видов неметаллов (или между атомами неметаллов с различными электроотрицательностями), называется полярной ковалентной связью.
Вещества с полярной ковалентной связью:
HCl, СО, SO2, NO2, P2O5, HNO3, H2CO3, H3PO4, SiO2, SiC, CS2, CH4, CF4
В большинстве полярных молекул центры положительных и отрицательных зарядов не совпадают. Одна сторона молекулы частично заряжается положительно, а другая сторона частично отрицательно. В результате создается диполь (поляризация в молекуле). Электронная пара перемещается в сторону атома с большей электроотрицательностью. Молекулы, образующие диполь, бывают полярными.
Полярная ковалентная связь
Слово «диполь» на греческом «polos» означает «полярный». +δ и δ (дельта) относительные заряды.
Их абсолютное значение бывает меньше 1.
Несмотря на то, что в молекулах некоторых веществ все связи полярноковалентные, однако из-за неспособности молекулы к поляризации (т.е. к созданию диполя), они являются неполярными (СО2, СН4).
σ (сигма) и π(пи) – связи
Сущность образования электронных пар, создающих связь, объясняется перекрыванием электронных облаков. В зависимости от направления перекрывания атомных орбиталей, ковалентные связи делятся на две части.
σ – связь. Если электронные облака перекрываются по прямой линии, соединяющей центры связывающих атомов, то такая связь называется сигма-связью. Вращение одного из атомов вокруг прямой линии, соединяющей ядра обоих атомов, не разрывает связи, σ- связь может образоваться во время перекрывания двух s-, двух р-, одного s- и одного р- электронных облаков в отдельности, а также всех гибридных электронных облаков.
При наличии между атамами одной ковалентной связи ее называют одинарной связью. Все одинарные связи σ– связи.
π– связь:
При образовании второй и третьей ковалентных связей между двумя атомами перекрывание электронных облаков происходит не по линии, соединяющей центры атомов. Электронные облака в атоме расположены в отношении друг к другу под определенным углом. И поэтому перекрывание электронных облаков происходит по обе стороны от линии, пересекающей центры атомов.
π- связь.
Ковалентная связь, созданная за счет перекрывания орбиталей по обе стороны от оси, соединяющей центры атомов, называется π- связью, π– связь образуется перекрыванием двух р- орбиталей по обе стороны от оси, соединяющей центры атомов, π– связь могут образовать негибридизированные р- орбитали (р- электроны).
В результате образования π– и σ- связей, находящихся на перпендикулярно расположенных друг к другу плоскостях в пространстве в составе одной молекулы, создаются двойные и тройные связи.
Все одинарные связи являются σ- связью, из двойных же связей одна σ- связь, а другая σ- связь, из тройных связей одна σ- связь, а две π– связи.
| Вещество | 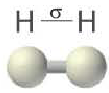 |
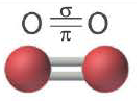 |
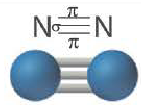 |
| Количество σ- связей | 1 | 1 | 1 |
| Количество π- связей | 0 | 1 | 2 |
Пространственное строение молекул и гибридизация
Определите соответствие.
Какое значение имеют гибридные орбитали в процессе гибридизации? Какие формы гибридизации вы знаете?
Пространственное строение молекулы зависит от формы и направления электронных орбиталей её атомов. Процесс образования новых орбиталей с одинаковыми энергией и формой из комбинации различных орбиталей (s- и р-) называется гибридизацией. Образовавшиеся новые орбитали называются гибридными орбиталями.
- Гибридизация орбиталей атомов происходит во время химических реакций.
- При образовании связи от гибридизированных орбиталей выделяется ещё больше энергии и связь становится более прочной.
- Число образованных гибридных орбиталей равно числу орбиталей, участвующих в гибридизации.
Для s- и р-орбиталей возможны три типа гибридизации.
sp- гибридизация:
При участии одной s- и одной р-орбитали образуются 2 sp- гибридные орбитали, расположенные под углом 180°. Подобная гибридизация характерна для некоторых элементов II группы: ZnCl2, BeCl2, Mgl2 и др. Электронное строение внешнего электронного слоя бериллия имеет вид 2s22p°. При возбуждении атома бериллия один из s- электронов переходит на р- подуровень, а затем, в результате гибридизации одной s- и одной р- орбиталей, образуются две sp-гибридные орбитали с одинаковой энергией,
расположенные под углом 180°.
Образовавшиеся две sp-гибридные орбитали, оттолкнувшись друг от друга, располагаются под углом 180°, т.е. вдоль прямой линии, двигаясь в противоположных направлениях. В результате перекрывания двух sp- гибридных электронных облаков атома Be р-электроными облаками атомов Cl образуется BeCl2 линейного строения.
BeF2, BeCl2, BeBr2, Bel2, СО2 это вещества линейного строения, образованные за счет перекрывания sp- гибридных орбиталей.
sp2– гибридизация:
При участии одной s- и двух р- орбиталей образуются три sp2– гибридные орбитали одинаковой формы, расположенные на одной плоскости под углом 120°. Подобный тип гибридизации характерен для некоторых элементов III группы.
Электронное строение внешнего энергетического уровня атома бора следующее: 2s22p1. При возбуждении атома бора один из электронов переходит с S- орбитали на р- орбиталь и в итоге образуются три одинаковые sp2 гибридные орбитали.
Эти три возбужденных гибридных электронных облака атома бора перекрываются р- электронными облаками атомов фтора и в результате образуется молекула BF3 треугольной формы. Все три образовавшиеся связи находятся на одной плоскости. BCl3, ВВr3, Bl3 также обладают подобным плоским строением.
sp3– гибридизация:
Процесс образования в пространстве четырех гибридных орбиталей из комбинации одной s- и трех р- орбиталей называют sp3– гибридизацией. Для некоторых элементов IV группы характерна sp3– гибридизация: СН4, CCl4, CF4 и др. В нормальном состоянии имеющиеся в наружном электронном слое атома углерода четыре электрона находятся в состоянии 2s22p2. При возбуждении атома углерода во время реакции один из электронов с 2s2– орбитали переходит на 2р- орбиталь и в результате гибридизации в возбужденном состоянии одного S- и трех р- электронных облаков образуются четыре одинаковые sp3– гибридные орбитали.
В метане все гибридные орбитали атома углерода (С), находящегося в состоянии sр3-гибридизации, образуют связь, и молекула приобретает форму тетраэдра (симметрическую), а угол связи составляет -109o28′.
Содержащийся в молекуле воды аnом кислорода не возбуждается. В результате гибридизации двух орбиталей, содержащих по одному электрону, и двух орбита-лей, содержащих по два электрона, образуются четыре sр3-гибридные орбитали.
Гибридные орбитали, содержащие электронные пары атома кислорода в молекуле воды, отталкивают другие гибридные орбитали и в результате молекула приобретает неправильную (несимметрическую) форму тетраэдра, образуя угол связи 104o5′.
В атоме азота в молекуле аммиака возбуждение не происходит. В результате гибридизации трех орбиталей, содержащих по одному электрону, и одной орбитали, содержащей два электрона, создаются 3sp3– гибридные орбитали.
Гибридные орбитали, содержащие электронные пары атома азота в молекуле аммиака, отталкивают другие гибридные орбитали и в результате молекула приобретает неправильную (несимметрическую) форму тетраэдра, а угол связи составляет 107o3′.
Свойства ковалентной связи
Основными характерными свойствами ковалентной связи являются ее прочность, энергия, насыщенность, направленность, полярность, длина и кратность.
Прочность ковалентной связи
Чем больше электронная плотность между ядрами атомов, тем прочнее будет связь. Прочность химической связи зависит от:
1) насыщенности связи; 2) длины связи; 3) полярности связи.
Энергия связи
Энергия связи это количество минимальной энергии, необходимой для того, чтобы разорвать связь. Единицей энергии связи является кДж/моль, которая предусмотрена для 1 моль связи. Энергия связи 1 моль водорода равна 436 кДж/моль. Процесс разрыва связи можно выразить в виде термохимического уравнения:
H H – 2Н 436 кДж/моль или ΔH=+436 кДж/моль
Энергия связи для 1 молекулы равна соотношению между минимальной энергией, необходимой для разрыва связи, и постоянной Авогадро.
Для вычисления энергии, необходимой для разрыва одной связи в многоатомных молекулах, следует поделить общую энергию связи на количество связей. Энергия связи в молекуле метана(СН4)
ΔH=+1647 кДж/моль Эсвязи= 1647 : 4 ≈ 412 кДж/моль
Однако действительное значение каждой отдельно взятой энергии связи несколько отличается от ее среднего значения.
Пользуясь понятием энергии связи, можно определить, являются ли химические реакции экзотермическими или эндотермическими.
Разница между суммой энергий связи между атомами продуктов реакции и суммой энергий связи между атомами веществ, вступивших в реакцию, определяет тепловой эффект химической реакции. Если эта разница положительная, то реакция экзотермическая, а при отрицательной разнице эндотермическая. При вычислении же по изменению энтальпии (ΔH) бывает наоборот.
Qpeaн.=(6 . QС H + QС С ) (4 ∙ QС H + QС=С + QH H ); ΔH= Q
В общем виде вычисляется следующим образом:
Δ H равен тепловому эффекту реакции с противоположным значением, называется изменением энтальпии. Оно находится только посредством вычислений.
Насыщенность связи
Насыщенность ковалентной связи определяется валентными возможностями атомов. Возможность образования ковалентной связи определяется числом валентных электронов (или образующих ковалентную связь орбиталей). Например, в атоме углерода, имеющем в наружном электронном слое всего 4 орбитали, в возбужденном состоянии содержится 4 одиночных электрона и поэтому атом углерода способен образовать не более 4-х ковалентных связей. Валентные возможности атомов определяются числом неподеленных электронных пар, которые могут быть отданы другим атомам с незаполненными орбиталями на наружном энергетическом уровне.
Направленность связи
Это свойство ковалентной связи обуславливает пространственное строение молекул. Направленность химических связей объясняется различным расположением электронных облаков в пространстве. Во время взаимного перекрывания электронных облаков в пространстве могут образоваться соединения, молекулы которых будут иметь линейную форму или форму угла. Н2, N2, F2, НСl, СО, NO имеют линейное строение, а H2O, SO2, NO2 форму угла.
Кратность связи определяется числом электронных пар (числом ковалентных связей), соединяющих два атома. В молекуле кислорода кратность связи равна 2. На внешнем энергетическом уровне каждого атома кислорода содержатся два неспаренных одиночных электрона: O=O
В молекуле азота кратность связи равна 3. На внешнем энергетическом уровне каждого атома азота содержатся три неспаренных одиночных электрона. N 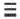
Длина связи это расстояние между ядрами атомов, образующих связь; измеряется в нанометрах (нм). Чем короче длина химической связи, тем прочнее будет связь.
Полярность связи зависит от смещения электронной пары, образующей ковалентную связь, в сторону одного из атомов.
В галогенидах водорода (HF, HC1, HBr, HI) в связи с увеличением радиуса по мере возрастания порядкового номера галогена, увеличивается и длина связи. Так как F (фтор) самый сильный неметалл, HF отличает большей полярностью и прочностью. В связи с увеличением длины связи в HF, HC1, HBr, HI, по мере увеличения радиуса, их полярность, прочность связи уменьшаются, а кислотность, восстановительные свойства усиливаются.
полярность, прочность связи уменьшаются, кислотность, восстановительные свойства усиливаются.
Природа и типы химической связи
При обычных условиях химические элементы существуют в форме различных атомных частиц в составе простых и сложных веществ. Из них только простые вещества благородных газов (элементов VIIIA-группы) являются одноатомными молекулами, а остальные представляют собой самые разнообразные соединения. Число атомов в таких соединениях колеблется от двух до сотен и тысяч. Силы, которые обеспечивают существование таких агрегатов (молекул, радикалов, кристаллов и др.), получили название химическая связь.
Химическая связь — это взаимодействие, которое связывает отдельные атомы в более сложные системы (молекулы, радикалы, кристаллы и т. д.).
Причиной образования химической связи является стремление атомов путем взаимодействия с другими атомами достичь более устойчивого состояния, т. е. состояния с минимально возможным запасом энергии. Следовательно, основным условием образования химической связи является понижение полной энергии Е многоатомной системы по сравнению с суммарной энергией изолированных атомов, т. е.
в случае образования вещества АВ из атомов А и В.
Таким образом, образование химической связи всегда сопровождается выделением энергии.
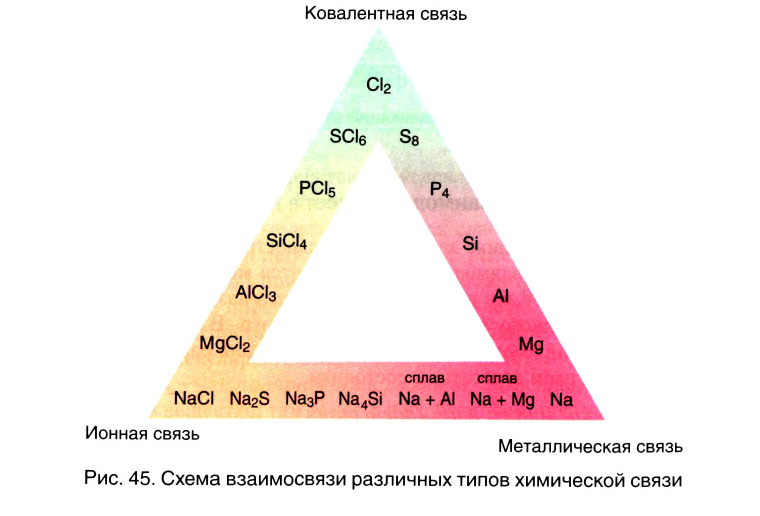
Природа сил химической связи — электростатическая, т. е. обусловлена различными видами взаимодействий положительно заряженных ядер и отрицательно заряженных электронов (рис. 15).
Главную роль при образовании химической связи между атомами играют их валентные электроны, т. е. те электроны, которые обычно находятся на внешнем энергетическом уровне и наименее прочно связаны с ядром атома. У атома на внешнем энергетическом уровне может содержаться от одного до восьми электронов. Завершенными, а поэтому и самыми устойчивыми, являются внешние электронные оболочки атомов благородных газов: у гелия там находится два электрона (1s2) и у остальных — по восемь электронов (ns2np6, где n — номер периода).
У атомов остальных элементов внешние энергетические уровни являются незавершенными, и поэтому в процессе химического взаимодействия атомы стремятся их завершить, т. е. приобрести электронное строение атома ближайшего благородного газа. Это соответствует нахождению двух электронов на внешнем уровне у атомов водорода, который расположен в одном периоде с гелием, и восьми электронов (октет) — у всех остальных атомов. Достичь такого электронного состояния атомы могут только за счет обобществления электронов, т. е. их совместного использования атомами, соединяющимися между собой. При этом образуются общие электронные пары, которые связывают атомы друг с другом — между ними возникает химическая связь.
В зависимости от способа обобществления электронов различают три основных типа химической связи: ковалентную, ионную и металлическую.
Ковалентная связь:
Ковалентная связь возникает обычно между двумя атомами неметаллов с одинаковыми или близкими значениями электроотрицательности. Рассмотрим образование ковалентной связи на примере простейшей молекулы — молекулы водорода Н2. У атома водорода всего один электрон, находящийся на внешнем (первом) энергетическом уровне, до завершения которого не хватает одного электрона.
При сближении двух атомов водорода за счет сил притяжения, действующих между их ядрами и электронами, происходит частичное перекрывание электронных облаков неспаренных электронов с антипараллельным спином (это одно из условий образования общей электронной пары!). В зоне их перекрывания плотность двухэлектронного облака увеличивается. Ядра атомов стягиваются к этой области повышенного отрицательного заряда до тех пор, пока не наступит равновесие между силами межъядерного отталкивания и силами притяжения. Расстояние между ядрами атомов уменьшается, энергия системы, состоящей из двух атомов водорода, также понижается. Область повышенной электронной плотности связывает два атома водорода в молекулу Н2 (рис. 16).
Образование химической связи между атомами водорода в молекуле можно показать различными способами. Например, с помощью электронных формул, в которых Указывают символы элементов и валентные электроны в виде точек:
В графических (или структурных) формулах пару электронов обозначают с помощью черточки:
В случае молекулы водорода эта единственная черточка символизирует ковалентную связь.
Химическая связь, возникающая в результате обобществления электронов с образованием общих электронных пар между атомами, называется ковалентной связью.
Образование ковалентной связи можно показать и с помощью электронно-графических схем, на которых обычно указываются только орбитали внешнего энергетического уровня:
Волнистая линия между двумя орбиталями 1s указывает на то, что каждый электрон как бы одновременно находится как на одной, так и на другой орбитали. В данном случае ковалентная связь образована в результате перекрывания двух s-opбиталей (или s-облаков) (рис. 17).
Подобным образом образуется ковалентная связь и между двумя атомами фтора в молекуле F2. Атом фтора имеет 7 электронов на внешнем электронном слое, один из них — неспаренный электрон. При сближении двух атомов фтора происходит перекрывание электронных облаков их неспаренных электронов, образуется общая электронная пара и внешний энергетический уровень каждого атома фтора завершается до октета (8 электронов):
Схема образования молекулы фтора с помощью электронных формул:
а графическая формула молекулы:
В данном случае образование ковалентной связи произошло за счет перекрывания р-электронных облаков (рис. 18).
Одинарная связь:
И в молекуле водорода, и в молекуле фтора атомы связаны электронной парой, образующей одну химическую связь, называемую одинарной. В обоих случаях перекрывание электронных облаков (как s-, так и р-) происходит вдоль линии, соединяющей центры взаимодействующих атомов. Эту условную прямую называют линией (или осью) связи.
Ковалентная связь, образованная за счет перекрывания атомных орбиталей вдоль линии связи, называется 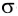
Пару электронов, образующих ковалентную связь, называют связывающей в отличие от электронных пар, которые не участвуют в образовании связей и, следовательно, являются несвязывающими. Такие пары часто также называют неподеленными, поскольку они принадлежат только одному атому.
У атомов водорода в молекуле Н2 нет несвязывающих пар, а в молекулах F2, С12, Вr2 или I2 у каждого из атомов галогенов их по три:
- Причиной образования химической связи является стремление атомов к достижению более устойчивого состояния, что приводит к выделению энергии при образовании связей.
- Природа сил химической связи — электростатическая, т. е. определяется различными видами взаимодействий электронов и ядер в системе связанных атомов.
- Различают три основных типа химической связи — ковалентную, ионную и металлическую.
- Ковалентная связь — это химическая связь, возникающая в результате образования общих электронных пар между двумя атомами.
Кратные связи. Полярная и неполярная ковалентная связь
Два атома могут быть связаны между собой не только одной, но и несколькими ковалентными связями. В таком случае говорят о кратности связи, понимая под этим термином число электронных пар, участвующих в образовании ковалентной связи.
Кратные связи
У атомов азота (элемента VA-группы) до завершения внешнего энергетического уровня не хватает трех электронов:
Поэтому при образовании молекулы N2 атомы азота обобщают уже не одну, а три пары электронов:
Схема образования молекулы азота:
а графическая формула молекулы:
Одна из ковалентных связей, образовавшаяся в результате перекрывания р-электронных облаков вдоль линии связи, представляет собой 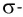
Такая ковалентная связь получила название 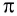
► 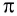
Облака s-электронов не могут образовывать 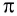
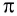
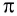
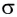
Если ковалентная связь между двумя атомами образуется двумя общими электронными парами, то такая ковалентная связь называется двойной связью, и она обозначается двумя черточками. Например, в молекуле этена С2Н4 атомы углерода соединены между собой двойной связью:
одна из которых — 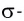
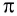
Если в молекуле имеется тройная связь, как, например, в молекуле азота N2, то одна из них — 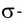
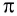
Полярная и неполярная ковалентная связь
До сих пор мы рассматривали ковалентную связь, образованную атомами одного и того же элемента. В этом случае общая пара электронов располагается симметрично между двумя атомами с одинаковой электроотрицательностью. Такая ковалентная связь называется неполярной.
Если же взаимодействуют атомы с различными электроотрицательностями, т. е. атомы разных элементов, то общая электронная пара смещается к атому с большей электроотрицательностью. В таких случаях возникает полярная ковалентная связь.
Например, в молекуле хлороводорода HCI общая электронная пара смещена в сторону более электроотрицательного элемента, каким является хлор:
В данном случае перекрываются сферическое s-электронное облако атома водорода и гантелеобразное р-облако атома хлора (рис. 21).
Схема такого перекрывания:
В результате смещения общей электронной пары в молекуле HCl на атоме хлора возникает частичный отрицательный заряд, а на атоме водорода — такой же по величине, по положительный заряд:
(греческая буква 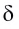
Значение заряда 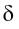
Чем больше разность электроотрицательностей связанных атомов, тем более полярна химическая связь межту ними.
С помощью ковалентной связи образуются молекулы и более сложных веществ, состоящих из трех, четырех и более атомов. В качестве примера рассмотрим образование молекулы аммиака NH3. Электронно-графическая схема взаимодействия трех атомов водорода и одного атома азота следующая:
Общая схема образования аммиака:
а графическая формула молекулы:
Таким образом, три неспаренных электрона атома азота принимают участие в образовании трех ковалентных связей с атомами водорода, а на внешнем энергетическом уровне у атома азота остается еще неподеленная пара электронов. Каждая связь N — Н является полярной. В целом вся молекула NH;i представляет собой диполь, так как она имеет форму пирамиды с атомом азота в ее вершине. Однако существует много молекул, которые содержат полярные связи, но сами являются неполярными. Это объясняется особенностями их пространственного строения. Об этом мы поговорим в следующих параграфах.
- Кратность связи определяется числом общих электронных пар между двумя связанными атомами.
- Ковалентная связь, при образовании которой области перекрывания электронных облаков находятся по обе стороны от линии, соединяющей ядра атомов, называется
-связью.
- При соединении двух атомов с разными электроотрицательностями возникает ковалентная полярная связь.
Механизмы образования ковалентной связи
Различают два основных механизма образования ковалентной связи — обменный и донорно-акцепторный.
Обменный механизм образования связи
Ковалентная связь образуется двумя атомами с помощью двух электронов с антипараллельным спином, т. е. химическая связь находится (локализована) между двумя атомами. Так как нахождение двух электронов в поле действия двух ядер энергетически выгоднее, чем пребывание каждого электрона в поле своего ядра, то в образовании ковалентной связи принимают участие все одноэлектронные орбитали внешнего энергетического уровня. Например, атом азота имеет три не-спаренных электрона на внешнем уровне:
атом кислорода — два:
а атом фтора — один:
Поэтому эти атомы могут образовывать за счет таких электронов соответственно три, две и одну ковалентные связи.
Число неспаренных электронов может увеличиваться при переходе атома в возбужденное состояние. Например, на внешнем энергетическом уровне атома углерода находится только два неспаренных электрона.
Однако в большинстве своих соединений углерод проявляет валентность, равную 4, образуя четыре ковалентные связи, например: С02, СН4, ССl4 и т.д. Такая валентность атома углерода становится возможной благодаря тому, что его атом при образовании химических связей с другими атомами переходит в возбужденное состояние (т. е. в состояние с большей энергией) за счет распаривания пары электронов 2s2 и перехода одного из них па подуровень 2р:
В возбужденном состоянии атом углерода имеет четыре неспаренных электрона, за счет которых он может образовывать четыре ковалентные связи с атомами других элементов. Распаривание электронов требует затраты энергии, но эта затрата с избытком компенсируется энергией, выделяющейся при образовании дополнительных связей. Распаривание, как правило, происходит лишь в пределах данного энергетического уровня, поскольку переход электронов на свободные орбитали другого уровня энергетически не выгоден. Поэтому в возбужденное состояние могут перейти атомы только тех элементов второго периода, у которых имеются свободные орбитали (бериллий, бор, углерод). У атомов азота, кислорода и фтора нет свободных орбиталей на втором энергетическом уровне, а переход электронов на третий уровень потребует слишком больших затрат энергии, которые не компенсируются выделением энергии при образовании дополнительных связей.
В то же время атомы элементов третьего и следующих периодов имеют на внешнем энергетическом уровне d-подуровень, на который при возбуждении могут переходить s- и р-электроны:
Благодаря этому атом хлора способен образовывать не одну, а несколько ко-валентных связей, вплоть до семи, как, например, в оксиде Сl207.
Таким образом, атомы при образовании ковалентных связей используют все свои неспаренные электроны, как находящиеся в основном состоянии, так и образовавшиеся при распаривании.
- Механизм образования ковалентной связи за счет обобществления не-спаренных электронов двух взаимодействующих атомов называется обменным.
Донорно-акцепторный механизм образования ковалентной связи
Образование ковалентной связи возможно и при взаимодействии атомов, один из которых имеет пару неподеленных электронов (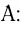

Атом, предоставляющий электронную пару для образования связи, называется донором, а участвующий в обобществлении пары за счет свободной орбитали, — акцептором. Такой механизм образования ковалентной связи получил название донорно-акцепторного.
Механизм образования ковалентной связи за счет неподеленной пары электронов одного атома и свободной орбитали другого называется донорно-акцепторным.
Примером такого механизма может служить образование иона аммония 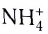
Сокращенно ионное уравнение этой реакции:
Составим электронную схему такого взаимодействия, обозначив точками электроны, принадлежащие атому азота, а звездочками — атомам водорода:
В ионе аммония каждый атом водорода связан с атомом азота общей электронной парой. И хотя одна из этих связей образована по донорно-акцепторному механизму, она не отличается по своим характеристикам от остальных ковалентных связей, образованных по обменному механизму.
Донорно-акцепторный механизм позволяет объяснить существование иона гидроксония Н30+, в виде которого находится в водных растворах ион водорода. Эта частица образуется в результате гидратации иона водорода:
Электронная схема этого процесса:
- Обменным называется механизм образования ковалентной связи, при котором каждый атом предоставляет для формирования общей электронной пары один неспаренный электрон.
- Механизм образования ковалентной связи за счет электронной пары одного атома и свободной орбитали другого называется донорно-акцепторным.
Свойства ковалентной связи
Вы уже познакомились с одной из характеристик ковалентной связи — полярностью. Полярность связи и всей молекулы в целом во многом определяет физические и химические свойства вещества, такие, как температуры кипения и плавления, растворимость и даже способность вступать в химические реакции с другими веществами.
Рассмотрим еще некоторые характеристики ковалентной связи.
Энергия и длина связи
Одной из важнейших характеристик химической связи является ее прочность. Прочность связей определяет реакционную способность вещества.
Мерой прочности связи является та энергия, которую необходимо затратить на ее разрыв. Эту характеристику называют энергией связи. В случае веществ с двухатомными молекулами ее величину рассчитывают на 1 моль вещества. Так. у молекулы водорода Н2 энергия связи Н — Н равна 435 кДж/моль, у молекулы фтора F2 — 159 кДж/моль, а у молекулы азота эта характеристика равна 943 кДж/моль. Чем меньше энергия связи, тем менее прочной является ковалентная связь, тем больше реакционная способность вещества.
Еще одной характеристикой прочности связи является длина связи — расстояние между ядрами химически связанных атомов. С увеличением радиусов атомов длина связи между ними увеличивается, а прочность — уменьшается. Ковалентная связь Н—Н более прочная, чем связь F—F, так как ее длина равна 0,074 нм, а связи F—F — 0,142 нм.
Увеличение кратности связи приводит к уменьшению межъядерного расстояния и упрочнению связи между атомами (табл. 9).
Из таблицы 9 видно, что энергия двойной связи 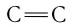


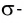
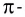
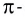
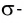
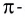
Насыщаемость
Ковалентная связь характеризуется насыщаемостью. Это свойство состоит в том, что образование связывающей два атома электронной пары исключает ее участие в других химических взаимодействиях. Благодаря этому общее число ковалентных связей, которые способен образовывать тот или иной атом, ограничено. Оно определяется числом орбиталей атома, использование которых для образования химических связей энергетически выгодно. Так, элементы второго периода, у атомов которых внешний энергетический уровень состоит только из четырех орбиталей (одна s- и три р-типа), могут образовать не более четырех ковалентных связей. У атомов следующих периодов в образовании ковалентных связей могут принимать участие и d-орбитали как внешнего, так и предвнешнего энергетических уровней.
Поэтому ковалентные соединения имеют строго определенный состав.
Направленность ковалентной связи
Ковалентная связь между двумя атомами располагается таким образом, чтобы обеспечить максимальное перекрывание электронных облаков. Поскольку в образовании связей принимают участие электронные облака различной формы и ориентации в пространстве, то и ковалентные связи, образованные этими облаками, также характеризуются определенной направленностью.
Если ковалентная связь образуется путем перекрывания сферических s-электронных облаков, как, например, в молекуле Н2, то она может располагаться в любом направлении (рис. 23) относительно центра данного атома.
А вот в молекуле Сl2, где ковалентная связь образована за счет перекрывания р-облаков, область перекрывания располагается только вдоль линии связи, определенной пространственной ориентацией р-облака (рис. 24).
Следовательно, направленность ковалентных связей объясняется различным расположением электронных облаков в пространстве.
- Основными характеристиками ковалентной связи являются ее длина, энергия, полярность, насыщаемость.
- Ковалентные химические связи характеризуются определенной направленностью.
Понятие о стереохимии и атомные кристаллические решетки
Каждая молекула представляет собой систему взаимосвязанных атомов, расположенных определенным образом относительно друг друга. Следовательно, молекула характеризуется определенным пространственным строением, или, говоря иначе, геометрией (формой).
Вопросы строения молекул рассматривает один из разделов химии, который называется стереохимией (в буквальном переводе с греческого языка — пространственная химия).
Согласно стереохимическим представлениям, когда один атом образует несколько связей, они будут направлены под определенными углами друг к другу. Угол между связями (или валентный угол) — это угол между воображаемыми прямыми, проходящими через ядра химически связанных атомов. Такие прямые, как вы уже знаете, называются линиями связи (рис. 25).
Например, в молекуле Н20 атом кислорода образует две 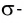
Аналогично в молекуле NH3 углы между связями N—Н, образованные тремя р-орбиталями атома азота, также должны быть близки к 90° (рис. 27), а вся молекула в целом должна иметь форму треугольной пирамиды с атомом азота в вершине.
Действительные значения углов между связями (104,5° в молекуле Н20 и 107° в молекуле NH3) отличаются от ожидаемых. Увеличение валентных углов можно объяснить взаимным отталкиванием положительно заряженных атомов водорода. Например, уже в молекуле H2S такое отталкивание слабее, чем в молекуле Н20 (так как радиус атома серы больше радиуса атома кислорода), и угол Н—S—Н ближе к 90°, чем угол Н—О—Н.
За счет ковалентной связи образуются не только молекулы. Некоторые простые и сложные вещества построены из атомов, связанных друг с другом ковалентными связями, и образуют протяженные кристаллические структуры — атомные кристаллические решетки.
Примерами таких веществ являются простые вещества — бор, алмаз, кремний. В кремнии (как и в кристалле алмаза)(рис. 28) каждый атом связан четырьмя ковалентными связями с другими атомами.
Подобное строение имеют и сложные вещества: карбид кремния SiC и оксид кремния Si02 (кварц).
Атомных кристаллов сравнительно немного. Благодаря высокой прочности ковалентных связей они имеют очень высокие температуры плавления, большую твердость. Так, самым твердым природным веществом является алмаз — его температура плавления более 3500 °С. Карбид кремния SiC также является одним из самых твердых веществ с очень высокой температурой плавления — более 2700 °С.
- Стереохимия — раздел химии, рассматривающий пространственное строение молекул или кристаллов.
- Кристаллические структуры, построенные из атомов, связанных друг с другом ковалентными связями, называются атомными кристаллическими решетками.
Гибридизация атомных орбиталей
Вы уже знаете, что в образовании ковалентных связей принимают участие как s-, так и р-электроны, орбитали которых имеют разную форму и направленность в пространстве. Вместе с тем связи, которые образуются при их участии, оказываются равноценными и расположенными симметрично.
В рамках электронной теории химической связи эти факты объясняются на основе концепции гибридизации атомных валентных орбиталей. Согласно данной концепции в образовании ковалентных связей участвуют не «чистые», а так называемые гибридные, усредненные по форме и размерам (а следовательно, и по энергии) орбитали. Число таких орбиталей равно числу исходных орбиталей. Гибридные орбитали более вытянуты в пространстве (рис. 29), что обеспечивает их более полное перекрывание с орбиталями соседних атомов при образовании связей. Гибридные орбитали, вследствие особой симметрии, в образовании 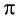
Условия устойчивой гибридизации:
- в гибридизации могут участвовать орбитали с близкими значениями энергий, т. е. s- и р-орбитали внешнего энергетического уровня и d-орбитали внешнего или предвнешнего уровня;
- гибридная атомная орбиталь должна более полно перекрываться с орбита-лями другого атома при образовании связей;
- в гибридизации участвуют орбитали с достаточно высокой электронной плотностью, которыми в большинстве случаев являются орбитали элементов начальных периодов;
- гибридные орбитали должны быть ориентированы в пространстве таким образом, чтобы обеспечить максимальное взаимное удаление друг от друга. В этом случае энергия их отталкивания (и, следовательно, энергия всей системы) минимальна.
Ориентация гибридных орбиталей определяет геометрическую структуру молекулы и молекулярных ионов. Так, при комбинации одной s- и одной р-орбитали возникают две sp-гибридные орбитали, расположенные симметрично под углом 180° (рис. 31). Соответственно связи, образованные с участием электронов этих орбиталей, также располагаются под углом 180°. Например, у атома бериллия sp-гибридизация орбиталей проявляется в молекуле ВеСl2, которая вследствие этого имеет линейную форму (рис. 32).
Комбинация трех орбиталей (одной s- и двух р-типа) приводит к образованию трех sp2-гибридных орбиталей, расположенных в одной плоскости под углом 120° (рис. 33) (например, в молекуле BF3) (рис. 34).
Комбинация четырех орбиталей (одной s- и трех р-типа) приводит к sр3-гибридизации, при которой четыре гибридные орбитали симметрично ориентированы в пространстве к четырем вершинам тетраэдра, т. е. под углом 109°28′ (рис. 35) (атом углерода в молекуле СН4) (рис. 36).
Основные характеристики указанных типов гибридизации приведены в таблице 10.
Существуют и другие типы гибридизации атомных орбиталей. Они достаточно доступны для понимания, но их рассмотрение выходит за рамки школьного курса.
- Гибридизация атомных орбиталей — усреднение по форме и энергии электронных облаков, соответствующих разным орбиталям.
- В гибридизации могут участвовать орбитали с близкими значениями энергии.
- Гибридные орбитали должны быть ориентированы в пространстве таким образом, чтобы обеспечить максимальное взаимное удаление друг от друга.
- Гибридные орбитали участвуют в образовании только
связи.
Пространственное строение молекул
Пространственное строение молекул или молекулярных ионов зависит от типа гибридизации и взаимного расположения в пространстве гибридизованных орбиталей центральных атомов.
В реальных молекулярных структурах углы между связями часто отличаются от углов, соответствующих типу гибридизации.
В чем причина таких отклонений?
Прежде чем ответить на этот вопрос, выделим несколько положений, на которых основываются подходы к рассмотрению геометрии молекул.
Линия связи (или ось связи) — это прежде всего область перекрывания электронных облаков при образовании 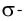
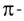
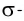
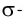
Основными причинами отклонений углов связей от углов, соответствующих типу гибридизации, являются следующие.
1. Не все гибридные орбитали участвуют в образовании связей, часть из них — несвязывающие. Электронные пары, находящиеся на этих орбиталях, также называются несвязывающими (или неподеленными). Например, у атома азота в молекуле NH3 одна пара электронов — несвязывающая, а в молекуле Н20 у атома кислорода две пары электронов являются несвязывающими:
Связывающая электронная пара локализована между двумя атомами и поэтому занимает меньше пространства, чем электронное облако несвязывающей пары. Вследствие этого отталкивающее действие несвязывающей пары проявляется в большей мере, чем связывающей. В молекулах воды и аммиака у атомов (N и О) один и тот же тип гибридизации атомных орбиталей sp3. Однако вследствие наличия одной (у азота) и двух (у кислорода) несвязывающих пар идеальный угол для этого типа гибридизации, равный 109°28′ уменьшается соответственно до 107° (угол Н — N — Н) и 104,5° (угол Н —О—Н) (рис.37, 38).
Число атомов В (в общем случае и число групп атомов), непосредственно связанных с центральным атомом А, называется его координационным числом. В соединениях с ковалентным типом связей координационное число атома равно числу 
2. Наличие 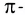
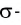
Предполагается, что электронные пары кратной связи занимают ту же область пространства, что и электронная пара простой связи. Суммарное электронное облако кратной связи (двойной или тройной) занимает больший объем пространства, чем одинарной, и поэтому обладает большим отталкивающим действием. Например, в молекуле COF2, имеющей плоскостное строение (sp2-гибридизация атома углерода), углы связи F—С—О больше угла связи F—С—F, так как связь С = 0 является двойной и обладает большим отталкивающим действием, чем одинарная связь С—F (рис. 39).
В молекуле углекислого газа С02, графическая формула которого
две ковалентные связи одинарные, т. е. являются 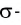
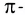
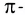
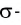
Многоцентровые связи
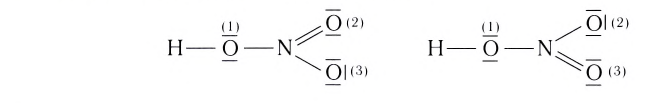
Строение многих молекул нельзя изобразить только одной графической формулой с точной локализацией кратной связи, поскольку истинные свойства молекулы оказываются промежуточными между теми, которые отражаются в каждой отдельной схеме. Например, строение молекулы HNO3 можно изобразить двумя равнозначными графическими формулами:
Поскольку в этой молекуле оба атома кислорода 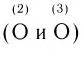
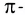
В этой формуле пунктирные линии означают, что одна из общих электронных пар в равной степени распределена между одной и другой связями N—О. Другими словами, эта электронная пара принадлежит не двум, а трем атомам и, следовательно, образованная ею связь является трехцентровой.
Примерами структур с многоцентровыми (делокализованными) 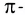
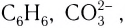
- Геометрия любой молекулы определяется в основном пространственной направленностью
связей, т. е. углами между воображаемыми прямыми, проходящими через ядра химически связанных атомов.
- На пространственное строение молекул оказывают влияние и несвязывающие (неподеленные) пары электронов, уменьшающие углы связей между
связями.
Валентность и степень окисления
Валентность и валентные возможности атомов
Мы установили, что атомы способны образовывать ковалентные связи различным образом. Количественно эта способность атомов оценивается с помощью характеристики, называемой валентностью.
Валентность — мера способности атомов данного элемента соединяться с другими атомами.
Такое толкование валентности является общим, или стехиометрическим. Оно обосновывает количественные соотношения атомов элементов в любых химических соединениях.
С развитием электронных представлений о строении веществ понятие валентности приобрело определенное физическое обоснование. В современной химии валентность химического элемента определяется числом ковалентных связей, которыми данный атом связан с другими атомами.
Ковалентные связи могут быть образованы как с помощью одноэлектронной орбитали атома, так и с помощью неподеленной пары электронов (если атом — донор) или свободной орбитали (если атом — акцептор). Следовательно, можно сказать, что валентность химического элемента также равна числу электронных орбиталей, которые данный атом использует для образования ковалентных связей.
Таким образом, валентность химического элемента определяется как числом ковалентных связей, которыми его атом связан с другими атомами, так и числом орбиталей, используемых этим атомом для образования связей.
Зная электронное строение атома того или иного элемента, можно определить его валентные возможности. Так, атом водорода всегда проявляет валентность, равную единице, поскольку у него всего одна орбиталь.
Анализируя строение простых и сложных веществ, образованных атомами элементов второго периода, нетрудно убедиться, что большинство этих элементов могут проявлять переменную валентность. Например, в молекулах простых веществ N2, 02, F2 атом азота имеет валентность, равную трем, кислорода — двум, а фтора — единице согласно графическим формулам этих молекул:
Простые вещества бора и углерода являются немолекулярными соединениями, однако атомы этих элементов связаны в кристаллах ковалентными связями: бор — тремя, а углерод — четырьмя. Поэтому их валентности равны соответственно III и IV.
В то же время в соединениях с атомами других элементов кислород, азот и фтор способны проявлять и другие валентности. Например, в молекулярном ионе 
В любом случае у элементов второго периода максимальная валентность не может быть больше четырех, так как на внешнем электронном слое у атомов этих элементов всего четыре орбитали, и, следовательно, атомы максимально могут образовать только четыре ковалентные связи.
У атомов элементов третьего периода в связи с появлением d-подуровня валентные возможности увеличиваются, так как в результате распаривания Зр- и 3s-электронов может образоваться от четырех до семи (у хлора) неспаренных электронов. Например, сера, помимо валентности II в основном состоянии:
может проявлять также валентности IV и VI:
Такое распаривание электронов проявляется обычно поддействием атома более электроотрицательного элемента, например фтора, кислорода, поэтому свои высшие валентности атомы проявляют обычно в соединениях с кислородом и фтором.
Таким образом, валентность является численной характеристикой способности атомов данного элемента образовывать ковалентные связи и поэтому может относиться только к соединениям с таким типом связи.
Степень окисления
Более универсальной характеристикой состояния атома в химическом соединении является степень окисления.
Степень окисления — это условный заряд атома в химическом соединении, если предположить, что оно состоит из ионов.
При определении степени окисления атомов предполагают, что все связывающие электронные пары перешли к более электроотрицательному атому. На самом деле такого полного смещения не происходит даже при взаимодействии элементов с большой разницей в электроотрицателыюстях.
Однако условно считают такое смещение электронных нар полным независимо от реальной степени смещения.
Численное значение этой характеристики выражается в единицах заряда электрона и может иметь положительное, отрицательное и нулевое значения.
Количественно степень окисления определяется числом валентных электронов, смещенных от атома данного элемента в химическом соединении (положительная степень окисления) или к нему (отрицательная степень окисления).
В основу расчета степени окисления атомов в соединениях положен принцип, согласно которому алгебраическая сумма степеней окисления атомов в соединении равна нулю, а в сложном ионе (типа 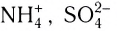
При расчетах надо знать несколько основных положений.
1. Металлы во всех сложных соединениях имеют только положительные степени окисления.
2. Неметаллы могут проявлять как положительные, так и отрицательные степени окисления.
3. Элементы, проявляющие постоянную степень окисления:
- а) щелочные металлы (Li, Na, К, Rb, Cs) — +1;
- б) металлы второй группы (А и В) — +2;
- в) алюминий — +3;
- г) фтор — -1.
Кислород практически во всех своих соединениях проявляет степень окисления —2, исключая его фторид OF2 и пероксид Н202.
4. Высшая положительная степень окисления, как правило, равна номеру группы периодической системы.
5. Низшая отрицательная степень окисления обычно равна разности:
Для большинства элементов характерно проявление переменных степеней окисления в зависимости от атомов, с которыми они связаны, и типа соединения, в котором они находятся. Например, атом азота может проявлять самые разнообразные степени окисления от —3 в молекуле аммиака NH3 до +5 в молекуле азотной кислоты HN03.
Степень окисления не следует отождествлять с валентностью элемента, хотя их численные значения часто совпадают:
В пероксиде Н — О — О — Н валентность кислорода равна двум, а степень окисления —1, в ионе Н30+ его валентность III, а степень окисления —2.
Очень часто степень окисления элемента определяется как алгебраическая сумма степеней окисления по всем связям с другими элементами. Например, в молекуле гидроксиламина NH2OH общая степень окисления азота равна —1. так как по двум связям с водородом азот проявляет суммарную степень окисления —2, а по связи с атомом кислорода +1:
Степень окисления характеризует состояние атомов элемента в сложном веществе независимо от типов связей его атомов. Особенно важна эта характеристика при составлении уравнений окислительно-восстановительных реакций.
- Валентность химического элемента определяется числом ковалентных связей, которыми его атом связан с другими атомами, или, что то же самое, числом орбиталей, используемых данным атомом для образования связей.
- Степень окисления — это условный заряд атома в химическом соединении, вычисленный из предположения, что оно состоит из ионов.
Ионная связь и металлическая связь
Ковалентная химическая связь обычно возникает между атомами неметаллов с одинаковой или не очень сильно различающейся электроотрицательностью. Если различие в электроотрицательности атомов, между которыми образуется химическая связь, велико (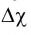
Ионная связь
Ионная связь, как правило, возникает между атомами типичных металлов и типичных неметаллов. Характерным свойством атомов металлов является то, что они легко отдают свои валентные электроны, тогда как атомы неметаллов способны легко их присоединять.
Рассмотрим возникновение ионной химической связи, например, между атомами натрия и атомами хлора в хлориде натрия NaCl.
Отрыв электрона от атома натрия приводит к образованию положительно заряженного иона — катиона натрия Na+ (рис. 40).
Присоединение электрона к атому хлора приводит к образованию отрицательно заряженного иона — аниона хлора CI— (рис. 41).
Между образовавшимися ионами Na+ и Cl—, имеющими противоположный заряд, возникает электростатическое притяжение, в результате которого образуется соединение — хлорид натрия с ионным типом химической связи.
Химическая связь, которая осуществляется за счет электростатического взаимодействия противоположно заряженных ионов, называется ионной связью.
Таким образом, процесс образования ионной связи сводится к переходу электронов от атомов натрия к атомам хлора с образованием противоположно заряженных ионов, имеющих завершенные электронные конфигурации внешних слоев:
Экспериментально установлено, что в действительности электроны не отрываются полностью от атома металла, а лишь смещаются в сторону атома хлора. Это смещение тем значительней, чем больше разность электроотрицательностей атомов, между которыми образуется ионная связь. Однако даже в случае фторида цезия CsF, в котором разность электроотрицательностей превышает 3,0, заряд атома цезия не равен 1+ . Это означает, что электрон атома цезия не полностью переходит к атому фтора. В случае других соединений, для которых разность электроотрицательностей не так велика, смещение электрона еще меньше, и поэтому следует говорить об ионной химической связи с определенной долей ковалентной.
Соединения, в которых вклад ионной связи значителен, принято называть ионными. Большинство бинарных соединений, содержащих атомы металлов, являются ионными, т. е. в них химическая связь в значительной степени ионная. К числу таких соединений относятся галогениды, оксиды, сульфиды, нитриды и др.
Ионная связь возникает не только между простыми катионами и простыми анионами типа 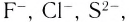
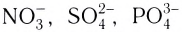
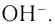
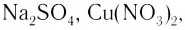
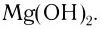
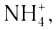
Ионные кристаллы
По своим свойствам ионная связь отличается от ковалентной. Так как силы электростатического взаимодействия направлены от иона во все стороны, то каждый ион может притягивать ионы противоположного знака в любом направлении. Поэтому ионное соединение представляет собой гигантскую ассоциацию ионов противоположных знаков, расположенных в определенном порядке, в форме ионного кристалла. Кристаллы ионных соединений состоят из катионов и анионов, которые определенным образом располагаются в пространстве благодаря равновесию сил притяжения и отталкивания. На рисунке 42 представлено строение кристалла хлорида натрия NaCl, состоящего из катионов натрия Na+ и анионов хлора Сl—. Каждый катион натрия окружен шестью анионами хлора, а каждый анион хлора — шестью катионами натрия.
Наименьшей структурной единицей кристалла (т. е. наименьшей частью), отражающей все особенности структуры его кристаллической решетки, является элементарная ячейка. Строение элементарной ячейки зависит от соотношения размеров катиона и аниона. На рисунке 43 приведено строение элементарных ячеек хлорида натрия NaCl и хлорида цезия CsCl. Существуют и другие типы элементарных ячеек.
Если частицы в веществе связаны ионной связью, то оно относится к веществам с немолекулярным строением. В твердом агрегатном состоянии такие вещества представляют собой ионные кристаллы. Так как ионная связь является прочной, то ионные кристаллы имеют обычно высокие температуры плавления и кипения, не имеют запаха. Сильное притяжение ионов друг к другу обусловливает хрупкость таких веществ при разрушении, а отсутствие свободных заряженных частиц объясняет тот факт, что при комнатной температуре они плохо проводят электрический ток.
Металлическая связь. Металлические кристаллы
Атомы большинства металлов достаточно легко отдают свои валентные электроны, в результате чего превращаются в положительно заряженные ионы. Это происходит не только при взаимодействии металлов с другими атомами, но и при образовании металлических кристаллов из одних и тех же атомов.
В кристалле металла непрерывно протекают два противоположных процесса — образование ионов металла из нейтральных атомов в результате отрыва от них валентных электронов:
и присоединение валентных электронов к ионам металла с образованием нейтральных атомов:
В узлах кристаллической решетки металлов попеременно находятся как нейтральные атомы, так и положительно заряженные катионы металла (рис. 44). Образующиеся при этом электроны свободно перемещаются внутри кристалла и компенсируют взаимное отталкивание между положительно заряженными катионами металла, а также удерживают атомы в составе кристалла. Они становятся общими для всех атомов и ионов металла, связывая их между собой.
► Химическая связь между атомами в металлическом кристалле посредством обобществления валентных электронов называется металлической связью.
Металлическая связь не имеет направленности в пространстве. Эта химическая связь является коллективной, как и ионная, в ней принимают участие все атомы кристалла металла.
Металлическая связь сходна с ковалентной связью тем, что при ее образовании так же, как и при образовании ковалентной связи, электроны обобществляются. Однако в случае металлической связи эти электроны связывают все атомы металлического кристалла, тогда как в ковалентном соединении связываются лишь находящиеся рядом атомы.
Взаимосвязь различных типов химической связи
Вы познакомились с тремя типами химической связи и соответствующими веществами, которые мы характеризовали как вещества с ковалентным (02, N2, Cl2), ионным (LiF, NaCl) и металлическим типом связи (металлы). В реальности в большинстве неорганических веществ взаимодействие между различными атомами носит более сложный характер, являясь как бы комбинацией различных типов связи. Это особенно характерно проявляется в ряду простых и сложных бинарных веществ элементов III периода, который Д. И. Менделеев назвал «типическим».
В углах представленного треугольника химических связей (рис. 45) расположены вещества, являющиеся наиболее характерными представителями каждого типа связи: NaCl — соединений ионного типа, Cl2 — ковалентного, а Na — металлического. В ряду от NaCl до Cl2 находятся бинарные вещества общей формулы ЭСl, где Э — элемент третьего периода:
Как вам уже известно, в периодах от щелочного металла до галогена электроотрицательность последовательно растет и, соответственно, уменьшается величина 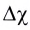
где 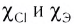
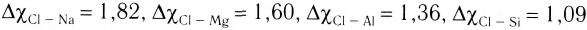
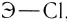
Подобные закономерности наблюдаются и в двух других рядах веществ. В ряду от Na до NaCl располагаются соединения условной формулы NaЭ, где Э — элемент третьего периода. Характер химической связи в этих веществах последовательно изменяется от металлического до ионного.
В ряду от Na до Cl2 располагаются простые вещества третьего периода. Свойства этих веществ последовательно изменяются от металлических к неметаллическим, что соответствует изменению характера химической связи от металлического к ковалентному.
Таким образом, мы можем заключить, что однозначное определение типа химической связи в большинстве неорганических соединений невозможно. В реальности химическая связь между разнородными атомами носит смешанный характер с той или иной долей ковалентной, ионной или металлической составляющей.
- Ионная связь осуществляется за счет электростатического притяжения между противоположно заряженными ионами.
- Химическая связь между атомами в металлическом кристалле посредством обобществления электронов называется металлической связью.
Межмолекулярное взаимодействие
Молекулы, несмотря на свою электронейтральность, способны взаимодействовать между собой. Такое взаимодействие называется межмолекулярным. Силы, за счет которых возникает это взаимодействие, часто называют ван-дер-ваальсовыми в честь голландского ученого И. Д. Ван-дер-Ваальса. Эти силы обусловливают притяжение молекул данного вещества (или разных веществ) друг к другу в жидком и твердом агрегатном состоянии.
Природа межмолекулярного взаимодействия
Межмолекулярное взаимодействие, как и химическая связь между атомами, имеет электростатическую природу. Несимметричность распределения электронов и ядер атомов в молекуле приводит к появлению у нее электрических полюсов — положительного с той стороны, где электронная плотность понижена, и отрицательного, где она повышена. Образовавшиеся полярные молекулы притягиваются друг к другу разноименными полюсами (рис. 46, а).
Взаимодействие может осуществляться также между полярной и неполярной молекулами. При этом в неполярной молекуле под действием электрического поля полярной молекулы возникает (индуцируется) диполь. Постоянный диполь и индуцированный диполь притягиваются друг к другу (рис. 46, б).
В неполярных молекулах вследствие непрерывного движения частиц с различными электрическими зарядами (ядер и электронов) также непрерывно возникают, перемещаются и исчезают электрические полюсы. Поэтому в разные моменты времени возникают мгновенные диполи, между которыми также действуют силы притяжения (рис. 46, в).
В этом и состоит объяснение существования притяжения между любыми молекулами, как полярными, так и неполярными.
Прочность межмолекулярного взаимодействия и агрегатное состояние вещества
Межмолекулярное взаимодействие обусловливает переход вещества из газообразного в жидкое, а затем и в твердое состояние. Но по сравнению с ковалентной связью межмолекулярные взаимодействия слабые, связи между молекулами относительно непрочные и легко разрываются. Именно поэтому молекулярные вещества плавятся и кипят при относительно низких температурах. Межмолекулярное взаимодействие определяет также механические свойства подобных веществ, их теплопроводность, электрическую проводимость и др.
Энергия межмолекулярного взаимодействия зависит в основном от двух характеристик молекулы — ее полярности и размера. Чем сильнее межмолекулярное взаимодействие в веществе, тем выше у него будут температуры плавления и кипения. Например, кислород из-за более прочного межмолекулярного взаимодействия кипит при более высокой температуре, чем азот, что и используется при получении этих газов из воздуха. Углеводороды с большой молекулярной массой кипят при более высокой температуре, чем низкомолекулярные углеводороды. Это свойство углеводородов лежит в основе процесса перегонки нефти.
Молекулярные кристаллы
В узлах молекулярной кристаллической решетки расположены молекулы, связанные между собой слабыми межмолекулярными связями (рис. 47). Молекулярные кристаллические решетки образуют водород, азот, кислород, сера, йод, вода, углекислый газ, многие органические вещества. Кристаллы благородных газов также молекулярные, они построены из одноатомных молекул.
Для веществ, образующих молекулярные кристаллы, характерны низкие температуры плавления и кипения, значительная сжимаемость, небольшая твердость. Нагревание некоторых молекулярных кристаллов, например иода, углекислого газа, приводит к переходу вещества из твердого состояния сразу в газообразное, минуя жидкую фазу. Этот процесс называется возгонкой или сублимацией.
В то же время многие органические вещества с большими молекулами, содержащими десятки тысяч и более атомов, вообще не плавятся, так как прочность связей между молекулами в сумме оказывается выше прочности связей внутри молекулы. Попробуйте расплавить, например, крахмал, целлюлозу, вату. Вы убедитесь в том, что вещество начнет разрушаться раньше, чем плавиться.
Однако надо иметь в виду, что реакционная способность молекулярных веществ зависит от прочности не межмолекулярных, а внутримолекулярных связей. Ведь при химическом взаимодействии разрываются именно внутримолекулярные связи. Например, парафин — механически непрочное вещество, связи между молекулами в нем слабые. Но это вещество химически достаточно устойчиво.
Водородная связь
Одной из разновидностей межмолекулярного взаимодействия является водородная связь. Она осуществляется между положительно поляризованным атомом водорода одной молекулы и отрицательно поляризованным атомом другой молекулы:
где X — атом одного из наиболее электроотрицательных элементов — F, О, N, реже CI и S.
Возникновение водородной связи (на схеме она показывается тремя точками) обусловлено прежде всего тем, что у атома водорода имеется только один электрон, который при образовании полярной ковалентной связи с атомом сильно электроотрицательного элемента смещается в сторону атома этого элемента. На атоме водорода возникает высокий эффективный положительный заряд, что в сочетании с отсутствием внутренних электронных слоев позволяет другому атому сближаться до расстояний, близких к длинам атомных связей.
В первом приближении образование водородной связи можно объяснить электростатическим взаимодействием между молекулами. Определенный вклад в образование водородной связи вносит донорно-акцепторное взаимодействие «свободной» 1s-орбитали атома водорода и орбитали с неподеленной парой электронов электроотрицательного атома. Поэтому водородная связь обладает свойством направленности, во многом определяя структуру вещества в конденсированном состоянии.
Благодаря водородным связям молекулы объединяются в ассоциаты, например молекулы уксусной кислоты образуют димеры (рис. 48). Водородные связи определяют кристаллическую структуру льда, где каждый атом кислорода в молекулах Н20 связан с четырьмя атомами водорода — двумя ковалентными и двумя водородными связями (рис. 49).
Водородная связь в несколько раз сильнее, чем обычное межмолекулярное взаимодействие, но слабее ковалентной связи. С повышением температуры прочность водородной связи уменьшается. Поэтому водородная связь более характерна для веществ в твердом и жидком состояниях.
Наличие водородной связи существенно влияет на физические свойства веществ. Так, аномально высокие температуры кипения H2O, HF, HN3 по сравнению с аналогичными веществами, образованными элементами этих же групп других периодов (рис.50), объясняются образованием ассоциатов за счет водородных связей.
Во дородная связь О…Н наиболее распространена в природе. Именно ее наличием обусловлены аномальные свойства воды, в том числе высокие температуры кипения и плавления, необычайно высокие теплоемкость и диэлектрическая проницаемость. Благодаря своей ажурной структуре (см.рис.49) лед имеет меньшую плотность, чем жидкая вода. Поэтому зимой лед находится на поверхности воды, и глубокие водоемы не промерзают до дна.
Светло-голубой цвет чистой воды и толстого слоя льда обусловлен водородными связями. Когда одна молекула воды колеблется, то она заставляет колебаться и другие, связанные с ней молекулы. В результате этого молекулы H2O частично поглощают красный цвет, а вода приобретает голубоватый оттенок.
Водородная связь может возникать и между атомами одной молекулы. Чаще всего внутримолекулярная водородная связь возникает в молекулах органических веществ, содержащих в своем составе такие группы атомов как —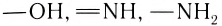
Особенно велика роль водородных связей в биохимических процессах с участием высокомолекулярных соединений (белки, ДНК и др.), пространственная структура которых определяется наличием водородных связей.
Межмолекулярное взаимодействие возникает между любыми молекулами, как полярными, так и неполярными, и имеет электростатическую природу.
Межмолекулярное взаимодействие обусловливает переход вещества из газообразного в жидкое, а затем и в твердое состояние.
Водородная связь осуществляется между положительно поляризованным атомом водорода одной молекулы и отрицательно поляризованным атомом фтора, кислорода, азота (реже хлора и серы), принадлежащим другой молекуле.
- Валентность и степень окисления
- Ионная связь
- Химические реакции
- Теория электролитической диссоциации
- Физические и химические явления
- Растворы в химии
- Периодический закон Д. И. Менделеева
- Химические связи
Ковалентная связь образуется при взаимодействии неметаллов. Атомы неметаллов имеют высокую электроотрицательность и стремятся заполнить внешний электронный слой за счёт чужих электронов. Два таких атома могут перейти в устойчивое состояние, если объединят свои электроны.
Ковалентная связь — это связь между атомами неметаллов, образованная за счёт общих электронных пар.
Рассмотрим возникновение ковалентной связи в простых веществах.
1. Образование молекулы водорода.
Каждый атом водорода имеет один электрон. Для перехода в устойчивое состояние ему необходим ещё один электрон.
При сближении двух атомов электронные облака перекрываются. Образуется общая электронная пара, которая связывает атомы водорода в молекулу.
В пространстве между двумя ядрами общие электроны бывают чаще, чем в других местах. Там формируется область с повышенной электронной плотностью и отрицательным зарядом. Положительно заряженные ядра притягиваются к ней, и образуется молекула.
При этом каждый атом получает завершённый двухэлектронный внешний уровень и переходит в устойчивое состояние.
Рис. (1). Образование молекулы водорода
Ковалентная связь за счёт образования одной общей электронной пары называется одинарной.
Общие электронные пары (ковалентные связи) образуются за счёт неспаренных электронов, расположенных на внешних энергетических уровнях взаимодействующих атомов.
У водорода — один неспаренный электрон. Для других элементов их число равно 8 – № группы.
Неметаллы VIIА группы (галогены) имеют на внешнем слое один неспаренный электрон.
У неметаллов VIА группы (кислород, сера) таких электронов два.
У неметаллов VА группы (азот, фосфор) — три неспаренных электрона.
2. Образование молекулы хлора.
Атом хлора на внешнем уровне имеет семь электронов. Шесть из них образуют пары, а седьмой неспаренный.
При соединении атомов образуется одна общая электронная пара, то есть возникает одна ковалентная связь. Каждый атом получает завершённый восьмиэлектронный внешний слой. Связь в молекуле хлора тоже одинарная. Такие же одинарные связи существуют в молекулах фтора, брома и иода.
Рис. (2). Образование молекулы хлора
Если атомы имеют несколько неспаренных электронов, то образуются две или три общие пары.
3. Образование молекулы кислорода.
У атома кислорода на внешнем уровне — два неспаренных электрона.
При взаимодействии двух атомов кислорода возникают две общие электронные пары. Каждый атом заполняет свой внешний уровень до восьми электронов. Связь в молекуле кислорода двойная.

Рис. (3). Образование молекулы кислорода
4. Образование молекулы азота.
Атом азота имеет три неспаренных электрона на внешнем уровне.
В молекуле образуются три общие электронные пары. Связь в молекуле азота тройная.
Рис. (4). Образование молекулы азота
Образование ковалентных связей показывают структурные (графические) формулы, в которых общая электронная пара обозначается чертой. Одна черта между атомами обозначает одинарную связь, две черты — двойную, три черты — тройную:
Источники:
Рис. 1. Образование молекулы водорода © ЯКласс
Рис. 2. Образование молекулы хлора © ЯКласс
Рис. 3. Образование молекулы кислорода © ЯКласс
Рис. 4. Образование молекулы азота © ЯКласс
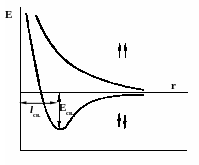
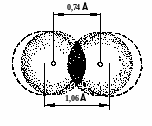
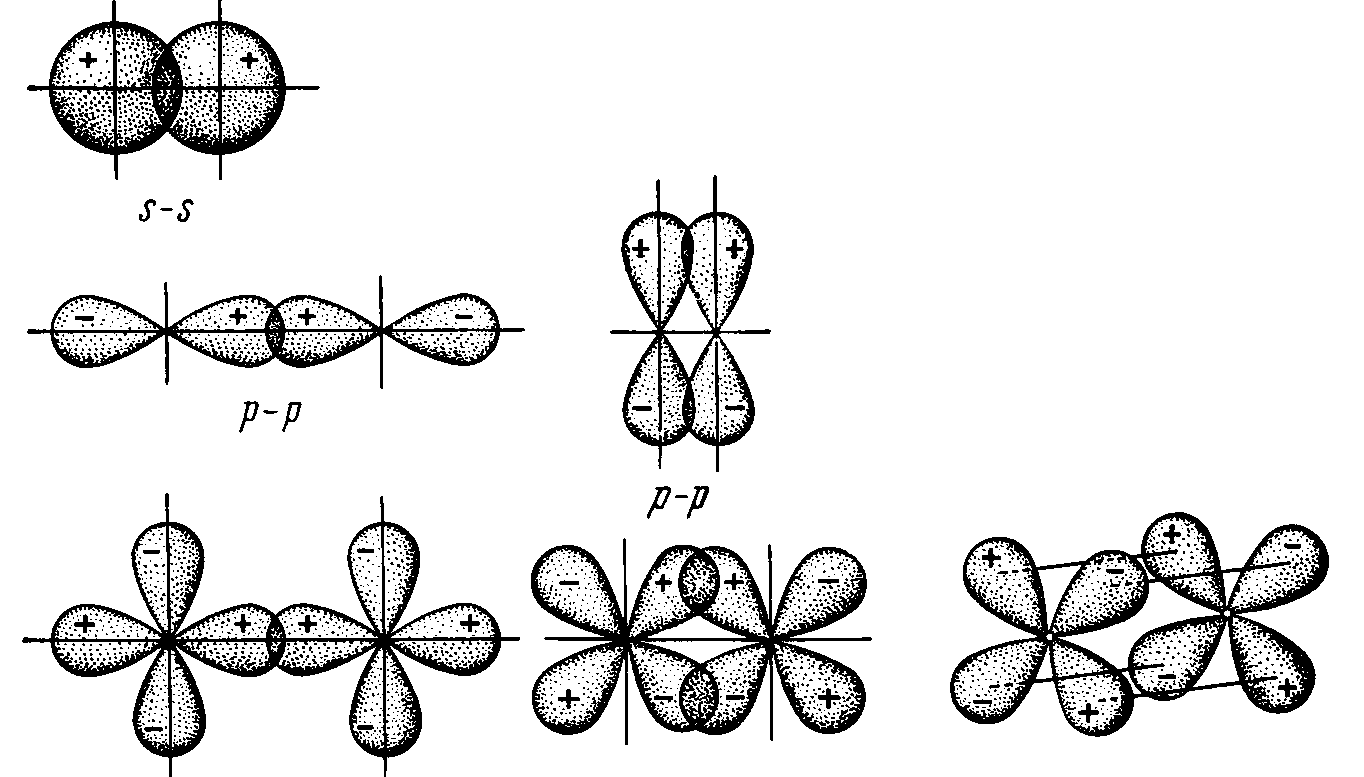
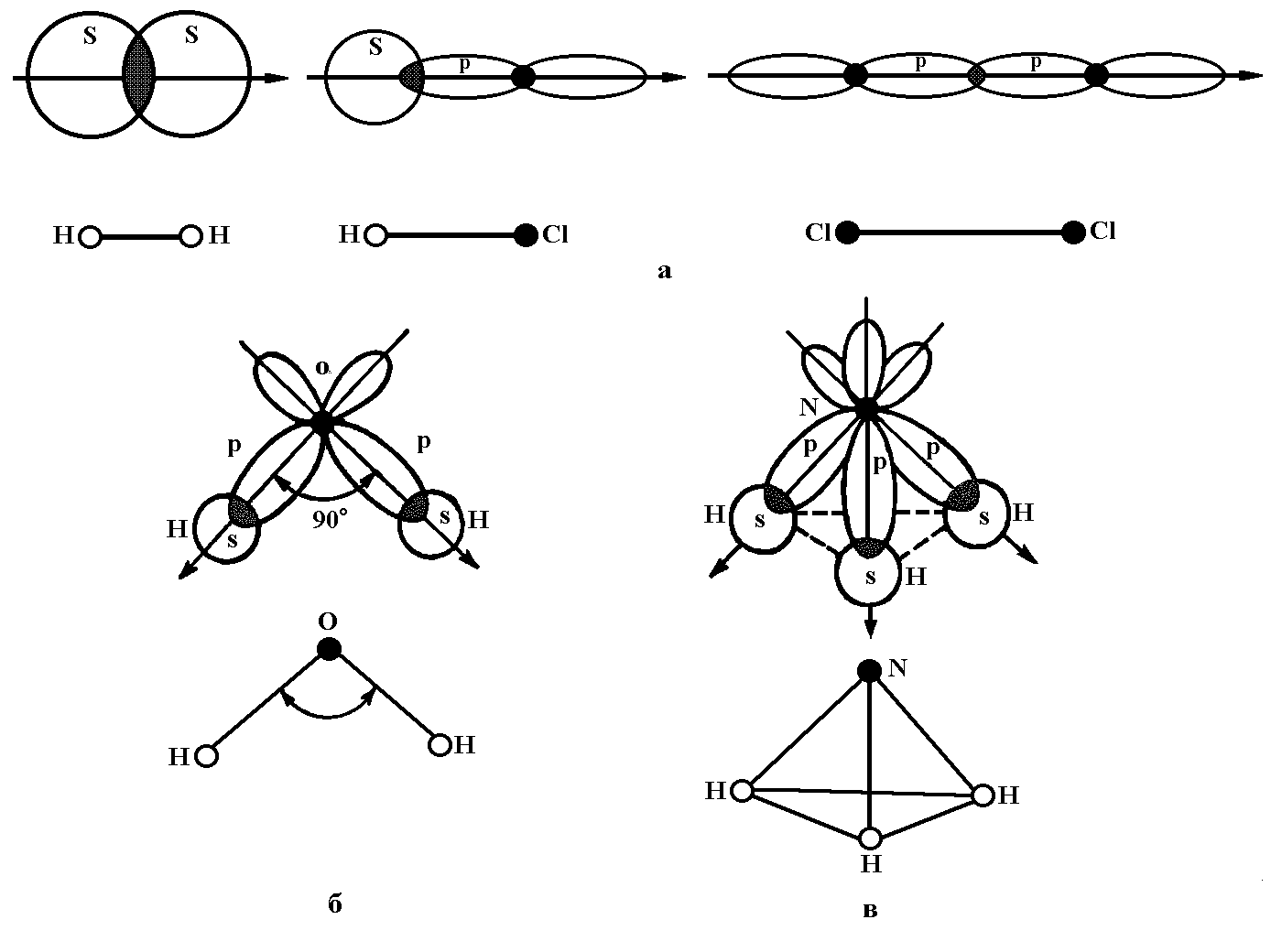
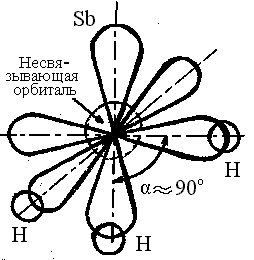
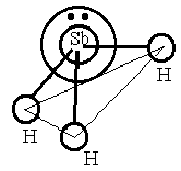
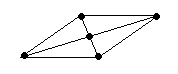
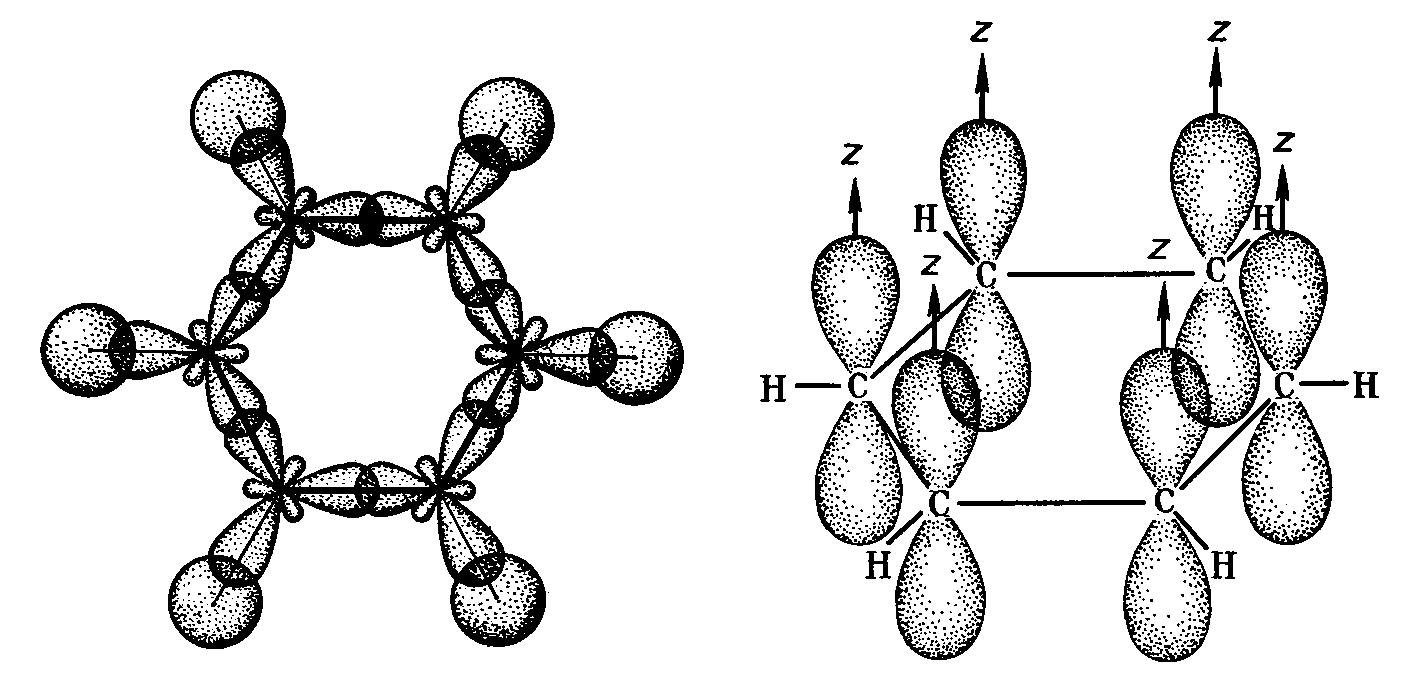
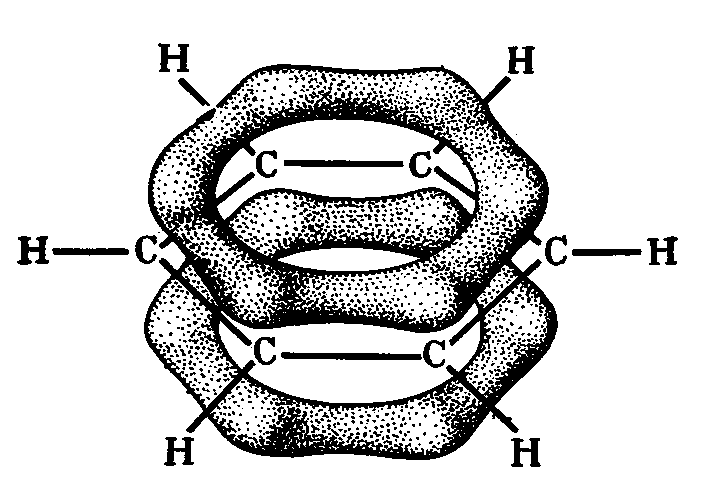
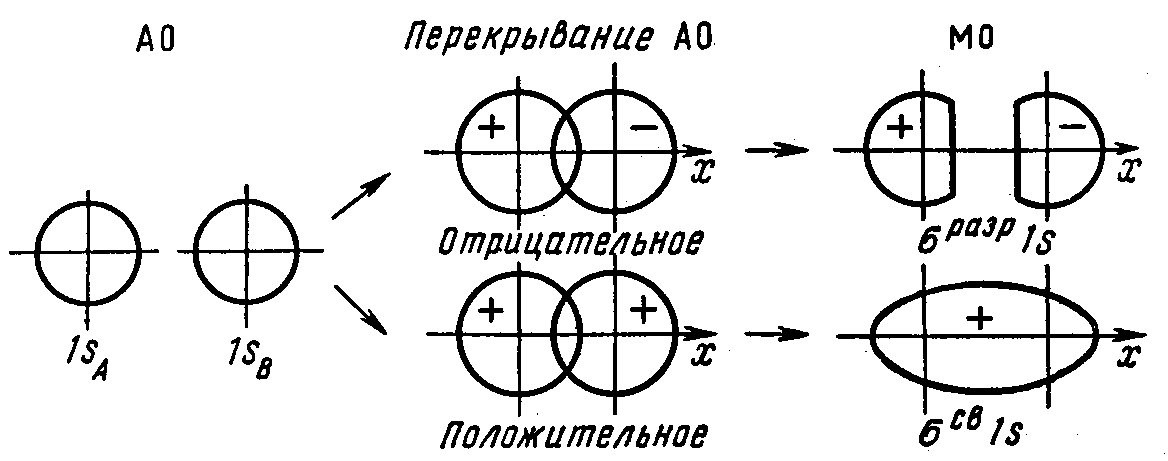
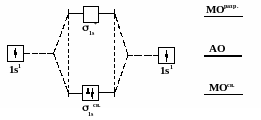
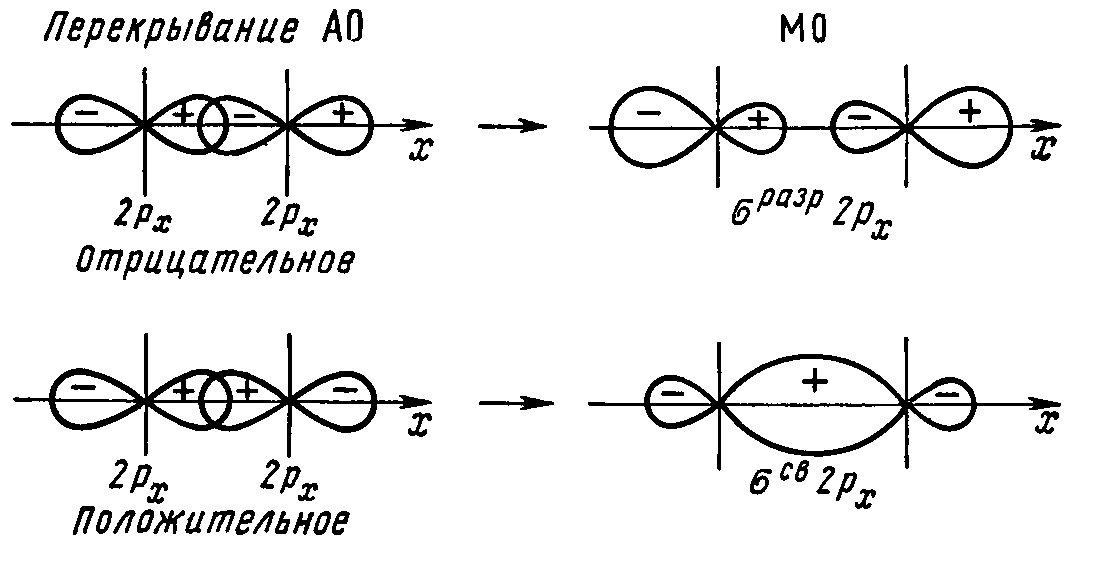
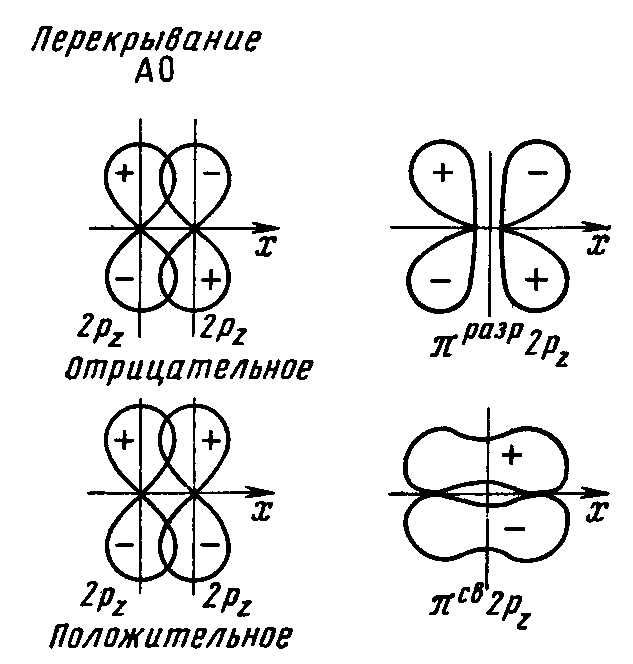
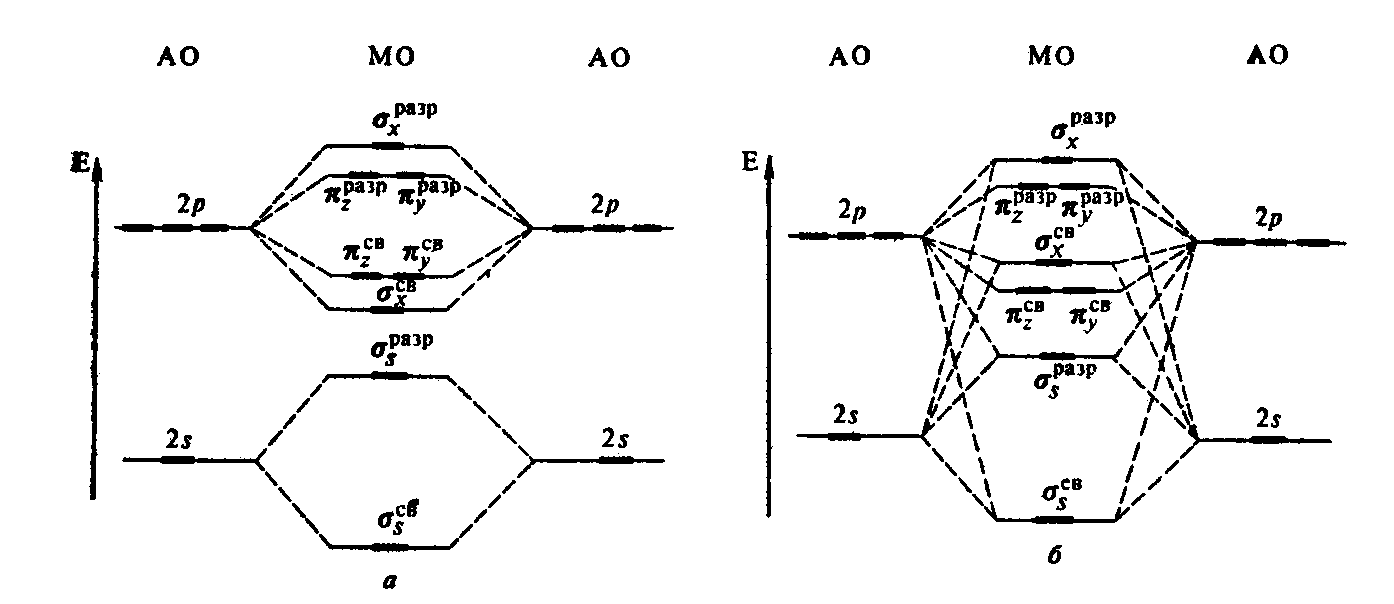
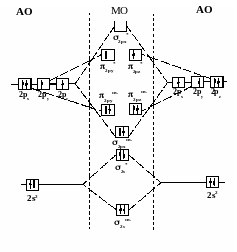
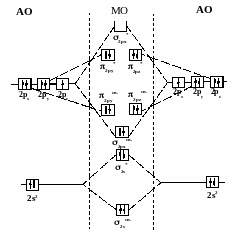

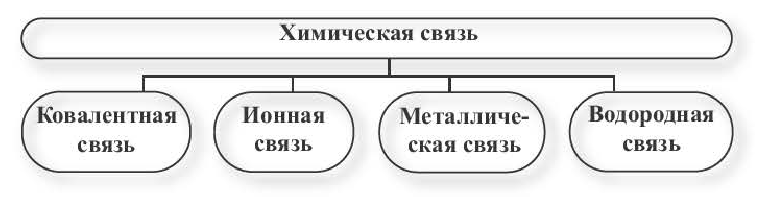

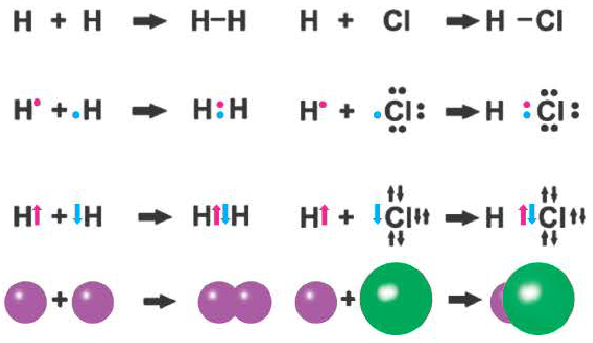
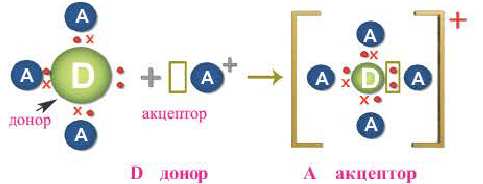
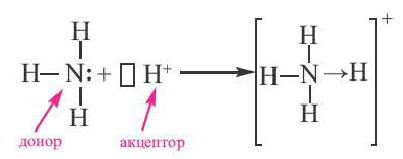
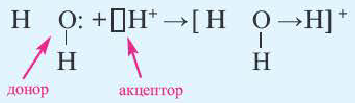



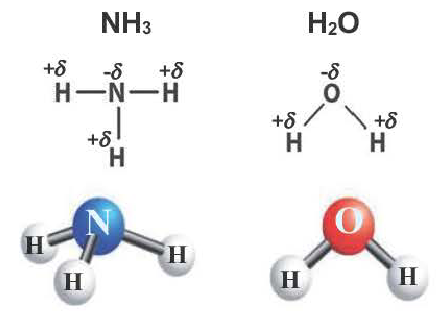
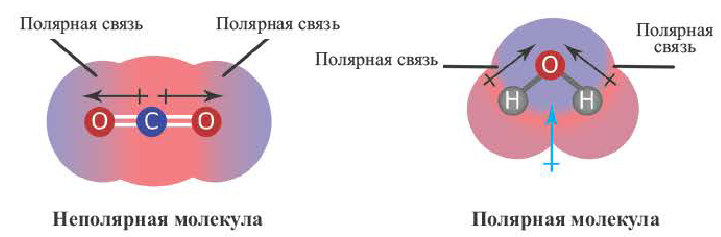
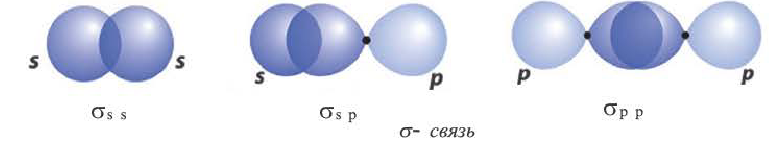
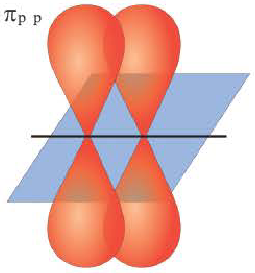
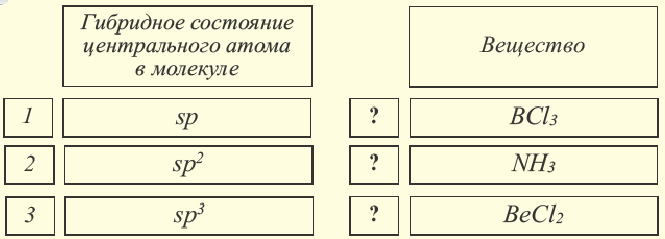
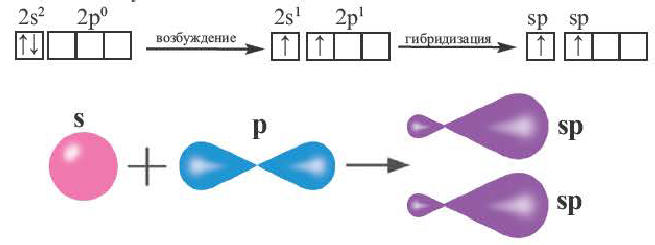

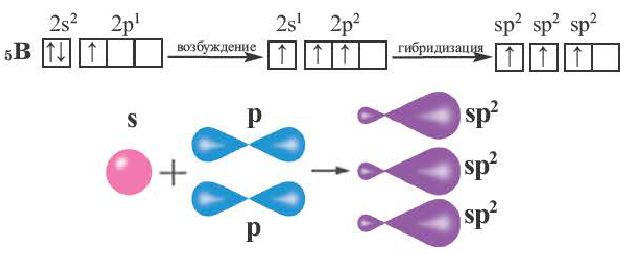
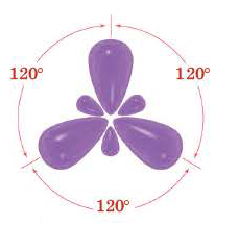
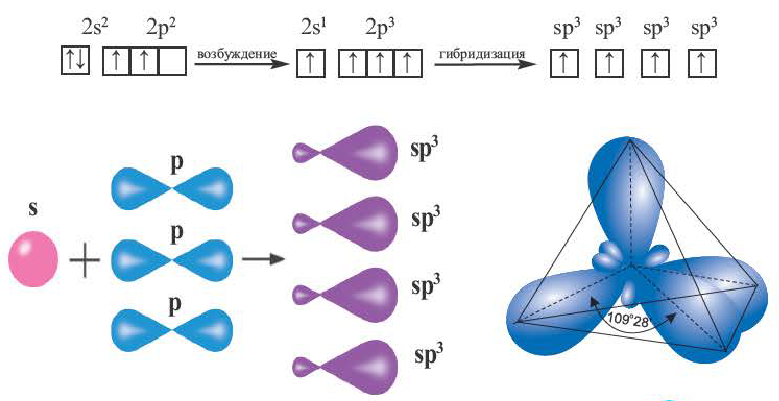
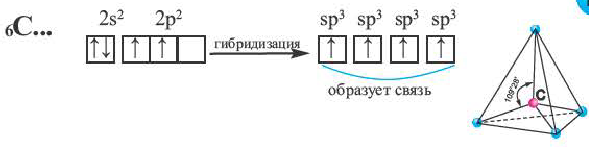
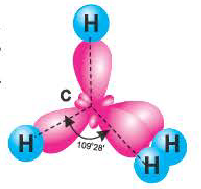
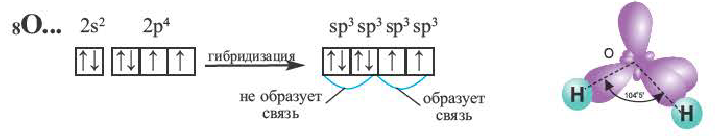
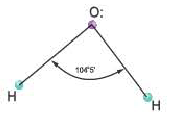
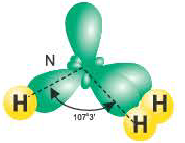
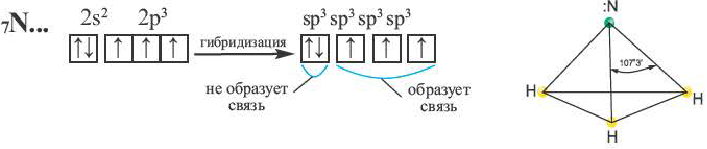
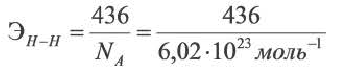
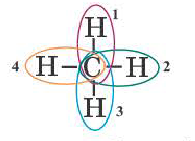
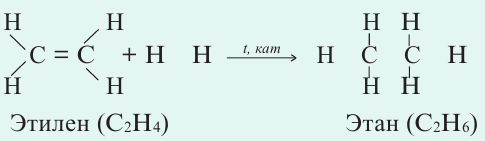



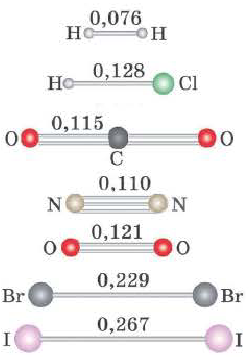
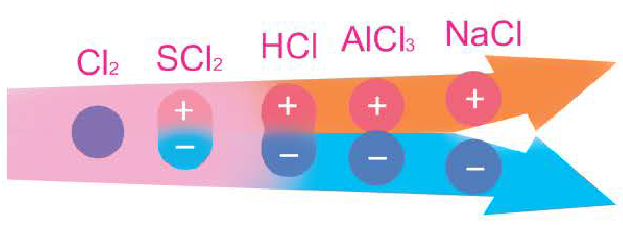
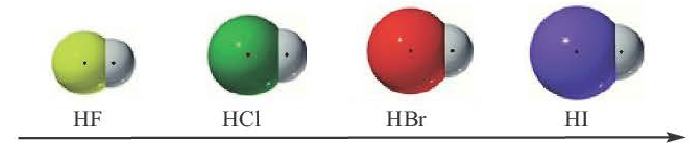

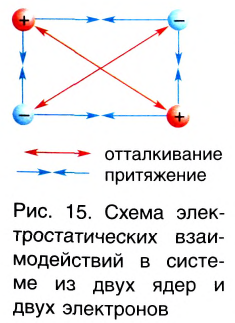
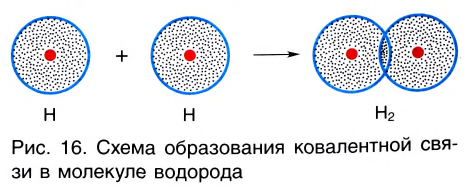
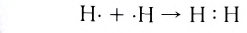

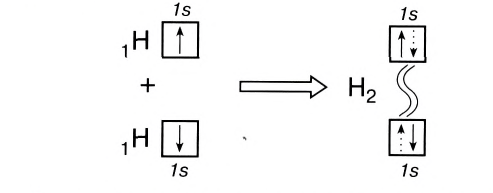
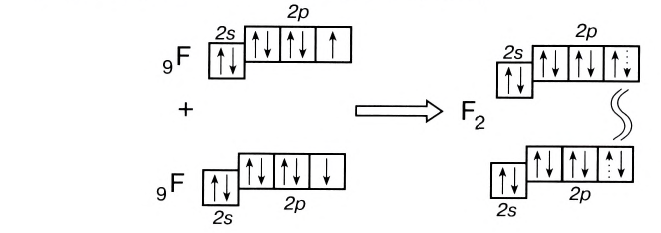
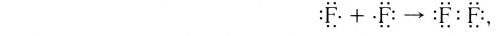


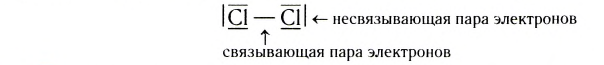
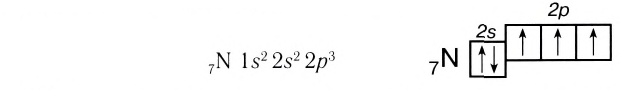
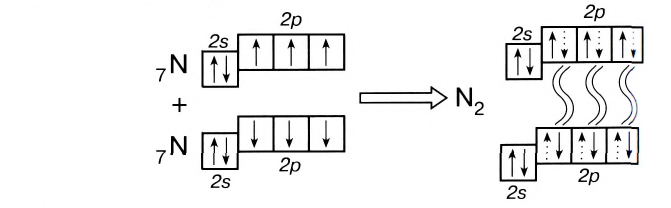


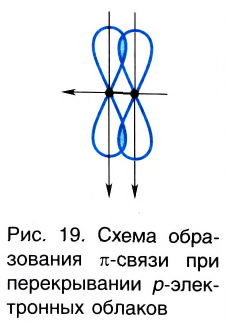

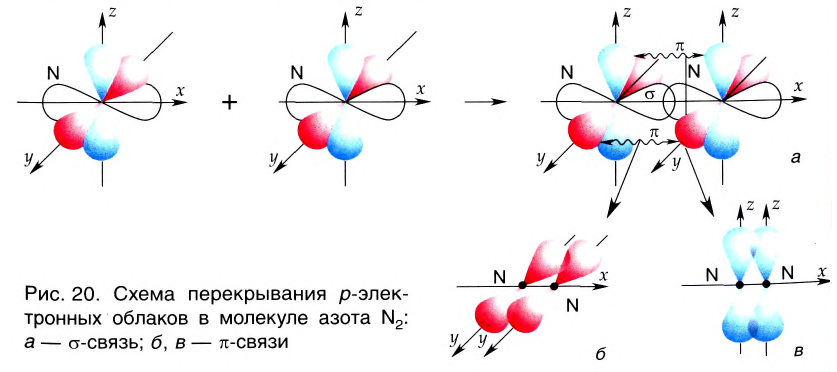


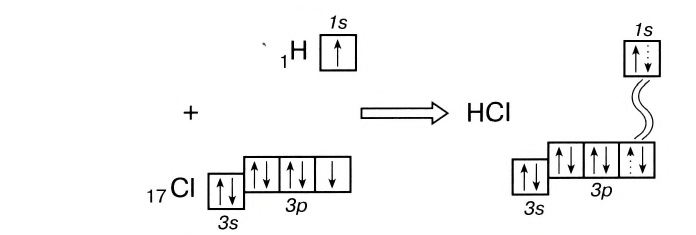

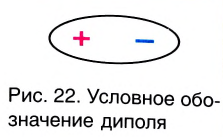
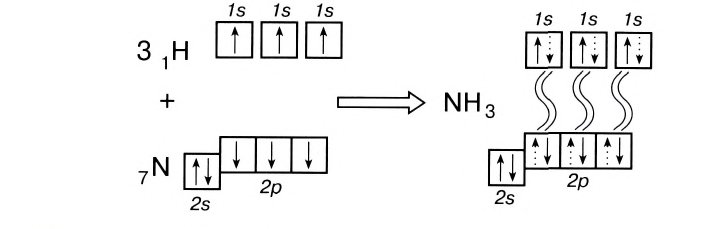


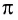 -связью.
-связью.


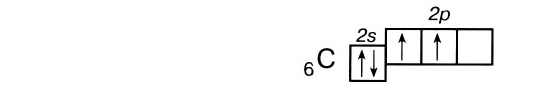
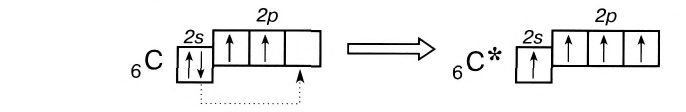
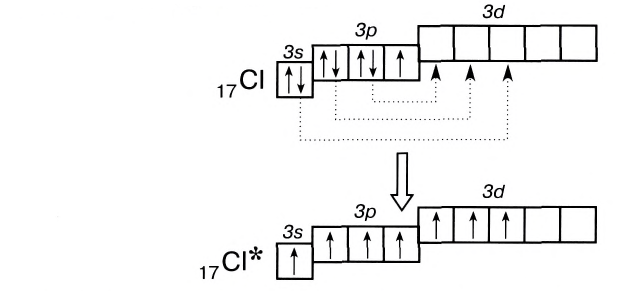



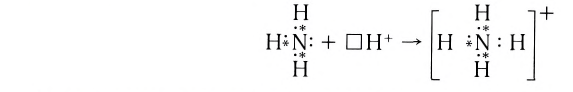

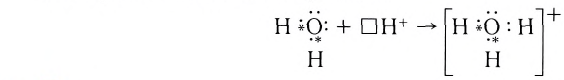
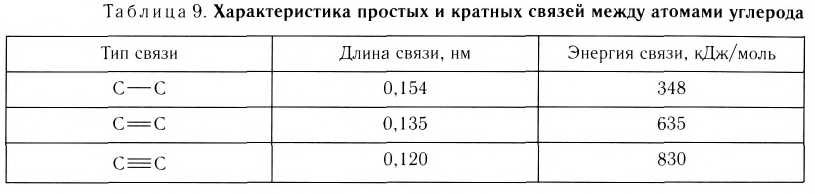
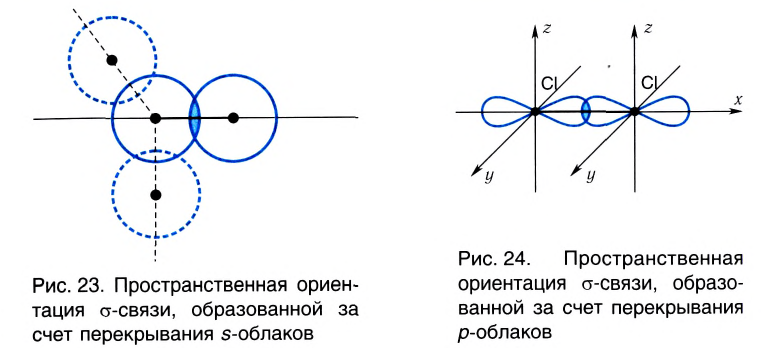

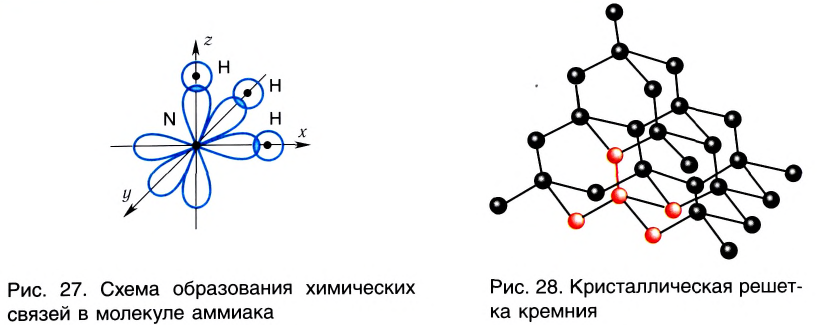
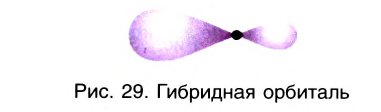
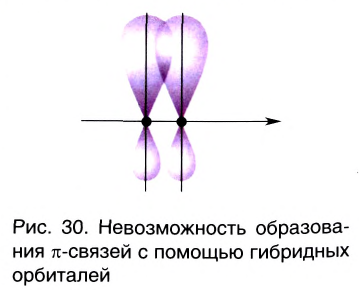
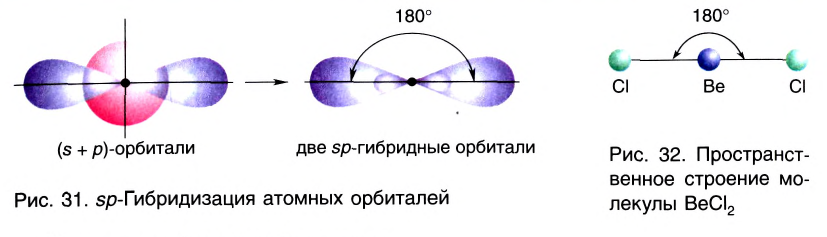
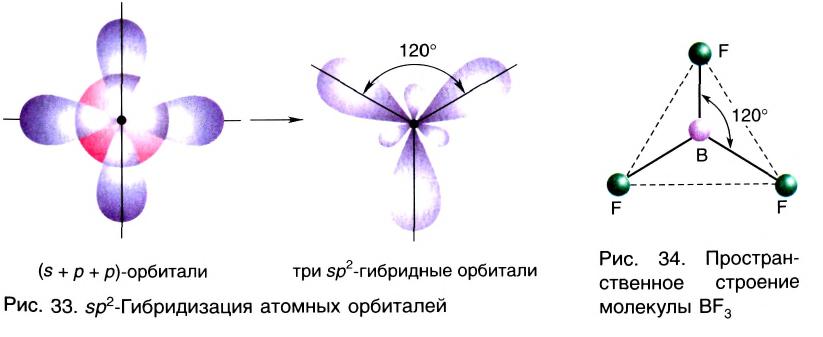
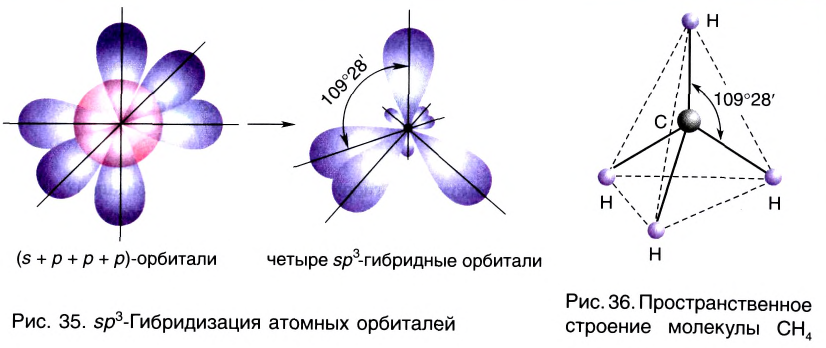

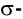 связи.
связи.