Смесь оксидов кальция (CaO) и магния (MgO) массой 2,08 грамм полностью растворили в азотной кислоте (HNO3) и получили 6,4 грамм смеси нитратов. Найдите массовую долю оксида магния (MgO) в смеси оксидов.
Решение задачи
I способ решения (II cпособ)
Запишем уравнения реакций взаимодействия азотной кислоты (HNO3) с оксидами кальция (CaO) и магния (MgO) в смеси оксидов:
![]()
![]()
Учитывая, что молярные массы оксида кальция (CaO), оксида магния (MgO), нитрата кальция (Ca(NO3)2) и нитрата магния (Mg(NO3)2) соответственно равны 56 г/моль, 40 г/моль, 164 г/моль и 148 г/моль (смотри таблицу Менделеева), обозначим содержание оксида кальция (CaO) в смеси оксидов кальция (CaO) и магния (MgO) через х грамм. Тогда содержание оксида магния (MgO) в смеси оксидов кальция (CaO) и магния (MgO) составит (2,08 – х) грамм.
Обозначим массу нитрата кальция (Ca(NO3)2), образующегося в уравнении (1) a грамм; массу нитрата магния (Mg(NO3)2), образующегося в уравнении (2) b грамм:
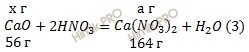
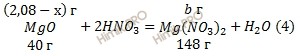
Из уравнений (3,4) следует, что масса образующегося нитрата кальция (Ca(NO3)2) ”а” составит:
а = 164 ⋅ х / 56 (г),
масса нитрата магния (Mg(NO3)2) ”b” составит:
b = 148 ⋅ (2,08 – х) / 40 (г).
По условию задачи масса смеси нитратов 6,4 г, то есть:
а + b = 6,4 (г).
Отсюда:
164 ⋅ х / 56 + 148 ⋅ (2,08 – х) / 40 = 6,4
2,93 х + 7,7 – 3,7 х = 6,4
0,77 х = 1,3
х = 1,69 (г).
Следовательно, масса оксида кальция (CaO) в смесь оксидов 2,08 грамма.
Найдем массу оксида магния (MgO) в смеси оксидов:
m (MgO) = 2,08 – 1,69 = 0,39 = 0,4 (г).
Используя формулу нахождения массовой доли вещества:
![]()
Рассчитаем массовую долю оксида магния (MgO) в смеси оксидов:
w (MgO) = 0,4 ⋅ 100% / 2,08 = 19,23 (%).
Ответ:
массовая доля оксида магния 19,23%.
Похожие задачи
Выбрать другой вопрос
Смотреть ответ
Перейти к выбору ответа
Вопрос от пользователя
Вычислите массу смеси оксидов, которая образуется при сгорании 200 г смеси порошка магния и алюминия. Массовая доля алюминия в смеси составляет 54%.
Ответ от эксперта
решение задания по химии

 Скачать ответ
Скачать ответ Распечатать решение
Распечатать решение
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,658 -
гуманитарные
33,653 -
юридические
17,917 -
школьный раздел
611,962 -
разное
16,905
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Easydrop | Изидроп промокоды 40%
Сочные промокоды на 40% для вас
Лучшие промокоды +40%:
3AAE3DF ~ 7EF8E52 ~ 5FC1375 ~ 9987CC6
21A6674 ~ CD36C82 ~ 2A25F4C ~ E6664DA
640BB38 ~ B2FADBD ~ A97F253
6AF8785 ~ 1C30382 ~ F5038BD
CD007E2 ~ 5D1870A ~ D0CECA9
28D6398 ~ 89A307C ~ ED8E194
0800578 ~ D89175C ~ A1AAC67
A449CDD ~ 142247A ~ 86792A1
E069B60 ~ AC75380 ~ 7EF2000
E4E0352 ~ 42BC3B8 ~ A413F5B
39A686D ~ 31222DA ~ 29785A0
8D7F130 ~ 37E488A ~ 0AB7C30
6FBFAC0 ~ 1A2FC52 ~ 05D22D1
47FEB24 ~ 6EA010F ~ B1367C7
299A110 ~ 930E584 ~ 51B1266
2337ADC ~ 105688B ~ D5B9275
Лучшие (много активаций) промокоды 35%:
EE33BED ~ 3DAE0BE ~ BA37BD7 ~ 3DAE0BE
3575154 ~ B3484DB ~ 91C3493 ~ EE33BED
439F997 ~ A9F9022 ~ 57944BA ~ BA37BD7
FA0155D ~ 65F42E9 ~ 720A2BB ~ 3575154
2727E91 ~ ABE7E4C ~ 3631312
Желаю вынести топового дропа
Методика решения задачи на определение начальной массы смеси двух веществ при полной нейтрализации полученной смеси
Задача 1.
В воде растворили смесь оксида натрия и оксида калия, где массовая доля натрия 46%. Определите массу начальной смеси, если для полной нейтрализации полученной смеси израсходовано 175 мл 2 молярного раствора серной кислоты.
Решение:
М(Na2O ) = (2 • 23) + 16 = 62 г/моль;
М(К2O ) = (2 •39) + 16=94 г/моль.
Из формулы оксида натрия Na2O следует, что на 46 весовых частей Na приходится 16 весовых частей О, т.е. на 46% Na в смеси оксидов будет приходится 16% О. Тогда смесь оксидов натрия и калия будет содержать 62% (46 + 16 = 62) Na2O. Соответственно, содержание К2О в смеси будет 38% (100 – 61 = 100).
Уравнение реакции имеет вид:
Me2O + H2SO4 = Me2SO4 + H2O
Из уравнения реакции следует, что на нейтрализацию 1 моля оксидов натрия или калия расходуется 1 моль серной кислоты.
Рассчитаем количество серной кислоты по условию задачи, получим:
(175мл • 2моль/1000мл) = 0,35 мол. Значит, n(смеси) = 0,35 мол.
Смесь содержит 0,35 моль оксидов натрия и калия .
Обозначим массу смеси оксидов через х г.
Тогда
n(Na2O) = (62% • х г)/(100% • 62 г/моль) = 0,01х моль;
n(К2O) = (38% • х г)/(100% • 94 г/моль) = 0,0004х моль.
Теперь рассчитаем массу смеси оксидов натрия и калия, используя алгебраическое уравнение, получим:
0,01х + 0,004х = 0,35;
0,014х = 0,35;
х = 0,35/0,014 = 25 г; m((смеси) = 25 г.
Отсюда
m(Na2O) = [m((смеси) • w%( Na2O)]/100% = [(25г • 62%)]/100% = 15,5 г;
m(К2O) = [m((смеси) • w%( К2O)]/100% = [(25 г • 38%)]/100% = 9,5 г.
Ответ: m(смеси) = 2 5г.
