Как найти омега в Химии?
Ученик
(116),
закрыт
7 лет назад
Вячек
Высший разум
(391245)
8 лет назад
Буквой “w” (греческая “омега”) в химии обычно обозначают массовую долю – или вещества в растворе, или элемента в сложном веществе. Для обоих случаев существую стандартные формулы:
1) w(в-ва) = m(в-ва) /m(р-ра)
2) w(эл-та) = n*Ar(эл-та) /M(в-ва), где n – количество атомов элемента в веществе, Аr – относительная атомная масса элемента (берётся в таблице Менделеева), Mr – относительная молекулярная масса сложного вещества
Расчетные задачи типа «Определение выхода продукта реакции в процентах от теоретического»
Признак
В условии задачи встречается слово «выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём, практическая масса или объём» могут быть использованы только для веществ-продуктов.
Доля выхода продукта обозначается буквой
(эта), измеряется в процентах или долях.
Также для расчётов может использоваться количественный выход:
I. Первый тип задач
Известны масса (объём) исходного вещества и масса (объём) продукта реакции. Необходимо определить выход продукта реакции в %.
Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5, 5 г. Определите выход продукта реакции (%).
| 1. Записываем краткое условие задачи |
Дано: m (Mg) = 1,2 г m практическая(MgSO4) = 5,5 г _____________________ Найти: |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(Mg) = 24 г/моль M(MgSO4) = 24 + 32 + 4 · 16 = 120 г/моль |
|
4. Находим количество вещества реагента по формулам |
ν(Mg) = 1,2 г / 24(г/моль) = 0,05 моль |
| 5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
m = ν · M mтеор (MgSO4) = M(MgSO4) · νтеор (MgSO4) = = 120 г/моль · 0,05 моль = 6 г |
|
6. Находим массовую (объёмную) долю выхода продукта по формуле |
Ответ: Выход сульфата магния составляет 91,7% по сравнению с теоретическим |
II. Второй тип задач
Известны масса (объём) исходного вещества (реагента) и выход (в %) продукта реакции. Необходимо найти практическую массу (объём) продукта реакции.
Задача 2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид кальция массой 16,8 г, если выход составляет 80%.
|
1. Записываем краткое условие задачи |
Дано: m(CaO) = 16,8 г
___________________ Найти: m практ (CaC2) = ? |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
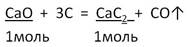 |
|
3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(CaO) = 40 + 16 = 56 г/моль M(CaC2) = 40 + 2 · 12 = 64г/моль |
|
4. Находим количество вещества реагента по формулам |
ν(CaO)=16,8 (г) / 56 (г/моль) = 0,3 моль |
|
5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
|
|
6. Находим массовую (объёмную) долю выхода продукта по формуле |
m практич (CaC2) = 0,8 · 19,2 г = 15,36 г Ответ: m практич (CaC2) = 15,36 г |
III. Третий тип задач
Известны масса (объём) практически полученного вещества и выход этого продукта реакции. Необходимо вычислить массу (объём) исходного вещества.
Задача 3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу карбоната натрия нужно взять для получения оксида углерода (IV) объёмом 28,56 л (н. у.). Практический выход продукта 85%.
| 1. Записываем краткое условие задачи |
Дано: н. у. Vm = 22,4 л/моль Vпрактич(CO2) = 28,56 л = 85% или 0,85 ____________________ Найти: m(Na2CO3) =? |
| 2. Находим по ПСХЭ молярные массы веществ, если это необходимо | M (Na2CO3) =2·23 + 12 + 3·16 = 106 г/моль |
|
3. Вычисляем теоретически полученный объём (массу) и количество вещества продукта реакции, используя формулы: |
Vтеоретич(CO2) = = 28,56 л / 0,85 = 33,6 л ν(CO2) = 33,6 (л) / 22,4 (л/моль) = 1,5 моль |
|
4. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 5. Находим количество вещества реагента по УХР |
По УХР:
ν(Na2CO3) = ν(CO2) = 1,5 моль |
|
6. Определяем массу (объём) реагента по формуле: m = ν · M V = ν · Vm |
m = ν · M m(Na2CO3) = 106 г/моль · 1,5 моль = 159 г |
IV. Решите задачи
Задача №1. При взаимодействии натрия количеством вещества 0, 5 моль с водой получили водород объёмом 4,2 л (н. у.). Вычислите практический выход газа (%).
Задача №2. Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно получить при восстановлении его оксида массой 228 г, если практический выход хрома составляет 95 %.
Задача №3. Определите, какая масса меди вступит в реакцию с концентрированной серной кислотой для получения оксида серы (IV) объёмом 3 л (н.у.), если выход оксида серы (IV) составляет 90%.
Задача №4. К раствору, содержащему хлорид кальция массой 4,1 г, прилили раствор, содержащий фосфат натрия массой 4,1 г. Определите массу полученного осадка, если выход продукта реакции составляет 88 %.
Приветствую вас, дорогие читатели!
В этой статье разберем такой вопрос: КАК РЕШАТЬ ЗАДАЧИ ТИПА №27?
Немного теории…
Данное задание связано с формулой определения массовой доли вещества (омега):
где
ω (омега) – массовая доля вещества (%);
m в-ва – масса вещества (г);
m р-ра – масса раствора (г).
Что это такое?
Отношение массы растворенного вещества к общей массе раствора называют массовой долей растворенного вещества.
Некоторая сложность заключается в том, что условии может быть дано несколько массовых долей, например. Классическим способом решать такие задачи будет труднее, и вы больше потратите времени при выполнении данного задания. На заметку: ЭТО ЗАДАНИЕ ОЦЕНИВАЕТСЯ В ОДИН БАЛЛ. Оно считается заданием базового уровня сложности.
Для того, чтобы упростить себе задачу, предлагаю вам «метод стаканчиков»:
Верхнюю часть дроби умножаем на нижнюю и получаем равенство:
w 1 * m 1 + w 2 * m 2 = w 3 * m 3
Массовые доли растворов будут даны в задаче, а вот некоторые необходимо запомнить:
– массовая доля H 2 O = 0%;
-массовая доля чистого вещества = 100%;
-массовая доля чистого вещества в кристаллогидрате:
Это все, что касается теории. Давайте разберем несколько примеров.
№1. К 300 г 6%-го раствора серной кислоты прилили 100 г воды. Массовая доля кислоты в полученном растворе равна__________%. (Запишите число с точностью до десятых.)
Решение
Имеется раствор серной кислоты с известной массой и массовой долей, поэтому записываем таким образом: 6%/300 г.
К нему добавляем воду. Масса воды известна, а массовая доля для воды всегда 0%, поэтому составляем второй стаканчик: 0%/100 г.
Так как воду прилили, то между этими дробями или стаканчиками ставим знак «+».
Масса раствора увеличилась, поэтому: 300 + 100 = 400 г, а массовая доля неизвестна, обозначаем за х .
В результате получается такое выражение:
которое несложно решить.
№2 . После упаривания 500 мл 10%-го раствора хлорида калия (плотность 1,11 г/мл) его масса уменьшилась на 100 г. Массовая доля соли в полученном растворе равна_______%. (Запишите число с точностью до десятых).
Решение
Особенность составления стаканчиков заключается в том, что в верхней части дроби всегда должны быть проценты, а в нижней – граммы.
Для составления первого стаканчика необходимо перевести мл в г по формуле: m 1(р-ра) = V 1(р-ра) * ρ1(р-ра) = 500 мл * 1,11 г/мл = 555 г.
Получаем: 10%/555 г.
В условии задачи есть слово «упарили» — это значит, что между дробями будет знак «-». Выпаривают воду, поэтому второй стаканчик выглядит следующим образом: 0%/100 г.
Получается раствор массой 555 – 100 = 455г, а массовая доля – x %.
Составляем выражение:
и решаем.
№3. При охлаждении 350 г 25%-го раствора сульфата меди (II) с 90 0С до 20 0С в осадок выпало 100 г осадка медного купороса CuSO4 * 5H2O . Массовая доля соли в полученном растворе равна______%. (Запишите число с точностью до десятых.)
Решение
Имеется раствор с массовой долей: 25%/350 г, затем его охладили и выпал осадок в виде кристаллогидрата CuSO4 *5H2O массой 100 г. Здесь необходимо найти массовую долю CuSO4 в кристаллогидрате по формуле:
Составляем второй стаканчик: 64%/100 г. Так как раствор охладили, то между дробями будет знак «-».
Получается раствор массой 350 – 100 = 250 г, а массовая доля – x %.
Составляем выражение:
и решаем.
Для закрепления материла предлагаю вам задачи с ответами для самопроверки.
№1. Для приготовления 2 л 37%-й аккумуляторной серной кислоты (плотностью 1,29 г/мл) потребуется 95%-я серная кислота массой_____г. (Запишите число с точностью до целых.)
Ответ: 1005 г.
№2. Масса уксусной кислоты, которую нужно растворить в 150 г столового 5%-го уксуса для получения 10%-го раствора равна_____г. (Запишите число с точностью до десятых.)
Ответ: 8,3%
№3. К 160 г 10%-го раствора хлорида натрия добавили 10 г этой соли и 200 г воды. Массовая доля соли в полученном растворе равна_____%. (Запишите число с точностью до целых.)
Ответ: 7%
№4. Массовая доля соляной кислоты в растворе, полученном при растворении 11,2 л хлороводорода в 1 л воды, равна_____%. (Запишите число с точностью до десятых.)
Ответ: 1,79%
Если данная статья понравилась и оказалась полезной, то ставьте лайк и подписывайтесь на канал!

В общем, мне нужны формулы по теме “Массовая доля компонентов в смеси” как найти массу вещества, как найти массу раствора, как найти массу смеси. Знаю как найти Омегу(раствора), Омегу(вещества), но не знаю как найти вот эти массы. Помогите пожалуйста, срочно нужны.
Выработать формулы 1)омега = 2 * пи * нью 2)омега = 2 * пи / Т 3) омега = нью / R То есть, объяснить, как они вышли.
Вы открыли страницу вопроса Выработать формулы 1)омега = 2 * пи * нью 2)омега = 2 * пи / Т 3) омега = нью / R То есть, объяснить, как они вышли?. Он относится к категории
Физика. Уровень сложности вопроса – для учащихся 5 – 9 классов.
Удобный и простой интерфейс сайта поможет найти максимально исчерпывающие
ответы по интересующей теме. Чтобы получить наиболее развернутый ответ,
можно просмотреть другие, похожие вопросы в категории Физика,
воспользовавшись поисковой системой, или ознакомиться с ответами других
пользователей. Для расширения границ поиска создайте новый вопрос, используя
ключевые слова. Введите его в строку, нажав кнопку вверху.
