как узнать молярную массу воздуха?
Ученик
(100),
закрыт
14 лет назад
Leonid
Высший разум
(388685)
14 лет назад
Как взвешенное среднее из молярных масс составляющих воздух газов. Скажем, если в воздухе 75% азота (28), 24% кислорода (32) и 1% аргона (39) – цифры взяты с потолка, и лучше их уточнить, – то средневзвешанная молярная масса будет 0,75*28+0,24*32+0,01*39.
Как найти молярную массу воздуха
Молярная масса – это масса одного моля вещества, то есть величина, показывающая, в каком количестве вещества содержится 6,022*10 (в степени 23) частиц (атомов, молекул, ионов). А если речь идет не о чистом веществе, а о смеси веществ? Например, о жизненно необходимом человеку воздухе, ведь он представляют собою смесь великого множества газов. Как вычислить его молярную массу?

Вам понадобится
- – точные лабораторные весы;
- – круглодонная колба со шлифом и краном;
- – вакуумный насос;
- – манометр с двумя кранами и соединительными шлангами;
- – термометр.
Инструкция
Прежде всего подумайте над допустимой погрешностью вычислений. Если вам не нужна высокая точность, ограничьтесь лишь тремя самыми «весомыми» компонентами: азотом, кислородом и аргоном, и возьмите «округленные» величины их концентраций. Если же необходим более точный результат, то используйте в расчетах еще и углекислый газ и можете обойтись без округления.
Предположим, что вас устроит первый вариант. Напишите молекулярные массы этих компонентов и их массовые концентрации в воздухе:
– азот (N2). Молекулярная масса 28, массовая концентрация 75,50%;
– кислород (О2). Молекулярная масса 32, массовая концентрация 23,15%;
– аргон (Ar). Молекулярная масса 40, массовая концентрация 1,29%.
Для облегчения расчетов, округлите величины концентраций:
– для азота – до 76%;
– для кислорода – до 23%;
– для аргона – до 1,3%.
Произведите несложное вычисление:
28* 0,76 + 32* 0,23 + 40*0, 013 = 29,16 граммов/моль.
Полученная величина очень близка к той, которая указана в справочниках: 28,98 граммов/моль. Расхождение объясняется округлением.
Можете определить молярную массу воздуха и с помощью несложного лабораторного опыта. Для этого измерьте массу колбы с находящимся в ней воздухом.
Запишите полученный результат. Потом, подсоединив шланг колбы к манометру, откройте кран и, включив насос, начните откачивать воздух из колбы.
Подождите некоторое время (чтобы воздух в колбе нагрелся до комнатной температуры), запишите показания манометра и термометра. Затем, закрыв кран на колбе, отсоедините ее шланг от манометра, и взвесьте колбу с новым (уменьшенным) количеством воздуха. Запишите результат.
Далее вам на помощь придет универсальное уравнение Менделеева-Клапейрона:
PVm = MRT.
Запишите его в несколько измененном виде:
∆PVm = ∆MRT, причем вам известны и изменение давления воздуха ∆P и изменение массы воздуха ∆M. Молярная масса воздуха m вычисляется элементарно: m = ∆MRT/∆PV.
Полезный совет
Уравнение Менделеева-Клапейрона описывает состояние идеального газа, которым воздух, конечно же, не является. Но при величинах давления и температуры, близких к нормальным, погрешности настолько незначительны, что ими можно пренебречь.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
В этой статье мы коснемся нескольких краеугольных понятий в химии, без которых совершенно невозможно
решение задач. Старайтесь понять смысл физических величин, чтобы усвоить эту тему.
Я постараюсь приводить как можно больше примеров по ходу этой статьи, в ходе изучения вы увидите множество примеров
по данной теме.

Относительная атомная масса – Ar
Представляет собой массу атома, выраженную в атомных единицах массы. Относительные атомные массы указаны в периодической
таблице Д.И. Менделеева. Так, один атом водорода имеет атомную массу = 1, кислород = 16, кальций = 40.
Относительная молекулярная масса – Mr
Относительная молекулярная масса складывается из суммы относительных атомных масс всех атомов, входящих в состав вещества.
В качестве примера найдем относительные молекулярные массы кислорода, воды, перманганата калия и медного купороса:
Mr (O2) = (2 × Ar(O)) = 2 × 16 = 32
Mr (H2O) = (2 × Ar(H)) + Ar(O) = (2 × 1) + 16 = 18
Mr (KMnO4) = Ar(K) + Ar(Mn) + (4 × Ar(O)) = 39 + 55 + (4 * 16) = 158
Mr (CuSO4*5H2O) = Ar(Cu) + Ar(S) + (4 × Ar(O)) + (5 × ((Ar(H) × 2) +
Ar(O))) = 64 + 32 + (4 × 16) + (5 × ((1 × 2) + 16)) = 160 + 5 * 18 = 250
Моль и число Авогадро
Моль – единица количества вещества (в системе единиц СИ), определяемая как количество вещества, содержащее столько же структурных единиц
этого вещества (молекул, атомов, ионов) сколько содержится в 12 г изотопа 12C, т.е. 6 × 1023.
Число Авогадро (постоянная Авогадро, NA) – число частиц (молекул, атомов, ионов) содержащихся в одном моле любого вещества.

Больше всего мне хотелось бы, чтобы вы поняли физический смысл изученных понятий. Моль – международная единица количества вещества, которая
показывает, сколько атомов, молекул или ионов содержится в определенной массе или конкретном объеме вещества. Один моль любого вещества
содержит 6.02 × 1023 атомов/молекул/ионов – вот самое важное, что сейчас нужно понять.
Иногда в задачах бывает дано число Авогадро, и от вас требуется найти, какое вам дали количество вещества (моль). Количество вещества в химии
обозначается N, ν (по греч. читается “ню”).
Рассчитаем по формуле: ν = N/NA количество вещества 3.01 × 1023 молекул воды и 12.04 × 1023 атомов углерода.
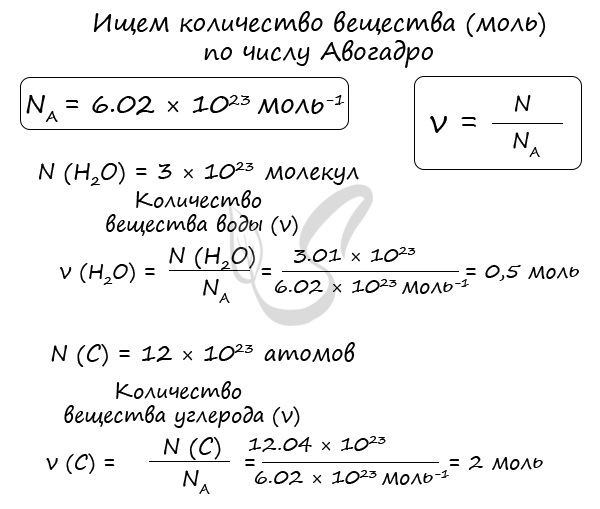
Мы нашли количества вещества (моль) воды и углерода. Сейчас это может показаться очень абстрактным, но, иногда не зная, как найти
количество вещества, используя число Авогадро, решение задачи по химии становится невозможным.
Молярная масса – M
Молярная масса – масса одного моля вещества, выражается в “г/моль” (грамм/моль). Численно совпадает с изученной нами ранее
относительной молекулярной массой.
Рассчитаем молярные массы CaCO3, HCl и N2
M (CaCO3) = Ar(Ca) + Ar(C) + (3 × Ar(O)) = 40 + 12 + (3 × 16) = 100 г/моль
M (HCl) = Ar(H) + Ar(Cl) = 1 + 35.5 = 36.5 г/моль
M (N2) = Ar(N) × 2 = 14 × 2 = 28 г/моль
Полученные знания не должны быть отрывочны, из них следует создать цельную систему. Обратите внимание: только что мы рассчитали
молярные массы – массы одного моля вещества. Вспомните про число Авогадро.
Получается, что, несмотря на одинаковое число молекул в 1 моле (1 моль любого вещества содержит 6.02 × 1023 молекул),
молекулярные массы отличаются. Так, 6.02 × 1023 молекул N2 весят 28 грамм, а такое же количество молекул
HCl – 36.5 грамм.
Это связано с тем, что, хоть количество молекул одинаково – 6.02 × 1023, в их состав входят разные атомы, поэтому и
массы получаются разные.

Часто в задачах бывает дана масса, а от вас требуется рассчитать количество вещества, чтобы перейти к другому веществу в реакции.
Сейчас мы определим количество вещества (моль) 70 грамм N2, 50 грамм CaCO3, 109.5 грамм HCl. Их молярные
массы были найдены нам уже чуть раньше, что ускорит ход решения.

ν (CaCO3) = m(CaCO3) : M(CaCO3) = 50 г. : 100 г/моль = 0.5 моль
ν (HCl) = m(HCl) : M(HCl) = 109.5 г. : 36.5 г/моль = 3 моль
Иногда в задачах может быть дано число молекул, а вам требуется рассчитать массу, которую они занимают. Здесь нужно использовать
количество вещества (моль) как посредника, который поможет решить поставленную задачу.
Предположим нам дали 15.05 × 1023 молекул азота, 3.01 × 1023 молекул CaCO3 и 18.06 × 1023 молекул
HCl. Требуется найти массу, которую составляет указанное число молекул. Мы несколько изменим известную формулу, которая поможет нам связать
моль и число Авогадро.

Теперь вы всесторонне посвящены в тему. Надеюсь, что вы поняли, как связаны молярная масса, число Авогадро и количество вещества.
Практика – лучший учитель. Найдите самостоятельно подобные значения для оставшихся CaCO3 и HCl.
Молярный объем
Молярный объем – объем, занимаемый одним молем вещества. Примерно одинаков для всех газов при стандартной температуре
и давлении составляет 22.4 л/моль. Он обозначается как – VM.
Подключим к нашей системе еще одно понятие. Предлагаю найти количество вещества, количество молекул и массу газа объемом
33.6 литра. Поскольку показательно молярного объема при н.у. – константа (22.4 л/моль), то совершенно неважно, какой газ мы
возьмем: хлор, азот или сероводород.
Запомните, что 1 моль любого газа занимает объем 22.4 литра. Итак, приступим к решению задачи. Поскольку какой-то газ
все же надо выбрать, выберем хлор – Cl2.


Моль (количество вещества) – самое гибкое из всех понятий в химии. Количество вещества позволяет вам перейти и к
числу Авогадро, и к массе, и к объему. Если вы усвоили это, то главная задача данной статьи – выполнена 🙂

Относительная плотность и газы – D
Относительной плотностью газа называют отношение молярных масс (плотностей) двух газов. Она показывает, во сколько раз одно вещество
легче/тяжелее другого. D = M (1 вещества) / M (2 вещества).
В задачах бывает дано неизвестное вещество, однако известна его плотность по водороду, азоту, кислороду или
воздуху. Для того чтобы найти молярную массу вещества, следует умножить значение плотности на молярную массу
газа, по которому дана плотность.
Запомните, что молярная масса воздуха = 29 г/моль. Лучше объяснить, что такое плотность и с чем ее едят на примере.
Нам нужно найти молярную массу неизвестного вещества, плотность которого по воздуху 2.5

Предлагаю самостоятельно решить следующую задачку (ниже вы найдете решение): “Плотность неизвестного вещества по
кислороду 3.5, найдите молярную массу неизвестного вещества”

Относительная плотность и водный раствор – ρ
Пишу об этом из-за исключительной важности в решении
сложных задач, высокого уровня, где особенно часто упоминается плотность. Обозначается греческой буквой ρ.
Плотность является отражением зависимости массы от вещества, равна отношению массы вещества к единице его объема. Единицы
измерения плотности: г/мл, г/см3, кг/м3 и т.д.
Для примера решим задачку. Объем серной кислоты составляет 200 мл, плотность 1.34 г/мл. Найдите массу раствора. Чтобы не
запутаться в единицах измерения поступайте с ними как с самыми обычными числами: сокращайте при делении и умножении – так
вы точно не запутаетесь.

Иногда перед вами может стоять обратная задача, когда известна масса раствора, плотность и вы должны найти объем. Опять-таки,
если вы будете следовать моему правилу и относится к обозначенным условным единицам “как к числам”, то не запутаетесь.
В ходе ваших действий “грамм” и “грамм” должны сократиться, а значит, в таком случае мы будем делить массу на плотность. В противном случае
вы бы получили граммы в квадрате 🙂
К примеру, даны масса раствора HCl – 150 грамм и плотность 1.76 г/мл. Нужно найти объем раствора.

Массовая доля – ω
Массовой долей называют отношение массы растворенного вещества к массе раствора. Важно заметить, что в понятие раствора входит
как растворитель, так и само растворенное вещество.
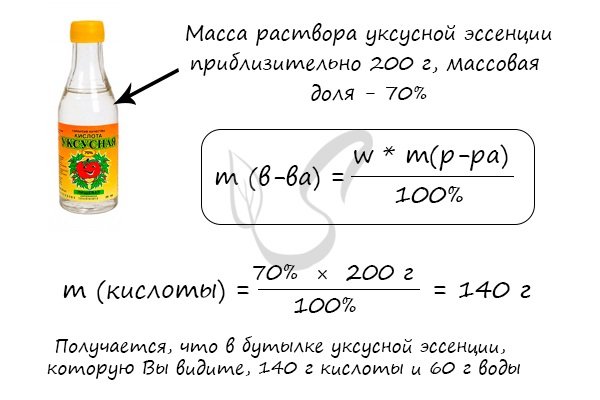
Массовая доля вычисляется по формуле ω (вещества) = m (вещества) / m (раствора). Полученное число будет показывать массовую долю
в долях от единицы, если хотите получить в процентах – его нужно умножить на 100%. Продемонстрирую это на примере.

Решим несколько иную задачу и найдем массу чистой уксусной кислоты в широко известной уксусной эссенции.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Что такое молярная масса?
Молярная масса вещества — это отношение его массы к количеству молей. Для воздуха тоже действует это отношение. Поэтому при проведении вычислений в результате получается масса одного моля. Но не все вещества можно рассчитать подобным образом. Для того, чтобы узнать, чему равна молярная масса воздуха в физике используют специальные формулы. Выражается результат в граммах на моль.
Воздух является смесью различных газов. Из этого следует, что молярная масса воздуха включает в себя молярные массы газов, входящих в его состав. Именно поэтому результаты таких вычислений будут различаться в зависимости от состава воздуха и количества различных газов и примесей в его составе. Существует и усредненный показатель, и средняя молярная масса воздуха равняется 29 г/моль.
Если же при расчетах было выявлено сильное отклонение от нормального показателя без объективных причин, то следует задуматься. Нарушение баланса газов – это очень серьезная проблема, которая очень часто встречается в больших городах. Именно там ежедневно в воздух выбрасывается огромное количество разнообразных веществ, которые меняют состав воздуха. Вредные примеси и их скопления очень плохо влияют на состояние организма человека. Также и увеличение или уменьшение содержания азота, кислорода, углекислого газа и других веществ влечет за собой тоже большие проблемы. Недостаток кислорода губителен для живых организмов и для человека может быть даже смертельно опасным.
Тщательное исследование воздуха может выявить отклонения от нормы и предотвратить их негативное влияние на организм человека. В нашей независимой лаборатории можно заказать комплексное обследование, которое представляет собой проведение исследований на различные показатели и выявление нарушений.

Как же определяется молярная масса воздуха?
Все вещества различаются по массе, и этот показатель является очень индивидуальным. Для сложных веществ учитывается число атомов, находящемся в нем. Так чему равна молярная масса воздуха? Это сумма всех массовых долей элементов, которые входят в данное вещество. В данном случае это молярные массы азота, кислорода, аргона, углекислого газа, водорода и других веществ. Из них азот составляет 78% от общего объема, кислород 21%, а остальные же вещества содержатся в гораздо меньшем количестве.
Существует несколько методов проведения измерения:
- Откачка воздуха из колбы позволяет при помощи уравнения состояния газа позволяет также вычислить этот показатель.
- При помощи классического химического уравнения, в котором находятся все молярные массы газов, входящих в состав воздуха.
- Также существуют уже готовые таблицы, со средними значениями.
Если производить расчеты, следуя определению, что объемы газов являются пропорциональными их количествам, то мы можем выражать среднюю массу как через объем, так и через количество. Поэтому молярная масса воздуха в химии рассчитывается по формуле, включающей в себя отношение массы вещества к его количеству. В сложных веществах надо найти отдельно массы каждого вещества, которое входит в состав.
Но этот способ расчетов по большей части затрагивает ситуации, когда воздух находится в своем обычном состоянии. Также можно вычислить и массу в других ситуациях.
Формула, по которой рассчитывается молярная масса влажного воздуха является формулой для смеси газов. При расчетах учитываются доли сухого воздуха и водяного пара, а также соответствующее для них давление и молярные массы. Получается формула выглядит как сумма объема с молярной массой водяного пара и объема с молярной массой сухого воздуха.

Известно, что молярная масса воздуха при нормальных условиях — 29 г/моль. Именно такой показатель принят за средний. Но он может колебаться в зависимости от состава воздуха. Поэтому сильные изменения свидетельствуют о нарушениях баланса газов в воздухе. Так если в воздухе будет содержаться 92% азота, то это будет смертельно опасно для человека. Именно поэтому состав воздуха так важен и необходимо его постоянно контролировать. Сейчас, в результате деятельности человека, наблюдается неблагоприятная экологическая картина и во многом она связана с загрязнением воздуха. Именно выбросы в воздух различных веществ нарушают его естественный состав, что приводит к ухудшению условий жизни. Многие экологические проблемы тоже являются уже следствием загрязнения воздуха. Смог, кислотные дожди и изменение состава всей атмосферы.
Закажите бесплатно консультацию эколога
Сколько азота в воздухе?
Если говорить о воздухе, то нельзя не затронуть тему содержания в нем азота. Он представляет собой бесцветный газ, у которого нет запаха и вкуса. Если разбирать химическую формулу, то молекула азота представляет собой два атома азота, которые скрещены между собой. Именно он составляет большую часть и составляет около 78% от всего объема воздуха. И молярная масса сжатого воздуха, высчитываемая по формуле, будет содержать в себе и молярную массу азота. Азот содержится практически везде и человек уже давно начал его использовать в своих нуждах. Даже в белке, который является основным строительным материалом всех живых организмов, тоже есть азот. Так аммиак, который применяется в сельском хозяйстве, получается при извлечении азота. И сам человек примерно на 2% состоит из азота.
Но азот может быть и опасным, если превышать его концентрацию. Безопасный азот обычно смешан с водородом в необходимых пропорциях. Азот необходим для разбавления кислорода, ведь чистый кислород тоже может быть губительным для живых организмов. Но если азот будет повышен, то это приведет к гипоксии, то есть понижению уровня кислорода в организме и внутренних органах. Вдыхаемый человеком азот не усваивается в организме, а выдыхается, так как служит только для защиты легких от кислорода.

Человек ежедневно сталкивается с тем, что было создано не без помощи азота. Азот нашел свое применение в различных областях и сейчас мы можем видеть его как в упаковках на прилавках магазинов, так и в медицине. К примеру, жидкую форму азота уже давно используют для транспортировки донорских органов.
Растения тоже не могут обойтись без азота и получают его из почвы в виде нитратов. В почве находится большое количество азота. Так потом он попадает в организмы животных, которые едят растения. Главным поставщиком азота являются бактерии, благодаря которым образовывается более ста тонн этого вещества.
Теплопроводность углекислого газа
Углекислым газом называют химическое соединение углерода и кислорода. В отличие от чистого углерода или кислорода, содержание углекислого газа в воздухе намного меньше. В нормальных условиях содержание будет равно 0,003% от общего объема воздуха. В молекулы газа входит один атом углерода и два атома кислорода. Для человека повышенный уровень углекислого газа может быть смертельно опасен, ведь он мешает поступлению кислорода в организм.
Углекислый газ также участвует в круговороте веществ и без него невозможны многие процессы. Так живые существа выделяют его в процессе дыхания, а растения, наоборот, при фотосинтезе поглощают этот газ. Он выделяется при горении углеродсодержащих предметов. Поэтому при пожарах нарушается естественный состав воздуха и увеличивается содержание в нем углекислого газа.
Теплопроводность представляет собой процесс равномерного перераспределения энергии. Эта способность является индивидуальной для каждых веществ, их состояний, а также зависит и от внешних факторов. Процесс непосредственно зависит от температуры и давления. Поэтому были разработаны таблицы, в которых показана зависимость этих показателей друг от друга.
В специальных таблицах уже рассчитаны показатели теплопроводности углекислого газа в различных его состояниях и условиях.
На основе этих таблиц можно сделать вывод, что теплопроводность углекислого газа уменьшается при повышении температуры и наоборот увеличивается если повысить давление.
Также состояние газа тоже влияет на эту зависимость. В газообразном состоянии он более теплопроводен как при увеличении давления, так и при повышении температуры, в отличие от конденсированного состояния.
На основе именно этого свойства газа работают приборы, которые измеряют содержание углекислого газа.

Зачем нужно проводить химический анализ воздуха?
Воздух является важным условием для жизни на земле. Все живые организмы зависят от воздуха и содержащегося в нем кислорода. Поэтому важно, чтобы в нем не содержалось вредных примесей и все показатели были в норме. Нарушение баланса может вызывать многие проблемы и в том числе, и со здоровьем.
Состав воздуха может изменяться не только в результате загрязнения различными предприятиями или автомобилями. Даже мебель или отделочные материалы в вашей квартиры на самом деле могут быть источниками выброса в воздух различных вредных веществ. Сейчас очень часто производители могут нарушать всевозможные нормы и изготовлять мебель из некачественных дешевых материалов. В процессе эксплуатации изделия начинают менять свои свойства и выделять иногда даже ядовитые вещества.
Для того, чтобы обезопасить себя и своих близких вы можете обратиться в нашу лабораторию «ЭкоТестЭкспресс» и заказать химический анализ воздуха.
Химический анализ представляет собой комплекс различных исследований, который позволяет определить точный состав воздуха, количество содержащихся в нем веществ и примесей. Таким образом можно выявить как нарушения в балансе, так и вредные вещества, которые загрязняют воздух и вызывают различные заболевания.
Наши эксперты-экологи проведут все необходимые измерения и выдадут вам официальные результаты исследования. Также после получения результатов вы можете получить консультацию и понять, какие именно источники вызвали нарушение норм. Своевременное устранение проблемы может сберечь ваше здоровье и комфорт.
Документы, которые выдает наша лаборатория, являются не только официальными, но и имеют юридическую силу. В случае выявления нарушений такие документы могут быть предъявлены в суд в качестве доказательства.
ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ МОЛЯРНОЙ МАССЫ ВОЗДУХА
- Авторы
- Руководители
- Файлы работы
- Наградные документы
Гудемчук В.А. 1
1МБОУ СШ №10
Ульянова С.Ю. 1
1МБОУ СШ №10
Текст работы размещён без изображений и формул.
Полная версия работы доступна во вкладке “Файлы работы” в формате PDF
Введение:
Изучая на уроках физики тему «Уравнение Менделеева–Клапейрона», я часто встречалась с задачами, в которых нужно было определить молярную массу воздуха. Например: шар, массой оболочки , заполненный гелием, поднимает груз массой m. Атмосферное давление и температуру считать известной величиной.
Меня заинтересовал вопрос, как экспериментально измерить молярную массу воздуха.
Один из способов определения молярной массы воздуха – метод откачки воздуха. Но для данного метода нужно специальное оборудование, которого у нас в школе нет. Я решила найти доступный способ определения молярной массы воздуха.
1.История открытия состава воздуха и его молярной массы
Воздух необходим для нормального существования на Земле живых организмов. В промышленности и в быту кислород воздуха используется для сжигания топлива с целью получения тепла и механической энергии в двигателях внутреннего сгорания.
Молярнаямасса — характеристика вещества, которая равна отношению массы вещества к количеству молей этого вещества,т.е. масса одного моля вещества. Для отдельных химических элементов молярной массой является масса одного моля отдельных атомов этого элемента, то есть масса атомов вещества взятых в количестве, равном Числу Авогадро. В этом случае молярная масса элемента, выраженная в г/моль, численно совпадает с молекулярной массой — массой атома элемента, выраженной в а. е. м. (атомная единица массы). Однако надо чётко представлять разницу между молярной массой и молекулярной массой, понимая, что они равны лишь численно и отличаются по размерности.
В XVII веке в работах Г. Галилея(1638) и Р. Бойля(1662) было показано, что воздух – материальное вещество и обладает вполне определенными физическими свойствами (массой и давлением).
Шведский ученый К. Шееле(1742-1786) поставил серию опытов. Изучая состав воздуха, он пришел к выводу, что атмосферный воздух состоит из 2 видов воздуха: «огненного», поддерживающего дыхание и горение (О2) и «испорченного», не поддерживающего горения (N2). Он провел опыты по изучению взаимодействия воздуха, находящегося в замкнутом пространстве в контакте с различными веществами. Во всех случаях было поглощено около 1/5 исходного объема воздуха. При этом оставшийся газ оказался легче обычного воздуха и не поддерживал горения. Шееле впервые открыл О2.
В 1774 году французский ученый А. Лавуазьедоказал, что воздух – это смесь в основном двух газов — N2и О2.Он написал работу «Анализ атмосферного воздуха». Он нагревал металлическую ртуть в реторте(см.ссылку) на жаровне в течение 12 суток. Конец реторты был подведен под колокол, поставленный в сосуд с Hg. В результате уровень ртути в колоколе поднялся примерно на 1/5. На поверхности ртути в реторте образовалось вещество оранжево-красного цвета – оксид ртути. Воздух, оставшийся под колоколом, был непригоден для дыхания. Опыт Лавуазье позволил судить о составе воздуха; выяснилось, что в воздухе содержится 4/5 N2 и 1/5 О2 по объему.
Практически одновременно с кислородом выделили и изучили другую важную составную часть воздуха – N2 (Даниель Резерфордв 1772 г.). Несколько раньше Резерфорда N2 был получен английским исследователем — Г. Кавендишеми назван “испорченным воздухом”.
________________________________________________________________________
Реторта (лат. retorta, буквально — повёрнутая назад) — аппарат, служащий в химической лабораторной и заводской практике для перегонки или для воспроизведения реакций, требующих нагревания и сопровождающихся выделением газообразных или жидких летучих продуктов, которые тут же непосредственно и подвергаются перегонке.
Химик У. Рамзайи физик Д. Рэлейв 1894 г. обнаружили тяжелый газ, который входит в состав воздуха – аргон. Через год Рамзай открыл гелий.Вместе с Траверсомон открыл криптон, ксенон и неон. В 1900 году английский физик Э. Резерфордоткрыл радон.
Итак,воздух- смесь газов,образующая земную атмосферу.
В его состав входят:
|
Состав атмосферного воздуха |
||
|
Наименование основных газов |
Содержание,% объемные |
Относительная молекулярная масса,г/моль |
|
Азот |
78,09 |
28 |
|
Кислород |
20,95 |
32 |
|
Аргон |
0,93 |
39 |
|
Углекислый газ |
0,03 |
44 |
|
Неон |
1,8 |
20 |
|
Гелий |
4 |
|
|
Криптон |
83 |
|
|
Ксенон |
131 |
|
|
Водород |
2 |
|
|
Озон |
48 |
Состав земной атмосферы остается постоянным над сушей, над морем, в городах и сельской местности. Не изменяется он также с высотой. При этом следует помнить, что речь идет о процентном содержании составных частей воздуха на разных высотах. Однако этого нельзя сказать о весовой концентрации газов. По мере подъема вверх плотность воздуха падает и количество молекул, содержащихся в единице пространства, тоже снижается. Вследствие этого падает весовая концентрация газа и его парциальное давление.
1.1Химический способ определения молярной массы воздуха
Молярной массойназывается масса одного моля вещества.
Существуют различные способы определения молекулярной массы воздуха. Определим её , используя формулу из курса химии.
Дано: СИ: Решение:
) 23% )* Mr( )+ 𝜔()* Mr()+
() 76 % + ( Ar)* Mr(Ar ) ;
𝜔( Ar) %
Mr()=32 г/моль 32*кг/моль
Mr( ) =28 г/моль 28* кг/моль
Mr(Ar ) =40 г/моль 40* кг/моль
-?
Ответ: Молярная масса воздуха равна
1.2 Метод откачки воздуха
Схема установки для откачки воздуха из колбы:
C – стеклянная колба;
K – кран;
A– резиновая трубка;
B– вакуумметр.
Используя уравнение состояния идеального газа, можно определить молярную массу газа. При не слишком высоких давлениях, но достаточно высоких температурах, газ можно считать идеальным.
Состояние такого газа описывается уравнением Менделеева–Клапейрона:
(1)
где P – давление газа; V – объем газа; m масса газа; M – молярная масса газа;
R = 8,3145 Дж/(моль∙К) – универсальная газовая постоянная; T – абсолютная температура газа.
Из формулы (1) получаем выражение для молярной массы газа:
M= (2)
Следовательно, для вычисления M необходимо знать массу газа m, температуру T, давление газа p и занимаемый им объем V.
Пусть в сосуде объемом V находится газ массой m1 под давлением p1 и при температуре T. Уравнение состояния (1) для этого газа примет вид
(3)
Откачаем часть газа из сосуда, не изменяя его температуры (изотермически). После откачки масса газа в сосуде и его давление уменьшатся. Обозначим их соответственно m2 и P2 и вновь запишем уравнение состояния
(4)
Из уравнений (3) и (4) получаем
M=. (5)
С помощью этого уравнения, зная изменение массы газа и изменение давления,а также температуру и объем газа, можно определить молярную массу воздуха.
В данной работе исследуемым газом является воздух, представляющий собой, как известно, смесь азота, кислорода, углекислого газа, аргона, паров воды и других газов. Формула (5) пригодна и для определения M смеси газов. В этом случае найденное значение M представляет собой некоторую среднюю или эффективную молярную массу смеси газов.
3. Практическая часть
3.1 Определение молярной массы воздуха
За основу нашего эксперимента взята задача: шар, массой оболочки , заполненный гелием, поднимает груз массой m. Давление и температуру считать известной величиной.
Приведем идею опыта:Шар, заполненный гелием, поднимает груз из пластилина. К детскому шарику, заполненному гелием, подберем груз такой массы, чтобы он завис в воздухе. Оболочку шара считать нерастяжимой. (Приложение 1)
Продемонстрируем схему опыта с указанием всех сил. На оболочку шара, гелий, грузик действует сила тяжести mg, а эту силу тяжести уравновешивает сила Архимеда. По второму закону Ньютона сила Архимеда равна сумме сил тяжести.
После получим формулу:
Воспользуемся формулой Менделеева-Клапейрона:
pV=
Выразим молярную массу:
M=
Подставим полученную плотность воздуха из третьей формулы в пятуюи получим формулу для расчета молярной массы воздуха:
M=
Отсюда следует, чтобы найти молярную массу воздуха, нужно измерить массу груза(приложение 2), массу гелия, массу оболочки(приложение 3),температуру(приложение 4) , давление воздуха(приложение 5), объем шара.
Найдем объем шара. Для этого нальем воду в аквариум, поставим метку, выпустим гелий из шарика и через отверстие в шарике, с помощью трубки и воронки, заполним шар водой, уровень воды поднялся ровно на объем шара. С помощью мензурки, выливая воду из аквариума до первоначальной метки, определим объем шара(приложение 6).
=13л = 13*
Массу гелия в шаре найдем с помощью уравнения Менделеева-Клапейрона, учитывая, что температура гелия и давление равны атмосферным показателям:
pV =
Выразим массу гелия:
Подставим известные значения:
0,002кг
Подставим найденные величины в общую формулу для молярной массы:
M==0,027 кг/моль
3.2 Погрешности измерений
При оценке результатов мы можем оценить погрешность измерений. Погрешности возникают при любых измерениях, но нам кажется, что наибольшую погрешность я допустила при измерении объема шара.
Найдём относительную погрешность измерений по формулам :
,
Где
Абсолютные инструментальные и абсолютные погрешности отсчёта:
|
Прибор |
|||
|
Весы электронные |
0 |
кг |
|
|
Барометр-анероид |
Па |
Па |
|
|
Термометр лабораторный |
|||
|
Объем шара |
Относительная погрешность измерения:
=27*кг/моль*0,044=
кг/моль27*кг/молькг/моль
*Я повторила опыт несколько раз и получила результат, близкий к первому.Это говорит о том, что предложенный мной опыт достаточно точный.
4.Вывод: Предложенный мной метод удобен в домашних или школьных условиях, поэтому я считаю, что его можно использовать в одной из работ практикума по физике 10 класса. Для более упрощенного варианта работы объем шара и массу оболочки считать известными величинами. Также целесообразно применять клапан многократного использования.
Поэтому мной была разработана методичка для проведения работы практикума по физике (приложение 6).
5. Список использованных источников:
Воздух//Символы,знаки,эмблемы:Энциклопедия/авт.-сост.В.Э.Багдасарян,И.Б.Орлов,В.Л. Телицын ;под общ. ред. В.Л.Теплицына.-2-е изд.-
М.:ЛОКИД-ПРЕСС,2005.-495с.
Г. И. Дерябина, Г. В. Кантария. 2.2.Моль,молярная масса. Органическая химия: веб-учебник.
http://kf.info.urfu.ru/glavnaja/
https://ru.wikipedia.org/wiki/Молярная_масса
https://ru.wikipedia.org/wiki/Воздух
http://pandia.ru/text/77/373/27738.php
http://ladyretryka.ru/?p=9387
6. Приложения:
Приложение 1
Приложение 2
Приложение 3
Приложение 4
Приложение 5
Приложение 6
Приложение 7
Просмотров работы: 1706
