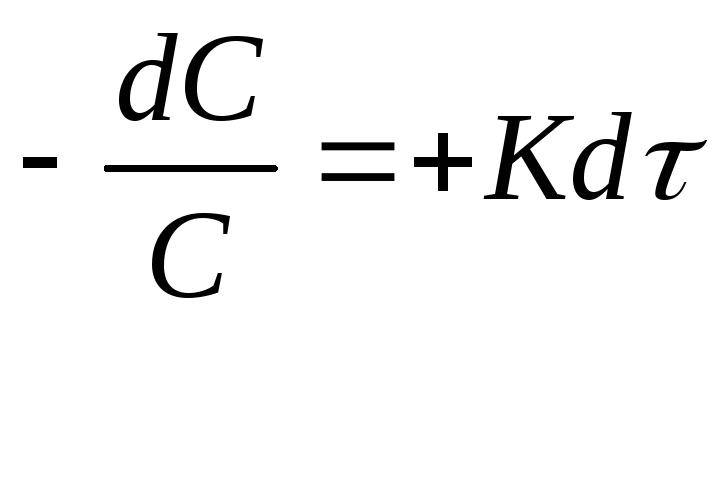Загрузить PDF
Загрузить PDF
Периодом полураспада вещества, которое находится в стадии распада, называют время, в течение которого количество этого вещества уменьшится в два раза. Первоначально этот термин использовался для описания распада радиоактивных элементов, таких как уран или плутоний, но, вообще говоря, он может быть использован для любого вещества, которое подвергается распаду в установленной или экспоненциальной скорости. Вы можете рассчитать период полураспада любого вещества, зная скорость распада, которая является разницей между начальным количеством вещества и количеством вещества, оставшимся после определенного периода времени. Читайте далее, чтобы узнать, как быстро и легко подсчитать период полураспада вещества.
-
1
Разделите количество вещества в одной точке во времени на количество вещества, оставшееся после определенного периода времени.
- Формула для вычисления периода полураспада: t1/2 = t * ln(2)/ln(N0/Nt)
- В этой формуле: t – прошедшее время, N0 – начальное количество вещества и Nt – количество вещества через прошедшее время.
- Например, если вначале количество составляет 1500 граммов, а конечный объем составляет 1000 граммов, начальное количество, деленное на конечный объем, равно 1,5. Предположим, что время, которое прошло, составляет 100 минут, то есть (t) = 100 мин.
-
2
Вычислите десятичный логарифм числа (log), полученного на предыдущем шаге. Для этого введите полученное число в научный калькулятор, а затем нажмите кнопку log, либо введите log(1,5) и нажмите знак равенства для получения результата.
- Логарифмом числа по заданному основанию называется такой показатель степени, в который необходимо возвести основание (то есть столько раз, сколько необходимо основание умножить на само себя), чтобы получить это число. В десятичных логарифмах используется основание 10. Кнопка log на калькуляторе соответствует десятичному логарифму. Некоторые калькуляторы вычисляют натуральные логарифмы ln.
- Когда log (1,5) = 0,176, то это означает, что десятичный логарифм 1,5 равен 0,176. То есть если число 10 возвести в степень 0,176, то получится 1,5.
-
3
Умножьте прошедшее время на десятичный логарифм 2. Если вы рассчитаете log(2) на калькуляторе, то получится 0,30103. Следует помнить, что прошедшее время составляет 100 минут.
- Например, если прошедшее время составляет 100 минут, умножьте 100 на 0,30103. Результат равен 30,103.
-
4
Разделите число, полученное на третьем шаге, на число, вычисленное на втором шаге.
- Например, если 30,103 разделить на 0,176, то получится 171,04. Таким образом, мы получили период полураспада вещества, выраженный в единицах времени, используемых в третьем шаге.
-
5
Готово. Теперь, когда вы рассчитали период полураспада для этой задачи, необходимо обратить внимание на то, что для расчетов мы использовали десятичный логарифм, но вы могли использовать и натуральный логарифм ln – результат был бы таким же. И, на самом деле, при расчете периода полураспада натуральный логарифм используется чаще.
- То есть, вам было бы необходимо рассчитать натуральные логарифмы: ln(1,5) (результат 0,405) и ln(2) (результат 0,693). Затем, если вы умножите ln(2) на 100 (время), получится 0,693 x 100=69,3, и разделите на 0,405, вы получите результат 171,04 – тот же, что и при использовании десятичного логарифма.
Реклама
-
1
Узнайте, сколько вещества с известным периодом полураспада осталось через определенное количество времени. Решите следующую задачу: Пациенту было дано 20 мг йода-131. Сколько останется через 32 дня? Период полураспада йода-131 составляет 8 дней. Вот, как решить эту задачу:
- Узнаем, сколько раз вещество сократилось вдвое за 32 дня. Для этого узнаем, сколько раз по 8 (таков период полураспада йода) умещается в 32 (в количестве дней). Для этого необходимо 32/8 = 4, так, количество вещества сокращалось вдвое четыре раза.
- Другими словами, это означает, что через 8 дней останется 20мг/2, то есть 10 мг вещества. Через 16 дней будет 10мг/2, или 5мг вещества. Через 24 дня останется 5мг/2, то есть 2,5 мг вещества. Наконец, через 32 дня у пациента будет 2,5мг/2, или 1,25 мг вещества.
-
2
Узнайте период полураспада вещества, если известно начальное и оставшееся количество вещества, а также прошедшее время. Решите следующую задачу: Лаборатория получила 200 г технеция-99m и через сутки осталось только 12,5 г изотопов. Каков период полураспада технеция-99m? Вот, как решить эту задачу:
- Будем действовать в обратном порядке. Если осталось 12,5г вещества, тогда прежде, чем его количество сократилось в 2 раза, вещества было 25 г (так как 12,5 x 2); до этого было 50г вещества, а еще до этого было 100г, и, наконец, до этого было 200г.
- Это означает, что прошло 4 периода полураспада прежде, чем от 200 г вещества осталось 12,5 г. Получается, что период полураспада составляет 24 часа/4 раза, или 6 часов.
-
3
Узнайте, сколько периодов полураспада необходимо для того, чтобы количество вещества сократилось до определенного значения. Решите следующую задачу: Период полураспада урана-232 составляет 70 лет. Сколько периодов полураспада пройдет, чтобы 20 г вещества сократилось до 1,25 г? Вот, как решить эту задачу:
- Начните с 20г и постепенно уменьшайте. 20г/2 = 10г (1 период полураспада), 10г/2 = 5 (2 периода полураспада), 5г/2 = 2,5 (3 периода полураспада) и 2,5/2 = 1,25 (4 периода полураспада). Ответ: необходимо 4 периода полураспада.
Реклама
Предупреждения
- Период полураспада – это приблизительное определение времени, необходимого для распада половины оставшегося вещества, а не точный расчет. Например, если остался только один атом вещества, то после полураспада не останется только половина атома, а останется один или ноль атомов. Чем больше количество вещества, тем более точным будет расчет по закону больших чисел
Реклама
Что вам понадобится
- Инженерный калькулятор
Об этой статье
Эту страницу просматривали 55 193 раза.
Была ли эта статья полезной?
| Ядерная физика |
|---|
 |
| Атомное ядро · Радиоактивный распад · Ядерная реакция · Термоядерная реакция |
|
Основные термины Атомное ядро · Изотопы · Изобары · Капельная модель ядра · Период полураспада · Массовое число · Составное ядро · Цепная ядерная реакция · Ядерное эффективное сечение |
|
Распад ядер Закон радиоактивного распада · Альфа-распад · Бета-распад · Кластерный распад |
|
Сложный распад Электронный захват · Двойной бета-распад · Двойной электронный захват · Внутренняя конверсия · Изомерный переход |
|
Излучения Ионизирующее излучение · Нейтронный распад · Позитронный распад · Протонный распад · Гамма излучение · Фоторасщепление |
|
Захваты Электронный захват · Нейтронный захват (r-процесс · s-процесс) · Протонный захват (p-процесс · rp-процесс) · Нейтронизация |
|
Деление ядра Спонтанное деление |
|
Нуклеосинтез Первичный нуклеосинтез · Протон-протонный цикл · CNO-цикл · Тройная гелиевая реакция · Гелиевая вспышка · Ядерное горение углерода · Углеродная детонация · Ядерное горение кислорода · Ядерное горение неона · Ядерное горение кремния · Реакции скалывания |
| См. также: Портал:Физика |
Пери́од полураспа́да квантовомеханической системы (частицы, ядра, атома, энергетического уровня и т. д.) — время 
Период полураспада наглядно характеризует скорость распада радиоактивных ядер, наряду со средним временем жизни и вероятностью распада в единицу времени (постоянной распада), эти величины связаны друг с другом простым однозначным соотношением[2][3][4][5][6].
Период полураспада является константой для данного радиоактивного ядра (изотопа). Для различных изотопов эта величина может изменяться от десятков йоктосекунд (10−24 с) у водорода-7 до более чем 1024 лет у теллура-128, что многократно превышает возраст Вселенной[4][5]. На основании постоянства периода полураспада строится метод радиоизотопного датирования[5].
Определение и основные соотношения[править | править код]
Понятие периода полураспада применяется как к испытывающим распад элементарным частицам, так и к радиоактивным ядрам[4]. Поскольку событие распада имеет квантовую вероятностную природу, то если рассматривать одну структурную единицу материи (частицу, атом радиоактивного изотопа), можно говорить о периоде полураспада как промежутке времени, по истечении которого средняя вероятность распада рассматриваемой частицы будет равна 1/2[1].
Если же рассматривать экспоненциально распадающиеся системы частиц, то периодом полураспада 



- где
— постоянная распада[7].
По определению, 

Далее, поскольку среднее время жизни 
то есть период полураспада примерно на 30,7 % короче, чем среднее время жизни. Например, для свободного нейтрона 

Не следует считать, что за два периода полураспада распадутся все частицы, взятые в начальный момент. Поскольку каждый период полураспада уменьшает число выживших частиц вдвое, за время 


Парциальный период полураспада[править | править код]
Если система с периодом полураспада 

Парциальный 


Значения для различных изотопов[править | править код]
Период полураспада конкретного изотопа является постоянной величиной, не зависящей от способа его получения, агрегатного состояния вещества, температуры, давления, химического состава соединения, куда оно входит, и практически любых других внешних факторов, за исключением акта прямого ядерного взаимодействия в результате, например, соударения с высокоэнергетической частицей в ускорителе[5][6].
На практике период полураспада определяют, измеряя активность исследуемого препарата через определённые промежутки времени. Учитывая, что активность препарата пропорциональна количеству атомов распадающегося вещества, и воспользовавшись законом радиоактивного распада, можно вычислить период полураспада данного вещества[8].
Значения периода полураспада для различных радиоактивных изотопов:
| Химический элемент | Обозначение | Порядковый номер (Z) | Массовое число (A) | Период полураспада |
|---|---|---|---|---|
| Актиний | Ac | 89 | 227 | 22 года[9][10] |
| Америций | Am | 95 | 243 | 7,3⋅103 лет[10][11] |
| Астат | At | 85 | 210 | 8,3 часа[9] |
| Бериллий | Be | 4 | 8 | 8,2⋅10-17 секунды[11] |
| Висмут | Bi | 83 | 208 | 3,68⋅105 лет[11][12] |
| 209 | 2⋅1019 лет[10][13] | |||
| 210 | 3,04⋅106 лет[12][13] | |||
| Берклий | Bk | 97 | 247 | 1,38⋅103 лет[10][11] |
| Углерод | C | 6 | 14 | 5730 лет[1][13] |
| Кадмий | Cd | 48 | 113 | 9⋅1015 лет[14] |
| Хлор | Cl | 17 | 36 | 3⋅105 лет[13] |
| 38 | 38 минут[13] | |||
| Кюрий | Cm | 96 | 247 | 4⋅107 лет[9] |
| Кобальт | Co | 27 | 60 | 5,27 года[13][15] |
| Цезий | Cs | 55 | 137 | 30,1 года[1][15] |
| Эйнштейний | Es | 99 | 254 | 1,3 года[9][10] |
| Фтор | F | 9 | 18 | 110 минут[11][15] |
| Железо | Fe | 26 | 59 | 45 дней[1][13] |
| Франций | Fr | 87 | 223 | 22 минуты[9][10] |
| Галлий | Ga | 31 | 68 | 68 минут[11] |
| Водород | H | 1 | 3 | 12,3 года[13][15] |
| Йод | I | 53 | 131 | 8 дней[13][15] |
| Иридий | Ir | 77 | 192 | 74 дня[13] |
| Калий | K | 19 | 40 | 1,25⋅109 лет[1][11] |
| Молибден | Mo | 42 | 99 | 66 часов[5][11] |
| Азот | N | 7 | 13 | 10 минут[13] |
| Натрий | Na | 11 | 22 | 2,6 года[13][15] |
| 24 | 15 часов[1][13][15] | |||
| Нептуний | Np | 93 | 237 | 2,1⋅106 лет[10][11] |
| Кислород | O | 8 | 15 | 124 секунды[13] |
| Фосфор | P | 15 | 32 | 14,3 дня[1][13] |
| Протактиний | Pa | 91 | 231 | 3,3⋅104 лет[11][13] |
| Полоний | Po | 84 | 210 | 138,4 дня[9][13] |
| 214 | 0,16 секунды[11] | |||
| Плутоний | Pu | 94 | 238 | 87,7 года[11] |
| 239 | 2,44⋅104 лет[1][13] | |||
| 242 | 3,3⋅105 лет[9] | |||
| Радий | Ra | 88 | 226 | 1,6⋅103 лет[9][11][10] |
| Рубидий | Rb | 37 | 82 | 76 секунд[11] |
| 87 | 49,7⋅109 лет[11] | |||
| Радон | Rn | 86 | 222 | 3,83 дня[9][13] |
| Сера | S | 16 | 35 | 87 дней[13] |
| Самарий | Sm | 62 | 147 | 1,07⋅1011 лет[11][12] |
| 148 | 6,3⋅1015 лет[11] | |||
| 149 | > 2⋅1015 лет[11][12] | |||
| Стронций | Sr | 38 | 89 | 50,5 дня[13] |
| 90 | 28,8 года[11] | |||
| Технеций | Tc | 43 | 99 | 2,1⋅105 лет[9][10] |
| Теллур | Te | 52 | 128 | 2⋅1024 лет[11] |
| Торий | Th | 90 | 232 | 1,4⋅1010 лет[9][10] |
| Уран | U | 92 | 233 | 1,⋅105 лет[13] |
| 234 | 2,5⋅105 лет[13] | |||
| 235 | 7,1⋅108 лет[1][13] | |||
| 238 | 4,5⋅109 лет[1][9][10][13] | |||
| Ксенон | Xe | 54 | 133 | 5,3 дня[13][15] |
| Иттрий | Y | 39 | 90 | 64 часа[13] |
Примеры расчётов[править | править код]
Пример 1[править | править код]
Если рассматривать достаточно близкие моменты времени 



С её помощью легко оценить число атомов урана-238, имеющего период полураспада 

Вычисления приводят к тому, что в одном килограмме урана в течение одной секунды распадается двенадцать миллионов атомов. Несмотря на такое огромное число, всё же скорость превращения ничтожно мала. Действительно, в секунду из наличного количества урана распадается его доля, равная
Пример 2[править | править код]
Образец содержит 10 г изотопа плутония Pu-239 с периодом полураспада 24 400 лет. Сколько атомов плутония распадается ежесекундно?
Поскольку рассматриваемое время (1 с) намного меньше периода полураспада, можно применить ту же, что и в предыдущем примере, приближённую формулу:
Подстановка численных значений даёт

Когда рассматриваемый период времени сравним с периодом полураспада, следует пользоваться точной формулой
Она пригодна в любом случае, однако для малых периодов времени требует вычислений с очень большой точностью. Так, для данной задачи:
Стабильность периода полураспада[править | править код]
Во всех наблюдавшихся случаях (кроме некоторых изотопов, распадающихся путём электронного захвата) период полураспада был постоянным (отдельные сообщения об изменении периода были вызваны недостаточной точностью эксперимента, в частности, неполной очисткой от высокоактивных изотопов). В связи с этим период полураспада считается неизменным. На этом основании строится определение абсолютного геологического возраста горных пород, а также радиоуглеродный метод определения возраста биологических останков: зная концентрацию радиоизотопа в настоящее время и в прошлом, можно рассчитать, сколько точно времени прошло с тех пор[5].
Предположение об изменяемости периода полураспада используется креационистами, а также представителями т. н. «альтернативной науки» для опровержения научной датировки горных пород, остатков живых существ и исторических находок, с целью дальнейшего опровержения научных теорий, построенных с использованием такой датировки. (См., например, статьи Креационизм, Научный креационизм, Критика эволюционизма, Туринская плащаница).
Вариабельность постоянной распада для электронного захвата наблюдалась в эксперименте, но она лежит в пределах процента во всём доступном в лаборатории диапазоне давлений и температур. Период полураспада в этом случае изменяется в связи с некоторой (довольно слабой) зависимостью плотности волновой функции орбитальных электронов в окрестности ядра от давления и температуры. Существенные изменения постоянной распада наблюдались также для сильно ионизованных атомов (так, в предельном случае полностью ионизованного ядра электронный захват может происходить только при взаимодействии ядра со свободными электронами плазмы; кроме того, распад, разрешённый для нейтральных атомов, в некоторых случаях для сильно ионизованных атомов может быть запрещён кинематически). Все эти варианты изменения постоянных распада, очевидно, не могут быть привлечены для «опровержения» радиохронологических датировок, поскольку погрешность самого радиохронометрического метода для большинства изотопов-хронометров составляет более процента, а высокоионизованные атомы в природных объектах на Земле не могут существовать сколько-нибудь длительное время.
Поиск возможных вариаций периодов полураспада радиоактивных изотопов, как в настоящее время, так и в течение миллиардов лет, интересен в связи с гипотезой о вариациях значений фундаментальных констант в физике (постоянной тонкой структуры, константы Ферми и т. д.). Однако тщательные измерения пока не принесли результата — в пределах погрешности эксперимента изменения периодов полураспада не были найдены. Так, было показано, что за 4,6 млрд лет константа α-распада самария-147 изменилась не более чем на 0,75 %, а для β-распада рения-187 изменение за это же время не превышает 0,5 %[16]; в обоих случаях результаты совместимы с отсутствием таких изменений вообще.
См. также[править | править код]
- Время жизни квантовомеханической системы
- Ширина распада
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Richard A. Muller. Physics and Technology for Future Presidents : An Introduction to the Essential Physics Every World Leader Needs to Know : [англ.]. — Princeton, New Jercey : Princeton University Press, 2010. — С. 128—129. — 526 с. — ISBN 978-0-691-13504-5.
- ↑ 1 2 3 4 5 Климов А. Н. Глава 3. Ядерные превращения // Ядерная физика и ядерные реакторы. — М.: Энергоатомиздат, 1985. — С. 74—75. — 352 с.
- ↑ 1 2 3 4 Период полураспада. Энциклопедия физики и техники. Дата обращения: 18 ноября 2019. Архивировано 4 декабря 2019 года.
- ↑ 1 2 3 4 5 6 Б.С. Ишханов, И.М. Капитонов, Э.И. Кэбин. Период полураспада. Частицы и атомные ядра. Основные понятия. Кафедра общей ядерной физики физического факультета МГУ. Дата обращения: 18 ноября 2019. Архивировано 6 ноября 2019 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Carl R. (Rod) Nave. Radioactive Half-Life. HyperPhysics. Georgia State University (2016). Дата обращения: 22 ноября 2019. Архивировано 27 сентября 2017 года.
- ↑ 1 2 3 4 5 6 Б.С. Ишханов, И.М. Капитонов, Н.П. Юдин. Радиоактивность // Частицы и атомные ядра. — 2-е. — М. : Издательство ЛКИ. — Гл. 1. Элементарные частицы. — С. 18—21. — 584 с. — (Классический университетский учебник). — ISBN 978-5-382-00060-2.
- ↑ Такой же вид имеет зависимость от времени интенсивности (скорости) распада, то есть активности образца, и аналогичным образом через неё определяется период полураспада как промежуток времени, по истечении которого интенсивность распада снизится вдвое
- ↑ Фиалков Ю. Я. Применение изотопов в химии и химической промышленности. — К.: Техніка, 1975. — С. 52. — 240 с. — 2000 экз.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 Период полураспада радиоактивных элементов и их излучение (Таблица). infotables.ru – Справочные таблицы. Дата обращения: 6 ноября 2019. Архивировано 6 ноября 2019 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 Half Life for all the elements in the Periodic Table. periodictable.com. Дата обращения: 11 ноября 2019. Архивировано 24 марта 2019 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Kondev F. G., Wang M., Huang W. J., Naimi S., Audi G. The Nubase2020 evaluation of nuclear properties (англ.) // Chinese Physics C. — 2021. — Vol. 45, iss. 3. — P. 030001-1—030001-180. — doi:10.1088/1674-1137/abddae.
- ↑ 1 2 3 4 Radioactive isotope table. Caltech Astronomy Department. Дата обращения: 10 ноября 2019. Архивировано 31 октября 2019 года.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 Период полураспада Т1/2 некоторых радиоактивных изотопов (выборочно), калькулятор онлайн, конвертер. Калькулятор – справочный портал. Дата обращения: 7 ноября 2019. Архивировано 7 ноября 2019 года.
- ↑ Рекорды в науке и технике. Элементы. МОО “Наука и техника”. Дата обращения: 7 ноября 2019. Архивировано 7 ноября 2019 года.
- ↑ 1 2 3 4 5 6 7 8 M. P. Unterweger, D. D. Hoppes, F. J. Schima, and J. S. Coursey. Radionuclide Half-Life Measurements Data (англ.). NIST (6 сентября 2009). Дата обращения: 26 ноября 2019. Архивировано 3 февраля 2020 года.
- ↑ Jean-Philippe Uzan. The fundamental constants and their variation: observational status and theoretical motivations. Rev.Mod.Phys. 75(2003)403. arXiv: hep-ph/0205340 Архивная копия от 3 июня 2015 на Wayback Machine.
Ссылки[править | править код]
- Наглядное объяснение вероятностной природы экспоненциального распада и периода полураспада как его характеристики
Download Article
Download Article
- Understanding Half-Life
- Learning the Half-Life Equation
- Calculating from a Graph
- Using a Calculator
- Example Problems
- Video
- Expert Q&A
- Tips
|
|
|
|
|
|
|
The half-life of a substance undergoing decay is the time it takes for the amount of the substance to decrease by half. It was originally used to describe the decay of radioactive elements like uranium or plutonium, but it can be used for any substance which undergoes decay along a set, or exponential, rate. You can calculate the half-life of any substance, given the rate of decay, which is the initial quantity of the substance and the quantity remaining after a measured period of time.[1]
-
1
What is half-life? The term “half-life” refers to the amount of time that half of the starting substance takes to decay or change. It’s most often used in radioactive decay to figure out when a substance is no longer harmful to humans.[2]
- Elements like uranium and plutonium are most often studied with half-life in mind.
-
2
Does temperature or concentration affect the half-life? The short answer is no. While chemical changes are sometimes affected by their environment or concentration, each radioactive isotope has its own unique half-life that isn’t affected by these changes.[3]
- Therefore, you can calculate the half-life for a particular element and know for certain how quickly it will break down no matter what.
Advertisement
-
3
Can half-life be used in carbon dating? Yes! Carbon dating, or figuring out how old something is based on how much carbon it has, is a very practical way to use half-life. Every living thing intakes carbon while it’s alive, so when it dies, it has a certain amount of carbon in its body. The longer it decays, the less carbon is present, which can be used to date the organism based on carbon’s half-life.[4]
- Technically, there are 2 types of carbon: carbon-14, which decays, and carbon-12, which stays constant.
Advertisement
-
1
Understand exponential decay. Exponential decay occurs in a general exponential function
where
[5]
-
2
Rewrite the function in terms of half-life. Of course, our function does not depend on generic variable
but time
[6]
-
3
-
4
Solve for the half-life. In principle, the above formula describes all the variables we need. But suppose we encountered an unknown radioactive substance. It is easy to directly measure the mass before and after an elapsed time, but not its half-life. So, let’s express half-life in terms of the other measured (known) variables. Nothing new is being expressed by doing this; rather, it is a matter of convenience. Below, we walk through the process one step at a time.[8]
Advertisement
-
1
Read the original count rate at 0 days. Take a look at your graph and find the starting point, or the 0 day mark, on the x-axis. The 0 day mark is right before the material starts decaying, so it’s at its original point.[9]
- On half-life graphs, the x-axis will usually show the timeline, while the y-axis usually shows the rate of decay.
-
2
Go down half the original count rate and mark it on the graph. Starting from the top of the curve, note the count rate on the y-axis. Then, divide that number by 2 to get the number at the halfway point. Mark that point on the graph with a horizontal line.[10]
- For example, if the starting point is 1,640, divide 1,640 / 2 to get 820.
- If you are working with a semi log plot, meaning the count rate is not evenly spaced, you’ll have to take the logarithm of any number from the vertical axis.[11]
-
3
Draw a vertical line down from the curve. Starting from the halfway point that you just marked on the graph, draw a second line going downward until it touches the x-axis. Hopefully, the line will touch an easy-to-read number that you can identify.[12]
-
4
Read the half-life where the line crosses the time axis. Take a look at the point that your line touched and read where on the timeline it hits. Once you identify the point on your timeline, you’ve found your half-life.[13]
Advertisement
-
1
Determine 3 of the 4 relevant values. If you’re solving for half-life, you’ll need to know the initial quantity, the quantity that remains, and the time that has passed. Then, you can use any half-life calculator online to determine the half-life.[14]
- If you know the half-life but you don’t know the initial quantity, you can input the half-life, the quantity that remains, and the time that has passed. As long as you know 3 of the 4 values, you’ll be able to use a half-life calculator.
-
2
Calculate the decay constant with a half-life calculator. If you want to calculate how old an organism is, you can input the half-life and the mean lifetime to get the decay constant. This is a great tool to use for carbon dating or figuring out the lifespan of an organism.[15]
- If you don’t know the half-life but you do know the decay constant and the mean lifetime, you can input those instead. Just like the initial equation, you only need to know 2 of the 3 values to get the third one.
-
3
Plot your half-life equation on a graphing calculator. If you know your half-life equation and you want to graph it, open up your Y-plots and input the equation into Y-1. Then, hit “graph” to open up your graph and adjust the window until you can see the whole curve. Finally, move your cursor above and below the midpoint of the graph to get your half-life.[16]
- This is a helpful visual, and it can be useful if you don’t want to do all of the equation work.
Advertisement
-
1
Problem 1. 300 g of an unknown radioactive substance decays to 112 g after 180 seconds. What is the half-life of this substance?
-
2
Problem 2. A nuclear reactor produces 20 kg of uranium-232. If the half-life of uranium-232 is about 70 years, how long will it take to decay to 0.1 kg?
-
3
Problem 3. Os-182 has a half-life of 21.5 hours. How many grams of a 10.0 gram sample would have decayed after exactly 3 half-lives?[17]
-
4
Problem 4. A radioactive isotope decayed to 17/32 of its original mass after 60 minutes. Find the half-life of this radioisotope.[18]
Advertisement
Add New Question
-
Question
If a sample contains 100 g of a radioactive isotope that has a half-life of 2 days, how much of the isotope remains after 6 days?
Meredith Juncker is a PhD candidate in Biochemistry and Molecular Biology at Louisiana State University Health Sciences Center. Her studies are focused on proteins and neurodegenerative diseases.
Scientific Researcher
Expert Answer
Support wikiHow by
unlocking this expert answer.One quick way to do this would be to figure out how many half-lives we have in the time given.
6 days/2 days = 3 half lives
100/2 = 50 (1 half life)
50/2 = 25 (2 half lives)
25/2 = 12.5 (3 half lives)So 12.5g of the isotope would remain after 6 days.
-
Question
If the half-life of a material is 6 hours, how much material remains in 36 hours?
Meredith Juncker is a PhD candidate in Biochemistry and Molecular Biology at Louisiana State University Health Sciences Center. Her studies are focused on proteins and neurodegenerative diseases.
Scientific Researcher
Expert Answer
-
Question
What is the half-life of an isotope that decays to 25% of its original activity in 26.7 hours?
Since the whole is 100%, the first half-life would drop to 50% and then to 25%. Because it takes the isotope 26.7 hours to reach 25%, and there are only 2 halves from 100 to 25%, divide 26.7/2, and you’ll get 13.35 hours as the half life.
See more answers
Ask a Question
200 characters left
Include your email address to get a message when this question is answered.
Submit
Advertisement
Video
References
About This Article
Article SummaryX
To find the half life of a substance, or the time it takes for a substance to decrease by half, you’ll be using a variation of the exponential decay formula. Plug in ½ for a, use the time for x, and multiply the left side by the initial quantity of the substance. Rearrange the equation so that you’re solving for what the problem asks for, whether that’s half life, mass, or another value. Plug in the values you have and solve, writing the answer in seconds, days, or years. To see the half life equation and look at examples, read on!
Did this summary help you?
Thanks to all authors for creating a page that has been read 1,121,135 times.
Reader Success Stories
-
Georgy Komissarov
Mar 14, 2018
“I am an IB student and am in the process of completing my Math IA. I needed an example of application of number e.…” more
Did this article help you?
Основы химической кинетики.
Кинетика –
учение о скорости химических реакций
и её зависимости от различных параметров.
Скорость хим. реакции
зависит:
-
от природы
реагирующих веществ -
от концентрации
-
от условий протекания
(P,T,V,
примеси, катализаторы)
Химические реакции
гомогенные
гетерогенные
+ поверхность
(её состояния)
Лекция №8
Основы
химической кинетики.
Кинетика позволяет
устанавливать, с какой скоростью проходит
данное химическое превращение.
Одна из главных задач
– установить элементарные факторы
определения реакции.
Скорость реакции
количественно определяется по изменению
концентрации в единицу времени, в единицу
реагирующего пространства.

Средняя – изменение
концентрации Истинная – полный
дифференциал
за время
.
от концентрации по
времени.
На скорость гетерогенной
реакции влияет состояние границы
раздела.
Единица реакции
пространства – S.
На скорость гомогенной
реакции
Единица реакции
пространства – Vвесь
объем.
Закон
действующих масс.
Действующая масса –
масса вещества в ед. объема V(м3)
A+B=D
Согласно закону
действующих масс, скорость реакции при
постоянной температуре, пропорциональна
концентрации реагирующих веществ.
,
– концентрация
А+2В = АВ2
Кпр– константа
прямой реакции, учитывает природу
реагирующих веществ
Молекулярность.
Порядок реакции.
С точки зрения числа
частиц реакции имеют:
Молекулярность –
число частиц, одновременное соударение
которых вызывает активность химического
превращения.
Реакции бывают: одно-
, двух- , и трехмолекулярные.
1.
одномолекулярная
минус, т.к. скорость реакции убывает с
течением времени
2.
двухмолекулярная
Порядок реакции:
определяется как сумма показателей
степеней при концентрации реагирующих
веществ в законе действующих масс.
Двухмолекулярные
реакции, как правило, первого порядка
Химическая реакция
проходит по стадиям
трехмолекулярная реакция может быть
второго порядка.
1)
медл.
2)
быстр.
Общая скорость определяется медленной стадией Интегрирование дифференциальных уравнений скорости.
коэф-т
рассмотрим уравнение
при
(*)
можно
определить константу К одномолекулярной
реакции:
Введем понятие периодов
полураспада.
Период полураспада.
из уравнения (*) при
Период полураспада –
время протекания реакции,
при котором концентрация
веществ уменьшается в 2 раза.
период полураспада одномолекулярной
реакции.
Классификация реакций по степени сложности
-
изолированные
-
параллельные
-
последовательные
-
сопряженные
-
обратимые
-
необратимые
-
цепные
-
колебательные
* Изолированная реакция
– это такая реакция в результате
протекания которой получается один и
тот же вполне определенный продукт
*
протекать в двух и более направлениях.обычн. нагрев

медл. Нагрев

* Сопряженные реакции
– группа реакций, в которых одна реакция
индуцирует другую
*
– последовательная реакция. Реакции
идут одна за другой.
* Обратимые, необратимые
– могут протекать в одном и другом
направлении.
Е

необратимая
Соседние файлы в предмете Химия
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Период полураспада

3.9
Средняя оценка: 3.9
Всего получено оценок: 88.
3.9
Средняя оценка: 3.9
Всего получено оценок: 88.
Одним из важнейших параметров радиоактивного распада является параметр, называемый периодом полураспада. Рассмотрим это понятие более подробно.
Закон радиоактивного распада
Радиоактивность – это способность атомов некоторых веществ превращаться в атомы других веществ с испусканием γ-лучей, а также α- и β- частиц. Такой способностью обладают все элементы с номером 84 и более.
Распад атомов – это случайный процесс, но, если взять большое число атомов, то можно заметить, что скорость распада зависит только от количества атомов в пробе. Например, количество атомов Калия-42 (цифра означает массовое число изотопа) в пробе равно:
|
Часы |
Количество,% |
|
0 |
100 |
|
6 |
70.7 |
|
12 |
50.0 |
|
18 |
35.4 |
|
24 |
25.0 |
|
30 |
17.7 |
|
36 |
12.5 |
|
42 |
8.8 |
|
48 |
6.3 |
То есть, если массовая доля Калия-42 в пробе изначально была 100г, то за первые шесть часов она уменьшилась на 30г, а за восьмой шестичасовый период – только на 2,5г. Произошло это потому, что в пробе к этому времени стало значительно меньше атомов, скорость распада уменьшилась.
Если взять другое вещество, с другой скоростью распада, например, Йод-124, и замерить массовую долю Йода в пробе в те же моменты, получим следующую таблицу:
|
Часы |
Количество,% |
|
0 |
100 |
|
6 |
95.8 |
|
12 |
91.7 |
|
18 |
87.8 |
|
24 |
84.1 |
|
30 |
80.5 |
|
36 |
77.1 |
|
42 |
73.8 |
|
48 |
70.7 |
Сравнивая ее с предыдущей, можно отметить, что скорость распада у Йода-124 гораздо меньше, чем у Калия-42, однако, и для этого элемента за первый период распадается большее количество атомов, в последующие периоды – меньшее.
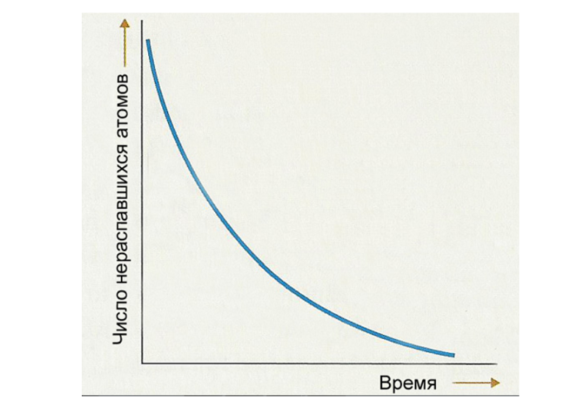
Таким образом, количество нераспавшегося вещества представляет собой бесконечно убывающую геометрическую прогрессию:
Это степенная функция с отрицательным показателем. В качестве основания функции удобно принять число 2. В результате закон, радиоактивного распада, выражающий, сколько атомов остается в пробе спустя время $t$, выражается формулой:
$$N=N_0×2^{-{1over T}t},$$
где:
- $t$ – прошедшее время,c;
- $N$ – оставшееся количество атомов;
- $N_0$ – начальное количество атомов в момент $t=0$.
- T – параметр интенсивности (период полураспада),c.
Период полураспада
В представленной формуле есть важный параметр $T$. Его физический смысл можно понять, если в принять $T=t$. В этом случае:
$$N=N_0×2^{-{1over T}t}=N_0×2^{-{Tover T}}={N_0over 2}$$
То есть, этот параметр представляет собой время, за которое распадется половина атомов исходного вещества. Он называется периодом полураспада. Подставляя в формулу период полураспада и текущее время, можно получать количество оставшихся атомов в данный момент времени.
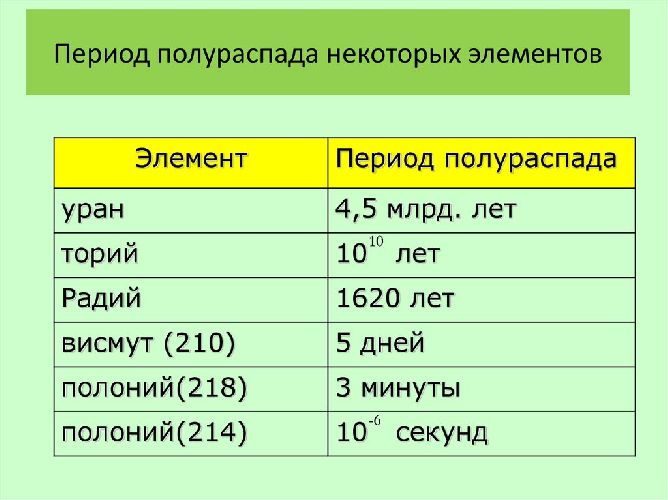
Все природные радиоактивные вещества – это изотопы с большими периодами полураспада, превышающими время жизни Солнечной системы. Изотопы с более короткими периодами к настоящему времени уже распались, и образуются только в результате распада более долгоживущих изотопов или в результате специальных реакций в ядерных реакторах. Наиболее длительный измеренный период полураспада имеет Теллур-128 – более $2×10^{24}$ лет, что намного больше больше, чем возраст Вселенной ($1.4×10^{10}$ лет).
Что мы узнали?
Доля атомов любых радиоактивных веществ, распадающихся за единицу времени постоянна (для каждого вещества – своя). Период полураспада – это время, за которое распадается половину исходных атомов.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
3.9
Средняя оценка: 3.9
Всего получено оценок: 88.
А какая ваша оценка?