Относительная плотность по… задачи
24-Фев-2013 | комментариев 26 | Лолита Окольнова
В ЕГЭ иногда встречаются задачи (часть С последнее задание), где в условии дана относительная плотность вещества по… водороду, кислороду, воздуху, азоту и т.д.
Например:
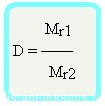
Относительная плотность вещества – отношение плотности вещества Б к плотности вещества А
Относительная плотность — величина безразмерная
Формула достаточно простая, и из нее вытекает другая формула —
Формула молярной массы вещества
Mr1 = D•Mr2
- Если дана относительная плотность паров по водороду, то Mr (вещества)=Mr(H2)•D=2 гмоль • D;
- если дана относительная плотность по воздуху, то Mr (вещества)=Mr(воздуха)•D=29 гмоль • D (обратите внимание, Mr(воздуха) принята равной 29 гмоль);
и т.д.
В условии задачи может быть полная формулировка — «относительная плотность (паров)…», а может быть просто «плотность вещества по…»
Давайте решим нашу задачу:
Дана плотность паров вещества по воздуху, значит, нам подходит формула молярной массы вещества —
Mr (вещества)=Mr(воздуха)•D=29 гмоль • D
Mr(вещества)=29 гмоль • 1.448 = 42 гмоль
Нам дан углеводород — СхHy, значит, мы можем найти Mr(Cx и Mr(Hy). Обратите внимание, именно молярные массы, т.к.у нас несколько атомов углерода и водорода.
Для этого надо молярную массу вещества умножить на процентное содержание элемента:
Mr(Cx)=Mr(вещества)•ω
Mr(Cx)= 42 гмоль · 0.8571=36 гмоль
x=Mr(Cx)Ar(C)=36 гмоль ÷ 12 гмоль =3.
Точно так же находим все данные для водорода:
Mr(Hy)=Mr(вещества)•ω
Mr(Hy)= 42 гмоль · 0.1429=6 гмоль
x=Mr(Hy)Ar(H)=6 гмоль ÷ 1 гмоль =6.
Искомое вещество — C3H6 — пропен.
Еще раз повторим определение —
Относительная плотность газа – это сравнение молярной или относительной молекулярной массы одного газа с аналогичным показателем другого газа.
Дана относительная плотность по аргону.
Mr (вещества)=Ar(Ar)•D
Mr (CxHy)=40 гмоль ·1.05=42 гмоль
Запишем уравнение горения:
СхHy + O2 = xCO2 + y2H2O
Найдем количество углекислого газа и воды:
n(CO2)=V22,4 лмоль = 33.622.4=1.5
n(H2O)=mMr=2718=1.5
Соотношение х : y2 как 1.5 : 1.5, т.е. y=2x, что соответствует общей формуле алкенов: CnH2n
Выражаем в общем виде молярную массу: Mr=Mr(C) + Mr(H)
12n +2n=42
n=3
Наше вещество — C3H6 — пропен
- pадание ЕГЭ по этой теме — задачи С5
Обсуждение: “Относительная плотность по… задачи”
(Правила комментирования)
From Wikipedia, the free encyclopedia
Vapour density is the density of a vapour in relation to that of hydrogen. It may be defined as mass of a certain volume of a substance divided by mass of same volume of hydrogen.
- vapour density = mass of n molecules of gas / mass of n molecules of hydrogen gas .
- vapour density = molar mass of gas / molar mass of H2
- vapour density = molar mass of gas / 2.016
- vapour density = 1⁄2 × molar mass
(and thus: molar mass = ~2 × vapour density)
For example, vapour density of mixture of NO2 and N2O4 is 38.3. Vapour density is a dimensionless quantity.
Alternative definition[edit]
In many web sources, particularly in relation to safety considerations at commercial and industrial facilities in the U.S., vapour density is defined with respect to air, not hydrogen.[1] Air is given a vapour density of one. For this use, air has a molecular weight of 28.97 atomic mass units, and all other gas and vapour molecular weights are divided by this number to derive their vapour density.[2] For example, acetone has a vapour density of 2[3] in relation to air. That means acetone vapour is twice as heavy as air. This can be seen by dividing the molecular weight of Acetone, 58.1[4] by that of air, 28.97, which equals 2.
With this definition, the vapour density would indicate whether a gas is denser (greater than one) or less dense (less than one) than air. The density has implications for container storage and personnel safety—if a container can release a dense gas, its vapour could sink and, if flammable, collect until it is at a concentration sufficient for ignition. Even if not flammable, it could collect in the lower floor or level of a confined space and displace air, possibly presenting an asphyxiation hazard to individuals entering the lower part of that space.
See also[edit]
- Relative density (also known as specific gravity)
- Victor Meyer apparatus
References[edit]
- ^ MSDS Glossary of Terms – Vapour Density. Msdsonline.com. Retrieved on 2012-02-09.
- ^ HazMat Math: Calculating Vapor Density Archived 2011-07-11 at the Wayback Machine. Firenuggets.com. Retrieved on 2012-02-09.
- ^ MSDS: Acetone. Hazard.com (1998-04-21). Retrieved on 2012-02-09.
- ^ NIOSH Pocket Guide: Acetone. Cdc.gov. Retrieved on 2012-02-09.
Как рассчитать относительную плотность паров химического вещества по воздуху? Есть какая-нибудь формула???
Алена Климчук
Ученик
(202),
закрыт
13 лет назад
Дополнен 13 лет назад
А плотность паров хлорэтана по воздуху какова???
Лучший ответ
Stone Angel
Гуру
(3022)
13 лет назад
Формула разумеется есть: D(по воздуху) =M(C2H5Cl)/M(воздух) =64.5г/моль: 29=2.224
M(C2H5Cl)=2Ar(C)+5Ar(H)+Ar(Cl)=12*2+5*1+35.5=64.5г/моль
*Средняя относительная молярная масса воздуха = 29
Остальные ответы
Art
Мыслитель
(5111)
13 лет назад
Вроде есть готовые коэффициенты
Оксана Иванова
Знаток
(378)
13 лет назад
По формуле R=M/V
Похожие вопросы
Плотность – физическая характеристика, присущая твердым, жидким и газообразным веществам.
В статье рассказывается о том, что такое плотность насыщенного пара, ее зависимость от различных условий среды. Дополнительно приведена таблица плотности по температуре, формула и примеры расчета этого параметра.
Содержание
- Что это за параметр, в чем измеряется, как обозначается?
- От чего зависит?
- Как изменяется при изменении температуры?
- Таблица зависимости
- Как определить?
- Формула и правила расчета
- Несколько примеров
- Где используют знания в жизни?
- Заключение
Что это за параметр, в чем измеряется, как обозначается?
Плотностью вещества называют физическую величину, которая указывает на отношение массы к занимаемому объему. Для насыщенного пара, простыми словами, это общее количество газа на единицу занимаемого им объема.
Единицей измерения плотности является кг/м3- килограмм на кубический метр (по системе СИ) или г/см3-грамм на кубический сантиметр (по системе СГС). Обозначается данная величина буквой «p».
Плотность насыщенного пара всегда приравнивается к уровню абсолютной влажности. Связано это с тем, что для данного вида пара свойственно насыщение молекулами воды, которые и повышают плотность.
От чего зависит?
Значение плотности насыщенных паров зависит от нескольких факторов:
Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.
-
Атмосферное давление. Чем оно выше, тем плотность меньше. Связано это с уменьшением числа свободных молекул, покидающих поверхность воды.
Также стоит учесть, что при снижении давления, плотность растет, так как снижается температура кипения, увеличивается парообразование и уровень насыщения.
- Температура внешней стенки (сосуда). Увеличивает конденсацию, снижает общую температуру жидкости, приводит к дисбалансу динамического равновесия. В следствии этих факторов, снижается плотность пара.
Также стоит учесть, что плотность насыщенного пара зависит от примесей других газов и твердых частиц в нем. Примеси снижают плотность самого пара, так как увеличивают конденсацию при сниженном уровне насыщения.
Как изменяется при изменении температуры?
Плотность насыщенного пара прямо зависит от температуры:
- При понижении температуры прослеживается уменьшение плотности. Связано это с тем, что замедляется процесс парообразования и насыщения пара. Молекулы воды теряют энергию и скорость выхода с поверхности воды, а значит перестают насыщать пар.
- При увеличении температуры плотность растет прямо пропорционально. Связано это с увеличением скорости насыщения среды до уровня 100%. При достижении этого уровня, наступает фазовый переход из газообразного состояния в жидкое (конденсация). Фазовый переход обусловлен термодинамическим равновесием между паром и водой. При таком условии, плотность стабилизируется без дальнейшего роста.
Рост и стабилизация плотности с увеличением температуры возможна только до температуры кипения воды. Дальнейший нагрев снижает плотность, так как выпаривает молекулы воды из пара, делая его перегретым.
Таблица зависимости
Зависимость плотности от температуры легко проследить по приведенной таблице:
| Температура °С | Плотность г/м3 |
| -30 | 0,3 |
| -20 | 0,8 |
| -10 | 2,1 |
| -5 | 3,6 |
| 0 | 4,8 |
| 3 | 6 |
| 4 | 6,4 |
| 5 | 6,8 |
| 10 | 9,4 |
| 11 | 10 |
| 12 | 10,6 |
| 13 | 11,3 |
| 14 | 12 |
| 15 | 12,8 |
| 16 | 13,6 |
| 17 | 14,4 |
| 18 | 15,3 |
| 19 | 16,3 |
| 20 | 17,3 |
| 21 | 18,3 |
| 22 | 19,4 |
| 23 | 20 |
| 24 | 21,7 |
| 25 | 23 |
| 30 | 30,4 |
| 35 | 39,6 |
| 40 | 51,2 |
| 45 | 65,4 |
| 50 | 82,8 |
| 55 | 104 |
| 60 | 129 |
| 65 | 160 |
| 70 | 196,4 |
| 75 | 239,3 |
| 80 | 289,7 |
| 85 | 348,7 |
| 90 | 417,3 |
| 95 | 496,4 |
| при 100 градусах Цельсия | 588,5 |
По таблице можно проследить рост плотности от отрицательной к положительной температуре.
Увеличение связано с ростом количества свободных молекул воды, насыщающих пар. При отрицательной температуре низкая плотность связана с кристаллизацией молекул воды и отсутствием конденсации.
Как определить?
Рассмотрим, как рассчитать параметр.
Формула и правила расчета
Для вычисления плотности вещества используется формула:
Выражение состоит из следующих значений:
- «p» — плотность вещества;
- «F» — абсолютная влажность воздуха (г/м3);
- «m» — его масса (грамм-килограмм);
- «V» — занимаемый объем (см3-м3).
Так как у насыщенного пара плотность связана с уровнем влажности, то данный параметр может быть рассчитан с использованием выражения:
Уравнение состоит из:
- «ф» — абсолютная влажность;
- «p» — плотность пара;
- «pо» — плотность насыщения;
- «100%» — относительная влажность.
При использовании формулы стоит учитывать зависимость плотности от температуры и использовать табличные значения этого параметра.
Несколько примеров
Формулу расчета плотности очень просто использовать для решения задач.
Задача:
- Масса водяного пара 250 г.
- Объем пара 300 м3.
- Плотность неизвестна.
Решение:
- P=m/v=грамм/м3.
- P=250/300=0,83 г/м3.
Ответ: плотность насыщенного пара, массой 250 г и объемом 300 м3 составляет 0,83 г/м3.
Задача:
- Масса водяного пара 700 г.
- Объем пара 150 м3.
- Плотность пара в кг/м3 неизвестна.
Решение:
- P=m/v=грамм/м3.
- P=700/150=4,66 г/м3 или 0,0046 кг/м3.
Ответ: плотность насыщенного пара массой 700 г и объемом 150 м3 составляет 0,0046 кг/м3
Где используют знания в жизни?

Метеорологи применяют расчет плотности для установления уровня насыщения атмосферы влагой.
Также расчет помогает контролировать испарения естественных источников в разные периоды года и устанавливать скорость испарения при различных температурах.
Инженеры применяют данные знания при проектировании:
- отопительных и охладительных систем,
- вентиляции,
- очистительного оборудования.
Плотность помогает рассчитать оптимальный уровень насыщения системы влагой.
Заключение
Плотность насыщенного пара имеет прямую зависимость от температуры, давления и наличия термодинамического равновесия с исходной водой.
Такая зависимость позволяет рассчитать климатические изменения в разный период, а также решить множество задач при проектировании климатических систем.
Вода – уникальное вещество, находящееся в трех состояниях в условиях Земли: твердом, жидком, газообразном. Пар – это вода в газообразной фазе. Он находится в подвижном равновесии с жидкой или твердой фракцией воды.
Читайте также: Какая скорость света?
Параметр плотности и единицы измерения пара
Образование пара с поверхности жидкой или твердой фракции называется испарением. Активное парообразование сопровождается обратным процессом конденсации – перехода из газообразного состояния в жидкое. Водяной пар не имеет вкуса, запаха.
Плотность вещества (ро, ) – это отношение его массы (m) к объему (V): = m / V. Этот показатель находится в прямой зависимости от температуры, изменяется с ее возрастанием и падением по определенным формулам, в зависимости от физических свойств вещества.
Измеряется этот параметр соответственно измерению массы и объема: кг/м
Измерение плотности пара при различных показателях среды имеет важное значение для развития теории термодинамики и применения ее на практике.
Сравнение плотности сухого воздуха и водяного пара
Сравнивать параметры сухого газа (например, воздуха) и пара имеет смысл в замкнутых сосудах.
Показатели сухого воздуха без частичек воды можно приравнять к идеальному газу. С возрастанием температуры количество молекул в ограниченном объеме не увеличивается. Значит, плотность газа в таких условиях будет постоянна при различной степени нагревания. При этом давление воздуха в замкнутом сосуде имеет линейную зависимость от температуры.
В замкнутом сосуде с насыщенным паром (имеющим соприкосновение с поверхностью жидкости) наблюдается противоположная картина. В сосуде имеется небольшое количество воды, из которого происходит испарение. При нагревании испарение становится более интенсивным, и концентрация молекул воды возрастает по экспоненциальной или логарифмической кривой. Как следствие, растет плотность пара, зависимая от концентрации.
В емкости с насыщенным паром, контактирующим с поверхностью воды, уравновешены процессы испарения и конденсации (превращение пара в жидкое состояние). При нагревании концентрация испаряющихся молекул стремительно возрастает. Происходит увеличение плотности и давления пара, при котором испарение и конденсация становятся более интенсивными.
Плотность насыщенного и ненасыщенного водяного пара — в чем разница?
Насыщенным считается пар, который постоянно контактирует с жидкой фракцией воды, постоянно пополняется из нее в закрытом сосуде. При этом наблюдается выравнивание числа испаряемых и конденсируемых молекул. С возрастанием температуры стремительно увеличивается плотность пара.
ВНИМАНИЕ: Давление насыщенного пара зависит от температуры и не зависит объема. Это объясняется активизацией конденсирования излишних молекул воды при уменьшении объема и возрастании давления.
Ненасыщенный пар образуется в открытом пространстве. Испаряемые молекулы воды разносятся на неограниченное расстояние, не создавая увеличение давления. Концентрация молекул в таком случае не увеличивается, плотность остается относительно стабильной. Поэтому конденсация значительно отстает от испарения, наступает при снижении температуры до точки росы.
СПРАВКА: Точкой росы называется температура, при которой ненасыщенный пар становится насыщенным. При такой температуре происходит конденсация жидкости из ненасыщенного модифицированного пара.
От чего зависит плотность и давление водяного пара?
Плотность вещества (в нашем варианте водяного пара) зависит от:
Количества молекул вещества (воды) в единице объема. Эта величина, в свою очередь, имеет зависимость:
от температуры;
давления.
Массы молекулы.
При нагревании газы стремятся к расширению. С увеличением температуры растет концентрация молекул воды, за счет испарения с поверхности жидкости. Если объем остается стабильным (в замкнутом пространстве, сосуде), то плотность пара возрастает.
При неизменной температуре увеличение давления сгущает концентрацию молекул. Их становится больше на единицу объема, поэтому плотность возрастает.
Масса молекул воды постоянна, поэтому для водяного пара плотность остается стабильной при неизменной температуре и постоянном давлении.
Таким образом, зависимость плотности пара от температуры можно выразить в формуле:
= n*k*T, где:
n – концентрация молекул;
k – постоянная, зависящая от массы молекулы (воды);
T – температура.
Что такое абсолютная плотность водяного пара?
Абсолютной плотностью пара принято считать показатель насыщенного пара в динамическом равновесии испарения и конденсации.
Плотность насыщенного пара при различных термических показателях варьирует, определяется по формуле:
= 216,49 * P / (Z * (T°+ 273)), где:
– плотность насыщенного пара в кг/м;
P – абсолютное давление в барах;
T° – температура в градусах Цельсия, изменяемая в шкалу Кельвина (+ 273);
Z – коэффициент, выражающий зависимость от способности сжатия насыщенного пара при показателе давления Р и температуре T°.
С абсолютной плотностью пара связано понятие абсолютной влажности воздуха. Значение абсолютной влажности отличается от плотности в связи с измерением ее согласно Международной метрической системе мер с коррекцией температуры по шкале Кельвина.
Как меняется плотность пара при изменении температуры?
Зависимость плотности пара от температуры прямая, но не линейная. Этим водяной пар отличается от сухого газа.
При достижении температуры, соответствующей точке росы, линейная зависимость плотности от температуры модифицируется в экспоненциальную (плотность стремительно растет до полного испарения зарезервированной воды). Когда вся жидкость переходит в газообразное состояние – линейная зависимость возобновляется. Эти переходы изображены на графике.
График зависимости плотности насыщенного пара от Т° при полном испарении воды (А–В – кривая зависимости насыщенного пара;
В–С – линейная зависимость ненасыщенного пара).
Таблица зависимости плотности паров от температуры
| Т°, °С | Плотность кг/м | Плотность г/м | Плотность г/см |
| 110 | 0,826 | 826 | 0,000826 |
| 100 | 0,597 | 597 | 0,000597 |
| 80 | 0,2929 | 292,9 | 0,0002929 |
| 60 | 0,1301 | 130,1 | 0,0001301 |
| 30 | 0,03037 | 30,37 | 0,00003037 |
| 25 | 0,02309 | 23,09 | 0,00002309 |
| 20 | 0,01729 | 17,29 | 0,00001729 |
| 17 | 0,01453 | 14,53 | 0,00001453 |
| 15 | 0,01280 | 12,8 | 0,0000128 |
| 10 | 0,00939 | 9,39 | 0,00000939 |
| 0 | 0,00484 | 4,84 | 0,00000484 |
ОСОБЕННОСТИ: При низком давлении и высокой температуре свойства пара модифицируются по подобию со свойствами идеального газа.
Пошаговая инструкция как определить плотность водяного пара
Задача 1. Как измерить относительную плотность водяного пара при снижении температуры до 10° С, если известно, что в 1 м воздуха 20°С содержится 13 г газообразной воды?
Для выполнения задачи необходимо воспользоваться экспериментальными таблицами зависимости плотности от давления и температуры.
Если при температуре 20° С плотность насыщенного водяного пара 17,3 г/м, то относительная плотность пара при 13 г/м рассчитывается по формуле пропорции:
100% – 17,3
Х – 13
Х = 100*13 / 17,3 = 75%.
При снижении температуры до 10°С относительная плотность водяного пара рассчитывается по новой пропорции:
100% – 9,39
Х – 13
Х = 100*13 / 9,39 = 138,4%.
Ответ: относительная плотность пара при Т°=10, массе воды 13 г равна 138,4%.
Интерпретация результата: при снижении температуры до 10° относительная плотность пара приведет к процессу усиленной конденсации и превышению над испарением. В этом случае в природе наблюдаются обильные осадки.
Задача 2. Расчет относительной плотности углекислого газа по воздуху.
Для решения необходимо соотнести массу молекулы СО с таковой воздуха:
Хair(CO) = М(СО) / М(air).
С учетом содержания в воздухе смеси газов кислорода, водорода, азота и других, молекулярную массу воздуха принимают как 29.
Молекулярная масса углекислого газа вычисляется по формуле суммы атомных масс:
М(СО) = А(С)+ 2А(О) = 12 + 2*16 = 44.
Результат:
Хair(CO) = М(СО) / М(air) = 44 / 29 = 1,52.
Ответ: относительная плотность углекислого газа по отношению к воздуху – 1,52.
Где используют знания о плотности насыщенного пара на практике?
Теория термодинамики водяного пара очень полезна для систем обогрева в различных хозяйственных отраслях. Соотношение варьирования плотности и температуры при парообразовании и конденсации создает условия для перемещения бльших масс насыщенного пара в трубах и резервуарах.
Термодинамические свойства пара используются:
в системах парового обогрева для отопления высотных домов;
в системах теплоизоляции;
в котельнях различного назначения;
для обеспечения циркуляции воздуха в теплицах, парниках;
в паровых двигателях;
паровых турбинах для производства электрической энергии на ТЭЦ, ТЭС, ГРЭС, АЭС.
Заключение
Свойства водяного пара интенсивно изучаются на протяжении столетий и продолжаются в настоящее время. Взаимозависимость плотности, давления, температуры открывает возможности применения газообразного состояния воды, которое таит в себе потенциал новой еще не познанной информации.


 Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.
Температура. С ее повышением увеличивается плотность пара, так как прослеживается рост числа молекул насыщения.

