Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 4 марта 2023 года; проверки требуют 4 правки.
Запрос «pH» перенаправляется сюда; см. также другие значения.

Водоро́дный показа́тель[1] (pH, от лат. pondus Hydrogenii[2] — «вес водорода»; произносится «пэ-аш») — мера кислотности водных растворов. Является способом выражения активности катионов водорода в растворах. Противоположна по знаку и равна по модулю десятичному логарифму активности (а) катионов водорода (Н+), выраженной в молях на литр, которую в сильно разбавленных растворах можно считать равной их равновесной молярной концентрация ([H+])[3]:
![{displaystyle mathrm {pH} =-lg(a_{mathrm {H^{+}} })thickapprox -lg([mathrm {H^{+}} ])}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fcfa999a67f799b196ed3ea9360602a68b0ebb51)
Для водных растворов (при стандартных условиях):
pH < 7 соответствует кисло́тному раствору;
pH = 7 соответствует нейтра́льному раствору, иногда относят к кислотному;
pH > 7 соответствует осно́вному раствору![]() .
.
Водородный показатель может быть определён с помощью кислотно-основных индикаторов, измерен потенциометрическим pH-метром.
Точное измерение и регулирование pH необходимо в различных отраслях химии, биологии, наук о материалах, технологий, медицины и агрономической химии[⇨].
История[править | править код]
Это понятие было введено в 1909 году датским химиком Сёренсеном. Показатель называется pH, по первым буквам латинских слов potentia hydrogenii — сила водорода, или pondus hydrogenii — вес водорода. Вообще в химии сочетанием pX принято обозначать величину, равную −lg X. Например, силу кислот часто выражают в виде pKa = −lg Ka.
В случае pH буква H обозначает концентрацию ионов водорода (H+), или, точнее, термодинамическую активность гидроксоний-ионов.
Уравнения, связывающие pH и pOH[править | править код]
Вывод значения pH[править | править код]
В чистой воде концентрации ионов водорода ([H+]) и гидроксид-ионов ([OH−]) одинаковы и при 22 °C составляют по 10−7 моль/л, это напрямую следует из определения ионного произведения воды, которое равно [H+] · [OH−] и составляет 10−14 моль2/л2 (при 25 °C).
Когда концентрации обоих видов ионов в растворе одинаковы, говорят, что раствор имеет нейтральную реакцию. При добавлении к воде кислоты концентрация ионов водорода увеличивается (на самом деле увеличивается не концентрация собственно ионов — иначе как способность кислот «присоединять» ион водорода могла бы приводить к этому — а концентрация именно таких соединений с «присоединённым» к кислоте ионом водорода), а концентрация гидроксид-ионов соответственно уменьшается, при добавлении основания — наоборот, повышается содержание гидроксид-ионов, а концентрация ионов водорода падает. Когда [H+] > [OH−], говорят, что раствор является кислотным, а при [OH−] > [H+] — осно́вным.
Для удобства представления, чтобы избавиться от отрицательного показателя степени, вместо концентрации ионов водорода используют её взятый с обратным знаком десятичный логарифм, который, собственно, и является водородным показателем — pH.
pOH[править | править код]
Несколько меньшее распространение получила обратная pH величина — показатель осно́вности раствора, pOH, равная отрицательному десятичному логарифму концентрации в растворе ионов OH−:
Так как в любом водном растворе при 25 °C ![[text{H}^+] [text{OH}^-] = 1{,}0 cdot 10^{-14}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fe924dbdb08faab9bd9648694c422ee5b5a9b5a1)
Значения pH в растворах различной кислотности[править | править код]
| Вещество | pH | Цвет индикатора |
|---|---|---|
| Геотермальная вода у вулкана Даллол | ≈ 0 | |
| Электролит в свинцовых аккумуляторах | <1,0 | |
| Желудочный сок | 1,0–2,0 | |
| Лимонный сок (5 % р-р лимонной кислоты) | 2,0±0,3 | |
| Пищевой уксус | 2,4 | |
| Яблочный сок | 3,0 | |
| Кока-кола | 3,0±0,3 | |
| Кофе | 5,0 | |
| Чай, шампунь, кожа здорового человека | 5,5 | |
| Кислотный дождь, моча | < 5,6 | |
| Питьевая вода | 6,5–8,5 | |
| Молоко | 6,6–6,93 | |
| Слюна | 6,8–7,4 [4] | |
| Чистая вода при 25 °C | 7,0 | |
| Кровь | 7,36–7,44 | |
| Морская вода | 8,0 | |
| Мыло (жировое) для рук | 9,0–10,0 | |
| Нашатырный спирт | 11,5 | |
| Отбеливатель (хлорная известь) | 12,5 | |
| Концентрированные растворы щелочей | >13 |
Так как при 25 °C (стандартных условиях) [H+] · [OH−] = 10−14, то понятно, что при этой температуре pH + pOH = 14.
Так как в кислотных растворах [H+] > 10−7, то у кислотных растворов pH < 7, аналогично, у осно́вных растворов pH > 7, pH нейтральных растворов равен 7. При более высоких температурах константа электролитической диссоциации воды повышается, соответственно увеличивается ионное произведение воды, поэтому нейтральной оказывается pH < 7 (что соответствует одновременно возросшим концентрациям как H+, так и OH−); при понижении температуры, напротив, нейтральная pH возрастает.
Связь pKa и pH[править | править код]

Уравнение Гендерсона-Хассельбахa[править | править код]
![{displaystyle {ce {pH}}=mathrm {p} K_{mathrm {a} }+lg left(mathrm {frac {[A^{-}]}{[HA]}} right)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9629f69c46b4bc19ae8dc5247fdebd352c49a47e)
Методы определения значения pH[править | править код]
Для определения значения pH растворов широко используют несколько методик. Водородный показатель можно приблизительно оценивать с помощью индикаторов, точно измерять pH-метром или определять аналитически путём, проведением кислотно-осно́вного титрования.
- Для грубой оценки концентрации водородных ионов широко используются кислотно-осно́вные индикаторы — органические вещества-красители, цвет которых зависит от pH среды. К наиболее известным индикаторам принадлежат лакмус, фенолфталеин, метиловый оранжевый (метилоранж) и другие. Индикаторы способны существовать в двух по-разному окрашенных формах — либо в кислотной, либо в осно́вной. Изменение цвета каждого индикатора происходит в своём интервале кислотности, обычно составляющем 1-2 единицы.
- Для расширения рабочего интервала измерения pH используют так называемый универсальный индикатор, представляющий собой смесь из нескольких индикаторов. Универсальный индикатор последовательно меняет цвет с красного через жёлтый, зелёный, синий до фиолетового при переходе из кислотной области в осно́вную. Определения pH индикаторным методом затруднено для мутных или окрашенных растворов.
- Использование специального прибора — pH-метра — позволяет измерять pH в более широком диапазоне и более точно, чем с помощью индикаторов. Ионометрический метод определения pH основывается на измерении милливольтметром-ионометром ЭДС гальванической цепи, включающей специальный стеклянный электрод, потенциал которого зависит от концентрации ионов H+ в окружающем растворе. Способ отличается удобством и высокой точностью, особенно после калибровки индикаторного электрода в избранном диапазоне pH, позволяет измерять pH непрозрачных и цветных растворов и потому широко используется.
- Аналитический объёмный метод — кислотно-осно́вное титрование — также даёт точные результаты определения кислотности растворов. Раствор известной концентрации (титрант) по каплям добавляется к исследуемому раствору. При их смешивании протекает химическая реакция. Точка эквивалентности — момент, когда титранта точно хватает, чтобы полностью завершить реакцию, — фиксируется с помощью индикатора. Далее, зная концентрацию и объём добавленного раствора титранта, вычисляется кислотность раствора.
- При отсутствии инструментальных средств определения рН могут быть использованы водные экстракты антоцианов — пигментов растений, окрашивающих цветки, плоды, листья, стебли. Основа их строения — катион флавилия, у которого кислород в пирановом кольце свободновалентен. Например, цианидин имеет красновато-фиолетовый цвет, однако цвет меняется с изменением рН: растворы имеют красный цвет при рН<3, фиолетовый при рН 7-8 и голубой при рН>11. Обычно в кислоте антоцианы имеют красный цвет различной интенсивности и оттенков, а в щелочной — синий. Такие изменения в окраске антоцианов можно наблюдать, добавляя кислоту или щелочь к окрашенному соку смородины, вишни, столовой свёклы или краснокочанной капусты[5].
Влияние температуры на значения pH[править | править код]
Влияние температуры на значения pH объясняется различной диссоциацией ионов водорода (H+) и не является ошибкой эксперимента. Температурный эффект невозможно компенсировать за счет электроники pH-метра.
Роль pH в химии и биологии[править | править код]
Кислотность среды имеет важное значение для множества химических процессов, и возможность протекания или результат той или иной реакции часто зависит от pH среды. Для поддержания определённого значения pH в реакционной системе при проведении лабораторных исследований или на производстве применяют буферные растворы, которые позволяют сохранять практически постоянное значение pH при разбавлении или при добавлении в раствор небольших количеств кислоты или щёлочи.
Водородный показатель pH широко используется для характеристики кислотно-осно́вных свойств различных биологических сред.
Кислотность реакционной среды особое значение имеет для биохимических реакций, протекающих в живых системах. Концентрация в растворе ионов водорода часто оказывает влияние на физико-химические свойства и биологическую активность белков и нуклеиновых кислот, поэтому для нормального функционирования организма поддержание кислотно-осно́вного гомеостаза является задачей исключительной важности. Динамическое поддержание оптимального pH биологических жидкостей достигается благодаря действию буферных систем организма.
В человеческом организме в различных органах водородный показатель различен. Нормальный pH крови составляет 7,36, то есть кровь имеет слабоосновную реакцию (с колебаниями от 7,34 у венозной крови до 7,40 у артериальной). В зависимости от биохимических изменений в крови может наблюдаться ацидоз (увеличение кислотности) или алкалоз (увеличение осно́вности), однако совместимый с жизнью диапазон pH крови невелик, поскольку уже при уменьшении pH до 6,95 наступает потеря сознания, а смещение реакции крови в щелочную сторону до pH = 7,7 вызывает тяжелейшие судороги. Поддержание кислотно-основного баланса крови в допустимых пределах осуществляется буферными системами крови, главной из которых является гемоглобиновая[6]. Нормальный водородный показатель желудочного сока (в просвете тела желудка натощак) равен 1,5…2,0[7]. У сока тонкой кишки pH в норме составляет 7,2…7,5, при усилении секреции достигает 8,6[8]. pH содержимого толстого кишечника может варьировать в норме от 6,0 до 7,2 единиц и зависит прежде всего от уровня продукции жирных кислот его микробиотой[9].
Примечания[править | править код]
- ↑ Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1 (Абл-Дар). — 623 с.
- ↑ история термина спорна
- ↑ The International Union of Pure and Applied Chemistry (IUPAC). IUPAC – pH (P04524). goldbook.iupac.org. Дата обращения: 20 марта 2023.
- ↑ Кислотность (pH) // Функциональная гастроэнтерология : сайт. Архивировано 9 мая 2013 года.
- ↑ Л.А.Красильникова. Биохимия растений. — 2004. — С. 163—164.
- ↑ Физиология человека. Под редакцией В. М. Покровского, Г. Ф. Коротько. Физико-химические свойства крови. Архивная копия от 15 августа 2019 на Wayback Machine
- ↑ Физиология человека. Под редакцией В. М. Покровского, Г. Ф. Коротько. Секреторная функция желудка Архивная копия от 15 августа 2019 на Wayback Machine
- ↑ Физиология человека. Под редакцией В. М. Покровского, Г. Ф. Коротько. Кишечная секреция Архивная копия от 13 августа 2019 на Wayback Machine.
- ↑ Akinori Osuka, Kentaro Shimizu, Hiroshi Ogura, Osamu Tasaki, Toshimitsu Hamasaki. Prognostic impact of fecal pH in critically ill patients // Critical Care. — 2012. — Т. 16, вып. 4. — С. R119. — ISSN 1364-8535. — doi:10.1186/cc11413. Архивировано 11 февраля 2021 года.
Литература[править | править код]
- Бейтс Р. Определение pH. Теория и практика / пер. с англ. под ред. акад. Б. П. Никольского и проф. М. М. Шульца. — 2 изд. — Л. : Химия, 1972.
Ссылки[править | править код]
- Водородный показатель pH. Таблицы показателей pH. Архивная копия от 14 января 2020 на Wayback Machine
Загрузить PDF
Загрузить PDF
В быту под pH подразумевают обычно шкалу, используемую для описания нейтральности или, наоборот, недостатка нейтральности того или иного вещества. В научном значении величина pH соответствует количеству ионов в химическом растворе. Если вы изучаете химию или связанные с ней предметы, вам может понадобиться рассчитать уровень pH, основываясь на концентрации веществ в растворе. Значение pH находится по следующей формуле: pH = -lg[H3O+].
-

1
Ознакомьтесь с понятием pH. Величина pH соответствует концентрации ионов водорода в растворе. Раствор с повышенной концентрацией ионов водорода называется кислотным, а раствор с пониженной концентрацией этих ионов – щелочным.[1]
Ионы водорода кратко обозначают как H+. Их можно представлять и в составе соединения, тогда они называются гидроксонием и записываются как H30+.- Ознакомьтесь со шкалой pH. Значения на шкале pH изменяются от 1 до 14. Чем меньше число, тем более кислотным является данный раствор. И наоборот, чем выше значение, тем более щелочным является раствор.[2]
Например, pH апельсинового сока составляет 2, поскольку этот сок представляет собой довольно кислотную жидкость. У хлорного отбеливателя pH равно 12, так как в нем много щелочи.[3]
В середине шкалы располагаются относительно нейтральные растворы, такие как вода, pH которой составляет 7. - Разница между двумя растворами на 1 пункт по шкале pH означает, что они различаются по кислотности в 10 раз. Например, если взять два раствора со значениями pH 6 и 7, кислотность первого раствора с pH 6 будет выше кислотности второго раствора с pH 7 в 10 раз. А, например, кислотность раствора с pH 6 выше кислотности раствора с pH 8 в 100 раз.[4]
- Ознакомьтесь со шкалой pH. Значения на шкале pH изменяются от 1 до 14. Чем меньше число, тем более кислотным является данный раствор. И наоборот, чем выше значение, тем более щелочным является раствор.[2]
-

2
Запомните уравнение для определения pH. Шкала pH вычисляется с помощью отрицательного десятичного логарифма. Отрицательный десятичный логарифм соответствует числу нулей, стоящих перед единицей, включая и ноль целых: например, отрицательный десятичный логарифм числа 0,1 равен 1, числа 0,01 — 2, и так далее.[5]
Формула для нахождения pH выглядит следующим образом: pH = -lg[H3O+].- Иногда формулу записывают в виде pH = -lg[H+]. Неважно, стоит ли в уравнении H3O+ или H+, обе формы записи равноценны.
- Для нахождения pH необязательно уметь рассчитывать десятичный логарифм, так как практически в каждом научном или инженерном калькуляторе есть опция его вычисления.
-

3
Ознакомьтесь с понятием концентрации. Концентрация какого-либо вещества соответствует числу частиц этого вещества, присутствующих в растворе.[6]
Как правило, концентрация выражается в количестве молей на единицу объема и обозначается как m/V, или M. В химических лабораториях концентрации растворов пишут на бутылках с ними. Если вы решаете химическую задачу, концентрация может быть дана в условии, либо ее требуется найти.Реклама
-

1
Вспомните формулу для нахождения pH. Вот эта формула: pH = -lg[H3O+].[7]
Убедитесь в том, что вы знакомы со всеми элементами, входящими в данную формулу. Посмотрите, какая величина соответствует концентрации.- В химии квадратные скобки означают концентрацию чего-либо. Так что формула для расчета pH читается как «pH равно отрицательному логарифму концентрации гидроксоний-ионов».
-

2
Определите действительную концентрацию. Внимательно прочитайте условие задачи. Найдите в исходных данных концентрацию кислоты или щелочи. Запишите полную формулу на листке бумаги, подставив в нее известные величины.[8]
Чтобы не возникло путаницы, рядом с числами всегда указывайте единицы измерения.- Например, если концентрация составляет 1,05 x 105 M, запишите формулу для расчета pH в следующем виде: pH = -lg[1,05 x 105 M]
-

3
Вычислите pH. Для этого удобно использовать научный калькулятор. Сначала введите знак минуса, нажав кнопку «+/-». Затем нажмите кнопку «log», соответствующую десятичному логарифму (в английском языке десятичный логарифм обозначается как log). На экране отобразится «-log».[9]
Затем нажмите левую скобку и введите концентрацию. При необходимости не забудьте указать значение степени.[10]
После этого закройте скобки.[11]
В результате на экране калькулятора вы увидите «-log(1,05×105). Нажмите «=». У вас должно получиться значение pH, приблизительно равное 4,98.Реклама
-

1
Определите, что дано и что требуется найти. Запишите формулу для вычисления pH. После этого выясните известные величины, выписав их значения под формулой. Например, если известно, что pH равно 10,1, запишите это число под pH в формуле.
-

2
Преобразуйте формулу. При этом вам понадобятся знания из школьного курса алгебры. Для вычисления концентрации по известному значению pH необходимо преобразовать формулу так, чтобы концентрация обособленно стояла с какой-либо из двух сторон уравнения. То есть необходимо, чтобы по одну сторону знака равенства было выражение, содержащее величину pH, а по другую — концентрация гидроксония. Сначала умножьте обе части уравнения на -1. Затем возведите 10 в степени, стоящие по обе стороны получившегося равенства.
- Преобразовывая равенство pH = -log[H3O+], получаем формулу +[H3O+] = 10-pH, то есть концентрация ионов равна десяти в степени -pH. Теперь вместо pH подставляем известное значение, в нашем случае 10,1.
-

3
Решите уравнение. Для возведения десяти в степень в калькуляторе предусмотрена определенная процедура. Сначала наберите 10. Затем нажмите клавишу возведения в степень «EXP». Введите знак минуса и значение степени. Нажмите «=».
- В нашем примере pH равно 10,1. Наберите «10» и нажмите клавишу «EXP». После этого нажмите «-/+», меняя знак. И наконец, введите значение pH «10,1» и нажмите клавишу «=». В результате у вас должно получиться 1e-100. Это означает, что концентрация составляет 1,00 x 10-100 M.
-

4
Обдумайте полученный ответ. Имеет ли он физический смысл? Если pH равно 10,1, это значит, что концентрация гидроксония чрезвычайно мала, и у вас щелочной раствор.[12]
Таким образом, найденная очень низкая концентрация соответствуетРеклама
Советы
- Если вычисление уровня pH поначалу кажется вам трудным, не забывайте, что существует множество источников, позволяющих больше узнать об этом вопросе. Воспользуйтесь учебником химии или попросите преподавателя помочь вам.
Реклама
Об этой статье
Эту страницу просматривали 129 928 раз.
Была ли эта статья полезной?

Теоретические основы
Вода является средой, в которой растворяются органические и неорганические химические вещества, и обладает способностью распадаться на ионы. Одна молекула отдает свой протон другой, поэтому в воде постоянно находится некоторое количество положительно заряженных ионов водорода H и отрицательно заряженных гидроксид-ионов OH. Этот процесс называется электролитической диссоциацией.
Говоря об ионе водорода, делается упрощение, так как на самом деле положительно заряженный ион в воде — это ион гидроксония H3O. Он образуется из целой молекулы воды и протона, оторванного от другой молекулы. Чем больше таких ионов в воде, тем больше и ее кислотность.
Ионы очень подвижны и постоянно переходят от одной молекулы к другой. Таким образом, процесс распада и процесс соединения в новую молекулу идут постоянно и уравновешивают друг друга, т. е. диссоциация воды находится в равновесии.

Количество ионов H+ и мера их активности в большинстве растворов очень малы, их записывают в виде числа с отрицательной степенью, что очень неудобно. Поэтому датским биохимиком Сёреном Сёренсеном в 1909 году было предложено выражать это число в виде показателя кислотности (водородного показателя) pH, который вычисляется как десятичный логарифм от меры активности ионов H+ с обратным знаком: pH = – lg [H+].
С. Сёренсен руководил химико-физиологической лабораторией при пивоваренном заводе Carlsberg, где разработал шкалу для измерения показателя pH. На ее основе были созданы специальные приборы: pH-метры, которые применяются для измерения кислотности растворов и жидкостей в промышленности, и ацидогастрометры для диагностики желудочно-кишечных заболеваний в медицине.
Показатель основности раствора, выражающийся десятичным логарифмом с отрицательным знаком от концентрации в растворе гидроксид-ионов: pOH = – lg [OH-], применяется гораздо реже. Величины pH и pOH могут быть как положительными, так и отрицательными.
Важно не путать pH с понятиями кислотности и щелочности. Главное различие заключается в том, что pH — это показатель не количества, а активности.
Он отражает степень кислотности или щелочности среды, а не количественное содержание в воде химических веществ. В разбавленных растворах мера активности эквивалентна концентрации, поэтому при определенном допущении один термин заменяют другим.
Влияние pH на свойства среды
С помощью несложных математических вычислений можно доказать, что сумма показателей pH и pOH для воды — величина постоянная и равна 14. Например, если рН = 5, то рОН = 9; для рН = -2 pOH = 16. У чистой воды без примесей (дистиллированной) и у водных растворов, образуемых неэлектролитами, pH = 7, а значит и рОН = 7, т. е. кислотный и основной (щелочной) показатели уравновешивают друг друга, и получается нейтральная среда.

При попадании в воду многих химических соединений происходит их гидролиз. Растворяемое вещество распадается на катионы и анионы, которые могут соединяться с ионами, получившимися в результате диссоциации воды. При этом получается смещение равновесия диссоциации воды. Показатель pH определяет, в какую сторону оно произошло. Если pH < 7, то получилась кислотная среда, когда pH > 7 — щелочная.
Показатель pH влияет на протекание химических реакций как на производстве, так и в природе и является универсальным показателем состояния среды. С помощью его контроля производят все виды горючего, краски, удобрения, средства личной гигиены и косметику. В пищевой промышленности проверяется качество изготовления напитков, молокопродуктов, изделий из злаков. Все живые обитатели природных почв и вод могут жить только при определенных значениях водородного показателя, от него же зависит и урожайность многих растений, поэтому ведется наблюдение за pH в почвоведении и земледелии, особенно в гидропонике.
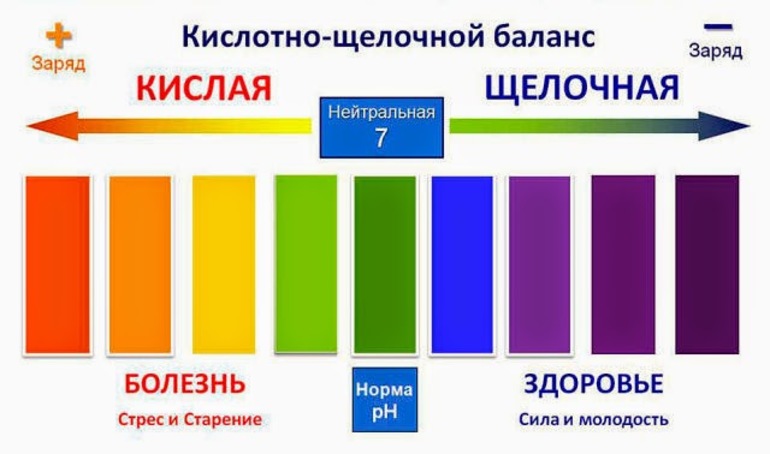
При этом обычно необходимо поддерживать постоянное значение pH в течение длительного времени. Для этого используют так называемые буферные растворы. Они представляют собой смеси слабого основания и его соли или слабой кислоты и ее соли, в которых мера активности ионов водорода постоянна и устойчива.
Измерение водородного показателя
Формулы для расчета pH зависят от того, к какому классу относится химическое вещество, входящее в исследуемый раствор, и приведены в специальных справочниках. Более точное значение получают другими методами. Цели и условия проведения исследований определяют, как будет измеряться водородный показатель.
Индикаторные способы
Приблизительно оценить меру активности ионов водорода можно с помощью кислотно-основных индикаторов. Такие вещества обычно относятся к органическим соединениям и имеют свойство изменять свой цвет в разных средах:

- Лакмус меняет цвет от красного в кислой среде через фиолетовый в нейтральной до синего в щелочной.
- Фенолфталеин становится синим в щелочной среде, оставаясь бесцветным в остальных.
- Метилоранж розового цвета соответствует повышенной кислотности, оранжевого — показывает нейтральность среды, в щелочах становится синим.
Изменение происходит для каждого индикатора в своём диапазоне кислотности, обычно составляющем 1—2 единицы. При этом методе результат можно получить быстрый и наглядный при небольших затратах, но недостаточно точный, с большой погрешностью при исследовании очень слабых растворов, окрашенных или мутных вод. Используется, когда нужно найти предварительное определение pH.

Более широкий диапазон и выше точность у универсального индикатора. Он соединяет в себе несколько индикаторов и градуируется в соответствии со значениями pH от единицы до десяти. Соответствие значения водородного показателя и цвета:
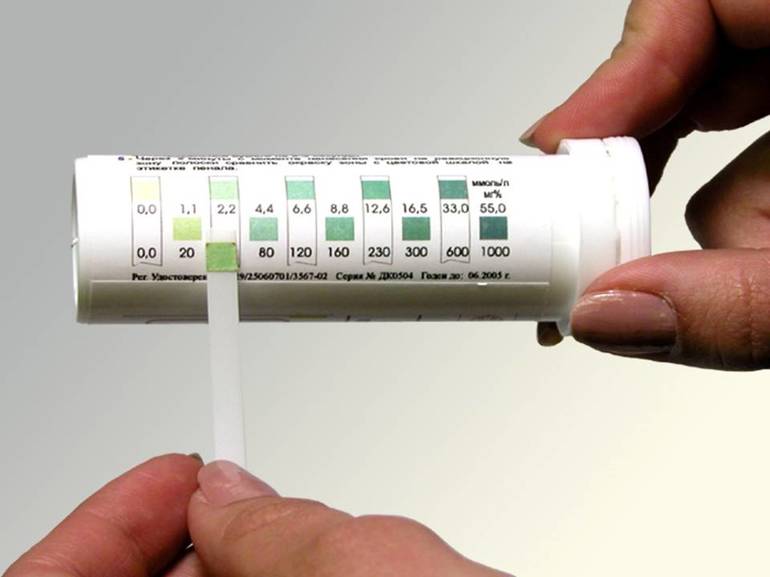
- 1 — красный;
- 2 — розовато-оранжевый;
- 3 — оранжевый;
- 4 — темно-желтый;
- 5 — желтый;
- 6 — желтовато-зеленый;
- 7 — светло-зеленый;
- 8 — насыщенный зеленый;
- 9 — сине-зеленый;
- 10 — сине-серый.
Аналитический объемный метод
Кислотно-основное титрирование — метод определения водородного показателя среды с помощью так называемых титрантов. В основном для этого используются сильные кислоты (серная, соляная) и сильные щелочи (едкий калий, каустическая сода).

Раствор-титрант добавляют в исследуемую жидкость по каплям. При этом они вступают в химическую реакцию. Когда она завершается, наступает точка эквивалентности, т. е. момент отчетливого изменения окраски исследуемого раствора. По установленному в результате опыта объему титранта, необходимому для получения точки эквивалентности, и известному значению его концентрации можно рассчитать pH с высокой точностью.
Измерительный прибор pH-метр
Ионометрический метод, при котором кислотный показатель можно измерить с помощью специализированного прибора — pH-метра, является наиболее точным (до сотых от единицы pH), удобным и имеет широкий диапазон измерения. PH-метр представляет собой милливольтметр, способный измерять разность потенциалов со стеклянных электродов. У него также есть система пересчета напряжения в pH.

В исследуемый раствор погружают индикаторный электрод и электрод сравнения, замыкая таким образом гальваническую цепь. Величина электродвижущей силы в ней зависит от активности ионов H+ в растворе, т. е. является функцией только его pH. Индикаторный электрод состоит из стеклянной трубки, заполненной специальной суспензией в растворе соляной кислоты, и погруженной в нее серебряной проволоки.
Полезный сигнал возникает на границе соприкосновения раствора и индикаторного электрода и передается через металлический проводник на вход pH-метра. Таким способом можно измерять pH любых жидкостей, в том числе непрозрачных и цветных.
Специализированный прибор, применяемый в медицине для исследований pH жидкостей желудочно-кишечного тракта, называется ацидогастрометром. Включает в себя регистрирующий блок и один или несколько зондов. Для измерения уровня pH таких биологических жидкостей, как слюна и моча, применяются электронные pH-метры.
Кислотно-щелочной баланс человека
Организмом человека вырабатываются разные жидкости, каждая из которых должна иметь определенное значение pH. Отклонение в ту или иную сторону может привести к развитию множества серьезных заболеваний. Вовремя обнаруженные изменения можно исправить, если повысить или понизить кислотность потребляемых продуктов и питьевой воды. Механизм регулирования пропорционального соотношения кислот и щелочей в клеточных и межклеточных жидкостях называют кислотно-щелочным балансом (равновесием). По значению pH можно определить, в каком состоянии находятся многие органы человека.

На pH почек и печени оказывают влияние не только метаболические процессы в самом организме, но также пища и вода. Излишнюю кислотность потребленных продуктов организм выводит через мочу. Низкий уровень pH мочи говорит о том, что почки работают на пределе. Когда излишняя кислота не может быть выведена из организма естественным путем, она скапливается в подкожной жировой прослойке, имеющей кислотный pH. Это приводит к излишнему весу. В борьбе с этим явлением помогает щелочная вода, снижая нагрузку на почки.
В желудке среда резко кислая, в момент пищеварения pH равен 1,8−3. Вопреки распространненому мнению, причиной таких неприятных симптомов, как изжога и дискомфорт в желудке, является пониженная, а не повышенная кислотность желудочного сока. Нормальный уровень pH создает благоприятные условия для развития правильных бактерий и запускает механизм переваривания пищи, а болезнетворные микроорганизмы и гельминты расщепляются пищеварительными ферментами.

pH крови организм поддерживает в постоянном состоянии на уровне 7,4—7,45. Малейшее отклонение его от нормы может привести к тяжелым последствиям для человека. При понижении pH ниже 7,35 возникает ацидоз. При превышении нормы — алкалоз. Это не самостоятельные заболевания, они свидетельствуют о нарушениях в работе легких, почек, печении. Такие состояния сопровождаются очень опасными для здоровья симптомами, приводящими иногда даже к коме. По мнению врачей, ацидоз переносится легче алкалоза.
Кровеносные сосуды питают слюнные железы, поэтому за уровнем pH крови можно следить по pH слюны. Поддержание кислотно-щелочного баланса в кровеносной системе — это важнейшая функция организма человека. Внешние факторы не оказывают влияния на pH крови, он регулируется только внутренними механизмами тела человека:
- Буферные системы крови поддерживают устойчивость среды.
- Легочная (респираторная) система удаляет излишки углекислого газа из крови.
- Выделительная система (почки). Самый медленный, но и самый мощный механизм, может полностью восстанавливать pH организма путем выведения ионов водорода через мочу.
Таким образом, хотя кислотный показатель крови совершенно не подвержен внешнему влиянию, механизмы его поддержания на нужном уровне имеют зависимость от того, чем человек питается и какую воду пьет. Мясо и молоко повышают общую кислотность организма, а зелень и зеленые овощи лучше всего нейтрализуют ее. Кислотность и щелочность различных пищевых продуктов можно узнать из специальных таблиц. Оптимальное значение pH для воды находится в пределах от 6 до 9.
Придерживаясь принципов правильного питания для поддержания кислотно-щелочного равновесия в своем организме, человек надолго сохранит молодость, красоту и здоровье.
Содержание
- 1 Понятие о водородном показателе
- 2 Шкала pH
- 3 Методы определения величины pH
- 3.1 Использование индикаторов
- 3.2 Ионометрический метод
- 3.3 Аналитический объемный метод
- 4 Влияние температуры на значение pH
- 5 Значения pH некоторых растворов
- 5.1 pH растворов кислот
- 5.2 pH растворов оснований
- 5.3 Значения pH некоторых бытовых веществ и пищевых продуктов
- 6 Роль показателя кислотности
Важной характеристикой водных растворов является уровень концентрации в них положительно заряженных ионов водорода и отрицательно заряженных гидроксид-ионов относительно друг друга. При одинаковых концентрациях и раствор считается нейтральным, при избытке катионов – кислотным и при избытке анионов – основным (щелочным). Величина, называемая водородным показателем, или pH раствора, – это количественное выражение кислотности.
Понятие о водородном показателе
Определение pH-фактора базируется на кислотно-основных свойствах воды. Ее молекулы способны к самопроизвольной диссоциации, благодаря чему в воде всегда присутствует некоторое количество ионов и . Их концентрация мала вследствие обратимости процесса диссоциации, который выражается формулой
![]() ⇄
⇄ ![]() +
+ ![]()
Из формулы видно, что ионы водорода и гидроксила содержатся в воде в равной концентрации: [![]() ]=[
]=[![]() ]. В стандартных условиях (при температуре 22–25° C) она составляет
]. В стандартных условиях (при температуре 22–25° C) она составляет ![]() моль⁄л.
моль⁄л.
Величина ![]() =[
=[![]() ]∙[
]∙[![]() ] называется ионным произведением воды. При заданной температуре она является постоянной (при 22–25° C
] называется ионным произведением воды. При заданной температуре она является постоянной (при 22–25° C ![]() =
=![]() моль
моль![]() /л
/л![]() ) не только для воды, но и для разбавленных растворов. При добавлении кислоты к воде повышается концентрация [
) не только для воды, но и для разбавленных растворов. При добавлении кислоты к воде повышается концентрация [![]() ] и понижается [
] и понижается [![]() ] (кислотность возрастает), при добавлении щелочи падает [
] (кислотность возрастает), при добавлении щелочи падает [![]() ] и растет [
] и растет [![]() ] (кислотность понижается).
] (кислотность понижается).
В качестве показателя кислотности удобно использовать десятичный логарифм величины [![]() ] с обратным знаком:
] с обратным знаком:
pH = -lg [![]() ]
]
Для воды и любой нейтральной среды водородный показатель составит: pH = — lg ![]() = -(-7) = 7
= -(-7) = 7
Шкала pH
На основе постоянства значения ионного произведения воды построена шкала величин pH различных растворов. Отметка «7» в ней соответствует нейтральной среде, числа слева от 7 – кислотной, и справа – основной (щелочной).

Важно помнить, что, поскольку для определения показателя кислотности для избавления от знака «минус» в показателе степени используется отрицательный логарифм, понижение pH означает повышение концентрации ![]() , то есть кислотных свойств, и наоборот. Так, значение
, то есть кислотных свойств, и наоборот. Так, значение ![]() 5 соответствует концентрации [
5 соответствует концентрации [![]() ] =
] = ![]() моль⁄л и большей кислотности, чем
моль⁄л и большей кислотности, чем ![]() 9, означающее, что в растворе содержится
9, означающее, что в растворе содержится ![]() моль⁄л катионов водорода.
моль⁄л катионов водорода.
Методы определения величины pH
В зависимости от целей и условий значение водородного показателя устанавливается различными методами. Качественно оценить кислотность среды позволяет применение индикаторов. Точные количественные результаты получают с помощью измерительных методов.
Использование индикаторов
Метод основан на способности ряда органических веществ к изменению окраски в зависимости от кислотности среды. Распространенные индикаторы – лакмус, метилоранж, фенолфталеин. Каждый из них проявляет свои свойства в ограниченном диапазоне значений pH.
| Индикатор | Интервал шкалы pH | Характер изменения цвета
по мере уменьшения кислотности |
| Лакмус | 5,0–8,0 | красный → фиолетовый → синий |
| Метилоранж | 3,1–4,4 | красный → оранжевый → желтый |
| Фенолфталеин | 8,2–10,0 | бесцветный → малиновый |
Индикаторный метод отличает простота наглядность и быстрота, но он недостаточно точен и зависит от субъективного восприятия цвета.
Достичь большей точности позволяет применение универсального индикатора. Он представляет собой смесь веществ и охватывает широкий диапазон pH от 0 до 14. Цвет, приобретенный нанесенным на бумажную полосу индикатором в той или иной среде, сравнивают с эталонной шкалой. Универсальный индикатор дает возможность определять pH с точностью до десятых долей.

Индикаторные методы неэффективны в случаях, когда раствор слишком слабый, имеет собственную яркую окраску или замутнен.
Ионометрический метод
Водородный показатель можно определить с точностью до 0,01 в широком диапазоне, применяя pH-метр. Прибор представляет собой электронный милливольтметр, определяющий разность потенциалов на электродах, один из которых (измерительный pH-электрод) помещен в исследуемый раствор. Другой (электрод сравнения) погружен в электролит с определенным pH. На нем создается стабильный потенциал, относительно которого измеряют pH анализируемой среды. Разность потенциалов пропорциональна величине показателя кислотности.
pH-метр требует тщательной калибровки. Для нее используются специально приготовленные буферные растворы с эталонными значениями pH, устойчивыми при разбавлении или добавкам небольших количеств сильных кислот или оснований. В приготовлении буферных растворов для pH-метрии применяются стандарт-титры – наборы чистых реактивов с точно известной массой, которые разводят дистиллированной водой до необходимой концентрации.

Конструкция современных pH-метров предусматривает вместо двух электродов один комбинированный, что значительно упрощает их использование.
Аналитический объемный метод
В данном способе определения водородного показателя применяется процедура кислотно-основного титрования, ведущую роль в которой играет реакция нейтрализации исследуемого образца титрантом – стандартным раствором с определенным pH. Если титруется раствор кислоты, в качестве титранта используют щелочь (гидроксид натрия или калия), если основание – титрантом является раствор сильной кислоты (соляной или серной).
Титрант медленно добавляют к образцу до достижения точки эквивалентности – момента, когда происходит полная нейтрализация титруемого раствора. Фиксация конечной точки титрования может производиться несколькими способами: с помощью индикатора, потенциометрии, спектрофотометрии или измерения электропроводности. Определив необходимый для нейтрализации объем титранта и зная его концентрацию, вычисляют pH препарата.

Влияние температуры на значение pH
Повышение температуры приводит к росту диссоциации слабых электролитов, в том числе и воды. Повышается равновесная концентрация ионов и и возрастает величина ионного произведения. Соответственно меняется и водородный показатель для нейтральной среды:
| Температура
T, 0° C |
0 | 20 | 25 | 40 | 60 | 80 | 100 |
| Ионное произведение воды, |
|||||||
| Нейтральный pH = — lg(√(K_W ))=-lg K_W/2 | 7,5 | 7,1 | 7 | 6,8 | 6,5 | 6,3 | 6,1 |
Температурные изменения оказывают сложное и неоднозначное влияние на измерения pH. В целом органические и щелочные пробы более зависимы от них, чем неорганические и кислотные. При pH-метрии и титровании температура строго контролируется, а полученные результаты пересчитываются с целью приведения к значению, характерному при 25° C.
Значения pH некоторых растворов
При определении величины pH для растворов кислот и оснований принято выражать концентрацию раствора в единицах нормальности. Нормальная концентрация – это количество моль-эквивалентов вещества в 1 л раствора: .
Эквивалентом называется частица (реальная либо условная), которая в химических реакциях равноценна одному катиону или одному электрону. Моль-эквивалент содержит эквивалентов, а его масса в единицах называется молярной массой эквивалента .
Многоосновные кислоты могут отдавать один или более ионов водорода, поэтому число моль-эквивалентов в растворе и, соответственно, нормальность будет в разных случаях неодинакова. Она имеет обозначение «н.» с указанием доли нормальной концентрации. Например, серная кислота, молекула которой при диссоциации отдает два протона , при молярной концентрации имеет нормальность 1н.
pH растворов кислот
| Кислота | Концентрация | pH |
| Азотная | 0,1 н. | 1,0 |
| Борная | 0,1 н. | 5,2 |
| Муравьиная | 0,1 н. | 2,3 |
| Серная | н. | 0,3 |
| 0,1 н. | 1,2 | |
| 0,01 н. | 2,1 | |
| Сернистая | 0,1 н. | 1,5 |
| Сероводородная | 0,1 н. | 4,1 |
| Уксусная | н. | 2,4 |
| 0,1 н. | 2,9 | |
| 0,01 н. | 3,4 | |
| Соляная | н. | 0,1 |
| 0,1 н. | 1,1 | |
| 0,01 н. | 2,0 | |
| Щавелевая | 0,1 н. | 1,3 |
pH растворов оснований
Нормальность щелочей определяется аналогично нормальности кислот, исходя из количества гидроксид-ионов, которые отщепляются при диссоциации.
| Основание | Концентрация | pH |
| Гидроксид калия | н. | 14,0 |
| 0,1 н. | 13,0 | |
| 0,01 н. | 12,0 | |
| Гидроксид кальция | насыщенный | 12,4 |
| Гидроксид натрия | н. | 14,0 |
| 0,1 н. | 13,0 | |
| 0,01 н. | 12,0 |
Значения pH некоторых бытовых веществ и пищевых продуктов
| Вещество | pH | Продукт | pH |
| электролит аккумуляторный на основе | <1 | сок лимонный | 2,0–2,6 |
| шампуни | 4,5–7,0 | уксус пищевой | 2,4–3,1 |
| мыла жидкие на основе синтетических ПАВ | 5,5–7,0 | кетчуп | 3,9 |
| средства для мытья стекол | 6,2–7,3 | томаты | 4,3–4,9 |
| средства для мытья пола | 6,9–8,6 | сыр | 4,8–6,4 |
| вода морская | 8,0 | кофе | 5,0 |
| мыло натуральное | 9,0–11,0 | чай | 5,5 |
| нашатырный спирт | 11,5 | вода питьевая | 6,5–8,5 |
| хлорная известь (отбеливатель) | 12,5 | молоко | 6,5–6,9 |
| раствор соды | 13,5 | яйцо куриное свежее | 7,6–8,0 |
Роль показателя кислотности
Знание и использование водородного показателя играет значительную роль во многих областях жизни людей, особенно в здравоохранении и медицине, в водоснабжении, в производстве и грамотном потреблении продуктов питания и средств бытовой химии. Оно также важно в организации сельского хозяйства, в производстве кормов и удобрений. Показатель pH имеет большое значение при проведении научно-исследовательских работ в химии и биологии, а также при мониторинге многих технологических процессов в нефтехимической, топливной, атомной и других отраслях промышленности.

Test tubes containing solutions of pH 1–10 colored with an indicator
In chemistry, pH (), also referred to as acidity, historically denotes “potential of hydrogen” (or “power of hydrogen”).[1] It is a scale used to specify the acidity or basicity of an aqueous solution. Acidic solutions (solutions with higher concentrations of hydrogen (H+) ions) are measured to have lower pH values than basic or alkaline solutions.
The pH scale is logarithmic and inversely indicates the activity of hydrogen ions in the solution.[2]
where [H+] is the equilibrium molar concentration (mol/L) of H+ in the solution. At 25 °C (77°F), solutions with a pH less than 7 are acidic, and solutions with a pH greater than 7 are basic. Solutions with a pH of 7 at 25 °C are neutral (i.e. have the same concentration of H+ ions as OH− ions, i.e. the same as pure water). The neutral value of the pH depends on the temperature and is lower than 7 if the temperature increases above 25 °C. The pH value can be less than 0 for very concentrated strong acids or greater than 14 for very concentrated strong bases.[3]
The pH scale is traceable to a set of standard solutions whose pH is established by international agreement.[4] Primary pH standard values are determined using a concentration cell with transference by measuring the potential difference between a hydrogen electrode and a standard electrode such as the silver chloride electrode. The pH of aqueous solutions can be measured with a glass electrode and a pH meter or a color-changing indicator. Measurements of pH are important in chemistry, agronomy, medicine, water treatment, and many other applications.
History[edit]
In 1909, the Danish chemist Søren Peter Lauritz Sørensen introduced the concept of pH at the Carlsberg Laboratory,[5] originally using the notation “pH•“, with H• as a subscript to the lowercase p. The concept was later revised in 1924 to the modern pH to accommodate definitions and measurements in terms of electrochemical cells.
For the sign p, I propose the name ‘hydrogen ion exponent’ and the symbol pH•. Then, for the hydrogen ion exponent (pH•) of a solution, the negative value of the Briggsian logarithm of the related hydrogen ion normality factor is to be understood.[5]
Sørensen did not explain why he used the letter p, and the exact meaning of the letter is still disputed.[6] Sørensen described a way of measuring pH using potential differences, and it represents the negative power of 10 in the concentration of hydrogen ions. The letter p could stand for the French puissance, German Potenz, or Danish potens, all meaning “power”, or it could mean “potential”. All of these words start with the letter p in French, German, and Danish, which where the languages Sørensen published in (Carlsberg Laboratory was French-speaking, German was the dominant language of scientific publishing, and Sørensen was Danish). He also used the letter q in much the same way elsewhere in the paper, and he might have arbitrarily labelled the test solution “p” and the reference solution “q”; these letters are often paired.[7] Some literature sources suggest that “pH” stands for the Latin term pondus hydrogenii (quantity of hydrogen) or potentia hydrogenii (power of hydrogen), although this is not supported by Sørensen’s writings.[8][9][10]
In modern chemistry, the p stands for “the negative decimal logarithm of”, and is used in the term pKa for acid dissociation constants,[11] so pH is “the negative decimal logarithm of H+ ion concentration”, while pOH is “the negative decimal logarithm of OH- ion concentration”.
Bacteriologist Alice Catherine Evans, who influenced dairying and food safety, credited William Mansfield Clark and colleagues, including herself, with developing pH measuring methods in the 1910s, which had a wide influence on laboratory and industrial use thereafter. In her memoir, she does not mention how much, or how little, Clark and colleagues knew about Sørensen’s work a few years prior.[12] She said:
In these studies [of bacterial metabolism] Dr. Clark’s attention was directed to the effect of acid on the growth of bacteria. He found that it is the intensity of the acid in terms of hydrogen-ion concentration that affects their growth. But existing methods of measuring acidity determined the quantity, not the intensity, of the acid. Next, with his collaborators, Dr. Clark developed accurate methods for measuring hydrogen-ion concentration. These methods replaced the inaccurate titration method of determining the acid content in use in biologic laboratories throughout the world. Also they were found to be applicable in many industrial and other processes in which they came into wide usage.[12]
The first electronic method for measuring pH was invented by Arnold Orville Beckman, a professor at the California Institute of Technology in 1934.[13] It was in response to a request from the local citrus grower Sunkist, which wanted a better method for quickly testing the pH of lemons they were picking from their nearby orchards.[14]
Definition[edit]
pH[edit]
The pH of a solution is defined as the decimal logarithm of the reciprocal of the hydrogen ion activity, aH+.[15] Mathematically, pH is expressed as:
For example, for a solution with a hydrogen ion activity of 5×10−6 (i.e., the concentration of hydrogen ions in moles per litre), the pH of the solution can be calculated as follows:
The concept of pH was developed because ion-selective electrodes, which are used to measure pH, respond to activity. The electrode potential, E, follows the Nernst equation for the hydrogen ion, which can be expressed as:
where E is a measured potential, E0 is the standard electrode potential, R is the gas constant, T is the temperature in kelvins, F is the Faraday constant. For H+, the number of electrons transferred is one. The electrode potential is proportional to pH when pH is defined in terms of activity.
The precise measurement of pH is presented in International Standard ISO 31-8 as follows:[16] A galvanic cell is set up to measure the electromotive force (e.m.f.) between a reference electrode and an electrode sensitive to the hydrogen ion activity when they are both immersed in the same aqueous solution. The reference electrode may be a silver chloride electrode or a calomel electrode, and the hydrogen-ion selective electrode is a standard hydrogen electrode.
- Reference electrode | concentrated solution of KCl || test solution | H2 | Pt
Firstly, the cell is filled with a solution of known hydrogen ion activity and the electromotive force, ES, is measured. Then the electromotive force, EX, of the same cell containing the solution of unknown pH is measured.
The difference between the two measured electromotive force values is proportional to pH. This method of calibration avoids the need to know the standard electrode potential. The proportionality constant, 1/z, is ideally equal to 
In practice, a glass electrode is used instead of the cumbersome hydrogen electrode. A combined glass electrode has an in-built reference electrode. It is calibrated against buffer solutions of known hydrogen ion (H+) activity proposed by the International Union of Pure and Applied Chemistry (IUPAC).[17] Two or more buffer solutions are used in order to accommodate the fact that the “slope” may differ slightly from ideal. To calibrate the electrode, it is first immersed in a standard solution, and the reading on a pH meter is adjusted to be equal to the standard buffer’s value. The reading from a second standard buffer solution is then adjusted using the “slope” control to be equal to the pH for that solution. Further details, are given in the IUPAC recommendations.[15] When more than two buffer solutions are used the electrode is calibrated by fitting observed pH values to a straight line with respect to standard buffer values. Commercial standard buffer solutions usually come with information on the value at 25 °C and a correction factor to be applied for other temperatures.
The pH scale is logarithmic and therefore pH is a dimensionless quantity.[18] The pH scale ranges from 0 to 14, with a pH of 7 indicating neutrality, values less than 7 indicating acidity, and values greater than 7 indicating basicity. The pH scale is based on the hydrogen ion concentration, with each pH value representing a tenfold difference in hydrogen ion concentration.
p[H][edit]
This was the original definition of Sørensen in 1909,[19] which was superseded in favor of pH in 1924. [H] is the concentration of hydrogen ions, denoted [H+] in modern chemistry. More correctly, the thermodynamic activity of H+ in dilute solution should be replaced by [H+]/c0, where the standard state concentration c0 = 1 mol/L. This ratio is a pure number whose logarithm can be defined.
It is possible to measure the concentration of hydrogen ions directly using an electrode calibrated in terms of hydrogen ion concentrations. One common method is to titrate a solution of known concentration of a strong acid with a solution of known concentration of strong base in the presence of a relatively high concentration of background electrolyte. By knowing the concentrations of the acid and base, the concentration of hydrogen ions can be calculated and the measured potential can be correlated with concentrations. The calibration is usually carried out using a Gran plot.[20] This procedure makes the activity of hydrogen ions equal to the numerical value of concentration.
The glass electrode (and other ion selective electrodes) should be calibrated in a medium similar to the one being investigated. For instance, if one wishes to measure the pH of a seawater sample, the electrode should be calibrated in a solution resembling seawater in its chemical composition.
The difference between p[H] and pH is quite small, and it has been stated that pH = p[H] + 0.04.[21] However, it is common practice to use the term “pH” for both types of measurement.
pOH[edit]

Relation between pH and pOH. Red represents the acidic region. Blue represents the basic region.
pOH is sometimes used as a measure of the concentration of hydroxide ions, OH−. pOH values are derived from pH measurements. The concentration of hydroxide ions in water is related to the concentration of hydrogen ions by
where KW is the self-ionization constant of water. Taking logarithms
So, at room temperature, pOH ≈ 14 − pH. However this relationship is not strictly valid in other circumstances, such as in measurements of soil alkalinity.
Measurement[edit]
pH Indicators[edit]
| Average pH of common solutions | ||
|---|---|---|
| Substance | pH range | Type |
| Battery acid | < 1 | Acid |
| Gastric acid | 1.0 – 1.5 | |
| Vinegar | 2.5 | |
| Orange juice | 3.3 – 4.2 | |
| Black coffee | 5 – 5.03 | |
| Milk | 6.5 – 6.8 | |
| Pure water at 25 °C | 7 | Neutral |
| Sea water | 7.5 – 8.4 | Base |
| Ammonia | 11.0 – 11.5 | |
| Bleach | 12.5 | |
| 0.1 M NaOH | 13 |
pH can be measured using indicators, which change color depending on the pH of the solution they are in. By comparing the color of a test solution to a standard color chart, the pH can be estimated to the nearest whole number. For more precise measurements, the color can be measured using a colorimeter or spectrophotometer. Universal indicator is a mixture of several indicators that can provide a continuous color change over a range of pH values, typically from about pH 2 to pH 10. Universal indicator paper is made from absorbent paper that has been impregnated with universal indicator. An alternative method of measuring pH is using an electronic pH meter, which directly measures the voltage difference between a pH-sensitive electrode and a reference electrode.
Non-aqueous solutions[edit]
pH values can be measured in non-aqueous solutions, but they are based on a different scale from aqueous pH values, because the standard states used for calculating hydrogen ion concentrations (activities) are different. The hydrogen ion activity, aH+, is defined[22][23] as:
where μH+ is the chemical potential of the hydrogen ion, 
pH is an example of an acidity function, but there are others that can be defined. For example, the Hammett acidity function, H0, has been developed in connection with superacids.
Unified absolute pH scale[edit]
In 2010, a new approach to measuring pH was proposed, called the “unified absolute pH scale”. This approach allows for a common reference standard to be used across different solutions, regardless of their pH range. The unified absolute pH scale is based on the absolute chemical potential of the proton, as defined by the Lewis acid–base theory. This scale is applicable to liquids, gases, and even solids.[24] The advantages of the unified absolute pH scale include consistency, accuracy, and applicability to a wide range of sample types. It is precise and versatile because it serves as a common reference standard for pH measurements. However, implementation efforts, compatibility with existing data, complexity, and potential costs are some challenges.
Extremes of pH measurements[edit]
The measurement of pH can become difficult at extremely acidic or alkaline conditions, such as below pH 2.5 (ca. 0.003 mol/dm3 acid) or above pH 10.5 (above ca. 0.0003 mol/dm3 alkaline). This is due to the breakdown of the Nernst equation in this conditions when using a glass electrode. There are several factors contribute to this problem. Firstly, liquid junction potentials may not be independent of pH.[25] Secondly, the high ionic strength of concentrated solutions can affect the electrode potentials. At high pH the glass electrode may be affected by “alkaline error”, because the electrode becomes sensitive to the concentration of cations such as Na+ and K+ in the solution.[26] To overcome these problems, specially constructed electrodes are available.
Runoff from mines or mine tailings can produce some extremely low pH values.[27]
Applications[edit]
The pH scale ranges from 0 to 14, with 7 being neutral. Pure water has a pH of 7 at 25°C, meaning it is neutral. When an acid is dissolved in water, the pH will be less than 7, while a base, or alkali, will have a pH greater than 7. A strong acid, such as hydrochloric acid, at concentration 1 mol dm−3 has a pH of 0, while a strong alkali like sodium hydroxide, at the same concentration, has a pH of 14. Since pH is a logarithmic scale, a difference of one in pH is equivalent to a tenfold difference in hydrogen ion concentration.
It’s important to note that neutrality isn’t exactly 7 at 25°C, although it’s a good approximation in most cases. Neutrality occurs when the concentration of hydrogen ions ([H+]) equals the concentration of hydroxide ions ([OH−]), or when their activities are equal. Since self-ionization of water holds the product of these concentration [H+] × [OH−] = Kw, it can be seen that at neutrality [H+] = [OH−] = √Kw, or pH = pKw/2. pKw is approximately 14 but depends on ionic strength and temperature, and so the pH of neutrality does also. Pure water and a solution of NaCl in pure water are both neutral, since dissociation of water produces equal numbers of both ions. However the pH of the neutral NaCl solution will be slightly different from that of neutral pure water because the hydrogen and hydroxide ions’ activity is dependent on ionic strength, so Kw varies with ionic strength.
When pure water is exposed to air, it becomes mildly acidic. This is because water absorbs carbon dioxide from the air, which is then slowly converted into bicarbonate and hydrogen ions (essentially creating carbonic acid).
- CO
2+ H
2O ⇌ HCO−
3+ H+
pH in soil[edit]

Nutritional elements availability within soil varies with pH. Light blue color represents the ideal range for most plants.
The United States Department of Agriculture Natural Resources Conservation Service, formerly Soil Conservation Service classifies soil pH ranges as follows:[28]
| Denomination | pH range |
|---|---|
| Ultra acidic | < 3.5 |
| Extremely acidic | 3.5–4.4 |
| Very strongly acidic | 4.5–5.0 |
| Strongly acidic | 5.1–5.5 |
| Moderately acidic | 5.6–6.0 |
| Slightly acidic | 6.1–6.5 |
| Neutral | 6.6–7.3 |
| Slightly alkaline | 7.4–7.8 |
| Moderately alkaline | 7.9–8.4 |
| Strongly alkaline | 8.5–9.0 |
| Very strongly alkaline | 9.0–10.5 |
| Hyper alkaline | > 10.5 |
In Europe, topsoil pH is influenced by soil parent material, erosional effects, climate and vegetation. A recent map[29] of topsoil pH in Europe shows the alkaline soils in Mediterranean, Hungary, East Romania, North France. Scandinavian countries, Portugal, Poland and North Germany have more acid soils.
pH in plants[edit]

Plants contain pH-dependent pigments that can be used as pH indicators, such as those found in hibiscus, red cabbage (anthocyanin), and grapes (red wine). Citrus fruits have acidic juice primarily due to the presence of citric acid, while other carboxylic acids can be found in various living systems. For instance, muscle activity results in the production of lactic acid. The protonation state of phosphate derivatives, including ATP, is pH-dependent. Hemoglobin, an oxygen-transport enzyme, is also affected by pH in a phenomenon known as the Root effect.
pH in the ocean[edit]
The pH of seawater plays an important role in the ocean’s carbon cycle. There is evidence of ongoing ocean acidification (meaning a drop in pH value): Between 1950 and 2020, the average pH of the ocean surface fell from approximately 8.15 to 8.05.[30] Carbon dioxide emissions from human activities are the primary cause of ocean acidification, with atmospheric carbon dioxide (CO2) levels exceeding 410 ppm (in 2020). CO2 from the atmosphere is absorbed by the oceans. This produces carbonic acid (H2CO3) which dissociates into a bicarbonate ion (HCO−3) and a hydrogen ion (H+). The presence of free hydrogen ions (H+) lowers the pH of the ocean.
Three pH scales in oceanography[edit]
The measurement of pH in seawater is complicated by the chemical properties of seawater, and three distinct pH scales exist in chemical oceanography.[31] In practical terms, the three seawater pH scales differ in their pH values up to 0.10, differences that are much larger than the accuracy of pH measurements typically required, in particular, in relation to the ocean’s carbonate system.[31] Since it omits consideration of sulfate and fluoride ions, the free scale is significantly different from both the total and seawater scales. Because of the relative unimportance of the fluoride ion, the total and seawater scales differ only very slightly.
As part of its operational definition of the pH scale, the IUPAC defines a series of buffer solutions across a range of pH values (often denoted with National Bureau of Standards (NBS) or National Institute of Standards and Technology (NIST) designation). These solutions have a relatively low ionic strength (≈0.1) compared to that of seawater (≈0.7), and, as a consequence, are not recommended for use in characterizing the pH of seawater, since the ionic strength differences cause changes in electrode potential. To resolve this problem, an alternative series of buffers based on artificial seawater was developed.[32] This new series resolves the problem of ionic strength differences between samples and the buffers, and the new pH scale is referred to as the total scale, often denoted as pHT. The total scale was defined using a medium containing sulfate ions. These ions experience protonation, H+ + SO2−
4↔ HSO−
4, such that the total scale includes the effect of both protons (free hydrogen ions) and hydrogen sulfate ions:
- [H+]T = [H+]F + [HSO−
4]
An alternative scale, the free scale, often denoted pHF, omits this consideration and focuses solely on [H+]F, in principle making it a simpler representation of hydrogen ion concentration. Only [H+]T can be determined,[33] therefore [H+]F must be estimated using the [SO2−
4] and the stability constant of HSO−
4, K*
S:
- [H+]F = [H+]T − [HSO−
4] = [H+]T ( 1 + [SO2−
4] / K*
S )−1
However, it is difficult to estimate K*
S in seawater, limiting the utility of the otherwise more straightforward free scale.
Another scale, known as the seawater scale, often denoted pHSWS, takes account of a further protonation relationship between hydrogen ions and fluoride ions, H+ + F− ⇌ HF. Resulting in the following expression for [H+]SWS:
- [H+]SWS = [H+]F + [HSO−
4] + [HF]
However, the advantage of considering this additional complexity is dependent upon the abundance of fluoride in the medium. In seawater, for instance, sulfate ions occur at much greater concentrations (>400 times) than those of fluoride. As a consequence, for most practical purposes, the difference between the total and seawater scales is very small.
The following three equations summarize the three scales of pH:
- pHF = −log [H+]F
- pHT = −log([H+]F + [HSO−
4]) = −log[H+]T - pHSWS = −log(H+]F + [HSO−
4] + [HF]) = −log[v]SWS
pH of various body fluids[edit]
-
pH of various body fluids[34]
Compartment pH Gastric acid 1.5–3.5[35] Lysosomes 4.5[34] Human skin 4.7[36] Granules of chromaffin cells 5.5 Urine 6.0 Cytosol 7.2 Blood (natural pH) 7.34–7.45[34] Cerebrospinal fluid (CSF) 7.5 Mitochondrial matrix 7.5 Pancreas secretions 8.1
In living organisms, the pH of various body fluids, cellular compartments, and organs is tightly regulated to maintain a state of acid-base balance known as acid–base homeostasis. Acidosis, defined by a pH below 7.35, is the most common disorder of acid–base homeostasis and occurs when there is an excess of acid in the body. In contrast, alkalosis is characterized by excessively high blood pH.
Blood pH is usually slightly basic, with a pH of 7.365, referred to as physiological pH in biology and medicine. Plaque formation in teeth can create a local acidic environment that results in tooth decay through demineralization. Enzymes and other proteins have an optimal pH range for function and can become inactivated or denatured outside this range.
pH calculations[edit]
When calculating the pH of a solution containing acids and/or bases, a chemical speciation calculation is used to determine the concentration of all chemical species present in the solution. The complexity of the procedure depends on the nature of the solution. Strong acids and bases are compounds that are almost completely dissociated in water, which simplifies the calculation. However, for weak acids, a quadratic equation must be solved, and for weak bases, a cubic equation is required. In general, a set of non-linear simultaneous equations must be solved.
Water itself is a weak acid and a weak base, so its dissociation must be taken into account at high pH and low solute concentration (see amphoterism). It dissociates according to the equilibrium
- 2 H2O ⇌ H3O+ (aq) + OH− (aq)
with a dissociation constant, Kw defined as
where [H+] stands for the concentration of the aqueous hydronium ion and [OH−] represents the concentration of the hydroxide ion. This equilibrium needs to be taken into account at high pH and when the solute concentration is extremely low.
Strong acids and bases[edit]
Strong acids and bases are compounds that are essentially fully dissociated in water. This means that in an acidic solution, the concentration of hydrogen ions (H+) can be considered equal to the concentration of the acid. Similarly, in a basic solution, the concentration of hydroxide ions (OH-) can be considered equal to the concentration of the base. The pH of a solution is defined as the negative logarithm of the concentration of H+, and the pOH is defined as the negative logarithm of the concentration of OH-. For example, the pH of a 0.01M solution of hydrochloric acid (HCl) is equal to 2 (pH = −log10(0.01)), while the pOH of a 0.01M solution of sodium hydroxide (NaOH) is equal to 2 (pOH = −log10(0.01)), which corresponds to a pH of about 12.
However, self-ionization of water must also be considered when concentrations of a strong acid or base is very low or high. For instance, a 5×10−8M solution of HCl would be expected to have a pH of 7.3 based on the above procedure, which is incorrect as it is acidic and should have a pH of less than 7. In such cases, the system can be treated as a mixture of the acid or base and water, which is an amphoteric substance. By accounting for the self-ionization of water, the true pH of the solution can be calculated. For example, a 5×10−8M solution of HCl would have a pH of 6.89 when treated as a mixture of HCl and water. The self-ionization equilibrium of solutions of sodium hydroxide at higher concentrations must also be considered.[37]
Weak acids and bases[edit]
A weak acid or the conjugate acid of a weak base can be treated using the same formalism.
- Acid HA: HA ⇌ H+ + A−
- Base A: HA+ ⇌ H+ + A
First, an acid dissociation constant is defined as follows. Electrical charges are omitted from subsequent equations for the sake of generality
and its value is assumed to have been determined by experiment. This being so, there are three unknown concentrations, [HA], [H+] and [A−] to determine by calculation. Two additional equations are needed. One way to provide them is to apply the law of mass conservation in terms of the two “reagents” H and A.
C stands for analytical concentration. In some texts, one mass balance equation is replaced by an equation of charge balance. This is satisfactory for simple cases like this one, but is more difficult to apply to more complicated cases as those below. Together with the equation defining Ka, there are now three equations in three unknowns. When an acid is dissolved in water CA = CH = Ca, the concentration of the acid, so [A] = [H]. After some further algebraic manipulation an equation in the hydrogen ion concentration may be obtained.
Solution of this quadratic equation gives the hydrogen ion concentration and hence p[H] or, more loosely, pH. This procedure is illustrated in an ICE table which can also be used to calculate the pH when some additional (strong) acid or alkaline has been added to the system, that is, when CA ≠ CH.
For example, what is the pH of a 0.01M solution of benzoic acid, pKa = 4.19?
- Step 1:
- Step 2: Set up the quadratic equation.
- Step 3: Solve the quadratic equation.
For alkaline solutions, an additional term is added to the mass-balance equation for hydrogen. Since the addition of hydroxide reduces the hydrogen ion concentration, and the hydroxide ion concentration is constrained by the self-ionization equilibrium to be equal to ![{displaystyle {frac {K_{w}}{{ce {[H+]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/671c1d10d6bce20ed4de57be093835a6aad5019f)
General method[edit]
Some systems, such as with polyprotic acids, are amenable to spreadsheet calculations.[38] With three or more reagents or when many complexes are formed with general formulae such as ApBqHr, the following general method can be used to calculate the pH of a solution. For example, with three reagents, each equilibrium is characterized by an equilibrium constant, β.
Next, write down the mass-balance equations for each reagent:
Note that there are no approximations involved in these equations, except that each stability constant is defined as a quotient of concentrations, not activities. Much more complicated expressions are required if activities are to be used.
There are three non-linear simultaneous equations in the three unknowns, [A], [B] and [H]. Because the equations are non-linear and their concentrations may range over many powers of 10, the solution of these equations is not straightforward. However, many computer programs are available which can be used to perform these calculations. There may be more than three reagents. The calculation of hydrogen ion concentrations, using this approach, is a key element in the determination of equilibrium constants by potentiometric titration.
See also[edit]
- pH indicator
- Arterial blood gas
- Chemical equilibrium
- pCO2
- pKa
References[edit]
- ^ Jensen, William B. (2004). “The Symbol for pH” (PDF). Journal of Chemical Education. 81 (1): 21. Bibcode:2004JChEd..81…21J. doi:10.1021/ed081p21. Archived (PDF) from the original on 14 December 2019. Retrieved 15 July 2020.
- ^ Bates, Roger G. Determination of pH: theory and practice. Wiley, 1973.
- ^ Lim, Kieran F. (2006). “Negative pH Does Exist”. Journal of Chemical Education. 83 (10): 1465. Bibcode:2006JChEd..83.1465L. doi:10.1021/ed083p1465.
- ^ Covington, A. K.; Bates, R. G.; Durst, R. A. (1985). “Definitions of pH scales, standard reference values, measurement of pH, and related terminology” (PDF). Pure Appl. Chem. 57 (3): 531–542. doi:10.1351/pac198557030531. S2CID 14182410. Archived (PDF) from the original on 24 September 2007.
- ^ a b Sørensen, S. P. L. (1909). “Über die Messung und die Bedeutung der Wasserstoffionenkonzentration bei enzymatischen Prozessen” (PDF). Biochem. Z. 21: 131–304. Archived (PDF) from the original on 15 April 2021. Retrieved 22 March 2021.
Original German: Für die Zahl p schlage ich den Namen Wasserstoffionenexponent und die Schreibweise pH• vor. Unter dem Wasserstoffionexponenten (pH•) einer Lösungwird dann der Briggsche Logarithmus des reziproken Wertes des auf Wasserstoffionenbezagenen Normalitäts faktors de Lösungverstanden.
Two other publications appeared in 1909, one in French and one in Danish. - ^ Francl, Michelle (August 2010). “Urban legends of chemistry”. Nature Chemistry. 2 (8): 600–601. Bibcode:2010NatCh…2..600F. doi:10.1038/nchem.750. ISSN 1755-4330. PMID 20651711. Archived from the original on 6 August 2020. Retrieved 21 July 2019.
- ^ Myers, Rollie J. (2010). “One-Hundred Years of pH”. Journal of Chemical Education. 87 (1): 30–32. Bibcode:2010JChEd..87…30M. doi:10.1021/ed800002c.
- ^ Otterson, David W. (2015). “Tech Talk: (11) pH Measurement and Control Basics”. Measurement and Control. 48 (10): 309–312. doi:10.1177/0020294015600474. S2CID 110716297. Retrieved 16 June 2022.
- ^ Lian, Ying; Zhang, Wei; Ding, Longjiang; Zhang, Xiaoai; Zhang, Yinglu; Wang, Xu-dong (2019). “Nanomaterials for Intracellular pH Sensing and Imaging”. Novel Nanomaterials for Biomedical, Environmental and Energy Applications. Micro and Nano Technologies: 241–273. doi:10.1016/B978-0-12-814497-8.00008-4. ISBN 9780128144978. S2CID 104410918. Retrieved 16 June 2022.
- ^ Bradley, David (21 February 2018). “When it comes to caustic wit and an acid tongue, mind your Ps and Qs”. Materials Today. Retrieved 16 June 2022.
- ^ Nørby, Jens (2000). “The origin and the meaning of the little p in pH”. Trends in Biochemical Sciences. 25 (1): 36–37. doi:10.1016/S0968-0004(99)01517-0. PMID 10637613.
- ^ a b Evans, Alice C. (1963). “Memoirs” (PDF). NIH Office of History. National Institutes of Health Office of History. Archived from the original (PDF) on 15 December 2017. Retrieved 27 March 2018.
- ^ “Origins: Birth of the pH Meter”. Caltech Engineering & Science Magazine. Archived from the original on 6 November 2018. Retrieved 11 March 2018.
- ^ Tetrault, Sharon (June 2002). “The Beckmans”. Orange Coast. Orange Coast Magazine. Archived from the original on 15 April 2021. Retrieved 11 March 2018.
- ^ a b Covington, A. K.; Bates, R. G.; Durst, R. A. (1985). “Definitions of pH scales, standard reference values, measurement of pH, and related terminology” (PDF). Pure Appl. Chem. 57 (3): 531–542. doi:10.1351/pac198557030531. S2CID 14182410. Archived (PDF) from the original on 24 September 2007.
- ^ Quantities and units – Part 8: Physical chemistry and molecular physics, Annex C (normative): pH. International Organization for Standardization, 1992.
- ^ Covington, A. K.; Bates, R. G.; Durst, R. A. (1985). “Definitions of pH scales, standard reference values, measurement of pH, and related terminology” (PDF). Pure Appl. Chem. 57 (3): 531–542. doi:10.1351/pac198557030531. S2CID 14182410. Archived (PDF) from the original on 24 September 2007.
- ^ Gold, Victor, ed. (2019). The IUPAC Compendium of Chemical Terminology: The Gold Book (4 ed.). Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC). doi:10.1351/goldbook.p04525.
- ^ “Carlsberg Group Company History Page”. Carlsberggroup.com. Archived from the original on 18 January 2014. Retrieved 7 May 2013.
- ^ Rossotti, F.J.C.; Rossotti, H. (1965). “Potentiometric titrations solution containing the background electrolyte”. J. Chem. Educ. 42. doi:10.1021/ed042p375.
- ^ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000), Vogel’s Quantitative Chemical Analysis (6th ed.), New York: Prentice Hall, ISBN 0-582-22628-7, Section 13.23, “Determination of pH”
- ^ IUPAC, Compendium of Chemical Terminology, 2nd ed. (the “Gold Book”) (1997). Online corrected version: (2006–) “activity (relative activity), a“. doi:10.1351/goldbook.A00115
- ^ International Union of Pure and Applied Chemistry (1993). Quantities, Units and Symbols in Physical Chemistry, 2nd edition, Oxford: Blackwell Science. ISBN 0-632-03583-8. pp. 49–50. Electronic version.
- ^ Himmel, Daniel; Goll, Sascha K.; Leito, Ivo; Krossing, Ingo (16 August 2010). “A Unified pH Scale for All Phases”. Angewandte Chemie International Edition. 49 (38): 6885–6888. doi:10.1002/anie.201000252. ISSN 1433-7851. PMID 20715223.
- ^ Feldman, Isaac (1956). “Use and Abuse of pH measurements”. Analytical Chemistry. 28 (12): 1859–1866. doi:10.1021/ac60120a014.
- ^ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K. (2000), Vogel’s Quantitative Chemical Analysis (6th ed.), New York: Prentice Hall, ISBN 0-582-22628-7, Section 13.19 The glass electrode
- ^ Nordstrom, D. Kirk; Alpers, Charles N. (March 1999). “Negative pH, efflorescent mineralogy, and consequences for environmental restoration at the Iron Mountain Superfund site, California”. Proceedings of the National Academy of Sciences of the United States of America. 96 (7): 3455–62. Bibcode:1999PNAS…96.3455N. doi:10.1073/pnas.96.7.3455. PMC 34288. PMID 10097057. Archived from the original on 23 September 2017. Retrieved 4 November 2018.
- ^ Soil Survey Division Staff. “Soil survey manual.1993. Chapter 3, selected chemical properties”. Soil Conservation Service. U.S. Department of Agriculture Handbook 18. Archived from the original on 14 May 2011. Retrieved 12 March 2011.
- ^ Ballabio, Cristiano; Lugato, Emanuele; Fernández-Ugalde, Oihane; Orgiazzi, Alberto; Jones, Arwyn; Borrelli, Pasquale; Montanarella, Luca; Panagos, Panos (2019). “Mapping LUCAS topsoil chemical properties at European scale using Gaussian process regression”. Geoderma. 355: 113912. Bibcode:2019Geode.355k3912B. doi:10.1016/j.geoderma.2019.113912. PMC 6743211. PMID 31798185.
- ^ Terhaar, Jens; Frölicher, Thomas L.; Joos, Fortunat (2023). “Ocean acidification in emission-driven temperature stabilization scenarios: the role of TCRE and non-CO2 greenhouse gases”. Environmental Research Letters. 18 (2): 024033. Bibcode:2023ERL….18b4033T. doi:10.1088/1748-9326/acaf91. ISSN 1748-9326. S2CID 255431338.
- ^ a b Zeebe, R. E. and Wolf-Gladrow, D. (2001) CO2 in seawater: equilibrium, kinetics, isotopes, Elsevier Science B.V., Amsterdam, Netherlands ISBN 0-444-50946-1
- ^ Hansson, I. (1973). “A new set of pH-scales and standard buffers for seawater”. Deep-Sea Research. 20 (5): 479–491. Bibcode:1973DSRA…20..479H. doi:10.1016/0011-7471(73)90101-0.
- ^ Dickson, A. G. (1984). “pH scales and proton-transfer reactions in saline media such as sea water”. Geochim. Cosmochim. Acta. 48 (11): 2299–2308. Bibcode:1984GeCoA..48.2299D. doi:10.1016/0016-7037(84)90225-4.
- ^ a b c Boron, Walter, F.; Boulpaep, Emile L. (13 January 2012). Medical Physiology: A Cellular And Molecular Approach (2nd ed.). Elsevier Health Sciences, Saunders. pp. 652–671. ISBN 9781455711819. OCLC 1017876653. Archived from the original on 8 May 2022. Retrieved 8 May 2022.
- ^ Marieb, Elaine N.; Mitchell, Susan J. (30 June 2011). Human anatomy & physiology. San Francisco: Benjamin Cummings. ISBN 9780321735287. Archived from the original on 8 May 2022. Retrieved 8 May 2022.
- ^ Lambers, H.; Piessens, S.; Bloem, A.; Pronk, H.; Finkel, P. (1 October 2006). “Natural skin surface pH is on average below 5, which is beneficial for its resident flora”. International Journal of Cosmetic Science. 28 (5): 359–370. doi:10.1111/j.1467-2494.2006.00344.x. ISSN 1468-2494. PMID 18489300. S2CID 25191984. Archived from the original on 21 March 2022. Retrieved 8 May 2022.
- ^ Maloney, Chris. “pH calculation of a very small concentration of a strong acid”. Archived from the original on 8 July 2011. Retrieved 13 March 2011.
- ^ Billo, E.J. (2011). EXCEL for Chemists (3rd ed.). Wiley-VCH. ISBN 978-0-470-38123-6.
External links[edit]
![]()
Wikimedia Commons has media related to pH.
![]()
![{displaystyle {text{pH}}=-lg left[{mbox{H}}^{+}right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/84b6c4df1005ec6425445f99f778382ccc74861f)
![{displaystyle {text{pOH}}=-lg left[{mbox{OH}}^{-}right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/87cffb2ebc7515d5cc635fda36511214022adcd8)

![{displaystyle {ce {pH}}=-log(a_{{ce {H+}}})thickapprox -log([{ce {H+}}])}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5cee635c4839a5a266cfa10c541a8c7e21d2707e)




![{displaystyle [{ce {OH^-}}]={frac {K_{{ce {W}}}}{[{ce {H^+}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0e914d2d8665e01b649b6ecc09acdb2bb823b33c)


![{displaystyle K_{w}={ce {[H+][OH^{-}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4bbddc96ecfaf0a74d351c6ce2c7de2eb8c01688)
![{displaystyle K_{a}={frac {{ce {[H] [A]}}}{{ce {[HA]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f29a403e204523dcc5d4345e9da4125d6bccc8e0)
![{displaystyle C_{{ce {A}}}={ce {[A]}}+{ce {[HA]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9ebde93fda69a21943e8842a9a32da905b2f645e)
![{displaystyle C_{{ce {H}}}={ce {[H]}}+{ce {[HA]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/920b90697a63b1c14c8302e733fc525ba0d9585b)
![{displaystyle [{ce {H}}]^{2}+K_{a}[{ce {H}}]-K_{a}C_{a}=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/46348613cafd9be4dcf2b772575b5af47f080d54)

![{displaystyle [{ce {H}}]^{2}+6.46times 10^{-5}[{ce {H}}]-6.46times 10^{-7}=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3b00dbc68e7860d66750e413f778916b6b915cd9)
![{displaystyle [{ce {H+}}]=7.74times 10^{-4};quad mathrm {pH} =3.11}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d23e6dd79b1f843749965771698d8a5403a236a4)
![{displaystyle C_{ce {H}}={frac {[{ce {H}}]+[{ce {HA}}]-K_{w}}{ce {[H]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e4eaeb404231cb0a9a118cd2972dc991b67adaab)
![{displaystyle [{ce {A}}_{p}{ce {B}}_{q}{ce {H}}_{r}]=beta _{pqr}[{ce {A}}]^{p}[{ce {B}}]^{q}[{ce {H}}]^{r}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0116cc100cbe49e89c845e94bfb7cfa9d41efdf4)
![{displaystyle {begin{aligned}C_{ce {A}}&=[{ce {A}}]+Sigma pbeta _{pqr}[{ce {A}}]^{p}[{ce {B}}]^{q}[{ce {H}}]^{r}\C_{ce {B}}&=[{ce {B}}]+Sigma qbeta _{pqr}[{ce {A}}]^{p}[{ce {B}}]^{q}[{ce {H}}]^{r}\C_{ce {H}}&=[{ce {H}}]+Sigma rbeta _{pqr}[{ce {A}}]^{p}[{ce {B}}]^{q}[{ce {H}}]^{r}-K_{w}[{ce {H}}]^{-1}end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/3d204f0d1baca5254f67602e86ba0091a004b673)
