Вычислить объем водорода
13,5 грамм цинка (Zn) взаимодействуют с соляной кислотой (HCl). Объемная доля выхода водорода (H2) составляет 85 % . Вычислить объем водорода, который выделился?
Решение задачи
Запишем уравнение реакции взаимодействия цинка (Zn) с соляной кислотой (HCl):
![]()
Напомню, что под выходом продукта реакции понимают отношение массы (объема, числа молей) практически полученного вещества к массе (объему, числу молей), теоретически рассчитанной по уравнению реакции.
Учитывая, что молярная масса цинка (Zn) равна 65 г/моль (смотри таблицу Менделеева), найдем химическое количество цинка (Zn) по формуле, устанавливающей связь между химическим количеством вещества и массой:
![]()
Получаем:
n (Zn) = 13,5 / 65 = 0,2 (моль).
Вычислить объем водорода. По уравнению реакции найдем химическое количество водорода (H2) (теоретический выход), который выделяется в ходе реакции:
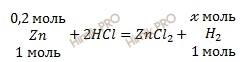
1 моль Zn вытесняет 1 моль водорода (H2)
0,2 моль Zn вытесняет х моль водорода (H2)
Откуда:
![]()
По формуле, устанавливающей связь между химическим количеством вещества и объемом, вычислим объем водорода, который образуется в ходе реакции:
![]()
Получаем:
V теор.(H2) = 0,2 ∙ 22,4 = 4,48 (л).
Вычислим объем водорода практический по формуле:
![]()
Получаем:
V практ. (H2) = 85 ⋅ 4,48 / 100 = 3,81 (л).
Ответ:
объем водорода равен 3,81 литра.
Расчетные задачи типа «Определение выхода продукта реакции в процентах от теоретического»
Признак
В условии задачи встречается слово «выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём, практическая масса или объём» могут быть использованы только для веществ-продуктов.
Доля выхода продукта обозначается буквой
![]()
(эта), измеряется в процентах или долях.
Также для расчётов может использоваться количественный выход:
![]()
I. Первый тип задач
Известны масса (объём) исходного вещества и масса (объём) продукта реакции. Необходимо определить выход продукта реакции в %.
Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5, 5 г. Определите выход продукта реакции (%).
| 1. Записываем краткое условие задачи |
Дано: m (Mg) = 1,2 г m практическая(MgSO4) = 5,5 г _____________________ Найти: |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(Mg) = 24 г/моль M(MgSO4) = 24 + 32 + 4 · 16 = 120 г/моль |
|
4. Находим количество вещества реагента по формулам
|
ν(Mg) = 1,2 г / 24(г/моль) = 0,05 моль |
| 5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
m = ν · M mтеор (MgSO4) = M(MgSO4) · νтеор (MgSO4) = = 120 г/моль · 0,05 моль = 6 г |
|
6. Находим массовую (объёмную) долю выхода продукта по формуле
|
Ответ: Выход сульфата магния составляет 91,7% по сравнению с теоретическим |
II. Второй тип задач
Известны масса (объём) исходного вещества (реагента) и выход (в %) продукта реакции. Необходимо найти практическую массу (объём) продукта реакции.
Задача 2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид кальция массой 16,8 г, если выход составляет 80%.
|
1. Записываем краткое условие задачи |
Дано: m(CaO) = 16,8 г
___________________ Найти: m практ (CaC2) = ? |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
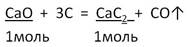 |
|
3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(CaO) = 40 + 16 = 56 г/моль M(CaC2) = 40 + 2 · 12 = 64г/моль |
|
4. Находим количество вещества реагента по формулам
|
ν(CaO)=16,8 (г) / 56 (г/моль) = 0,3 моль |
|
5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
|
|
6. Находим массовую (объёмную) долю выхода продукта по формуле
|
m практич (CaC2) = 0,8 · 19,2 г = 15,36 г Ответ: m практич (CaC2) = 15,36 г |
III. Третий тип задач
Известны масса (объём) практически полученного вещества и выход этого продукта реакции. Необходимо вычислить массу (объём) исходного вещества.
Задача 3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу карбоната натрия нужно взять для получения оксида углерода (IV) объёмом 28,56 л (н. у.). Практический выход продукта 85%.
| 1. Записываем краткое условие задачи |
Дано: н. у. Vm = 22,4 л/моль Vпрактич(CO2) = 28,56 л = 85% или 0,85 ____________________ Найти: m(Na2CO3) =? |
| 2. Находим по ПСХЭ молярные массы веществ, если это необходимо | M (Na2CO3) =2·23 + 12 + 3·16 = 106 г/моль |
|
3. Вычисляем теоретически полученный объём (массу) и количество вещества продукта реакции, используя формулы: |
Vтеоретич(CO2) = = 28,56 л / 0,85 = 33,6 л ν(CO2) = 33,6 (л) / 22,4 (л/моль) = 1,5 моль |
|
4. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 5. Находим количество вещества реагента по УХР |
По УХР:
ν(Na2CO3) = ν(CO2) = 1,5 моль |
|
6. Определяем массу (объём) реагента по формуле: m = ν · M V = ν · Vm |
m = ν · M m(Na2CO3) = 106 г/моль · 1,5 моль = 159 г |
IV. Решите задачи
Задача №1. При взаимодействии натрия количеством вещества 0, 5 моль с водой получили водород объёмом 4,2 л (н. у.). Вычислите практический выход газа (%).
Задача №2. Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно получить при восстановлении его оксида массой 228 г, если практический выход хрома составляет 95 %.
Задача №3. Определите, какая масса меди вступит в реакцию с концентрированной серной кислотой для получения оксида серы (IV) объёмом 3 л (н.у.), если выход оксида серы (IV) составляет 90%.
Задача №4. К раствору, содержащему хлорид кальция массой 4,1 г, прилили раствор, содержащий фосфат натрия массой 4,1 г. Определите массу полученного осадка, если выход продукта реакции составляет 88 %.
Как найти объем водорода
Водород – первый элемент таблицы Менделеева, бесцветный газ. В природе существует в виде трех изотопов, самый распространенный из них – протий. Широко применяется в разных областях промышленности, а также в качестве компонента ракетного топлива. Весьма перспективен и в качестве автомобильного топлива, поскольку продукты сгорания водорода не причиняют вреда окружающей среде. Часто возникает необходимость определить, какой объем водорода потребуется для реакции с тем или иным веществом. Как это можно сделать?

Инструкция
Перед вами стоит следующая задача: сколько литров водорода понадобится, чтобы провести гидрирование 20-и литров этилена? То есть, чтобы осуществить реакцию: С2Н4 + Н2 = С2Н6. Сделайте вывод: и этилен, и водород – газы. Исходя из уравнения реакции и закона Авогадро вы увидите, что объемы прореагировавших газов в данном случае пропорциональны их количествам. Следовательно, требуемый объем водорода такой же, как и объем этилена, и равен двадцати литрам.
Или: определите какой объем водорода выделится при взаимодействии 2,23 граммов натрия с избытком соляной кислоты? Вы видите, что кислота взята в избытке, значит, реакция прошла до конца, то есть было израсходовано все количество натрия, с образованием соли – хлорида натрия – и вытеснением водорода. Запишите уравнение реакции следующим образом: 2Na + 2HCl = 2NaCl + H2
Исходя из коэффициентов, а также из того, что 2,23 грамма натрия составляют 0,1 моля этого вещества, сделайте вывод: выделилось 0,05 моля водорода. Поскольку, согласно закону Авогадро, при нормальных условиях один моль газа занимает 22,4 литра, получите ответ:22,4 * 0,05 = 1,12 литра
Найдите объем, занимаемый водородом, зная его массу. Тут вам на помощь придет универсальное уравнение Менделеева – Клапейрона, описывающее состояние идеального газа. Разумеется, водород не является идеальным газом, но при температурах и давлениях, не слишком отличающихся от нормальных, это уравнение используйте в расчетах. Запишите его следующим образом:PVm = MRT
Путем элементарного преобразования, вы получите нужную формулу: V = MRT/Pm, где M – известная нам масса водорода, R – универсальная газовая постоянная, Т – температура в градусах Кельвина, Р – давление в паскалях, m – молярная масса водорода.
Подставляя в формулу известные вам величины, получите искомый результат.
Видео по теме
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Вычислите объём водорода (н. у.), который может быть получен при растворении в воде 11,5 г натрия, содержащего 2% примесей, если выход водорода составляет 95% от теоретически возможного.
Ответ
Дано:
m(Na) = 11,5 г
ω(примеси) = 0.02
ω(практ.) = 0.95
Найти:
Vпракт.(Н2) — ?
Решение:
1. Найдем массу примеси натрия:
m(примеси) = ω(примеси) · m(Na) = 0,02 · 11,5 = 0,23 г.
2. Найдем массу чистого натрия:
m(Na) = 11,5 − 0,23 = 11,27 г.
3. Уравнение реакции:
2Na + 2Н2O = 2NaOH + Н2↑
M(Na) = 23 г/моль.
Составим пропорцию:
11,27 г Na — x л H2
2 · 23 г/моль Na — 22,4 л H2
x = 11,27 · 22,4/(2 · 23) = 5,49 л.
3. Найдем практический выход:
Vпракт.(Н2) = ω(практ.) · V(H2) = 0,95 · 5,49 = 5,21 л.
Ответ:
Vпракт.(Н2) = 5,21 л.
Опубликовано: 07.11.2018
Обновлено: 07.11.2018

