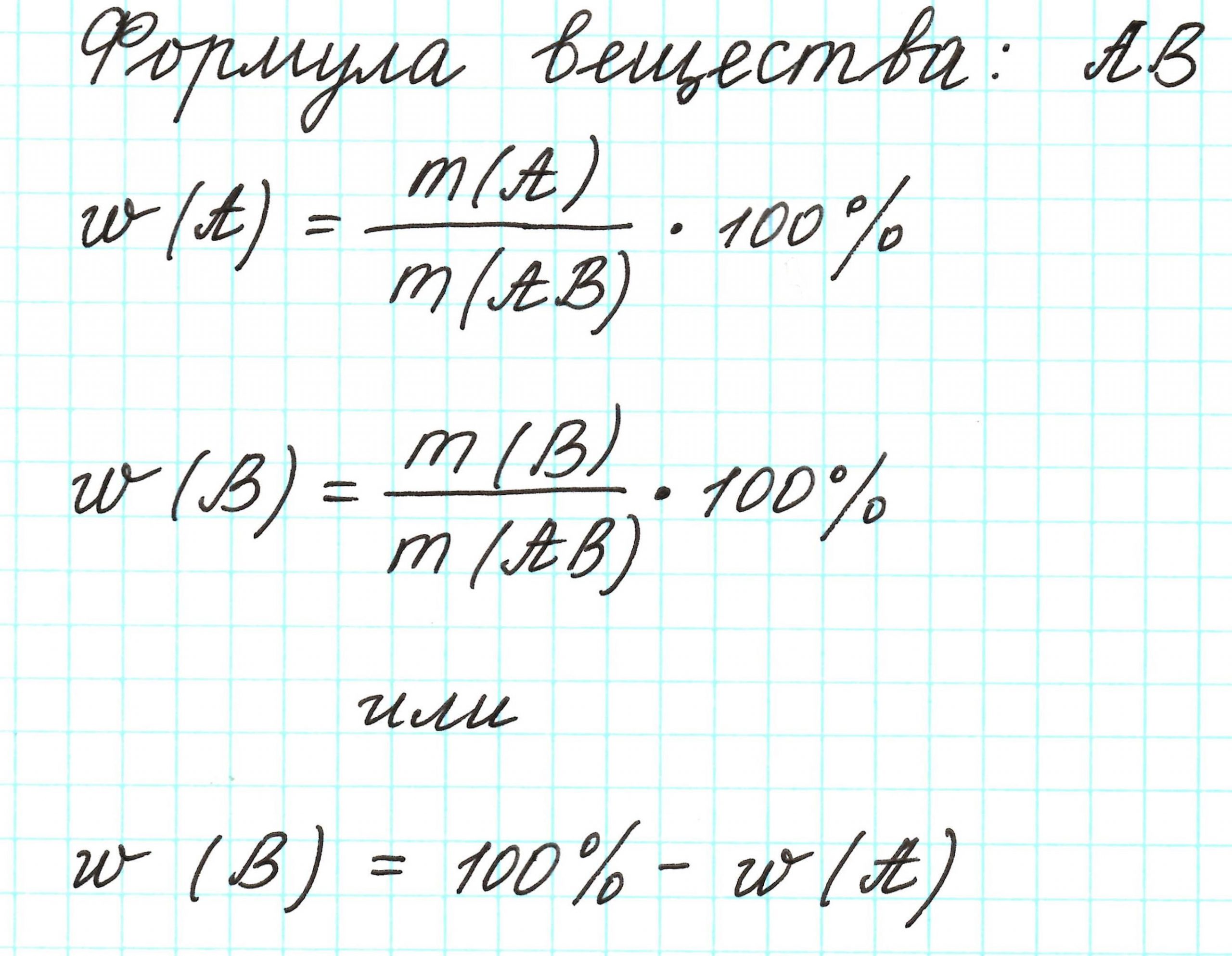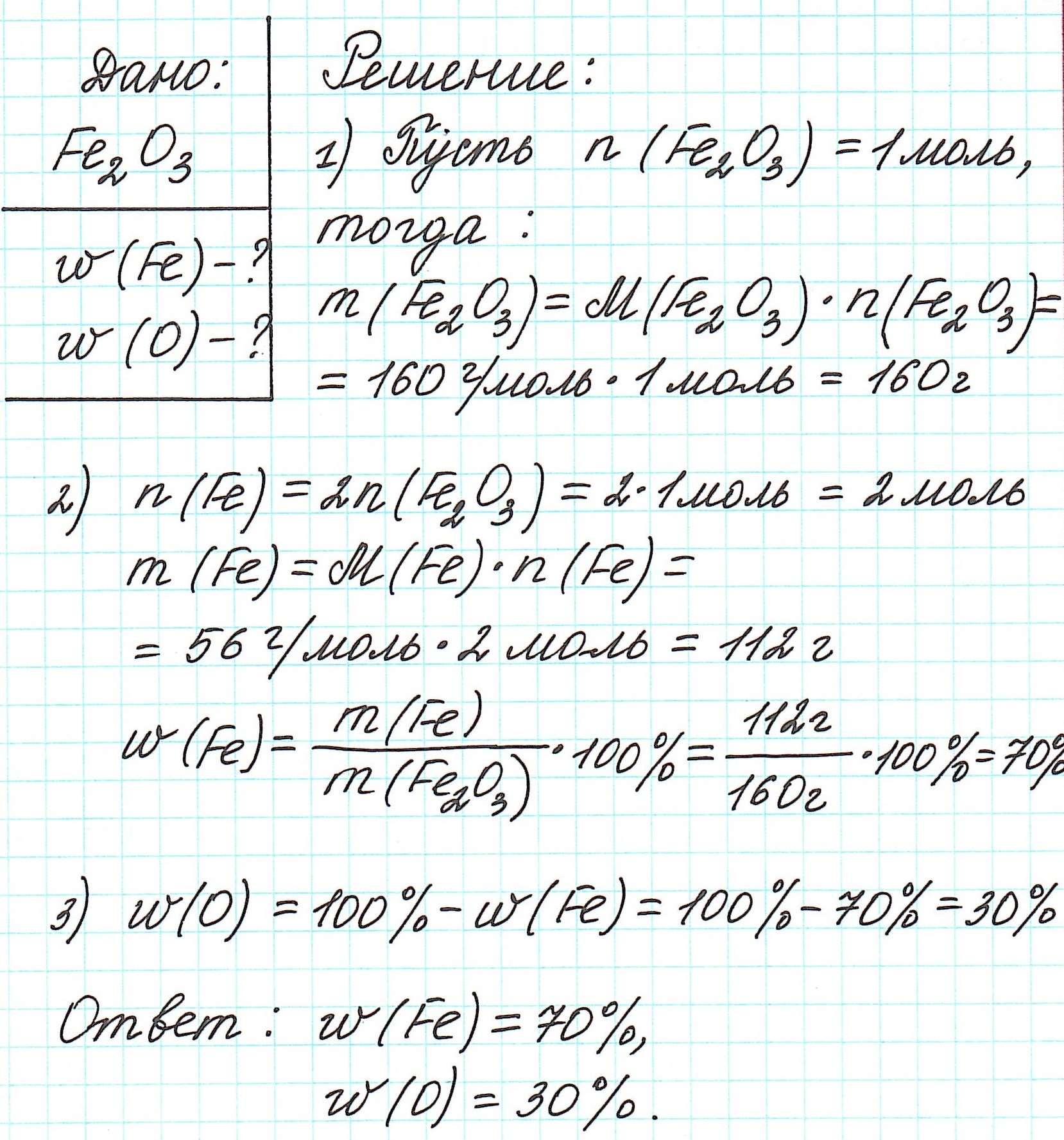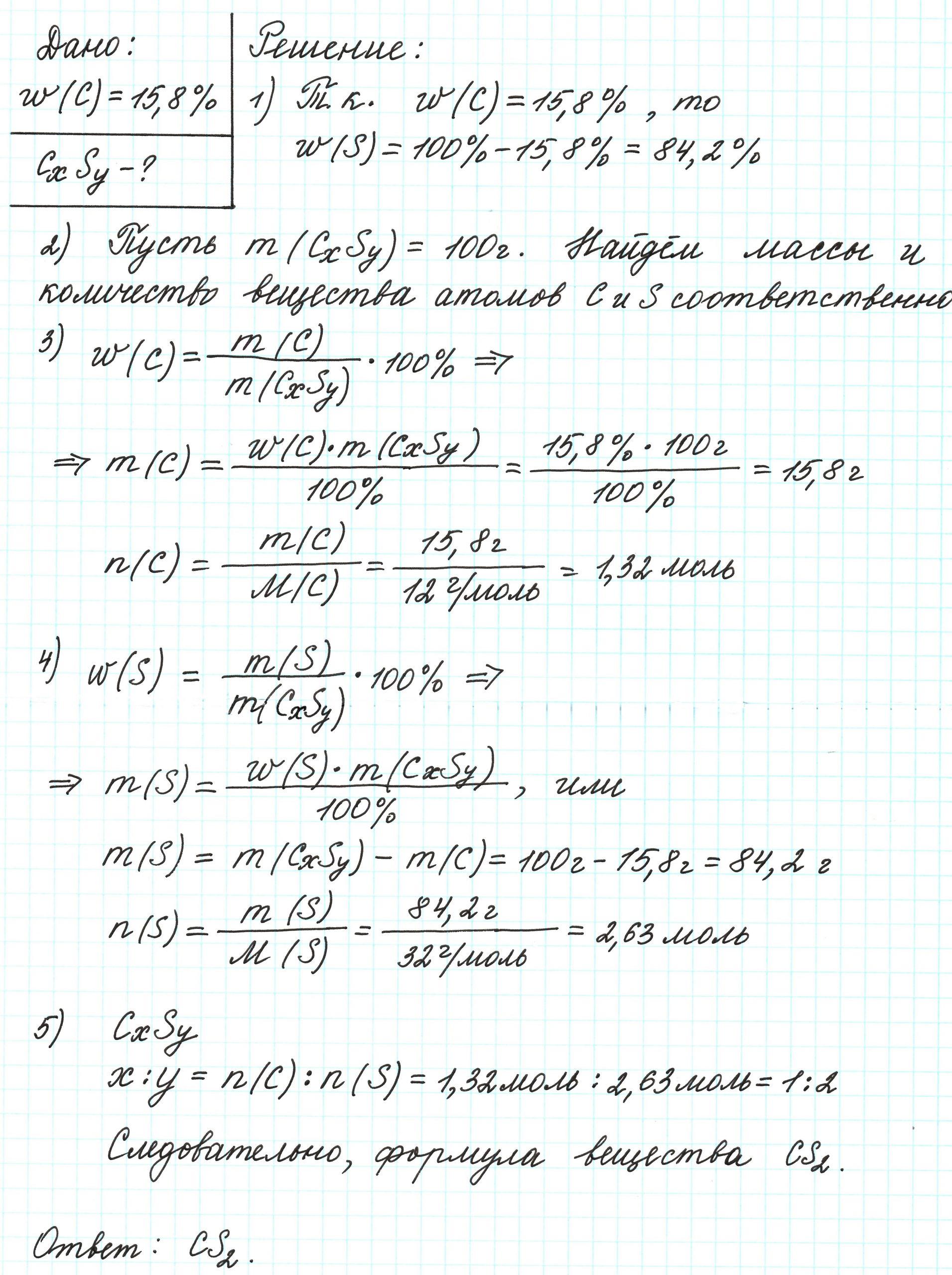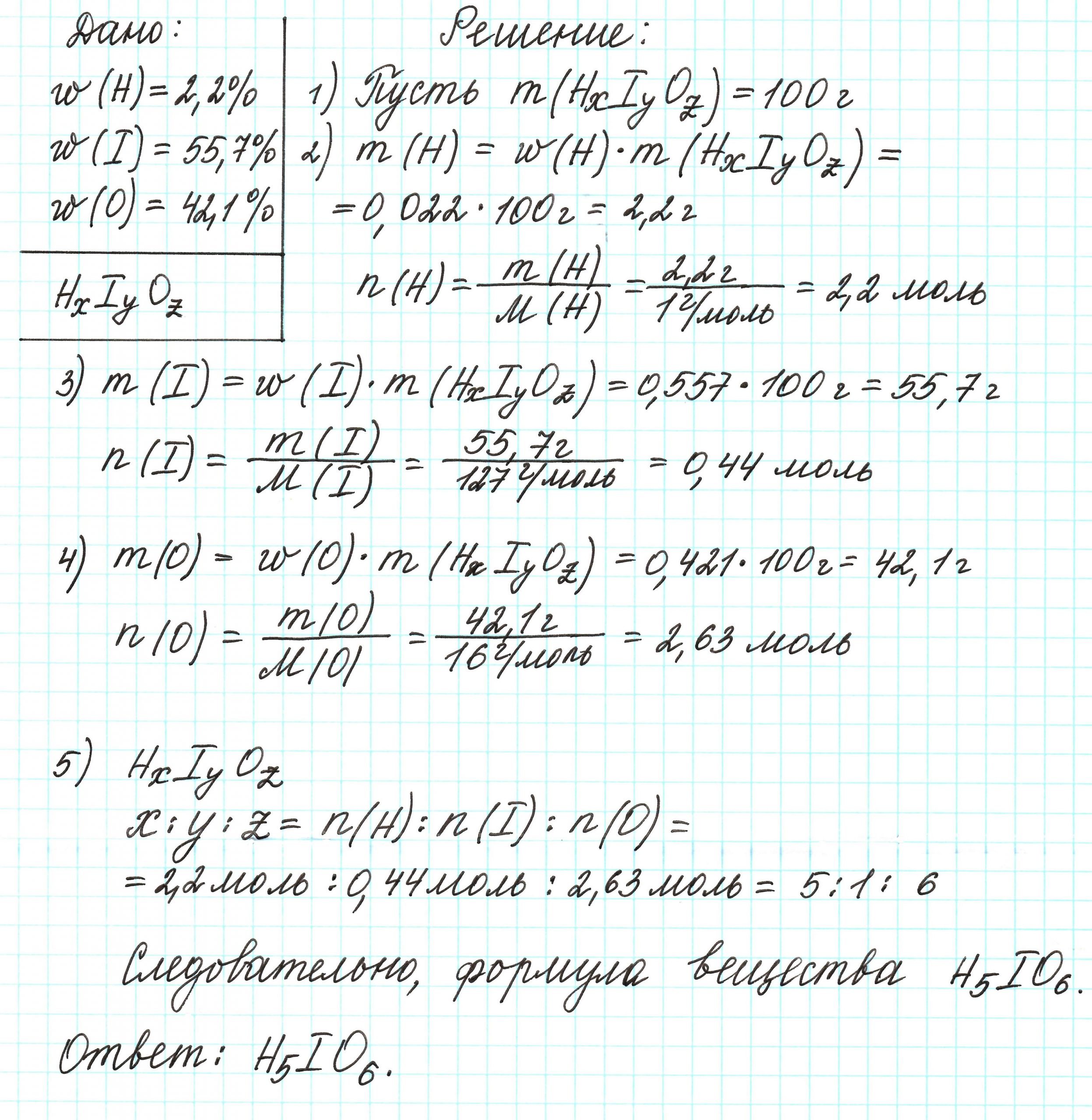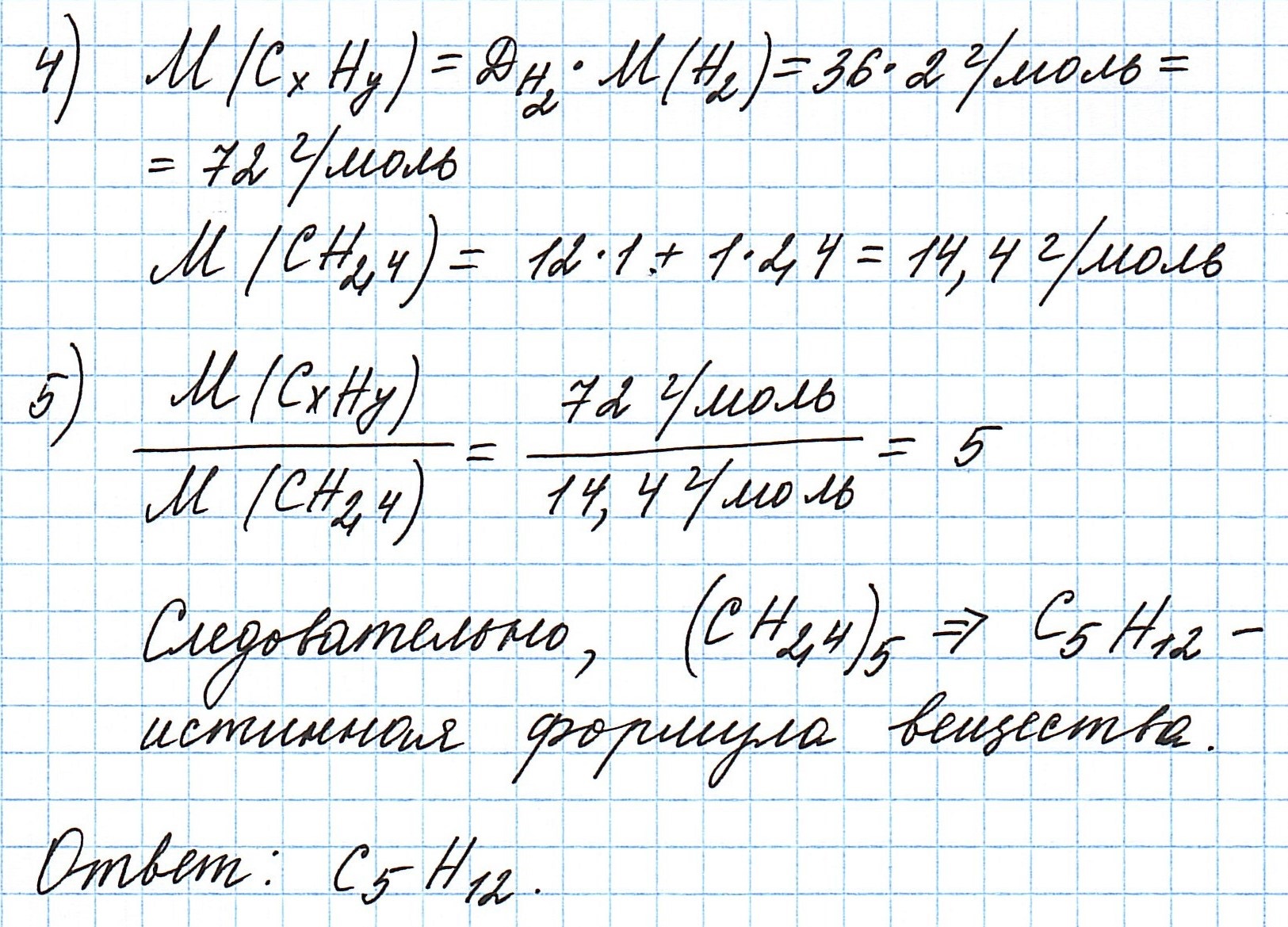Вы хотите изучать химию и профессионально, и с удовольствием? Тогда вам сюда! Автор методики системно-аналитического изучения химии Богунова В.Г. раскрывает тайны решения задач, делится секретами мастерства при подготовке к ОГЭ, ЕГЭ, ДВИ и олимпиадам
А вы знаете, что такое аффирмация?
Аффирмация – это короткая фраза, содержащая словесную формулу (лингвистический код), которая при многократном повторении закрепляет требуемую установку в подсознании.
Как работает аффирмация?
Если сосредоточить свое внимание на действиях (целях, установках), в головном мозге включаются интересные процессы. Между лимбической системой и корой больших полушарий формируются нейронные связи, определяющие конкретные чувства и действия человека. В результате, когда вы думаете о конкретных действиях (установках, целях), мозг начинает вырабатывать особые химические вещества – нейромедиаторы, которые активируют программу достижения ваших целей. Если вы натренируете свой мозг таким образом, чтобы он ассоциировал ваши действия по достижению результата с позитивными чувствами, вы каждый раз будете испытывать чувство радости и удовлетворения, вспоминая о целях, о действиях по достижению целей, о результатах работы. Таким образом, ваше подсознание будет ставить важные цели и действия на первое место среди остальных приоритетов.
Совет психолога
Возьмите ручку в руки и напишите три аффирмации, определяющие ваши цели и действия на ближайшие месяцы. Например:
1) Я хорошо себя чувствую и уверен в своих силах
2) Я буду изучать химию и решать задачи по химии каждый день
3) Я сдам ЕГЭ по химии на очень высокий балл
Прикрепите ваши аффирмации на видное место, например, над компьютером. Каждый день в течение пяти минут вы должны стать перед зеркалом и вслух произнести эти фразы. Произносите слова уверенно, так, словно вы уже достигли поставленных целей. Если вы чувствуете в своем теле дискомфорт, связанный с определенной аффирмацией, поместите свою руку на эту область тела и, в момент произношения фразы, мысленно направьте энергию руки в эту область.
Наверняка, у вас возник вопрос: “Откуда репетитор по химии Богунова В.Г. так хорошо знает психотерапевтические техники?” Отвечу. У меня есть советник. Мой психолог-консультант – Кристина. Это она знакомит меня с тайнами практик психотерапии. Чуть позже я расскажу о Кристине много интересного, а пока вернемся к основной теме статьи – Вывод формулы вещества по массовым долям. Итак, поехали!
Алгоритм решения лучше разобрать на конкретной задаче. Все задачи, конечно, решаются по Четырем Заповедям. Но если алгоритм решения – очень специфичный, лучше акцентировать внимание именно на нем.
Задача 1
Найти простейшую формулу соединения, содержащего 43,4% натрия, 11,3% углерода и 45,3% кислорода.
Выписываем данные в разделе Дано.
Выписываем формулу вещества в общем виде (по данным задачи) и определяем основную логическую структуру алгоритма
Выясняем происхождение каждой составляющей структуры (Как рассчитать количества вещества?). Это – логические рассуждения, как бы мои мысли вслух (т.е. на бумаге), поэтому я их обвела другим цветом.
Количества вещества можно рассчитать, например, из масс, а в задаче предлагаются только относительные данные (массовые доли), поэтому мы имеем право ввести свободный параметр – абсолютное значение массы. Зная массу элемента, легко рассчитать его количество вещества.
Поскольку максимальное значение массовой доли 100%, лучше ввести значение массы 100 г, тогда абсолютные значение массы элемента и его массовой доли в % – равны (по модулю).
Дальнейшее решение задачи лучше проводить в таблице, куда выписываем массы (бывшие массовые доли в %), молярные массы, рассчитанные количества вещества. Нужно как можно точнее рассчитать значение количество вещества (не менее трех знаков после запятой).
Теперь начинается Копперфильд, т.е. самое интересное и загадочное. Нам нужно привести к целым значениям соотношения количества вещества каждого элемента. Как это сделать? Внимательно слушаем и повторяем за мной на калькуляторе.
Как получить целые значения в дробных соотношениях?
Каждый показатель количества вещества делим на самое маленькое число из всех полученных значений
В нашем случае, самое маленькое число 0,9417. Делим каждый показатель на это число и получаем целые значения соотношений. После этого выводим простейшую формулу вещества. В представленных задачах простейшая формула является окончательной. Называем вещество.
Иногда (не часто) с первого раза не удается добиться целого результата. Тогда нужно умножить каждый показатель на наименьшее целое число, чтобы получить целые соотношения. Все вопросы – к математике.
Если делимое и делитель умножить (или разделить) на одно и тоже число, то частное не изменится
Попробуем решить еще одну задачу на закрепление мастерства.
Задача 2
Найти простейшую формулу соединения, содержащего 27,38% натрия, 1,19% водорода, 14,29% углерода и 57,14% кислорода.
Последовательность действий:
1) Выписать данные в разделе Дано
2) Составить логическую структуру алгоритма
3) Выяснить источник для расчета количества вещества атомов элемента
4) Ввести свободный параметр (Пусть было 100 г вещества)
5) Составить таблицу (масса, молярная масса, количество вещества)
6) Рассчитать целые значения соотношений количества вещества
7) Вывести простейшую формулу вещества
Надеюсь, вы поняли, как работать с алгоритмом Вывод формул вещества по массовым долям элементов? Если нет, пишите в комментариях или ВКонтакте в личку. Я обязательно отвечу на все ваши вопросы, замечания и пожелания.
Вернемся к моему другу, психотерапевту Кристине. Звонит мне как-то моя хорошая знакомая. С ее сыном случилась страшная беда – наркотики. Правда, не очень тяжелые, но все же… Из дома начали пропадать вещи, сын стал грубить, успеваемость съехала до нижнего предела. Что делать?! Не хочется выносить сор из избы (элитная школа, папа занимает солидную должность, мама – достаточно известная личность). Она не просила меня ни о чем, позвонила больше для того, чтобы выплакаться. Я, конечно, как могла, поддержала ее. Но одного моего сочувствия мало. И тут я вспомнила о Кристине. Я давно знаю эту уже взрослую девочку. Знаю ее непростую судьбу, ее серьезную психологическую практику. Я дала своей знакомой телефон Кристины. Они созвонились.
Пол-года я не получала никакой информации ни от одной, ни от другой. Сама боялась позвонить и услышать о самом страшном. Однажды утром раздался звонок и счастливый голос подруги радостно сообщил мне о том, что ее сын стал студентом престижного московского ВУЗа! Именно Кристина спасла “тонущего” мальчика и всю семью. “Я каждое воскресенье хожу в церковь и ставлю свечки за здравие всех родных, в том числе, за здравие нашей спасительницы Кристины!” – сказала мне знакомая. С тех пор я советую Кристину всем своим близким и знакомым.
Вы готовитесь к ЕГЭ и хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии. Здесь вы найдете огромное количество задач, заданий и теоретического материала, познакомитесь с моими учениками, многие из которых уже давно работают врачами. Звоните мне +7 (903) 186-74-55. Приходите ко мне на курс, на Мастер-классы “Решение задач по химии” – и вы сдадите ЕГЭ с высочайшими баллами, и станете студентом престижного ВУЗа!
PS! Если вы не можете со мной связаться из-за большого количества звонков от моих читателей, пишите мне в личку ВКонтакте или на Facebook. Я обязательно отвечу вам.
Репетитор по химии и биологии кбн В.Богунова
Способов, как определить формулу вещества, достаточно много. Все зависит от исходных данных. Наиболее разнообразны подобные вычисления в органической химии. И это не удивительно, так как органических соединений значительно больше, чем неорганических.
Содержание:
1.Понятие простейшей и истинной формулы вещества
2.Массовая доля химического элемента: что означает и как высчитывается
3.Как определить формулу вещества по массовым долям элементов
4.Как определить формулу органического соединения:
4.1. по общей формуле вещества
4.2. по продуктам сгорания вещества
5. Как определить формулу вещества: комбинированные задачи
1.Понятие простейшей и истинной формулы вещества
В одних задачах на определение формулы вещества необходимо найти его простейшую формулу, а в других – истинную. В чем разница?
Простейшая, или иными словами, эмпирическая формула, указывает на соотношение атомов в молекуле (или в формульной единице, если речь идет о не ковалентном соединении).
Так, например: СН2 – простейшая формула алкена – показывает, что на каждый 1 атом углерода приходится 2 водородных атома. То есть существует соотношение 1:2. Поэтому для нахождения простейшей (эмпирической) формулы вещества важно рассчитать количество вещества атомов, которые входят в его состав, то есть n(C) и n(H).
Истинная формула, или иначе молекулярная, отражает действительное количество атомов всех элементов в молекуле.
Например, для пропилена, относящегося к классу алкенов, истинная (молекулярная) формула будет C3H6. Она говорит о том, что молекула данного вещества включает 3 атома С и 6 атомов Н. Это вполне соответствует простейшей формуле, отвечающей соотношению атомов 1:2. Для нахождения истинной (молекулярной) формулы соединения требуется посчитать его относительную молекулярную (Mr) или молярную массу (M).
2.Массовая доля химического элемента: что означает и как высчитывается
Массовая доля – это отношение массы компонента системы к массе системы, выраженное в процентах или долях от единицы.
Ну, а теперь проще.
Молекула имеет массу. Все атомы в молекуле также имеют свои массы. Атомов одного химического элемента в молекуле может быть 1 или несколько. Важна масса всех атомов одного элемента. Если ее разделить на массу молекулы, то получится массовая доля этого элемента. Ее выражают либо в процентах, которые всегда меньше 100%, либо в долях от единицы, которые всегда меньше 1.
Массовая доля элемента обозначается греческой буквой «омега» — ω. И записывается, например, так: ω(Н), ω(Сl), ω(С) и т.д. и рассчитывается:
Пример 1. Каковы массовые доли элементов в оксиде железа (III) Fe2O3.
3.Как определить формулу вещества по массовым долям элементов
Нахождение формулы вещества по массовым долям элементов применимо как к органическим, так и к неорганическим соединениям.
Пример 2. Сероуглерод содержит 15,8% углерода по массе. Какова простейшая формула этого вещества?
Поскольку речь идет о массовых долях элементов, то необходимо знать массу вещества. В нашем случае – массу сероуглерода. В условии задачи о ней ничего не говорится. Поэтому допускаем, что масса вещества равна 100 г.
Почему 100 г? Это «круглое» число, и его использование облегчает все расчеты. Так как в итоге будем находить соотношения количеств веществ элементов, то какое-то особенное значение массы вещества не играет никакой роли.
Попробуйте ради эксперимента принять массу сероуглерода равной 23 г, 467 г и т.п. Результат будет один и тот же.
Допустим, что атомов углерода в молекуле х, а атомов серы – у. В таком случае формула вещества примет вид: СхSу.
Пример 3. Содержание углерода в углеводороде составляет 83,33%. Плотность паров соединения по водороду – 36. Какова молекулярная формула углеводорода?
Из данных задачи следует, что углеводород может находиться в газообразном состоянии, так как известна плотность его паров. Эта величина всегда требуется для нахождения молярной (относительной молекулярной) массы вещества. Как она находится и что это такое читайте подробнее здесь.
Чтобы не загромождать записи, массовую долю элементов будем считать не в процентах, а в долях от единицы.
Пусть вас не удивляет получившаяся простейшая формула. Ведь, исходя из определения простейшей формулы, на каждый 1 атом углерода приходится 2,4 атома водорода. Это всего лишь соотношение. Соединения с формулой СН2,4 в принципе не существует. Не всегда простейшая и истинная формулы совпадают друг с другом.
А если полученная формула СН2,4 вас все же смущает, вы можете решать задачу и вторым способом. Но это несколько более сложный способ, когда требуется составить и решить уравнение с двумя неизвестными.
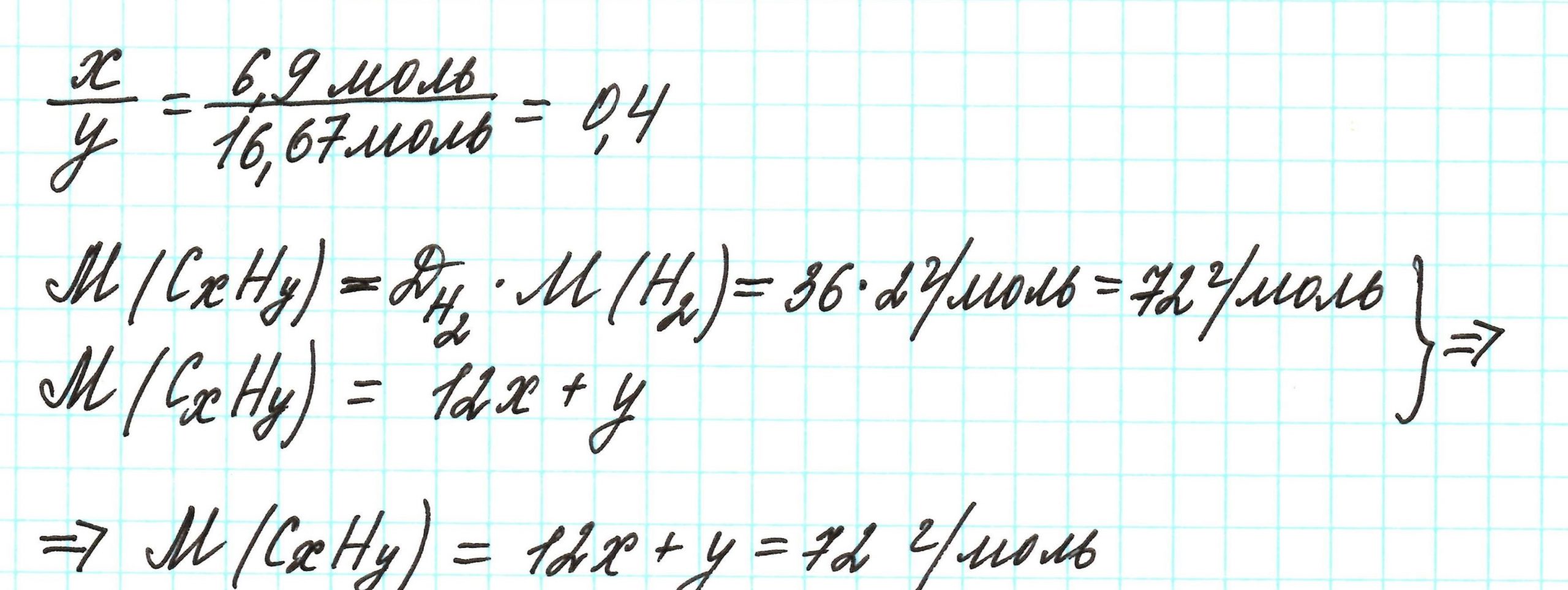
Не все химические вещества являются бинарными, то есть состоят из атомов двух химических элементов. Но в любом случае, алгоритм решения задачи тот же.
Пример 4. Некоторая кислота содержит водород (2,2%), иод (55,7%) и кислород (42,1%). Определите простейшую формулу этой кислоты.
4.Как определить формулу органического соединения
Определить формулу органического вещества можно не только зная массовые доли элементов в его составе.
4.1. Как определить формулу органического соединения
по общей молекулярной формуле вещества
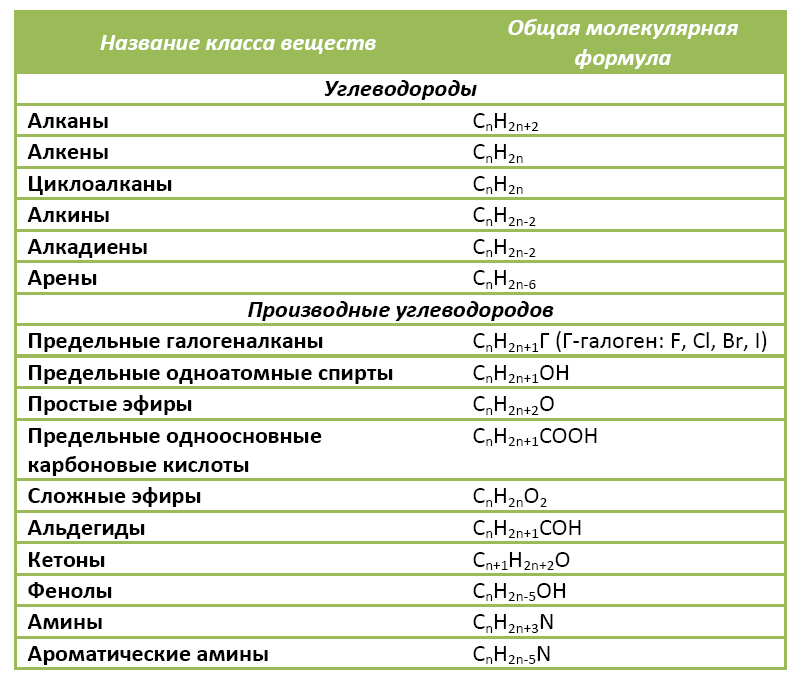
Органические вещества сгруппированы по самостоятельным классам на основе общности строения и свойств. Каждый класс соединений характеризуется своей общей молекулярной формулой. Особенно это наглядно видно на примере углеводородов.
Если другие органические вещества рассматривать как их производные, в молекулы которых введена какая-либо функциональная группа, то и для них также можно составить общую молекулярную формулу.
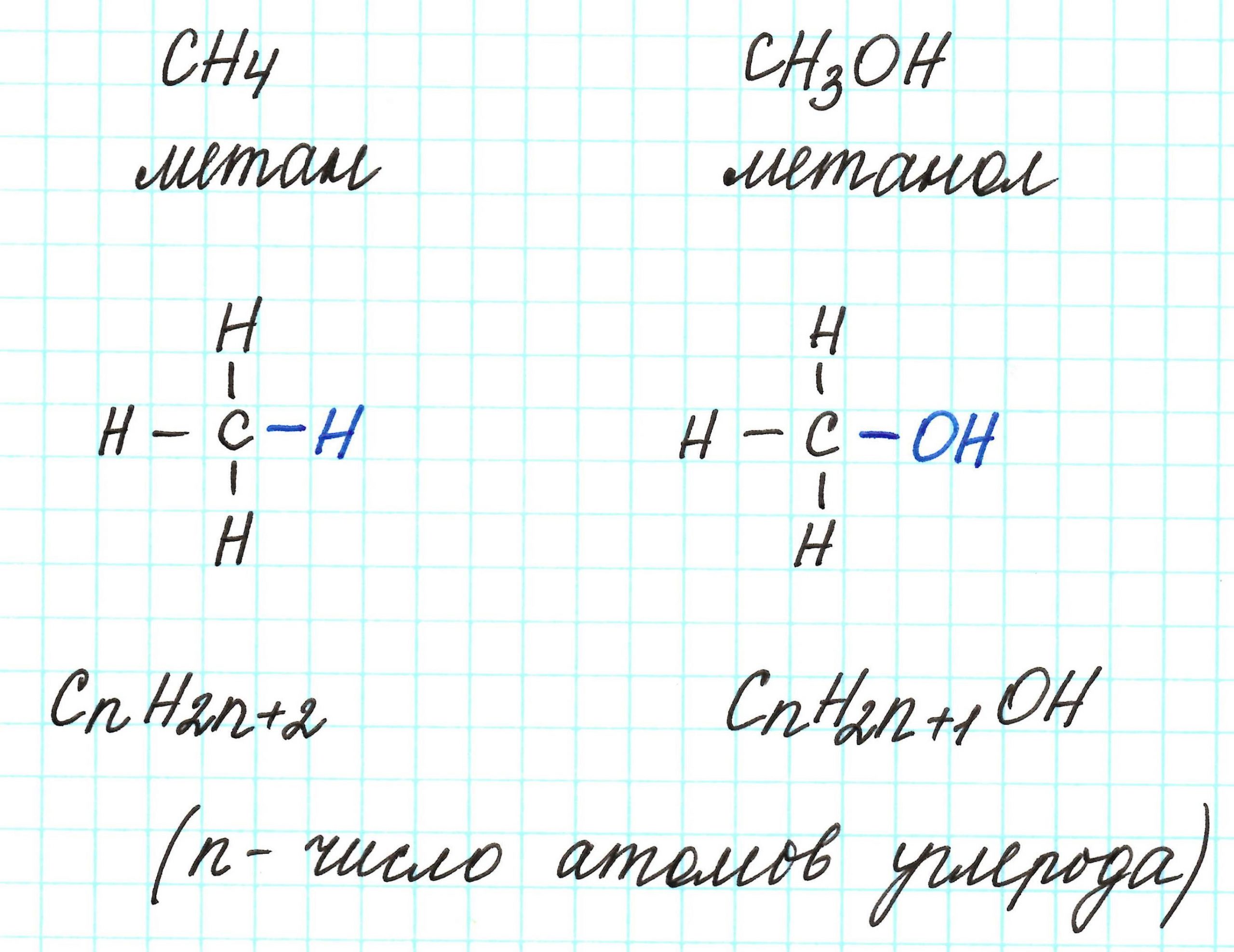
К слову, метан СН4 является представителем алканов, в молекулах которых на n атомов углерода и приходится 2n+2 атомов водорода. Алканы имеют общую молекулярную формулу, отражающую их состав: СnH2n+2.
Предельные одноатомные спирты можно рассматривать как производные алканов, в молекулах которых 1 атом водорода замещен на гидроксильную группа –ОН. Таким образом, их общая молекулярная формула такая: СnH2n+1ОН.
Ниже в таблице приведены общие молекулярные формулы основных классов органических соединений.
Пример 5. Плотность паров по воздуху некоторого алкана 4,414. Какова формула алкана?

4.2. Как определить формулу органического соединения
по продуктам его сгорания
Это еще один распространенный тип задач на определение формулы органического соединения.
Необходимо запомнить и понять основные моменты:
— так как все органические вещества содержат атомы С, Н, а также атомы О (кислородсодержащие соединения), то всегда при их сгорании выделяется углекислый газ СО2 и образуется вода Н2О;
— все углеродные атомы, входящие в состав органического соединения, окажутся в составе углекислого газа СО2; следовательно, n(С) как в соединении, так и в СО2 – это одна и та же величина;
— все атомы водорода Н, которые имеются в составе вещества, перейдут в состав воды Н2О; следовательно, n(Н) и в данном веществе, и в Н2О – это одна и та же величина;
— при сгорании веществ, включающих в себя азот (например, амины), кроме СО2 и Н2О, образуется еще и N2.
Разберем несколько примеров.
Пример 6. Сожгли 7,2 г углеводорода. Плотность его паров по водороду составляет 36. В результате реакции образовалось 22 г оксида углерода (IV) и 10,8 г воды. Какова молекулярная формула соединения?
Пример 7. В результате сгорания 4,8 г органического соединения выделилось 3,36 л (н.у.) оксида углерода (IV) и образовалось 5,4 г воды. Плотность паров искомого соединения по кислороду равна 1. Вычислите молекулярную формулу вещества.
Пример 8. Результатом сжигания 0,31 г газообразного органического соединения, имеющего плотность 1,384 г/л, стало выделение 0,224 л (с.у.) оксида углерода (IV), 0,112 л азота и образование 0,45 г воды. Вычислите молекулярную формулу этого вещества.

5. Как определить формулу вещества: комбинированные задачи
Наибольший интерес и некоторую трудность представляют комбинированные задачи, сочетающие в себе необходимость найти формулу соединения:
— используя приемы, применяемые в рассмотренных выше задачах;
— используя сведения не только о химических, но и физических свойствах вещества.
Вот несколько примеров.
Пример 9. Какова молекулярная формула предельного углеводорода, при полном сгорании 8,6 г которого выделилось 13, 44 л (н.у.) оксида углерода (IV).
В этой задаче:
1) известен класс вещества, поэтому возможно применить его общую молекулярную формулу;
2) речь идет о сгорании вещества, поэтому количество атомов в составе молекулы будем искать, используя данные о продукте сгорания – СО2.
Пример 10. Алкен нормального строения содержит двойную связь при первом углеродном атоме. Образец этого алкена массой 0,7 г присоединил бром массой 1,6 г. Вычислите формулу алкена и назовите его.
В предлагаемых условиях:
1) известен класс вещества, следовательно, применим его общую молекулярную формулу;
2) речь идет об одном из химических свойств: способности алкенов присоединять галогены по месту разрыва двойной связи.
Пример 11. После полного сжигания в кислороде арена, имевшего массу 0,92 г, выделился оксид углерода (IV). Пропуская газ через избыток раствора щелочи Ca(OH)2, получили 7 грамм осадка. Какова молекулярная формула арена?
В предлагаемой задаче:
1) известен класс вещества;
2) речь идет о сжигании соединения и образовании в качестве продукта горения углекислого газа, который при взаимодействии со щелочью Са(ОН)2 привел к выпадению осадка известной массы.
Следующий пример очень характерен для задач, встречающихся в заданиях второй части ЕГЭ по химии.
Пример 12. Некоторое соединение, образующее альдегид в реакции окисления, взаимодействует с избытком бромоводородной кислоты, образуя 9,84 г продукта (выход составляет 80% от теоретического), имеющего плотность паров по Н2 61,5. Определите строение этого соединения, а также его массу, вступившую в реакцию?
В этой задаче:
1) говорится о химических свойствах искомого соединения; анализируя их, приходим к выводу, что заданным веществом является предельный одноатомный спирт;
2) известна общая молекулярная формула предельных одноатомных спиртов;
3) более подробно говорится о взаимодействии заданного вещества с бромоводородной кислотой; спирт, реагируя с HBr, дает галогеналкан, для которого известны его масса, практический выход и относительная плотность по Н2; именно от этих данных и нужно отталкиваться при решении данной задачи.
Итак, способов, как определить формулу вещества, действительно, множество. Мы рассмотрели лишь основные из них. Важно правильно уяснить понятия «простейшая формула вещества» и «истинная формула вещества», чтобы не путать их.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
определим молекулярную формулу углеводорода, в котором содержится (85,71)
%
углерода и (14,29)
%
водорода. Известно, что относительная плотность этого углеводорода по воздуху составляет (0,966).
Первый вариант решения
1. В веществе содержатся только атомы углерода и водорода, значит, его формулу можно записать так —
CxHy
. Индексы в формуле показывают отношение количеств атомов:
x:y=n(C):n(H).
По массовым долям определяем, что в (100) г углеводорода содержится (85,71) г углерода и (14,29) г водорода.
Найдём количества этих элементов:
x=m(C)Ar(C)=85,71 г12 г/моль=7,1425 моль;
y=m(H)Ar(H)=14,29г1г/моль=14,29моль;
x:y=7,1425:14,29=7,14257,1425:14,297,1425=1:2.
Значит, простейшая формула углеводорода —
CH2
.
2. Определим относительную молекулярную массу вещества и сравним её с массой
CH2
:
Mr(CxHy)=Dвозд.(CxHy)⋅Mr(возд.)=0,966⋅29=28,014≈28.
Mr(CxHy)Mr(CH2)=2814=2.
Следовательно, молекулярная формула вещества
(CH2)2=C2H4.
Второй вариант решения
1. Определим относительную молекулярную массу углеводорода:
Mr(CxHy)=Dвозд.(CxHy)⋅Mr(возд.)=0,966⋅29=28,014≈28.
2. Найдём число атомов углерода и водорода в молекуле:
x=Mr(C)⋅w(C)Ar(C)⋅100%=28⋅85,71%12⋅100%=2;
y=Mr(CxHy)⋅w(H)Ar(H)⋅100%=28⋅14,29%1⋅100%=4.
Подготовка к ЕГЭ:
-
выполнение заданий высокого уровня
сложности, задачи на вывод формул.
Задачи на вывод формул соединений –
это задания С5 из 3 части экзаменационной
работы ЕГЭ.
При выводе формул нужно различать
простейшую и
истинную
формулы.
Простейшая формула показывает соотношение
числа атомов каждого элемента.
Истинная формула показывает точный
количественный состав. Например,
простейшая формула бензола СН, она
показывает, что на один атом углерода
в молекуле бензола приходится один атом
водорода. Истинная формула бензола,
показывающая точный количественный
состав молекулы – С6Н6.
Чтобы установить истинную формулу,
нужно знать истинную молекулярную
(молярную) массу, она в целое число раз
больше массы, найденной по простейшей
формуле. На это число нужно умножить
индексы в простейшей формуле, чтобы
получить истинную формулу. Если в условии
задачи нет данных для нахождения истинной
молярной массы, а найденная простейшая
формула явно не соответствует истинной,
то полученные индексы нужно увеличить
в два раза. Например, получилась простейшая
формула С3Н7, значит истинная
будет С6Н14
При всём многообразии задач на вывод
формул можно выделить несколько основных
типов. Рассмотрим алгоритмы решений
этих задач наиболее простыми способами.
-
Написать формулу вещества, обозначив
индексы через x, y,
z. -
Если неизвестна массовая доля одного
из элементов, то её находят, отняв от
100 % известные массовые доли.
3. Найти соотношение индексов, для
этого массовую долю каждого элемента
(лучше в %) разделить на его атомную массу
(округлить до тысячных долей)
x : y: z
= ω1 / Ar1
: ω2 / Ar2
: ω3 / Ar3
4. Полученные числа
привести к целым. Для этого разделить
их на наименьшее из полученных чисел.
При необходимости (если опять получилось
дробное число) после этого домножить
до целого числа на 2, 3, 4 … .
5. Получится простейшая формула.
Для большинства неорганических веществ
она совпадает с истинной, для органических,
наоборот, не совпадает.
Задача № 1.
Массовая доля азота в оксиде азота равна
36,84 % . Найти формулу данного оксида.
Дано:
ω
(N)
= 36,84 % Решение:
1. Напишем формулу:
NxOy
М.Ф. = ? 2. Найдём
массовую долю кислорода:
ω(О) = 100 % – 36,84 % =
61,16 %
3. Найдём соотношение
индексов:
x : y
= 36,84 / 14 : 61,16 / 16 = 2,631: 3,948 =
2,631 / 2,631: 3,948 / 2,631 = 1:
1,5 =
= 1 ∙ 2 : 1,5 ∙ 2 = 2 : 3
N2O3
Ответ: N2O3.
Задача № 2.
Установите формулу неорганического
соединения, содержащего 20 % магния, 53,33
% кислорода и 26,67 % некоторого элемента.
Дано:
ω
(Mg)
= 20 % Решение:
ω(O) = 53,33 %
1. Напишем формулу: Mgx
Эy Оz.
ω(э) = 26,67 % 2. Найдём
соотношение индексов магния и кислорода:
х : у = 20 / 24 : 53,33 / 16 =
0,83 : 3,33 = 1 : 4.
М.Ф. = ? 3. Найдём молекулярную
массу вещества, исходя из значения
массовой доли магния:
ω(Mg) = Ar(Mg)
∙ индекс / Mr
Mr = Ar(Mg) ∙
индекс / ω
= 24 ∙ 1 / 0,2 = 120.
4. Найдём
атомную массу неизвестного элемента:
ω(Э) = Ar(Э)
∙ индекс / Mr
Ar(Э) ∙ индекс =
= ω(Э) ∙ Мr
= 0,2667 ∙ 120 = 32 элемент
– сера.
Ответ: MgSO4.
Задача № 3.
Массовая доля углерода в углеводороде
равна 83,72 %. Найти молекулярную формулу
углеводорода.
Д
ано:
Решение:
ω(С) = 83,72 % 1. Напишем формулу –
СхНу
2. Найдём массовую
долю водорода:
М.Ф. = ? ω(Н) = 100 % – 83,72 % = 16,28 %
3. Найдём соотношение
индексов:
х : у = 83,72 / 12 : 16,28 / 1
= 6,977 : 16,28 = 1 : 2,333 = 3 : 7
4. Простейшая
формула – С3Н7, но
она не соответствует истинной.
Выход – увеличить
индексы в 2 раза
С6Н14.
Ответ: С6Н14.
Задача № 4.
Массовая доля фосфора в его оксиде
равна 43,66 %. Какова формула оксида?
Ответ: Р2О5.
Задача № 5.
Определить формулу вторичного
амина, массовые доли углерода, водорода
и азота, в котором составляют 61; 15,3 и
23,7 % соответственно.
Ответ: CH3
– NH – C2H5.
Задача № 6.
Массовая доля углерода в диеновом
углеводороде составляет 88,89 %. Найти
молекулярную формулу диена.
Ответ: С4Н6.
II. Вывод формул
веществ по массовым долям элементов и
данным для нахождения истинной молярной
массы (плотности,
массе и объёму газа или относительной
плотности).
-
Найти истинную молярную массу:
-
если известна плотность:
= m / V = M
/ Vm
M
= ∙
Vm
= г/л
∙ 22,4 л/моль
если известна масса и объём
газа, молярную массу можно найти двумя
способами:
– через плотность
= m / V, M
= ∙ Vm;
– через количество вещества:
= V / Vm, M
= m / .
-
если известна относительная плотность
первого газа по другому:
D21
= M1
/ M2
M1
= D2
∙ M2
M =
DH2
∙ 2 M = DO2
∙ 32
M
= Dвозд. ∙
29 M = DN2
∙ 28 и т.д.
2. Найти простейшую формулу вещества
(см. предыдущий алгоритм) и его молярную
массу.
3. Сравнить истинную молярную массу
вещества с простейшей и увеличить
индексы в нужное число раз.
Задача № 1.
Найти формулу углеводорода, в котором
содержится 14,29 % водорода, а его
относительная плотность по азоту равна
2.
Дано:
ω
(Н)
= 14,29 % Решение:
D(N2)
= 2 1. Найдём истинную молярную
массу СхНу :
М = DN2
∙ 28 = 2 ∙ 28 = 56 г/моль.
М.Ф. = ? 2. Найдём массовую
долю углерода:
ω(С) = 100 % – 14,29 % = 85,71 %.
3. Найдём простейшую
формулу вещества и его молярную массу:
х : у = 85,7 / 12 : 14,29 / 1 = 7,142 : 14,29 = 1 :
2 СН2
М(СН2) = 12 + 1 ∙ 2 = 14 г/моль
4. Сравним молярные
массы:
М(СхНу)
/ М(СН2) = 56 / 14 = 4
истинная формула – С4Н8.
Ответ: С4Н8.
Задача № 2.
Массовая доля углерода в углеводороде
– 87,5 %, а относительная плотность
углеводорода по воздуху равна 3,31.
Определить формулу вещества.
Ответ: C7H12.
Задача № 3.
Определить молекулярную формулу амина,
массовые доли углерода, азота и водорода
в котором составляют 38,7; 45,15 и 16,15 %
соответственно. Относитель-
ная плотность его паров по воздуху равна
1,069.
Ответ: CH3NH2.
Задача № 4.
Определите формулу углеводорода,
массовая доля водорода в котором
составляет 14,3 %. Относительная плотность
этого вещества по водороду равна 21.
Ответ: С3Н6.
Задача № 5.
Относительная плотность паров
углеводорода по воздуху равна 3,31, а
массовая доля водорода в нём равна 12,5
%. Определите молекулярную формулу
углеводорода.
Ответ: С7Н12.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
12.02.2015398.43 Кб275.pdf
- #
- #
- #
- #
- #
- #
- #
- #
В химии простейшая формула химического соединения — формула с простейшим положительным целочисленным соотношением атомов, присутствующих в соединении[1]. Простым примером этой концепции является то, что простейшая формула монооксида серы, или SO, будет просто SO, как и простейшая формула диоксида дисеры, S2O2. Таким образом, оксид серы и диоксид дисеры, оба являющиеся соединением серы и кислорода, имеют одну и ту же простейшую формулу. Однако их химические формулы, которые выражают количество атомов в каждой молекуле химического соединения, не совпадают.
В простейшей формуле ничего не говорится о расположении или количестве атомов. Она стандартна для многих ионных соединений[en], таких как хлорид кальция (CaCl2), и для макромолекул, таких как диоксид кремния (SiO2).
С другой стороны, химическая формула показывает количество атомов каждого вещества в молекуле. Структурная формула показывает расположение атомов в молекуле. Как показано выше, вполне возможно, что разные типы соединений имеют одинаковые простейшие формулы.
Для того, чтобы определить, сколько процентов каких элементов содержит образец, он анализируется при помощи элементного анализа.
Примеры[править | править код]
- Глюкоза (C6H12O6), рибоза (C5H10O5), уксусная кислота (C2H4O2) и формальдегид (CH2O) имеют разные химические формулы, но одну и ту же простейшую формулу: CH2O. Это реальная химическая формула формальдегида, но у уксусной кислоты количество атомов в два раза больше, у рибозы в пять раз, а у глюкозы в шесть раз больше атомов.
- Химическое соединение н-гексан имеет структурную формулу CH3CH2CH2CH2CH2CH3, которая показывает, что он имеет 6 атомов углерода, расположенных в цепочку, и 14 атомов водорода. Химическая формула гексана — C6H14, а его простейшая формула — C3H7, что говорит о соотношении C:H как 3:7.
Пример расчета[править | править код]
Химический анализ образца метилацетата даёт следующие элементные данные: 48,64 % углерода (C), 8,16 % водорода (H) и 43,20 % кислорода (O). Для определения простейшей формулы предположим, что у нас есть 100 граммов соединения. В этом случае проценты будут соответствовать массе каждого элемента в граммах.
- Шаг 1: Замените каждый процент на массу каждого элемента в граммах. То есть 48,64 % C превращается в 48,64 г C, 8,16 % H превращается в 8,16 г H, а 43,20 % O превращается в 43,20 г O.
- Шаг 2. Преобразуйте количество каждого элемента в граммах в его количество в молях:
- Шаг 3. Разделите каждое из полученных значений на наименьшее из них (2.7):
- Шаг 4: При необходимости умножьте эти числа на целое число, чтобы получить в результате целые числа:
Таким образом, простейшая формула метилацетата — C3H6O2. Она также является его химической формулой.
Примечания[править | править код]
- ↑ IUPAC Gold Book internet edition: «Empirical formula».