1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| Глицерин | ||
|---|---|---|
|
||
 |
||
| Общие | ||
| Традиционные названия | глицерин | |
| Хим. формула | C3H8O3 | |
| Рац. формула | HOCH2-CH(OH)-CH2OH | |
| Физические свойства | ||
| Молярная масса | 92,09 г/моль | |
| Плотность | 1,261 г/см³ | |
| Термические свойства | ||
| Температура | ||
| • плавления | 17,9 °C | |
| • кипения | 290 °C | |
| • разложения | 290 °C | |
| • вспышки | 160 °C | |
| Давление пара | 0,003 ± 0,001 мм рт.ст.[1] | |
| Оптические свойства | ||
| Показатель преломления | 1,4740 | |
| Классификация | ||
| Рег. номер CAS | 56-81-5 | |
| PubChem | 753 | |
| Рег. номер EINECS | 200-289-5 | |
| SMILES |
OCC(O)CO |
|
| InChI |
InChI=1S/C3H8O3/c4-1-3(6)2-5/h3-6H,1-2H2 PEDCQBHIVMGVHV-UHFFFAOYSA-N |
|
| Кодекс Алиментариус | E422 | |
| RTECS | MA8050000 | |
| ChEBI | 17754 | |
| ChemSpider | 733 | |
| Безопасность | ||
| NFPA 704 |
1 1 0 |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | ||
Глицери́н (от греч. γλυκερός «сладкий») — органическое соединение, простейший представитель трёхатомных спиртов с формулой 
Синонимы: глицерóл, пропантриол-1,2,3, Е422.
Физические свойства[править | править код]
Бесцветная вязкая жидкость без запаха. Сладкий на вкус, отчего и получил своё название (греч. γλυκερός — сладкий). Имеет молярную массу 92,09 г/моль, относительную плотность 

При растворении глицерина в воде выделяется теплота и происходит контракция — уменьшение объёма раствора. Смеси глицерина с водой обладают температурой плавления значительно более низкой, чем каждое из веществ по отдельности, например, при массовом содержании глицерина в 66,7 % его смесь с водой будет замерзать при −46,5 °C[2].
Образует азеотропы с нафталином, его производными и рядом других веществ[2].
Химические свойства[править | править код]
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
Глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканио Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
-
,
и окисляется до глицеринового альдегида 


Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, существенное биологическое значение также имеют фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Получение[править | править код]
Глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии оксидов свинца[3]. Основную массу глицерина получают как побочный продукт при омылении жиров[4].
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, 

На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы.
Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный 

Глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Биологическая роль[править | править код]
Глицерин используется в глюконеогенезе (процессе образования глюкозы в печени). Под действием ферментов печени глицерин последовательно превращается в глицеральдегид-3-фосфат, дигидроксиацетонфосфат, глицеральдегидтрифосфат, который далее участвует в цепи гликолиза[5].
Глицерин синтезируется дрожжами, при этом его количество зависит от условий их культивирования[6].
В небольших количествах глицерин образуется при ферментации виноматериалов и придаёт им сладковатый оттенок. Наибольшая концентрация глицерина, около 10 г/л, присутствует в сладких винах, в частности, ботритизированных.
В медицине[править | править код]
Содержание глицерина в сыворотке крови человека отражает концентрацию триглицеридов и сумму насыщенных жирных кислот, моно жирных кислот и ненасыщенных жирных кислот, которые структурированы в составе липопротеинов очень низкой плотности (ЛПОНП). Уровень глицерина характеризует нарушение поглощения клетками моно- и насыщенных жирных кислот в составе ЛПОНП. Высокий уровень глицерина в плазме крови и в ЛПОНП прогностически более неблагоприятный фактор риска, чем повышение уровня холестерина[7].
Производные глицерина[править | править код]
Глицериды[править | править код]

Шариковая модель триглицерида. Красным цветом выделен кислород, чёрным — углерод, белым — водород
Триглицериды (жиры) являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах. Они гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Применение[править | править код]
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность.
Глицерин является компонентом многих пищевых продуктов, кремов и косметических средств[8]. В косметической промышленности глицерин применяется как влагоудерживающий, смягчающий и увлажняющий компонент. Также он может выступать в роли растворителя, регулятора вязкости и эмульгатора.
Глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка Е422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддаётся желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей и основы для жидкости, используемой в дым-машинах.
В прошлом глицерин использовался для изготовления динамита[9].
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.
Примечания[править | править код]
- ↑ http://www.cdc.gov/niosh/npg/npgd0302.html
- ↑ 1 2 3 Дьяконов, 1988.
- ↑ Горбов А. И., Менделеев Д. И. Глицерин // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ Горбов А. И., Менделеев Д. И. Глицерин, способ определения // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- ↑ Вхождение глицерина в гликолиз : [арх. 25 июля 2021]. — 18 с.
- ↑ Вустин, М. М. Биологическая рль глицерина в клетках дрожжей. Дрожжи как продуценты глицерина // Биотехнология. — 2020. — Т. 36, № 6. — С. 6–16. — УДК 579.66(G). — ISSN 0234-2758. — doi:10.21519/0234-2758-2020-36-6-6-16.
- ↑ Титов, В. Н. Единение физико-химического и биологического действия спиртов глицерина и холестерина в поглощении клетками жирных кислот. Особенности патогенеза «метаболических пандемий» : [арх. 4 октября 2016] // Клиническая лабораторная диагностика : журн. — 2013. — № 1.
- ↑ Применение глицерина // Справочник по химии : для школьников и студентов. — SolverBook. — Глицерин.
- ↑ Канонников И. И., Менделеев Д. И. Глицерин, в технике // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
Литература[править | править код]
- Дьяконов И. А. Глицерин // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А — Дарзана. — С. 585. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.
Ссылки[править | править код]
- Физические свойства глицерина
- What is Glycerin?
- Glossary for the Modern Soap Maker
- Glycerol soap
- Absolute alcohol using glycerol
- Computational Chemistry Wiki
- Health.gov dietary guidelines
Как химическим путем доказать, что в пробирке находится раствор глицерина? Опишите действия и наблюдения, запишите уравнения необходимых реакций.
Найди верный ответ на вопрос ✅ «Как химическим путем доказать, что в пробирке находится раствор глицерина? Опишите действия и наблюдения, запишите уравнения необходимых …» по предмету 📙 Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Искать другие ответы
Главная » Химия » Как химическим путем доказать, что в пробирке находится раствор глицерина? Опишите действия и наблюдения, запишите уравнения необходимых реакций.
Химическое соединение
 |
||
|
||
 |
||
| Имена | ||
|---|---|---|
| Предпочтительное название IUPAC Пропан-1,2,3-триол | ||
| Другие наименования Глицерин. Глицерин. Пропанетриол. 1,2,3-Тригидроксипропан. 1,2,3-Пропанетриол | ||
| Идентификаторы | ||
| Номер CAS |
|
|
| 3D-модель (JSmol ) |
|
|
| ChEBI |
|
|
| ChEMBL |
|
|
| ChemSpider |
|
|
| DrugBank |
|
|
| ECHA InfoCard | 100.000.263 |
|
| Номер E | E422 (загустители,…) | |
| IUPHAR / BPS |
|
|
| KEGG |
|
|
| PubChem CID |
|
|
| UNII |
|
|
| CompTox Dashboard (EPA ) |
|
|
InChI
|
||
УЛЫБКА
|
||
| Свойства | ||
| Химическая формула | C3H8O3 | |
| Молярный масса | 92,094 г · моль | |
| Внешний вид | Бесцветный гигроскопичная жидкость | |
| Запах | Без запаха | |
| Плотность | 1,261 г / см | |
| Точка плавления | 17,8 ° C (64,0 ° F; 290,9 K) | |
| Температура кипения | 290 ° C (554 ° F; 563 K) | |
| Растворимость в воде | смешиваемый | |
| log P | -2,32 | |
| Давление пара | 0,003 мм рт. Ст. (50 ° C) | |
| Магнитная восприимчивость (χ) | -57,06 · 10 см / моль | |
| Показатель преломления (nD) | 1,4746 | |
| Вязкость | 1,412 Па · с | |
| Фармакология | ||
| Код АТС | A06AG04 (WHO ) A06AX01 (WHO ), QA16QA03 (ВОЗ ) | |
| Опасности | ||
| Паспорт безопасности | См.: страница данных. JT Baker | |
| NFPA 704 (огненный алмаз) |  1 0 0 1 0 0 |
|
| Температура вспышки | 160 ° C (320 ° F; 433 K) (закрытый стакан). 176 ° C (349 ° F; 449 K) (открытый стакан) | |
| NIOSH (пределы воздействия на здоровье в США): | ||
| PEL (Допустимо) | TWA 15 мг / м (всего) TWA 5 мг / м (соответственно) | |
| REL (Рекомендуется) | Не установлено | |
| IDLH (Непосредственная опасность) | ND | |
| Страница дополнительных данных | ||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. Д.. | |
| Термодинамические. данные | Фазовое поведение. твердое тело – li quid – gas | |
| Спектральные данные | UV, IR, ЯМР, MS | |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | ||
| Ссылки в информационном окне | ||
Глицерин (; также называемый глицерином или глицерином ) представляет собой простое соединение полиола. Это бесцветная, вязкая жидкость без запаха, сладкая и нетоксичная. Основа глицерина находится в тех липидах, известных как глицериды. Благодаря антимикробным и противовирусным свойствам он широко используется в одобренных FDA средствах для лечения ран и ожогов. Его также можно использовать в качестве эффективного маркера для измерения заболеваний печени. Он также широко используется в качестве подсластителя в пищевой промышленности и в качестве увлажнителя в фармацевтических составах. Благодаря наличию трех гидроксильных групп, глицерин смешивается с водой и гигроскопичен по природе.
Содержание
- 1 Структура
- 2 Производство
- 2.1 Синтетический глицерин
- 3 Область применения
- 3.1 Пищевая промышленность
- 3.2 Применение в медицине, фармацевтике и личной гигиене
- 3.3 Растительные экстракты
- 3.4 Жидкость для электронных сигарет
- 3.5 Антифриз
- 3.6 Химический промежуточный продукт
- 3.7 Демпфирование вибрации
- 3.8 Ниши использования
- 3.8.1 Киноиндустрия
- 3.8.2 Ультразвуковой контакт
- 3.9 Топливо внутреннего сгорания
- 3.10 Исследования по использованию
- 4 Метаболизм
- 5 Исторические случаи загрязнения диэтиленгликолем
- 6 Этимология
- 7 См. также
- 8 Ссылки
- 9 Внешние ссылки
Структура
Хотя ахиральный, глицерин является прохиральным по отношению к реакциям одного из двух первичных спиртов. Таким образом, в замещенных производных стереоспецифическая нумерация помечает молекулу префиксом «sn-» перед названием основы молекулы.
Производство
Обычно получают глицерин. из растительных и животных источников, где он встречается в триглицеридах, сложных эфирах глицерина с длинноцепочечными карбоновыми кислотами. гидролиз, омыление или переэтерификация этих триглицеридов дает глицерин, а также производное жирной кислоты:
триглицерид

3 NaOH / H. 2O
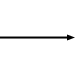
Δ
3 × мыло
3 × 
глицерин

Триглицериды могут быть омылены гидроксидом натрия с получением глицерина и жирная натриевая соль или мыло.
Типичные растительные источники включают соевые бобы или пальму. Другой источник – жир животного происхождения. Около 950 000 тонн в год производится в США и Европе; С 2000 по 2004 год только в США производилось 350 000 тонн глицерина в год. Директива ЕС 2003/30 / EC устанавливает требование о замене 5,75% нефтяного топлива на биотопливо. источников во всех государствах-членах к 2010 году. В 2006 году прогнозировалось, что к 2020 году производство будет в шесть раз больше, чем спрос, что создаст избыток глицерина.
Глицерин. из триглицеридов производится в больших масштабах, но неочищенный продукт имеет переменное качество с низкой продажной ценой всего 2-5 центов США за килограмм в 2011 году. Его можно очистить, но этот процесс стоит дорого. Некоторое количество глицерина сжигается для получения энергии, но его теплотворная способность низкая.
Неочищенный глицерин от гидролиза триглицеридов может быть очищен обработкой активированным углем для удаления органических примеси, щелочь для удаления непрореагировавших сложных эфиров глицерина и ионный обмен для удаления солей. Глицерин высокой чистоты (>99,5%) получают многостадийной перегонкой; вакуумная камера необходима из-за ее высокой температуры кипения (290 ° C).
Синтетический глицерин
Хотя обычно это не является рентабельным, глицерин можно производить различными маршруты из пропилена. Процесс эпихлоргидрина является наиболее важным: он включает хлорирование пропилена с получением аллилхлорида, который окисляется гипохлоритом до, который реагирует с сильным основанием с получением эпихлоргидрина. Этот эпихлоргидрин затем гидролизуют с образованием глицерина. Процессы без хлора из пропилена включают синтез глицерина из акролеина и оксида пропилена.
из-за крупномасштабного производства биодизеля из жиры, где глицерин является побочным продуктом, рынок глицерина снижен. Таким образом, синтетические процессы не экономичны. Из-за избыточного предложения прилагаются усилия для преобразования глицерина в синтетические предшественники, такие как акролеин и эпихлоргидрин. (См. Раздел Промежуточный продукт в этой статье).
Применение
Пищевая промышленность
В продуктах питания и напитках глицерин служит увлажнителем, растворителем и подсластитель, и может помочь сохранить продукты. Он также используется в качестве наполнителя в коммерческих нежирных пищевых продуктах (например, печенье ) и в качестве загустителя в ликерах. Глицерин и вода используются для сохранения некоторых видов листьев растений. Как заменитель сахара, он содержит примерно 27 килокалорий на чайную ложку (сахар содержит 20) и составляет 60% от сладкого как <409.>сахароза. Он не питает бактерии, которые образуют бляшки и вызывают кариес. Как пищевая добавка, глицерин имеет маркировку E номер E422. Его добавляют в глазурь (глазурь), чтобы она не затвердела.
Используемый в пищевых продуктах глицерин классифицируется Академией питания и диетологии США как углевод. Обозначение углеводов в соответствии с Управлением по контролю за продуктами и лекарствами (FDA) США включает все калорийные макроэлементы, за исключением белков и жиров. Глицерин имеет калорийность, аналогичную столовому сахару, но более низкий гликемический индекс и другой метаболический путь в организме, поэтому некоторые защитники диеты принимают глицерин в качестве подсластителя, совместимого с низким содержанием сахара. -углеводные диеты.
Также рекомендуется в качестве добавки при использовании полиольных подсластителей, таких как эритрит и ксилит, которые обладают охлаждающим эффектом из-за теплового эффекта во рту, если охлаждающий эффект нежелателен.
Применение в медицине, фармацевтике и личной гигиене
 Бутылка глицерина, купленная в аптеке
Бутылка глицерина, купленная в аптеке  Лубриканты для личного пользования обычно содержат глицерин
Лубриканты для личного пользования обычно содержат глицерин  Глицерин является ингредиентом таких продуктов, как гель для волос
Глицерин является ингредиентом таких продуктов, как гель для волос  Глицериновые суппозитории, используемые в качестве слабительного
Глицериновые суппозитории, используемые в качестве слабительного
Глицерин обладает умеренным антимикробным и противовирусным действием и является одобренным FDA средством для лечения ран. Красный Крест сообщает, что 85% раствор глицерина проявляет бактерицидные и противовирусные эффекты, а в ранах, обработанных глицерином, наблюдается уменьшение воспаления примерно через 2 часа. В связи с этим он широко используется в продуктах для ухода за ранами, включая листы на основе глицерина гидрогелевые для ожогов и других средств ухода за ранами. Он одобрен для всех видов ухода за ранами, кроме ожогов третьей степени, и используется для упаковки донорской кожи, используемой в кожных трансплантатах. Не существует одобренного местного лечения ожогов третьей степени, поэтому это ограничение распространяется не только на глицерин.
Глицерин используется в медицине, фармацевтике и препараты личной гигиены, часто в качестве средств улучшения гладкости, обеспечивающих смазку, а также в качестве увлажнителя.
ихтиоза и ксероза были облегчены путем местное применение глицерина. Он содержится в аллергенах иммунотерапии, сиропах от кашля, эликсирах и отхаркивающих средствах, зубной пасте, жидкости для полоскания рта., средства по уходу за кожей, крем для бритья, средства по уходу за волосами, мыло и личные лубриканты на водной основе. В твердых лекарственных формах, таких как таблетки, глицерин используется в качестве удерживающего агента. Для потребления человеком глицерин классифицируется FDA США среди сахарных спиртов как калорийный макроэлемент. Глицерин также используется в банке крови для сохранения красных кровяных телец перед замораживанием.
Глицерин является компонентом глицеринового мыла. Эфирные масла добавлены для ароматизатора. Это мыло используют люди с чувствительной, легко раздражаемой кожей, поскольку оно предотвращает высыхание кожи благодаря своим увлажняющим свойствам. Он выводит влагу через слои кожи и замедляет или предотвращает чрезмерное высыхание и испарение.
При ректальном приеме глицерин действует как слабительное, раздражая слизистую оболочку анального канала и вызывая гиперосмотический эффект, расширяя толстую кишку за счет втягивания в нее воды, чтобы вызвать перистальтику, что приводит к эвакуации. Его можно вводить в неразбавленном виде в виде суппозитория или небольшого объема (2–10 мл) клизмы. В качестве альтернативы его можно вводить в разбавленном растворе, например 5%, в виде клизмы большого объема.
При пероральном приеме (часто смешанном с фруктовым соком для уменьшения сладкого вкуса) глицерин может вызвать быстрое, временное снижение внутреннего давления глаза. Это может быть полезно для начального неотложного лечения сильно повышенного глазного давления.
Глицерин также был включен в состав биочернил в области биопечати. Содержание глицерина увеличивает вязкость биочернил без добавления крупных молекул белка, углеводов или гликопротеинов.
Ботанические экстракты
При использовании в экстрактах методом «настойки», особенно в виде 10% раствора, глицерин предотвращает осаждение таннинов в этанольных экстрактах растений (настойки ). Он также используется в качестве «не содержащей спирта» альтернативы этанолу в качестве растворителя при приготовлении экстрактов трав. Он менее экстрактивен при использовании в стандартной методике настойки. Из настоев на основе спирта можно также удалить спирт и заменить его глицерином для сохранения его свойств. Такие продукты не являются «свободными от спирта» в научном или нормативном смысле FDA, поскольку глицерин содержит три гидроксильные группы. Жидкий экстракт производители часто экстрагируют травы в горячей воде перед добавлением глицерина для получения глицеритов.
При использовании в качестве основного «настоящего» растворителя для экстракции растений без спирта в методиках, не основанных на настойках, глицерин имеет Было показано, что он обладает высокой степенью экстрактивной универсальности для растений, включая удаление множества компонентов и сложных соединений, с экстрактивной способностью, которая может соперничать с таковой у спирта и водно-спиртовых растворов. Тот факт, что глицерин обладает такой высокой экстрактивной способностью, предполагает, что он используется с динамическими (то есть критическими) методологиями, в отличие от стандартных пассивных методик «подкрашивания», которые лучше подходят для спирта. Глицерин обладает внутренним свойством не денатурировать и не делать компоненты растений инертными, как спирты (например, этиловый (зерновой) спирт, метиловый (древесный) спирт и т. Д.). Глицерин является стабильным консервантом для растительных экстрактов, который при использовании в надлежащих концентрациях в основе экстракционного растворителя не позволяет инвертировать или смягчать восстановительно-окисление (РЕДОКС) компонентов готового экстракта даже в течение нескольких лет. И глицерин, и этанол являются жизнеспособными консервантами. Глицерин бактериостатичен по своему действию, а этанол обладает бактерицидным действием.
Жидкость для электронных сигарет
 Глицерин часто используется в электронных сигаретах для создания пара
Глицерин часто используется в электронных сигаретах для создания пара
Глицерин вместе с пропиленгликолем является обычным компонентом жидкости для электронных сигарет, раствора, используемого в электронных испарителях (электронных сигарет ). Этот глицерин нагревают с помощью распылителя (нагревательный змеевик, часто сделанный из проволоки Kanthal ), образуя аэрозоль, который доставляет никотин к пользователя.
Антифриз
Подобно этиленгликолю и пропиленгликолю, глицерин является неионогенным космотропом, который образует прочный водородные связи с молекулами воды, конкурирующие с водородными связями вода-вода . Это взаимодействие нарушает образование льда. Минимальная температура замерзания составляет около -36 ° F (-38 ° C), что соответствует 70% глицерина в воде.
Глицерин исторически использовался в качестве антифриза для автомобильной промышленности, прежде чем был заменен на этиленгликоль, который имеет более низкую температуру замерзания. Хотя минимальная температура замерзания смеси глицерин-вода выше, чем у смеси этиленгликоль-вода, глицерин не токсичен и повторно исследуется для использования в автомобилях.
В лаборатории глицерин является общий компонент растворителей для ферментативных реагентов, хранящихся при температурах ниже 0 ° C из-за снижения температуры замерзания. Он также используется в качестве криопротектора, когда глицерин растворяется в воде, чтобы уменьшить повреждение кристаллами льда лабораторных организмов, хранящихся в замороженных растворах, таких как грибы, бактерии, нематоды и эмбрионы млекопитающих.
Промежуточное звено
Глицерин используется для производства нитроглицерина, который является важным ингредиентом различных взрывчатых веществ, таких как динамит, гелигнит и топливо, такое как кордит. Опора на мыловарение в качестве побочного продукта глицерина затрудняла увеличение производства для удовлетворения спроса во время войны. Следовательно, процессы синтеза глицерина были приоритетами национальной обороны в дни, предшествующие Второй мировой войне. Нитроглицерин, также известный как тринитрат глицерина (GTN), обычно используется для облегчения стенокардии, принимается в форме таблеток или в виде аэрозоля в виде спрея.
Окисление глицерина дает мезоксалевую кислоту. Обезвоживание глицерина дает гидроксиацетон.
Демпфирование вибрации
Глицерин используется в качестве наполнителя для манометров для гашения вибрации. Внешние колебания от компрессоров, двигателей, насосов и т. Д. Вызывают гармонические колебания внутри датчиков Бурдона, которые могут вызвать чрезмерное перемещение стрелки, что приведет к неточным показаниям. Чрезмерное раскачивание иглы также может повредить внутренние шестерни или другие компоненты, что приведет к преждевременному износу. Глицерин, залитый в датчик для замены воздушного пространства, снижает гармонические колебания, передаваемые на иглу, увеличивая срок службы и надежность датчика.
Niche использует
Кинопромышленность
Глицерин используется в киноиндустрии при съемке сцен с участием воды, чтобы участки не высыхали слишком быстро.
Глицерин используется в сочетании с водой (примерно в пропорции 1:99) для создать ровную дымную среду. Раствор испаряется и выталкивается в комнату с помощью вентилятора.
Ультразвуковое связующее
Глицерин иногда можно использовать вместо воды в ультразвуковых испытаниях, так как он имеет более высокий акустический импеданс (2,42 МБ против 1,483 МБ для воды ), будучи относительно безопасным, нетоксичным, некоррозионным и относительно дешевым.
Топливо внутреннего сгорания
Глицерин также используется для питания дизельных генераторов, поставляющих электроэнергию для гоночных электромобилей серии FIA Formula E.
Исследования по использованию
Были проведены исследования проведено для производства продуктов с добавленной стоимостью из глицерина, полученного при производстве биодизеля. Примеры (помимо сжигания отработанного глицерина):
- водород газ производство
- ацетат глицерина является потенциальной добавкой к топливу.
- Глицерин является одной из наиболее часто используемая добавка для крахмала термопласта.
- преобразование в пропиленгликоль
- преобразование в акролеин
- преобразование в этанол
- преобразование в эпихлоргидрин, сырье для эпоксидных смол
Метаболизм
Глицерин является предшественником для синтеза триацилглицеринов и фосфолипидов в печень и жировая ткань. Когда организм использует накопленный жир в качестве источника энергии, глицерин и жирные кислоты попадают в кровоток.
Глицерин метаболизируется в основном в печени. Инъекции глицерина можно использовать в качестве простого теста на повреждение печени, поскольку скорость его поглощения печенью считается точным показателем здоровья печени. Метаболизм глицерина снижается как при циррозе, так и при жировой болезни печени.
Уровни глицерина в крови сильно повышаются во время диабета и, как полагают, являются причиной снижения фертильности у пациентов, страдающих диабетом и метаболическим синдромом. Уровни глицерина в крови у пациентов с диабетом в среднем в три раза выше, чем у здоровых людей. Было обнаружено, что прямая обработка семенников глицерином вызывает значительное долгосрочное снижение количества сперматозоидов. Дальнейшие испытания по этому предмету были прекращены из-за неожиданных результатов, поскольку это не было целью эксперимента.
Циркулирующий глицерин не гликирует белки, как глюкоза или фруктоза, и не приводят к образованию конечных продуктов гликирования (AGE). У некоторых организмов глицериновый компонент может напрямую вступать в путь гликолиза и, таким образом, обеспечивать энергию для клеточного метаболизма (или, потенциально, превращаться в глюкозу посредством глюконеогенеза).
Прежде чем глицерин сможет вступить в путь гликолиза или глюконеогенеза (в зависимости от физиологических условий), он должен быть преобразован в их промежуточное соединение глицеральдегид-3-фосфат на следующих этапах:
Глицерин
![]()
Глицеринкиназа
АТФ АДФ 
Глицерин-3-фосфат
![]()
Глицерин-3-фосфатдегидрогеназа
НАД NADH  NAD NADH
NAD NADH
Дигидроксиацетонфосфат
![]()
Триозофосфатизомераза

Глицеральдегид-3-фосфат

Фермент глицеринкиназа присутствует в основном в печень и почки, но также и другие ткани организма, включая мышцы и мозг. В жировой ткани глицерин-3-фосфат получают из дигидроксиацетонфосфата (DHAP) с помощью фермента глицерин-3-фосфатдегидрогеназа.
. Глицерин имеет очень низкую токсичность при приеме внутрь; его LD50 пероральная доза для крыс составляет 12600 мг / кг и 8700 мг / кг для мышей. По-видимому, он не вызывает токсичности при вдыхании, хотя изменения в зрелости клеток произошли в небольших участках легких у животных при максимальной измеренной дозе. Субхроническое 90-дневное исследование ингаляции только через нос на крысах Sprague-Dawley (SD), подвергавшихся воздействию 0,03, 0,16 и 0,66 мг / л глицерина (на литр воздуха) в течение 6-часовых непрерывных сеансов, не выявило связанной с лечением токсичности. чем минимальная метаплазия эпителиальной выстилки в основании надгортанника у крыс, подвергшихся воздействию глицерина 0,66 мг / л.
Исторические случаи загрязнения диэтиленгликолем
4 мая 2007 г. в США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов посоветовало всем производителям лекарств в США проверить все партии глицерина на токсичный диэтиленгликоль. Это последовало за случаем сотен смертельных отравлений в Панаме в результате фальсификации импортной таможенной декларации панамской импортно-экспортной фирмой Aduanas Javier de Gracia Express, SA. Более дешевый диэтиленгликоль был переименован в более дорогой глицерин. 65>
Этимология
Префиксы gly- и glu- для гликолей и сахаров происходят от греческого γλυκύς glukus, что означает сладкий.
См. Также
- Диоксалин
- Эпихлоргидрин
- Нитроглицерин
- Олеохимия
- Омыление / Мыло
- Солкетал
- Сахарный спирт
- Трансэтерификация
Ссылки
Внешние ссылки
- Масс-спектр глицерина
- CDC – Карманное руководство NIOSH по химическим опасностям – Глицерин (туман)
Качественная реакция на глицерин
При проведении опыта используем Микролабораторию для химического эксперимента
Цель опыта: изучить качественную реакцию на глицерин.
Оборудование: пробирки (2 шт.).
Реактивы: раствор гидроксида натрия NaOH, раствор сульфата меди(II) CuSO4, глицерин C3H5(OH)3.
Ход работы
1. В две пробирки вносим по 20-25 капель сульфата меди(II).

2. Добавляем к нему избыток гидроксида натрия.

3. Образуется осадок гидроксида меди(II) голубого цвета.

4. В одну пробирку по каплям добавляем глицерин.
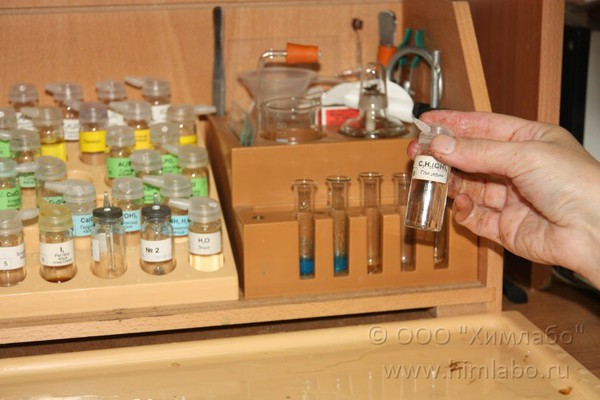
5. Встряхиваем пробирку до исчезновения осадка и образования темно-синего раствора глицерата меди(II).
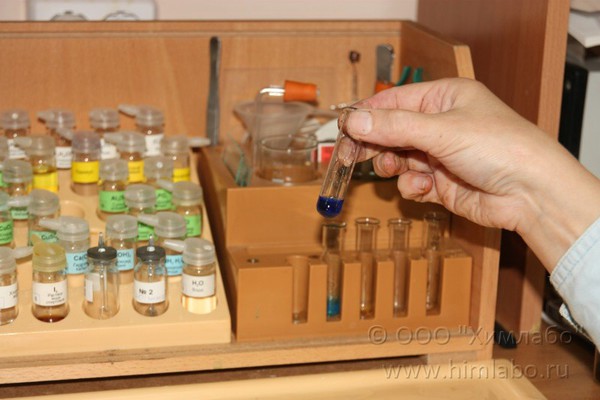
6. Сравниваем окраску раствора с окраской гидроксида меди(II) в контрольной пробирке.

Вывод:
Качественной реакцией на глицерин является его взаимодействие с гидроксидом меди (II).
Оказываем содействие в подготовке технических требований для тендерной документации.
Внимание! Изображение товара может отличаться от полученного Вами товара. Производитель оставляет за собой право изменять комплектацию и технические характеристики товара без предварительного уведомления без ухудшения функциональных и качественных показателей. Информация о товаре носит справочный характер и не является публичной офертой, определяемой Статьей 437 ГК РФ.
Убедительная просьба, при покупке учебного оборудования согласовывать с менеджером важные для Вас характеристики, комплектацию и цену учебного оборудования.
Источник
Как можно обнаружить в растворах глицерин
Войти
Авторизуясь в LiveJournal с помощью стороннего сервиса вы принимаете условия Пользовательского соглашения LiveJournal
Польза и коварство глицерина
В общем, глицерин используется во многих других сферах жизнедеятельности человека: в сельском хозяйстве, текстильной, военной, бумажной промышленности, для приготовления табака и др.
Мы повседневно используем глицерин в том или ином виде. Но нам интерснее знать как используется глицерин в косметологии. Реклама средств с глицерином так обширна, что порой человек не задумывается над свойствами главного составляющего большинства косметических средств.
Тут и домашние маски для лица, и средства после бритья, препараты против морщин, средства для любой уожи, препараты для защиты от загара, обещающие фантастическое увлажнение:
«Глицерин образует на коже тонкую, малопроницаемую для молекул воды пленку. Вещество обладает удивительной способностью поглощать влагу из воздуха, мгновенно притягивая ее к кожной поверхности. За счет этого сухая кожа лица, рук быстро восстанавливается, от пятен шелушения не остается следа.»
Применение глицерина в домашних условиях очень популярно среди женщин, ведь с его помощью можно решить многие проблемы с кожей без особых усилий и больших затрат времени и денег.
 Однако, не всем известен тот факт, что данный компонент может увлажнять кожу, вытягивая влагу из воздуха только при определённом климате в комнате. Таким образом, чтобы появился положительный результат от использования этого ингредиента, нужно, чтобы во время его применения влажность воздуха в помещении была примерно 50-65 %. Только в таких условиях может оказать положительный результат на кожу глицерин для лица. Вред и польза от его применения напрямую зависят от соблюдения данного фактора.
Однако, не всем известен тот факт, что данный компонент может увлажнять кожу, вытягивая влагу из воздуха только при определённом климате в комнате. Таким образом, чтобы появился положительный результат от использования этого ингредиента, нужно, чтобы во время его применения влажность воздуха в помещении была примерно 50-65 %. Только в таких условиях может оказать положительный результат на кожу глицерин для лица. Вред и польза от его применения напрямую зависят от соблюдения данного фактора.
Если правильно наносить данное средство и использовать только проверенные рецепты, то можно добиться не только увлажняющего результата, но и омолаживающего действия.
Если все меры предосторожности при использовании глицерина будут соблюдены, то никакого вреда от него быть не может. Так как у него есть масса достоинств, благодаря которым его ценят многие ведущие косметологи и используют в составах своих кремов и лосьонов. Например, он может ускорять обмен веществ в верхних слоях кожи, тем самым выводя все вредные вещества и жир. Также это средство используется при лечении ангины и помогает людям избавляться от мимических морщин. Если соединить глицерин с уксусом, то он способен избавить от трещин в сухих местах на теле. Подробнее
Глицерин как способ консервации живых цветов
Сохранение цветов в их первозданном виде при помощи глицерина – это не новый способ, но известный далеко не всем. Это абсолютной безвредный процесс, так как глицерин не является токсичным веществом.
Для консервации в глицерине подходят почти все растения. Предпочтение отдается вызревшим, одревесневшим частям растений.
Раствор глицерина поступает в клетки листьев и цветков, вытесняя из них воду. В результате вода испаряется, а глицерин остается, поддерживая эластичность всех тканей. Растения будут готовыми, если на кончиках их листьев и лепестков выступают маленькие блестящие капли глицерина. Теперь глицериновый раствор можно слить. Законсервированные таким способом цветы становятся глянцевыми и гибкими, словно покрытие лаком.
Готовые цветы ни в коем случае нельзя ставить в воду, лучше поставить в вазу, наполненную сухим песком. Периодически их следует очищать от осевшей пыли при помощи сухой тряпочки.
Эффектно выглядят цветы, консервированные в декоративные стеклянные баночки и бутылочки. Для этого чистую емкость заполняют цветками и полностью заливают глицериновым раствором. Емкость плотно закрывают и опять же ставят на 2-3 недели для пропитки глицерином в темное прохладное место.
Затем раствор сливают, цветы изнутри промывают холодной водой и заполняют новым раствором.
Читать про Другие способы консервации цветов
Источник
Глицерин

Глицерин (от греч. γλυκερός — «сладкий», глицерол, пропантриол-1,2,3, Е422) относится к органическим соединениям, простейшим представителям трехатомных спиртов. Это вязкая прозрачная сиропообразная жидкость, которая обладает сладковатым вкусом, отличается нетоксичностью.
Впервые глицерин получили в конце 18 века в процессе омыления жиров в присутствии оксидов свинца. Первооткрывателем вещества считается Карл Вильгельм Шееле (шведский химик-фармацевт). Основную долю глицерина получают при омылении жиров и по сей день.
В организме глицерин играет важную роль в образовании глюкозы в печени (глюконеогенезе).
Вещество активно применяют в пищевой промышленности (добавка Е422) в качестве стабилизатора, который помогает регулировать степень вязкости и консистенцию пищевых продуктов, а также в качестве эмульгатора.
Глицерин находит применение в медицине, при табачном производстве, в сельском хозяйстве, при производстве бытовой химии, в косметологии и многих других областях.
В качестве БАД его принимают при кашле, проблемах с глазами и сосудами, запорах и при повышенном внутричерепном давлении. Все это строго по рекомендации врача.
Из-за влагоудерживающего свойства глицерин входит в состав многих кремов, лосьонов, масок и других косметических средств. Средства на его основе эффективно увлажняют и смягчают кожу и волосы. Вещество формирует на поверхности защитную пленку, которая способствует сохранению влаги, предотвращая обезвоживание.
Глицерин также можно найти в составе лечебных мазей и кремов.
Благоприятное воздействие глицерина на кожу:
Маски и другие косметические средства на основе глицерина можно готовить в домашних условиях. Для этого обычно используют раствор вещества для наружного применения, который легко приобрести в аптеке или магазине товаров для красоты и здоровья.
При использовании раствора глицерина в домашних условиях необходимо соблюдать некоторые правила безопасности:
Источник
Гайморит: симптомы, особенности лечения и правила профилактики
Гайморит – это воспалительный процесс в области гайморовой пазухи, расположенной в толще черепной кости над верхней челюстью, слева и справа. Этот процесс является одной из разновидностей синуситов (это общее название для воспалительных процессов в области придаточных пазух – лобной, гайморовой, решетчатой или клиновидной). Обычно воспалительный процесс затрагивает слизистые оболочки, выстилающие пазухи изнутри, реже затрагиваются более глубокие слои тканей, вплоть до костных структур. Обычно процесс возникает как осложнение вирусных или бактериальных инфекций в области носоглотки и верхних дыхательных путей.
Исходя из причины развития, механизмов формирования и симптомов, гайморит бывает нескольких типов. Выделение каждого из них важно для определения тактики лечения, прогноза и разработки мер профилактики.
Острый – развивается быстро, как осложнение ОРВИ, насморков, простудных заболеваний, воспаления в области корней зубов на верхней челюсти. Возбудители проникают через каналы, соединяющие пазухи с полостью носа с гайморовыми пазухами, размножаются в полости. Тело начинает активно вырабатывать иммунные клетки и слизь, чтобы обезвредить патогенные организмы. Если слизь закупорит проток пазухи, возникает давление на стенки, усиление воспалительного процесса. По мере очищения пазухи от содержимого воспалительный процесс постепенно затухает.
Хронический – воспалительный процесс, который длится более 4 недель, имеет вялое или волнообразное течение, с периодами обострений. Обычно возникает из-за не долеченной острой формы, наличия аденоидов, тонзиллитов, отитов.
Гнойный – обычно становится осложнением острой формы либо обострения хронического процесса, если процесс не лечится, предпринимаются попытки самолечения или пациент переносит инфекцию на ногах. Патогенные бактерии накапливаются в пазухах, в смеси с лейкоцитами образуют гнойное содержимое. Самое опасное осложнение при этой форме – прорыв гноя в полость черепа, поражение костных тканей, мозга.
Двусторонний – одна из тяжелых форм, поражение локализовано сразу в обеих пазухах – левой и правой. Нередко возникает как осложнение инфекций в полости рта и носоглотки, обычно грибковой или бактериальной. Обычно имеет острое течение, редко переходит в хроническую форму.
Аллергическое поражение возникает у пациентов, страдающих от чрезмерно активной реакции иммунной системы на различные вещества. Особенно часто эта форма синусита бывает при поллинозе, круглогодичном рините, реакции на плесень, пылевых клещей.
Катаральный – преимущественно бывает у детей. Он развивается при проникновении в полость пазух патогенных организмов, что формирует отек и раздражение слизистых. Считается самой легкой формой болезни, проходящей при активном лечении без осложнений и последствий.
Полипозная форма формируется при образовании полипозных разрастаний слизистых из-за чрезмерно быстрого деления клеток. Рост полипов могут провоцировать инфекции, травмы, велика роль наследственности.
Одонтогенный – формируется как результат серьезных проблем зубов, особенно 4-6 зуба на верхней челюсти, корни которых расположены в непосредственной близости от пазухи. Если возникают проблемы в области корней этих зубов, воспаление и нагноение может переходить на пазуху, она заполняется секретом и воспаляется.
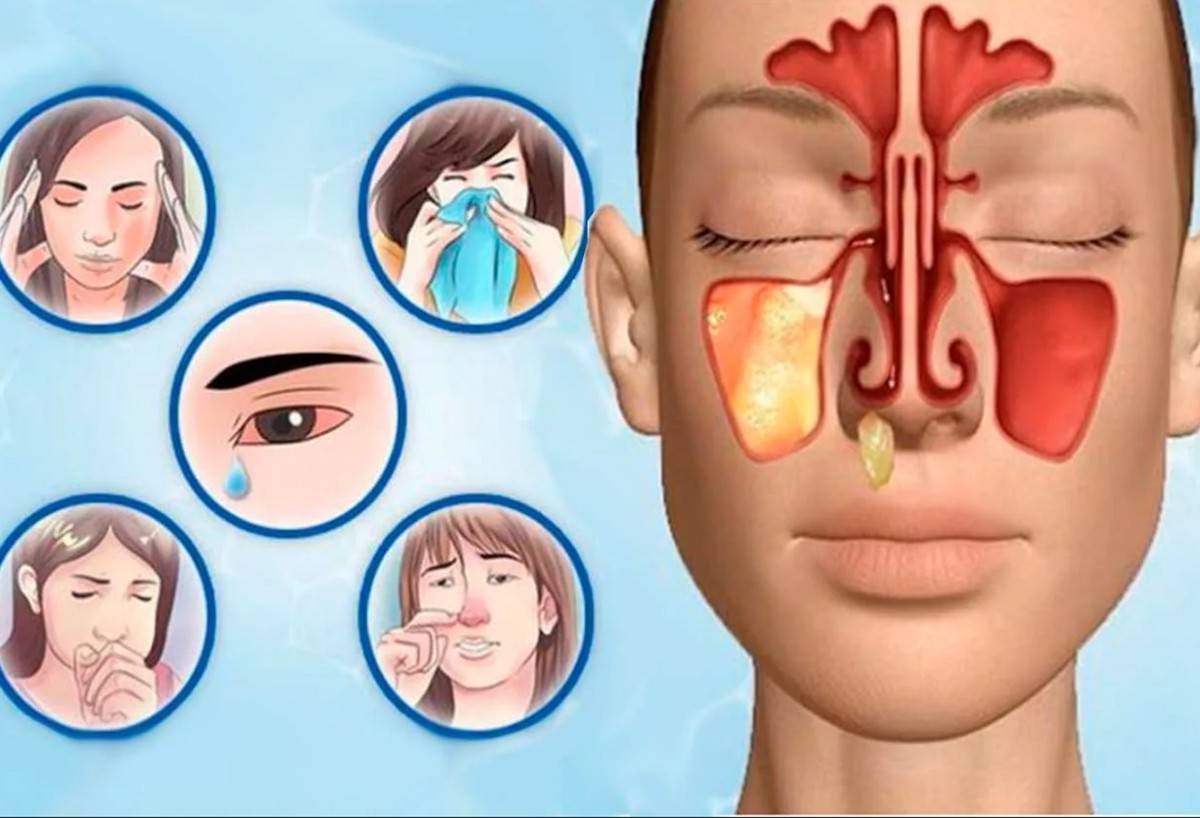
Причины
Придаточные пазухи, включая гайморовы, созданы как естественный барьер на пути инфекций, фильтр для различных опасных веществ в воздухе. Они помогают согревать воздух, увлажнять его и очищать от примесей перед попаданием в гортань, и ниже по респираторному тракту. Основная причина воспаления и появления признаков гайморита – это проникновение бактерий, грибков или вирусов, аллергенов. Реже инфекция попадает с током крови из других, отдаленных очагов.
Нарушать работу пазух могут патологии иммунной системы, частые ОРВИ, респираторная форма аллергии, носительство патогенных бактерий в носоглотке (стафило-, стрепто- или менингококк).
Среди ключевых причин, которые могут привести к развитию гайморита, можно выделить:
Осложнения
Не все люди знают, как начинается гайморит, поэтому многие принимают симптомы за тяжелую простуду и лечатся самостоятельно. Это может привести к определенным осложнениям, отдаленным последствиям. Среди ключевых осложнений можно выделить поражения бронхов и распространение инфекции на легкие, развитие отитов (поражение среднего уха), переход болезни в хроническую форму.
Тяжелый и запущенный, своевременно не вылеченный гайморит может привести к воспалению внутренних органов – сердца, глаз, почек, поражению суставов и мозга, его оболочек. Если образуются гнойные полости в гайморовых пазухах, возможен прорыв гноя в кровь (возникает сепсис), проникновение его в соседние пазухи с развитием пансинусита, воспаление мозговых оболочек с явлениями менингита. Всех этих осложнений можно избежать при полноценном лечении гайморита под руководством лор-врача.
Симптомы и диагностика
Конечно, при развитии гайморита нужно немедленно обращаться к врачу, но как понять, что гайморит начался? Начальные признаки неспецифичные – это повышение температуры от незначительной до высокой, сильная слабость, заложенность носа или обильные густые выделения, болезненность в проекции пазух или в области лица.
Боль при гайморите может быть различной – от тупой, давящей до сильной, мучительной. Она локализуется в подглазничной области, может отдавать в область переносицы, лобную зону или верхние зубы. При надавливании на область пазух или наклонах головы вперед она усиливается, распространяясь по подглазничной области. Могут краснеть и отекать веки.
Врачи отмечают некоторые особенности того, как проявляется болезнь в определенных возрастных группах. Так, у взрослых самым ключевым признаком могут быть болевые ощущения, головная боль, нарушение восприятия запахов. Может меняться голос, он становится гнусавым, нос сильно заложен, выделяется полупрозрачная или желто-зеленая слизь. Высокая лихорадка типична для острой формы, при хроническом или аллергическом гайморите болезнь может протекать без температуры.
На фоне поражения пазух возможно слезотечение, неприятный привкус во рту, слабость, постоянное утомление, нарушения аппетита, расстройства сна, ознобы и приступы кашля.
Заразен ли гайморит? Само по себе воспаление – это результат влияния патогенных факторов, и это не заразно. Бактерии или вирусы, которые спровоцировали заболевание, могут передаваться от человека к человеку, но не обязательно вызовут поражение пазух.
Диагноз гайморита ставит лор-врач после проведения ряда тестов и осмотра пациента. Важно подробно рассказать, как началось заболевание, какие жалобы были ранее и имеются в данный момент. Врач осмотрит полость носа и глотку, прощупает проекцию пазух, определяя болезненность.
Дополнительно могут понадобиться КТ или МРТ придаточных пазух, рентгенограмма, УЗИ исследование, эндоскопия носоглотки, при необходимости – биопсия полипозных образований. Назначаются анализы крови, посевы отделяемой из носа слизи для определения флоры, чтобы подобрать необходимые препараты.
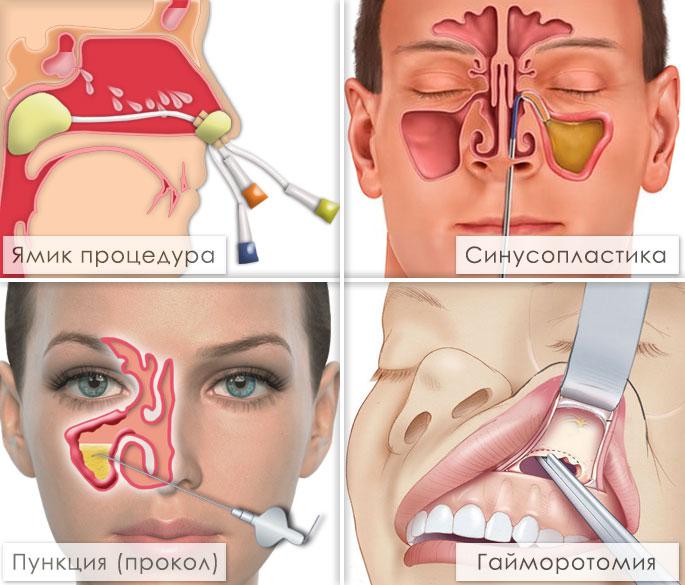
Как лечить у взрослого
Терапия болезни должна быть комплексной. Она направлена на борьбу с инфекцией, устранение воспаления, налаживание оттока слизи из пазух и улучшение носового дыхания. В неосложненных случаях возможно лечение гайморита дома под постоянным контролем оториноларинголога. В тяжелых случаях и при необходимости хирургического лечения пациент госпитализируется в стационар.
Возможно консервативное лечение с назначением антибактериальных препаратов, противовоспалительных средств, антигистаминных препаратов и различных капель, спреев для носа. Также применяют пункционное лечение или хирургические вмешательства. Выбор зависит от возраста пациента, вида патологии, тяжести состояния и возможных осложнений.
Многим пациентам назначают пункции (с местным обезболиванием) – они помогают удалить гнойное содержимое, помочь в оценке характера воспаления, плюс приносят существенное облегчение. После удаления содержимого пазухи промывают физраствором или фурациллином, вводят растворы антибиотиков и противовоспалительные препараты. Минус подобной тактики – не всегда достаточно одного прокола, поэтому требуется курс процедур в течение нескольких недель. Метод достаточно неприятный, имеет ряд противопоказаний и осложнений, процедура болезненна как во время прокола, так и после него.
Источник
Как можно обнаружить в растворах глицерин
Правила приемки и методы испытаний
Glycerine.
Acceptance rules and test methods
Дата введения 1998-01-01
1 РАЗРАБОТАН Всероссийским научно-исследовательским институтом жиров (ВНИИЖ) и Межгосударственным техническим комитетом по стандартизации МГК 238 «Масла растительные и продукты их переработки»
ВНЕСЕН Госстандартом России
2 ПРИНЯТ Межгосударственным Советом по стандартизации, метрологии и сертификации (протокол N 10 от 4 октября 1996 г.)
За принятие проголосовали:
Наименование национального органа по стандартизации
Минэкономики Республики Армения
Госстандарт Республики Казахстан
Главная государственная инспекция Туркменистана
3 Постановлением Государственного комитета Российской Федерации по стандартизации, метрологии и сертификации от 12 мая 1997 г. N 162 межгосударственный стандарт ГОСТ 7482-96 введен в действие непосредственно в качестве государственного стандарта Российской Федерации с 1 января 1998 г. с правом досрочного введения
5 ПЕРЕИЗДАНИЕ. Ноябрь 2001 г.
ВНЕСЕНА поправка, опубликованная в ИУС N 6, 2019 год с учетом уточнения, опубликованного в ИУС 11-2019
Поправка внесена изготовителем базы данных
1 ОБЛАСТЬ ПРИМЕНЕНИЯ
Настоящий стандарт распространяется на сырой и дистиллированный глицерин и устанавливает правила приемки и следующие методы испытаний:
— методы определения цвета, запаха, прозрачности, присутствия жирных кислот и смол, акролеина и других восстанавливающих веществ, железа, мышьяка, хлоридов, углеводов, белковых веществ, сернокислых соединений;
— методы измерения цветного числа, плотности, реакции глицерина, массовой доли чистого глицерина, массовой доли золы, массовой доли нелетучего органического остатка, коэффициента омыления.
Настоящий стандарт не распространяется на методы испытаний глицерина-реактива и синтетического глицерина.
2 НОРМАТИВНЫЕ ССЫЛКИ
В настоящем стандарте использованы ссылки на следующие стандарты:
3 ПРАВИЛА ПРИЕМКИ
3.1 Партией является любое количество сырого или дистиллированного глицерина, оформленное одним документом о качестве и предназначенное к одновременной сдаче-приемке.
3.2. Каждая партия глицерина, отгружаемая с предприятия-изготовителя, должна сопровождаться документом, удостоверяющим ее качество, с указанием:
— наименования предприятия-изготовителя, его товарного знака и местонахождения;
— наименования марки или сорта глицерина (на языке суверенного государства, на территории которого находится предприятие-изготовитель, или на другом языке, согласованном в договорах о поставках);
— даты изготовления или отгрузки;
— массы партии (брутто, нетто);
— информации о сертификации для стран, принявших законодательство о сертификации (для глицерина марки ПК-94);
— обозначения НД на продукт;
3.3 Присутствие сернокислых соединений, углеводов, белковых веществ предприятие-изготовитель определяет периодически, но не реже одного раза в квартал, или по требованию потребителя.
Показатели безопасности определяют в соответствии с порядком, гарантирующим безопасность продукции и установленным производителем продукции по согласованию с органами Госкомсанэпиднадзора.
3.4 Для контроля качества продукции из разных мест партии отбирают 10% бочек, бутылей или банок, но не менее четырех.
При отборе проб из баков-хранилищ объединенную пробу составляют по 4.1.2.
При поставках продукции в цистернах каждую цистерну принимают за партию.
3.5. При получении неудовлетворительных результатов испытаний хотя бы по одному из показателей по нему проводят повторные испытания удвоенной выборки от той же партии глицерина. Результаты повторных испытаний распространяют на всю партию.
При получении неудовлетворительных результатов периодических испытаний их переводят в приемо-сдаточные до получения положительных результатов на трех партиях подряд.
3.6 Сертификацию дистиллированного глицерина марки ПК-94 по показателям безопасности проводят в установленном порядке.
Источник





