Основной структурной единицей веществ, имеющих молекулярное строение является молекула. Молекула состоит из ограниченного числа атомов, связанных друг с другом ковалентными химическими связями. Заряд молекулы также как и атома равен нулю.
Объединяясь в молекулу, атомы образуют определённую 2D или 3D-структуру (треугольник, квадрат, тетраэдр, октаэдр и т.д.).
Молекула – электронейтральная частица вещества, состоящая из конечного числа атомов, связанных между собой ковалентными связями и имеющая определённую пространственную структуру.
Отметим, что в некоторых случаях вещество может состоять из химически несвязанных атомов, но при этом иметь “молекулярное строение”, например, все инертные газы. Для инертных газов понятия атом и молекула пересекаются.
Ковалентные связи между атомами образуются в результате обобществления атомами валентных электронов.
Валентные электроны – это электроны, принимающие участие в образовании химических связей.
Валентные электроны в атомах элементов главных подгрупп находятся на внешнем электронном слое. В атомах элементов побочных подгрупп часть валентных электронов находится на внешнем электронном слое, их там как правило 2, а иногда 1, с учётом эффекта провала электрона, а оставшаяся часть на d-подуровне предвнешнего электронного слоя.
При обобществлении валентных электронов атомами возникают общие электронные пары. Поэтому более точно, ковалентная связь – это связь, возникающая за счёт общих электронных пар.
Общие электронные пары могут возникать двумя способами: в результате обобществления неспаренных валентных электронов (обменный или коллигативный механизм) и в результате обобществления неподелённой электронной пары одного из атомов (донорно-акцепторный механизм). Более подробно речь об этих механизмах пойдёт в соответствующей главе.
Количество общих электронных пар, образуемых атомом принято называть его валентностью.
Валентность – это количество ковалентных связей атома с другими атомами.
Особо отметим, что если связи между атомами ковалентные, то это не свидетельство того, что вещество имеет молекулярное строение, т.е. состоит из молекул. Например, связи между атомами кремния и кислорода в SiO2 являются ковалентными, но SiO2 имеет атомное строение.
Чтобы однозначно определить имеет ли вещество молекулярное строение, необходимо знать его физические свойства: температуру кипения, температуру плавления и т.д. Вещества, имеющие молекулярное строение, как правило легкоплавки, имеют относительно низкую температуру кипения, так как связи между молекулами (межмолекулярное взаимодействие) достаточно слабые, имеющие низкие значения энергии.
Молекулы всегда имеют постоянный состав, поэтому и вещества молекулярного строения имеют постоянный состав, т.е. являются дальтонидами. Дальтониды подчиняются закону постоянства состава – закону Пруста (Ж. Л. Пруст, 1801—1808 гг.).
Для того, чтобы отразить состав молекулы применяют условную запись под названием химическая формула.
Химическая формула – условная запись, отражающая качественный и количественный состав веществ, имеющих молекулярное строение (условная запись состава молекулы).
Если вещество имеет немолекулярное строение (атомное или ионное), то его состав отражает формульная единица.
К примеру, если хлорид натрия находится при стандартных условиях, то он имеет ионное строение, а значит запись NaCl для кристаллического хлорида натрия не является химической формулой, а является записью формульной единицы.
При достаточно высоких температурах хлорид натрия можно перевести в газообразное агрегатное состояние, в этом случае резко повышается степень ковалентности связи. Это значит, что в газовой фазе существуют молекулы состава NaCl. На сей счёт имеются экспериментальные доказательства. Действительно, подобные молекулы в настоящее время удаётся получить, изолировав их друг от друга в твёрдом аргоне при температуре -2630 С. В приведённом примере запись NaCl является химической формулой, отражающей состав молекулы.
Во многих пособиях и учебниках до сих пор встречается определение молекулы, как наименьшей частицы вещества, обладающей его химическими свойствами.
Отметим, что данное определение является устаревшим и неправильным. Так молекулу определял Канницаро в 1860 году.
Ошибочность определения заключается в следующем.
Молекула не является наименьшей частицей вещества, так как существуют вещества атомного строения.
Молекула не является носителем химических свойств вещества, свойства обусловлены не единичной частицей, а их совокупностью, характером их взаимодействия.
Одна молекула тринитротолуола не обладает свойством взрывчатости, как даже две, три и большее их количество. Свойством взрывчатости будет обладать совокупность громадного числа молекул тринитротолуола – вещество.
Состав и строение молекулы определяют свойства вещества, но не молекула является носителем этих свойств.
Для наглядного изображения пространственного строения молекул применяют различные модели: шаростержневая модель, полусферическая модель Стюарта-Бриглеба, модель Драйдинга.
Способов, как определить формулу вещества, достаточно много. Все зависит от исходных данных. Наиболее разнообразны подобные вычисления в органической химии. И это не удивительно, так как органических соединений значительно больше, чем неорганических.
Содержание:
1.Понятие простейшей и истинной формулы вещества
2.Массовая доля химического элемента: что означает и как высчитывается
3.Как определить формулу вещества по массовым долям элементов
4.Как определить формулу органического соединения:
4.1. по общей формуле вещества
4.2. по продуктам сгорания вещества
5. Как определить формулу вещества: комбинированные задачи
1.Понятие простейшей и истинной формулы вещества
В одних задачах на определение формулы вещества необходимо найти его простейшую формулу, а в других – истинную. В чем разница?
Простейшая, или иными словами, эмпирическая формула, указывает на соотношение атомов в молекуле (или в формульной единице, если речь идет о не ковалентном соединении).
Так, например: СН2 – простейшая формула алкена – показывает, что на каждый 1 атом углерода приходится 2 водородных атома. То есть существует соотношение 1:2. Поэтому для нахождения простейшей (эмпирической) формулы вещества важно рассчитать количество вещества атомов, которые входят в его состав, то есть n(C) и n(H).
Истинная формула, или иначе молекулярная, отражает действительное количество атомов всех элементов в молекуле.
Например, для пропилена, относящегося к классу алкенов, истинная (молекулярная) формула будет C3H6. Она говорит о том, что молекула данного вещества включает 3 атома С и 6 атомов Н. Это вполне соответствует простейшей формуле, отвечающей соотношению атомов 1:2. Для нахождения истинной (молекулярной) формулы соединения требуется посчитать его относительную молекулярную (Mr) или молярную массу (M).
2.Массовая доля химического элемента: что означает и как высчитывается
Массовая доля – это отношение массы компонента системы к массе системы, выраженное в процентах или долях от единицы.
Ну, а теперь проще.
Молекула имеет массу. Все атомы в молекуле также имеют свои массы. Атомов одного химического элемента в молекуле может быть 1 или несколько. Важна масса всех атомов одного элемента. Если ее разделить на массу молекулы, то получится массовая доля этого элемента. Ее выражают либо в процентах, которые всегда меньше 100%, либо в долях от единицы, которые всегда меньше 1.
Массовая доля элемента обозначается греческой буквой «омега» — ω. И записывается, например, так: ω(Н), ω(Сl), ω(С) и т.д. и рассчитывается:
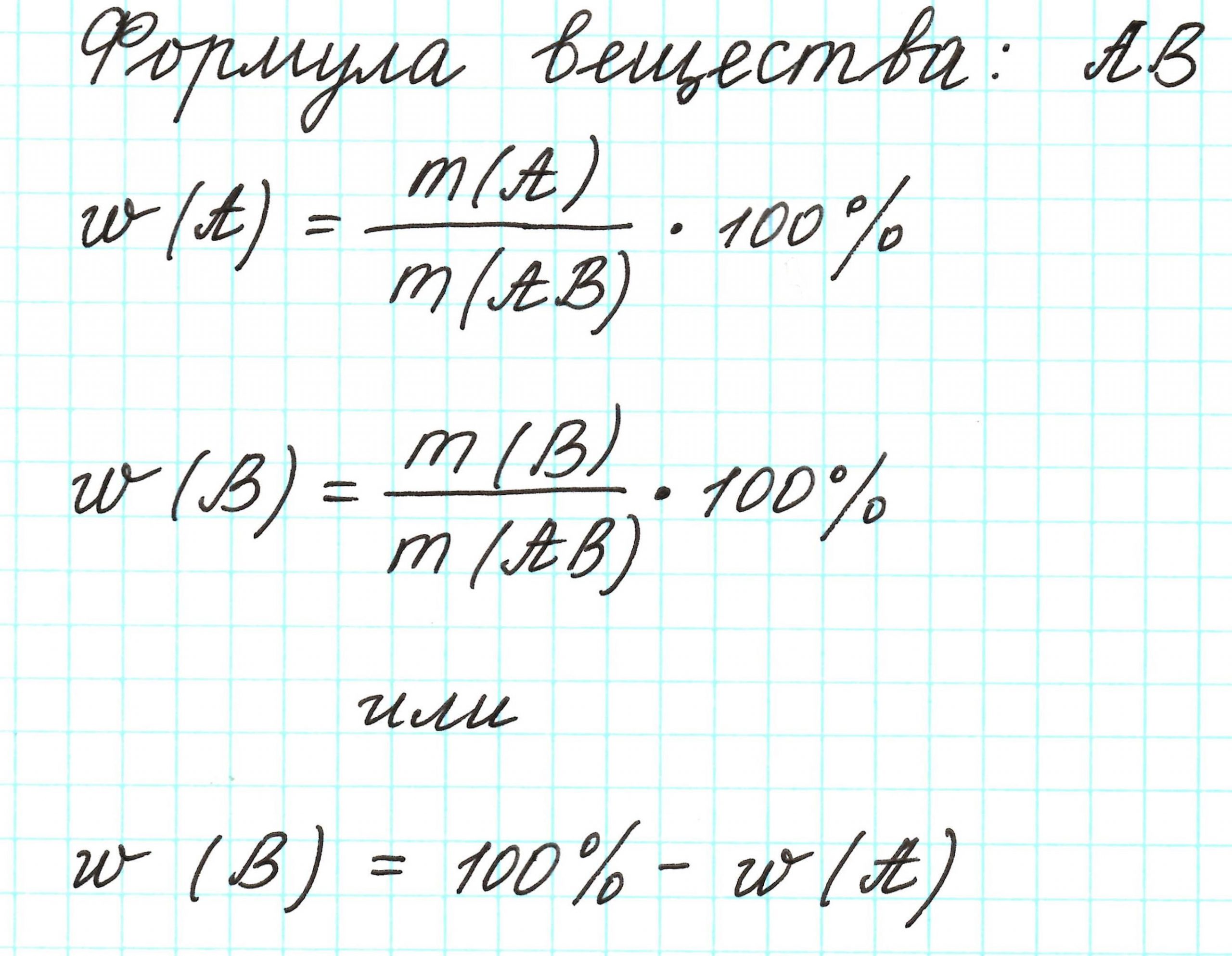
Пример 1. Каковы массовые доли элементов в оксиде железа (III) Fe2O3.
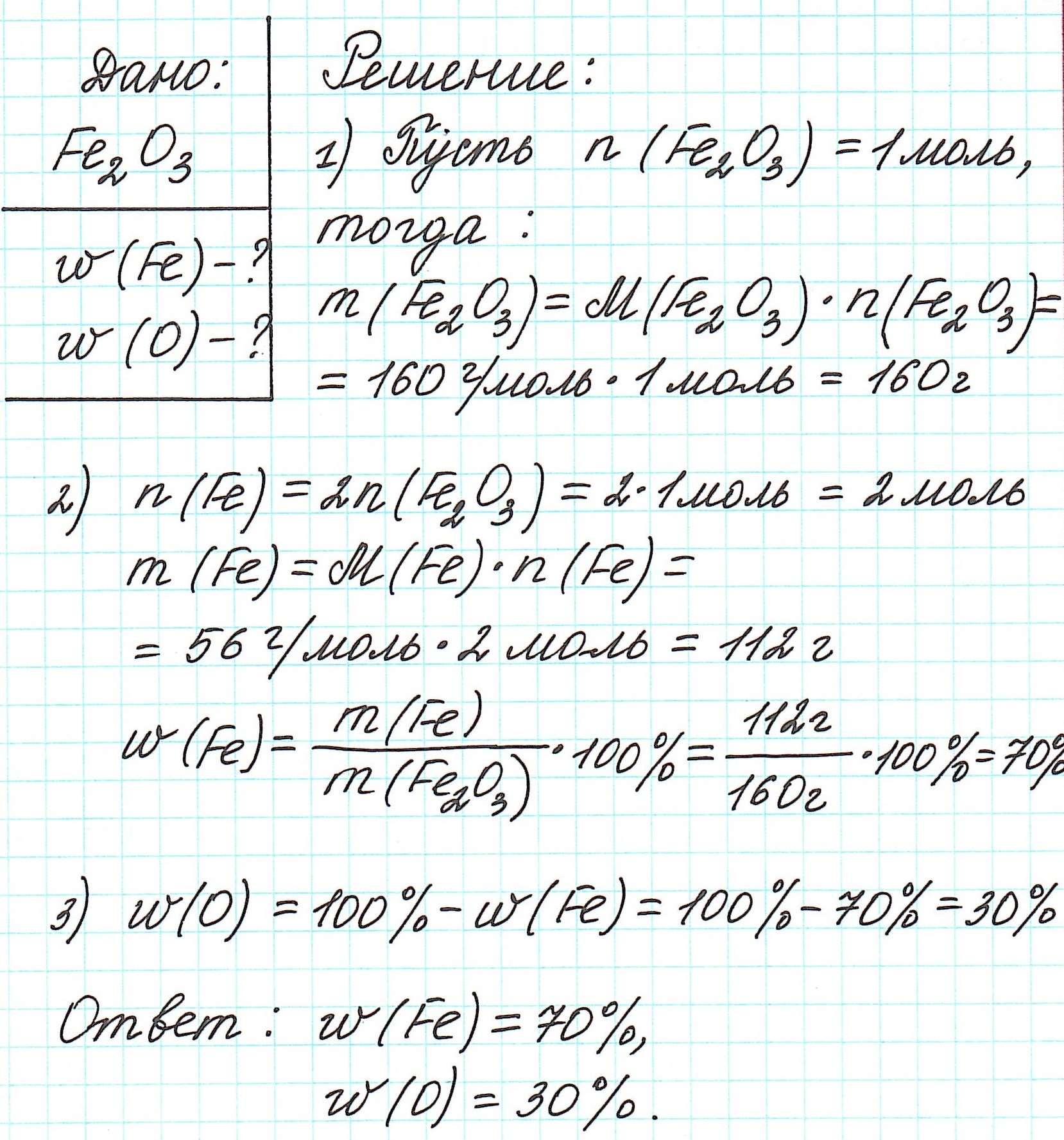
3.Как определить формулу вещества по массовым долям элементов
Нахождение формулы вещества по массовым долям элементов применимо как к органическим, так и к неорганическим соединениям.
Пример 2. Сероуглерод содержит 15,8% углерода по массе. Какова простейшая формула этого вещества?
Поскольку речь идет о массовых долях элементов, то необходимо знать массу вещества. В нашем случае – массу сероуглерода. В условии задачи о ней ничего не говорится. Поэтому допускаем, что масса вещества равна 100 г.
Почему 100 г? Это «круглое» число, и его использование облегчает все расчеты. Так как в итоге будем находить соотношения количеств веществ элементов, то какое-то особенное значение массы вещества не играет никакой роли.
Попробуйте ради эксперимента принять массу сероуглерода равной 23 г, 467 г и т.п. Результат будет один и тот же.
Допустим, что атомов углерода в молекуле х, а атомов серы – у. В таком случае формула вещества примет вид: СхSу.
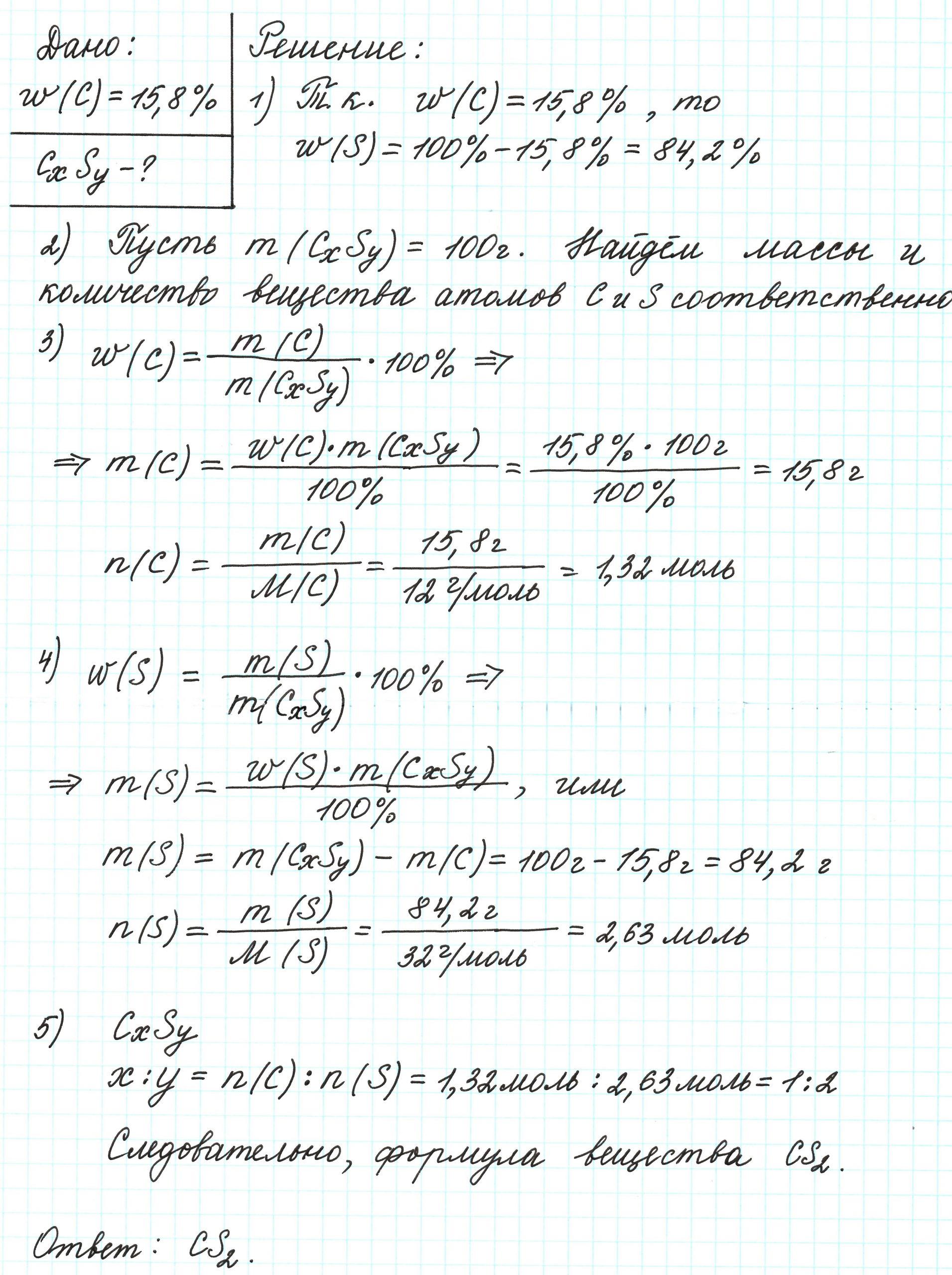
Пример 3. Содержание углерода в углеводороде составляет 83,33%. Плотность паров соединения по водороду – 36. Какова молекулярная формула углеводорода?
Из данных задачи следует, что углеводород может находиться в газообразном состоянии, так как известна плотность его паров. Эта величина всегда требуется для нахождения молярной (относительной молекулярной) массы вещества. Как она находится и что это такое читайте подробнее здесь.
Чтобы не загромождать записи, массовую долю элементов будем считать не в процентах, а в долях от единицы.

Пусть вас не удивляет получившаяся простейшая формула. Ведь, исходя из определения простейшей формулы, на каждый 1 атом углерода приходится 2,4 атома водорода. Это всего лишь соотношение. Соединения с формулой СН2,4 в принципе не существует. Не всегда простейшая и истинная формулы совпадают друг с другом.
А если полученная формула СН2,4 вас все же смущает, вы можете решать задачу и вторым способом. Но это несколько более сложный способ, когда требуется составить и решить уравнение с двумя неизвестными.
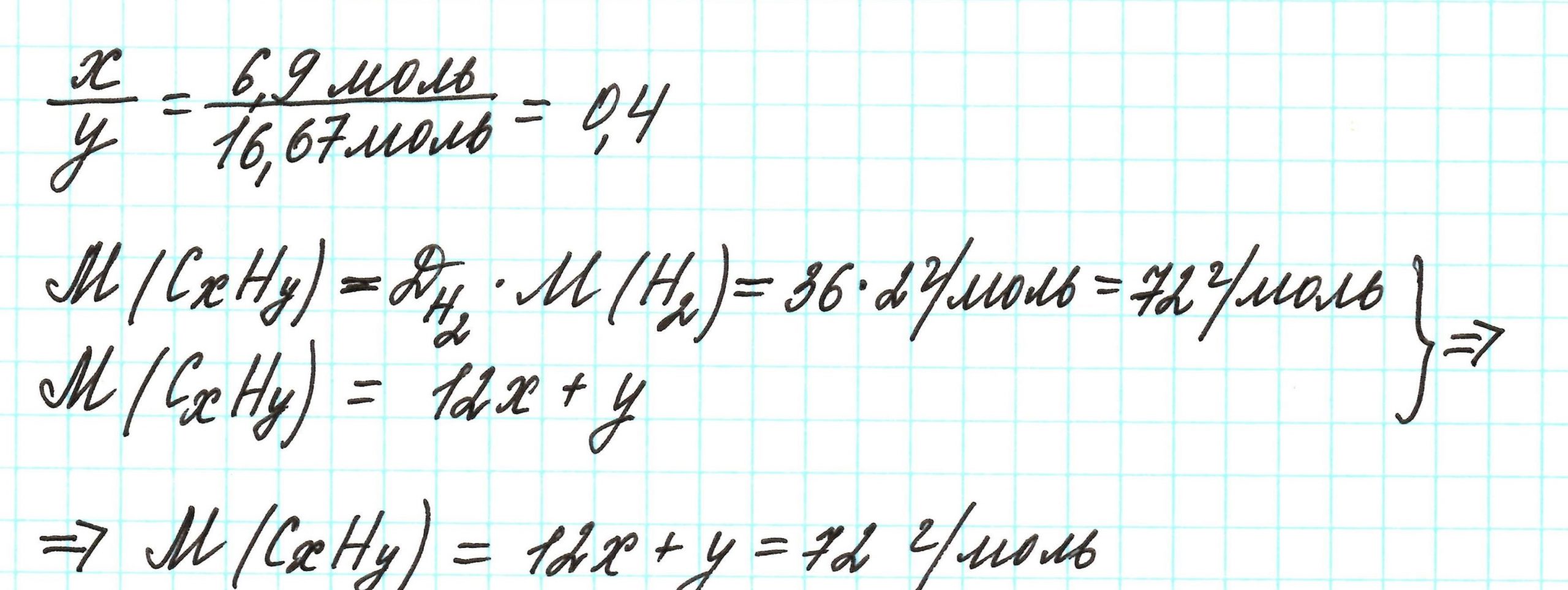

Не все химические вещества являются бинарными, то есть состоят из атомов двух химических элементов. Но в любом случае, алгоритм решения задачи тот же.
Пример 4. Некоторая кислота содержит водород (2,2%), иод (55,7%) и кислород (42,1%). Определите простейшую формулу этой кислоты.
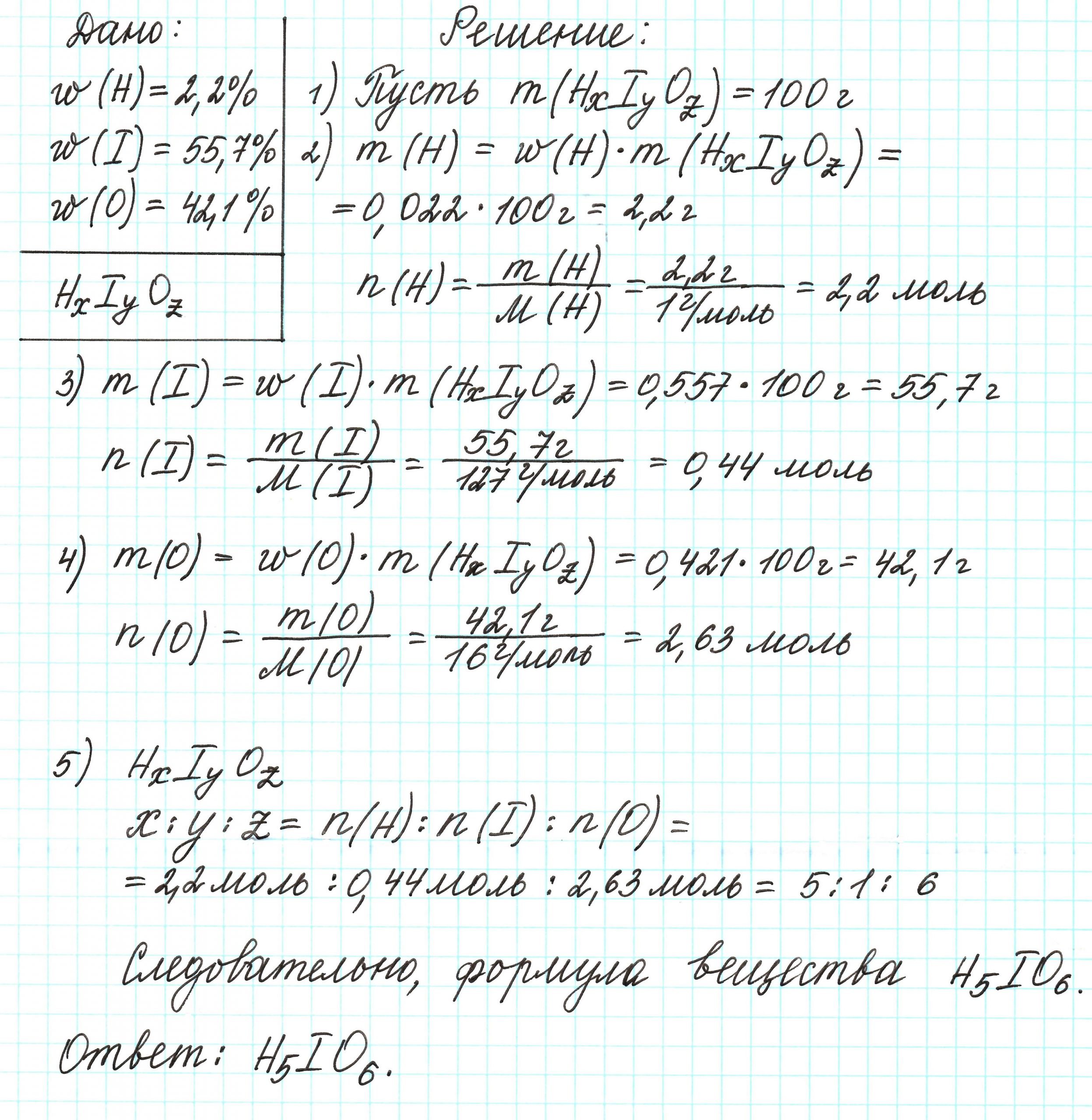
4.Как определить формулу органического соединения
Определить формулу органического вещества можно не только зная массовые доли элементов в его составе.
4.1. Как определить формулу органического соединения
по общей молекулярной формуле вещества
Органические вещества сгруппированы по самостоятельным классам на основе общности строения и свойств. Каждый класс соединений характеризуется своей общей молекулярной формулой. Особенно это наглядно видно на примере углеводородов.
Если другие органические вещества рассматривать как их производные, в молекулы которых введена какая-либо функциональная группа, то и для них также можно составить общую молекулярную формулу.
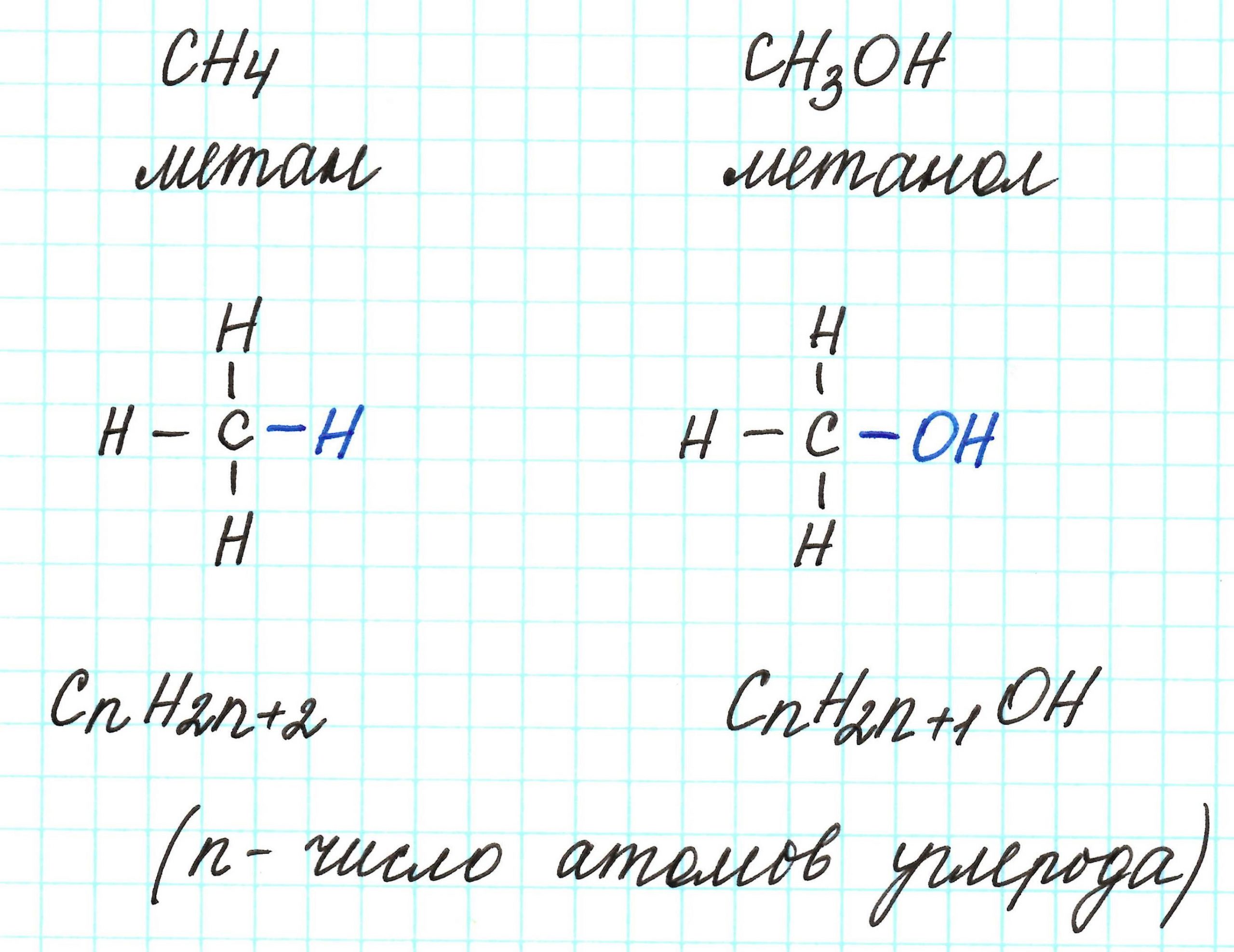
К слову, метан СН4 является представителем алканов, в молекулах которых на n атомов углерода и приходится 2n+2 атомов водорода. Алканы имеют общую молекулярную формулу, отражающую их состав: СnH2n+2.
Предельные одноатомные спирты можно рассматривать как производные алканов, в молекулах которых 1 атом водорода замещен на гидроксильную группа –ОН. Таким образом, их общая молекулярная формула такая: СnH2n+1ОН.
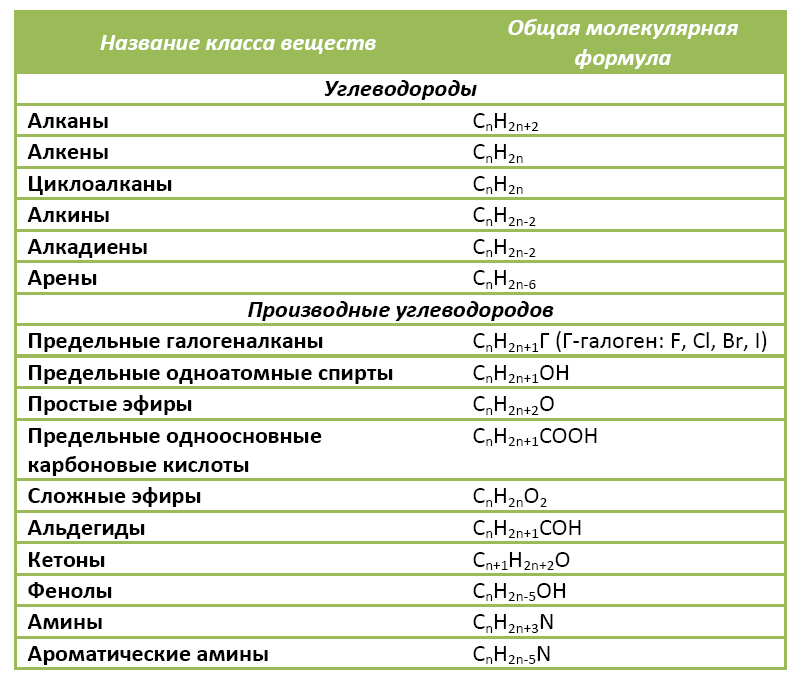
Ниже в таблице приведены общие молекулярные формулы основных классов органических соединений.
 Разберем примеры решения задач с использованием общей молекулярной формулы вещества.
Разберем примеры решения задач с использованием общей молекулярной формулы вещества.
Пример 5. Плотность паров по воздуху некоторого алкана 4,414. Какова формула алкана?

4.2. Как определить формулу органического соединения
по продуктам его сгорания
Это еще один распространенный тип задач на определение формулы органического соединения.
Необходимо запомнить и понять основные моменты:
— так как все органические вещества содержат атомы С, Н, а также атомы О (кислородсодержащие соединения), то всегда при их сгорании выделяется углекислый газ СО2 и образуется вода Н2О;
— все углеродные атомы, входящие в состав органического соединения, окажутся в составе углекислого газа СО2; следовательно, n(С) как в соединении, так и в СО2 – это одна и та же величина;
— все атомы водорода Н, которые имеются в составе вещества, перейдут в состав воды Н2О; следовательно, n(Н) и в данном веществе, и в Н2О – это одна и та же величина;
— при сгорании веществ, включающих в себя азот (например, амины), кроме СО2 и Н2О, образуется еще и N2.
Разберем несколько примеров.
Пример 6. Сожгли 7,2 г углеводорода. Плотность его паров по водороду составляет 36. В результате реакции образовалось 22 г оксида углерода (IV) и 10,8 г воды. Какова молекулярная формула соединения?

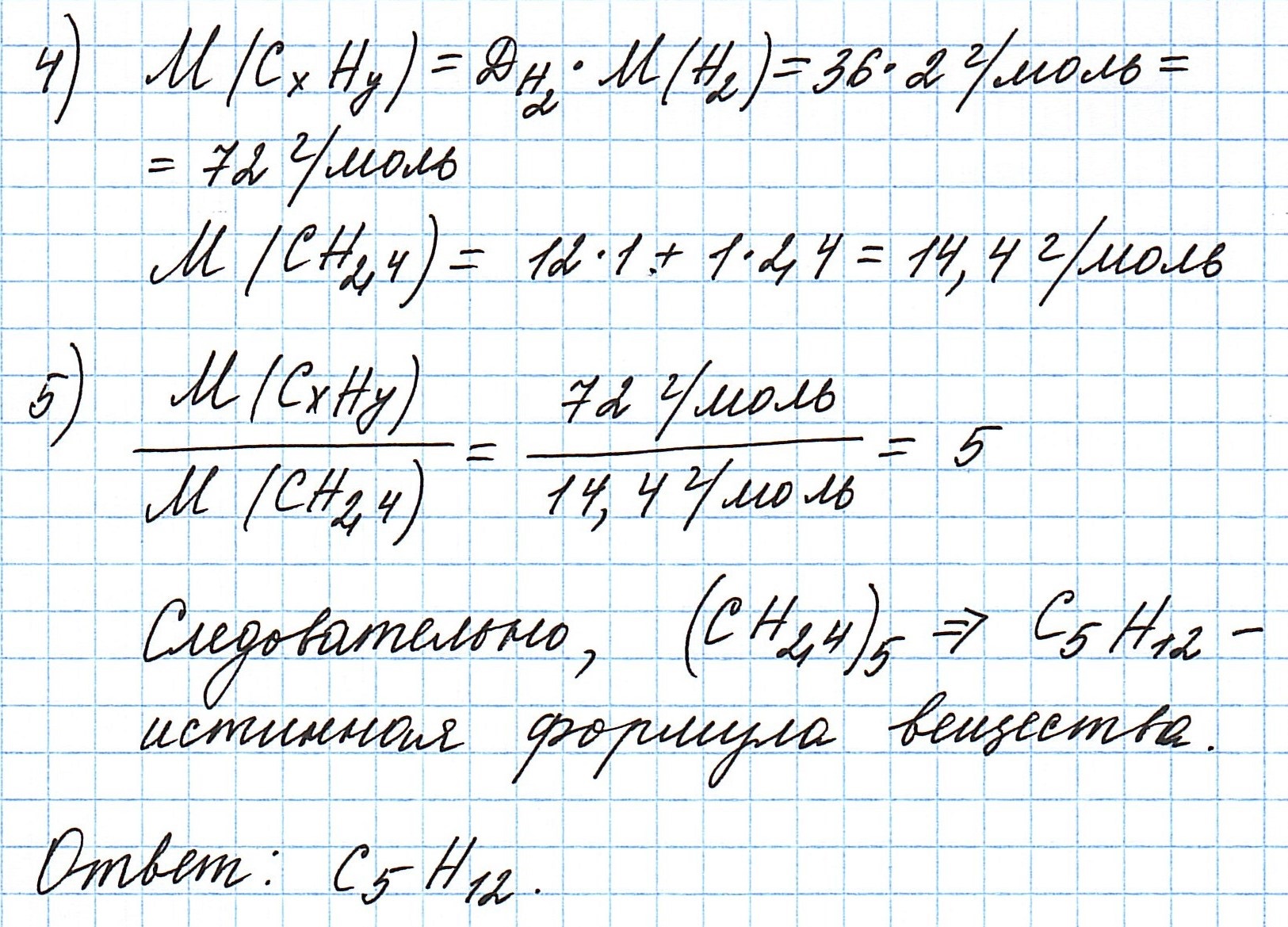
Пример 7. В результате сгорания 4,8 г органического соединения выделилось 3,36 л (н.у.) оксида углерода (IV) и образовалось 5,4 г воды. Плотность паров искомого соединения по кислороду равна 1. Вычислите молекулярную формулу вещества.


Пример 8. Результатом сжигания 0,31 г газообразного органического соединения, имеющего плотность 1,384 г/л, стало выделение 0,224 л (с.у.) оксида углерода (IV), 0,112 л азота и образование 0,45 г воды. Вычислите молекулярную формулу этого вещества.


5. Как определить формулу вещества: комбинированные задачи
Наибольший интерес и некоторую трудность представляют комбинированные задачи, сочетающие в себе необходимость найти формулу соединения:
— используя приемы, применяемые в рассмотренных выше задачах;
— используя сведения не только о химических, но и физических свойствах вещества.
Вот несколько примеров.
Пример 9. Какова молекулярная формула предельного углеводорода, при полном сгорании 8,6 г которого выделилось 13, 44 л (н.у.) оксида углерода (IV).
В этой задаче:
1) известен класс вещества, поэтому возможно применить его общую молекулярную формулу;
2) речь идет о сгорании вещества, поэтому количество атомов в составе молекулы будем искать, используя данные о продукте сгорания – СО2.

Пример 10. Алкен нормального строения содержит двойную связь при первом углеродном атоме. Образец этого алкена массой 0,7 г присоединил бром массой 1,6 г. Вычислите формулу алкена и назовите его.
В предлагаемых условиях:
1) известен класс вещества, следовательно, применим его общую молекулярную формулу;
2) речь идет об одном из химических свойств: способности алкенов присоединять галогены по месту разрыва двойной связи.

Пример 11. После полного сжигания в кислороде арена, имевшего массу 0,92 г, выделился оксид углерода (IV). Пропуская газ через избыток раствора щелочи Ca(OH)2, получили 7 грамм осадка. Какова молекулярная формула арена?
В предлагаемой задаче:
1) известен класс вещества;
2) речь идет о сжигании соединения и образовании в качестве продукта горения углекислого газа, который при взаимодействии со щелочью Са(ОН)2 привел к выпадению осадка известной массы.

Следующий пример очень характерен для задач, встречающихся в заданиях второй части ЕГЭ по химии.
Пример 12. Некоторое соединение, образующее альдегид в реакции окисления, взаимодействует с избытком бромоводородной кислоты, образуя 9,84 г продукта (выход составляет 80% от теоретического), имеющего плотность паров по Н2 61,5. Определите строение этого соединения, а также его массу, вступившую в реакцию?
В этой задаче:
1) говорится о химических свойствах искомого соединения; анализируя их, приходим к выводу, что заданным веществом является предельный одноатомный спирт;
2) известна общая молекулярная формула предельных одноатомных спиртов;
3) более подробно говорится о взаимодействии заданного вещества с бромоводородной кислотой; спирт, реагируя с HBr, дает галогеналкан, для которого известны его масса, практический выход и относительная плотность по Н2; именно от этих данных и нужно отталкиваться при решении данной задачи.

Итак, способов, как определить формулу вещества, действительно, множество. Мы рассмотрели лишь основные из них. Важно правильно уяснить понятия «простейшая формула вещества» и «истинная формула вещества», чтобы не путать их.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.

Моле́кула (новолат. molecula, уменьшительное от лат. moles — масса[1]) — электрически нейтральная частица, образованная из двух или более связанных атомов[2][3][4][5][6][7].
В отдельных разделах физики к молекулам причисляют также одноатомные молекулы, то есть свободные (химически не связанные) атомы (например, инертных газов, ртути и т. п.).
Обычно подразумевается, что молекулы нейтральны (не несут электрических зарядов) и не несут неспаренных электронов (все валентности насыщены); заряженные молекулы называют молекулярными ионами, молекулы с мультиплетностью, отличной от единицы (то есть с неспаренными электронами и ненасыщенными валентностями), — радикалами.
Молекулы относительно высокой молекулярной массы, состоящие из повторяющихся низкомолекулярных фрагментов, называются макромолекулами[8].
С точки зрения квантовой механики[9] молекула представляет собой систему не из атомов, а из электронов и атомных ядер, взаимодействующих между собой.
Особенности строения молекул определяют физические свойства вещества, состоящего из этих молекул.
К веществам, сохраняющим молекулярную структуру в твёрдом состоянии, относятся, например, вода, оксид углерода(IV), многие органические вещества. Они характеризуются низкими температурами плавления и кипения. Большинство же твёрдых (кристаллических) неорганических веществ состоят не из молекул, а из других частиц (ионов, атомов) и существуют в виде макротел (кристалл хлорида натрия, кусок меди и т. д.).
Состав молекул сложных веществ выражается при помощи химических формул.

История[править | править код]
На международном съезде химиков в Карлсруэ в 1860 году были приняты определения понятий молекулы и атома. Молекула была определена как наименьшая частица химического вещества, обладающая всеми его химическими свойствами.
Классическая теория химического строения[править | править код]

Шаро-стержневая модель молекулы диборана B2H6. Атомы бора показаны розовым, водорода — серым.
Центральные «мостиковые» атомы одновалентного водорода образуют с соседними атомами бора трёхцентровые связи

Пространственная структура молекулы диборана.
Длины связей показаны серым, валентные углы — цветным.
Диэдральный угол между плоскостями периферических и мостиковых троек ядер H-B-H составляет 90°
В классической теории химического строения молекула рассматривается как наименьшая стабильная частица вещества, обладающая всеми его химическими свойствами. В этом определении к молекулам относятся и одноатомные частицы (в частности, молекулы инертных газов)
Молекула данного вещества имеет постоянный состав, то есть одинаковое количество атомов, объединённых химическими связями, при этом химическая индивидуальность молекулы определяется именно совокупностью и конфигурацией химических связей, то есть валентными взаимодействиями между входящими в её состав атомами, обеспечивающими её стабильность и основные свойства в достаточно широком диапазоне внешних условий. Невалентные взаимодействия (например, водородные связи), которые зачастую могут существенно влиять на свойства молекул и вещества, образуемого ими, в качестве критерия индивидуальности молекулы не учитываются.
Центральным положением классической теории является положение о химической связи, при этом допускается наличие не только двухцентровых связей, объединяющих пары атомов, но и наличие многоцентровых (обычно трёхцентровых, иногда — четырёхцентровых) связей с «мостиковыми» атомами — как, например, мостиковых атомов водорода в боранах, природа химической связи в классической теории не рассматривается — учитываются лишь такие интегральные характеристики, как валентные углы, диэдральные углы (углы между плоскостями, образованными тройками ядер), длины связей и их энергии.
Таким образом, молекула в классической теории представляется динамической системой, в которой атомы рассматриваются как материальные точки и в которой атомы и связанные группы атомов могут совершать механические вращательные и колебательные движения относительно некоторой равновесной ядерной конфигурации, соответствующей минимуму энергии молекулы и рассматривается как система гармонических осцилляторов.
Молекула состоит из атомов, а если точнее, то из атомных ядер, окружённых определённым числом внутренних электронов, и внешних валентных электронов, образующих химические связи. Внутренние электроны атомов обычно не участвуют в образовании химических связей. Состав и строение молекул вещества не зависят от способа его получения.
Атомы объединяются в молекуле в большинстве случаев с помощью химических связей. Как правило, такая связь образуется одной, двумя или тремя парами электронов, находящихся в совместном владении двух атомов, образуя общее электронное облако, форма которого описывается типом гибридизации. Молекула может иметь положительно и отрицательно заряженные атомы (ионы).
Состав молекулы передаётся химическими формулами. Эмпирическая формула устанавливается на основе атомного соотношения элементов вещества и молекулярной массы.
Геометрическая структура молекулы определяется равновесным расположением атомных ядер. Энергия взаимодействия атомов зависит от расстояния между ядрами. На очень больших расстояниях эта энергия равна нулю. Если при сближении атомов образуется химическая связь, то атомы сильно притягиваются друг к другу (слабое притяжение наблюдается и без образования химической связи), при дальнейшем сближении начинают действовать электростатические силы отталкивания атомных ядер. Препятствием к сильному сближению атомов является также невозможность совмещения их внутренних электронных оболочек.
Каждому атому в определённом валентном состоянии в молекуле можно приписать определённый атомный, или ковалентный радиус (в случае ионной связи — ионный радиус), который характеризует размеры электронной оболочки атома (иона) образующего химическую связь в молекуле. Размер электронной оболочки молекулы, является условной величиной. Существует вероятность (хотя и очень малая) найти электроны молекулы и на большем расстоянии от её атомного ядра. Практические размеры молекулы определяются равновесным расстоянием, на которое они могут быть сближены при плотной упаковке молекул в молекулярном кристалле и в жидкости. На бо́льших расстояниях молекулы притягиваются друг к другу, на меньших — отталкиваются. Размеры молекулы можно найти с помощью рентгеноструктурного анализа молекулярных кристаллов. Порядок величины этих размеров может быть определён из коэффициентов диффузии, теплопроводности и вязкости газов и с плотности вещества в конденсированном состоянии. Расстояние, на которое могут сблизиться валентно не связанные атомы одного и того же или разных молекул, может быть охарактеризована средними значениями так называемых ван-дер-ваальсовых радиусов.
Радиус Ван-дер-Ваальса существенно превышает ковалентный. Зная величины ван-дер-ваальсовых, ковалентных и ионных радиусов, можно построить наглядные модели молекул, которые бы отражали форму и размеры их электронных оболочек.
Ковалентные химические связи в молекуле расположены под определёнными углами, которые зависят от состояния гибридизации атомных орбиталей. Так, для молекул насыщенных органических соединений характерно тетраэдральное (четырёхгранное) расположение связей, образуемых атомом углерода, для молекул с двойной связью (С = С) — плоское расположение атомов углерода, для молекул соединений с тройной связью (С ≡ С) — линейное расположение связей. Таким образом, многоатомная молекула имеет определённую конфигурацию в пространстве, то есть определённую геометрию расположения связей, которая не может быть изменена без их разрыва. Молекула характеризуется той или иной симметрией расположения атомов. Если молекула не имеет плоскости и центра симметрии, то она может существовать в двух конфигурациях, которые представляют собой зеркальные отражения друг друга (зеркальные антиподы, или стереоизомеры). Все важнейшие биологические функциональные вещества в живой природе существуют в форме одного определённого стереоизомера.
Молекулы, содержащие единичные связи, или сигма-связи, могут существовать в различных конформациях, возникающих при поворотах атомных групп вокруг единичных связей. Важные особенности макромолекул синтетических и биологических полимеров определяются именно их конформационными свойствами.
Квантохимическая теория химического строения[править | править код]
В квантохимической теории химического строения основными параметрами, определяющими индивидуальность молекулы, является её электронная и пространственная (стереохимическая) конфигурации. При этом в качестве электронной конфигурации, определяющей свойства молекулы, принимается конфигурация с наинизшей энергией, то есть основное энергетическое состояние.
Представление структуры молекул[править | править код]
Молекулы состоят из электронов и атомных ядер, расположение последних в молекуле передаёт структурная формула (для передачи состава используется т. н. брутто-формула). Молекулы белков и некоторых искусственно синтезированных соединений могут содержать сотни тысяч атомов. Отдельно рассматриваются макромолекулы полимеров.
Молекулы являются объектом изучения теории строения молекул, квантовой химии, аппарат которых активно использует достижения квантовой физики, в том числе релятивистских её разделов. Также в настоящее время развивается такая область химии, как молекулярный дизайн. Для определения строения молекул конкретного вещества современная наука располагает колоссальным набором средств: электронная спектроскопия, колебательная спектроскопия, ядерный магнитный резонанс и электронный парамагнитный резонанс и многие другие, но единственными прямыми методами в настоящее время являются дифракционные методы, как то: рентгеноструктурный анализ и дифракция нейтронов.
Взаимодействие атомов при образовании молекулы[править | править код]
Природа химических связей в молекуле оставалась загадкой до создания квантовой механики — классическая физика не могла объяснить насыщаемость и направленность валентных связей. Основы теории химической связи были заложены в 1927 году Гайтлером и Лондоном на примере простейшей молекулы Н2. Позже теория и методы расчётов были значительно усовершенствованы.
Химические связи в молекулах подавляющего большинства органических соединений является ковалентными. Среди неорганических соединений существуют ионные и донорно-акцепторные связи, которые реализуются в результате обобществления пары электронов атома. Энергия образования молекулы из атомов во многих рядах подобных соединений приближённо аддитивна. То есть можно считать, что энергия молекулы — это сумма энергий её связей, имеющих постоянные значения в таких рядах.
Аддитивность энергии молекулы выполняется не всегда. Примером нарушения аддитивности являются плоские молекулы органических соединений с так называемыми сопряжёнными связями, то есть с кратными связями, которые чередуются с единичными. Сильная делокализация p-состояний электронов приводит к стабилизации молекулы. Выравнивание электронной плотности вследствие коллективизации p-состояний электронов по связям выражается в укорочении двойных связей и удлинении одинарных. В правильном шестиугольнике межуглеродных связей бензола все связи одинаковы и имеют длину, среднюю между длиной одинарной и двойной связи. Сопряжение связей ярко проявляется в молекулярных спектрах. Современная квантовомеханическая теория химических связей учитывает делокализации не только p-, но и s-состояний электронов, которая наблюдается в любых молекулах.
В подавляющем большинстве случаев суммарный спин валентных электронов в молекуле равен нулю. Молекулы, содержащие неспаренные электроны — свободные радикалы (например, атомарный водород Н, метил ·CH3), обычно неустойчивы, поскольку при их взаимодействии друг с другом происходит значительное снижение энергии вследствие образования ковалентных связей. Они могут устойчиво существовать при таких температурах, когда средняя кинетическая энергия молекулы превосходит или сравнима с энергией связи, но при этом ниже энергии разрушения (например ионизации) радикала.
Межмолекулярное взаимодействие[править | править код]
Межмолекулярное взаимодействие — взаимодействие между электрически нейтральными молекулами в пространстве. В зависимости от полярности молекул характер межмолекулярного взаимодействия разный. Природа последнего оставалась неясной до создания квантовой механики.

- Ориентационный тип межмолекулярного взаимодействия возникает между двумя полярными молекулами, то есть, такими, которые имеют собственный дипольный момент. Взаимодействие дипольных моментов и определяет результирующую силу — притяжения или отталкивания. В случае, если дипольные моменты молекул размещаются на одной линии, взаимодействие молекул будет интенсивней.
- Индукционный тип — между одной полярной и одной неполярной молекулами. Полярная молекула поляризует неполярную так, что заряд неполярной молекулы, противоположный действующему на неё заряда полярной молекулы, смещается до последнего: в общем, положительный заряд смещается по направлению электрического поля, которое создаёт полярная молекула, а отрицательный — против. Это обусловливает поляризацию неполярной молекулы, то есть явления смещения связанной электронной оболочки относительно центра положительного заряда.
- Дисперсионный — между двумя неполярными молекулами. В общем, дипольные моменты неполярных молекул равны нулю, однако в определённый момент времени, есть вероятность распределения электронов по всему объёму молекулы неравномерно. Вследствие этого возникает мгновенный дипольный момент. При этом, мгновенный диполь или поляризует соседние неполярные молекулы, или взаимодействует с мгновенным диполем другой нейтральной молекулы.
Электрические и оптические свойства молекул[править | править код]
Поведение вещества в электрическом поле определяется основными электрическими характеристиками молекул — постоянным дипольным моментом и поляризуемостью.
Дипольный момент означает несовпадение «центров тяжести» положительных и отрицательных зарядов в молекуле (электрическую асимметрию молекулы). То есть молекулы, имеющие центр симметрии, например H2, лишены постоянного дипольного момента, и наоборот.
Поляризуемость — это способность электронной оболочки любой молекулы перемещаться под действием электрического поля, в результате чего в молекуле образуется наведённый дипольный момент. Значение дипольного момента и поляризуемости находят экспериментально с помощью измерения диэлектрической проницаемости.
Оптические свойства вещества характеризуют его поведение в переменном электрическом поле световой волны и определяются поляризуемостью молекулы этого вещества. С поляризуемостью непосредственно связаны преломление и рассеяние света, оптическая активность и другие явления, изучаемые молекулярной оптикой.
Магнитные свойства молекул[править | править код]
Молекулы и макромолекулы подавляющего большинства химических соединений являются диамагнитными. Магнитная восприимчивость молекул (χ) для отдельных органических соединений может быть выражена как сумма значений χ для отдельных связей.
Молекулы, имеющие постоянный магнитный момент, является парамагнитными. К таковым относятся молекулы с нечётным количеством электронов на внешней оболочке (например, NO и любые свободные радикалы), молекулы, содержащие атомы с незаполненными внутренними оболочками (переходные металлы и т. д.). Магнитная восприимчивость парамагнитных веществ зависит от температуры, поскольку тепловое движение препятствует ориентации магнитных моментов в магнитном поле.
Спектры и строение молекул[править | править код]
Электрические, оптические, магнитные и другие свойства молекул связаны с волновыми функциями и энергиями различных состояний молекул. Информацию о состояниях молекул и вероятности перехода между ними дают молекулярные спектры.
Частоты колебаний в спектрах определяются массами атомов, их расположением и динамикой межатомных взаимодействий. Частоты в спектрах зависят от моментов инерции молекул, определение которых из спектроскопических данных позволяет получить точные значения межатомных расстояний в молекуле. Общее число линий и полос в колебательном спектре молекулы зависит от её симметрии.
Электронные переходы в молекулах характеризуют структуру их электронных оболочек и состояние химических связей. Спектры молекул, которые имеют большее количество связей, характеризуются длинноволновыми полосами поглощения, попадающими в видимую область. Вещества, которые построены из таких молекул, характеризуются окраской; к таким веществам относятся все органические красители.
Молекулы в химии, физике и биологии[править | править код]
Понятие молекулы является основным для химии, и большей частью сведений о строении и функциональность молекул наука обязана химическим исследованиям. Химия определяет строение молекул на основе химических реакций и, наоборот, на основе строения молекулы определяет, каким будет ход реакций.
Строением и свойствами молекулы определяются физические явления, которые изучаются молекулярной физикой. В физике понятие молекулы используется для объяснения свойств газов, жидкостей и твёрдых тел. Подвижностью молекул определяется способность вещества к диффузии, его вязкость, теплопроводность и т. д. Первое прямое экспериментальное доказательство существования молекул было получено французским физиком Жаном Перреном в 1906 году при изучении броуновского движения.
Поскольку все живые организмы существуют на основе тонко сбалансированного химического и нехимического взаимодействия между молекулами, изучение строения и свойств молекул имеет фундаментальное значение для биологии и естествознания в целом.
Развитие биологии, химии и молекулярной физики привели к возникновению молекулярной биологии, которая исследует основные явления жизни, исходя из строения и свойств биологически функциональных молекул.
См. также[править | править код]
- Химический элемент
- Молекулярные вещества
- Супрамолекула
- Теория молекулярных орбиталей
Примечания[править | править код]
- ↑ Молекула — статья из Большой советской энциклопедии.
- ↑ IUPAC Gold Book internet edition: (1994) «molecule».
- ↑ Pauling, Linus. General Chemistry (неопр.). — New York: Dover Publications, Inc., 1970. — ISBN 0-486-65622-5.
- ↑ Ebbin, Darrell, D. General Chemistry, 3rd Ed (неопр.). — Boston: Houghton Mifflin Co. (англ.) (рус., 1990. — ISBN 0-395-43302-9.
- ↑ Brown, T.L. Chemistry – the Central Science, 9th Ed (неопр.). — New Jersey: Prentice Hall, 2003. — ISBN 0-13-066997-0.
- ↑ Chang, Raymond. Chemistry, 6th Ed (неопр.). — New York: McGraw-Hill Education, 1998. — ISBN 0-07-115221-0.
- ↑ Zumdahl, Steven S. Chemistry, 4th ed (неопр.). — Boston: Houghton Mifflin (англ.) (рус., 1997. — ISBN 0-669-41794-7.
- ↑ macromolecule (polymer molecule) // IUPAC Gold Book. Дата обращения: 12 сентября 2011. Архивировано 9 мая 2010 года.
- ↑ Татевский В. М. Квантовая механика и теория строения молекул. — М.: Изд-во МГУ, 1965. — 162 с.
Литература[править | править код]
- Татевский В. М. Квантовая механика и теория строения молекул. — М.: Изд-во МГУ, 1965. — 162 с.
- Бейдер Р. Атомы в молекулах. Квантовая теория. — М.: Мир, 2001. — 532 c. ISBN 5-03-003363-7
- Минкин В. И., Симкин Б. Я., Миняев Р. М. Теория строения молекул. — М.: Высшая школа, 1979. — 408 с.
- Кук Д. Квантовая теория молекулярных систем. Единый подход. Пер с англ. М.: Интеллект, 2012. — 256 с. ISBN 978-5-91559-096-9
- Степанов Н. Ф. Молекула // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Большая Российская энциклопедия, 1992. — Т. 3: Меди — Полимерные. — С. 106—109. — 639 с. — 48 000 экз. — ISBN 5-85270-039-8.
Ссылки[править | править код]
- Молекула // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Молекулы (видеурок, программа 7 класса)
- Molecule // IUPAC Gold Book
- Molecular entity // IUPAC Gold Book
- Шредингер Э. Волновая теория механики атомов и молекул. УФН 1927
- Статья «Молекула» в Физической энциклопедии
- Урок по теме «Молекулы и атомы»
Известно, что все вещества состоят из молекул. Классическая теория химического строения вещества рассматривает молекулу как самую маленькую постоянную частицу, которой присущи все его свойства. Но из чего состоят сами молекулы? Давайте рассмотрим этот вопрос подробнее.
Что такое молекула?
Название «молекула» происходит от латинского molecula – это уменьшительное от слова moles (в переводе масса). Впервые их существование было доказано в эксперименте в 1906 г. Ж. Перреном, французским физиком, когда он изучал броуновское движение.

В химии так называется отдельная частица вещества, которая состоит из 2 или больше атомов, связанных между собой ковалентными связями. Квантовая механика определяет ее как систему, состоящую не из атомов, а из их ядер и электронов, с ними взаимодействующих.
Интересный факт: физика называет молекулами не только многоатомные частицы, но и одноатомные, состоящие из атомов, не соединенных между собой химическими связями (чистая ртуть или инертные газы). В этом случае понятия «молекула» и «атом» совмещаются.
Обыкновенно молекулы электрически нейтральны, так как число протонов и электронов в них одинаково, но бывают молекулы, имеющие электрический заряд (называются они ионы).
Частицы вещества с большой молекулярной массой получили название макромолекулы. Из них состоят протеины, нуклеиновые кислоты, ферменты, полисахариды, аминокислоты, сложные липиды и отдельные созданные искусственно соединения, например, полимеры. Они включают в себя сотни и тысячи атомов. Производные углеводородов – органические вещества и биополимеры, как правило, не только имеют большую массу, но и устроены сложнее, чем неорганические соединения.
Строение молекул
У молекулы какого-либо соединения состав неизменный, в ней всегда одинаковое число атомов, химические свойства зависят от валентных связей, их скрепляющих. Классическая теория рассматривает молекулу как динамическую структуру, состоящую из ядер атомов и их групп и некоторого числа электронов, находящихся на внутренних и внешних уровнях.

Химические связи образуют обычно только внешние электроны. Связь создается 1,2 или 3 парами электронов 2 соседних атомов (в результате чего появляется электронное облако). Энергия взаимодействия атомов зависит от дистанции, на которой они находятся, и способствует стабильности молекулы при обычных условиях: она не дает атомам чересчур сближаться.
Атомы могут быть заряжены положительно и отрицательно, их число всегда постоянно. На строение и состав молекул определенного вещества не влияет то, как оно было получено, то есть искусственно произведенное вещество будет точно таким же, как и натуральное.
Молекулярный состав записывается с помощью химических формул. Строение определяет, какими физическими свойствами будет обладать вещество.
Интересный факт: органические вещества, вода, углекислый газ плавятся и кипят при относительно низких температурах, сохраняют свою структуру и в твердом состоянии. Многие неорганические вещества состоят не из молекул, а атомов (кристаллы, чистые металлы и др.).
Молекулы в науке
В химии это основное понятие, молекулярное строение определяется исходя из химических реакций с веществом. Также можно, зная строение, установить, какими будут реакции. В результате химических исследований получена основная доля знаний о молекулярной функциональности и строении.
Строением в физике объясняются физические свойства жидкостей, газов и твердых тел. Подвижность молекул определяет, как быстро вещество способно проникать в другое при соприкосновении, уровень вязкости и показатель теплопроводности.
В биологии молекулярные свойства и пространственное строение имеют первостепенное значение, так как все живое функционирует благодаря тонкому балансу взаимодействия между молекулами (химического и нехимического).
На вопрос, из чего состоят молекулы, можно ответить так – из определенного числа атомов, соединенных вместе химическими связями. Из молекул состоят все вещества на планете, физические и химические свойства которых определяются строением и составом молекул.
Если Вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Загрузить PDF
Загрузить PDF
Молекулярная формула содержит важную информацию о соответствующем химическом соединении. По ней можно определить, из каких атомов состоит данное соединение, и сколько атомов каждого элемента содержится в нем. Для нахождения молекулярной формулы необходимо знать эмпирическую формулу. Чтобы получить из эмпирической формулы молекулярную, следует умножить экспериментальные значения на целочисленный множитель.
-

1
Необходимо понимать связь между молекулярной и эмпирической формулами. Эмпирическая формула показывает количественное соотношение атомов в молекуле: например, два атома кислорода на каждый атом углерода. Молекулярная формула указывает на то, сколько атомов каждого вида входит в состав молекулы: к примеру, один атом углерода и два атома кислорода (диоксид углерода, или углекислый газ). Эти две формулы однозначно соотносятся друг с другом, и если умножить эмпирическую формулу на их целочисленное отношение, то получится молекулярная формула.[1]
-

2
Вычислите количество молей газа. Используйте для этого уравнение состояния идеального газа. С его помощью можно найти количество молей вещества, если известны давление, объем и температура, которые определяются экспериментальным путем. Количество молей находится по следующей формуле: n = PV/RT.[2]
- В данной формуле n — количество молей, P — давление, V — объем, T — температура в Кельвинах, и R — универсальная газовая постоянная.
- Например: n = PV/RT = (0,984 атм * 1 л) / (0,08206 л атм моль-1 K-1 * 318,15 K) = 0,0377 моль
-

3
Определите молекулярный вес газа. Это можно сделать лишь после того, как с помощью уравнения состояния идеального газа вы найдете количество молей газа. Необходимо также знать массу газа. Для того, чтобы найти молекулярный вес газа, следует поделить его массу в граммах на количество молей.
- Например: 14,42 г / 0.0377 моль = 382,49 г/моль
-

4
Сложите атомные веса всех атомов, которые входят в эмпирическую формулу. Каждый атом в эмпирической формуле имеет свой атомный вес. Этот вес можно найти в периодической таблице Менделеева под символом соответствующего элемента. Сложите атомные веса входящих в эмпирическую формулу элементов.[3]
- Например: (12,0107 г * 12) + (15,9994 г * 1) + (1,00794 г * 30) = 144,1284 + 15,9994 + 30,2382 = 190,366 г
-

5
Найдите соотношение между весами в молекулярной и эмпирической формулах. Таким образом вы определите, сколько раз эмпирический вес повторяется в реальной молекуле. Это позволит вам найти число повторений эмпирической формулы в молекулярной. Найденная величина должна представлять собой целое число. Если получится дробное число, необходимо округлить его до целого.
- Например: 382,49 / 190,366 = 2,009
-

6
Умножьте эмпирическую формулу на найденное соотношение. Умножьте подстрочные индексы в эмпирической формуле на полученное соотношение. В результате вы найдете молекулярную формулу. Если соотношение равно “1”, то молекулярная формула совпадает с эмпирической.
- Например: C12OH30 * 2 = C24O2H60
Реклама
-

1
Найдите массу каждого атома. Иногда массы атомов даются в условии. В некоторых задачах указываются массовые проценты. В последнем случае предположите, что полная масса вещества составляет 100 граммов — это позволит вам записать массовые проценты в виде обычной массы в граммах.[4]
- Например: 75,46 г C, 8,43 г O, 16,11 г H
-

2
Переведите массу в моли. Следует перевести молекулярную массу каждого элемента в количество молей. Для этого необходимо поделить молекулярную массу каждого элемента на его атомную массу. Атомные массы можно найти в периодической таблице Менделеева под символами соответствующих элементов.[5]
- Например:
- 75,46 г C * (1 моль / 12,0107 г) = 6,28 моль C
- 8,43 г O * (1 моль / 15,9994 г) = 0,53 моль O
- 16,11 г H * (1 моль / 1,00794) = 15,98 моль H
- Например:
-

3
Поделите все молярные значения на наименьшее количество молей. Необходимо найти элемент с минимальным количеством молей и поделить на эту величину количество молей каждого элемента, входящего в данное соединение. Таким образом вы найдете простейшие мольные соотношения. В результате для самого малочисленного элемента у вас получится “1”, а для остальных элементов числа больше единицы.[6]
- Например: меньше всего в соединении кислорода, его количество составляет 0,53 моль.
- 6,28 моль/0,53 моль = 11,83
- 0,53 моль/0,53 моль = 1
- 15,98 моль/0,53 моль= 30,15
- Например: меньше всего в соединении кислорода, его количество составляет 0,53 моль.
-

4
Округлите количество молей до целых чисел. Молярные количества войдут в эмпирическую формулу в виде подстрочных индексов. Необходимо округлить их до ближайших целых чисел. После нахождения этих чисел можно записать эмпирическую формулу.[7]
- Например: эмпирическая формула имеет вид C12OH30:
- 11,83 = 12
- 1 = 1
- 30,15 = 30
Реклама
- Например: эмпирическая формула имеет вид C12OH30:
-

1
Ознакомьтесь с понятием эмпирической формулы. Эмпирическая формула содержит информацию о соотношении количества атомов в молекуле. Она не показывает, сколько именно атомов входит в состав данной молекулы. Кроме того, эмпирическая формула не позволяет судить о структуре молекулы и связях между входящими в нее атомами.[8]
-

2
Узнайте о том, какая информация содержится в молекулярной формуле. Как и эмпирическая формула, молекулярная формула не позволяет судить о структуре молекулы и связях между атомами. Однако в отличие от эмпирической формулы, молекулярная формула показывает, сколько атомов того или иного элемента входит в состав молекулы. Между эмпирической и молекулярной формулами существует целочисленное соотношение.[9]
-

3
Ознакомьтесь с понятием структурной формулы. Структурная формула содержит больше информации, чем молекулярная формула. Помимо количества атомов каждого вида, структурная формула содержит информацию о связях между атомами и структуре молекулы. Эта информация очень важна для понимания того, как молекула будет реагировать с другими веществами.[10]
Реклама
Советы
- Внимательно прочитайте условие задачи и начальные данные.
Реклама
Предупреждения
- Не путайте эмпирические и молекулярные формулы.
Реклама
Что вам понадобится
- Периодическая таблица Менделеева
- Калькулятор
- Карандаш
- Лист бумаги
Похожие статьи
Об этой статье
Эту страницу просматривали 22 404 раза.
