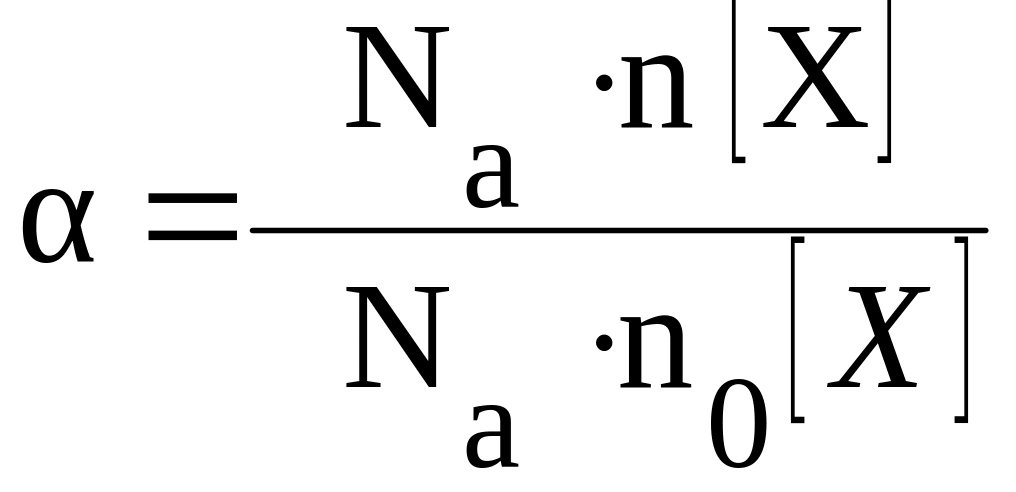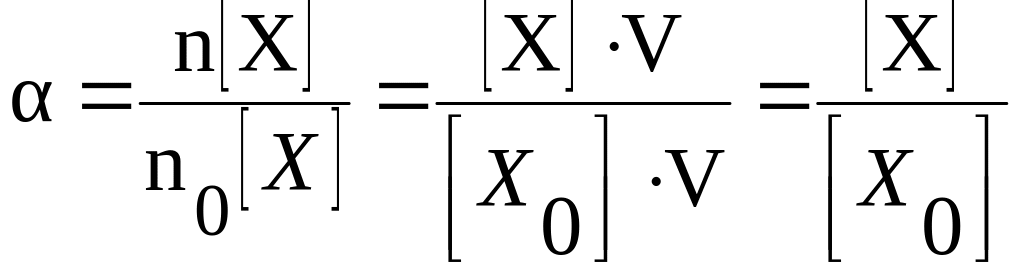Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 28 декабря 2018 года; проверки требуют 24 правки.
Степень диссоциации — величина, характеризующая состояние равновесия в реакции диссоциации в (однородных)[1] системах.
Определение[править | править код]
Степень диссоциации равна отношению продиссоциированных молекул вещества 

Степень диссоциации зависит как от природы растворённого электролита, так и от концентрации раствора.
Пример. Для уксусной кислоты CH3COOH величина 
М растворе). Это значит, что в водном растворе кислоты лишь 4 из каждых 100 молекул диссоциированы, то есть находятся в виде ионов Н+ и СН3СОО−, остальные же 96 молекул не диссоциированы. Как видно в таком примере, количества частиц, о которых идёт речь в определении степени диссоциации (они же концентрации при условии единичного объёма) – это равновесные количества (концентрации соответственно).
Экспериментальные методы[править | править код]
Степень диссоциации определяется:
- по электропроводности раствора
- по понижению температуры замерзания
Мнимая степень электрической диссоциации[править | править код]
Поскольку сильные электролиты диссоциируют практически полностью, можно было бы ожидать для них изотонический коэффициент, равный количеству ионов (или поляризованных атомов) в формульной единице (молекуле). Однако в действительности этот коэффициент всегда меньше определённого по формуле (например, изотонический коэффициент для 0,05-молярного раствора NaCl равен i = 1,9 вместо 2,0, а (для раствора сульфата магния той же концентрации вовсе i = 1,3). Это объясняет теория сильных электролитов, разработанная в 1923 году П. Дебаем и Э. Хюккелем: передвижение ионов в растворе затруднено образовавшейся оболочкой сольватации. К тому же, ионы взаимодействуют и между собой: разноимённо заряженные притягиваются, а одноимённо заряженные — отталкиваются; силы взаимного притяжения приводят к образованию групп ионов, перемещающихся по раствору совместно. Такие группы называют ионными ассоциатами или ионными па́рами. Соответственно, раствор ведёт себя так, будто содержит меньше частиц, чем на самом деле, ведь свобода их перемещения ограничена. Наиболее очевиден пример, касающийся электропроводности растворов 

,
где 

Связь с константой диссоциации[править | править код]
Из закона разбавления Оствальда следует:


Зависимость степени диссоциации 

при малых значениях 


|

|

|
|---|---|---|
| 100% | 0.61803398875 | 61.803398875% |
| 50% | 0.2807 | 39.04% |
| 40% | 0.2198 | 32.79% |
| 30% | 0.1612 | 25.84% |
| 20% | 0.1050 | 18.10% |
| 15% | 0.0778 | 13.92% |
| 10% | 0.0512 | 9.51% |
| 5% | 0.0225 | 4.88% |
| x | 0.5*x + 0.1184*x^2 | 
|
для диссоциации вида AnBm = nA + mB
![{displaystyle alpha ={sqrt[{n+m}]{Kcdot (1-alpha ) over n^{n}m^{m}C^{n+m-1}}} {overset {underset {mathrm {alpha <<1} }{}}{approx }} {sqrt[{n+m}]{K over n^{n}m^{m}C^{n+m-1}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9e2661fda430566fea8f53b201b3921272c8a483)
Поскольку диссоциация описывается постадийно, данная формула не применяется.
См. также[править | править код]
- Закон разбавления Оствальда
- Константа диссоциации
Примечания[править | править код]
- ↑ Stray Kids // Википедия. — 2023-02-28.
Литература[править | править код]
- Глинка Н. Л. Общая химия — 24-е издание, исправленное. М. 1985. с. 228.
Материалы из методички: Сборник задач по теоретическим основам химии для студентов заочно-дистанционного отделения / Барботина Н.Н., К.К. Власенко, Щербаков В.В. – М.: РХТУ им. Д.И. Менделеева, 2007. -155 с.
Степень диссоциации
Классификация электролитов
Диссоциация электролитов
Константа диссоциации
Примеры решения задач
Задачи для самостоятельного решения
Степень диссоциации
Вещества, которые в растворах или расплавах полностью или частично распадаются на ионы, называются электролитами.
Степень диссоциации α — это отношение числа молекул, распавшихся на ионы N′ к общему числу растворенных молекул N:
α = N′/N
Степень диссоциации выражают в процентах или в долях единицы. Если α =0, то диссоциация отсутствует и вещество не является электролитом. В случае если α =1, то электролит полностью распадается на ионы.
Классификация электролитов
Согласно современным представлениям теории растворов все электролиты делятся на два класса: ассоциированные (слабые) и неассоциированные (сильные). Неассоциированные электролиты в разбавленных растворах практически полностью диссоциированы на ионы. Для этого класса электролитов a близко к единице (к 100 %). Неассоциированными электролитами являются, например, HCl, NaOH, K2SO4 в разбавленных водных растворах.
Ассоциированные электролиты подразделяются на три типа:
-
-
- Слабые электролиты существуют в растворах как в виде ионов, так и в виде недиссоциированных молекул. Примерами ассоциированных электролитов этой группы являются, в частности, Н2S, Н2SO3, СН3СOОН в водных растворах.
- Ионные ассоциатыобразуются в растворах путем ассоциации простых ионов за счет электростатического взаимодействия. Ионные ассоциаты возникают в концентрированных растворах хорошо растворимых электролитов. В результате в растворе находятся как простые ионы, так и ионные ассоциаты. Например, в концентрированном водном растворе КCl образуются простые ионы К+, Cl— , а также возможно образование ионных пар (К+Cl— ), ионных тройников (K2Cl+, KCl2— ) и ионных квадруполей (K2Cl2, KCl32- , K3Cl2+).
- Комплексные соединения(как ионные, так и молекулярные), внутренняя сфера которых ступенчато диссоциирует на ионные и (или) молекулярные частицы.
Примеры комплексных ионов: [Cu(NH3)4]2+, [Fe(CN)6]3+, [Cr(H2O)3Cl2]+.
-
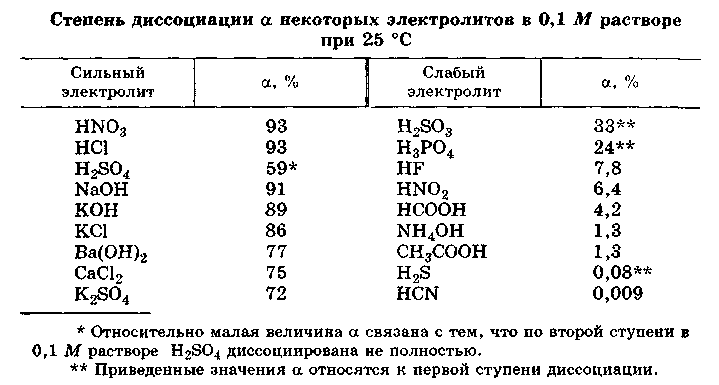
При таком подходе один и тот же электролит может относиться к различным типам в зависимости от концентрации раствора, вида растворителя и температуры. Подтверждением этому являются данные, приведенные в таблице.
Таблица. Характеристика растворов KI в различных растворителях
| Концентрация электролита, С, моль/л | Температура
t,оС |
Растворитель | Тип электролита |
| 0,01 | 25 | Н2О | Неассоциированный (сильный) |
| 5 | 25 | Н2О | Ионный ассоциат |
| 0,001 | 25 | С6Н6 | Ассоциированный (слабый) |
Приближенно, для качественных рассуждений можно пользоваться устаревшим делением электролитов на сильные и слабые. Выделение группы электролитов “средней силы” не имеет смысла. Эти электролиты являются ассоциированными. К слабым электролитам обычно относят электролиты, степень диссоцииации которых мала α<<1.
Таким образом, к сильным электролитам относятся разбавленные водные растворы почти всех хорошо растворимых в воде солей, многие разбавленные водные растворы минеральных кислот (НСl, HBr, НNО3, НСlO4 и др.), разбавленные водные растворы гидроксидов щелочных металлов. К слабым электролитам принадлежат все органические кислоты в водных растворах, некоторые водные растворы неорганических кислот, например, H2S, HCN, H2CO3, HNO2, HСlO и др. К слабым электролитам относится и вода.
Диссоциация электролитов
Уравнение реакции диссоциации сильного электролита можно представить следующим образом. Между правой и левой частями уравнения реакции диссоциации сильного электролита ставится стрелка или знак равенства:
HCl → H+ + Cl—
Na2SO3 = 2Na+ + SO32-
Допускается также ставить знак обратимости, однако в этом случае указывается направление, в котором смещается равновесие диссоциации, или указывается, что α≈1. Например:
NaOH → Na+ + OH—
Диссоциация кислых и основных солей в разбавленных водных растворах протекает следующим образом:
NaHSO3 → Na+ + HSO3—
Анион кислой соли будет диссоциировать в незначительной степени, поскольку является ассоциированным электролитом:
HSO3— → H+ + SO32-
Аналогичным образом происходит диссоциация основных солей:
Mg(OH)Cl → MgOH+ + Cl—
Катион основной соли подвергается дальнейшей диссоциации как слабый электролит:
MgOH+ → Mg2+ + OH—
Двойные соли в разбавленных водных растворах рассматриваются как неассоциированные электролиты:
KAl(SO4)2 → K+ + Al3+ + 2SO42-
Комплексные соединения в разбавленных водных растворах практически полностью диссоциируют на внешнюю и внутреннюю сферы:
K3[Fe(CN)6] → 3K+ + [Fe(CN)6]3-
В свою очередь, комплексный ион в незначительной степени подвергается дальнейшей диссоциации:
[Fe(CN)6]3- → Fe3+ + 6CN—
Константа диссоциации
При растворении слабого электролита КА в растворе установится равновесие:
КА ↔ К+ + А—
которое количественно описывается величиной константы равновесия Кд, называемой константой диссоциации:
Kд = [К+] · [А—] /[КА] (2)
Константа диссоциации характеризует способность электролита диссоциировать на ионы. Чем больше константа диссоциации, тем больше ионов в растворе слабого электролита. Например, в растворе азотистой кислоты HNO2 ионов Н+ больше, чем в растворе синильной кислоты HCN, поскольку К(HNO2) = 4,6·10— 4, а К(HCN) = 4,9·10— 10.
Для слабых I-I электролитов (HCN, HNO2, CH3COOH) величина константы диссоциации Кд связана со степенью диссоциации α и концентрацией электролита c уравнением Оствальда:
Кд = (α2·с)/(1-α) (3)
Для практических расчетов при условии, что α<<1 используется приближенное уравнение:
Кд = α2·с (4)
Поскольку процесс диссоциации слабого электролита обратим, то к нему применим принцип Ле Шателье. В частности, добавление CH3COONa к водному раствору CH3COOH вызовет подавление собственной диссоциации уксусной кислоты и уменьшение концентрации протонов. Таким образом, добавление в раствор ассоциированного электролита веществ, содержащих одноименные ионы, уменьшает его степень диссоциации.
Следует отметить, что константа диссоциации слабого электролита связана с изменением энергии Гиббса в процессе диссоциации этого электролита соотношением:
ΔGT0 = — RTlnKд (5)
Уравнение (5) используется для расчета констант диссоциации слабых электролитов по термодинамическим данным.
Примеры решения задач
Задача 1. Определите концентрацию ионов калия и фосфат-ионов в 0,025 М растворе K3PO4.
Решение. K3PO4 – сильный электролит и в водном растворе диссоциирует полностью:
K3PO4 → 3К+ + РО43-
Следовательно, концентрации ионов К+ и РО43- равны соответственно 0,075М и 0,025М.
Задача 2. Определите степень диссоциации αд и концентрацию ионов ОН— (моль/л) в 0,03 М растворе NH3·H2О при 298 К, если при указанной температуре Кд(NH3·H2О) = 1,76× 10— 5.
Решение. Уравнение диссоциации электролита:
NH3·H2О → NH4+ + OH—
Концентрации ионов: [NH4+] = αС ; [OH—] = αС , где С – исходная концентрация NH3·H2О моль/л. Следовательно:
Kд = αС · αС /(1 — αС)
Поскольку α << 1, то:
Кд ≈ α 2С
Константа диссоциации зависит от температуры и от природы растворителя, но не зависит от концентрации растворов NH3·H2О. Закон разбавления Оствальда выражает зависимость α слабого электролита от концентрации.
α = √(Кд / С) = √(1,76× 10— 5 / 0,03) = 0,024 или 2,4 %
[OH—] = αС, откуда [OH— ] = 2,4·10— 2·0,03 = 7,2·10-4 моль/л.
Задача 3. Определите константу диссоциации уксусной кислоты, если степень диссоциации CH3CОOH в 0,002 М растворе равна 9,4 %.
Решение. Уравнение диссоциации кислоты:
CH3CОOH → СН3СОО— + Н+.
α = [Н+] / Сисх(CH3CОOH)
откуда [Н+] = 9,4·10—2·0,002 = 1,88·10-4 М.
Так как [CH3CОO—] = [Н+] и [CH3CОOH] ≈ Сисх(CH3CОOH), то:
Kд = [Н+]2 / Сисх(CH3CОOH)
Константу диссоциации можно также найти по формуле: Кд ≈ α 2С.
Задача 4. Константа диссоциации HNO2 при 298К равна 4,6× 10— 4. Найдите концентрацию азотистой кислоты, при которой степень диссоциации HNO2 равна 5 %.
Решение.
Кд =α 2С , откуда получаем Сисх(HNO2) = 4,6·10— 4/(5·10— 2)2 = 0,184 М.
Задача 5. На основе справочных данных рассчитайте константу диссоциации муравьиной кислоты при 298 К.
Решение. Уравнение диссоциации муравьиной кислоты
НСООН →Н+ + СООН—
В “Кратком справочнике физико–химических величин” под редакцией А.А. Равделя и А.М. Пономаревой приведены значения энергий Гиббса образований ионов в растворе, а также гипотетически недиссоциированных молекул. Значения энергий Гиббса для муравьиной кислоты и ионов Н+ и СООН— в водном растворе приведены ниже:
| Вещество, ион | НСООН | Н+ | СООН— |
| ΔGT0, кДж/моль | — 373,0 | 0 | — 351,5 |
Изменение энергии Гиббса процесса диссоциации равно:
ΔGT0 = — 351,5- (- 373,0) = 21,5 кДж/моль.
Для расчета константы диссоциации используем уравнение (5). Из этого уравнения получаем:
lnKд = — Δ GT0/RT= — 21500/(8,31 298) = — 8,68
Откуда находим: Kд = 1,7× 10— 4.
Задачи для самостоятельного решения
1. К сильным электролитам в разбавленных водных растворах относятся:
- СН3СOOH
- Na3PO4
- NaCN
- NH3
- C2H5OH
- HNO2
- HNO3
13.2. К слабым электролитам в водных растворах относятся:
- KAl(SO4)2
- NaNO3
- HCN
- NH4Cl
- C2H5OH
- H2SO3
- H2SO4
3. Определите концентрацию ионов NH4+ в 0,03 М растворе (NH4)2Fe(SO4)2;
4. Определите концентрацию ионов водорода в 6 мас.% растворе H2SO4, плотность которого составляет 1,038 г/мл. Принять степень диссоциации кислоты по первой и второй ступеням равной 100 %.
5. Определите концентрацию гидроксид-ионов в 0,15 М растворе Ba(OH)2.
6. Степень диссоциации муравьиной кислоты в 0,1 М растворе равна 4 %. Рассчитайте Концентрацию ионов водорода в этом растворе и константу диссоциации НСООН.
7. Степень диссоциации муравьиной кислоты в водном растворе увеличится при:
а) уменьшении концентрации HCOOH;
б) увеличении концентрации HCOOH;
в) добавлении в раствор муравьиной кислоты HCOONa;
г) добавлении в раствор муравьиной кислоты НCl.
8. Константа диссоциации хлорноватистой кислоты равна 5× 10— 8. Определите концентрацию HClO, при которой степень диссоциации HClO равна 0,5 %, и концентрацию ионов Н+ в этом растворе.
9. Вычислите объем воды, который необходимо добавить к 50 мл 0,02 М раствора NH3·H2О, чтобы степень диссоциации NH3·H2О увеличилась в 10 раз, если Кд(NH4OH) = 1,76·10— 5.
10. Определите степень диссоциации азотистой кислоты в 0,25 М растворе при 298 К, если при указанной температуре Кд(HNO2) = 4,6× 10— 4.
Изучая
свойства растворов электролитов, С.
Аррениус ввёл понятие «степень
диссоциации», предположив, что некоторые
электролиты не могут полностью
диссоциировать на ионы.
Степенью
диссоциации называется отношение
числа молекул, распавшихся в растворе
на ионы, к общему числу молекул электролита
в растворе.
|
|
(1) |
где:
N(X)
– число продиссоциировавших молекул
электролита X;
N0(X)
– общее число молекул электролита X
в растворе.
Степень
диссоциации ()
зависит от следующих факторов:
– от
природы электролита и растворителя;
– концентрации
электролита;
– температуры.
Степень
диссоциации можно также выразить через
количество вещества по формуле:
|
|
(2) |
где
n(X)
– количество молей продиссоциировавшего
вещества X;
n0б(X)
– общее количество молей вещества X
в растворе;
Na
–
число Авогадро.
Количество вещества
можно выразить через молярную концентрацию
раствора и объём раствора, поэтому
степень диссоциации можно также
определить как отношение молярной
концентрации продиссоциировавшего
вещества к молярной концентрации всего
вещества, находящегося в растворе.
|
|
( |
где
[Х] – молярная концентрация
продиссоциировавшего вещества X;
[Х0]
– общая молярная концентрация вещества
X
в растворе.
Электролиты
можно разделить на 2 большие группы:
электролиты сильные и слабые.
Сильные
электролиты
диссоциируют в растворах полностью и
процесс диссоциации необратим:
HNO3
H+
+ NO3–
. Из этого следует, что степень
диссоциации сильного электролита равна
1.
Сильными
электролитами являются:
–все
растворимые соли;
– гидроксиды
щелочных и щелочно-земельных металлов
(NaOH,
KOH,
Ba(OH)2;
– некоторые
кислоты (H2SO4,
HNO3,
HCl,
HBr,
HI.
Для
слабых электролитов степень диссоциации
α < 1,
поскольку слабые электролиты диссоциируют
лишь частично, и
процесс диссоциации обратим, т.е.
в растворе устанавливается динамическое
равновесие между ионами и
непродиссоциировавшими молекулами.
Основные
слабые электролиты:
– вода
H2O;
– гидроксиды
Al(OH)3;
Обратимый
характер диссоциации слабых электролитов
отражается при записи уравнений.
CH3COOH
⇆
CH3COO–
+ H+
H3PO4
⇆
H+
+ H2PO4–
H2PO4–
⇆
H+
+ HPO42–
HPO42–
⇆
H+
+ PO43–
4 Константа диссоциации
К
равновесию, которое устанавливается в
растворе слабого электролита между
молекулами и ионами, можно применить
законы химического равновесия и записать
выражение константы равновесия.
Ниже
приводится выражение константы равновесия
для процесса диссоциации уксусной
кислоты CH3COOH
⇆
CH3COO–
+ H+.
К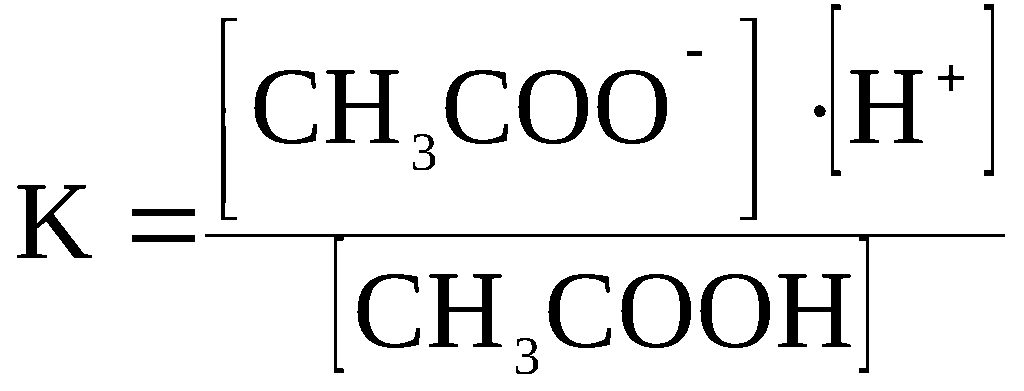
онстанта
равновесия, соответствующая процессу
диссоциации слабого электролита,
называется
константой
диссоциации.
Величина
константы диссоциации зависит от природы
электролита и растворителя, температуры,
но не зависит от концентрации электролита
в растворе.
Она
характеризует способность данной
кислоты или данного основания распадаться
на ионы: чем легче электролит диссоциирует
на ионы, тем больше константа диссоциации.
Константа
диссоциации является справочной
величиной.
Ступенчатая
диссоциация электролитов. Многоосновные
кислоты и многокислотные основания
диссоциируют ступенчато.
Каждая
стадия ступенчатой диссоциации
многоосновной кислоты характеризуется
своей константой диссоциации.
H3PO4
⇆
H+
+ H2PO4–
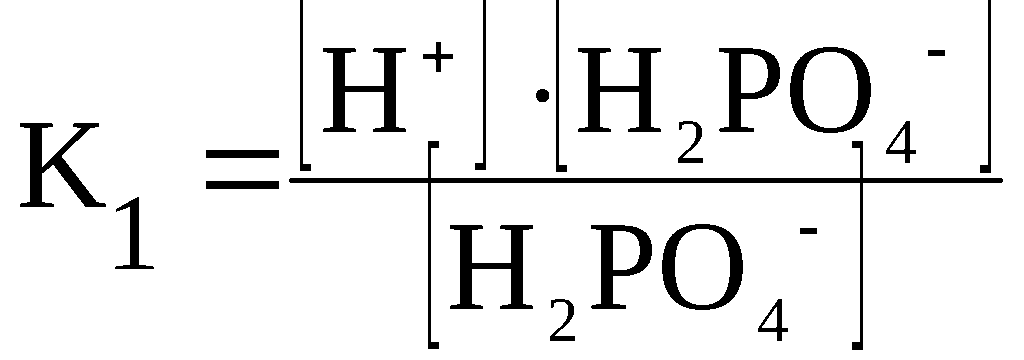
H2PO4–
⇆
H+
+ HPO42–
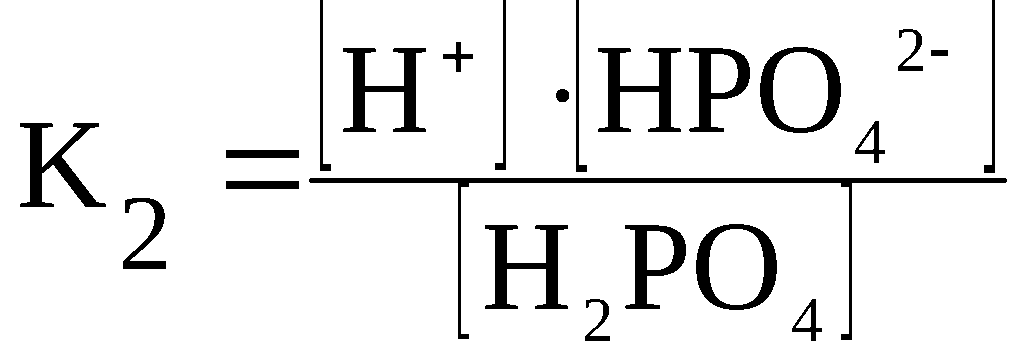
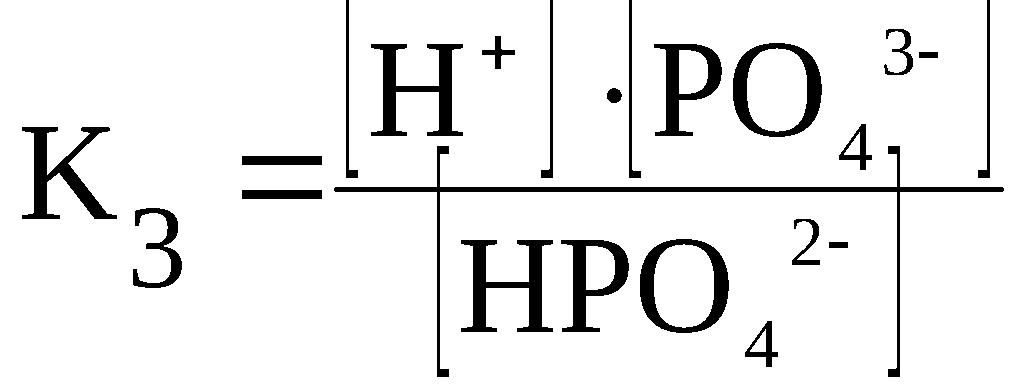
HPO42–
⇆
H+
+ PO43–
Аналогичные
соотношения характеризуют и ступенчатую
диссоциацию оснований многовалентных
металлов.
Fe(OH)2
⇆
FeOH+
+ OH–
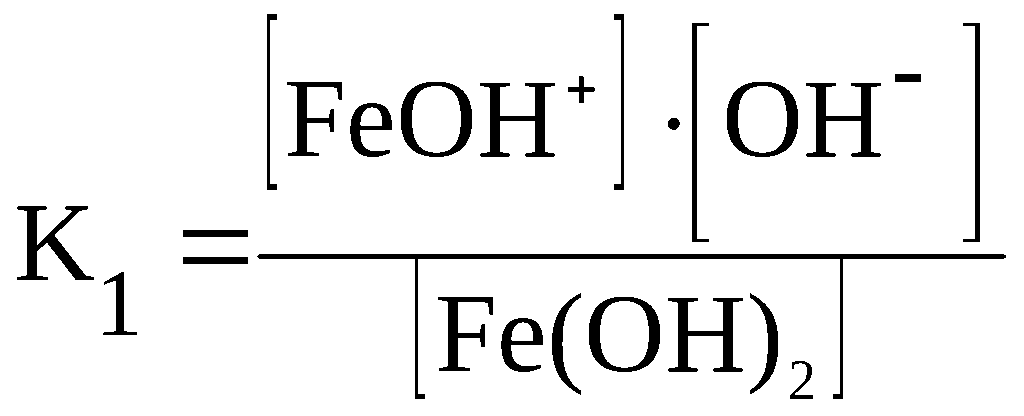
F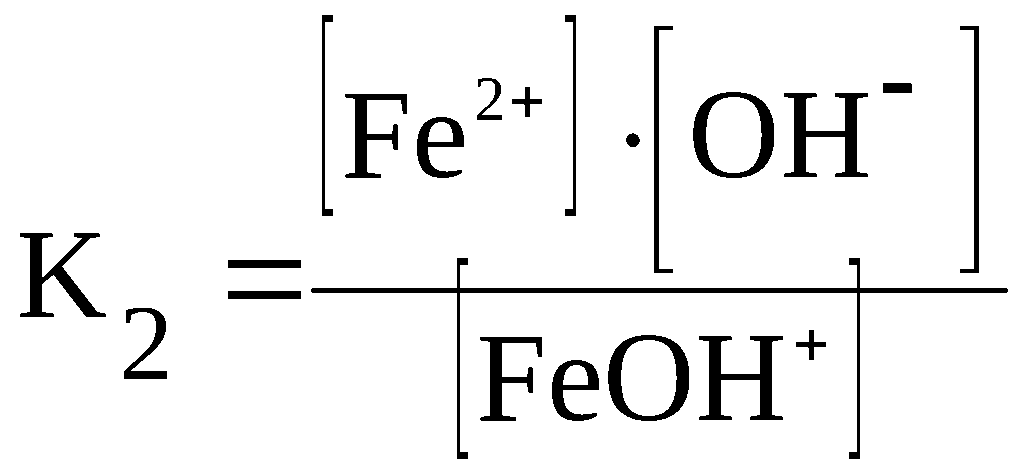
eOH+
⇆
Fe2+
+ OH–
При
ступенчатой диссоциации веществ распад
по первой ступени всегда происходит в
гораздо большей степени, чем по второй;
по второй стадии – больше, чем по третьей
и т.д. Иначе говоря, соблюдается
неравенство:
K1
>> K2
> K3
> … .
Это
объясняется тем, что энергия, необходимая
для отрыва иона от нейтральной молекулы,
меньше, чем от заряженной частицы.
Например, отрыв иона H+
будет происходить более легко от
нейтральной частицы – молекулы H3PO4,
чем от отрицательно заряженного иона
H2PO4–.
В свою очередь, отрыв иона H+
от однозарядного иона H2PO4–
требует меньшей энергии, чем от
двухзарядного иона HPO4–.
Кислые
и основные соли также диссоциируют
ступенчато, например:
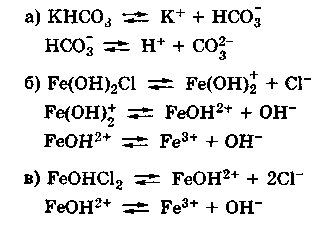
Нетрудно заметить,
что диссоциация гидроаниона или
гидроксокатиона идентична второй или
третьей ступени диссоциации соответствующих
кислоты или основания и потому подчиняется
тем же закономерностям, которые были
сформулированы для ступенчатой
диссоциации кислот и оснований. В
частности, если основная соль
соответствует слабому основанию, а
кислая соль – слабой кислоте, то диссоциация
гидроаниона или гидроксокатиона (т. е.
вторая или третья ступень диссоциации
соли) протекает в незначительной степени.
Во всякой
кислородсодержащей кислоте и во всяком
основании (имеются в виду кислоты и
основания в традиционном понимании)
имеются гидроксогруппы. Разница между
кислотой и основанием заключается в
том, что в первом случае диссоциация
происходит по связи ЭО—Н, а во втором
— по связи Э—ОН.
Амфотерные
гидроксиды диссоциируют и как основания,
и как кислоты (и те и другие очень слабые).
Так, ионизацию гидроксида цинка можно
представить следующей схемой (без учета
гидратации образующихся ионов):
![]()
Прибавление кислоты
смещает эти равновесия влево, а
прибавление щелочи – вправо. Поэтому
в кислой среде преобладает диссоциация
по типу основания, а в щелочной — по
типу кислоты. В обоих случаях связывание
в молекулы воды ионов, образующихся
при диссоциации малорастворимого
амфотерного электролита, вызывает
переход в раствор новых порций таких
ионов, их связывание, переход в раствор
новых ионов и т. д. Следовательно,
растворение такого электролита происходит
как в растворе кислоты, так и в растворе
щелочи.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Электролитическая диссоциация
Материалы портала onx.distant.ru
Примеры решения задач
Задачи для самостоятельного решения
Степень диссоциации
Вещества, которые в растворах или расплавах полностью или частично распадаются на ионы, называются электролитами.
Степень диссоциации α — это отношение числа молекул, распавшихся на ионы N′ к общему числу растворенных молекул N:
α = N′/N
Степень диссоциации выражают в процентах или в долях единицы. Если α =0, то диссоциация отсутствует и вещество не является электролитом. В случае если α =1, то электролит полностью распадается на ионы.
Классификация электролитов
Согласно современным представлениям теории растворов все электролиты делятся на два класса: ассоциированные (слабые) и неассоциированные (сильные) . Неассоциированные электролиты в разбавленных растворах практически полностью диссоциированы на ионы. Для этого класса электролитов a близко к единице (к 100 %). Неассоциированными электролитами являются, например, HCl, NaOH, K2SO4 в разбавленных водных растворах.
Ассоциированные электролиты подразделяются на три типа:
-
-
- Слабые электролиты существуют в растворах как в виде ионов, так и в виде недиссоциированных молекул. Примерами ассоциированных электролитов этой группы являются, в частности, Н2S, Н2SO3, СН3СOОН в водных растворах.
- Ионные ассоциаты образуются в растворах путем ассоциации простых ионов за счет электростатического взаимодействия. Ионные ассоциаты возникают в концентрированных растворах хорошо растворимых электролитов. В результате в растворе находятся как простые ионы, так и ионные ассоциаты. Например, в концентрированном водном растворе КCl образуются простые ионы К + , Cl — , а также возможно образование ионных пар (К + Cl — ), ионных тройников (K2Cl + , KCl2 — ) и ионных квадруполей (K2Cl2, KCl3 2- , K3Cl 2+ ).
- Комплексные соединения (как ионные, так и молекулярные), внутренняя сфера которых ступенчато диссоциирует на ионные и (или) молекулярные частицы.
Примеры комплексных ионов: [Cu(NH3)4] 2+ , [Fe(CN)6] 3+ , [Cr(H2O)3Cl2] + .
-
При таком подходе один и тот же электролит может относиться к различным типам в зависимости от концентрации раствора, вида растворителя и температуры. Подтверждением этому являются данные, приведенные в таблице.
Таблица. Характеристика растворов KI в различных растворителях
| Концентрация электролита, С, моль/л | Температура
t, о С |
Растворитель | Тип электролита |
| 0,01 | 25 | Н2О | Неассоциированный (сильный) |
| 5 | 25 | Н2О | Ионный ассоциат |
| 0,001 | 25 | С6Н6 | Ассоциированный (слабый) |
Приближенно, для качественных рассуждений можно пользоваться устаревшим делением электролитов на сильные и слабые. Выделение группы электролитов “средней силы” не имеет смысла. Эти электролиты являются ассоциированными. К слабым электролитам обычно относят электролиты, степень диссоцииации которых мала α
Таким образом, к сильным электролитам относятся разбавленные водные растворы почти всех хорошо растворимых в воде солей, многие разбавленные водные растворы минеральных кислот (НСl, HBr, НNО3, НСlO4 и др.), разбавленные водные растворы гидроксидов щелочных металлов. К слабым электролитам принадлежат все органические кислоты в водных растворах, некоторые водные растворы неорганических кислот, например, H2S, HCN, H2CO3, HNO2, HСlO и др. К слабым электролитам относится и вода.
Диссоциация электролитов
Уравнение реакции диссоциации сильного электролита можно представить следующим образом. Между правой и левой частями уравнения реакции диссоциации сильного электролита ставится стрелка или знак равенства:
HCl → H + + Cl —
Допускается также ставить знак обратимости, однако в этом случае указывается направление, в котором смещается равновесие диссоциации, или указывается, что α≈1. Например:
NaOH → Na + + OH —
Диссоциация кислых и основных солей в разбавленных водных растворах протекает следующим образом:
NaHSO3 → Na + + HSO3 —
Анион кислой соли будет диссоциировать в незначительной степени, поскольку является ассоциированным электролитом:
HSO3 — → H + + SO3 2-
Аналогичным образом происходит диссоциация основных солей:
Mg(OH)Cl → MgOH + + Cl —
Катион основной соли подвергается дальнейшей диссоциации как слабый электролит:
MgOH + → Mg 2+ + OH —
Двойные соли в разбавленных водных растворах рассматриваются как неассоциированные электролиты:
Комплексные соединения в разбавленных водных растворах практически полностью диссоциируют на внешнюю и внутреннюю сферы:
В свою очередь, комплексный ион в незначительной степени подвергается дальнейшей диссоциации:
[Fe(CN)6] 3- → Fe 3+ + 6CN —
Константа диссоциации
При растворении слабого электролита К А в растворе установится равновесие:
КА ↔ К + + А —
которое количественно описывается величиной константы равновесия Кд, называемой константой диссоциации :
Kд = [К + ] · [А — ] /[КА] (2)
Константа диссоциации характеризует способность электролита диссоциировать на ионы. Чем больше константа диссоциации, тем больше ионов в растворе слабого электролита. Например, в растворе азотистой кислоты HNO2 ионов Н + больше, чем в растворе синильной кислоты HCN, поскольку К(HNO2) = 4,6·10 — 4 , а К(HCN) = 4,9·10 — 10 .
Для слабых I-I электролитов (HCN, HNO2, CH3COOH) величина константы диссоциации Кд связана со степенью диссоциации α и концентрацией электролита c уравнением Оствальда:
Кд = (α 2· с)/(1-α) (3)
Для практических расчетов при условии, что α
Кд = α 2· с (4)
Поскольку процесс диссоциации слабого электролита обратим, то к нему применим принцип Ле Шателье. В частности, добавление CH3COONa к водному раствору CH3COOH вызовет подавление собственной диссоциации уксусной кислоты и уменьшение концентрации протонов. Таким образом, добавление в раствор ассоциированного электролита веществ, содержащих одноименные ионы, уменьшает его степень диссоциации.
Следует отметить, что константа диссоциации слабого электролита связана с изменением энергии Гиббса в процессе диссоциации этого электролита соотношением:
ΔGT 0 = — RTlnKд (5)
Уравнение (5) используется для расчета констант диссоциации слабых электролитов по термодинамическим данным.
Примеры решения задач
Задача 1. Определите концентрацию ионов калия и фосфат-ионов в 0,025 М растворе K3PO4.
Решение. K3PO4 – сильный электролит и в водном растворе диссоциирует полностью:
Следовательно, концентрации ионов К + и РО4 3- равны соответственно 0,075М и 0,025М.
Задача 2. Определите степень диссоциации αд и концентрацию ионов ОН — (моль/л) в 0,03 М растворе NH3·H2О при 298 К, если при указанной температуре Кд(NH3·H2О) = 1,76× 10 — 5 .
Решение. Уравнение диссоциации электролита:
Концентрации ионов: [NH4 + ] = α С ; [OH — ] = α С , где С – исходная концентрация NH 3 ·H 2 О моль/л. Следовательно:
Kд = αС · αС /(1 — αС)
Кд ≈ α 2 С
Константа диссоциации зависит от температуры и от природы растворителя, но не зависит от концентрации растворов NH 3 ·H 2 О . Закон разбавления Оствальда выражает зависимость α слабого электролита от концентрации.
α = √( Кд / С) = √(1,76× 10 — 5 / 0,03 ) = 0,024 или 2,4 %
[OH — ] = αС, откуда [OH — ] = 2,4·10 — 2 ·0,03 = 7,2·10 -4 моль/л.
Задача 3. Определите константу диссоциации уксусной кислоты, если степень диссоциации CH3CОOH в 0,002 М растворе равна 9,4 %.
Решение. Уравнение диссоциации кислоты:
CH3CОOH → СН3СОО — + Н + .
α = [Н + ] / Сисх(CH3CОOH)
откуда [Н + ] = 9,4·10 — 2 ·0,002 = 1,88·10 -4 М.
Kд = [Н + ] 2 / Сисх(CH3CОOH)
Константу диссоциации можно также найти по формуле: Кд ≈ α 2 С .
Задача 4. Константа диссоциации HNO2 при 298К равна 4,6× 10 — 4 . Найдите концентрацию азотистой кислоты, при которой степень диссоциации HNO2 равна 5 %.
Решение.
Кд = α 2 С , откуда получаем С исх (HNO 2 ) = 4,6·10 — 4 /(5·10 — 2 ) 2 = 0,184 М.
Задача 5. На основе справочных данных рассчитайте константу диссоциации муравьиной кислоты при 298 К.
Решение. Уравнение диссоциации муравьиной кислоты
В “Кратком справочнике физико–химических величин” под редакцией А.А. Равделя и А.М. Пономаревой приведены значения энергий Гиббса образований ионов в растворе, а также гипотетически недиссоциированных молекул. Значения энергий Гиббса для муравьиной кислоты и ионов Н + и СООН — в водном растворе приведены ниже:
| Вещество, ион | НСООН | Н + | СООН — |
| ΔGT 0 , кДж/моль | — 373,0 | 0 | — 351,5 |
Изменение энергии Гиббса процесса диссоциации равно:
ΔGT 0 = — 351,5- (- 373,0) = 21,5 кДж/моль.
Для расчета константы диссоциации используем уравнение (5). Из этого уравнения получаем:
lnKд = — Δ GT 0 /RT= — 21500/(8,31 298) = — 8,68
Откуда находим: Kд = 1,7× 10 — 4 .
Задачи для самостоятельного решения
1. К сильным электролитам в разбавленных водных растворах относятся:
- СН3СOOH
- Na3PO4
- NaCN
- NH3
- C2H5OH
- HNO2
- HNO3
13.2. К слабым электролитам в водных растворах относятся:
3. Определите концентрацию ионов NH4 + в 0,03 М растворе (NH4)2Fe(SO4)2;
4. Определите концентрацию ионов водорода в 6 мас.% растворе H2SO4, плотность которого составляет 1,038 г/мл. Принять степень диссоциации кислоты по первой и второй ступеням равной 100 %.
5. Определите концентрацию гидроксид-ионов в 0,15 М растворе Ba(OH)2.
6. Степень диссоциации муравьиной кислоты в 0,1 М растворе равна 4 %. Рассчитайте Концентрацию ионов водорода в этом растворе и константу диссоциации НСООН.
7. Степень диссоциации муравьиной кислоты в водном растворе увеличится при:
а) уменьшении концентрации HCOOH;
б) увеличении концентрации HCOOH;
в) добавлении в раствор муравьиной кислоты HCOONa;
г) добавлении в раствор муравьиной кислоты НCl.
8. Константа диссоциации хлорноватистой кислоты равна 5× 10 — 8 . Определите концентрацию HClO, при которой степень диссоциации HClO равна 0,5 %, и концентрацию ионов Н + в этом растворе.
0,002М; 1× 10 — 5 М.
9. Вычислите объем воды, который необходимо добавить к 50 мл 0,02 М раствора NH 3·H 2О, чтобы степень диссоциации NH 3·H 2О увеличилась в 10 раз, если Кд(NH4OH) = 1,76·10 — 5 .
10. Определите степень диссоциации азотистой кислоты в 0,25 М растворе при 298 К, если при указанной температуре Кд(HNO2) = 4,6× 10 — 4 .
Электролитическая диссоциация
Электролитической диссоциацией называют процесс, в ходе которого молекулы растворенного вещества распадаются на ионы в результате взаимодействия с растворителем (воды). Диссоциация является обратимым процессом.
Диссоциация обуславливает ионную проводимость растворов электролитов. Чем больше молекул вещества распадается на ионы, тем лучше оно проводит электрический ток и является более сильным электролитом.
В общем виде процесс электролитической диссоциации можно представить так:
KA ⇄ K + (катион) + A – (анион)

Замечу, что сила кислоты определяется способностью отщеплять протон. Чем легче кислота его отщепляет, тем она сильнее.
У HF крайне затруднен процесс диссоциации из-за образования водородных связей между F (самым электроотрицательным элементом) одной молекулы и H другой молекулы.
Ступени диссоциации
Некоторые вещества диссоциируют на ионы не в одну стадию (как NaCl), а ступенчато. Это характерно для многоосновных кислот: H2SO4, H3PO4.
Посмотрите на ступенчатую диссоциацию ортофосфорной кислоты:

Важно заметить, что концентрация ионов на разных ступенях разная. На первых ступенях ионов всегда много, а до последних доходят не все молекулы. Поэтому в растворе ортофосфорной кислоты концентрация дигидрофосфат-анионов будет больше, чем фосфат-анионов.
Для серной кислоты диссоциация будет выглядеть так:

Для средних солей диссоциация чаще всего происходит в одну ступень:
Из одной молекулы ортофосфата натрия образовалось 4 иона.
Из одной молекулы сульфата калия образовалось 3 иона.
Электролиты и неэлектролиты
Химические вещества отличаются друг от друга по способности проводить электрический ток. Исходя из этой способности, вещества делятся на электролиты и неэлектролиты.

Электролиты – жидкие или твердые вещества, в которых присутствуют ионы, способные перемещаться и проводить электрический ток. Связи в их молекулах обычно ионные или ковалентные сильнополярные.
К ним относятся соли, сильные кислоты и щелочи (растворимые основания).
Степень диссоциации сильных электролитов составляет от 0,3 до 1, что означает 30-100% распад молекул, попавших в раствор, на ионы.

Неэлектролиты – вещества недиссоциирующие в растворах на ионы. В молекулах эти веществ связи ковалентные неполярные или слабополярные.
К неэлектролитам относятся многие органические вещества, слабые кислоты, нерастворимые в воде основания и гидроксид аммония.
Степень их диссоциации до 0 до 0.3, то есть в растворе неэлектролита на ионы распадается до 30% молекул. Они плохо или вообще не проводят электрический ток.

Молекулярное, полное и сокращенное ионные уравнения
Молекулярное уравнение представляет собой запись реакции с использованием молекул. Это те уравнения, к которым мы привыкли и которыми наиболее часто пользуемся. Примеры молекулярных уравнений:

Полные ионные уравнения записываются путем разложения молекул на ионы. Запомните, что нельзя раскладывать на ионы:
- Слабые электролиты (в их числе вода)
- Осадки
- Газы

Сокращенное ионное уравнение записывается путем сокращения одинаковых ионов из левой и правой части. Просто, как в математике – остается только то, что сократить нельзя.

© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Электролитическая диссоциация
Электролитическая диссоциация. Степень и константа диссоциации
По способности проводить электрический ток в водном растворе или в расплаве, вещества делятся на электролиты и неэлектролиты.
Электролитами называются вещества, растворы или расплавы которых проводят электрический ток. К электролитам относятся соли, кислоты, основания. В молекулах этих веществ имеются ионные или ковалентные сильно полярные химические связи.
Неэлектролитами называются вещества, растворы или расплавы которых не проводят электрический ток. К неэлектролитам относятся, например, кислород, водород, многие органические вещества (сахар, эфир, бензол и др.). В молекулах этих веществ существуют ковалентные неполярные или малополярные связи.
Для объяснения электропроводности растворов и расплавов солей, кислот и оснований шведский ученый С. Аррениус создал теорию электролитической диссоциации (1887 г.):
1.Молекулы электролитов при растворении или расплавлении распадаются на ионы.
Процесс распада молекул электролитов на ионы в растворе или в расплаве называется электролитической диссоциацией, или ионизацией.
Ионы — это атомы или группы атомов, имеющие положительный или отрицательный заряд.
2.В растворе или расплаве электролитов ионы движутся хаотически. При пропускании через раствор или расплав электрического тока, положительно заряженные ионы движутся к отрицательно заряженному электроду (катоду), а отрицательно заряженные ионы движутся к положительно заряженному электроду (аноду). Поэтому положительные ионы называются катионами, отрицательные ионы — анионами.
К катионам относятся: ион водорода Н + , ион аммония NH4 + , ионы металлов Na + , K + , Fe 2+ , Al 3+ , катионы основных солей CuOH + , Аl(ОН)2 + , FeOH 2+ и т. д.
К анионам относятся: гидроксид-ион ОН — , ионы кислотных остатков Сl — , NO3 — , SO4 2- , Cr2O7 2- , анионы кислых солей НСО3 — , Н2РО4 — , HPO4 2- и т. д.
3.Диссоциация — процесс обратимый. Это значит, что одновременно идут два противоположных процесса: распад молекул на ионы (ионизация, или диссоциация) и соединение ионов в молекулы (ассоциация, или моляризация).
Диссоциацию молекул электролитов выражают уравнениями, в которых вместо знака равенства ставят знак обратимости. В левой части уравнения записывают формулу молекулы электролита, в правой — формулы ионов, которые образуются в процессе электролитической диссоциации. Например:
Каждая молекула нитрата магния диссоциирует на ион магния и два нитрат-иона. Следовательно, в результате диссоциации одной молекулы Mg(NO3)2 образуются три иона.
Общая сумма зарядов катионов равна общей сумме зарядов анионов и противоположна по знаку (так как растворы электролитов электронейтральны).
Механизм электролитической диссоциации. Гидратация ионов
Причины и механизм диссоциации электролитов объясняются химической теорией раствора Д. И. Менделеева и природой химической связи. Как известно, электролитами являются вещества с ионной или ковалентной сильно полярной связями. Растворители, в которых происходит диссоциация, состоят из полярных молекул. Например, вода — полярный растворитель. Диссоциация электролитов с ионной и полярной связями протекает различно. Рассмотрим механизм диссоциации электролитов в водных растворах.
I. Механизм диссоциации электролитов с ионной связью
При растворении в воде ионных соединений, например хлорида натрия NaCl, дипольные молекулы воды ориентируются вокруг ионов натрия и хлорид-ионов. При этом положительные полюсы молекул воды притягиваются к хлорид-ионам Сl — , отрицательные полюсы — к положительным ионам Na + .
В результате этого взаимодействия между молекулами растворителя и ионами электролита притяжение между ионами в кристаллической решетке вещества ослабевает. Кристаллическая решетка разрушается, и ионы переходят в раствор. Эти ионы в водном растворе находятся не в свободном состоянии, а связаны с молекулами воды, т. е. являются гидратированными ионами.
Диссоциация ионных соединений в водном растворе протекает полностью. Так диссоциируют соли и щелочи: KCl, LiNO3, Ba(OH)2 и др.
II. Механизм диссоциации электролитов, которые состоят из полярных молекул
При растворении в воде веществ с полярной ковалентной связью происходит взаимодействие дипольных молекул электролита с дипольными молекулами воды. Например, при растворении в воде хлороводорода происходит взаимодействие молекул НСl с молекулами Н2O. Под влиянием этого взаимодействия изменяется характер связи в молекуле HCl: сначала связь становится более полярной, а затем переходит в ионную связь. Результатом процесса является диссоциация электролита и образование в растворе гидратированных ионов.
Так диссоциируют кислородсодержащие и бескислородные кислоты: H2SO4, HNO3, НI и др. Диссоциация электролитов с полярной связью может быть полной или частичной. Это зависит от полярности связей в молекулах электролитов.
Таким образом, главной причиной диссоциации в водных растворах является гидратация ионов. В растворах электролитов все ионы находятся в гидратированном состоянии. Например, ионы водорода соединяются с молекулой воды и образуют ионы гидроксония Н3O+ по донорно-акцепторному механизму:
Для простоты в химических уравнениях ионы изображают без молекул воды: Н + , Ag + , Mg 2 + , F — , SO4 2- и т. д.
Свойства ионов
Ионы по физическим, химическим и физиологическим свойствам отличаются от нейтральных атомов, из которых они образовались. Например, ионы натрия Na + и хлорид-ионы Сl — не взаимодействуют с водой, не имеют цвета, запаха, неядовиты.
Атомы натрия Na 0 энергично взаимодействуют с водой. Вещество хлор C12 в свободном состоянии — газ желто-зеленого цвета, ядовит, сильный окислитель.
Различные свойства атомов и ионов одного и того же элемента объясняются разным электронным строением этих частиц. Химические свойства свободных атомов металлов определяются валентными электронами, которые атомы металлов легко отдают и переходят в положительно заряженные ионы. Атомы неметаллов легко присоединяют электроны и переходят в отрицательно заряженные ионы. Ионы находятся в более устойчивых электронных состояниях, чем атомы.
Ионы имеют различную окраску. Гидратированные и негидратированные ионы s- и р-элементов обычно бесцветны. Так, бесцветны ионы Н + , Na + , K + , Ва 2 + , Аl 3+ и др. Ионы некоторых d-элементов имеют окраску. Окраска гидратированных и негидратированных ионов одного и того же d-элемента может быть различной. Например, негидратированные ионы Cu 2+ — бесцветные, а гидратированные ионы меди Cu 2+ • 4Н2О — синего цвета
Степень диссоциации
В водных растворах некоторые электролиты полностью распадаются на ионы. Другие электролиты распадаются на ионы частично, часть их молекул остается в растворе в недиссоциированном виде.
Число, показывающее, какая часть молекул распалась на ионы, называется степенью электролитической диссоциации (степенью ионизации).
Степень электролитической диссоциации (α) равна отношению числа молекул, которые распались на ионы, к общему числу молекул в растворе:
где n — число молекул, распавшихся на ионы; N — общее число растворенных молекул.
Например, степень диссоциации (α) уксусной кислоты СН3СООН в 0,1 М растворе равна 1,36%. Это означает, что из 10000 молекул СН3СООН 136 молекул распадаются на ионы по уравнению:
Степень диссоциации зависит от природы растворителя и природы растворяемого вещества, концентрации раствора, температуры и других факторов.
Различные вещества диссоциируют в разной степени. Например, муравьиной кислоты НСООН при одинаковых условиях больше α уксусной кислоты СН3СООН.
При уменьшении концентрации электролита, т. е. при разбавлении раствора, степень диссоциации увеличивается, так как увеличиваются расстояния между ионами в растворе и уменьшается возможность соединения их в молекулы.
При повышении температуры степень диссоциации, как правило, увеличивается.
В зависимости от степени диссоциации электролиты делятся на сильные и слабые.
Сильные электролиты — это такие электролиты, которые в водных растворах полностью диссоциируют на ионы, т. е. их степень диссоциации равна 1 (100%). К сильным электролитам относятся: 1) соли; 2) сильные кислоты (HClO4, НСlO3, НNО3, H2SO4, HCl, НВr, HI и др.); 3) щелочи (LiОН, NaOH, КОН, RbOH, СsОН, Ca(OH)2, Sr(OH)2, Ba(OH)2.
Слабые электролиты — это такие электролиты, которые в водных растворах не полностью диссоциируют на ионы, т. е. их степень диссоциации меньше 1 (100%). К слабым электролитам относятся: 1) слабые кислоты (НСlO2, HClO, HNO2, H2SO3, Н2СO3, H2SiO3, Н3РО4, H3РО3, H3BO3, СН3СООН, Н2S, HCN, HF и др.); 2) слабые нерастворимые в воде основания Fe(OH)2, Pb(OH)2, Cu(OH)2 и др.); 3) гидроксид аммония (NH4OH); 4) вода (Н2О).
Константа диссоциации (ионизации)
Для характеристики слабых электролитов применяют константу диссоциации (Kд). Вследствие того, что слабые электролиты диссоциируют на ионы не полностью, в их растворах устанавливается динамическое равновесие между недиссоциированными молекулами и ионами. Для слабого электролита общей формулы АnВm уравнение диссоциации имеет вид:
Применяя закон действующих масс, запишем выражение константы равновесия:
где [А m + ], [B n — ] — равновесные концентрации ионов А m + и B n — , [АnВm] — равновесная концентрация недиссоциированных молекул АnВm.
Константу равновесия в этом случае называют константой диссоциации (Kд), или константой ионизации.
Константа ионизации характеризует способность электролита диссоциировать на ионы. Чем больше константа диссоциации, тем легче электролит распадается на ионы, тем больше ионов в его растворе, тем сильнее электролит. Например:
Следовательно, уксусная кислота СН3СООН более сильный электролит, чем циановодородная кислота HCN.
Для слабого электролита константа диссоциации — постоянная величина при данной температуре, которая не зависит от концентрации раствора. Константа диссоциации зависит от природы электролита, природы растворителя и температуры. Константы диссоциации некоторых слабых электролитов приведены в таблице.
Значение электролитов для живых организмов
Электролиты являются составной частью жидкостей и плотных тканей живых организмов. Ионы натрия Na + , калия K + , кальция Са 2+ , магния Mg 2+ , водорода Н + , анионы ОН — , Сl — , SO4 2- , НСО3 — имеют большое значение для физиологических и биохимических процессов. Концентрации различных ионов в организме человека различны. Концентрации ионов водорода Н+ и гидроксид-ионов ОН — очень малы, но они играют большую роль в жизненных процессах. Ионы водорода Н + способствуют нормальному функционированию ферментов, обмену веществ, перевариванию пищи и т.д. Концентрации ионов натрия Na + и хлорид-ионов Cl — в организме человека весьма значительны. Эти ионы человек получает ежедневно, используя в пищу поваренную соль NaCl. В медицине применяется 0,85%-ный раствор хлорида натрия в качестве физиологического раствора при большой потере жидкости организмом.
[spoiler title=”источники:”]
http://studarium.ru/article/159
http://al-himik.ru/jelektroliticheskaja-dissociacija-stepen-i-konstanta-dissociacii/
[/spoiler]
Вычислить степень диссоциации
Вычислить степень диссоциации (α) и равновесную концентрацию ионов водорода ([H+]) в 0,1 М растворе хлорноватистой кислоты (HClO). Константа диссоциации составляет 5 ∙ 10-8. Как изменится равновесная концентрация ионов водорода ([H+]), если к 1 литру 0,1 М раствора хлорноватистой кислоты (HClO) добавить 0,2 моля гипохлорита натрия (NaClO)?
Решение задачи
Перед тем как решить предложенную задачу и вычислить степень диссоциации, думаю, следует напомнить, что степень диссоциации слабого электролита резко снижается при добавлении к нему сильного электролита с одноименным ионом. Если в растворе слабого электролита , диссоциирующего по схеме:
увеличить концентрацию H+-ионов за счет прибавления сильной кислоты или концентрацию ионов A— за счет прибавления соли этой кислоты, это приведет к сдвигу равновесия влево, то есть к уменьшению относительного количества диссоциированных молекул электролита.
Запишем уравнение диссоциации хлорноватистой кислоты (HClO):
![]()
Найдем равновесную концентрацию ионов водорода ([H+]) по формуле:
![]()
Вычислим степень диссоциации хлорноватистой кислоты (HClO), используя формулу вычисления степени диссоциации:
![]()
Если к 1 л раствора хлорноватистой кислоты (HClO) добавить 0,2 моля гипохлорита натрия (NaClO), то концентрация ионов водорода (H+) уменьшится за счет увеличения концентрации ионов ClO—.
Запишем уравнение диссоциации гипохлорита натрия (NaClO):
![]()
Обозначим концентрацию ионов водорода (H+) через х, тогда концентрация ионов ClO— будет равна:
х + αClO— (αClO— – активность ионов ClO—, образовавшихся при диссоциации гипохлорита натрия (NaClO)).
Из таблицы 1 находим, что для 0,2 раствора гипохлорита натрия (NaClO) (µ = 0,2) коэффициент активности ионов ƒ = 0,7, а αClO— составит 0,14 моля (0,2 ∙ 0,7).
Таблица 1. Приближенные значения средних коэффициентов активности (ƒ) в зависимости от ионной силы (µ) раствора и заряда иона
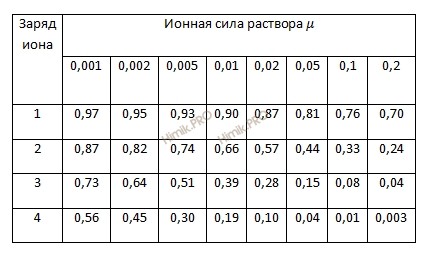
Подставим эти величины в выражение для константы диссоциации:
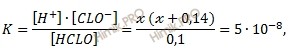
откуда:
х2 + 0,14х = 5 ⋅ 10-9.
Так как х2 величина очень маленькая, для упрощения вычислений пренебрегаем ею, тогда:
0,14х = 5 ⋅ 10-9
х = 3,6 ⋅ 10-8 (моль/л).
Найдем во сколько раз уменьшилась равновесную концентрацию ионов водорода ([H+]), а следовательно и степень диссоциации:
![]()
Ответ:
степень диссоциации равна 0,07 % или 7 ⋅ 10-4 моль/л;
равновесная концентрация ионов водорода равна 7 ⋅ 10-5 моль/л;
равновесная концентрация ионов водорода уменьшится в 1950 раз.