Мы уже говорили, что термин валентность допустимо применять только к атомам, которые связаны с другими атомами ковалентными химическими связями. Так как по определению, валентность – это количество ковалентных связей конкретного атома.
Во многих школьных учебниках и пособиях учат составлять формулы по валентностям, даже для соединений с ионными связями. Для упрощения процедуры составления формул это, на наш взгляд, допустимо. Но нужно понимать, что это не совсем корректно ввиду вышеизложенной причины.
Более универсальным понятием является понятие о степени окисления. По значениям степеней окисления атомов так же как и по значениям валентности можно составлять химические формулы и записывать формульные единицы.
Отметим, что степень окисления и формальный заряд – совершенно разные понятия. Обстоятельно о формальном заряде и методах его рассчёта мы поговорим чуть позже, в последующих главах, а пока же можете поинтересоваться этим вопросом в литературных источниках.
Степень окисления – это условный заряд атома в частице (молекуле, ионе, радикале), вычисленный в приближении того, что все связи в частице являются ионными.
Прежде чем определять степени окисления, необходимо сравнить электроотрицательности связуемых атомов. Атом с большим значением электроотрицательности имеет отрицательную степень окисления, а с меньшим положительную.
Для определения значений электроотрицательностей можно пользоваться шкалой Полинга, но мы не рекомендуем это делать по ряду причин. Например, по шкале Полинга электроотрицательность хлора выше чем электроотрицательность азота. Если бы это было так, то реакция гидролиза NCl3 протекала бы с образованием HNO2 и HCl (гидролиз — не окислительно восстановительный процесс). Известно, что при гидролизе NCl3 образуется NH3 и HClO (допустимо в качестве продукта указывать NH4ClO). Из этого следует, что электроотрицательность азота выше, нежели чем электроотрицательность хлора.
С целью объективного сравнения значений электроотрицательности атомов при расчёте степеней окисления, в 2013 году IUPAC дал рекомендацию использовать шкалу Аллена.
- Так, например, по шкале Аллена электроотрицательность азота 3,066, а хлора 2,869.
Проиллюстрируем данное выше определение на примерах. Составим структурную формулу молекулы воды.
Ковалентные полярные связи O-H обозначены синим цветом.
Представим, что обе связи являются не ковалентными, а ионными. Если бы они были ионными, то с каждого атома водорода на более электроотрицательный атом кислорода перешло бы по одному электрону. Обозначим эти переходы синими стрелками.
*В этом примере, стрелка служит для наглядной иллюстрации полного перехода электронов, а не для иллюстрации индуктивного эффекта.
Легко заметить, что число стрелок показывает количество перешедших электронов, а их направление – направление перехода электронов.
На атом кислорода направлено две стрелки, это значит, что к атому кислорода переходит два электрона: 0 + (-2) = -2. На атоме кислорода образуется заряд равный -2. Это и есть степень окисления кислорода в молекуле воды.
С каждого атома водорода уходит по одному электрону: 0 – (-1) = +1. Значит, атомы водорода имеют степень окисления равную +1.
Сумма степеней окисления всегда равняется общему заряду частицы.
Например, сумма степеней окисления в молекуле воды равна: +1(2) + (-2) = 0. Молекула – электронейтральная частица.
Если мы вычисляем степени окисления в ионе, то сумма степеней окисления, соответственно, равна его заряду.
Значение степени окисления принято указывать в верхнем правом углу от символа элемента. Причём, знак пишут впереди числа. Если знак стоит после числа – то это заряд иона.
Теперь рассмотрим случай, когда соединение имеет смешанные связи: Na2SO4. Связь между сульфат-анионом и катионами натрия – ионная, связи между атомом серы и атомами кислорода в сульфат-ионе – ковалентные полярные. Запишем графическую формулу сульфата натрия, а стрелками укажем направление перехода электронов.
Структурная формула отображает порядок ковалентных связей в частице (молекуле, ионе, радикале). Структурные формулы применяют только для частиц с ковалентными связями. Для частиц с ионными связями понятие структурной формулы не имеет смысла. Если в частице имеются ионные связи, то применяют графическую формулу.
Видим, что от центрального атома серы уходит шесть электронов, значит степень окисления серы 0 – (-6) = +6.
Концевые атомы кислорода принимают по два электрона, значит их степени окисления 0 + (-2) = -2
Мостиковые атомы кислорода принимают по два электрона, их степень окисления равна -2.
В этой формуле мостиковые атомы кислорода уже имеют единичные отрицательные заряды и к ним дополнительно приходит по электрону от атома серы -1 + (-1) = -2, значит их степени окисления равны -2.
Определим степени окисления элементов в надпероксиде (супероксиде) калия. Для этого составим графическую формулу супероксида калия, стрелочкой покажем перераспределение электронов. Связь O-O является ковалентной неполярной, поэтому в ней перераспределение электронов не указывается.
Надпероксид-анион является ион-радикалом. Формальный заряд одного атома кислорода равен -1, а другого, с неспаренным электроном, 0.
Видим, что степень окисления калия равна +1. Степень окисления атома кислорода, записанного в формуле напротив калия, равна -1. Степень окисления второго атома кислорода равна 0.
Точно также можно определить степени окисления и по структурно-графической формуле.
В кружочках указаны формальные заряды иона калия и одного из атомов кислорода. При этом значения формальных зарядов совпадают со значениями степеней окисления.
Так как оба атома кислорода в надпероксид-анионе имеют разные значения степени окисления, то можно вычислить средне-арифметическую степень окисления кислорода.
Она будет равна [0 + (-1)] / 2 = – 1/2 = -0,5.
Значения среднеарифметических степеней окисления обычно указывают в брутто-формулах или формульных единицах, чтобы показать что сумма степеней окисления равна общему заряду системы.
Для случая с надпероксидом: +1 + 2(-0,5) = 0
Легко определить степени окисления используя электронно-точечные формулы, в которых указывают точками неподеленные электронные пары и электроны ковалентных связей.
Кислород – элемент VIА – группы, следовательно в его атоме 6 валентных электронов. Представим, что в молекуле воды связи ионные, в этом случае атом кислорода получил бы октет электронов.
Степень окисления кислорода соответственно равна: 6 – 8 = -2.
А атомов водорода: 1 – 0 = +1
Умение определять степени окисления по графическим формулам бесценно для понимания сущности этого понятия, так же это умение потребуется в курсе органической химии. Если же мы имеем дело с неорганическими веществами, то необходимо уметь определять степени окисления по молекулярным формулам и формульным единицам.
Для этого прежде всего нужно понять, что степени окисления бывают постоянными и переменными. Элементы, проявляющие постоянную степень окисления необходимо запомнить.
Любой химический элемент характеризуется высшей и низшей степенями окисления.
Низшая степень окисления – это заряд, который приобретает атом в результате приёма максимального количества электронов на внешний электронный слой.
Ввиду этого, низшая степень окисления имеет отрицательное значение.
Даже атомы металлов могут проявлять отрицательные значения ЭО, например железо в Na2[Fe(CO)4]. Связано это с тем, что степень окисления — условная величина.
Большинство неметаллов главных подгрупп старается заполнить свой внешний электронный слой до восьми электронов, после этого атом приобретает устойчивую конфигурацию (правило октета). Поэтому, чтобы определить низшую степень окисления, необходимо понять сколько атому не хватает валентных электронов до октета.
Например, азот – элемент VА группы, это значит, что в атоме азота пять валентных электронов. До октета атому азота не хватает трёх электронов. Значит низшая степень окисления азота равна: 0 + (-3) = -3
Высшая степень окисления – это заряд, который приобретает атом в результате отдачи максимального количества валентных электронов.
По этой причине высшая степень окисления имеет положительное значение, за исключением фтора, атом которого электроны никогда и никому из атомов простых веществ не отдаёт, фтор – самый электроотрицательный элемент.
Высшая степень окисления фтора равна 0.
Чтобы определить высшую степень окисления, необходимо понять какое максимальное количество валентных электронов может отдать атом другим атомам.
Например, в атоме азота пять валентных электронов, если все пять электронов атом азота отдаст другому, более электроотрицательному атому 0 – (-5), то он приобретет степень окисления равную +5.
Атом кислорода не может отдать все шесть валентных электронов, так как у кислорода высокое значение электроотрицательности. Кислород максимум может отдать два валентные электрона и то только атому фтора. По этой причине высшая степень окисления кислорода равна +2 в соединении OF 2 – фторид кислорода.
Значение степени окисления часто не совпадает с валентностью.
Формальный заряд при этом тоже может отличаться (он указывается в кружочках).
Рекомендуем запомнить некоторые примеры, иллюстрирующие этот факт.
В катионе аммония валентность азота равна IV, а степень окисления -3.
В молекуле угарного газа (CO) валентность углерода и кислорода равна III, а степени окисления +2 и -2 (не удивляйтесь этому, даже если Вас учили, что кислород всегда двухвалентен, так как в современном понимании валентность – всего лишь число ковалентных связей атома).
В катионе гидроксония атом кислорода трёхвалентен, а его степень окисления равна -2.
В молекуле азотной кислоты атом азота четырёхвалентен, а его степень окисления равна +5. При этом один из атомов кислорода I-валентен, но его степень окисления равна -2.
*Попробуйте для примера определить валентности и степени окисления атомов кислорода в молекуле озона, а также в синглетном и триплетном состояниях молекулы кислорода.
Загрузить PDF
Загрузить PDF
В химии термины «окисление» и «восстановление» означает реакции, при которых атом или группа атомов теряют или, соответственно, приобретают электроны. Степень окисления — это приписываемая одному либо нескольким атомам численная величина, характеризующая количество перераспределяемых электронов и показывающая, каким образом эти электроны распределяются между атомами при реакции. Определение этой величины может быть как простой, так и довольно сложной процедурой, в зависимости от атомов и состоящих из них молекул. Более того, атомы некоторых элементов могут обладать несколькими степенями окисления. К счастью, для определения степени окисления существуют несложные однозначные правила, для уверенного пользования которыми достаточно знания основ химии и алгебры.
-

1
Определите, является ли рассматриваемое вещество элементарным. Степень окисления атомов вне химического соединения равна нулю. Это правило справедливо как для веществ, образованных из отдельных свободных атомов, так и для таких, которые состоят из двух, либо многоатомных молекул одного элемента.
- Например, Al(s) и Cl2 имеют степень окисления 0, поскольку оба находятся в химически несвязанном элементарном состоянии.
- Обратите внимание, что аллотропная форма серы S8, или октасера, несмотря на свое нетипичное строение, также характеризуется нулевой степенью окисления.
-

2
Определите, состоит ли рассматриваемое вещество из ионов. Степень окисления ионов равняется их заряду. Это справедливо как для свободных ионов, так и для тех, которые входят в состав химических соединений.
- Например, степень окисления иона Cl– равняется -1.
- Степень окисления иона Cl в составе химического соединения NaCl также равна -1. Поскольку ион Na, по определению, имеет заряд +1, мы заключаем, что заряд иона Cl -1, и таким образом степень его окисления равна -1.
-

3
Учтите, что ионы металлов могут иметь несколько степеней окисления. Атомы многих металлических элементов могут ионизироваться на разные величины. Например, заряд ионов такого металла как железо (Fe) равняется +2, либо +3.[1]
Заряд ионов металла (и их степень окисления) можно определить по зарядам ионов других элементов, с которыми данный металл входит в состав химического соединения; в тексте этот заряд обозначается римскими цифрами: так, железо (III) имеет степень окисления +3.- В качестве примера рассмотрим соединение, содержащее ион алюминия. Общий заряд соединения AlCl3 равен нулю. Поскольку нам известно, что ионы Cl– имеют заряд -1, и в соединении содержится 3 таких иона, для общей нейтральности рассматриваемого вещества ион Al должен иметь заряд +3. Таким образом, в данном случае степень окисления алюминия равна +3.
-

4
Степень окисления кислорода равна -2 (за некоторыми исключениями). Почти во всех случаях атомы кислорода имеют степень окисления -2. Есть несколько исключений из этого правила:
- Если кислород находится в элементарном состоянии (O2), его степень окисления равна 0, как и в случае других элементарных веществ.
- Если кислород входит в состав перекиси, его степень окисления равна -1. Перекиси — это группа соединений, содержащих простую кислород-кислородную связь (то есть анион перекиси O2-2). К примеру, в составе молекулы H2O2 (перекись водорода) кислород имеет заряд и степень окисления -1.
- В соединении с фтором кислород обладает степенью окисления +2, читайте правило для фтора ниже.
-

5
Водород характеризуется степенью окисления +1, за некоторыми исключениями. Как и для кислорода, здесь также существуют исключения. Как правило, степень окисления водорода равна +1 (если он не находится в элементарном состоянии H2). Однако в соединениях, называемых гидридами, степень окисления водорода составляет -1.
- Например, в H2O степень окисления водорода равна +1, поскольку атом кислорода имеет заряд -2, и для общей нейтральности необходимы два заряда +1. Тем не менее, в составе гидрида натрия степень окисления водорода уже -1, так как ион Na несет заряд +1, и для общей электронейтральности заряд атома водорода (а тем самым и его степень окисления) должен равняться -1.
-

6
Фтор всегда имеет степень окисления -1. Как уже было отмечено, степень окисления некоторых элементов (ионы металлов, атомы кислорода в перекисях и так далее) может меняться в зависимости от ряда факторов. Степень окисления фтора, однако, неизменно составляет -1. Это объясняется тем, что данный элемент имеет наибольшую электроотрицательность — иначе говоря, атомы фтора наименее охотно расстаются с собственными электронами и наиболее активно притягивают чужие электроны. Таким образом, их заряд остается неизменным.
-

7
Сумма степеней окисления в соединении равна его заряду. Степени окисления всех атомов, входящих в химическое соединение, в сумме должны давать заряд этого соединения. Например, если соединение нейтрально, сумма степеней окисления всех его атомов должна равняться нулю; если соединение является многоатомным ионом с зарядом -1, сумма степеней окисления равна -1, и так далее.
- Это хороший метод проверки — если сумма степеней окисления не равна общему заряду соединения, значит вы где-то ошиблись.
Реклама
-

1
Найдите атомы, не имеющие строгих правил относительно степени окисления. По отношению к некоторым элементам нет твердо установленных правил нахождения степени окисления. Если атом не подпадает ни под одно правило из перечисленных выше, и вы не знаете его заряда (например, атом входит в состав комплекса, и его заряд не указан), вы можете установить степень окисления такого атома методом исключения. Вначале определите заряд всех остальных атомов соединения, а затем из известного общего заряда соединения вычислите степень окисления данного атома.
- Например, в соединении Na2SO4 неизвестен заряд атома серы (S) — мы лишь знаем, что он не нулевой, поскольку сера находится не в элементарном состоянии. Это соединение служит хорошим примером для иллюстрации алгебраического метода определения степени окисления.
-

2
Найдите степени окисления остальных элементов, входящих в соединение. С помощью описанных выше правил определите степени окисления остальных атомов соединения. Не забывайте об исключениях из правил в случае атомов O, H и так далее.
- Для Na2SO4, пользуясь нашими правилами, мы находим, что заряд (а значит и степень окисления) иона Na равен +1, а для каждого из атомов кислорода он составляет -2.
-

3
Умножьте количество атомов на их степень окисления. Теперь, когда нам известны степени окисления всех атомов за исключением одного, необходимо учесть, что атомов некоторых элементов может быть несколько. Умножьте число атомов каждого элемента (оно указано в химической формуле соединения в виде подстрочного числа, следующего за символом элемента) на его степень окисления.
- В Na2SO4 мы имеем 2 атома Na и 4 атома O. Таким образом, умножая 2 × +1, получаем степень окисления всех атомов Na (2), а умножая 4 × -2 — степень окисления атомов O (-8).
-

4
Сложите предыдущие результаты. Суммируя результаты умножения, получаем степень окисления соединения без учета вклада искомого атома.
- В нашем примере для Na2SO4 мы складываем 2 и -8 и получаем -6.
-

5
Найдите неизвестную степень окисления из заряда соединения. Теперь у вас есть все данные для простого расчета искомой степени окисления. Запишите уравнение, в левой части которого будет сумма числа, полученного на предыдущем шаге вычислений, и неизвестной степени окисления, а в правой — общий заряд соединения. Иными словами, (Сумма известных степеней окисления) + (искомая степень окисления) = (заряд соединения).
- В нашем случае Na2SO4 решение выглядит следующим образом:
- (Сумма известных степеней окисления) + (искомая степень окисления) = (заряд соединения)
- -6 + S = 0
- S = 0 + 6
- S = 6. В Na2SO4 сера имеет степень окисления 6.
Реклама
- В нашем случае Na2SO4 решение выглядит следующим образом:
Советы
- В соединениях сумма всех степеней окисления должна равняться заряду. Например, если соединение представляет собой двухатомный ион, сумма степеней окисления атомов должна быть равна общему ионному заряду.
- Очень полезно уметь пользоваться периодической таблицей Менделеева и знать, где в ней располагаются металлические и неметаллические элементы.
- Степень окисления атомов в элементарном виде всегда равна нулю. Степень окисления единичного иона равна его заряду. Элементы группы 1A таблицы Менделеева, такие как водород, литий, натрий, в элементарном виде имеют степень окисления +1; степень окисления металлов группы 2A, таких как магний и кальций, в элементарном виде равна +2. Кислород и водород, в зависимости от вида химической связи, могут иметь 2 различных значения степени окисления.
Реклама
Что вам понадобится
- Периодическая таблица элементов
- Доступ в интернет или справочники по химии
- Лист бумаги, ручка или карандаш
- Калькулятор
Об этой статье
Эту страницу просматривали 644 676 раз.
Была ли эта статья полезной?
Профи
(752),
закрыт
9 лет назад
Вячек
Высший разум
(391245)
10 лет назад
Если в простом ионе (из одного элемента) , то его заряд и есть степени окисления атом. Например, S(2-) – это и заряд иона, и степень окисления.
В сложном ионе сумма всех зарядов атомов должна быть равна заряду иона. Например, нужно определить степень окисления атомов фосфора в анионе пирофосфата, Р2О7(4-):
Принимаем за Х степень окисления атома фосфора, а у кислорода она -2. Составляем простенькое уравнение:
2Х +7(-2) = -4, или 2Х = +10, или Х = +5 это и есть степень окисления атомов фосфора
Успехов!
Сте́пень окисле́ния (окислительное число[1]) — вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов: она не является истинным зарядом атома в молекуле (см. #Условность).
Представления о степени окисления элементов положены в основу и используются при классификации химических веществ, описании их свойств, составлении формул соединений и их международных названий (номенклатуры). Но особенно широко оно применяется при изучении окислительно-восстановительных реакций.
Понятие степень окисления часто используют в неорганической химии вместо понятия валентность.
Определение[править | править код]
Степень окисления атома равна численной величине электрического заряда, приписываемого атому в предположении, что электронные пары, осуществляющие связь, полностью смещены в сторону более электроотрицательных атомов (то есть исходя из предположения, что соединение состоит только из ионов). В случае ковалентной связи между одинаковыми атомами электроны делят поровну между атомами.
Степень окисления соответствует числу электронов, которое следует присоединить к положительному иону, чтобы восстановить его до нейтрального атома, или отнять от отрицательного иона, чтобы окислить его до нейтрального атома:
Описание[править | править код]
В научной литературе для обозначения степени окисления элемента используется метод Штока[2]. Степень окисления указывается после названия либо символа элемента римскими цифрами в круглых скобках, причём пробел перед открывающей скобкой не ставится: железо(III), Ni(II).
Степень окисления также может указываться арабскими цифрами сверху над символом элемента: 


Степень окисления (в отличие от валентности) может иметь нулевое, отрицательное и положительное значения, которые обычно ставятся над символом элемента сверху: 
Правила вычисления степени окисления:
- Степень окисления атома любого элемента в свободном (несвязанном) состоянии (простое вещество) равна нулю, так, например, атомы в молекулах имеют нулевую степень окисления:
- Степень окисления любого простого одноатомного иона соответствует его заряду, например: Na+ = +1, Ca2+ = +2, Cl− = −1.
- Степень окисления водорода в любом неионном соединении равна +1. Это правило применимо к подавляющему большинству соединений водорода, таких, как H2O, NH3 или CH4. (Определение через электротрицательность даёт исключение для некоторых веществ:
). Для ионных гидридов металлов, например NaH, степень окисления водорода −1.
- Степень окисления кислорода равна −2 во всех соединениях, где кислород не образует простой ковалентной связи O—O, то есть в подавляющем большинстве соединений — оксидах. Так, степень окисления кислорода равна −2 в H2O, H2SO4, NO, CO2 и CH3OH; но в пероксиде водорода, H2O2 (HO—OH), она равна −1 (другими исключениями из правила, согласно которому кислород имеет степень окисления −2, являются
, а также свободные радикалы, например
).
- В соединениях неметаллов, не включающих водород и кислород, неметалл с большей электроотрицательностью считается отрицательно заряжённым. Степень окисления такого неметалла полагается равной заряду его наиболее распространённого отрицательного иона. Например, в CCl4 степень окисления хлора −1, а углерода +4. В CH4 степень окисления водорода +1, а углерода −4. В SF6 степень окисления фтора −1, а серы +6, но в CS2 степень окисления серы −2, а степень окисления углерода +4.
- Алгебраическая сумма степеней окисления всех атомов в формуле нейтрального соединения всегда равна нулю:


- Алгебраическая сумма степеней окисления всех атомов в комплексном ионе (катионе либо анионе) должна быть равна его общему заряду (см. также выше 2-й пункт). Так, в ионе NH4+ степень окисления N должна быть равной −3 и, следовательно, −3 + 4 = +1. Поскольку в ионе SO42− сумма степеней окисления четырёх атомов кислорода равна −8, сера должна иметь степень окисления, равную +6, чтобы полный заряд иона оказался равным −2.
- В химических реакциях должно выполняться правило сохранения алгебраической суммы степеней окисления всех атомов. Именно это правило делает понятие степени окисления столь важным в современной химии. Если в ходе химической реакции степень окисления атома повышается, говорят, что он окисляется, если же степень окисления атома понижается, говорят, что он восстанавливается. В полном уравнении химической реакции окислительные и восстановительные процессы должны точно компенсировать друг друга.
- Максимальная положительная степень окисления элемента обычно численно совпадает с номером его группы в периодической системе (классического короткого варианта таблицы). Максимальная отрицательная степень окисления элемента равна максимальной положительной степени окисления минус восемь (например, для халькогена S положительная степень окисления +6, макс. отрицательная 6 − 8 = −2).
Исключение составляют фтор, кислород, благородные газы (кроме ксенона), а также железо, кобальт, родий и элементы подгруппы никеля: их высшая степень окисления выражается числом, значение которого ниже, чем номер группы, к которой они относятся. Иридий имеет высшую степень окисления +9[4]. У элементов подгруппы меди, наоборот, высшая степень окисления больше единицы, хотя они и относятся к I группе. У лантаноидов степени окисления не превышают +4 (в особых условиях зафиксирована степень окисления +5 для празеодима[5]); у актиноидов зафиксированы степени окисления вплоть до +7.
Правило о равенстве числу восемь суммы абсолютных величин степеней окисления элемента (R) по кислороду (RO) и по водороду (HR; то есть положительных и отрицательных степеней окисления) соблюдается лишь для p-элементов IV—V—VI—VII групп таблицы ПСХЭ. - Элементы-металлы в соединениях обычно имеют положительную степень окисления. Однако встречаются соединения, где степень окисления металлов нулевая (нейтральные карбонилы и некоторые другие комплексы) и отрицательная (алкалиды, ауриды, анионные карбонилы, фазы Цинтля)[6][7].
Понятие степени окисления вполне применимо и для нестехиометрических соединений (КС8, Mo5Si3, Nb3B4 и др.).
Условность[править | править код]
Следует помнить, что степень окисления является сугубо условной величиной, не имеющей физического смысла, но характеризующей образование химической связи межатомного взаимодействия в молекуле.
Степень окисления в ряде случаев не совпадает с валентностью. Например, в органических соединениях углерод всегда четырёхвалентен, а степень окисления атома углерода в соединениях метана CH4, метилового спирта CH3OH, формальдегида HCOH, муравьиной кислоты HCOOH и диоксида углерода CO2, соответственно, равна −4, −2, 0, +2 и +4.
Степень окисления зачастую не совпадает с фактическим числом электронов, которые участвуют в образовании связей. Обычно это молекулы с различными электрондефицитными химическими связями и делокализацией электронной плотности. Например, в молекуле азотной кислоты степень окисления центрального атома азота равна +5, тогда как ковалентность равна 4, а координационное число — 3. В молекуле озона, имеющей сходное с SO2 строение, атомы кислорода характеризуется нулевой степенью окисления (хотя часто говорят, что центральный атом кислорода имеет степень окисления +4).
Степень окисления в большинстве случаев не отражает также действительный характер и степень электрической поляризации атомов (истинного заряда атомов, определённых экспериментальным путём). Так, и в HCl, и в NaCl степень окисления хлора принимается равной −1, тогда как на самом деле поляризация его атома (относительный эффективный заряд δ−) в этих соединениях различна:
δCl(HCl) = −0,17 единицы заряда,
δCl(NaCl) = −0,9 единицы заряда (абсолютного заряда электрона); водорода и натрия — соответственно +0,17 и +0,90[8].
А в кристаллах сульфида цинка ZnS заряды атомов цинка и серы равны соответственно +0,86 и −0,86, вместо степеней окисления +2 и −2[9].
На примере хлорида аммония удобно затронуть существующее в современной химии перекрещивание различных понятий. Так, в NH4Cl атом азота имеет степень окисления −3, ковалентность IV, электровалентность (формальный заряд по Льюису) +1 {аммоний-катион имеет заряд также 1+}, и общую валентность (структурную; общее координационное число) 5, а для его эффективного заряда предлагалось значение −0,45[10].
Проблемы[править | править код]
Применение понятия степени окисления проблематично для следующих классов соединений[11]:
- Соединения, содержащие ковалентные связи между атомами близкой электроотрицательности, например: PH3, Cl3N. В этом случае использование различных шкал электроотрицательности даёт различные результаты. В 2014 году ИЮПАК дал рекомендацию пользоваться шкалой электроотрицательности Аллена, поскольку другие шкалы используют понятия валентного состояния атома (что усложняет определение условной величины) или его степени окисления (что создаёт порочный круг)[12].
- Соединения, содержащие делокализованные ковалентные связи и являющиеся промежуточными между резонансными структурами, где степени окисления атомов различны. Например, в молекуле N2O крайний атом азота имеет степень окисления от −1 до 0, средний — от +2 до +3. В случае, когда атомы одного элемента в структуре равноправны, им приписывают среднее из возможных значений степени окисления, которое может быть дробным. Например:
. В уравнениях окислительно-восстановительных реакций часто используют средние (в том числе дробные) значения степени окисления даже в том случае, когда атомы неравноправны, например
(по строгому определению
).
- Соединения, содержащие полностью делокализованные электроны (металлическая связь). Например, дикарбид лантана LaC2 состоит из ионов La3+, C22− и делокализованных электронов. Наличие в соединении ионов C22− позволяет считать степень окисления лантана равной +2; с другой стороны, бо́льшая длина связи C≡C по сравнению с CaC2, объясняемая взаимодействием делокализованных электронов с антисвязывающими орбиталями, позволяет считать степень окисленния углерода равной −3/2. Третья возможность — рассматривать такие соединения как электриды, то есть не приписывать делокализованные электроны ни одному из атомов. В случае, когда все элементы в соединении — металлы (см. Интерметаллиды), их степени окисления обычно считают равными нулю.
Пример составления уравнения окислительно-восстановительной реакции[править | править код]
Составляем электронные уравнения:
Найденные коэффициенты проставляем в схему процесса, заменяя стрелку на знак равенства:
(то есть в электронных реакциях (методе электронного баланса) железо с дробной степенью окисления записывается только с коэффициентом 3).
На самом деле, в растворе нет ионов Fe2+, Fe3+ (и уж тем более Fe+8/3), также как и Cr6+, Mn7+, S6+, а есть ионы CrO42−, MnO4−, SO42−, а равно и малодиссоциированные «электролиты» Fe3O4 (FeO•Fe2O3). Именно поэтому следует отдать предпочтение методу полуреакций (ионно-электронным методам) и применять его при составлении уравнении всех окислительно-восстановительных реакций, протекающих в водных растворах. То есть мы можем воспользоваться готовой реакцией стандартного электродного потенциала:
Fe3O4 + 8H+ + 8e− = 3Fe + 4H2O, E° = −0,085 В.
См. также[править | править код]
- Валентность
- Координационное число
Примечания[править | править код]
- ↑ Окислительное число // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- ↑ Справочник химика. Под ред. Б. П. Никольского, Л: Химия, 1971. С. 13.
- ↑ Эту фиктивную зарядность в молекулах с ковалентными связями правильнее называть степенью окисления элемента, иначе, его окислительным числом. Для отличия от положительной или отрицательной зарядности (например,
,
) знаки при степени окисления (окислительном числе) меняют на обратные (например,
). Адекватны этой формуле и изображения: H→F и Hδ+—Fδ−. Агафошин Н.П. Периодический закон и периодическая система хим. элементов Д. И. Менделеева. — 2-е изд. — М.: Просвещение, 1982. — с. 56
- ↑ Guanjun Wang, Mingfei Zhou, James T. Goettel, Gary J. Schrobilgen, Jing Su, Jun Li, Tobias Schlöder, Sebastian Riedel. Identification of an iridium-containing compound with a formal oxidation state of IX (англ.) // Nature. — 2014. — Vol. 514. — P. 575—577. — doi:10.1038/nature13795.
- ↑ Qingnan Zhang, Shu‐Xian Hu, Hui Qu, Jing Su, Guanjun Wang, Jun‐Bo Lu, Mohua Chen, Mingfei Zhou, Jun Li. Pentavalent Lanthanide Compounds: Formation and Characterization of Praseodymium(V) Oxides (англ.) // Angewandte Chemie International Edition. — 2016. — Vol. 55. — P. 6896–6900. — ISSN 1521-3773. — doi:10.1002/anie.201602196.
- ↑ John E. Ellis. Adventures with Substances Containing Metals in Negative Oxidation
States (англ.) // Inorganic Chemistry. — 2006. — Vol. 45. — P. 3167—3186. — doi:10.1021/ic052110i. - ↑ Metalle in negativen Oxidationszuständen (нем.). Дата обращения: 14 марта 2015. Архивировано 29 марта 2015 года.
- ↑ Степень окисления не следует путать с истинным эффективным зарядом атома, который практически всегда выражается дробным числом.
Рассмотрим для наглядности ряд соединений хлора:В HCl хлор отрицательно одновалентен.
В молекуле Cl2, к примеру, ни один из атомов не оттягивает электронов больше другого, следовательно, заряд [а равно и степень окисления] равен нулю. В Cl2O хлор снова одновалентен, но уже положительно. В Cl2O7 хлор положительно семивалентен:
Определяемые подобным образом электрохимические валентности (степени окисления) отдельных атомов могут не совпадать с их обычными (структурными) валентностями. Например, в молекуле Cl2 (Cl-Cl) каждый атом хлора электрохимически нуль-валентен (точнее, степень окисления = 0), но структурно он одновалентен (валентность = I).
Некрасов Б.В. Основы общей химии. — 3-е изд., испр. и доп. — М.: Химия, 1973. — Т. I. — стр. 285—295
см. также Эффективный заряд. - ↑ Угай Я. А. Валентность, химическая связь и степень окисления — важнейшие понятия химии Архивная копия от 13 апреля 2014 на Wayback Machine // Соросовский образовательный журнал. — 1997. — № 3. — С. 53-57
- ↑ Некрасов Б.В. Основы общей химии. — 3-е изд., испр. и доп. — М.: Химия, 1973. — Т. I. — стр. 395
- ↑ Pavel Karen, Patrick McArdle, Josef Takats. Toward a comprehensive definition of oxidation state (IUPAC Technical Report) (англ.) // Pure and Applied Chemistry. — 2014. — Vol. 86, no. 6. — P. 1017—1081. — ISSN 1365-3075. — doi:10.1515/pac-2013-0505.
- ↑ P. Karen, P. McArdle, J. Takats. Comprehensive definition of oxidation state (англ.) // Pure Appl. Chem.. — 2015. — 16 December. Архивировано 2 февраля 2017 года.

Как определить степень окисления
Материал по химии
Что такое степень окисления?
Степень окисления – это условная величина, отражающая количество принятых или отданных электронов при образовании заряженной частицы из электронейтрального атома при условии, что электроны переходят от одного атома к другому полностью.
Вспомним, что идеальное количество электронов на внешнем электронном уровне атома равно восьми. Такую конфигурацию внешнего слоя имеют атомы большинства благородных газов (кроме гелия). И к такой электронной конфигурации стремятся атомы других элементов.
Как определить степень окисления
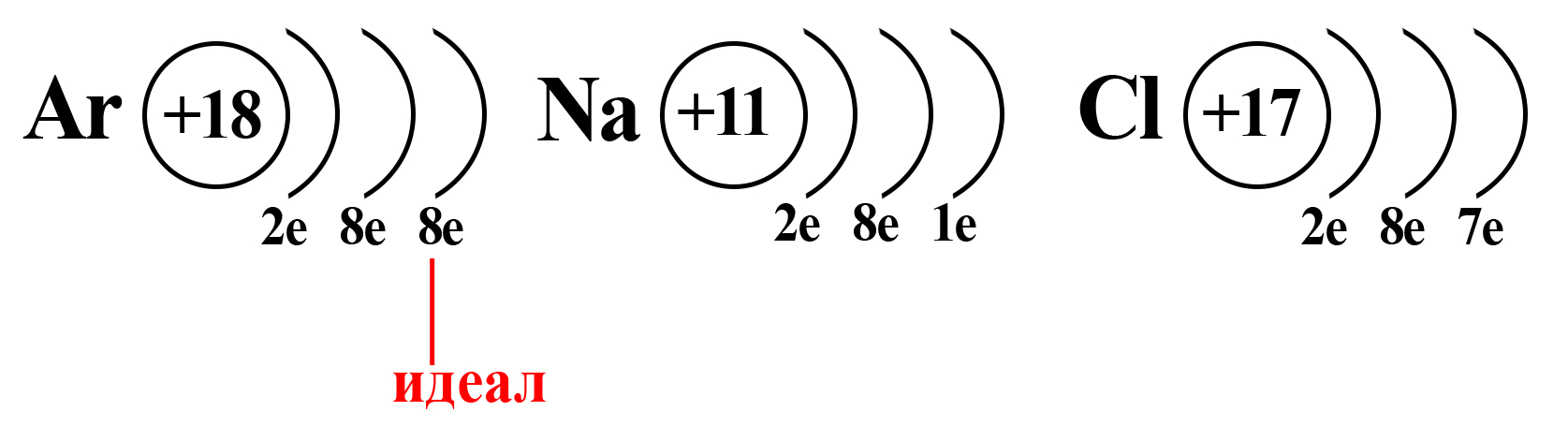
Конфигурация благородного газа
Натрий и хлор не так далеки от «идеала», как может показаться. Если атомы этих элементов столкнуться, внешний электрон натрия притянется на внешний электронный уровень хлора (из-за большей электроотрицательности хлора):
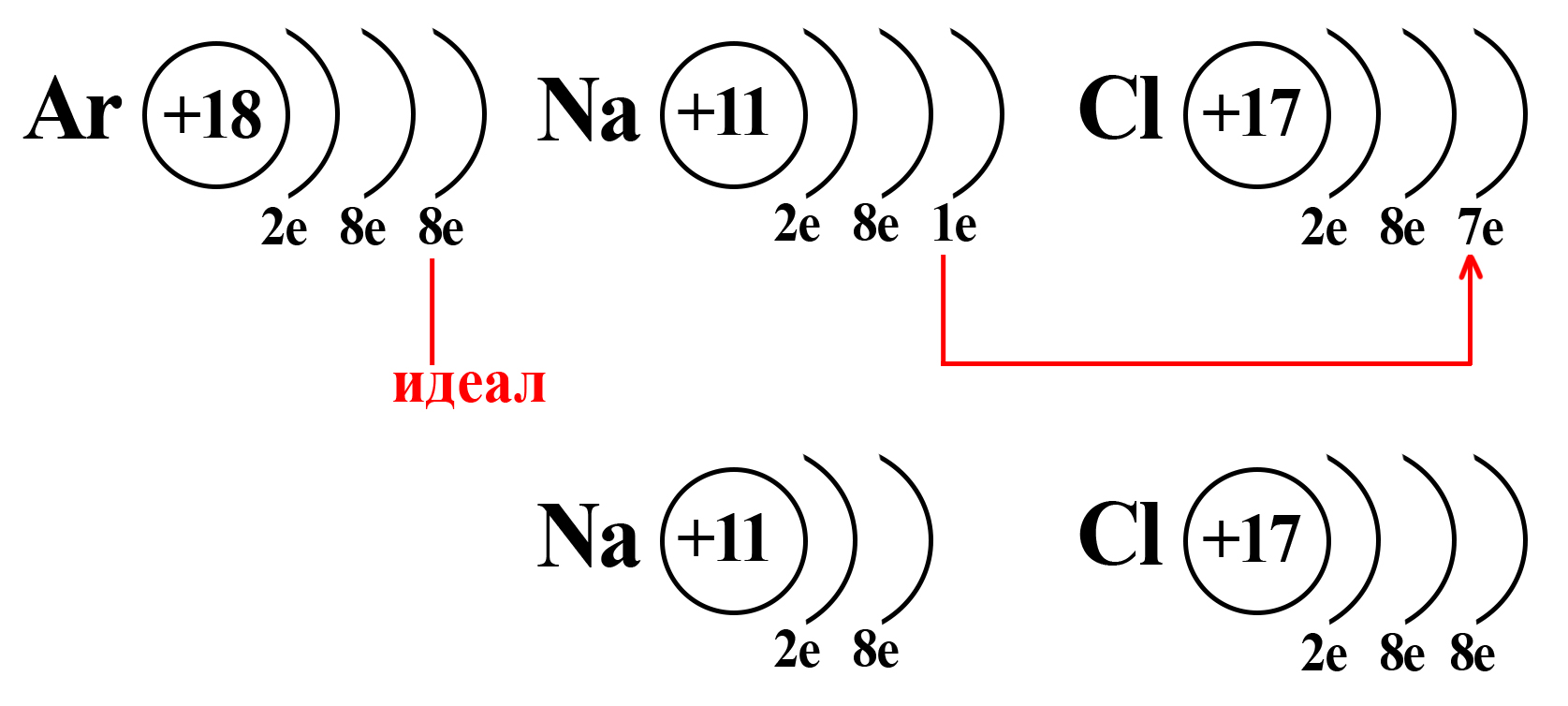
Таким образом, натрий и хлор как будто вступают в симбиоз: натрию, для приобретения «благородной» конфигурации необходимо избавиться от внешнего электрона (при потере внешнего электрона теряется и внешний уровень, а предвнешний уровень, имеющий идеальное количество электронов, становится внешним), тогда как хлору необходимо получить один электрон, чтобы завершить внешний энергетический уровень.
Потеряв один электрон, натрий приобретает положительный заряд, становится катионом (положительно заряженной частицей). Это объясняется тем, что ядро натрия по-прежнему имеет 11 протонов, а вот электронная оболочка, после взаимодействия с хлором, содержит 10 электронов. Таким образом, натрий будет иметь 11 положительно заряженных частиц и 10 отрицательно заряженных частиц. По простейшему уравнению: +11 – 10 = +1, становится ясно, откуда взялся положительный заряд.
Аналогичный расчет можно привести и для хлора. После взаимодействия с натрием ядро атома хлора не изменяется, оно содержит 17 положительно заряженных частиц (протонов), а оболочка – 18 отрицательно заряженных частиц (электронов). +17 – 18 = ‒1.
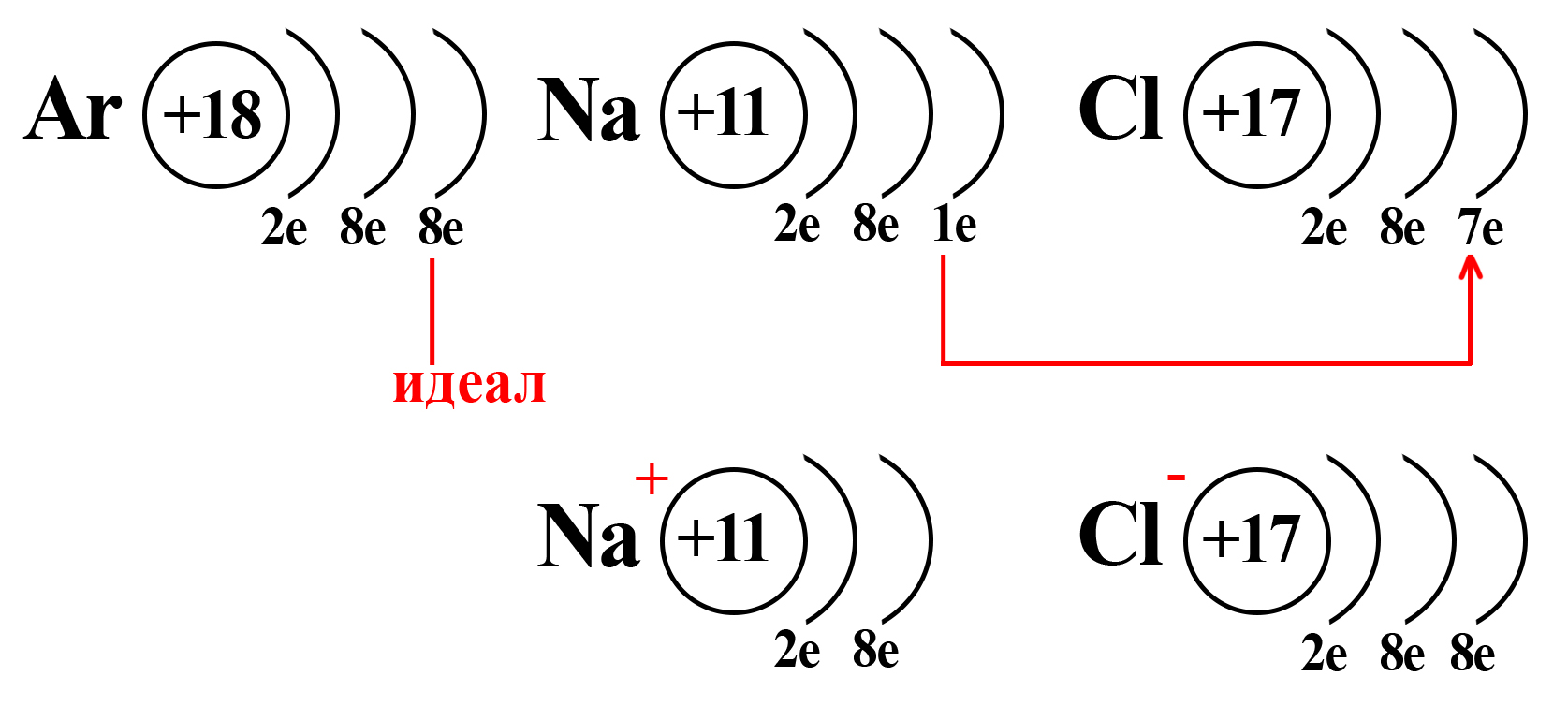
Полученные заряды и являются степенями окисления.
Также степень окисления можно выразить количеством электронов, которые иону нужно получить или отдать для того, чтобы стать электронейтральным атомом. Так, катион натрия, имеющий заряд «+1», должен получить 1 электрон, чтобы превратиться в атом натрия: Na+ +1ē = Na0. А анион хлора (хлорид-ион), имеющий заряд «‒1» должен отдать один электрон: Cl– -1ē = Cl0.
Для упрощения понятие «степень окисления» применяется не только для веществ с ионным строением (металл + неметалл), но и для веществ с ковалентными полярными связями. Несмотря на то, что в таком типе связи полного перехода электронов от одного атома к другому не происходит, полученные частичные заряды превращаются в целые.
Постоянные степени окисления.
Знания этой простой, базовой темы помогут Вам решать не только тестовые задания. Одно из самых сложных заданий ЕГЭ – расстановка коэффициентов с помощью электронного баланса – не решается без знания степеней окисления.
Таблица «Элементы, имеющие постоянную степень окисления»
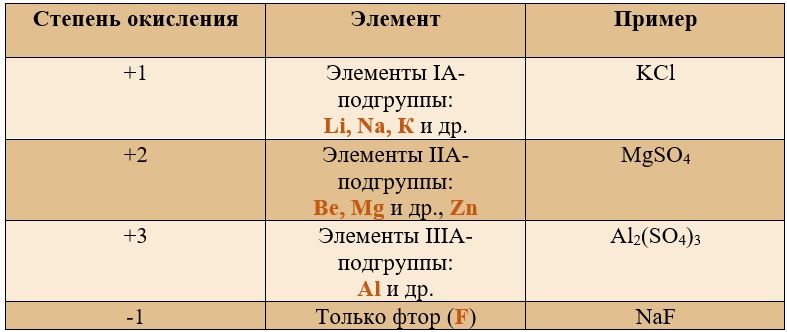
Таблица «Наиболее популярные степени окисления у остальных элементов» (Выделены бурым)*
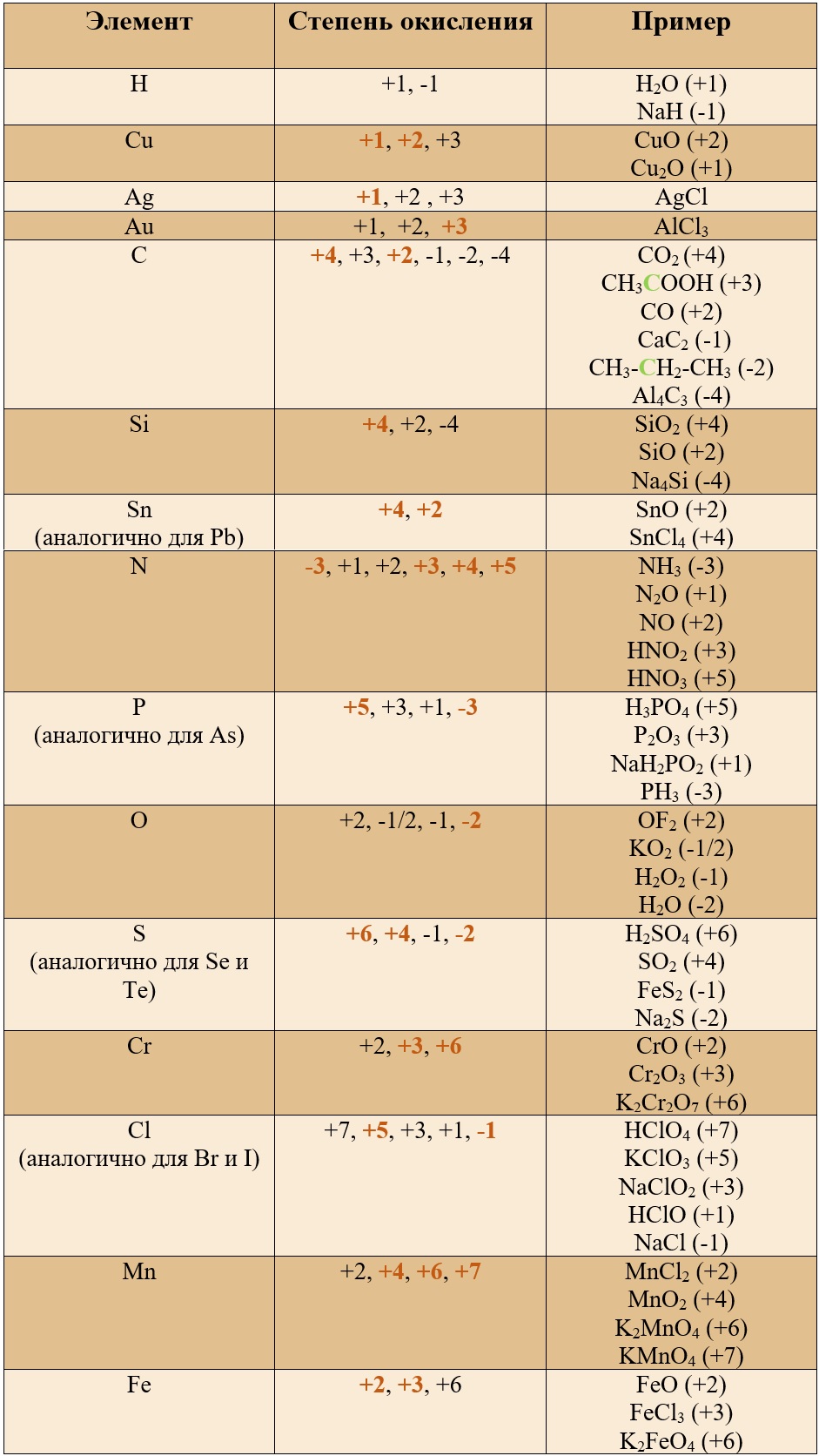
*В таблице указаны не все возможные степени окисления.
Таким образом, медь, серебро, золото и железо не проявляют высшей степени окисления, равной номеру группы, у остальных же элементов высшая степень окисления равна номеру группы.
Для определения степени окисления не нужно учить всю таблицу, и тем более все степени окисления. Они приведены для справки, наиболее важными являются:
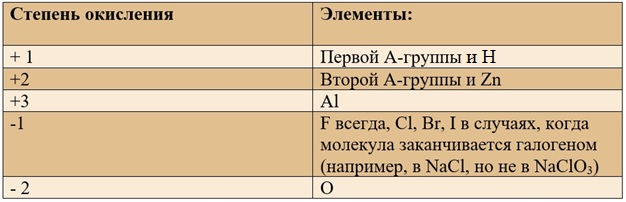
Определение степеней окисления в бинарных соединениях
Для примера возьмём оксид фосфора (P2O5)
- Определим степень окисления известного элемента (в нашем случае это кислород).

- Условно разделим молекулу на две части: чаще всего первая часть молекулы положительная, а вторая – отрицательная (искл: NH3 и PH3).

- Индекс после кислорода указывает на, что в молекуле содержится пять атомов кислорода, каждый из них имеет степень окисления «-2», поэтому общее количество отрицательных зарядов будет равно «-10».
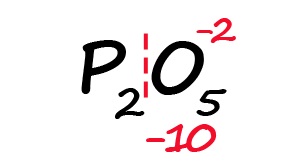
- Молекула должна быть электронейтральной, то есть количество положительных и отрицательных зарядов должны быть равными. Из этого следует, что все атомы фосфора в данной молекуле в сумме должны иметь десять положительных зарядов.
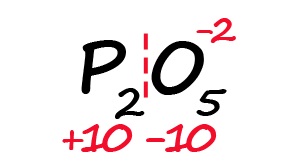
- Индекс «2» после фосфора означает, что в молекуле содержится два атома фосфора, между которыми поровну нужно разделить общий положительный заряд (+10:2=+5)
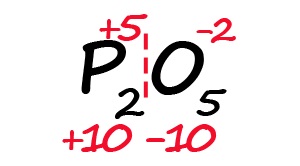
Аналогичным образом происходит определение степени окисления в более сложных веществах, для примера возьмём перманганат калия (KMnO4):
- Подпишем степени окисления для элементов, имеющих постоянные их значения:

- Разделим молекулу на положительный и отрицательный «полюс» (в соединениях, состоящих из атомов трех элементов, чаще всего первые два являются положительными, а третий – отрицательным).

- Посчитаем общее количество положительных и отрицательных зарядов с учетом индексов:
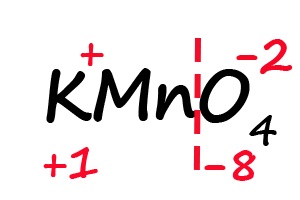
- Ответим на вопрос: какого количества плюсов не хватает, что бы положительные и отрицательные заряды имели одинаковое значение? До +8 не хватает семи положительных зарядов, откуда следует, что степень окисления марганца равна «+7».
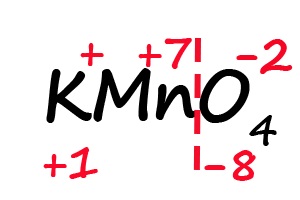
Ну и напоследок разберем степени окисления элементов в дихромате калия (K2Cr2O7):
- Подписываем известные степени окисления:
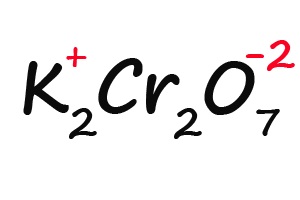
- Делим молекулу на положительную и отрицательную части:
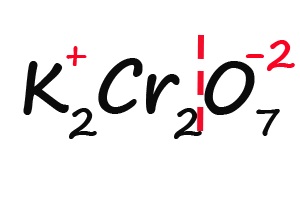
- Считаем общее количество «плюсов» и «минусов»:
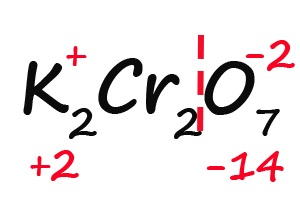
- Подсчитываем, сколько положительных зарядов не достает для того, чтобы молекула стала электронейтральной (т. е. такой молекулой, в которой количество положительных и отрицательных зарядов было одинаковым):
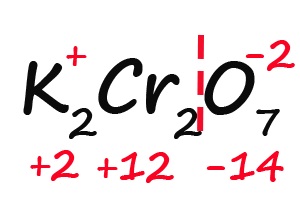
- Так как молекула содержит два атома хрома, двенадцать положительных зарядов должны распределиться между ними поровну, то есть, каждый хром имеет заряд +6:
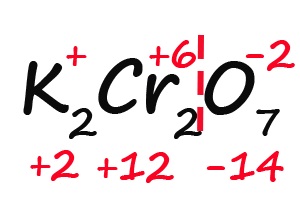
Как быть, если в формуле встретились скобки? Например, как посчитать степень окисления брома в пербромате кальция?

- Для начала определим все известные степени окисления, как делали в предыдущих примерах:
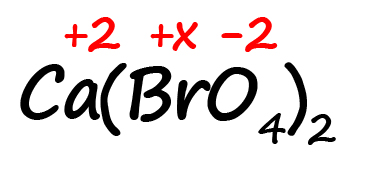
- Посчитаем сумму положительных и отрицательных зарядов. Важно учесть все индексы. Помните, что индекс. Расположенный за атомом действует только на этот атом, а индекс, расположенный за скобкой, действует на всё содержимое скобок:
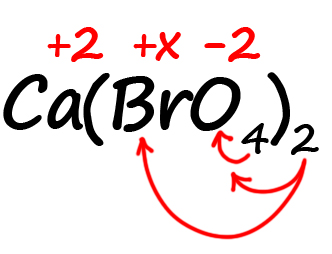
Таким образом, в пербромате кальция содержится: один атом кальция, два атома брома и 8 атомов кислорода (индексы, относящиеся к одному и тому же атому перемножаются).
Следовательно, мы имеем два положительных заряда от кальция и шестнадцать отрицательных от кислорода. Так как индекс «2» за скобками действует и на бром, его заряд можно выразить как 2х.
Получаем уравнение:
2 + 2х ‒ 16 = 0
2х = 14
х = 7
Степень окисления брома в пербромате кальция равна «+7».








