Строение атома кислорода

4.5
Средняя оценка: 4.5
Всего получено оценок: 334.
4.5
Средняя оценка: 4.5
Всего получено оценок: 334.
Кислород (O) – жизненно важный газ, необходимый для дыхания, поддержания горения, окисления. Относится к группе халькогенов. Самый распространённый на Земле элемент. Строение атома кислорода позволяет ему соединяться с металлами и неметаллами, образуя оксиды.
Строение
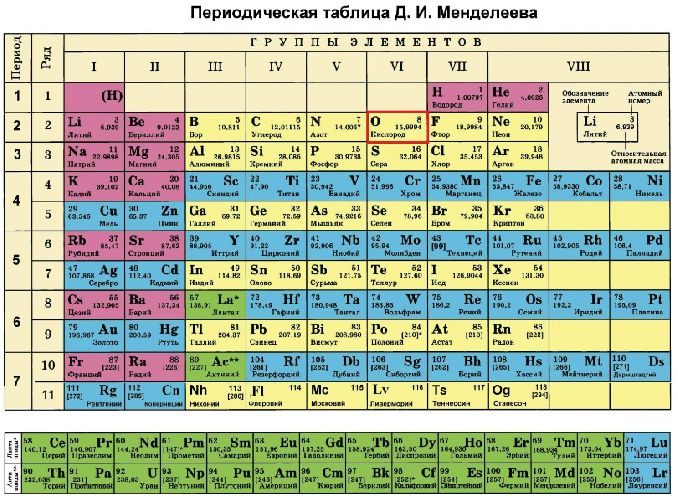
По положению в периодической таблице Менделеева можно определить строение атома элемента кислорода. Это восьмой элемент, расположенный в VI группе, втором периоде. Относительная атомная масса – 16. Существует три изотопа элемента:
- 16O;
- 17O;
- 18O.
Наиболее распространён 16O.
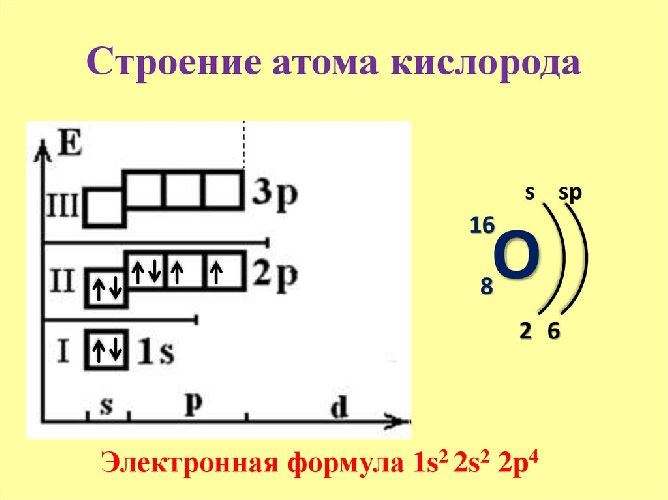
Электронная конфигурация атома кислорода – 1s22s22p4. Ядро атома кислорода имеет заряд +8. Кислород относится к элементам р-семейства. На внешнем энергетическом уровне находится шесть валентных электронов. Два спаренных электрона находится на 2s-орбитали. На 2р-уровне находится два спаренных и два неспаренных электрона, поэтому во всех соединениях кислород проявляет вторую валентность.
Молекула кислорода имеет два атома – О2. При присоединении ещё одного атома образуется озон – О3.
Физические свойства
Кислород – бесцветный и безвкусный газ, плохо растворимый в воде и спирте. Хорошо растворим в жидком серебре. В сжиженном виде приобретает светло-голубой цвет, в твёрдом – синий. Занимает 21 % атмосферного воздуха.
Кислород поддерживает горение, поэтому его легко обнаружить с помощью тлеющей лучины (вспыхивает).
Химические свойства
Благодаря электронному строению обладает высокой степенью окисления. Однако большую активность проявляет при нагревании из-за прочных двойных связей между атомами. При комнатной температуре быстро реагирует с наиболее активными элементами – щелочными и щелочноземельными металлами, некоторыми неметаллами.
Соединяясь с элементами, образует оксиды. Окисляет органические вещества. Примеры реакций с простыми веществами:
- K + O2 → KO2;
- 3Fe + 2O2 → Fe3O4;
- S + O2 → SO2.
С фосфором, серой, углеродом (графитом), водородом кислород реагирует при нагревании:
- 4Р + 5О2 → 2Р2О5;
- S + O2 → SO2;
- С + О2 → СО2;
- 2Н2 + О2 → 2Н2О.
Быстро пропуская фтор через щёлочь, получают реакцию кислорода с фтором:
2F2 + 2NaOH → 2NaF + H2O + OF2.
Кислород с фтором непосредственно взаимодействует при электрическом разряде. В этом случае кислород играет роль восстановителя:
O2 + F2 → F2O2.
Кислород реагирует со сложными веществами, образуя оксиды:
- 2CuS + 3O2 → 2CuO + 2SO2;
- 2H2S + 3O2 → 2SO2 + 2H2O;
- 2C6H6 + 15O2 → 12CO2 + 6H2O;
- CH4 + 2O2 → CO2 + 2H2O.
Кислород не реагирует с золотом и инертными газами. Взаимодействие с галогенами происходит в условиях ультрафиолета или электрического тока.
Что мы узнали?
Кислород – распространённый в природе бесцветный газ. Схема строения атома – +8 О)2)6. Кислород всегда проявляет валентность II за счёт двух неспаренных электронов. Кислород – сильный окислитель, проявляющий в некоторых реакциях свойства восстановителя. Взаимодействует с металлами и неметаллами, сложными неорганическими и органическими веществами. Наибольшую активность проявляет при нагревании. Не реагирует с благородными газами и золотом.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
-
Александр Котков
5/5
-
Мила Кондратьева
5/5
-
Семён Гольдфарб
5/5
-
Александр Котков
5/5
Оценка доклада
4.5
Средняя оценка: 4.5
Всего получено оценок: 334.
А какая ваша оценка?
Строение
По положению в периодической таблице Менделеева можно определить строение атома элемента кислорода. Это восьмой элемент, расположенный в VI группе, втором периоде. Относительная атомная масса – 16. Существует три изотопа элемента:
- 16O;
- 17O;
- 18O.
Наиболее распространён 16O.
Электронная конфигурация атома кислорода – 1s22s22p4. Ядро атома кислорода имеет заряд +8. Кислород относится к элементам р-семейства. На внешнем энергетическом уровне находится шесть валентных электронов. Два спаренных электрона находится на 2s-орбитали. На 2р-уровне находится два спаренных и два неспаренных электрона, поэтому во всех соединениях кислород проявляет вторую валентность.
Молекула кислорода имеет два атома – О2. При присоединении ещё одного атома образуется озон – О3.
Видео
Физические свойства
Кислород – бесцветный и безвкусный газ, плохо растворимый в воде и спирте. Хорошо растворим в жидком серебре. В сжиженном виде приобретает светло-голубой цвет, в твёрдом – синий. Занимает 21 % атмосферного воздуха.
Рис. 3. Твёрдый кислород.
Кислород поддерживает горение, поэтому его легко обнаружить с помощью тлеющей лучины (вспыхивает).
Электронное строение атома кислорода
Атом кислорода имеет две оболочки, как и все элементы, расположенные во втором периоде. Номер группы –VI (халькогены) – свидетельствует о том, что на внешнем электронном уровне атома азота находится 6 валентных электронов. Обладает высокой окислительной способностью (выше только у фтора).
Рис. 1. Схематичное изображение строения атома кислорода.
Электронная конфигурация основного состояния записывается следующим образом:
1s22s22p4.
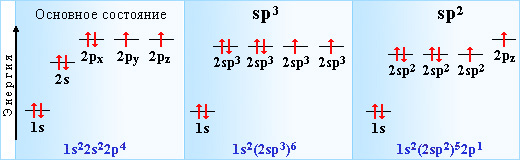
Кислород – элемент p-семейства. Энергетическая диаграмма для валентных электронов в невозбужденном состоянии выглядит следующим образом:
У кислорода есть 2 пары спаренных электронов и два неспаренных электрона. Во всех своих соединениях кислород проявляет валентность II.
Рис. 2. Пространственное изображение строения атома кислорода.
Получение и применение
Благодаря наличию свободного кислорода в атмосфере наиболее эффективным методом его извлечения является сжижение воздуха, из которого удаляют примеси, CO2, пыль и т.д. химическими и физическими методами. Циклический процесс включает сжатие, охлаждение и расширение, что и приводит к сжижению воздуха. При медленном подъеме температуры (метод фракционной дистилляции) из жидкого воздуха испаряются сначала благородные газы (наиболее трудно сжижаемые), затем азот и остается жидкий кислород. В результате жидкий кислород содержит следы благородных газов и относительно большой процент азота. Для многих областей применения эти примеси не мешают. Однако для получения кислорода особой чистоты процесс дистилляции необходимо повторять. Кислород хранят в танках и баллонах. Он используется в больших количествах как окислитель керосина и других горючих в ракетах и космических аппаратах. Сталелитейная промышленность потребляет газообразный кислород для продувки через расплав чугуна по методу Бессемера для быстрого и эффективного удаления примесей C, S и P. Сталь при кислородном дутье получается быстрее и качественнее, чем при воздушном. Кислород используется также для сварки и резки металлов (кислородно-ацетиленовое пламя). Применяют кислород и в медицине, например, для обогащения дыхательной среды пациентов с затрудненном дыханием. Кислород можно получать различными химическими методами, и некоторые из них применяют для получения малых количеств чистого кислорода в лабораторной практике.
Строение атома
Также по теме:
Любой природный атом кислорода содержит 8 протонов в ядре, но число нейтронов может быть равно 8, 9 или 10. Наиболее распространенный из трех изотопов кислорода (99,76%) – это 168O (8 протонов и 8 нейтронов). Содержание другого изотопа, 188O (8 протонов и 10 нейтронов), составляет всего 0,2%. Этот изотоп используется как метка или для идентификации некоторых молекул, а также для проведения биохимических и медико-химических исследований (метод изучения нерадиоактивных следов). Третий нерадиоактивный изотоп кислорода 178O (0,04%) содержит 9 нейтронов и имеет массовое число 17. После того как в 1961 масса изотопа углерода 126C была принята Международной комиссией за стандартную атомную массу, средневзвешенная атомная масса кислорода стала равна 15,9994. До 1961 стандартной единицей атомной массы химики считали атомную массу кислорода, принятую для смеси трех природных изотопов кислорода равной 16,000. Физики за стандартную единицу атомной массы принимали массовое число изотопа кислорода 168O, поэтому по физической шкале средняя атомная масса кислорода составляла 16,0044 (см. также АТОМНАЯ МАССА).
В атоме кислорода 8 электронов, при этом 2 электрона находятся на внутреннем уровне, а 6 электронов – на внешнем. Поэтому в химических реакциях кислород может принимать от доноров до двух электронов, достраивая свою внешнюю оболочку до 8 электронов и образуя избыточный отрицательный заряд (см. также АТОМА СТРОЕНИЕ).
Атомы кислорода в соединениях проявляют валентность II, I.
Валентность кислорода характеризует способность атома O к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Получение кислорода
1. Промышленный способ — перегонка жидкого воздуха и электролиз воды:
2Н2О → 2Н2 + О2
2. В лаборатории кислород получают: 1.Электролизом щелочных водных растворов или водных растворов кислородосодержащих солей (Na2SO4 и др.)
2. Термическим разложением перманганата калия KMnO4: 2KMnO4 = K2MnO4 + MnO2 + O2↑,
Бертолетовой соли KClO3: 2KClO3 = 2KCl + 3O2↑ (катализатор MnO2)
Оксида марганца (+4) MnO2: 4MnO2 = 2Mn2O3 + O2↑ (700 oC),
3MnO2 = 2Mn3O4 + O2↑ (1000 oC),
Пероксид бария BaO2 : 2BaO2 = 2BaO + O2↑
3. Разложением пероксида водорода: 2H2O2 = H2O + O2↑ (катализатор MnO2)
4. Разложение нитратов: 2KNO3 → 2KNO2 + O2
На космических кораблях и подводных лодках кислород получают из смеси K2O2 и K2O4: 2K2O4 + 2H2O = 4KOH +3O2↑ 4KOH + 2CO2 = 2K2CO3 + 2H2O
Суммарно: 2K2O4 + 2CO2 = 2K2CO3 + 3О2 ↑
Когда используют K2O2, то суммарная реакция выглядит так: 2K2O2 + 2CO2 = 2K2CO3 + O2 ↑
Если смешать K2O2 и K2O4 в равномолярных (т.е. эквимолярных) количествах, то на 1 моль поглощенного СО2 выделится один моль О2.
Что мы узнали?
Кислород – распространённый в природе бесцветный газ. Схема строения атома – +8 О)2)6. Кислород всегда проявляет валентность II за счёт двух неспаренных электронов. Кислород – сильный окислитель, проявляющий в некоторых реакциях свойства восстановителя. Взаимодействует с металлами и неметаллами, сложными неорганическими и органическими веществами. Наибольшую активность проявляет при нагревании. Не реагирует с благородными газами и золотом.
Теги
Электронное строение атома кислорода
Электронное строение нейтрального атома кислорода в основном состоянии.
Схема строения электронных оболочек
Распределение электронов по энергетическим уровням (или по электронным слоям) в атоме кислорода.
O
+8
2
6
Электронно-графическая схема
Распределение электронов по атомным орбиталям в атоме кислорода.
| 2 | ↑↓ | ↑↓ | ↑ | ↑ | ||
| 1 | ↑↓ | |||||
| s | p |
Валентные орбитали атома кислорода выделены фиолетовым цветом.
Электронная конфигурация
Полная электронная конфигурация атома кислорода.
8O 1s2 2s2 2p4
Сокращённая электронная конфигурация атома кислорода.
8O [He] 2s2 2p4
Квантовые числа валентных электронов
Главное (n), орбитальное (l), магнитное (m) и спиновое (s) квантовые числа валентных электронов атома кислорода.
| Орбиталь | Квантовое число | |||
|---|---|---|---|---|
| n | l | m | s | |
| 2s | 2 | 0 | 0 | +½ |
| -½ | ||||
| 2p | 2 | 1 | -1 | +½ |
| -½ | ||||
| 1 | +½ | |||
| 2 | +½ |
O (кислород) – элемент с прядковым номером 8 в периодической системе.
Находится во II периоде. Температура плавления: -218.4 ℃. Плотность: 0.00133 г/см3.
Электронная формула атома кислорода:
1s2 2s2 2p4
Сокращенная электронная конфигурация O:
[He] 2s2 2p4
Ниже приведена электронно-графическая схема атома кислорода
Распределение электронов по энергетическим уровням в атоме O
1-й уровень (K): 2
2-й уровень (L): 6
Валентные электроны кислорода
Количество валентных электронов в атоме кислорода – 6.
Ниже приведены их квантовые числа (N – главное, L – орбитальное, M – магнитное, S – спин)
| Орбиталь | N | L | M | S |
|---|---|---|---|---|
| s | 2 | 0 | 0 | +1/2 |
| s | 2 | 0 | 0 | -1/2 |
| p | 2 | 1 | -1 | +1/2 |
| p | 2 | 1 | 0 | +1/2 |
| p | 2 | 1 | 1 | +1/2 |
| p | 2 | 1 | -1 | -1/2 |
Степени окисления, которые может проявлять кислород: -2, -1, +1, +2
Строение атома кислорода
Кислород – элемент VIА группы 2-го периода Периодической системы элементов; атомый номер 8; атомная масса 16; электроотрицательность 3,5. Электронная конфигурация в основном состоянии 1s22s22p4.
В различных соединениях кислород может находиться в состояниях sp3 и sp2-гибридизации.
sp3-Атом кислорода содержат молекулы и ионы, строение которых можно показать с помощью атомно-орбитальных моделей (часть I):
sp2-Гибридизованный атом кислорода присутствует в соединениях с карбонильной группой >С=О:
Например:
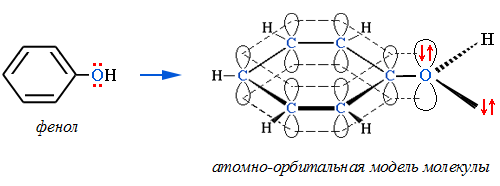
Кроме того, кислород в sp2-состоянии может быть и в группах ОН или ОR, если они связаны с sp2-атомом углерода (или другого элемента). В этом случае негибридизованная p-орбиталь атома кислорода содержит неподеленную пару электронов. Например, в феноле C6H5OH: