Содержание:
Температура:
Перед тем как, например, пойти на пляж, многие интересуются прогнозом погоды. И если ожидается температура воздуха 10 °С, то, скорее всего, планы будут изменены. А стоит ли отказываться от прогулки, если прогнозируется температура 300 К (кельвинов)? И что на самом деле вкладывают физики в понятие «температура»?

Что такое температура
Эксперименты показывают, что макроскопическая система может переходить из одного состояния в другое. Например, если в морозный день занести в комнату шарик, наполненный гелием, то гелий в шарике будет нагреваться и при этом будут изменяться давление, объем и некоторые другие параметры газа. После того как шарик пробудет в комнате некоторое время, изменения прекратятся. Один из постулатов молекулярной физики и термодинамики — его еще называют нулевое начало термодинамики — гласит: любое макроскопическое тело или система тел при неизменных внешних условиях самопроизвольно переходит в термодинамическое равновесное состояние (состояние теплового равновесия), после достижения которого все части системы имеют одинаковую температуру. Нулевое начало термодинамики фактически вводит и определяет понятие температуры.
Температура — физическая величина, характеризующая состояние теплового равновесия макроскопической системы.
Состояние теплового равновесия — это такое состояние макроскопической системы, при котором все макроскопические параметры системы остаются неизменными сколь угодно долго.
В состоянии теплового равновесия все части системы имеют одинаковую температуру; другие макроскопические параметры неизменны, но могут быть разными. Вспомните пример с шариком: после того как установится тепловое равновесие, температура окружающего воздуха и температура гелия в шарике будут одинаковыми, а давление, плотность и объем — разными.
Как работают термометры
Температура — это физическая величина, и ее можно измерять. Для этого нужно установить шкалу температур. Самые распространенные температурные шкалы — шкалы Цельсия, Кельвина, Фаренгейта (рис. 29.1).
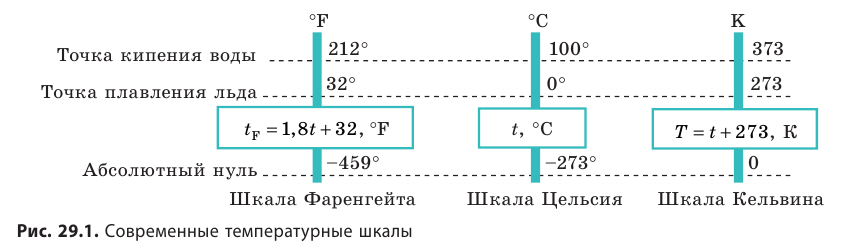
Построение шкалы температур начинается с выбора реперных (опорных) точек, которые должны быть однозначно связаны с какими-либо физическими процессами, которые легко воспроизвести. Например, за нулевую точку температурной шкалы Цельсия принята температура таяния льда при нормальном атмосферном давлении ( t = 0 °С). Температуре кипения воды при нормальном атмосферном давлении приписывают значение t =100 °С. Единица температуры по шкале Цельсия — градус Цельсия: 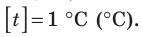 .
.

Рис. 29.2. различные виды термометров: а — жидкостный (принцип действия: изменение объема жидкости при изменении температуры); б — термометр сопротивления (изменение электрического сопротивления проводника при изменении температуры); в — биметаллический деформационный (изменение длин двух разных металлических пластин при изменении температуры)
Приборы для измерения температуры — термометры (рис. 29.2). Основные части любого термометра — термометрическое тело (ртуть или спирт в жидкостном термометре, биметаллическая пластина в металлическом деформационном термометре и т. д.) и шкала. Если термометрическое тело привести в контакт с телом, температуру которого нужно измерить, система придет в неравновесное состояние. При переходе в равновесное состояние будут изменяться некоторые параметры термометрического тела (объем, сопротивление и т. п.). Зная, как эти параметры зависят от температуры, определяют температуру тела.
Обратите внимание!
- Термометр фиксирует собственную температуру, равную температуре тела, с которым термометр находится в термодинамическом равновесии.
- Термометрическое тело не должно быть массивным, иначе оно существенно изменит температуру тела, с которым контактирует.
Температура и средняя кинетическая энергия молекул
То, что температура тела должна быть связана с кинетической энергией его молекул, следует из простых соображений. Например, с увеличением температуры увеличивается скорость движения броуновских частиц, ускоряется диффузия, повышается давление газа, а это значит, что молекулы движутся быстрее и их кинетическая энергия становится больше. Можно предположить: если газы находятся в состоянии теплового равновесия, средние кинетические энергии молекул этих газов одинаковы. Но как это доказать, ведь непосредственно измерить эти энергии невозможно?
Обратимся к основному уравнению МКТ идеального газа: 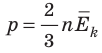 . По определению
. По определению 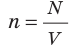 , поэтому
, поэтому 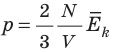 . После преобразований получим:
. После преобразований получим: 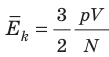 .
.
Таким образом, чтобы экспериментально убедиться в равенстве средних кинетических энергий молекул различных газов при одинаковой температуре, нужно измерить объемы (V), давления (p) и массы (m) газов и, зная их молярную массу (M), найти число молекул каждого газа (N) по формуле 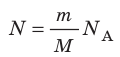 .
.
Чтобы обеспечить одинаковую температуру, можно, например, погрузить баллоны с различными газами в сосуд с водой и дождаться состояния теплового равновесия (рис. 29.3).
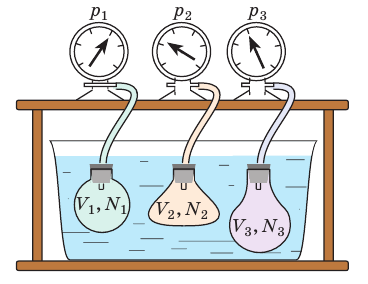
Рис. 29.3. опыт, позволяющий установить связь между температурой и средней кинетической энергией поступательного движения молекул газа. Газы в сосудах находятся в состоянии теплового равновесия со средой, а следовательно, и друг с другом
Эксперименты показывают, что для всех газов в состоянии теплового равновесия отношение 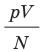 одинаково, а следовательно, одинаковыми являются и средние кинетические энергии молекул газов. (Отношение
одинаково, а следовательно, одинаковыми являются и средние кинетические энергии молекул газов. (Отношение 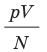 часто обозначают символом θ (тета).)
часто обозначают символом θ (тета).)
Например, при температуре 0 °С (сосуды с газами погрузили в тающий лед) 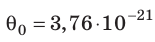 , Дж, то есть
, Дж, то есть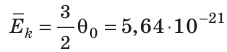 Дж; при температуре 100 °С (сосуды погрузили в кипящую воду)
Дж; при температуре 100 °С (сосуды погрузили в кипящую воду) 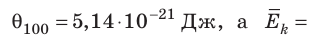
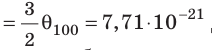 Дж. Так как в состоянии теплового равновесия значение θ для любых газов одинаково, то температуру можно измерять в джоулях.
Дж. Так как в состоянии теплового равновесия значение θ для любых газов одинаково, то температуру можно измерять в джоулях.
Абсолютная шкала температур
Понятно, что в джоулях представлять температуру неудобно (прежде всего потому, что значения θ очень малы), к тому же неудобно полностью отказываться от шкалы Цельсия. В 1848 г. английский физик Уильям Томсон (лорд Кельвин) (1824–1907) предложил абсолютную шкалу температур (сейчас ее называют шкалой Кельвина).
Температуру Т, измеренную по шкале кельвина, называют абсолютной температурой.
Единица абсолютной температуры — кельвин — основная единица СИ: [T] = 1 К (К).
Шкала Кельвина построена следующим образом:
- изменение температуры по шкале Кельвина равно изменению температуры по шкале Цельсия: ∆ = T t ∆ , то есть цена деления шкалы Кельвина равна цене деления шкалы Цельсия: 1 °С = 1 К; температуры, измеренные по шкалам Кельвина и Цельсия, связаны соотношениями:
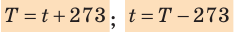
- температура по шкале Кельвина связана с величиной
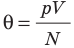 соотношением θ = kT, где k — постоянная Больцмана — коэффициент пропорциональности, не зависящий ни от температуры, ни от состава и количества газа:
соотношением θ = kT, где k — постоянная Больцмана — коэффициент пропорциональности, не зависящий ни от температуры, ни от состава и количества газа: 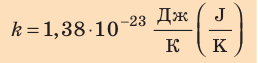
- абсолютная температура имеет глубокий физический смысл: средняя кинетическая энергия поступательного движения молекул идеального газа прямо пропорциональна абсолютной температуре:
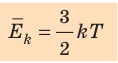 (1) То есть, если газ охладить до температуры T= 0 К, движение его молекул должно прекратиться (
(1) То есть, если газ охладить до температуры T= 0 К, движение его молекул должно прекратиться (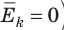 ). Таким образом, нулевая точка шкалы Кельвина — это самая низкая теоретически возможная температура. На самом деле движение молекул не прекращается никогда, поэтому достичь температуры 0 К (–273 °С) невозможно.
). Таким образом, нулевая точка шкалы Кельвина — это самая низкая теоретически возможная температура. На самом деле движение молекул не прекращается никогда, поэтому достичь температуры 0 К (–273 °С) невозможно.
Абсолютный нижний предел температуры, при котором движение молекул и атомов должно прекратиться, называют абсолютным нулем температуры. Давление p газа полностью определяется его абсолютной температурой T и концентрацией n молекул газа: p=nkT (2).
Выводы:
- Физическая величина, характеризующая состояние теплового равновесия макроскопической системы, называется температурой. Абсолютный нижний предел температуры, при котором движение молекул и атомов должно прекратиться, называют абсолютным нулем температуры. Шкала, за нулевую точку которой взят абсолютный нуль температуры, называется абсолютной шкалой температур (шкалой Кельвина). Единица абсолютной температуры — кельвин (К) — основная единица СИ. Температуры по шкале Кельвина и Цельсия связаны соотношением: T=t + 273; t=T – 273.
- Средняя кинетическая энергия поступательного движения молекул идеального газа прямо пропорциональна абсолютной температуре, а давление газа определяется абсолютной температурой и концентрацией молекул газа:
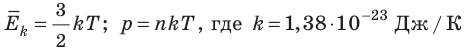 — постоянная Больцмана.
— постоянная Больцмана.
- Парообразование и конденсация
- Тепловое равновесие в физике
- Изопроцессы в физике
- Твердые тела и их свойства в физике
- Механизмы, работающие на основе правила моментов
- Идеальный газ в физике
- Уравнение МКТ идеального газа
- Уравнение состояния идеального газа
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 сентября 2021 года; проверки требуют 15 правок.

Рисунок термометра, сделанный самим Цельсием, из статьи Observationer om twänne beständiga grader på en thermometer, 1742
Гра́дус Це́льсия (обозначение: °C или юникод символ U+2103 ℃) — широко распространённая единица температуры, применяемая в Международной системе единиц (СИ) наряду с кельвином[1]. Используется всеми странами, кроме США[2], Багамских Островов, Белиза, Каймановых Островов и Либерии.
Градус Цельсия назван в честь шведского учёного Андерса Цельсия, предложившего в 1742 году новую шкалу для измерения температуры[3].
Первоначальное определение градуса Цельсия зависело от определения стандартного атмосферного давления, потому что и температура кипения воды, и температура таяния льда зависят от этого параметра. Это не очень удобно для стандартизации единицы. Поэтому после принятия кельвина (K) в качестве основной единицы выражения температуры определение градуса Цельсия было пересмотрено.
Согласно современному определению, один градус Цельсия равен одному кельвину (K), а ноль шкалы Цельсия установлен таким образом, что температура тройной точки воды равна 0,01 °C. В итоге шкалы Цельсия и Кельвина сдвинуты на 273,15 единиц:
Терминология[править | править код]
В рамках Международной системы единиц (СИ) проводится различие между величиной «термодинамическая температура», выражаемой в кельвинах, и той величиной, которая выражается в градусах Цельсия. Основные международные и российские документы, содержащие описание единиц СИ и регламентирующие их использование, называют градус Цельсия не единицей температуры, а единицей температуры Цельсия (фр. température Celsius, англ. Celsius temperature). Этот термин используется в Брошюре СИ (фр. Brochure SI, англ. The SI Brochure), опубликованной Международным бюро мер и весов (МБМВ) и содержащей полное официальное описание СИ вместе с её толкованием. Он применяется в ГОСТ 8.417-2002 «Единицы физических величин» и в «Положении о единицах величин, допускаемых к применению в Российской Федерации», утверждённом Правительством РФ. В свою очередь температуру Цельсия (обозначение t) Брошюра СИ и ГОСТ 8.417-2002 определяют выражением t = T — T0, где T — термодинамическая температура, выражаемая в кельвинах, а T0 = 273,15 К[1][4][5].
В соответствии со сказанным градус Цельсия относится к производным единицам СИ, имеющим специальные наименования и обозначения.
История[править | править код]
В 1665 году голландский физик Христиан Гюйгенс вместе с английским физиком Робертом Гуком впервые предложили использовать в качестве отсчётных точек температурной шкалы точки таяния льда и кипения воды[6][неавторитетный источник][7].

В 1742 году шведский астроном, геолог и метеоролог Андерс Цельсий (1701–1744) на основе этой идеи разработал новую температурную шкалу. Первоначально в ней за ноль была принята точка кипения воды, а за 100 °C — температура замерзания воды (точка плавления льда). Позже, уже после смерти Цельсия, его современники и соотечественники ботаник Карл Линней и астроном Мортен Штремер использовали эту шкалу в перевёрнутом виде (за 0 °C стали принимать температуру таяния льда, а за 100 °C — кипения воды). В таком виде шкала и используется до нашего времени.
По одним сведениям, Цельсий сам перевернул свою шкалу по совету Штремера[8]. По другим сведениям, шкалу перевернул Карл Линней в 1745 году. А по третьим — шкалу перевернул преемник Цельсия Мортен Штремер, и в XVIII веке такой термометр был широко распространён под названием «шведский термометр», а в самой Швеции — под именем Штремера, но известнейший шведский химик Йёнс Якоб Берце́лиус в своём труде «Руководство по химии» назвал шкалу «Цельсиевой» и с тех пор стоградусная шкала стала носить имя Андерса Цельсия[6]. Однако чаще шкалу именовали просто стоградусной шкалой (англ. и фр. centigrade). Официально наименование градус Цельсия принято на IX Генеральной конференции по мерам и весам в 1948 году.
Цельсий в своей работе «Наблюдения двух фиксированных положений на термометре» (швед. Observationer om twänne beständiga grader på en thermometer) рассказал о своих экспериментах, показывающих, что температура таяния льда (0 °C) не зависит от давления. Он также определил с удивительной точностью, как температура кипения воды варьировалась в зависимости от атмосферного давления.
Он предположил, что отметку 100 °C (точку кипения воды) можно откалибровать, зная, на каком уровне относительно поверхности моря находится термометр.
Шкала Цельсия линейна в интервале от 0 до 100 °C и также линейно продолжается в области ниже 0 °C и выше 100 °C. Линейность является основной проблемой при точных измерениях температуры. Достаточно упомянуть, что классический термометр, заполненный водой, невозможно разметить для температур ниже 4 °C, так как в этом диапазоне вода начинает снова расширяться при охлаждении.
Некоторые основные температуры[править | править код]
| кельвин | градус Цельсия | градус Фаренгейта | |
|---|---|---|---|
| Абсолютный ноль | 0 K | −273,15 °C | −459,67 °F |
| Температура кипения жидкого азота | 77,4 K | −195,8 °C[9] | −320,3 °F |
| Сублимация (переход из твёрдого состояния в газообразное) сухого льда | 195,1 K | −78 °C | −108,4 °F |
| Точка пересечения шкал Цельсия и Фаренгейта | 233,15 K | −40 °C | −40 °F |
| Температура плавления льда | 273,1499 K | −0,0001 °C[10] | 31,99982 °F |
| Тройная точка воды | 273,16 K | 0,01 °C | 32,018 °F |
| Нормальная температура человеческого тела[11] | 310 K | 36,6 °C | 97,9 °F |
| Температура кипения воды при давлении в 1 атмосферу (101,325 кПа) | 373,1339 K | 99,9839 °C[10] | 211,971 °F |
Диаграмма перевода температур[править | править код]


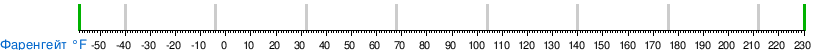





Примечания[править | править код]
- ↑ 1 2 Положение о единицах величин, допускаемых к применению в Российской Федерации. Архивная копия от 2 ноября 2013 на Wayback Machine Утверждено Постановлением Правительства РФ от 31 октября 2009 г. № 879
- ↑ Why Americans still use Fahrenheit long after everyone else switched to Celsius Архивная копия от 6 апреля 2019 на Wayback Machine // vox.com.
- ↑ Дойников А. С. Цельсия шкала // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1999. — Т. 5: Стробоскопические приборы — Яркость. — С. 424. — 692 с. — 20 000 экз. — ISBN 5-85270-101-7.
- ↑ The International System of Units (SI) / Bureau International des Poids et Mesures. — Paris, 2006. — P. 114. — ISBN 92-822-2213-6. Архивная копия от 5 ноября 2013 на Wayback Machine (англ.)
- ↑ ГОСТ 8.417—2002. Государственная система обеспечения единства измерений. Единицы величин
- ↑ 1 2 Сайт «МАСТЕР КИТ» (недоступная ссылка). Журнал «Радиодело» 2005`04, статья «О Цельсии бедном замолвите слово», автор М. Лебедев.
- ↑ Заметка Архивная копия от 3 августа 2017 на Wayback Machine. Автор Н. Филипецкий
- ↑ Склярова Е. К., Дергоусова Т. Г., Жаров Л. В. Первые медицинские и фармацевтические приборы // История фармации: краткий курс. — Ростов н/Д : Фенкс, 2015. — С. 119. — (Шпаргалки).
- ↑ Lide, D.R., ed. (1990—1991). Handbook of Chemistry and Physics (Справочник по химии и физике). 71st ed. CRC Press. p. 4-22.
- ↑ 1 2 Температурные шкалы — Шкала Цельсия и Кельвин // Университет Алабамы в Хантсвилле (недоступная ссылка)
- ↑ Elert, Glenn (2005). Температура здорового человека Архивировано 26 сентября 2010 года. The Physics Factbook. Retrieved 2007-08-22.
Ссылки[править | править код]
- SI brochure, section 2.1.1.5 Архивная копия от 23 июня 2018 на Wayback Machine (англ.)
- Преобразование температур
- Онлайн-конвертор градусов Цельсия в другие системы счислений
From Wikipedia, the free encyclopedia
| degree Celsius | |
|---|---|

A thermometer calibrated in degrees Celsius |
|
| General information | |
| Unit system | SI |
| Unit of | temperature |
| Symbol | °C |
| Named after | Anders Celsius |
| Conversions | |
| x °C in … | … corresponds to … |
| SI base units | (x + 273.15) K |
| Imperial/US units | (9/5x + 32) °F |
The degree Celsius is the unit of temperature on the Celsius scale[1] (originally known as the centigrade scale outside Sweden),[2] one of two temperature scales used in the International System of Units (SI), the other being the Kelvin scale. The degree Celsius (symbol: °C) can refer to a specific temperature on the Celsius scale or a unit to indicate a difference or range between two temperatures. It is named after the Swedish astronomer Anders Celsius (1701–1744), who developed a variant of it in 1742. Before being renamed in 1948 to honour Celsius, the unit was called centigrade, from the Latin centum, which means 100, and gradus, which means steps. Most countries use this scale; the other major scale, Fahrenheit, is still used in the United States, some island territories, and Liberia. The Kelvin scale is of use in the sciences, with 0 K (−273.15 °C) representing absolute zero.
Since 1743, the Celsius scale has been based on 0 °C for the freezing point of water and 100 °C for the boiling point of water at 1 atm pressure. Prior to 1743 the values were reversed (i.e. the boiling point was 0 degrees and the freezing point was 100 degrees). The 1743 scale reversal was proposed by Jean-Pierre Christin.
By international agreement, between 1954 and 2019 the unit degree Celsius and the Celsius scale were defined by absolute zero and the triple point of water. After 2007, it was clarified that this definition referred to Vienna Standard Mean Ocean Water (VSMOW), a precisely defined water standard.[3] This definition also precisely related the Celsius scale to the scale of the kelvin, the SI base unit of thermodynamic temperature with symbol K. Absolute zero, the lowest temperature possible, is defined as being exactly 0 K and −273.15 °C. Until 19 May 2019, the temperature of the triple point of water was defined as exactly 273.16 K (0.01 °C).[4]
On 20 May 2019, the kelvin was redefined so that its value is now determined by the definition of the Boltzmann constant rather than being defined by the triple point of VSMOW. This means that the triple point is now a measured value, not a defined value. The newly-defined exact value of the Boltzmann constant was selected so that the measured value of the VSMOW triple point is exactly the same as the older defined value to within the limits of accuracy of contemporary metrology. The temperature in degree Celsius is now defined as the temperature in kelvins subtracted by 273.15,[5][6] meaning that a temperature difference of one degree Celsius and that of one kelvin are exactly the same,[7] and that the degree Celsius remains exactly equal to the kelvin (i.e., 0 °C remains exactly 273.15 K).
History[edit]

An illustration of Anders Celsius’s original thermometer. Note the reversed scale, where 100 is the freezing point of water and 0 is its boiling point.
In 1742, Swedish astronomer Anders Celsius (1701–1744) created a temperature scale that was the reverse of the scale now known as “Celsius”: 0 represented the boiling point of water, while 100 represented the freezing point of water.[8] In his paper Observations of two persistent degrees on a thermometer, he recounted his experiments showing that the melting point of ice is essentially unaffected by pressure. He also determined with remarkable precision how the boiling point of water varied as a function of atmospheric pressure. He proposed that the zero point of his temperature scale, being the boiling point, would be calibrated at the mean barometric pressure at mean sea level. This pressure is known as one standard atmosphere. The BIPM’s 10th General Conference on Weights and Measures (CGPM) in 1954 defined one standard atmosphere to equal precisely 1,013,250 dynes per square centimeter (101.325 kPa).[9]
In 1743, the Lyonnais physicist Jean-Pierre Christin, permanent secretary of the Academy of Lyon, inverted the Celsius scale so that 0 represented the freezing point of water and 100 represented the boiling point of water. Some credit Christin for independently inventing the reverse of Celsius’s original scale, while others believe Christin merely reversed Celsius’s scale.[10][11] On 19 May 1743 he published the design of a mercury thermometer, the “Thermometer of Lyon” built by the craftsman Pierre Casati that used this scale.[12][13][14]
In 1744, coincident with the death of Anders Celsius, the Swedish botanist Carl Linnaeus (1707–1778) reversed Celsius’s scale.[15] His custom-made “linnaeus-thermometer”, for use in his greenhouses, was made by Daniel Ekström, Sweden’s leading maker of scientific instruments at the time, whose workshop was located in the basement of the Stockholm observatory. As often happened in this age before modern communications, numerous physicists, scientists, and instrument makers are credited with having independently developed this same scale;[16] among them were Pehr Elvius, the secretary of the Royal Swedish Academy of Sciences (which had an instrument workshop) and with whom Linnaeus had been corresponding; Daniel Ekström [sv], the instrument maker; and Mårten Strömer (1707–1770) who had studied astronomy under Anders Celsius.
The first known Swedish document[17] reporting temperatures in this modern “forward” Celsius scale is the paper Hortus Upsaliensis dated 16 December 1745 that Linnaeus wrote to a student of his, Samuel Nauclér. In it, Linnaeus recounted the temperatures inside the orangery at the University of Uppsala Botanical Garden:
… since the caldarium (the hot part of the greenhouse) by the angle of the windows, merely from the rays of the sun, obtains such heat that the thermometer often reaches 30 degrees, although the keen gardener usually takes care not to let it rise to more than 20 to 25 degrees, and in winter not under 15 degrees …
Centigrade vis-à-vis Celsius[edit]

Countries that use Celsius (°C)
Countries that use both Celsius (°C) and Fahrenheit (°F)
Since the 19th century, the scientific and thermometry communities worldwide have used the phrase “centigrade scale” and temperatures were often reported simply as “degrees” or, when greater specificity was desired, as “degrees centigrade”, with the symbol °C.
In the French language, the term centigrade also means one hundredth of a gradian, when used for angular measurement. The term centesimal degree was later introduced for temperatures[18] but was also problematic, as it means gradian (one hundredth of a right angle) in the French and Spanish languages. The risk of confusion between temperature and angular measurement was eliminated in 1948 when the 9th meeting of the General Conference on Weights and Measures and the Comité International des Poids et Mesures (CIPM) formally adopted “degree Celsius” for temperature.[19][a]
While “Celsius” is the term commonly used in scientific work, “centigrade” remains in common use in English-speaking countries, especially in informal contexts.[20]
While in Australia from 1 September 1972, only Celsius measurements were given for temperature in weather reports/forecasts,[21] it was not until February 1985 that the weather forecasts issued by the BBC switched from “centigrade” to “Celsius”.[22]
Common temperatures[edit]
All phase transitions are at standard atmosphere. Figures are either by definition, or approximated from empirical measurements.
| Kelvin | Celsius | Fahrenheit | Rankine | |
|---|---|---|---|---|
| Absolute zero[A] | 0 K | −273.15 °C | −459.67 °F | 0 °R |
| Intersection of Celsius and Fahrenheit scales[A] | 233.15 K | −40 °C | −40 °F | 419.67 °R |
| Boiling point of water[b] | 373.1339 K | 99.9839 °C | 211.971 °F | 671.6410 °R |
| Boiling point of liquid nitrogen | 77.4 K | −195.8 °C[23] | −320.4 °F | 139.3 °R |
| Melting point of ice[24] | 273.1499 K | −0.0001 °C | 31.9998 °F | 491.6698 °R |
| Sublimation point of dry ice | 195.1 K | −78 °C | −108.4 °F | 351.2 °R |
| Room temperature[B][25] | 293.15 K | 20.0 °C | 68.0 °F | 527.69 °R |
| Average normal human body temperature[26] | 310.15 K | 37.0 °C | 98.6 °F | 558.27 °R |
- ^ a b Exact value, by SI definition of the kelvin
- ^ Exact value, by NIST standard definition
Name and symbol typesetting[edit]
The “degree Celsius” has been the only SI unit whose full unit name contains an uppercase letter since 1967, when the SI base unit for temperature became the kelvin, replacing the capitalized term degrees Kelvin. The plural form is “degrees Celsius”.[27]
The general rule of the International Bureau of Weights and Measures (BIPM) is that the numerical value always precedes the unit, and a space is always used to separate the unit from the number, e.g. “30.2 °C” (not “30.2°C” or “30.2° C”).[28] The only exceptions to this rule are for the unit symbols for degree, minute, and second for plane angle (°, ′, and ″, respectively), for which no space is left between the numerical value and the unit symbol.[29] Other languages, and various publishing houses, may follow different typographical rules.
Unicode character[edit]
Unicode provides the Celsius symbol at code point U+2103 ℃ DEGREE CELSIUS. However, this is a compatibility character provided for roundtrip compatibility with legacy encodings. It easily allows correct rendering for vertically written East Asian scripts, such as Chinese. The Unicode standard explicitly discourages the use of this character: “In normal use, it is better to represent degrees Celsius “°C” with a sequence of U+00B0 ° DEGREE SIGN + U+0043 C LATIN CAPITAL LETTER C, rather than U+2103 ℃ DEGREE CELSIUS. For searching, treat these two sequences as identical.”[30]
Temperatures and intervals[edit]
The degree Celsius is subject to the same rules as the kelvin with regard to the use of its unit name and symbol. Thus, besides expressing specific temperatures along its scale (e.g. “Gallium melts at 29.7646 °C” and “The temperature outside is 23 degrees Celsius”), the degree Celsius is also suitable for expressing temperature intervals: differences between temperatures or their uncertainties (e.g. “The output of the heat exchanger is hotter by 40 degrees Celsius”, and “Our standard uncertainty is ±3 °C”).[31] Because of this dual usage, one must not rely upon the unit name or its symbol to denote that a quantity is a temperature interval; it must be unambiguous through context or explicit statement that the quantity is an interval.[c] This is sometimes solved by using the symbol °C (pronounced “degrees Celsius”) for a temperature, and C° (pronounced “Celsius degrees”) for a temperature interval, although this usage is non-standard.[32] Another way to express the same is “40 °C ± 3 K”, which can be commonly found in literature.
Celsius measurement follows an interval system but not a ratio system; and it follows a relative scale not an absolute scale. For example, an object at 20 °C does not have twice the energy of when it is 10 °C; and 0 °C is not the lowest Celsius value. Thus, degrees Celsius is a useful interval measurement but does not possess the characteristics of ratio measures like weight or distance.[33]
Coexistence of Kelvin and Celsius scales[edit]
In science and in engineering, the Celsius scale and the Kelvin scale are often used in combination in close contexts, e.g. “a measured value was 0.01023 °C with an uncertainty of 70 μK”. This practice is permissible because the magnitude of the degree Celsius is equal to that of the kelvin. Notwithstanding the official endorsement provided by decision no. 3 of Resolution 3 of the 13th CGPM,[34] which stated “a temperature interval may also be expressed in degrees Celsius”, the practice of simultaneously using both °C and K remains widespread throughout the scientific world as the use of SI-prefixed forms of the degree Celsius (such as “μ°C” or “microdegrees Celsius”) to express a temperature interval has not been well adopted.
Melting and boiling points of water[edit]
| from Celsius | to Celsius | |
|---|---|---|
| Fahrenheit | x °C ≘ (x × 9/5 + 32) °F | x °F ≘ (x − 32) × 5/9 °C |
| Kelvin | x °C ≘ (x + 273.15) K | x K ≘ (x − 273.15) °C |
| Rankine | x °C ≘ (x + 273.15) × 9/5 °R | x °R ≘ (x − 491.67) × 5/9 °C |
| For temperature intervals rather than specific temperatures, 1 °C = 1 K = 9/5 °F = 9/5 °R Conversion between temperature scales |
The melting and boiling points of water are no longer part of the definition of the Celsius scale. In 1948, the definition was changed to use the triple point of water.[35] In 2005 the definition was further refined to use water with precisely defined isotopic composition (VSMOW) for the triple point. In 2019, the definition was changed to use the Boltzmann constant, completely decoupling the definition of the kelvin from the properties of water. Each of these formal definitions left the numerical values of the Celsius scale identical to the prior definition to within the limits of accuracy of the metrology of the time.
When the melting and boiling points of water ceased being part of the definition, they became measured quantities instead. This is also true of the triple point.
In 1948 when the 9th General Conference on Weights and Measures (CGPM) in Resolution 3 first considered using the triple point of water as a defining point, the triple point was so close to being 0.01 °C greater than water’s known melting point, it was simply defined as precisely 0.01 °C. However, later measurements showed that the difference between the triple and melting points of VSMOW is actually very slightly (< 0.001 °C) greater than 0.01 °C. Thus, the actual melting point of ice is very slightly (less than a thousandth of a degree) below 0 °C. Also, defining water’s triple point at 273.16 K precisely defined the magnitude of each 1 °C increment in terms of the absolute thermodynamic temperature scale (referencing absolute zero). Now decoupled from the actual boiling point of water, the value “100 °C” is hotter than 0 °C – in absolute terms – by a factor of exactly 373.15/273.15 (approximately 36.61% thermodynamically hotter). When adhering strictly to the two-point definition for calibration, the boiling point of VSMOW under one standard atmosphere of pressure was actually 373.1339 K (99.9839 °C). When calibrated to ITS-90 (a calibration standard comprising many definition points and commonly used for high-precision instrumentation), the boiling point of VSMOW was slightly less, about 99.974 °C.[36]
This boiling-point difference of 16.1 millikelvins between the Celsius scale’s original definition and the previous one (based on absolute zero and the triple point) has little practical meaning in common daily applications because water’s boiling point is very sensitive to variations in barometric pressure. For example, an altitude change of only 28 cm (11 in) causes the boiling point to change by one millikelvin.
See also[edit]
- Comparison of temperature scales
- Degree of frost
- Thermodynamic temperature
Notes[edit]
- ^ According to The Oxford English Dictionary (OED), the term “Celsius thermometer” had been used at least as early as 1797. Further, the term “The Celsius or Centigrade thermometer” was again used in reference to a particular type of thermometer at least as early as 1850. The OED also cites this 1928 reporting of a temperature: “My altitude was about 5,800 metres, the temperature was 28° Celsius.” However, dictionaries seek to find the earliest use of a word or term and are not a useful resource as regards to the terminology used throughout the history of science. According to several writings of Dr. Terry Quinn CBE FRS, Director of the BIPM (1988–2004), including “Temperature Scales from the early days of thermometry to the 21st century” (PDF). Archived from the original (PDF) on 26 December 2010. Retrieved 31 May 2016. (146 KiB) as well as Temperature (2nd Edition/1990/Academic Press/0125696817), the term Celsius in connection with the centigrade scale was not used whatsoever by the scientific or thermometry communities until after the CIPM and CGPM adopted the term in 1948. The BIPM was not even aware that “degree Celsius” was in sporadic, non-scientific use before that time. It is also noteworthy that the twelve-volume, 1933 edition of OED didn’t even have a listing for the word Celsius (but did have listings for both centigrade and centesimal in the context of temperature measurement). The 1948 adoption of Celsius accomplished three objectives:
- 1. All common temperature scales would have their units named after someone closely associated with them; namely, Kelvin, Celsius, Fahrenheit, Réaumur and Rankine.
- 2. Notwithstanding the important contribution of Linnaeus who gave the Celsius scale its modern form, Celsius’s name was the obvious choice because it began with the letter C. Thus, the symbol °C that for centuries had been used in association with the name centigrade could remain in use and would simultaneously inherit an intuitive association with the new name.
- 3. The new name eliminated the ambiguity of the term “centigrade”, freeing it to refer exclusively to the French-language name for the unit of angular measurement.
- ^ For Vienna Standard Mean Ocean Water at one standard atmosphere (101.325 kPa) when calibrated solely per the two-point definition of thermodynamic temperature. Older definitions of the Celsius scale once defined the boiling point of water under one standard atmosphere as being precisely 100 °C. However, the current definition results in a boiling point that is actually 16.1 mK less. For more about the actual boiling point of water, see VSMOW in temperature measurement. A different approximation uses ITS-90, which approximates the temperature to 99.974 °C
- ^ In 1948, Resolution 7 of the 9th CGPM stated, “To indicate a temperature interval or difference, rather than a temperature, the word ‘degree’ in full, or the abbreviation ‘deg’ must be used.” This resolution was abrogated in 1967/1968 by Resolution 3 of the 13th CGPM, which stated that [“The names “degree Kelvin” and “degree”, the symbols “°K” and “deg” and the rules for their use given in Resolution 7 of the 9th CGPM (1948),] …and the designation of the unit to express an interval or a difference of temperatures are abrogated, but the usages which derive from these decisions remain permissible for the time being.” Consequently, there is now wide freedom in usage regarding how to indicate a temperature interval. The most important thing is that one’s intention must be clear and the basic rule of the SI must be followed; namely that the unit name or its symbol must not be relied upon to indicate the nature of the quantity. Thus, if a temperature interval is, say, 10 K or 10 °C (which may be written 10 kelvins or 10 degrees Celsius), it must be unambiguous through obvious context or explicit statement that the quantity is an interval. Rules governing the expressing of temperatures and intervals are covered in the BIPM’s “SI Brochure, 8th edition” (PDF). (1.39 MiB).
References[edit]
- ^ “Celsius temperature scale”. Encyclopædia Britannica. Retrieved 19 February 2012.
Celsius temperature scale, also called centigrade temperature scale, scale based on 0 ° for the melting point of water and 100 ° for the boiling point of water at 1 atm pressure.
- ^ Helmenstine, Anne Marie (15 December 2014). “What Is the Difference Between Celsius and Centigrade?”. Chemistry.about.com. About.com. Retrieved 25 April 2020.
- ^ “Resolution 10 of the 23rd CGPM (2007)”. Retrieved 27 December 2021.
- ^ “SI brochure, section 2.1.1.5”. International Bureau of Weights and Measures. Archived from the original on 26 September 2007. Retrieved 9 May 2008.
- ^ “SI Brochure: The International System of Units (SI) – 9th edition”. BIPM. Retrieved 21 February 2022.
- ^ “SI base unit: kelvin (K)”. bipm.org. BIPM. Retrieved 5 March 2022.
- ^ “Essentials of the SI: Base & derived units”. Retrieved 9 May 2008.
- ^ Celsius, Anders (1742) “Observationer om twänne beständiga grader på en thermometer” (Observations about two stable degrees on a thermometer), Kungliga Svenska Vetenskapsakademiens Handlingar (Proceedings of the Royal Swedish Academy of Sciences), 3 : 171–180 and Fig. 1.
- ^ “Resolution 4 of the 10th meeting of the CGPM (1954)”.
- ^ Don Rittner; Ronald A. Bailey (2005): Encyclopedia of Chemistry. Facts On File, Manhattan, New York City. p. 43.
- ^ Smith, Jacqueline (2009). “Appendix I: Chronology”. The Facts on File Dictionary of Weather and Climate. Infobase Publishing. p. 246. ISBN 978-1-4381-0951-0.
1743 Jean-Pierre Christin inverts the fixed points on Celsius’ scale, to produce the scale used today.
- ^ Mercure de France (1743): MEMOIRE sur la dilatation du Mercure dans le Thermométre. Chaubert; Jean de Nully, Pissot, Duchesne, Paris. pp. 1609–1610.
- ^ Journal helvétique (1743): LION. Imprimerie des Journalistes, Neuchâtel. pp. 308–310.
- ^ Memoires pour L’Histoire des Sciences et des Beaux Arts (1743): DE LYON. Chaubert, París. pp. 2125–2128.
- ^ Citation: Uppsala University (Sweden), Linnaeus’ thermometer
- ^ Citation for Christin of Lyons: Le Moyne College, Glossary, (Celsius scale); citation for Linnaeus’s connection with Pehr Elvius and Daniel Ekström: Uppsala University (Sweden), Linnaeus’ thermometer; general citation: The Uppsala Astronomical Observatory, History of the Celsius temperature scale
- ^ Citations: University of Wisconsin–Madison, Linnæus & his Garden and; Uppsala University, Linnaeus’ thermometer
- ^ Comptes rendus des séances de la cinquième conférence générale des poids et mesures, réunie à Paris en 1913. Bureau international des poids et mesures. 1913. pp. 55, 57, 59. Retrieved 10 June 2021. p. 60:
…à la température de 20° centésimaux
- ^ “CIPM, 1948 and 9th CGPM, 1948”. International Bureau of Weights and Measures. Archived from the original on 5 April 2021. Retrieved 9 May 2008.
- ^ “centigrade, adj. and n.” Oxford English Dictionary. Oxford University Press. Retrieved 20 November 2011.
- ^ “Temperature and Pressure go Metric” (PDF). Commonwealth Bureau of Meteorology. 1 September 1972. Retrieved 16 February 2022.
- ^ 1985 BBC Special: A Change In The Weather on YouTube
- ^ Lide, D.R., ed. (1990–1991). Handbook of Chemistry and Physics. 71st ed. CRC Press. p. 4–22.
- ^ The ice point of purified water has been measured at 0.000089(10) degrees Celsius – see Magnum, B.W. (June 1995). “Reproducibility of the Temperature of the Ice Point in Routine Measurements” (PDF). Nist Technical Note. 1411. Archived from the original (PDF) on 10 July 2007. Retrieved 11 February 2007.
- ^ “SI Units – Temperature”. NIST Office of Weights and Measures. 2010. Retrieved 21 July 2022.
- ^ Elert, Glenn (2005). “Temperature of a Healthy Human (Body Temperature)”. The Physics Factbook. Retrieved 22 August 2007.
- ^ “Unit of thermodynamic temperature (kelvin)”. The NIST Reference on Constants, Units, and Uncertainty: Historical context of the SI. National Institute of Standards and Technology (NIST). 2000. Archived from the original on 11 November 2004. Retrieved 16 November 2011.
- ^ BIPM, SI Brochure, Section 5.3.3.
- ^ For more information on conventions used in technical writing, see the informative SI Unit rules and style conventions by the NIST as well as the BIPM’s SI brochure: Subsection 5.3.3, Formatting the value of a quantity. Archived 5 July 2014 at the Wayback Machine
- ^ “22.2”. The Unicode Standard, Version 9.0 (PDF). Mountain View, CA, USA: The Unicode Consortium. July 2016. ISBN 978-1-936213-13-9. Retrieved 20 April 2017.
- ^ Decision No. 3 of Resolution 3 of the 13th CGPM.
- ^ H.D. Young, R. A. Freedman (2008). University Physics with Modern Physics (12th ed.). Addison Wesley. p. 573.
- ^ This fact is demonstrated in the book Biostatistics: A Guide to Design, Analysis, and Discovery By Ronald N. Forthofer, Eun Sul Lee and Mike Hernandez
- ^ “Resolution 3 of the 13th CGPM (1967)”.
- ^ “Resolution 3 of the 9th CGPM (1948)”. International Bureau of Weights and Measures. Retrieved 9 May 2008.
- ^ Citation: London South Bank University, Water Structure and Behavior, notes c1 and c2
External links[edit]
![]() The dictionary definition of Celsius at Wiktionary
The dictionary definition of Celsius at Wiktionary
- NIST, Basic unit definitions: Kelvin
- The Uppsala Astronomical Observatory, History of the Celsius temperature scale
- London South Bank University, Water, scientific data
- BIPM, SI brochure, section 2.1.1.5, Unit of thermodynamic temperature
- TAMPILE, Comparison of temperature scales
Что же такое температура?
Добавлено: 17 декабря 2021 в 17:49

Температура — базовое физическое понятие, которое понятно нам на бытовом уровне, но часто вызывает затруднения при решении задач ОГЭ по физике . Основная сложность состоит в том, что мы путаем тепло, температуру и процессы теплопередачи.
Попробуем разобраться в этих явлениях и закономерностях.
Шкалы температуры
Для восприятия температуры, то есть степени нагретости вещества у человека есть рецепторы, благодаря которым мы ощущаем: теплая вода или холодная, какая погода на улице и остыла ли уже кружка с чаем.
Понятия «холодный», «горячий», «теплый» хороши для повседневной жизни, но для науки требуется более совершенный инструмент, который позволяет однозначно понимать состояние материи или воспринимать условия проведения эксперимента.
Мы измеряем температуру веществ с помощью прибора, называемого термометром. Он имеет шкалу, которая показывает величину «нагрева» в градусах — единицах температуры. На этом этапе возникает первая проблема, потому что существует три распространенных единицы измерения температуры:
- градус Цельсия (°C)— 1/100 часть диапазона температур между точкой плавления льда и кипения воды, принятыми, соответственно за 0 °C и 100 °C;
- градус Кельвина (°K)— количественно равен градусу Цельсия (вернее, наоборот) и рассчитывается, как 1/273,16 доля тройной точки воды (что это такое, мы расскажем ниже);
- градус Фаренгейта (°F) — 1/180 часть диапазона температур между точкой плавления льда и кипения воды, которые равны, соответственно +32 °F и +212 °F.
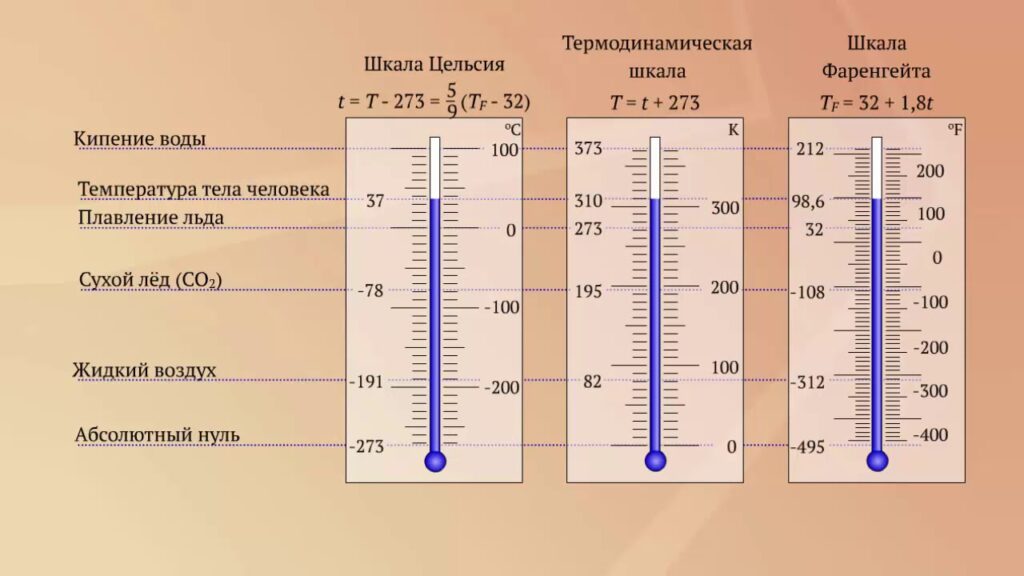
Единицы и шкала измерения температуры в физике
Внимание! Тройная точка — условия, при которых вода пребывает в равновесии между газообразным, жидким и твердым состоянием и может одновременно существовать в любом из них. При обычных условиях в природе такого не происходит — состояние равновесия достижимо лишь при понижении давления до 0,006 атм и температуре 0,01 °С.
Градус Фаренгейта используется, в основном, в США. Градус Цельсия распространен в остальном мире, но в науке базовой единицей является градус Кельвина.
Изначально все три параметра были привязаны к свойствам воды, но сейчас ситуация изменилась, поскольку в современной науке и технике важно очень точно знать состояние системы, поэтому градус Кельвина был переопределен через постоянную Больцмана.
Единицы и шкала измерения температуры в физике
Перевод температуры
Для бытовых и школьных расчетов мы можем преобразовать результат измерения по шкале Цельсия в шкалу Кельвина или Фаренгейта и наоборот, используя следующее уравнение:
Пример: нормальная температура человеческого тела составляет 36,6 °C — она обозначена на наших медицинских градусниках. Определите, какая температура обозначена на американских термометрах и сколько это будет в Кельвинах.
Решение
- На американском термометре, как мы уже знаем, указана температура в Фаренгейтах. Чтобы найти соответствующее значение, составим пропорцию для перевода между двумя шкалами:
Подставим значение температуры в левую часть и решим пропорцию относительно °F:
°F = 97.88
- На термометре специалиста по термодинамике указана температура в Кельвинах. Чтобы найти соответствующее значение, составим пропорцию для перевода между двумя шкалами:
Подставим значение температуры в левую часть и решим пропорцию относительно °F:
Заметим, что обе части имеют одинаковый знаменатель, от которого можно избавиться, умножив каждую из них на 100. Проделаем этот маневр и одновременно решим относительно °K:
°K = 36,6 + 273 = 309,75
Вывод: Градусы Цельсия можно перевести в градусы Кельвина, просто прибавив 273.
Важно: 0 °K или -273,15 °C — самая низкая возможная температура или абсолютный ноль! На практике этой отметки достичь нельзя, хотя ученые и инженеры приблизились очень близко к этому значению, снизив температуру газовой среды до 38∙10-12 °К.

Единицы и шкала измерения температуры в физике
Что же такое температура?
Му уже знаем, как измерить температуру и как выразить ее количественно, но не знаем, что это такое. Заглянем внутрь материи: нам известно, что все вещества состоят из атомов и молекул.
О микромире мы знаем, что все частицы материи находятся в случайном движении, они колеблются, сталкиваясь случайным образом. Из механики мы знаем, что движущийся объект имеет кинетическую энергию. Таким образом, в объекте все частицы обладают кинетической энергией.
Температура — это величина, которая прямо пропорциональна средней кинетической энергии атомов вещества.
Важно! Будьте осторожны, это не энергия, это просто количество средней кинетической энергии одного атома или одной молекулы.
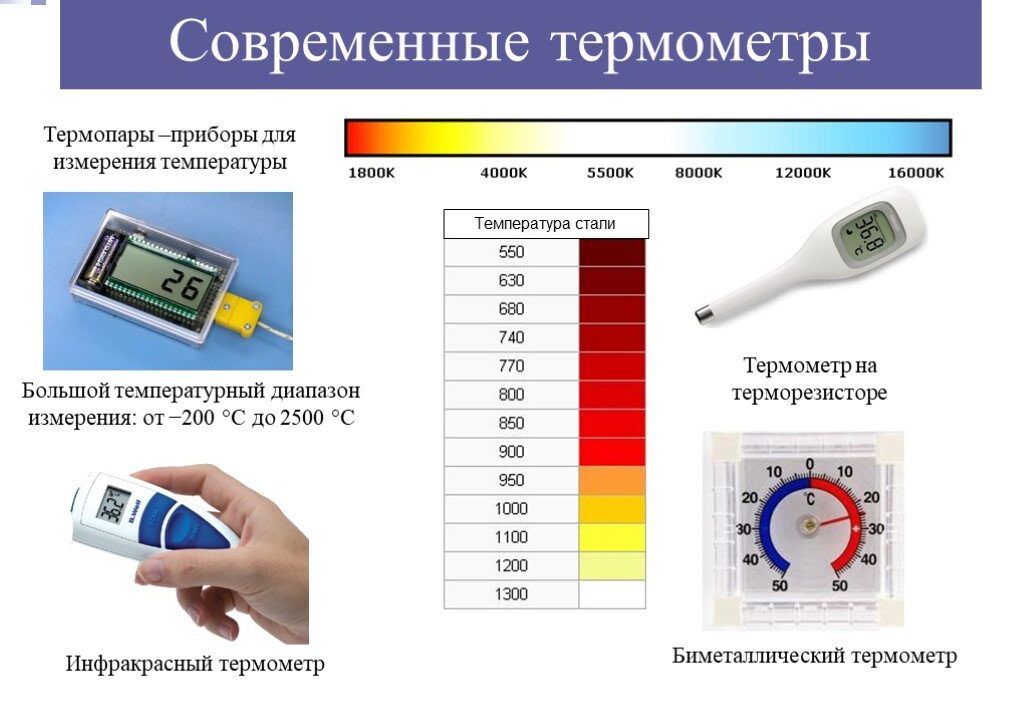
Единицы и шкала измерения температуры в физике
Тепло — это энергия, которую можно преобразовывать из одной формы в другую или передавать от одного объекта к другому.
Природный газ, сгорая, выделяет тепло и передает эту энергию через чайник воде. Это увеличивает кинетическую энергию молекул воды, заставляя их двигаться все быстрее и быстрее. При определенной температуре (точке кипения) атомы набирают достаточно энергии, чтобы разорвать молекулярные связи в жидкости и превратиться в пар.
Теплопередача — передача тепловой энергии от одного, более нагретого тела (участка) к другому, менее нагретому до момента достижения равновесия. Она может осуществляться по следующим механизмам:
- теплопроводность: холодная часть стены дома нагревается путем «перетекания» тепла от нагретой части;
- конвекция: воздух у батареи отопления нагревается и поднимается вверх, перенося тепловую энергию в пространстве комнаты;
- радиация или тепловое излучение: кусок раскаленного металла или инфракрасный обогреватель (вообще, любое тело) излучает электромагнитные волны, передавая тепловую энергию.
Занимайтесь на курсах ЕГЭ и ОГЭ в паре TwoStu и получите максимум баллов на экзамене:

Эксперт по подготовке к ЕГЭ, ОГЭ и ВПР
Задать вопрос
Закончил Московский физико-технический институт (Физтех) по специальности прикладная физика и математика. Магистр физико-математических наук. Преподавательский стаж более 13 лет. Соучредитель курсов ЕГЭ и ОГЭ в паре TwoStu.
Читайте также:
Физика, 10 класс
Урок №19. Температура. Энергия теплового движения молекул
На уроке рассматриваются понятия: температура и тепловое равновесие; шкалы Цельсия и Кельвина; абсолютная температура как мера средней кинетической энергии теплового движения частиц вещества, зависимость давления от концентрации молекул и температуры.
Глоссарий по теме:
Макроскопические параметры – величины объём V, давление p и температура t, характеризующие состояние макроскопических тел без учёта их молекулярного строения.
Температура характеризует степень нагретости тела (холодное, тёплое, горячее).
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
Тепловым равновесием называют – такое состояние тел, при котором температура во всех точках системы одинакова.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом. Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
Абсолютная температура Т прямо пропорциональна температуре Θ (тета), выражаемой в энергетических единицах (Дж).
Абсолютный нуль – предельная температура, при которой давление идеального газа обращается в нуль при фиксированном объёме или объём идеального газа стремится к нулю при неизменном давлении.
Абсолютный нуль – температура, при которой прекращается тепловое движение молекул.
Абсолютная шкала температур (Шкала Кельвина) – здесь нулевая температура соответствует абсолютному нулю, а каждая единица температуры равна градусу по шкале Цельсия.
Кельвин – единица абсолютной температуры в Международной системе измерений (СИ).
Постоянная Больцмана – коэффициент , связывает температуру Θ энергетических единицах (Дж) с абсолютной температурой Т (К).
, связывает температуру Θ энергетических единицах (Дж) с абсолютной температурой Т (К).
Абсолютная температура есть мера средней кинетической энергии молекул.
Давление газа прямо пропорционально концентрации его молекул и абсолютной температуре Т.
Закон Авогадро – в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул
Обязательная литература:
- Мякишев Г.Я., Буховцев Б.Б., Сотский Н.Н. Физика.10 класс. Учебник для общеобразовательных организаций М.: Просвещение, 2017. – С. 195 – 203.
Дополнительная литература:
- Смородинский Я.А. Температура. – 3-е издание. – М.: Бюро Квантум, 2007. (Библиотечка «Квант». Вып. 103. Приложение к журналу «Квант» № 5/2007.) С. 5— 25.
- Кирик Л.А., Генденштейн Л.Э., Гельфгат И.М.. Задачи по физике. 10-11 классы для профильной школы. – М.: Илекса, 2010. – С. 111-115.
- Рымкевич А.П. Физика. Задачник. 10-11 классы. – М.: Дрофа, 2013. – С. 65 – 67.
- Орлов В.А., Сауров Ю.А. Практика решения физических задач. 10-11классы. – М.: Вентана-Граф, 2014. – С. 98-99.
- http://kvant.mccme.ru/1991/09/idealnyj_gaz_-_universalnaya_f.htm
Теоретический материал для самостоятельного изучения
Измеряя расположение звёзд на небе, расстояния на земле, время, люди знали, для чего они это делают и изобретали, телескопы, часы, прототипы современных линеек. О температуре такого же сказать было нельзя. О том, что такое тепловое равновесие и что означает степень нагрева тела (температура), существовали разные мнения. Но человек с незапамятных времен точно знал, что, когда два тела плотно соприкасаются, между ними устанавливается, выражаясь современным языком, тепловое равновесие.
Любое макроскопическое тело или группа макроскопических тел при неизменных внешних условиях самопроизвольно переходят в состояние теплового равновесия.
Тепловым равновесием называют такое состояние тел, при котором температура во всех точках системы одинакова.
Температура (от лат. temperatura — надлежащее смешение, соразмерность, нормальное состояние) – физическая величина, характеризующая состояние термодинамического равновесия макроскопической системы.
К числу характеристик состояния макроскопических тел (твёрдых тел, жидкостей, газов) и процессов изменения их состояний, относят объём, давление и температуру. Эти величины описывают в целом тела, состоящие из большого числа молекул, а не отдельные молекулы. При этом микроскопические процессы внутри тела не прекращаются при тепловом равновесии: расположения молекул всё время меняются и меняются их скорости при столкновениях.
Величины объём, давление и температуру, характеризующие состояние макроскопических тел без учёта их молекулярного строения, называют макроскопическими параметрами.
Тепловым или термодинамическим равновесием, изолированной системы тел, называют состояние, при котором все макроскопические параметры в системе остаются неизменными.
Для точной характеристики нагретости тела, необходим прибор, способный измерить температуры тел и дать возможности их сравнения.
Термометр — это прибор для измерения температуры путём контакта с исследуемым телом. Различают жидкостные, газовые термометры, термопары, термометры сопротивления.
В 1597 году Галилей создал термоскоп, в собственных сочинениях учёного нет описания этого прибора, но его ученики засвидетельствовали этот факт. Аппарат представлял собой устройство для поднятия воды при помощи нагревания.
Изобретение термометра, данные которого не зависели бы от перепадов атмосферного давления, произошли благодаря экспериментам физика Э. Торричелли, ученика Галилея.
Во всех приборах, изобретённых в XVIII веке, измерение температуры было относительно расширению столбика воды, спирта или ртути и произвольности выбора начала отсчёта, т.е. нулевой температуры. Наполняющие их вещества замерзали или кипели и этими термометрами нельзя было измерять очень низкие или очень высокие температуры. Необходимо было изобрести такую шкалу, чтобы избавиться от зависимости выбранного вещества, на основе которого формировалось градуирование.
Шкала, предложенная шведским учёным Андерсом Цельсием в 1742 г., точно устанавливала положение двух точек: 0 и 100 градусов. По шкале Цельсия температура обозначается буквой t, измеряется в градусах Цельсия (ºС).
На территории Англии и США используется шкала Фаренгейта. Такая шкала была предложена немецким учёным Даниелем Габриелем Фаренгейтом в 1724 г.: 0 °F — температура смеси снега с нашатырём или поваренною солью, 96 °F —температура здорового человеческого тела, во рту или под мышкой.
Рене Антуан де Реомюр не одобрял применения ртути в термометрах вследствие малого коэффициента расширения ртути. В 1730 году изобрёл водно-спиртовой термометр и предложил шкалу от 0 до 80°.
Шкала Реомюра очень долго использовалась на родине учёного во Франции вплоть до настоящего времени.
Различные жидкости при нагревании расширяются не одинаково. Поэтому расстояния на шкале между нулевой отметкой 0 °C и 100 °C будут разными.
Однако существует способ создать тело, которое приближенно обладает нужными качествами. Это идеальный газ. Было замечено, что в отличие от жидкостей все разряжённые газы – водород, гелий, кислород – расширяются при нагревании одинаково и одинаково меняют своё давление при изменении температуры. Это свойство газов позволяет избавиться в термометрах от одного существенного недостатка шкалы Цельсия – произвольности выбора начала отсчёта, то есть нулевой температуры.
При тепловом равновесии, если давление и объём газа массой m постоянны, то средняя кинетическая энергия молекул газа должна иметь строго определённое значение, как и температура.
Практически такую проверку произвести непосредственно невозможно, но с помощью основного уравнения молекулярно-кинетической теории её можно выразить через макроскопические параметры:

 ;
;  ;
;  ;
;  ;
; 

Если кинетическая энергия действительно одинакова для всех газов в состоянии теплового равновесия, то и значение давления р должно быть тоже одинаково для всех газов при постоянном значении отношения объёма к числу молекул. Подтвердить или опровергнуть данное предположение может только опыт.

Возьмём несколько сосудов, заполненных различными газами, например, водородом, гелием и кислородом. Сосуды имеют определённые объёмы и снабжены манометрами, для измерения давления газов в сосудах. Массы газов известны, тем самым известно число молекул в каждом сосуде. Приведём газы в состояние теплового равновесия. Для этого поместим их в тающий лёд и подождём, пока не установится тепловое равновесие и давление газов перестанет меняться.
Здесь устанавливается тепловое равновесие и все газы имеют одинаковую температуру 0 °С. При этом показания манометра показывают разное давление р, объёмы сосудов V изначально были разными и число молекул N различно, так как газы, закаченные в баллоны разные. Найдём отношение для водорода всех параметров для одного моля вещества:

Такое значение отношения произведения давления газа на его объём к числу молекул получается для всех газов при температуре тающего льда. Обозначим это отношение через Θ0 (тета нулевое):

Таким образом, предположение, что средняя кинетическая энергия, а также давление р в состоянии теплового равновесия одинаковы для всех газов, если их объёмы и количества вещества одинаковы или если отношение

Если же сосуды с газами поместить в кипящую воду при нормальном атмосферном давлении, то согласно эксперименту, отношение макроскопических параметров будет также одинаковым для всех газов, но значение будет больше предыдущего

Отсюда следует, что величина Θ растёт с повышением температуры и не зависит от других параметром, кроме температуры. Этот опытный факт позволяет рассматривать величину Θ тета как естественную меру температуры и измерять в энергетических единицах — джоулях.
А теперь вместо энергетической температуры введём температуру, которая будет измеряться в градусах. Будем считать величину тета Θ прямо пропорциональной температуре Т, где k- коэффициент пропорциональности

Так как  , то тогда
, то тогда 
По этой формуле вводится температура, которая даже теоретически не может быть отрицательной, так как все величины левой части этого равенства больше или равны нулю. Следовательно, наименьшим значением этой температуры является нуль, при любом другом параметре p, V, N равным нулю.
Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объёме или при которой объём идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулём температуры.
Тепловое движение молекул непрерывно и бесконечно, а при абсолютном нуле молекулы поступательно не двигаются. Следовательно, абсолютный нуль температур при наличии молекул вещества не может быть достигнут. Абсолютный нуль температур — это самая низкая температурная граница, верхней не существует, та «наибольшая или последняя степень холода», существование которой предсказывал М.В. Ломоносов.
В 1848 г. английскому физику Вильяму Томсону (лорд Кельвин) удалось построить абсолютную температурную шкалу (её в настоящее время называют шкалой Кельвина), которая имеет две основные точки 0 К (или абсолютный нуль) и 273К, точка в которой вода существует в трёх состояниях (в твёрдом, жидком и газообразном).
Абсолютная температурная шкала — шкала температур, в которой за начало отсчёта принят абсолютный нуль. Температура здесь обозначается буквой T и измеряется в кельвинах (К).
На шкале Цельсия, есть две основные точки: 0°С (точка, в которой тает лёд) и 100°С (кипение воды). Температура, которую определяют по шкале Цельсия, обозначается t. Шкала Цельсия имеет как положительные, так и отрицательные значения.
Из опыта мы определили значения величины Θ (тета) при 0 °С и 100 °С. Обозначим абсолютную температуру при 0 °С через Т1, а при 100 °С через Т2. Тогда согласно формуле:



Отсюда можно вычислить коэффициент k, который связывает температуру в Θ энергетических единицах (Дж) с абсолютной температурой Т (К)
k = 1,38 • 10-23 Дж/К – постоянная Больцмана.
Зная постоянную Больцмана, можно найти значение абсолютного нуля по шкале Цельсия. Для этого найдём сначала значение абсолютной температуры, соответствующее 0°С:

 значение абсолютной температуры.
значение абсолютной температуры.
Один кельвин и один градус шкалы Цельсия совпадают. Поэтому любое значение абсолютной температуры Т будет на 273 градуса выше соответствующей температуры t по Цельсию:


Теперь выведем ещё одну зависимость температуры от средней кинетической энергии молекул. Из основного уравнения молекулярно-кинетической теории и уравнения для определения абсолютной температуры


Здесь видно, что левые части этих уравнений равны, значит правые равны тоже.

Средняя кинетическая энергия хаотического поступательного движения молекул газа пропорциональна абсолютной температуре.
Абсолютная температура есть мера средней кинетической энергии движения молекул.
Из выведенных формул мы можем получить выражение, которое показывает зависимость давления газа от концентрации молекул и температуры



Из этой зависимости вытекает, что при одинаковых давлениях и температурах концентрация молекул у всех газов одна и та же. Отсюда следует закон Авогадро, известный нам из курса химии.
Закон Авогадро: в равных объёмах газов при одинаковых температурах и давлениях содержится одинаковое число молекул.
Рассмотрим задачи тренировочного блока урока.
1. При температуре _______ (370C; 2830C; 270C) средняя кинетическая энергия поступательного движения молекул равна 6,21·10-21Дж.
Дано:

k = 1,38 • 10-23 Дж/К – постоянная Больцмана
t -?
Решение:
Запишем значение средней кинетической энергии хаотического поступательного движения молекул с зависимостью от абсолютной температуры:

Отсюда выразим Т:


Соотношение между абсолютной температурой и температурой в градусах Цельсия:

Подставим значение абсолютной температуры:

Правильный вариант ответа:
2. При температуре 290 К и давлении 0,8 МПа, средняя кинетическая энергия молекул равна __________ Дж, а концентрация составляет молекул ___________ м-3.
Дано:
Т = 290К
р = 0,8 МПа =0,8·106 Па
k = 1,38 • 10-23 Дж/К – постоянная Больцмана
Ек -? n – ?
Решение:
Значение средней кинетической энергии хаотического поступательного движения молекул:

Подставив значение абсолютной температуры, найдём ответ:

Определим концентрацию газа из соотношения:



Правильный вариант ответа: 6·10-21; 2·1026 м-3.

