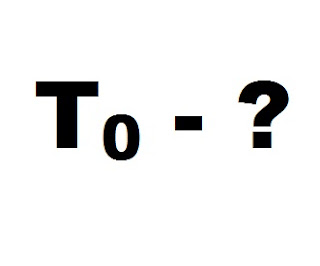Как найти температуру газа?
Vova
Мастер
(1913),
закрыт
8 лет назад
Помогите плизз с задачей по физике! Вот условия:
При нагревании газа до температуры 474к давление его увеличилось вдвое при том же объеме. Найти начальную температуру газа.
daybit
Высший разум
(146291)
8 лет назад
PV/T=const
V = const
значит P/T = const, то есть давление P прямо пропорционально температуре T, и если давление увеличилось в 2 раза, то и температура тоже, значит начальная температура = 474/2 = 237 К = -36С
Источник: 2015-05-04 23:17 (utc3)
Перейти к контенту
Условие задачи:
Определить начальную температуру газа, если при изохорном нагревании до 580 К его давление увеличилось вдвое.
Задача №4.3.1 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(T_1=580) К, (p_1=2p_0), (T_0-?)
Решение задачи:
Поскольку процесс в задаче изохорный ((V = const)), то воспользуемся законом Шарля:
[frac{{{p_0}}}{{{T_0}}} = frac{{{p_1}}}{{{T_1}}}]
Так как в условии сказано, что давление увеличилось вдвое, т.е. (p_1=2p_0), то подставим эту формулу в закон Шарля выше:
[frac{{{p_0}}}{{{T_0}}} = frac{{2{p_0}}}{{{T_1}}}]
Сократим обе части уравнения на неизвестное (p_0):
[frac{1}{{{T_0}}} = frac{2}{{{T_1}}} Rightarrow {T_0} = frac{{{T_1}}}{2}]
Подставив в итоговую формулу исходные величины, получим численный ответ:
[{T_0} = frac{{580}}{2} = 290 ; К = 17; ^circ С].
Ответ: 17° С.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
4.2.111 Когда из сосуда выпустили некоторое количество газа, давление в нем упало на 40%
4.3.2 В закрытом баллоне находится газ при температуре 295 К
4.3.3 Давление в откачанной рентгеновской трубке при 15 градусах Цельсия
( 8 оценок, среднее 4.5 из 5 )
Температура – термодинамическая макроскопическая характеристика, которая играет важную роль практически во всех физических процессах. В данной статье сосредоточим свое внимание на освещении вопросов, что такое абсолютная температура газа идеального и как ее можно вычислить.
Абсолютная шкала температур
Для начала познакомимся со шкалой, которая используется в физике для описания температуры. Она называется абсолютной или шкалой Кельвина. Впервые ее ввел в использование английский физик лорд Кельвин в 1848 году. При этом ученый основывался на завоевавшей популярность шкале Цельсия.
Абсолютная температура так называется потому, что она имеет нижний предел – 0 кельвин, при котором считается “замороженным” любой вид движения (на самом деле при 0 К существуют так называемые нулевые колебания). Верхнего предела у этой шкалы нет.
С градусами Цельсия C абсолютная шкала T связана следующим простым равенством:
T = C + 273,15.
В отличие от других температурных шкал, например, от шкалы Фаренгейта, кельвин имеет точно такой же масштаб, что и градус Цельсия. Последнее означает, что для перевода в абсолютную любой температуры по Цельсию достаточно добавить к ней число 273,15. Так, по шкале Кельвина вода замерзает при 273,15 К, а кипит при 373,15 К.
Краткое понятие о газе идеальном
Поскольку далее будет рассмотрена формула для определения абсолютной температуры газа идеального, то будет полезным познакомиться с этим понятием поближе. Под идеальным понимают такой газ, молекулы которого практически не взаимодействуют друг с другом, обладают большой кинетической энергией по сравнению с потенциальной, и расстояния между которыми значительно превышают их собственные размеры.
Все реальные газы проявляют поведение идеальных при небольших давлениях и высоких температурах. Примерами могут служить благородные газы, воздух, метан и другие. В то же время пар H2O даже при низких давлениях сильно отличается от идеального газа, поскольку в нем всегда присутствуют значительные водородные связи между полярными молекулами воды.
Температура абсолютная идеального газа
Существует два подхода к определению температуры в газах. Рассмотрим каждый из них.
Первый подход заключается в привлечении положений молекулярно-кинетической теории (МКТ) и физического смысла самой температуры T. Последний заключается в кинетической энергии частиц газа. Чем больше эта энергия, тем выше температура, причем зависимость является прямо пропорциональной. Используя формулу из механики для энергии кинетической и постоянную Больцмана kB можно записать следующее равенство МКТ:
m*v2/2 = 3/2*kB*T.
Где m – масса движущейся поступательно частицы. Выражая из этого равенства величину T, получаем формулу:
T = m*v2/(3*kB).
Чем меньше масса частицы и чем больше ее скорость, тем выше абсолютная температура.
Второй подход в определении величины T заключается в использовании универсального уравнения Клапейрона-Менделеева. Это уравнение было записано в XIX веке Эмилем Клапейроном (впоследствии модифицировано Д. И. Менделеевым) как результат обобщения открытых экспериментально в XVII-XIX веках газовых законов (Шарля, Гей-Люссака, Бойля-Мариотта, Авогадро). Математически универсальное уравнение записывается так:
P*V = n*R*T.
Как видно, оно связывает три основных термодинамических величины системы: давление P, объем V и температуру абсолютную T. Две другие величины, присутствующие в уравнении, – это n – количество вещества и R – газовая постоянная.
Не представляет особого труда получить формулу для температуры из Клапейрона-Менделеева закона:
T = P*V/(n*R).
В закрытой системе (n = const) температура газа прямо пропорциональна произведению объема на давление.
Пример задачи
Воздух, которым мы дышим, является смесью газов идеальных. Известно, что молярная масса воздуха составляет 29 г/моль. Необходимо определить температуру воздуха, если средняя скорость его молекул составляет 530 м/с.
Очевидно, что решение этой задачи можно получить, если воспользоваться следующим выражением:
T = m*v2/(3*kB).
Массу одной молекулы m воздуха можно получить, если поделить величину M на число Авогадро NA. Произведение же числа NA на константу Больцмана kB – это не что иное, как газовая постоянная R, которая равна 8,314 Дж/(К*моль). Учитывая эти рассуждения, получаем рабочую формулу:
T = M*v2/(3*R ) = 0,029*6002/(3*8,314) = 326,60 К.
В градусах Цельсия найденной температуре соответствует значение 53,45 oC. На нашей планете такие температуры характерны для жарких песчаных пустынь в полдень.
Как определить начальную температуру газа?
При нагревании газа до температуры 376 К средняя квадратичная
скорость его молекул увеличилась вдвое. Найти начальную температуру газа.
Решение.
Запишем формулу средней кинетической энергии молекулы газа.
m0
– масса молекулы; <vкв>
– средняя квадратичная скорость молекулы; k –
постоянная Больцмана; T
–
абсолютная температура газа.
Следовательно, T1
= T2/4
= 376/4 = 94,0 К.
Ответ: Начальная температура газа равна 94,0 К.
Источник: Пособие-репетитор для подготовки к централизованному тестированию. С.Н.Капельян, Л.А.Аксенович.
Как найти первоначальную температуру газа
Часто в ходе какого-либо технологического процесса или при решении задач из курса термодинамики возникает необходимость ответить на вопрос: какова была начальная температура смеси газов, находившейся при определенных условиях (объеме, давлении и т.д.)

Инструкция
Предположим, заданы такие условия. Смесь трех газов: водорода, углекислого газа и кислорода, первоначально занимала сосуд объемом 22, 4 литра. Масса водорода составляла 8 г, масса углекислого газа – 22 г, а кислорода – 48 г. При этом парциальное давление водорода ровнялось примерно 4,05*10^5 Па, углекислого газа – 5,06*10^4 Па, а кислорода, соответственно – 3,04*10^5 Па. Требуется определить первоначальную температуру этой газовой смеси.
Прежде всего вспомните закон Дальтона, гласящий: общее давление смеси газов, находящейся в каком-то объеме, равно сумме парциальных давлений каждого из компонентов этой смеси. Сложите известные вам величины: 4,05*10^5 + 0,506*10^5 + 3,04*10^5 = 7,596*10^5 Па. Для упрощения расчетов примите округленное значение: 7,6*10^5 Па. Таково давление газовой смеси.
Теперь вам на помощь придет универсальное уравнение Менделеева-Клапейрона, описывающее состояние идеального газа. Разумеется, ни один из компонентов вашей смеси не является идеальным газом, но его вполне можно использовать в расчетах – погрешность будет очень невелика. Это уравнение записывается в такой форме: PV = MRT/m, где P – давление газа, V – его объем, R – универсальная газовая постоянная, M – фактическая масса газа, m – его молярная масса.
Но ведь у вас смесь газов. Как же быть в этом случае? Надо лишь немного преобразовать уравнение Менделеева-Клапейрона, записав его в таком виде: PV = (M1/m1 + M2/m2 + M3/m3) RT.
Легко можно понять, что если бы количество компонентов газовой смеси было равно 4, 5, 6 и т.д., уравнение преобразовывалось бы абсолютно аналогичным образом. Следовательно, искомая начальная температура газовой смеси вычисляется по формуле: Т = PV/(M1/m1 + M2/m2 + M3/m3)R.
Подставив в эту формулу известные вам значения (с учетом того, что величина R равна 8,31), и произведя вычисления, вы получите: 7,6*10^5* 0,0224 / (8,31 * 7,5) = 17024/62,325 = 273,15. Это значение температуры выражено, разумеется, в градусах Кельвина. То есть получается, что первоначально газовая смесь содержалась при температуре, равной 0 градусов по шкале Цельсия. Задача решена.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.