Загрузить PDF
Загрузить PDF
В химии термин “теоретический выход” используется для описания максимального количества продукта, которое может получиться в результате химической реакции. Сначала следует записать сбалансированное химическое уравнение и определить ключевой компонент реакции. После того как вы измерите количество этого компонента, можно будет рассчитать количество продукта реакции. Это и будет теоретический выход продукта реакции. В реальных экспериментах часть продукта обычно теряется из-за неидеальных условий.
-

1
Начните со сбалансированного уравнения химической реакции. Уравнение реакции подобно рецепту. С левой стороны в нем приведены реагенты, а с правой — продукты реакции. В правильно сбалансированном уравнении химической реакции слева и справа стоит одинаковое число атомов каждого элемента.[1]
-

2
Рассчитайте молярные массы реагентов. С помощью таблицы Менделеева или справочника определите молярные массы атомов всех элементов, которые входят в участвующие в реакции соединения. Сложите их, чтобы определить молярную массу каждого реагента. Проделайте это для одной молекулы соединения. Рассмотрим еще раз реакцию между кислородом и глюкозой с образованием углекислого газа и воды:
→
.[2]
-

3
Переведите количество каждого реагента из граммов в моли. В реальном эксперименте известны массы реагентов в граммах. Чтобы перевести их в количество молей, поделите массу каждого реагента на его молярную массу.[3]
-

4
Определите соотношение реагентов. Моль используется в химии для того, чтобы по массе вещества определить количество его молекул. Определив количество молей кислорода и глюкозы, вы узнаете, сколько молекул каждого вещества вступает в реакцию. Чтобы найти соотношение между двумя реагентами, поделите число молей одного реагента на количество молей другого реагента.[4]
- В рассматриваемом примере в начале реакции имеется 1,25 моля кислорода и 0,139 моля глюкозы. Таким образом, отношение количества молекул кислорода к числу молекул глюкозы составляет 1,25 / 0,139 = 9,0. Это означает, что молекул кислорода в 9 раз больше, чем молекул глюкозы.
-

5
Найдите стехиометрическое соотношение реагентов. Посмотрите на сбалансированное уравнение химической реакции. Коэффициенты перед каждой молекулой показывают относительное количество данного вида молекул, необходимое для протекания реакции. Уравнение химической реакции дает так называемое стехиометрическое соотношение реагентов, при котором они будут расходоваться полностью.[5]
- Для данной реакции имеем
. Коэффициенты указывают на то, что на каждую молекулу глюкозы требуется 6 молекул кислорода. Таким образом, стехиометрическое соотношение для этой реакции составляет 6 молекул кислорода / 1 молекула глюкозы = 6,0.
- Для данной реакции имеем
-

6
Сравните соотношения, чтобы найти ключевой компонент реакции. В большинстве химических реакций один из реагентов расходуется раньше остальных. Этот реагент называют ключевым компонентом реакции. Он определяет, как долго будет продолжаться данная реакция и каким будет теоретический выход продукта реакции. Сравните два рассчитанных соотношения, чтобы определить ключевой компонент реакции:[6]
- В рассматриваемом примере начальное количество молей кислорода в 9 раз превышает число молей глюкозы. Согласно уравнению, стехиометрическое отношение кислорода к глюкозе составляет 6:1. Следовательно, у нас имеется больше кислорода, чем требуется, поэтому второй реагент, глюкоза, является ключевым компонентом реакции.
Реклама
-

1
Посмотрите на уравнение и определите ожидаемый продукт реакции. Правая часть уравнения содержит продукты реакции. Если уравнение сбалансировано, коэффициенты перед каждым продуктом реакции показывают его относительное количество в молях. Они соответствуют теоретическому выходу продуктов реакции в том случае, если взять стехиометрическое соотношение реагентов.[7]
-

2
Запишите количество молей ключевого компонента реакции. Всегда следует сравнивать число молей реагента с количеством молей продукта реакции. Сравнение их масс не даст правильного результата.[8]
- В рассматриваемом примере ключевым компонентом реакции является глюкоза. Расчеты молярной массы показали, что 25 граммов глюкозы соответствуют 0,139 моля.
-

3
Сравните соотношение молекул продукта и реагента. Вернитесь к сбалансированному уравнению и поделите количество молекул ожидаемого продукта на число молекул ключевого компонента реакции.
-

4
Умножьте найденное отношение на количество ключевого компонента реакции в молях. В результате вы получите теоретический выход ожидаемого продукта реакции в молях.
- В рассматриваемом примере 25 граммов глюкозы соответствуют 0,139 моля. Отношение углекислого газа к глюкозе равно 6:1. То есть ожидается, что из каждого моля глюкозы получится шесть молей углекислого газа.
- Теоретический выход углекислого газа составляет (0,139 моля глюкозы) x (6 молей углекислого газа / 1 моль глюкозы) = 0,834 моля углекислого газа.
-

5
Переведите полученный результат в граммы. Это обратно тому, что вы делали, когда в самом начале вычисляли количество молей реагента. Если известно ожидаемое число молей, достаточно умножить его на молярную массу продукта реакции, чтобы получить его теоретический выход в граммах.[9]
- В нашем примере молярная масса CO2 составляет около 44 г/моль (молярная масса углерода ~12 г/моль, кислорода ~16 г/моль, в итоге имеем 12 + 16 + 16 = 44).
- Умножьте 0,834 моля CO2 x 44 г/моль CO2 = ~36,7 грамма. Таким образом, теоретический выход продукта реакции равен 36,7 грамма CO2.
-

6
При желании проделайте такие же вычисления для других продуктов реакции. Во многих экспериментах интерес представляет лишь один продукт реакции. Однако если вы хотите найти теоретический выход второго продукта, просто повторите вычисления.
- В нашем примере вторым продуктом реакции является вода,
. Согласно сбалансированному уравнению реакции, из 6 молекул глюкозы получается 6 молекул воды. Это соответствует соотношению 1:1. Таким образом, если в начале реакции имеется 0,139 моля глюкозы, в конце должно получиться 0,139 моля воды.
- Умножьте количество молей воды на ее молярную массу. Молярная масса воды составляет 2 + 16 = 18 г/моль. В результате получаем 0,139 моля H2O x 18 г/моль H2O = ~2,50 грамма. Таким образом, в данном эксперименте теоретический выход воды составит 2,50 грамма.
Реклама
- В нашем примере вторым продуктом реакции является вода,
Об этой статье
Эту страницу просматривали 23 568 раз.
Была ли эта статья полезной?
Задачи на выход продукта химической реакции. Как решать задачи на выход продукта реакции. Что такое выход продукта химической реакции. Теоретическое и практическое количество продукта химической реакции.
При решении задач на расчеты по уравнениям химических реакций мы принимаем, что в ходе реакции образуется точно рассчитанное количество продукта, исходя из мольного соотношения реагентов и продуктов. Количество продукта реакции, которое должно получится из реагентов согласно стехиометрическим расчетам — это теоретическое количество (масса, объем) или теоретический выход продукта реакции nтеор.
Однако на практике это соотношение не выполняется, и в большинстве случаев образуется меньшее количество продукта реакции, чем было рассчитано — практическое количество (масса, объем) или практический выход продукта реакции nпр.
Практический и теоретический выход не совпадают в силу разных причин — неэффективные соударения реагирующих частиц, побочные процессы, потери в ходе проведения реакции и т.д.
Обратите внимание! Понятия теоретического или практического количества реагента не существует. Ведь мы всегда берем определенное количество реагентов. А вот вступать в реакцию не полностью реагенты могут.
Массовая (мольная, объемная) доля выхода продукта реакции η или ω — это соотношение массы (количества вещества, объема) продукта, которая практически получена в ходе реакции, mпр., к массе (количеству, объему) продукта, которая рассчитана теоретически, mтеор.:
η = mпр./mтеор.
Массовую (мольную, объемную) долю выхода продукта реакции можно выражать в долях, а можно в процентах:
η = mпр./mтеор.·100%
Рассмотрим несколько задач на определение и использование выхода продукта реакции.
1. Какое количество вещества аммиака получится при действии избытка раствора гидроксида натрия на 500 г сульфата аммония, если выход в данной реакции 70%?
Решение.
2NaOH + (NH4)2SO4 = Na2SO4 + 2NH3 + 2H2O
Количество вещества сульфата аммония:
n((NH4)2SO4) = m/M = 500/132 = 3,79 моль
Теоретическое количество аммиака:
nтеор.(NH3) = 2·n((NH4)2SO4) = 2·3,79 = 7,58 моль
Зная мольную долю выхода продукта реакции, определим практический выход аммиака:
nпр.(NH3) = η·nтеор.(NH3) = 0,7·7,58 = 5,3 моль
Ответ: nпр.(NH3) = 5,3 моль
2. При хлорировании метана объемом 112 л (н. у.) получен дихлорметан массой 255 г. Определите долю выхода дихлорметана.
Решение.
CH4 + 2Cl2 = CH2Cl2 + 2HCl
Количество вещества метана:
n(CH4) = V/Vm = 112/22,4 = 5 моль
Теоретическое количество дихлорметана:
nтеор.(CH2Cl2) = n(CH4) = 5 моль
mтеор.(CH2Cl2) = M·nтеор.(CH2Cl2) = 85 г/моль·5 моль = 425 г
Масса дихлорметана, которая приведена в условии задачи — это практический выход дихлорметана.
Доля выхода дихлорметана:
η = mпр./mтеор. = 255/425 = 0,6 или 60%
Ответ: выход продукта реакции 60%
3. Определите массу оксида меди (II), которая потребуется для получения 500 г нитрата меди, если доля выхода в реакции взаимодействия оксида меди с HNO3 составляет 92%?
4. Определите объем (н.у., л) аммиака, который получится при действии избытка раствора гидроксида натрия на 48 г карбоната аммония, если выход в реакции составляет 70%?
5. Определите массу соли, г, которая образуется при растворении в избытке азотной кислоты 80 г оксида меди (II), если выход в реакции составляет 80%?
6. При термическом разложении 1700 г нитрата натрия было получено 174,4 л кислорода (н.у.). Определите массовую долю выхода в этой реакции.
7. Рассчитайте массу оксида магния, которая образуется при разложении гидроксида магния массой 50 г, если реакция разложений прошла с выходом 95,5%.
8. Какая масса бензола (кг) может получиться из 369,6 м3 (н.у.) ацетилена, если доля выхода бензола составила 65% от теоретически возможного?
9. Определите массу спирта, полученного при гидратации 40 л пропилена (н.у.), если доля выхода продукта реакции составляет 65% от теоретически возможного.
10. Определите долю выхода в реакции каталитического окисления аммиака кислородом, если при окислении 10 моль аммиака образуется 200 л оксида азота (II) при н.у.?
11. Пары брома объемом 20 л смешали с избытком водорода, в результате из смеси выделили 32 л бромоводорода. Определите долю выхода, %, если объемы газов измерялись при одинаковых условиях.
12. Оксид кальция массой 0,64 кг нагрели до 1200° С с достаточной массой оксида кремния (IV). Масса образовавшегося силиката кальция оказалась равной 1,024 кг. Определите выход (%) реакции соединения.
13. Из 36 г метанола было получено 24 г диметилового эфира. Рассчитайте выход реакции дегидратации
14. Углекислый газ объемом 6 л (н.у.) пропустили над раскалённым углем, продукт реакции пропустили через избыток известковой воды, после чего собрали 7,2 л (н.у.) газа. Определите степень превращения углекислого газа, %.
15. Определите массу, г нитрата аммония, которая содержалась в растворе, если при действии на этот раствор избытка гидроксида кальция выделилось 6 г аммиака. Реакция прошла с выходом 88,2 %.
16. При термическом разложении не загрязненного примесями карбоната кальция образовалось 20 г оксида кальция. Известно, что реакция прошла с выходом 85%. Вычислите массу карбоната кальция, взятого для проведения реакции разложений и объем (н.у.) образовавшегося углекислого газа.
17. Какой объем пропана (н.у.) потребуется для получения 42 г пропена, если доля выхода продуктов реакции составляет 60% от теоретически возможного?
18. При бромировании пентена-2 массой 8,4 г получен 2,3-дибромпентан массой 24,3 г. Определите долю выхода продукта реакции.
19. Из 69 г этанола получен бутадиен-1,3 массой 36,85 г. Определите массовую долю выхода продукта реакции.
20. При бромировании 5,4 г дивинила избытком брома образуется 28,2 г 1,2,3,4-тетрабромбутана. Определите выход продукта реакции.
21. Определите, какая масса 2-метилбутана необходима для получения 46,24 г изопрена, если доля выхода продукта реакции составляет 85%?
22. Определите объем метана, который потребуется для получения 63 л ацетилена (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
23. Определите, какую массу уксусного альдегида можно получить по реакции Кучерова из 11,2 л ацетилена (н. у.), если доля выхода продуктов реакции составляет 80% от теоретически возможного?
24. При действии избытка воды на 48 г технического карбида кальция, содержащего 10% примесей, образовался ацетилен объемом 10,08 л (н.у.). Определите долю выхода продукта реакции.
25. Определите массу технического карбида алюминия, содержащего 7% примесей, необходимого для получения 56 л метана (н.у.), если доля выхода продуктов реакции составляет 70% от теоретически возможного.
26. Из 179,2 л бутана (н.у.) с объемной долей примесей 25% двухстадийным синтезом получен бутанол-2 массой 159,84 г. Доли выхода продуктов на первой и второй стадиях одинаковы. Определите доли выхода продуктов реакций.
27. Циклогексан массой 16 г сожгли в избытке кислорода и полученный углекислый газ пропустили через избыток раствора гидроксида кальция, в результате чего выпал осадок массой 90 г. Определите массовую долю негорючих примесей в циклогексане, если доля выхода продуктов горения составляет 90% от теоретически возможного.
28. При нитровании 46,8 г бензола получен нитробензол массой 66,42 г. Определите выход продуктов реакции.
Утром меня разбудил телефонный звонок. Звонила моя ученица Лена Д. Со слезами в голосе она начала говорить, что ЕГЭ по химии точно завалит, потому как даже “такая простая и понятная 35 задача” может включать фишку на выход реакции, не считая кучи других “садистских приколов”. Лена скинула мне ВК условие злополучной 35-й задачи: “При гидратации 31,50 г этиленового углеводорода образовалось 23,76 г органического вещества. Выход продукта составил 60 %. Определите молекулярную формулу углеводорода и установите его структуру, если известно, что при его жёстком окислении перманганатом калия образуются кетон и кислота. Напишите уравнение реакции углеводорода с водой, в уравнении изобразите структурные формулы органических веществ”
В своей практике я, действительно, столкнулась с парадоксом, когда очень толковые ребята, хорошо знающие химию, жутко боятся элементарных расчетов на степень превращения вещества и выход продукта реакции. Их начинает терзать сомнение: “А справлюсь ли я на ЕГЭ?!” Такие переживания могут зайти далеко и перерасти в никому не нужную депрессию. Думаю, вы тоже сталкивались с аналогичными проблемами. Что делать? Я предлагаю все трудности преодолевать вместе. Вначале мы повторим тему “Выход продукта реакции”, поучимся решать задачи, обязательно разберем 35-ю задачу, предложенную моей ученицей, а в конце статьи я расскажу вам секретное упражнение, которое нужно выполнять всякий раз, когда вы начинаете сомневаться в собственных силах и способностях. Упражнение так и называется “У меня все получится!”. Итак, поехали!
Выход продукта реакции (выход реакции) – это коэффициент, определяющий полноту протекания химической реакции. Он численно равен отношению количества (массы, объема) реально полученного продукта к его количеству (массе, объему), которое может быть получено по стехиометрическим расчетам (по уравнению реакции).
Решим задачи на выход продукта реакции, используя Четыре Заповеди. Каждое действие обводится зеленым овалом. Читайте внимательно и обязательно записывайте решение каждой задачи. После проработки статьи попробуйте самостоятельно решить все разобранные задачи.
Задача 1
При действии алюминия на оксид цинка массой 32,4 г получили 24 г цинка. Определите выход продукта реакции
1) Первая Заповедь. Выписать данные задачи в разделе “Дано”
2) Вторая Заповедь. Написать уравнение реакции
Повторим теорию химии. Способ восстановления металлов алюминием – алюмотермия. Следует помнить: металлы, стоящие в ряду активности левее (более активные) восстанавливают металлы, стоящие правее, из расплавов оксидов или растворов солей
Li→Rb→K→Ba→Sr→Ca→Na→Mg→Al→Mn→Cr→Zn→Fe→Cd→Co→Ni→Sn→Pb→(H)→Sb→Bi→Cu→Hg→Ag→Pd→Pt→Au
3. Третья Заповедь. Сделать предварительные расчеты по данным условия задачи и по уравнению реакции
В условии задачи представлены данные по одному из реагентов (оксиду цинка) и по одному из реально полученных продуктов (цинку). Составляем два досье, в каждом – масса, молярная масса, количество вещества (моль). Для цинка (продукт), масса и количество вещества – практические, т.к. продукт был получен реально.
Теоретическое значение продукта рассчитываем по уравнению реакции. Точка расчета – количество вещества реагента (оксида цинка). Расчеты выполняем на основании закона кратных отношений по схеме: точку расчета делим на коэффициент при этом веществе, умножаем на коэффициент при искомом веществе и получаем результат. Выписывать отдельно пропорцию для расчетов не обязательно. Это – Легкие Расчеты по уравнениям реакций, которые не противоречат закону кратных отношений, но значительно упрощают решение задач по химии.
4. Четвертая заповедь. Составить алгоритм решения задачи.
Формулизируем вопрос задачи “Определите выход продукта реакции”, – записываем соответствующую формулу и анализируем ее компоненты.
Подробно разберем решение обратной задачи: по известному выходу реакции определим неизвестное значение реагента или продукта.
Задача 2
Определите массу оксида алюминия, которая может быть получена из 23,4 г гидроксида алюминия, если выход реакции составляет 92% от теоретически возможного.
1) Первая Заповедь. Выписать данные задачи в разделе “Дано”.
2) Вторая Заповедь. Написать уравнение реакции.
Небольшой экскурс в теорию химии. Многие нерастворимые в воде гидроксиды разлагаются при нагревании. Продукты разложения – оксиды соответствующих металлов и вода.
3. Третья Заповедь. Сделать предварительные расчеты по данным условия задачи и по уравнению реакции
Составляем досье на реагент (гидроксид алюминия) – определяем его молярную массу и количество вещества (моль). По уравнению реакции рассчитываем теоретическое количество продукта (оксида алюминия). Расчеты выполняем на основании закона кратных отношений по схеме: точку расчета делим на коэффициент при этом веществе, умножаем на коэффициент при искомом веществе и получаем результат.
4. Четвертая заповедь. Составить алгоритм решения задачи.
Формулизируем вопрос задачи “Определите массу оксида алюминия”, т.е. записываем формулу расчета массы, которая для нас, как для химиков, должна быть представлена произведением количества вещества на молярную массу. Анализируем компоненты формулы: молярную массу определяем по таблице Менделеева, количество вещества (практическое) рассчитываем по формуле выхода реакции.
Решим на закрепление еще несколько обратных задач с выходом реакции.
Задача 3
Карбонат натрия взаимодействует с соляной кислотой. Вычислите массу карбоната натрия для получения оксида углерода (IV) массой 56,1 г. Практический выход продукта 85%.
Задача 4
При действии оксида углерода (II) на оксид железа (III) получено железо массой 11,2 г. Найдите массу использованного оксида железа (III), если выход реакции составляет 80%.
Задача 5
При взаимодействии железа с хлором получено 10 г соли, что составляет 85% от теоретически возможного. Сколько граммов железа было взято для реакции с хлором?
В этой статье я не буду разбирать пошагово 35-ю задачу ЕГЭ, предложенную моей ученицей. На фото – подробное решение. Тот, кто уже решал аналогичные задачи, поймет без дополнительных объяснений. Для всех остальных – обязательно будем наслаждаться анализом этой задачи (и не только этой) в следующей статье. Обещаю ДРАЙВ!
Задача 35 ЕГЭ (восстановлена по памяти моей ученицы)
При гидратации 31,50 г этиленового углеводорода образовалось 23,76 г органического вещества. Выход продукта составил 60 %. Определите молекулярную формулу углеводорода и установите его структуру, если известно, что при его жёстком окислении перманганатом калия образуются кетон и кислота. Напишите уравнение реакции углеводорода с водой, в уравнении изобразите структурные формулы органических веществ
Вернемся к проблеме, которую я затронула в начале статьи. Что делать, если резко упала самооценка, ты чувствуешь себя полным идиотом и боишься не справиться с трудными заданиями ЕГЭ? Все очень просто – выполни секретное упражнение “У меня все получится!” Я подсмотрела его на просторах Интернета (автора не знаю) и модифицировала это упражнение под себя и своих учеников:
1. Сядь в спокойной обстановке, закрой глаза, успокой дыхание. Сосредоточься на своей цели. Представь, что у тебя уже все получилось и ты достиг всего, к чему стремился.
2. Сожми ладони вместе перед собой и прижми их к груди. Обратись к Высшему Разуму (как ты его себе представляешь – Бог, Вселенная, Космос, Мир, Природа) с просьбой реализовать твою цель и мечты.
3. Побудь в таком состоянии несколько минут, затем встань, расправь плечи и стряхни с себя все плохое.
В конце статьи хочу привести цитату из стихотворения американского поэта Эдгара Геста, который был очень популярен 100 лет назад:
“И ты не верь тому, кто скажет: “Это слишком сложно!”
Не слушай тех, кто будет утверждать, что это невозможно,
Не бойся трудностей – скорей берись за дело,
Гони сомненья прочь – к мечте иди решительно и смело!”
Вы готовитесь к ЕГЭ и хотите поступить в медицинский? Обязательно посетите мой сайт Репетитор по химии и биологии http://repetitor-him.ru. Здесь вы найдете огромное количество задач, заданий и теоретического материала, познакомитесь с моими учениками, многие из которых уже давно работают врачами. Звоните мне +7(903) 186-74-55. Приходите ко мне на курс, на Мастер-классы “Решение задач по химии” – и вы сдадите ЕГЭ с высочайшими баллами, и станете студентом престижного ВУЗа!
PS! Если вы не можете со мной связаться из-за большого количества звонков от моих читателей, пишите мне в личку ВКонтакте, или на Facebook. Я обязательно отвечу вам.
Репетитор по химии и биологии кбн В.Богунова
Расчетные задачи типа «Определение выхода продукта реакции в процентах от теоретического»
Признак
В условии задачи встречается слово «выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём, практическая масса или объём» могут быть использованы только для веществ-продуктов.
Доля выхода продукта обозначается буквой
![]()
(эта), измеряется в процентах или долях.
Также для расчётов может использоваться количественный выход:
![]()
I. Первый тип задач
Известны масса (объём) исходного вещества и масса (объём) продукта реакции. Необходимо определить выход продукта реакции в %.
Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5, 5 г. Определите выход продукта реакции (%).
| 1. Записываем краткое условие задачи |
Дано: m (Mg) = 1,2 г m практическая(MgSO4) = 5,5 г _____________________ Найти: |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(Mg) = 24 г/моль M(MgSO4) = 24 + 32 + 4 · 16 = 120 г/моль |
|
4. Находим количество вещества реагента по формулам
|
ν(Mg) = 1,2 г / 24(г/моль) = 0,05 моль |
| 5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
m = ν · M mтеор (MgSO4) = M(MgSO4) · νтеор (MgSO4) = = 120 г/моль · 0,05 моль = 6 г |
|
6. Находим массовую (объёмную) долю выхода продукта по формуле
|
Ответ: Выход сульфата магния составляет 91,7% по сравнению с теоретическим |
II. Второй тип задач
Известны масса (объём) исходного вещества (реагента) и выход (в %) продукта реакции. Необходимо найти практическую массу (объём) продукта реакции.
Задача 2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид кальция массой 16,8 г, если выход составляет 80%.
|
1. Записываем краткое условие задачи |
Дано: m(CaO) = 16,8 г
___________________ Найти: m практ (CaC2) = ? |
|
2. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
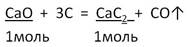 |
|
3. Находим по ПСХЭ молярные массы подчёркнутых веществ |
M(CaO) = 40 + 16 = 56 г/моль M(CaC2) = 40 + 2 · 12 = 64г/моль |
|
4. Находим количество вещества реагента по формулам
|
ν(CaO)=16,8 (г) / 56 (г/моль) = 0,3 моль |
|
5. По УХР вычисляем теоретическое количество вещества (νтеор) и теоретическую массу (mтеор) продукта реакции |
|
|
6. Находим массовую (объёмную) долю выхода продукта по формуле
|
m практич (CaC2) = 0,8 · 19,2 г = 15,36 г Ответ: m практич (CaC2) = 15,36 г |
III. Третий тип задач
Известны масса (объём) практически полученного вещества и выход этого продукта реакции. Необходимо вычислить массу (объём) исходного вещества.
Задача 3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу карбоната натрия нужно взять для получения оксида углерода (IV) объёмом 28,56 л (н. у.). Практический выход продукта 85%.
| 1. Записываем краткое условие задачи |
Дано: н. у. Vm = 22,4 л/моль Vпрактич(CO2) = 28,56 л = 85% или 0,85 ____________________ Найти: m(Na2CO3) =? |
| 2. Находим по ПСХЭ молярные массы веществ, если это необходимо | M (Na2CO3) =2·23 + 12 + 3·16 = 106 г/моль |
|
3. Вычисляем теоретически полученный объём (массу) и количество вещества продукта реакции, используя формулы: |
Vтеоретич(CO2) = = 28,56 л / 0,85 = 33,6 л ν(CO2) = 33,6 (л) / 22,4 (л/моль) = 1,5 моль |
|
4. Запишем УХР. Расставим коэффициенты. Под формулами (из дано) напишем стехиометрические соотношения, отображаемые уравнением реакции. |
|
| 5. Находим количество вещества реагента по УХР |
По УХР:
ν(Na2CO3) = ν(CO2) = 1,5 моль |
|
6. Определяем массу (объём) реагента по формуле: m = ν · M V = ν · Vm |
m = ν · M m(Na2CO3) = 106 г/моль · 1,5 моль = 159 г |
IV. Решите задачи
Задача №1. При взаимодействии натрия количеством вещества 0, 5 моль с водой получили водород объёмом 4,2 л (н. у.). Вычислите практический выход газа (%).
Задача №2. Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно получить при восстановлении его оксида массой 228 г, если практический выход хрома составляет 95 %.
Задача №3. Определите, какая масса меди вступит в реакцию с концентрированной серной кислотой для получения оксида серы (IV) объёмом 3 л (н.у.), если выход оксида серы (IV) составляет 90%.
Задача №4. К раствору, содержащему хлорид кальция массой 4,1 г, прилили раствор, содержащий фосфат натрия массой 4,1 г. Определите массу полученного осадка, если выход продукта реакции составляет 88 %.
Здравствуйте! Друзья!
Сегодня
мы познакомимся и научимся решать ещё один тип расчетных задач, связанных с
вычислениями по уравнению химической реакции. Это расчетные задачи типа
«Определение выхода продукта реакции в процентах от теоретического».
На
уроке нам понадобятся:
1.
Периодическая система химических элементов Д. И. Менделеева.
2.
Калькулятор.
3.
И, как всегда, огромное желание научиться чему-то новому!
Желаю вам успехов!
Задачи
на вычисление выхода продукта реакции от теоретически возможного
Признак
В условии задачи встречается слово
«выход». Теоретический выход продукта всегда выше практического.
Понятия «теоретическая масса или объём,
практическая масса или объём» могут быть использованы только для
веществ-продуктов.


Массовая доля выхода продукта обозначается
буквой h (эта), измеряется в процентах или долях,
объёмная доля выхода продукта может обозначаться в различных источниках h (эта)
Также для расчётов может использоваться
отношения количеств веществ:

Первый
тип задач – Известны масса (объём) исходного
вещества и масса (объём) продукта реакции. Необходимо определить выход продукта
реакции в %.
Задача
1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили
соль массой 5, 5 г. Определите выход продукта реакции (%).
|
1. |
Дано: m(Mg) = 1,2 г mпрактическая (MgSO4) = 5,5 _____________________ Найти:
|
|
2. Запишем Под |
|
|
3. |
M(Mg) = 24 г/моль M(MgSO4) = 24 |
|
4.
|
ν(Mg) = 1,2 г / 24(г/моль) = 0,05 |
|
5. По |
m = ν · M mтеор (MgSO4) = M(MgSO4) · νтеор (MgSO4) = = 120 г/моль · 0,05 моль = 6 г |
|
6. Находим
|
Ответ: Выход сульфата магния составляет |
Второй
тип задач – Известны масса (объём) исходного
вещества (реагента) и выход (в %) продукта реакции. Необходимо найти
практическую массу (объём) продукта реакции.
Задача
2. Вычислите массу карбида кальция, образовавшегося при действии угля на оксид
кальция массой 16,8 г, если выход составляет 80%.
|
1. |
Дано: m(CaO) = 16,8 г
____________________ Найти: mпракт (CaC2) = ? |
|
2. Запишем Под |
|
|
3. |
M(CaO) = 40 + 16 = 56 M(CaC2) = 40 + |
|
4.
|
ν(CaO) = 16,8 (г) / 56 |
|
5. По |
|
|
6. Находим
|
mпрактич (CaC2) = 0,8 Ответ: mпрактич (CaC2) = 15,36 |
Третий
тип задач – Известны масса (объём) практически
полученного вещества и выход этого продукта реакции. Необходимо вычислить массу
(объём) исходного вещества.
Задача
3. Карбонат натрия взаимодействует с соляной кислотой. Вычислите, какую массу
карбоната натрия нужно взять для получения оксида углерода (IV)
объёмом 28,56 л (н. у.). Практический выход продукта 85%.
|
1. |
Дано: н. у. Vm = 22,4 л/моль Vпрактич(CO2) = φ = 85% или 0,85 _____________________ Найти: m(Na2CO3) =? |
|
2. Находим |
M (Na2CO3) =2·23 + |
|
3.
|
Vтеоретич(CO2) = Vпрактич(CO2) / 0,85 = 28,56 л / 0,85 = 33,6 л ν(CO2) = 33,6 |
|
4. Запишем Под |
|
|
5. |
По УХР:
, следовательно ν(Na2CO3) = ν(CO2) = 1,5 моль |
|
5. Определяем m V |
m = ν · M m (Na2CO3) = 106 |














