Уде́льная теплота́ сгора́ния то́плива — физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой 1 кг.
Удельная теплота сгорания измеряется в Дж/кг или калория/кг (1 Дж = 0,2388459 кал). Для экспериментального измерения этой величины используются методы калориметрии.
Определить удельную теплоту сгорания топлива можно по формуле
где 


Чем больше удельная теплота сгорания топлива, тем меньше удельный расход топлива при той же величине коэффициента полезного действия (КПД) двигателя.
Теплота сгорания на основе справочника по физике под редакцией Х.Кухлинга[1][править | править код]
| Теплота сгорания и газообразная плотность бутана, метана и пропана | |||
|---|---|---|---|
| Газ | Теплота сгорания, МДж/м3* | Плотность (нормальные условия), кг/м3 | Теплота сгорания, МДж/кг |
| Бутан | 124 | 2,588 | 47,9 |
| Метан | 35,9 | 0,714 | 50,2 |
| Пропан | 93,4 | 1,96 | 48,4 |
| * – табличное значение согласно справочнику по физике под редакцией Х.Кухлинга |
| Удельная теплота сгорания веществ в воздухе | |
|---|---|
| Вещество | Теплота сгорания, МДж/кг |
| Водород | 141[2] |
| Бор | 58[3] |
| Ацетилен | 50,4[2] |
| Метан (лабораторный) | 50,1[2] |
| Этилен | 48,0[2] |
| Пропан | 47,54[2] |
| Бутан | 47,2[4] |
| Бытовой газ | 46,1[5] |
| Пропан-бутан (баллонный) | 43,8[6] |
| Бензин | 43,6[6] 44[7], 42[8] |
| Литий | 43[3] |
| Дизельное топливо | 42,7[8] |
| Нефть | 41[8] |
| Керосин | 40,8[8] |
| Рапсовое масло | 39,6[9] |
| Подсолнечное масло | 39,5[9] |
| Мазут | 39,2[7] |
| Химически чистый углерод | 32,8[3] |
| Древесный уголь | 31[8] |
| Каменный уголь антрацит | 31[8] |
| Алюминий | 31[3] |
| Условное топливо | 29,308 (7000 ккал)[7] |
| Этанол | 30[10] |
| Каменный уголь | 29,3[8] |
| Магний | 24,7[3] |
| Метанол | 22,7[8] |
| Топливные брикеты | 19—20,5[источник не указан 1486 дней] |
| Дрова сухие (березовые, сосновые) | 15[10] |
| Бурый уголь | 15[7], 14,7[8] |
| Пиролизный газ (англ.) (рус. | 12,0[2] |
| Природный газ | 41-49 |
| Торф | 8,1[7], 15[8][10] |
| Порох | 3,8[11] |
Для сравнения средняя энергия, выделяющаяся при распаде одного ядра урана-235 с учётом распада осколков, составляет приблизительно 202,5 МэВ = 3,244⋅10−11 Дж, или 19,54 ТДж/моль = 83,14⋅106 МДж/кг.
См. также[править | править код]
- Теплота сгорания
- Адиабатическое горение
- Воздух
Примечания[править | править код]
- ↑ Теплота сгорания метана, бутана и пропана. Авторский блог Алексея Зайцева. Дата обращения: 7 октября 2022.
- ↑ 1 2 3 4 5 6 Теплотворная способность газов. Дата обращения: 11 января 2008. Архивировано 16 декабря 2007 года.
- ↑ 1 2 3 4 5 Справочные материалы. Дата обращения: 4 мая 2018. Архивировано 5 мая 2018 года.
- ↑ Теплотворная способность различных видов топлива. Сравнительный анализ. antonio-merloni.ru. Дата обращения: 27 апреля 2021. Архивировано 6 июля 2014 года.
- ↑ ГОСТ 5542-)87. Газы горючие природные для промышленного и коммунально-бытового назначения. Газы горючие природные для промышленного и коммунально-бытового назначения, предназначены в качестве сырья и топлива для промышленного и коммунально-бытового использования. www.nge.ru. Дата обращения: 26 февраля 2016. Архивировано 4 марта 2016 года.
- ↑ 1 2 Удельная теплота сгорания топлива и горючих материалов – таблицы энергии топлива. Thermalinfo.ru. Дата обращения: 7 июля 2019. Архивировано 22 марта 2019 года.
- ↑ 1 2 3 4 5 Теплота сгорания // Физическая энциклопедия : [в 5 т.] / Гл. ред. А. М. Прохоров. — М.: Большая российская энциклопедия, 1999. — Т. 5: Стробоскопические приборы — Яркость. — С. 81. — 692 с. — 20 000 экз. — ISBN 5-85270-101-7.
- ↑ 1 2 3 4 5 6 7 8 9 10 Удельная теплота сгорания твердых и жидких веществ. Дата обращения: 27 июля 2008. Архивировано 15 сентября 2008 года.
- ↑ 1 2 Максимук Ю. В., Антонова З. А., Фесько В. В., Курсевич В. Н. Вязкость и теплота сгорания дизельного биотоплива // Химия и технология топлив и масел. — 2009. — № 5. — С. 27—30. — ISBN 0023-1169. Архивировано 22 февраля 2014 года.
- ↑ 1 2 3 Топлива. Высшая теплотворная способность — таблица. (Удельная теплота сгорания). Дата обращения: 15 октября 2012. Архивировано из оригинала 3 ноября 2012 года.
- ↑ Удельная теплота сгорания топлива. Дата обращения: 27 июля 2008. Архивировано из оригинала 2 октября 2008 года.
Удельная теплота сгорания

4.2
Средняя оценка: 4.2
Всего получено оценок: 311.
4.2
Средняя оценка: 4.2
Всего получено оценок: 311.
Человечество в процессе своей эволюции научилось получать тепловую энергию с помощью сжигания разных видов топлива. Простейшим примером можем служить костер из дров, который разжигали первобытные люди, и с тех пор торф, уголь, бензин, нефть, природный газ — все это виды топлива, сжигая которые человек получает тепловую энергию. Так что же такое удельная теплота сгорания?
Откуда берется тепло в процессе горения?
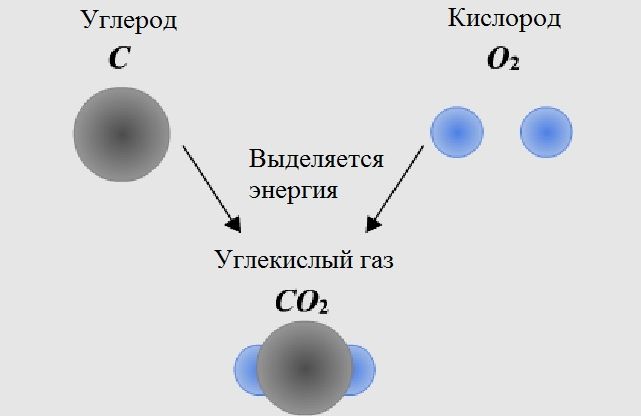
Сам по себе процесс сгорания топлива — это химическая, окислительная реакция. Большинство видов топлива содержит большое количество углерода С, водорода H, серы S и других веществ. Во время горения атомы C, H, и S соединяется с атомами кислорода О2, в результате чего получается молекулы СО, СО2, Н2О, SO2. При этом происходит выделение большого количества тепловой энергии, которую люди научились использовать в своих целях.
Основной вклад в выделение тепла дает углерод C. Второй по количеству тепла вклад вносит водород H.
Что такое удельная теплота сгорания?
Удельная теплота сгорания q — это физическая величина равная количеству тепла, выделяющегося при полном сгорания 1 кг топлива.
Формула удельной теплоты сгорания выглядит так:
$$q={Q over m}$$
где:
Q — количество тепла, выделившееся в процессе горения топлива, Дж;
m — масса топлива, кг.
Единицей измерения q в интернациональной системе единиц СИ является Дж/кг.
$$[q]={Дж over кг}$$
Для обозначения больших величин q часто используются внесистемные единицы энергии: килоджоули (кДж), мегаджоули (МДж) и гигаджоули (ГДж).
Значения q для разных веществ определяют экспериментально.
Зная q, можно вычислить количество тепла Q, которое получится в результате сжигания топлива массой m:
$$Q={q * m}$$
Как измеряют удельную теплоту сгорания
Для измерения q используют приборы, которые называются калориметрами (calor – тепло, metreo – измеряю).
Контейнер с порцией топлива сжигается внутри прибора. Контейнер помещен в воду с известной массой. В результате горения выделившееся тепло нагревает воду. Величина массы воды и изменение ее температуры позволяют вычислить теплоту сгорания. Далее q определяется по вышеприведенной формуле.
Рис. 3. Измерение удельной теплоты сгорания.
Где можно найти значения q
Информацию о величинах удельной теплоты сгорания для конкретных видов топлива можно найти в технических справочниках или в их электронных версиях на интернет-ресурсах. Обычно они приводятся в виде такой таблицы:
Удельная теплота сгорания, q
|
Вещество |
МДж/кг |
Вещество |
МДж/кг |
|
Торф |
8,1 |
Дизельное топливо |
42,7 |
|
Дрова |
10,2 |
Керосин |
44,0 |
|
Уголь бурый |
15,0 |
Бензин |
48,0 |
|
Уголь каменный |
29,3 |
Пропан |
47,5 |
|
Нефть |
41,3 |
Метан |
50,11 |
Ресурсы разведанных, современных видов топлива ограничены. Поэтому в будущем на смену им придут другие источники энергии:
- атомные, использующие энергию ядерных реакций;
- солнечные, преобразовывающие энергию солнечных лучей в тепло и электричество;
- ветряные;
- геотермальные, использующие тепло природных горячих источников.
Что мы узнали?
Итак, мы узнали почему выделяется много тепла при горении топлива. Для вычисления количества тепла, выделяемого при сгорании некоторой массы m топлива, необходимо знать величину q — удельную теплоту сгорания этого топлива. Значения q определены экспериментально методами калориметрии и приведены в справочниках.
Тест по теме
Доска почёта

Чтобы попасть сюда – пройдите тест.
-
Айана Капсаргина
5/5
-
Камилла Бабаева
5/5
Оценка доклада
4.2
Средняя оценка: 4.2
Всего получено оценок: 311.
А какая ваша оценка?
Различные виды топлива (твёрдое, жидкое и газообразное) характеризуются общими и специфическими свойствами. К общим свойствам топлива относятся удельная теплота сгорания и влажность, к специфическим — зольность, сернистость (содержание серы), плотность, вязкость и другие свойства.
Удельная теплота сгорания топлива — это количество теплоты, которое выделяется при полном сгорании (1) кг твёрдого или жидкого топлива или (1) м³ газообразного топлива.
Энергетическая ценность топлива в первую очередь определяется его удельной теплотой сгорания.
Удельная теплота сгорания обозначается буквой (q). Единицей удельной теплоты сгорания является (1) Дж/кг для твёрдого и жидкого топлива и (1) Дж/м³ — для газообразного топлива.
Удельную теплоту сгорания на опыте определяют довольно сложными методами.
Таблица (2). Удельная теплота сгорания некоторых видов топлива.
Твёрдое топливо
|
Вещество |
Удельная теплота сгорания, МДж/кг |
| Бурый уголь |
(9,3) |
| Древесный уголь |
(29,7) |
| Дрова сухие |
(8,3) |
| Древесные чурки |
(15,0) |
|
Каменный уголь марки А-(I) |
(20,5) |
|
Каменный уголь марки А-(II) |
(30,3) |
| Кокс |
(30,3) |
| Порох |
(3,0) |
| Торф |
(15,0) |
Жидкое топливо
|
Вещество |
Удельная теплота сгорания, МДж/кг |
| Бензин, нефть |
(46,0) |
| Дизельное топливо |
(42,0) |
| Керосин |
(43,0) |
| Мазут |
(40,0) |
| Спирт этиловый |
(27,0) |
Газообразное топливо
(при нормальных условиях)
|
Вещество |
Удельная теплота сгорания, МДж/м³ |
| Водород |
(120,8) |
| Генераторный газ |
(5,5) |
| Коксовый газ |
(16,4) |
| Природный газ |
(35,5) |
| Светильный газ |
(21,0) |
Из этой таблицы видно, что наибольшей является удельная теплота сгорания водорода, она равна (120,8) МДж/м³. Это значит, что при полном сгорании водорода объёмом (1) м³ выделяется (120,8) МДж (=) (120,8)
⋅106
Дж энергии.
Водород — один из высокоэнергетических видов топлива. Кроме того, продуктом сгорания водорода является обычная вода, в отличие от других видов топлива, где продуктами сгорания являются углекислый и угарный газы, зола и топочные шлаки. Это делает водород экологически наиболее чистым топливом.
Однако газообразный водород взрывоопасен. К тому же он имеет самую малую плотность в сравнении с другими газами при равной температуре и давлении, что создаёт сложности со сжижением водорода и его транспортировкой.
Общее количество теплоты (Q), выделяемое при полном сгорании (m) кг твёрдого или жидкого топлива, вычисляется по формуле:
Общее количество теплоты (Q), выделяемое при полном сгорании (V) м³ газообразного топлива, вычисляется по формуле:
Влажность (содержание влаги) топлива снижает его теплоту сгорания, так как увеличивается расход теплоты на испарение влаги и увеличивается объём продуктов сгорания (из-за наличия водяного пара).
Зольность — это количество золы, образующейся при сгорании минеральных веществ, содержащихся в топливе. Минеральные вещества, содержащиеся в топливе, понижают его теплоту сгорания, так как уменьшается содержание горючих компонентов (основная причина) и увеличивается расход тепла на нагрев и плавление минеральной массы.
Сернистость (содержание серы) относится к отрицательному фактору топлива, так как при его сгорании образуются сернистые газы, загрязняющие атмосферу и разрушающие металл. Кроме того, сера, содержащаяся в топливе, частично переходит в выплавляемый металл, сваренную стекломассу, снижая их качество. Например, для варки хрустальных, оптических и других стёкол нельзя использовать топливо, содержащее серу, так как сера значительно понижает оптические свойства и колер стекла.
Энергия, которую тело получает или отдает при теплопередаче, называется количеством теплоты. Мы проделали не один опыт, рассмотрели как при теплообмене одни тела отдают энергию, а другие получают. Во многих опытах мы использовали горелку, чтобы сообщить телу какое-то количество теплоты. А как рассчитать это количество теплоты?
С давних времен, чтобы получить энергию, люди используют топливо. Сейчас топливо является источником энергии в промышленности, сельском хозяйстве, на транспорте и, конечно, в повседневном быту. Это нефть, природный газ, торф, уголь, дрова и др.
В данном уроке мы рассмотрим, за счет чего выделяется энергия при сгорании топлива и как ее рассчитать. Также вы узнаете новое определение (удельная теплота сгорания) и научитесь им пользоваться.
Сгорание топлива и энергия
Для начала давайте вспомним строение молекулы воды (рисунок 1). Она состоит из одного атома кислорода и двух атомов водорода.
Между атомами действуют силы притяжения. Если мы захотим разделить атомы, составляющие молекулы, придется преодолеть эти силы. В таком случае будет совершена работа, и затрачена некоторая энергия. При соединение атомов, наоборот, энергия будет выделяться.
Выделение энергии при соединении атомов — явление, на котором основано использование топлива.
В любом топливе содержатся атомы углерода. В процессе горения они соединяются с двумя атомами кислорода (рисунок 2).
В результате:
- Образуется молекула углекислого газа (оксида углерода)
- Выделяется энергия
Удельная теплота сгорания
При сгорании разных видов топлива одинаковой массы выделяется разное количество теплоты. Для того чтобы характеризовать каждый вид топлива используют такую величину, как удельная теплота сгорания. При проектировании двигателей эта величина помогает рассчитать, какое количество теплоты может выделить сжигаемое топливо.
Удельная теплота сгорания топлива — это физическая величина, показывающая, какое количество теплоты выделяется при полном сгорании топлива массой $1 space кг$.
- Обозначается буквой $q$
- Единица измерения — $1 frac{Дж}{кг}$
Величину удельной теплоты сгорания устанавливают на опыте. Мы будем использовать уже готовые результаты таких исследований, представленные в таблице 1.
| Вещество | $q, space frac{Дж}{кг}$ | Вещество | $q, space frac{Дж}{кг}$ |
| Порох | $0.38 cdot 10^7$ | Древесный уголь | $3.4 cdot 10^7$ |
| Дрова сухие | $1.0 cdot 10^7$ | Природный газ | $4.4 cdot 10^7$ |
| Торф | $1.4 cdot 10^7$ | Нефть | $4.4 cdot 10^7$ |
| Каменный уголь | $2.7 cdot 10^7$ | Бензин | $4.6 cdot 10^7$ |
| Спирт | $2.7 cdot 10^7$ | Керосин | $4.6 cdot 10^7$ |
| Антрацит | $3.0 cdot 10^7$ | Водород | $12 cdot 10^7$ |
Возьмем табличное значение удельной теплоты сгорания нефти — $4.4 cdot 10^7 frac{Дж}{кг}$. Эта величина говорит нам о том, что при полном сгорании нефти массой $1 space кг$ выделяется $4.4 cdot 10^7 frac{Дж}{кг}$ энергии.
Формула для расчета количества теплоты, выделяемого при сгорании топлива
Для расчета полного количества теплоты, выделяемого при полном сгорании топлива некоторой массы, используют формулу:
$Q = qm$,
где $Q$ — выделяемое количество теплоты,
$q$ -удельная теплота сгорания топлива,
$m$ — масса сгораемого топлива.
Упражнения
Упражнение №1
Какое количество теплоты выделится при полном сгорании керосина объемом $2 space л$ и плотностью $800 frac{кг}{м^3}$?
Дано:
$V = 2 space л$
$rho = 800 frac{кг}{м^3}$
$q = 4.6 cdot 10^7 frac{Дж}{кг}$
СИ:
$2 cdot 10^{-3} space м^3$
$Q — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Формула для расчета количества теплоты:
$Q = qm$.
Массу выразим через объем и плотность: $m = rho V$.
Рассчитаем количество теплоты:
$Q = qrho V = 4.6 cdot 10^7 frac{Дж}{кг} cdot 800 frac{кг}{м^3} cdot 2 cdot 10^{-3} space м^3 = 7360 cdot 10^4 space Дж = 73.6 cdot 10^6 space Дж = 73.6 space МДж$.
Ответ: $Q = 73.6 space МДж$.
Упражнение №2
Вычислите массу сухих дров, если при их полном сгорании выделилось $70 000 space кДж$ энергии.
Дано:
$Q = 70 000 space кДж$
$q = 1.0 cdot 10^7 frac{Дж}{кг}$
СИ:
$7 cdot 10^7 space Дж$
$m — ?$
Посмотреть решение и ответ
Скрыть
Решение:
Из формулы $Q = qm$ выразим массу дров $m$:
$m = frac{Q}{q}$.
Рассчитаем:
$m = frac{7 cdot 10^7 space Дж}{1.0 cdot 10^7 frac{Дж}{кг}} = 7 space кг$.
Ответ: $m = 7 space кг$.
Топливо широко используется в промышленности и в быту.
Энергию топлива мы используем на заводах, для транспорта, для топки и т.д.
Почти все слышали выражение «двигатель внутреннего сгорания». Действительно,
ведь топливо сгорает, вследствие чего выделяется энергия. Этому и будет
посвящен наш урок.
При горении топлива происходит выделение углекислого
газа, который состоит из двух атомов кислорода и одного атома углерода. Для
того чтобы эти три атома соединились в молекулу требуется совершить работу (как
и для любого другого действия). Поэтому, при сгорании топлива выделяется
энергия.
Подобно удельной теплоёмкости, экспериментальным путём
установлено количество выделяемой энергии 1 кг того или иного топлива при
сгорании. В таблице дана удельная теплота сгорания некоторых веществ.
Заметим, что единицей измерения является Дж/кг. Из
этого можно сделать вывод, что для расчета количества теплоты, выделяемого
при сгорании того или иного вида топлива, нужно удельную теплоту сгорания
умножить на массу сгоревшего топлива. Как брать данные из таблицы мы уже
научились, поэтому рассмотрим примеры расчетов.
Задача 1. Сколько
выделится энергии при сгорании 4 кг нефти?
Задача 2. Известно,
что при сгорании природного газа выделилось 88 МДж теплоты. Найдите объём
сгоревшего газа, если его плотность составляет 0,85 кг/м3.
Задача 3. Находясь
на пикнике, вы хотите нагреть два 2 л воды до 50 ℃.
Для этого вы используете железный котел массой 3 кг и 4,5 кг дров. Хватит ли этого
количества дров, если учесть 70% энергии от сгорания дров передалось окружающей
среде, а начальная температура воды и котла 20 ℃.
Чтобы ответить на этот вопрос, нам нужно объединить
знания, полученные на прошлом уроке и на этом.