Содержание
|
1. |
3 |
|
2. |
5 |
|
2.1. |
5 |
|
2.2. |
6 |
|
2.3. |
6 |
|
2.4. |
7 |
|
2.5. |
7 |
|
2.6 |
9 |
|
2.7 |
11 |
|
3. |
15 |
|
3.1 |
15 |
|
3.2 |
16 |
|
3.3 |
18 |
|
3.4 |
18 |
|
3.5 |
19 |
|
3.6 |
19 |
|
4. |
20 |
|
5. |
26 |
Смесь
газов имеет массовый состав: N2
– 72 %, СО – 2 %, CO2
– 17 %,
H2O
– 9 %.
Определить:
а)
объемный состав смеси;
б)
газовую постоянную компонентов и смеси;
в)
кажущийся молекулярный вес смеси;
г)
парциальные давления компонентов смеси
в точке цикла 3;
д)
плотность и удельный объем компонентов
и смеси при заданных и нормальных
физических условиях;
е)
истинные теплоемкости смеси (мольную,
объемную и массовую при p
= const и v
= const) для заданной температуры;
ж)
средние теплоемкости смеси (мольную,
объемную и массовую).
2.1 Определение объемного состава смеси
Объемные
доли компонентов смеси ri
связаны с массовыми gi
зависимостью:
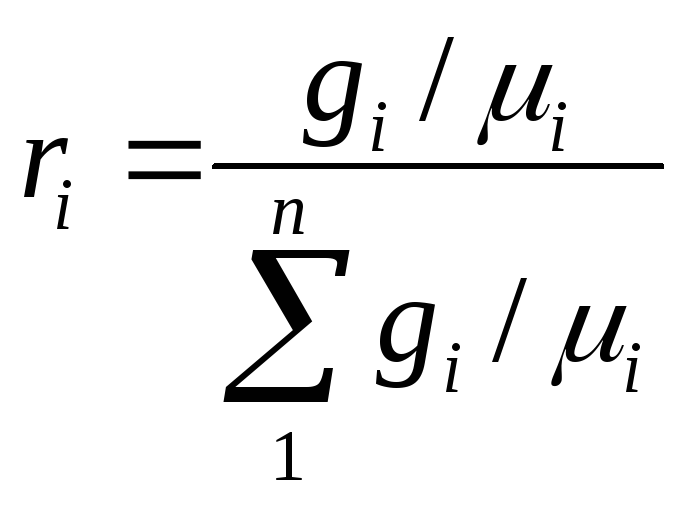 ,
,
где
µi
– молесулярные массы компонентов смеси.
Зная,
что
µN2
= 0,028
моль/кг; µCO
= 0,028
моль/кг;
µСО2
= 0,044
моль/кг; µН2О
= 0,018
моль/кг.
![]() (0,72/0,028)+(0,02/0,028)+(0,17/0,044)+(0,09/0,018)=35,292
(0,72/0,028)+(0,02/0,028)+(0,17/0,044)+(0,09/0,018)=35,292
![]() .
.
Отсюда:
![]() ;
;
![]() ;
;
![]() ;
;
![]() .
.
2.2
Газовые постоянные компонентов и смеси
Газовые
постоянные компонентов смеси рассчитываются
по зависимости:
![]() ,
,
где
![]() 8314
8314
![]() – универсальная газовая постоянная.
– универсальная газовая постоянная.
Тогда:
![]() 8314/0,028
8314/0,028
= 297
![]() ;
;
![]() 8314/0,028
8314/0,028
= 297
![]() ;
;
![]() 8314/0,044
8314/0,044
= 189
![]() ;
;
![]() 8314/0,018
8314/0,018
= 462
![]() .
.
Газовая
постоянная смеси определяется как:
![]() ,
,
Таким
образом получим:
![]() 297·0,72+297·0,02+189·0,17+462·0,09
297·0,72+297·0,02+189·0,17+462·0,09
= 293
![]() .
.
2.3
Кажущаяся молекулярная масса смеси
Кажущаяся
молекулярная масса смеси определяется
по выражению:
![]() ,
,
![]() 0,7286·0,028+0,0202·0,028+0,1095·0,044+0,1417·0,018
0,7286·0,028+0,0202·0,028+0,1095·0,044+0,1417·0,018
= 29,06
![]() .
.
2.4 Масса и парциальные
давления компонентов смеси по параметрам
газа в начальной точке расширения газа
в двигателе
Начальная
точка расширения газа – точка 3.
Определим
значение
![]() через начальные параметры состояния в
через начальные параметры состояния в
заданном цикле.
Для
процесса 1–2:
![]() ,
,
т.е.![]()
или
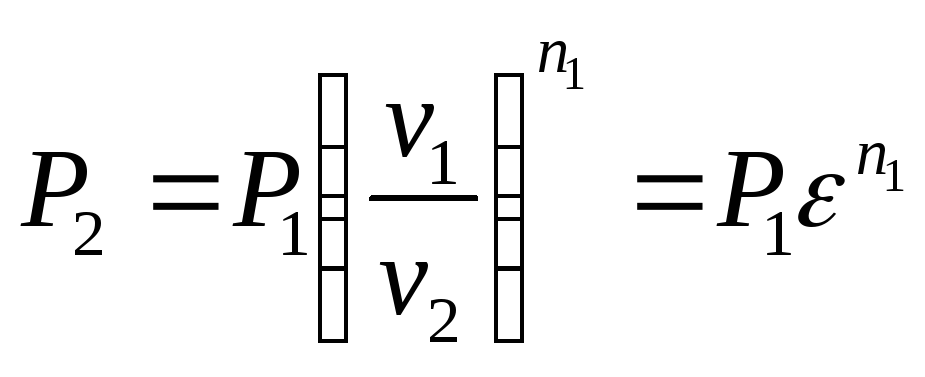 .
.
Для
процесса 2–3:
![]() ,
,
откуда![]() .
.
![]() 120
120
000·61,3·4
= 4 929 897 Па
Тогда
парциальные давления компонентов смеси:
![]()
![]() 4
4
929 897·0,7286 = 3 591 923 Па;
![]() 4
4
929 897·0,0202 = 99 584 Па;
![]() 4
4
929 897·0,1095 = 539 824 Па;
![]() 4
4
929 897·0,1417 = 698 566 Па.
2.5
Плотность и удельный объем компонентов
смеси при расчетных и нормальных
условиях.
Удельный
объем компонентов смеси можно определить
из выражения:
![]() .
.
![]() .
.
При
нормальных условиях
![]() (293·273)/101300
(293·273)/101300
= 0,7924
![]() .
.
Таким
образом, удельный
объем компонентов смеси при нормальных
условиях:
![]() 0,7286·0,7924
0,7286·0,7924
= 0,5773
![]() ;
;
![]() 0,0202·0,7924
0,0202·0,7924
= 0,0160
![]() ;
;
![]() 0,1095·0,7924
0,1095·0,7924
= 0,0868
![]() ;
;
![]() 0,1417·0,7924
0,1417·0,7924
= 0,1123
![]() .
.
Плотность
компонентов смеси при нормальных
условиях:
![]() .
.
Тогда:
![]() 0,72/0,5773
0,72/0,5773
= 1,247
![]() ;
;
![]() 0,02/0,016
0,02/0,016
= 1,250
![]() ;
;
![]() 0,17/0,0868
0,17/0,0868
= 1,959
![]() ;
;
![]() 0,09/0,1123
0,09/0,1123
= 0,801
![]()
Плотность
газовой смеси при нормальных условиях:
![]()
![]() 0,7286·1,247+0,0202·1,25+0,1095·1,959+0,1417·0,801
0,7286·1,247+0,0202·1,25+0,1095·1,959+0,1417·0,801
= 1,262
![]()
Определяем
![]() через начальные параметры состояния в
через начальные параметры состояния в
заданном цикле:
![]() ;
;
![]() ;
;![]() ;
;![]() ;
;![]() .
.
![]() 293·303/(120000·6)
293·303/(120000·6)
= 0,1233
![]() .
.
При
расчетных условиях удельные объемы
компонентов смеси:
![]() 0,7286·0,1233
0,7286·0,1233
= 0,0898
![]() ;
;
![]() 0,0202·0,1233
0,0202·0,1233
= 0,0025
![]() ;
;
![]() 0,1095·0,1233
0,1095·0,1233
= 0,0135
![]() ;
;
![]() 0,1417·0,1233
0,1417·0,1233
= 0,0175
![]() .
.
При
расчетных условиях плотности компонентов
смеси:
![]() 0,072/0,0898
0,072/0,0898
= 8,018
![]() ;
;
![]() 0,02/0,0025
0,02/0,0025
= 8,000
![]() ;
;
![]() 0,17/0,0135
0,17/0,0135
= 12,593
![]() ;
;
![]() 0,09/0,0175
0,09/0,0175
= 5,143
![]() .
.
Плотность
смеси при расчетных условиях составит:
![]() .
.
Тогда:
![]() 0,7286·8,018+0,0202·8+0,1095·12,593+0,1417·5,143
0,7286·8,018+0,0202·8+0,1095·12,593+0,1417·5,143
= 8,111
![]() .
.
2.6
Истинные теплоемкости смеси (массовые,
мольные и объемные) при постоянном
давлении и объеме.
В
точке 3:
![]() 4
4
929 897·0,1233/293 = 2075 К (1802 ºC).
Истинная
мольная теплоемкость при
![]() находиться по интерполяционным формулам
находиться по интерполяционным формулам
[1,c.40,
табл.4 и 5]:
![]() 32,7466+0,001652·2075
32,7466+0,001652·2075
= 35,723 ![]() ;
;
![]() 33,6991+0,0013406·2075
33,6991+0,0013406·2075
= 36,115
![]() ;
;
![]() 56,8768+0,002174·2075
56,8768+0,002174·2075
= 60,794
![]() ;
;
![]() 40,2393+0,005985·2075
40,2393+0,005985·2075
= 51,025
![]() .
.
Истинная
мольная теплоемкость газовой смеси при
![]() :
:
![]()
![]() 35,723·0,7286+36,115·0,202+60,115·0,1095+51,025·0,1417
35,723·0,7286+36,115·0,202+60,115·0,1095+51,025·0,1417
= 40,644
![]() .
.
Истинная
мольная теплоемкость газовой смеси при
![]() :
:
![]() ;
;
![]() .
.
Тогда:
![]() 40,644–28,3·293
40,644–28,3·293
= 32,352
![]() .
.
Истинная
массовая теплоемкость:
при
![]()
![]() 40,644/28,3
40,644/28,3
= 1,4362
![]() ;
;
при
![]()
![]() =32,352/28,3
=32,352/28,3
= 1,1432
![]() .
.
Истинная
объемная теплоемкость:
при
![]()
![]() 40,644/22,4
40,644/22,4
= 1,814
![]() ;
;
при
![]()
![]() 32,352/22,4
32,352/22,4
![]() .
.
2.7
Средняя теплоемкость смеси
![]() и
и![]() (массовая, мольная и объемная) в процессе
(массовая, мольная и объемная) в процессе
росширения газа в цикле двигателя
(процесс 3–4).
Для
определения средних теплоемкостей
процесса, необходимо рассчитать
теплоемкости смеси в начальной и конечной
точках процесса.
Точка
3:
![]() 2075
2075
К (1802 ºC).
Средняя
мольная теплоемкость при
![]() находиться по интерполяционным формулам
находиться по интерполяционным формулам
[1,c.40,
табл.4 и 5]:
![]() 29,7815+0,0016835·2075
29,7815+0,0016835·2075
= 29,782
![]() ;
;
![]() 30,4242+0,0015579·2075
30,4242+0,0015579·2075
= 33,232
![]() ;
;
![]() 48,4534+0,0030032·2075
48,4534+0,0030032·2075
= 53,865
![]() ;
;
![]() 34,5118+0,0045979·2075
34,5118+0,0045979·2075
= 42,797
![]() .
.
Средняя
мольная теплоемкость смеси при
![]() :
:
![]() ,
,
![]() 29,782·0,7286+33,232·0,0202+53,865·0,1095+42,797·0,1417
29,782·0,7286+33,232·0,0202+53,865·0,1095+42,797·0,1417
= 34,333
![]() .
.
Средняя
мольная теплоемкость смеси при
![]() :
:
![]() ;
;
![]() .
.
![]() 34,333–28,3·293
34,333–28,3·293
= 26,041
![]() .
.
Средняя
массовая теплоемкость смеси при
![]() :
:
![]() 34,333/28,3
34,333/28,3
= 1,2132
![]() ;
;
при
![]()
![]() 26,041/28,3
26,041/28,3
= 0,9202
![]() .
.
Средняя
объемная теплоемкость смеси:
при
![]()
![]() 34,333/22,4
34,333/22,4
= 1,533
![]()
при
![]()
![]() 26,041/22,4
26,041/22,4
= 1,163
![]() .
.
Точка
4:
![]() ;
;
![]() ;
;
![]() ;
;
 ;
;
![]() ;
;
![]() 1374
1374
К (1101 ºC).
Средняя
мольная теплоемкость при
![]() находиться по интерполяционным формулам
находиться по интерполяционным формулам
[1,c.40,
табл.4 и 5]:
![]() 29,7815+0,0016835·1374
29,7815+0,0016835·1374
= 31,631
![]() ;
;
![]() 30,4242+0,0015579·1374
30,4242+0,0015579·1374
= 32,139
![]() ;
;
![]() 48,4534+0,0030032·1374
48,4534+0,0030032·1374
= 50,044
![]() ;
;
![]() 34,5118+0,0045979·1374
34,5118+0,0045979·1374
= 39,576
![]() .
.
Средняя
мольная теплоемкость смеси при
![]() :
:
![]()
![]() 31,631·0,7286+32,139·0,0202+50,044·0,1095+39,576·0,1417
31,631·0,7286+32,139·0,0202+50,044·0,1095+39,576·0,1417
= 34,783
![]() .
.
при
![]()
![]() ;
;
![]() ;
;
![]() 34,783–28,3·293
34,783–28,3·293
= 26,491
![]() .
.
Средняя
массовая теплоемкость смеси:
при
![]()
![]() 34,783/28,3
34,783/28,3
= 1,229
![]() ;
;
при
![]()
![]() 26,491/28,3
26,491/28,3
= 0,936
![]() .
.
Средняя
объемная теплоемкость:
при
![]()
![]() 34,783/22,4
34,783/22,4
= 1,553
![]() ;
;
при
![]()
![]() 26,491/22,4
26,491/22,4
= 1,183
![]() .
.
Средняя
мольная теплоемкость процесса 3–4:
при
![]()
![]() ,
,
![]()
![]() ;
;
при
![]()
![]()
![]()
![]() .
.
Средняя
массовая теплоемкость процесса 3–4:
![]() 33,626/28,3
33,626/28,3
= 1,188
![]() ;
;
![]() 25,334/28,3
25,334/28,3
= 0,895![]() .
.
Средняя
объемная теплоемкость процесса 3–4:
![]() 33,626/22,4
33,626/22,4
= 1,501
![]() ;
;
![]() 25,334/22,4
25,334/22,4
= 1,131
![]() .
.
3.
РАСЧЕТ И ТЕРМОДИНАМИЧЕСКИЙ АНАЛИЗ ЦИКЛА
ГАЗОВОГО ДВИГАТЕЛЯ
Цикл
поршневого двигателя имеет следующие
характеристики:
![]() =30°C
=30°C
и давление 120 000 Па. Принимается за
рабочее тело воздух для процесса 1–2.
(![]() 1,004
1,004![]() ,
,![]() 0,716
0,716![]() ,R=287
,R=287
Дж/(кг град)), требуется:
-
определить
параметры цикла p,
v,
t,
u,
s,
i
для основных точек цикла; -
определить
с,
 ,q,
,q,
l
для каждого процесса входящего в цикл; -
найти
работу цикла, термический КПД и среднее
индикаторное давление; -
определить
среднеинтегральные температуры
процессов; -
изобразить
цикл на T–s
диаграмме.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Удельный объем газа
Количество вещества n характеризует число структурных элементов содержащихся в данной системе.
Это могут быть атомы, молекулы, а также ионы, электроны и другие частицы.
Единица количества вещества n является одной из основных единиц СИ.
Единица СИ количества вещества:
[ [n] = (моль) enspace основная enspace единица ]
Один моль – это такое количества вещества , в котором содержится столько же структурных элементов,
сколько атомов в 12 грамм изотопа углерода-12. В количестве вещества, равном один моль, содержится
6.022 × 1023 структурных элементов.
Часто бывает удобно относить объем и массу газа к количеству вещества.
Если
| m | масса газа, | кг |
|---|---|---|
| ρ | плотность газа, | кг/м3 |
| V | объем газа, | м3 |
| n | количество вещества (газа), | кмоль |
| M | молярная масса (отнесенная к количеству вещества), | кг/кмоль |
| Vm | молярный объем (отнесенный к количеству вещества), | м3/кмоль |
| υ | удельный объем газа, | м3/кг |
то
[ υ = frac{V}{m} ]
[ M = frac{m}{n} ]
[ V_m = frac{V}{n} ]
[ υ = frac{V_m}{M} = frac{V}{m} = frac{1}{ρ} ]
Вычислить, найти удельный объем газа по формуле (5)
Удельный объем газа |
стр. 531 |
|---|
Примеры решения задач по теме “Смеси идеальных газов”
1. Объемный состав газообразного топлива следующий: $H2 = 10$ %, $CH4 = 90$ %. Определить среднюю молекулярную массу и газовую постоянную смеси.
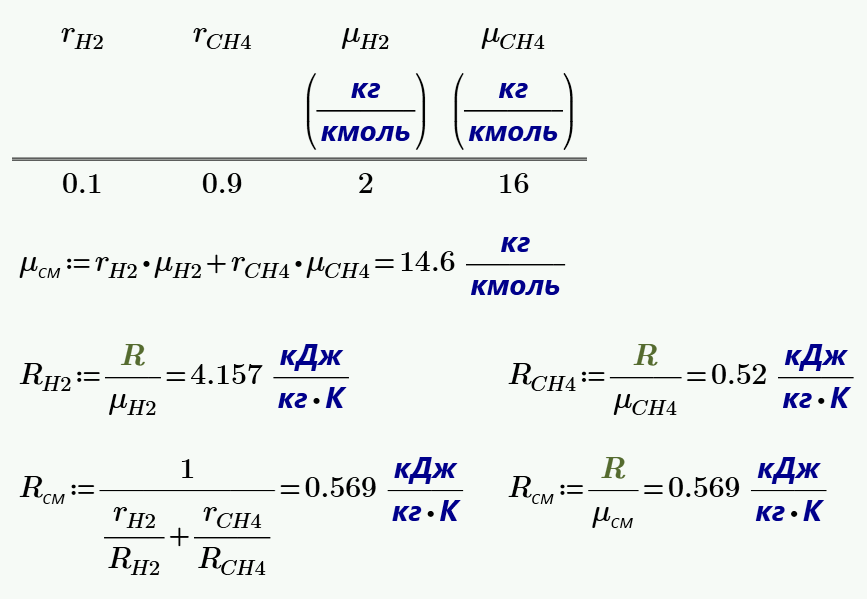
2. Объемный состав продуктов сгорания $СО2 = 12.3$ %; $O2 = 7.2$ %; $N2 = 80.5$ %. Определить плотность и удельный объем смеси при $t = 800$ °C и $P_{бар} = 740$ мм.рт.ст.

3. В резервуаре емкостью $V = 155$ м3 находится светильный газ при давлении $Р = 4$ ат и температуре $t = 18$ °C. Объемный состав газа $Н2 = 46$ %; $СН4 = 32$ %; $СО = 15$ %; $N2 = 7$ %. После израсходования некоторого количества газа давление его понизилось до $3.1$ ат, а температура упала до $12$ °С. Определить массу израсходованного газа.

4. Массовый состав смеси следующий: $СО2 = 18$ %; $O2 = 10$ %; $N2 = 72$ %. До какого давления нужно сжать эту смесь, находящуюся при нормальных условиях, чтобы при $t = 180$ °C $8$ кг ее занимали объем $40$ л?

5. Анализ продуктов сгорания топлива показал следующий объемный состав: $CO2 = 12.2$ %; $O2 = 7.1$ %; $CO = 10$ %; $N2 = 70.7$ %. Найти массовый состав газов, составляющих продукты сгорания.

6. В резервуаре объемом $10$ м3 находится газовая смесь, состоящая из $1$ кг кислорода и $39$ кг азота. Температура смеси равна $27$ °С. Определить парциальные давления компонентов смеси.

7. Плотность смеси азота и углекислого газа при давлении $1.4$ бар и температуре $45$ °C равна $2$ кг/м3. Определить массовый состав смеси.

8. Определить массовый состав газовой смеси, состоящей из углекислого газа и азота, если известно, что парциальное давление углекислого газа $p_{CO2}=120$ кПа, а давление смеси $p_{см}=300$ кПа.

9. Определить газовую постоянную, удельный объем газовой смеси и парциальные давления ее составяющих, если объемный состав смеси следующий: $CO_2=12$ %, $O_2= 8$ % и $N_2= 80$ %, а общее давление $p=100$ кПа и температура $t=40$ °C.

10. Газовая смесь имеет следующий массовый состав: $CO_2=12$ %, $O_2= 8$ % и $N_2= 80$ %. До какого давления нужно изотермически сжать эту смесь, находящуюся при нормальных условиях, чтобы плотность ее составляла $1.6$ кг/м3?