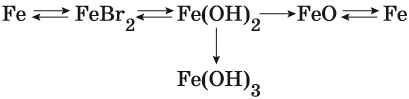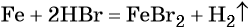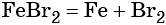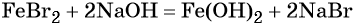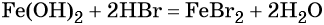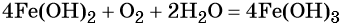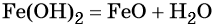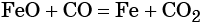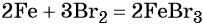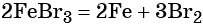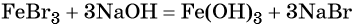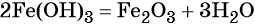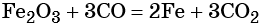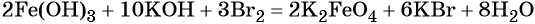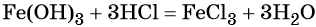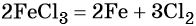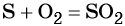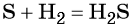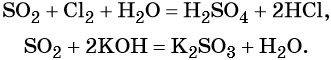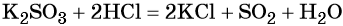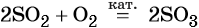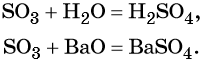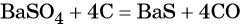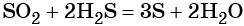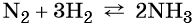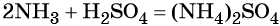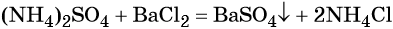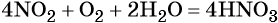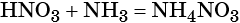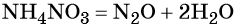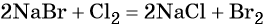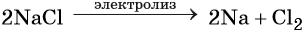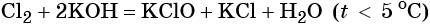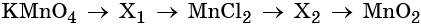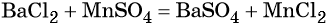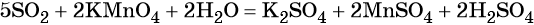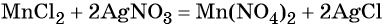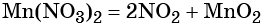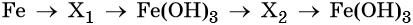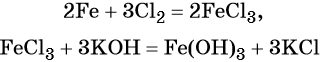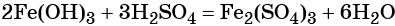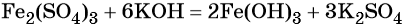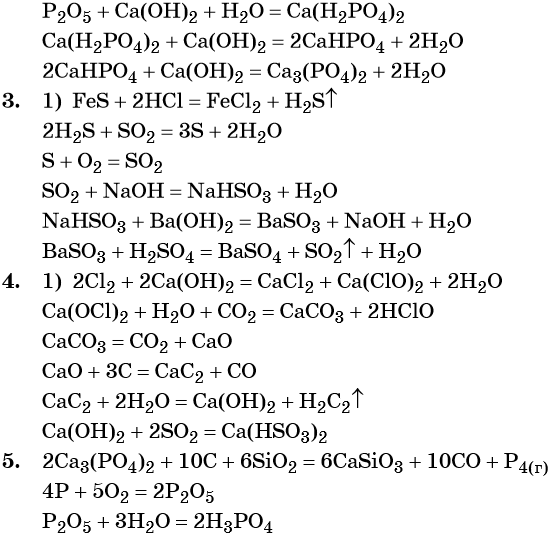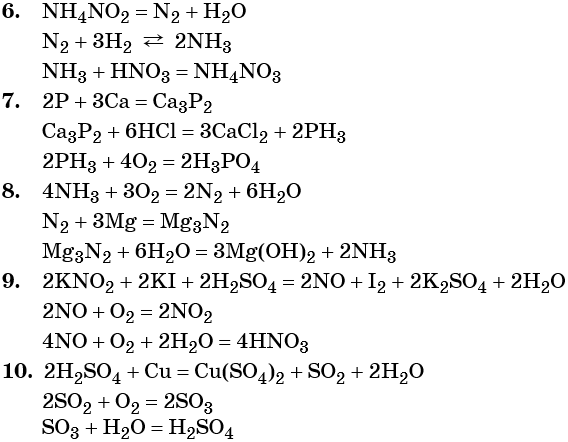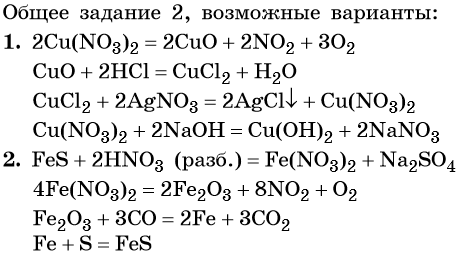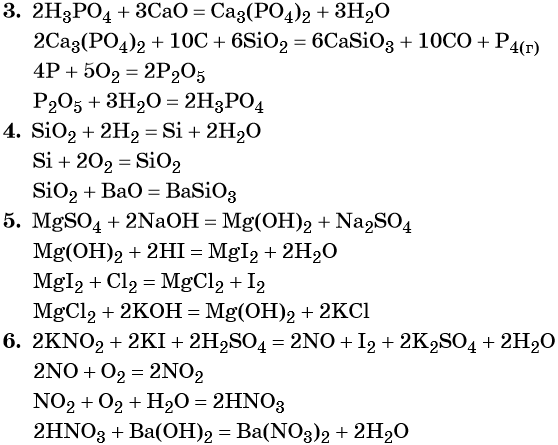Всего: 251 1–20 | 21–40 | 41–60 | 61–80 …
Добавить в вариант
Задания Д9 № 70
i
В схеме превращений:
Определите вещества X и Y:
1)
2)
3)
4)
Задания Д9 № 113
i
В схеме превращений:
определите вещества и
:
1)
2)
3)
4)
При сгорании 0,45 г газообразного органического вещества выделилось 0,448 л (н. у.) углекислого газа, 0,63 г воды и 0,112 л (н. у.) азота. Плотность исходного газообразного вещества по азоту 1,607. Установите молекулярную формулу этого вещества.
При полном сгорании углеводорода образовалось 27 г воды и 33,6 л (н. у.) углекислого газа. Относительная плотность углеводорода по аргону равна 1,05. Установите его молекулярную формулу.
При сгорании амина выделилось 0,448 л (н. у.) углекислого газа, 0,495 г воды и 0,056 л азота. Установите молекулярную формулу этого амина.
Определите вещества X и Y в схеме превращений:
1) X − SO2, Y − Cl2
2) X − FeSO4, Y − AgCl
3) X − H2SO4, Y − ВаСl2
4) X − SO3, Y − HCl
Определите вещества X и Y в схеме превращений:
1) X − Cl2, Y − NaOH
2) X − HCl, Y − Cu(OH)2
3) X − CuCl2, Y − KOH
4) X − MgCl2, Y − H2O
Дана схема превращений:
Определите вещества X и Y
1) X − I2, Y − HBr
2) X − Cl2, Y − HBrO
3) X − Cl2, Y − HBr
4) X − I2, Y − HBrO
Дана схема превращений:
CO2 K2CO3
KNO3
Определите вещества X и Y.
1) Х − KCl, Y − Ca(NO3)2
2) X − NaHSO3, Y − H2SO4
3) X − KOH, Y − HNO3
4) X − K2O, Y − NaNO3
Определите вещества X и Y в схеме превращений:
1)
2)
3)
4)
Определите вещества X и Y в схеме превращений:
1)
2)
3)
4)
Определите конечное вещество Y в схеме превращений:
1)
2)
3)
4)
Определите конечное вещество Y в схеме превращений:
1)
2)
3)
4)
Определите вещества X и Y в схеме превращений.
1)
2)
3)
4)
Определите вещества X и Y в схеме превращений.
1)
2)
3)
4)
Определите вещества X и Y в схеме превращений.
1)
2)
3)
4)
Определите вещества X и Y в схеме превращений.
1)
2)
3)
4)
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующим буквам:
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами и
.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующим буквам.
Задана следующая схема превращений веществ:
Определите, какие из указанных веществ являются веществами X и Y.
1)
2)
3)
4)
5)
Запишите в ответ цифры, расположив их в порядке, соответствующим буквам:
Всего: 251 1–20 | 21–40 | 41–60 | 61–80 …
ЦЕПОЧКИ ПРЕВРАЩЕНИЙ: КАКИЕ БЫВАЮТ И ОСНОВНОЙ АЛГОРИТМ РЕШЕНИЯ
Цепочки превращений – вид качественных задач по химии.
ОСНОВНЫЕ РАЗНОВИДНОСТИ ЦЕПОЧЕК ПРЕВРАЩЕНИЙ
Можно выделить несколько основных разновидностей подобных задач:
1. Цепочки превращений, в которых известны все вещества
Предлагаются формулы конкретных химических веществ. Формулы дают представление о том, к какому (каким) классу (классам) веществ относятся участники цепочки. Это значительно упрощает ее решение. И это, пожалуй, самый простой вид цепочек превращений.
2. Цепочки с неизвестными веществами
Одно из веществ цепи может быть не известно и зашифровано с помощью какой-либо буквы (латиница или кириллица). В таком случае, над стрелкой указывается вещество, которое необходимо добавить к предыдущему, чтобы получилось зашифрованное вещество. Если этого не делать, то можно предположить несколько вариантов решения.
Очень часто вместо химических формул предлагаются названия соединений. Это очень полезно для отработки знаний их номенклатуры и умений по названию определять принадлежность к определенному классу. Например:
В цепочках данного вида могут быть не известны несколько веществ или даже все, кроме одного, например, исходного.
3. Цепочки превращений, в которых указаны только степени окисления основного химического элемента
Многие химические элементы имеют несколько степеней окисления. Подобные задачи направлены на знание окислительно-восстановительных свойств веществ и на отработку умений составлять окислительно-восстановительные реакции.
4. Цепочки превращений с неизвестными промежуточными веществами
В подобных случаях предлагаются только исходное вещество и конечный продукт. Так, в данном примере из пропана напрямую получить этиловый эфир аланина невозможно. Промежуточных стадий получения конечного продукта может быть несколько. Это определяет тот, кто решает данную цепочку превращений. Ясно, что и путей решения может быть несколько.
ЦЕПОЧКИ ПРЕВРАЩЕНИЙ: ОСНОВНОЙ АЛГОРИТМ РЕШЕНИЯ
Главное правило в решении любой цепочки превращений: из каждого предыдущего вещества необходимо получить следующее за ним.
На конкретном примере рассмотрим основной алгоритм решения:
1) записываем цепочку;
2) под формулами веществ подписываем их названия;
3) над стрелками ставим номера реакций;
4) решаем цепочку, записывая каждую реакцию под своим номером;
5) если требуется, над стрелками в реакциях указываем условия протекания реакций.
Цепочки превращений направлены на закрепление и углубление знаний химических свойств веществ и способов их получения. Они помогают развивать логическое мышление, память, умение выявлять закономерности. Часто требуют не стандартного подхода к решению.
Если вам известны другие виды цепочек превращений, пожалуйста, напишите в комментариях.
Продолжение следует…
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
|
FeO –> X –> FeCl2 ?? 1 ) Fe2O3 2)FeCl3 3) Fe 4) Fe(OH)3 пожалуйста с решением ! ) В реальности ответов несколько. Если я правильно понимаю логику составителей этого теста, они от вас хотят вот такого порядка реакций: FeO + C = Fe + CO Fe + 2HCl = FeCl2 + H2 Именно поэтому они остальные ответы дали с трехвалентным железом. автор вопроса выбрал этот ответ лучшим Michiru 9 лет назад Из этих ответов самый подходящий – fecl3 Поскольку это единственное растворимое вещество Feo + HCl + KMnO4 = FeCl3 + MnCl2 + H2O + KCl FeCl3 + Fe = FeCl2 Знаете ответ? |
xthipery
Вопрос по химии:
Определить вещество «Х» из схемы превращения: C → X → CaCO3
а)CO2 б)CO в)CaO г)O2
Определить вещество «Y» из схемы превращения: Na → Y→NaOH
а)Na2O б)Na2O2 в)H2O г)Na
В схеме превращения: CuCl2 → A → B→ Cu формулами промежуточных продуктов А и В являются: а)CuO и Cu(OH)2 б)CuSO4 и Cu(OH)2
в)CuCO3 и Cu(OH)2 г)Cu(OH)2 и CuO
Конечным продуктом в цепочке превращений на основе соединений углерода:
CO2 → X1 → X2 → NaOH
а)карбонат натрия б)гидрокарбонат натрия
в)карбид натрия г)ацетат натрия
Элементом «Э», участвующим в цепочке превращений:
Э → Э2О5 → Н3ЭО4 → Na3ЭO4
а)N б) Mn в)P г)Cl
Трудности с пониманием предмета? Готовишься к экзаменам, ОГЭ или ЕГЭ?
Воспользуйся формой подбора репетитора и занимайся онлайн. Пробный урок – бесплатно!
Ответы и объяснения 1
zigrlede540
1) В
2)А
3)Г
4)Х2 надо?
5) В
Знаете ответ? Поделитесь им!
Гость ?
Как написать хороший ответ?
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете
правильный ответ; - Писать подробно, чтобы ответ был исчерпывающий и не
побуждал на дополнительные вопросы к нему; - Писать без грамматических, орфографических и
пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся
уникальные и личные объяснения; - Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не
знаю» и так далее; - Использовать мат – это неуважительно по отношению к
пользователям; - Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует?
Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие
вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи –
смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Взаимосвязь различных классов неорганических веществ
Рассмотрим её на нескольких примерах.
Пример 1. Взаимосвязь соединений железа.
Переход из железа в бромид железа (II) возможен при реакции железа с бромоводородной кислотой:
Получить из бромида железа (II) чистое железо можно при электролизе расплава:
При добавлении к бромиду железа (II) щёлочи образуется гидроксид железа (II):
Обратный переход возможен при взаимодействии гидроксида железа (II) с бромоводородной кислотой:
Окисление гидроксида железа (II) приводит к гидроксиду железа (III):
При нагревании гидроксид железа (II) теряет воду, превращаясь в оксид железа (II):
Восстановление оксида железа (II) приводит к железу:
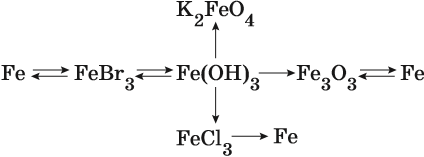
Пример 2. Взаимосвязь соединений железа.
Реакция железа с бромом приводит к бромиду железа (III):
Получить из этого соединения железо можно электролизом расплава:
Переход из бромида железа (III) в гидроксид железа (III) возможен под действием щёлочи:
При нагревании гидроксид железа (III) теряет воду, превращаясь в оксид железа (III):
Восстановлением оксида железа (III) можно получить железо:
Железо в степени окисления +6 можно получить из гидроксида железа (III) по реакции:
Гидроксид железа (III) под действием соляной кислоты переходит в хлорид железа (III):
Из хлорида железа (III) электролизом можно получить железо:
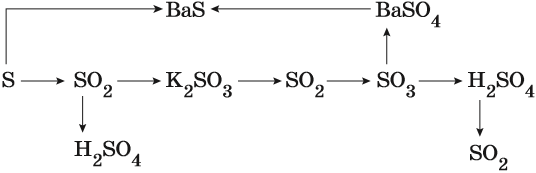
Пример 3. Взаимосвязь соединений серы.
Сера окисляется кислородом воздуха до оксида серы (IV):
Взаимодействие серы с водородом приводит к сероводороду:
Оксид серы (IV) может вступить в окислительно-восстановительную реакцию с образованием серной кислоты или в обменную реакцию с образованием сульфита калия:
Под действием сильных кислот сульфит калия разлагается до SO2:
Каталитическое окисление SO2 приводит к оксиду серы (VI):
Из оксида серы (VI) можно получить как серную кислоту, так и сульфат бария:
Из сульфата бария восстановлением углём можно получить сульфид бария:
Восстановление SO2 приводит к сере:
Пример 4. Осуществить следующую цепочку превращений: N2 → NH3 → (NH4)2SO4 → NH4Cl.
Азот взаимодействует с водородом при повышенной температуре в присутствии катализатора с образованием аммиака:
Реакция газообразного аммиака с серной кислотой приводит к сульфату аммония:
При взаимодействии водных растворов сульфата аммония и хлорида бария образуется нерастворимый сульфат бария, эта реакция идёт до конца. После отделения осадка и упаривания водного раствора можно выделить чистый хлорид аммония:
Пример 5. Осуществить следующую цепочку превращений: NO2 → HNO3 → NH4NO3 → N2O.
Оксид азота (IV) при взаимодействии с кислородом и водой даёт азотную кислоту:
При реакции азотной кислоты с аммиаком образуется нитрат аммония:
Контролируемое разложение нитрата аммония приводит к образованию оксида азота (I) и воды:
Пример 6. Осуществить следующую цепочку превращений: NaBr → NaCl → Cl2 → KClO.
Хлор способен вытеснять бром из бромидов:
Электролиз расплава хлорида натрия приводит к образованию молекулярного хлора:
Гипохлорид калия образуется при взаимодействии газообразного хлора с водным раствором гидроксида калия при охлаждении:
Особенностью заданий, в которых требуется определить неизвестное вещество Х как промежуточный продукт в цепочке химических превращений, является принципиальная возможность наличия нескольких правильных ответов. Вам нужно обосновать свой выбор.
Пример 7. Предложите формулы неизвестных веществ в приведённых ниже последовательностях химических превращений и обоснуйте этот выбор. Приведите уравнения химических реакций, с помощью которых эти превращения можно осуществить:
Каким же может быть вещество X1? Возможны несколько вариантов. Предположим, что марганец в этом соединении имеет степень окисления +2, тогда этим веществом будет, например, сульфат марганца (II). Почему? Из него удобно получит хлорид марганца (II) с помощью обменной реакции:
Данная реакция пойдёт до конца, потому что сульфат бария выпадет в осадок.
Перманганат калия — сильный окислитель, который при реакции с восстановителем в кислой среде может понизить свою степень окисления до +2. Чтобы получить сульфат марганца (II) из перманганата калия, можно использовать окислительно-восстановительную реакцию:
Другой вариант ответа:
Из хлорида марганца (II) можно получить нитрат марганца (II) с помощью обменной реакции с нитратом серебра. Эта реакция идёт до конца благодаря образованию нерастворимого хлорида серебра:
Термическое разложение нитрата марганца (II) — обычный способ получения оксида марганца (IV):
Пример 8. Предложите формулы неизвестных веществ в приведённых ниже последовательностях химических превращений и обоснуйте этот выбор. Приведите уравнения химических реакций, с помощью которых эти превращения можно осуществить:
Наиболее рациональным вариантом будет следующий. Вначале железо под действием хлора окисляется до хлорида железа (III) (вещество X1), из которого по обменной реакции получают гидроксид железа (III):
Веществом (X2) может быть любая растворимая соль железа (III), например сульфат, нитрат и т. д.:
Под действием расчётного количества щёлочи в осадок выпадает гидроксид железа (III):
Тренировочные задания
Общее задание 1. Составьте уравнения реакций, с помощью которых можно осуществить следующие цепочки превращений:
1. Al → AlCl3 → Al(OH)3 → KAlO2 → K[Al(OH)4] → Al(OH)3.
2. Ca3(PO4)2 → P → P2O5 → → Ca(H2PO4)2 → CaHPO4 → Ca3(PO4)2.
3. FeS → H2S → S → SO2 → NaHSO3 → BaSO3 → BaSO4.
4. Cl2 → CaOCl2 → CaCO3 → CaO → → CaC2 → Ca(OH)2 → Ca(HSO3)2.
5. Ca3(PO4)2 → P → P2O5 → H3PO4.
6. NH4NO2 → N2 → NH3 → NH4NO3.
7. P → Ca3P2 → PH3 → H3PO4.
8. NH3 → N2 → Mg3N2 → NH3.
9. KNO2 → NO → NO2 → HNO3.
10. H2SO4 → SO2 → SO3 → H2SO4.
11. HCl → Cl2 → KClO3 → Cl2.
12. Cl2 → NaCl → HCl → AlCl3.
13. KCl → Cl2 → NaClO → NaClO3.
14. HBr → NaBr → Br2 → HBr.
15. KBr → Br2 → HBr → NaBr.
16. NaCl → HCl → Cl2 → KClO3.
17. Mg → Mg3N2 → NH3 → Al(OH)3.
18. Ba(NO3)2 → Fe(NO3)2 → Fe2O3 → Fe.
Общее задание 2. Предложите формулы неизвестных веществ в приведённых ниже последовательностях химических превращений и обоснуйте ваш выбор. Приведите уравнения химических реакций, с помощью которых эти превращения можно осуществить:
1. Cu(NO3)2 → X1 → CuCl2 → X2 → Cu(OH)2.
2. FeS → X1 → Fe2O3 → X2 → FeS.
3. H3PO4 → X1 → P → X2 → H3PO4.
4. SiO2 → Si → X → BaSiO3.
5. MgSO4 → X1 → MgI2 → X2 → Mg(OH)2.
6. KNO2 → X1 → NO2 → X2 → Ba(NO3)2.