Главная » Вопросы и ответы» Школа » Химия
Напишите изомеры пентана
|
Напишите изомеры пентана. |
Рейтинг: 2.7/6 |
|
« Назад
| Следующий » Просмотров: 11715 | Добавил: аgent (08.12.2019) (Изменено: 08.12.2019) |
|
Всего ответов: 3 |
|
Обсуждение вопроса:Всего ответов: 3 Порядок вывода комментариев:
0 buzz Запишем все изомеры пентана (С₅Н₁₂). Пентан относится к классу алканов, значит везде будут одинарные связи. Нравится
0 Oleg74 Три изомера пентана (С₅Н₁₂): Нравится
0 Forget Все изомеры пентана: Нравится |
|
Войдите:
Напишите структурные формулы всех изомеров пентана и назовите их.
Чефонова Юлия
Мыслитель
(9016),
закрыт
11 лет назад
Лучший ответ
Штирлиц
Высший разум
(317505)
11 лет назад
CН3-СН2-СН2-СН2-СН3 пентан
СН3-СН2-СН (СН3)-СН3 2-метиобутан
СН3-С (СН3)2-СН3 2,2-диметилпропан
Остальные ответы
Kaa
Гений
(58556)
11 лет назад
Смотреть здесь
http://ru.wikipedia.org/wiki/Пентан
Похожие вопросы
Пентан C5H12 – это предельный углеводород, содержащий пять атомов углерода в углеродной цепи. Бесцветная жидкость с характерным запахом, нерастворим в воде и не смешивается с ней.
CH3-CH2-CH2-CH2-CH3
Гомологический ряд пентана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение пентана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp3:
При образовании связи С–С происходит перекрывание sp3-гибридных орбиталей атомов углерода:
При образовании связи С–H происходит перекрывание sp3-гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp3-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109о 28′ друг к другу:
Это соответствует тетраэдрическому строению.
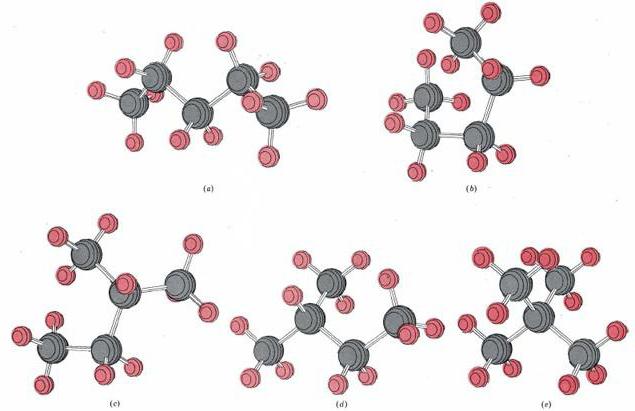
Например, в молекуле пентана C5H12 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет имеет зигзагообразное строение.
Изомерия пентана
Структурная изомерия
Для пентана характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
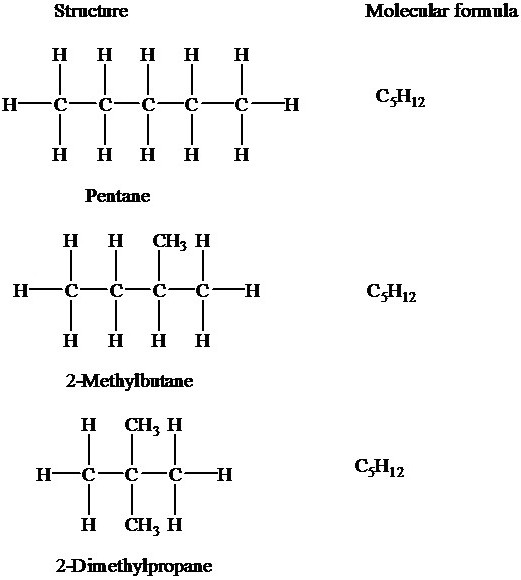
Для углеводородов состава С5Н12 существуют три изомера углеродного скелета: н-пентан, метилбутан (изопентан), диметилпропан (неопентан)
| Пентан | Изопентан |
| CH3-CH2-CH2-CH2-CH3 | CH3-CH(CH3)-CH2-CH3 |
Для пентана не характерна пространственная изомерия.
Химические свойства пентана
Пентан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для пентана характерны реакции:
- разложения,
- замещения,
- окисления.
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для пентана характерны радикальные реакции.
Пентан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Пентан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании пентана образуется смесь хлорпроизводных.
CH3-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CH2-CH2-CH2Cl + HCl
CH3-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CH2-CHCl-CH3 + HCl
CH3-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CHCl-CH2-CH3 + HCl
Бромирование протекает более медленно и избирательно.
С третичный–Н > С вторичный–Н > С первичный–Н
CH3-CH2-CH2-CH2-CH3 + Br2 → CH3-CH2-CH2-CHBr-CH3 + HBr
CH3-CH2-CH2-CH2-CH3 + Br2 → CH3-CH2-CHBr-CH2-CH3 + HBr
1.2. Нитрование пентана
Пентан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в пентане замещается на нитрогруппу NO2.
Например. При нитровании пентана образуются преимущественно 2-нитропентан и 3-нитропентан:
CH3-CH2-CH2-CH2-CH3 + HNO3 → CH3-CH2-CH2-CHNO2-CH3 + H2O
CH3-CH2-CH2-CH2-CH3 + HNO3 → CH3-CH2-CHNO2-CH2-CH3 + H2O
2. Дегидрирование пентана
Дегидрирование – это реакция отщепления атомов водорода.
В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др.
Алканы с длинным углеродным скелетом, содержащие 5 и более атомов углерода в главной цепи, при дегидрировании образуют циклические соединения.
При этом протекает дегидроциклизация – процесс отщепления водорода с образованием замкнутого цикла.
Пентан и его гомологи, содержащие пять атомов углерода в главной цепи, при нагревании над платиновым катализатором образуют циклопентан и его гомологи:
3. Окисление пентана
Пентан– слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.).
3.1. Полное окисление – горение
Пентан горит с образованием углекислого газа и воды. Реакция горения пентана сопровождается выделением большого количества теплоты.
C5H12 + 😯2 → 5CO2 + 6H2O + Q
Уравнение сгорания алканов в общем виде:
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
При горении пентана в недостатке кислорода может образоваться угарный газ СО или сажа С.
Получение пентана
1. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении.
R–COONa + NaOH → R–H + Na2CO3
Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты.
При взаимодействии гексаноата натрия с гидроксидом натрия при сплавлении образуются пентан и карбонат натрия:
CH3–CH2–CH2–CH2–CH2–COONa + NaOH → CH3–CH2–CH2–CH2–CH3 + Na2CO3
3. Гидрирование алкенов и алкинов
Пентан можно получить из пентена или пентина:
При гидрировании пентена-1 или пентена-2 образуется пентан:
CH2=CH-CH2-CH2-CH3 + H2 → CH3-CH2-CH2-CH2-CH3
CH3-CH=CH-CH2-CH3 + H2 → CH3-CH2-CH2-CH2-CH3
При полном гидрировании пентина-1 или пентина-2 также образуется пентан:
CH≡C-CH2-CH2-CH3 + 2H2 → CH3-CH2-CH2-CH2-CH3
CH3-C≡C-CH2-CH3 + 2H2 → CH3-CH2-CH2-CH2-CH3
4. Синтез Фишера-Тропша
Из синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды:
nCO + (3n+1)H2 = CnH2n+2 + nH2O
Это промышленный процесс получения алканов.
Из угарного газа и водорода можно получить пентан:
5CO + 11H2 = C5H12 + 5H2O
5. Получение пентана в промышленности
В промышленности пентан получают из нефти, каменного угля, природного и попутного газа. При переработке нефти используют ректификацию, крекинг и другие способы.
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 15 сентября 2022 года; проверки требуют 3 правки.
| Пентан | ||
|---|---|---|
|
||
| Общие | ||
| Хим. формула | C5H12 | |
| Физические свойства | ||
| Молярная масса | 72.15 г/моль | |
| Плотность | 0,6262 (20°С) | |
| Энергия ионизации | 10,34 ± 0,01 эВ[2] | |
| Термические свойства | ||
| Температура | ||
| • плавления | −129,72 °C | |
| • кипения | 36,07 °C | |
| • вспышки | −49 °C | |
| Пределы взрываемости | 1,5 ± 0,1 об.%[2] | |
| Энтальпия | ||
| • кипения | 26,43 кДж/моль[1] | |
| Давление пара | 420 ± 1 мм рт.ст.[2] | |
| Классификация | ||
| Рег. номер CAS | 109-66-0 | |
| PubChem | 8003 | |
| Рег. номер EINECS | 203-692-4 | |
| SMILES |
CCCCC |
|
| InChI |
InChI=1S/C5H12/c1-3-5-4-2/h3-5H2,1-2H3 OFBQJSOFQDEBGM-UHFFFAOYSA-N |
|
| RTECS | RZ9450000 | |
| ChEBI | 37830 | |
| Номер ООН | 1265 | |
| ChemSpider | 7712 | |
| Безопасность | ||
| NFPA 704 |
4 1 0 |
|
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | ||
Пентаны — насыщенные ациклические углеводороды класса алканов. Имеют пять атомов углерода в молекуле (от др.-греч. πέντε — пять).
Изопентан обладает наркотическим действием. Класс опасности четвёртый[3].
Нормальный пентан и изопентан представляют собой легколетучие подвижные жидкости с характерным запахом, неопентан — бесцветный газ с характерным запахом.
Изомерия[править | править код]
У пентана существуют 3 структурных изомера:
| название | формула | структурная
формула |
температура
плавления, °С |
температура
кипения, °С |
плотность
при 20 °C, г/см³ |
октановое
число (ИМ) |
октановое
число (ММ) |
| н-пентан | CH3(CH2)3CH3, | −129,72 | 36,07 | 0,6260 | 61,7 | 61,9 | |
| 2-метилбутан
(изопентан) |
(CH3)2CHCH2CH3 | −159,89 | 27,85 | 0,6197 | 92,3 | 90,3 | |
| 2,2-диметилпропан
(неопентан) |
(CH3)4C | −16,55 | 9,50 | 0,613 (0°С) | 85,5 | 83,0 |
ИМ — исследовательский метод
ММ — моторный метод
Пентил С5Н11 — одновалентный радикал пентана.
Получение[править | править код]
Пентаны выделяют из конденсатов природного газа, из нефти, лёгких погонов сланцевой смолы, из углеводородов, синтезируемых из CO и H2 (синтез-газа).
Применение[править | править код]
Пентановую фракцию используют как сырьё для процесса изомеризации. н-Пентан при этом превращается в смесь изомеров. Обогащенная изопентанами фракция используется как компонент бензинов или служит для выделения изопентана — сырья для получения изопрена, который является мономером для синтеза синтетических каучуков. Также пентаны в составе прямогонных бензиновых фракций нефти используются при производстве нефтяных растворителей.
См. также[править | править код]
- Пентен
- Циклопентан
Примечания[править | править код]
- ↑ (unspecified title)
- ↑ 1 2 3 http://www.cdc.gov/niosh/npg/npgd0486.html
- ↑ Газохроматографическое измерение массовых концентраций углеводородов: метана, этана, этилена, пропана, пропилена, нбутана, альфа-бутилена, изопентана в воздухе рабочей зоны. Методические указания. МУК 4.1.1306-03 (УТВ. ГЛАВНЫМ ГОСУДАРСТВЕННЫМ САНИТАРНЫМ ВРАЧОМ РФ 30.03.2003) (недоступная ссылка)
Литература[править | править код]
- Р. Д. Оболенцев. Физические константы углеводородов жидких топлив и масел. 2-е изд. Гостоптехиздат, 1953.
Прежде чем рассматривать основные формулы изомеров пентана, выявим, к какому классу органических веществ принадлежит это соединение. Кроме того, определим, какими особенностями строения обладает данное вещество, каковы основные области его применения.
Общая характеристика
Пентан, изомеры которого мы будем рассматривать, принадлежит к классу насыщенных (предельных) углеводородов. Они имеют формулу CnH2n+2, sp3 гибридизацию углеродных атомов, одинарные связи. Среди свойств, характерных для представителей данного класса, включая пентан, изомеры которого также принадлежат к классу алканов, выделим реакции радикального замещения (галогенирования).
Номенклатура соединений
Разработан определенный порядок действий, согласно которому можно дать название любому предельному углеводороду. Прямой углеродный скелет имеет сам пентан, изомеры его отличаются наличием радикалов (ответвлений) от основной цепи.
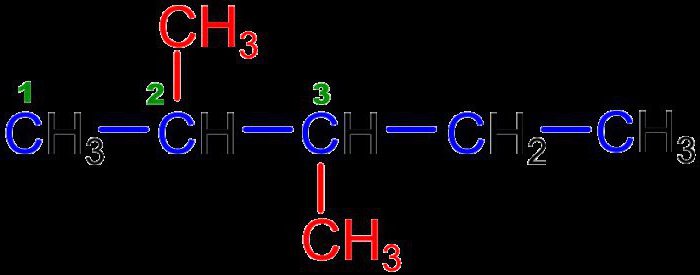
Сначала потребуется выбрать самую длинную углеродную цепочку. Для нумерации углеродных атомов выбирают ту часть, в которой ближе к началу располагаются радикалы. При наличии разветвлений с обеих сторон главной цепи учитывают количество радикалов, а также их строение (используют русский алфавит).
При наличии нескольких одинаковых углеводородных радикалов после указания цифрами места их расположения используют уточняющие приставки: ди-, три-, тетра.
Только после того, как будут указаны все активные частицы, дают название основной углеродной цепи.
Структуры пентана
Составим основные структурные формулы изомеров пентана, используя общепринятый алгоритм. Для начала расположим углеродные атомы в одну цепь, получим структурную формулу нормального пентана: СН3-(СН2)3-СН3.
Если оставить в основной цепи четыре атома углерода, оставшийся будет представлен в виде радикала СН3. В таком случае можно составить две структурные формулы веществ, отличающиеся друг от друга расположением метильных групп: 2-метилбутана, 3-метилбутана.
Как еще может выглядеть пентан? Изомеры, отвечающие формуле С5Н12, могут быть представлены и 2,2-диметилпропаном.
Все эти вещества отвечают одной общей формуле CnH2n+2, следовательно, принадлежат к классу предельных углеводородов (алканов), являются структурными изомерами.
Явление изомерии объясняет существование нескольких веществ, имеющих одну общую формулу, но отличающихся друг от друга расположением атомов в молекуле. Структурные изомеры имеют некоторые отличия и в реакционной способности, несмотря на принадлежность к одному классу углеводородов.
Заключение
Пентан, изомеры которого мы рассмотрели, является типичным представителем парафинов. Для данного класса органических веществ не характерна изомерия кратной связи. Насыщенные углеводороды не имеют межклассовых изомеров. Среди основных отраслей, в которых востребован пентан и его структурные изомеры, выделим химическую промышленность.
При изомеризации пентана получают 2-метилбутан, дегидрирование которого приводит к получению непредельного углеводорода, принадлежащего к ряду с общей формулой CnH2n-2. Полимеризация данного непредельного СхНу является промышленным способом получения синтетического полимера, используемого при производстве резины.
Среди многочисленных сфер использования насыщенных алканов, типичным представителем которых является нормальный пентан, выделим и применение данного соединения в качестве природного топлива. В заключение отметим, что для представителей предельного ряда углеводородов, характерна изомерия главной цепи. В связи с тем, что в молекуле нет двойных связей, для парафинов не характерна геометрическая изомерия, то есть нет цис- и транс-изомеров.