Как определить заряд атома
Заряд атома, наряду с его квантовыми числами, является одной из важнейших числовых характеристик атома. Знание заряда атома необходимо для решения различных задач электростатики, электродинамики, атомной и ядерной физики.

Вам понадобится
- Знание структуры атома, атомный номер
Инструкция
Атом любого вещества состоит из электронной оболочки и ядра. Ядро состоит из двух типов частиц – нейтронов и протонов. Нейтроны не имеют электрического заряда, то есть электрический заряд нейтронов не равен нулю. Протоны являются положительно заряженными частицами и имеют электрический заряд, равный +1. Количество протонов характеризует атомный номер данного атома..
Электронная оболочка ядра состоит из электронных орбиталей, на которых расположено разное количество электронов. Электрон – отрицательно заряженная элементарная частица. Ее электрический заряд равен -1.
Для того чтобы определить заряд атома, необходимо знать его структуру – количество протонов в ядре и количество электронов в электронной оболочке. Суммарный заряд атома получается в результате алгебраического суммирования зарядов входящих в него протонов и электронов.
Как правило, атом является электронейтральным, то есть количество протонов в нем равно количеству электронов. Заряд такого атома, очевидно, равен нулю. Пример – атом водорода H состоит из одного протона и одного электрона. Q = 1+(-1) = 0 – заряд электронейтрального водорода.
В силу некоторых причин количество протонов и электронов в атоме может не совпадать. В этом случае атом является положительно или отрицательно заряженным ионом. Например, положительный ион натрия имеет 11 протонов и 10 электронов. Его заряд Q = 11+(-10) = 1.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Когда атом имеет одинаковое количество положительных и отрицательных частиц, он имеет нейтральный заряд. Но если у атома есть лишние электроны или отсутствуют электроны, он называется ионом и может иметь положительный или отрицательный заряд. Проще говоря, если нет электронов, атом имеет положительный заряд. Если атом содержит электроны, он имеет отрицательный заряд.
TL; DR (слишком долго; не читал)
Самый простой способ определить заряд атома – взглянуть на таблицу Менделеева. Элементы на левой стороне стола обычно становятся положительно заряженными ионами, а элементы на правой стороне стола обычно имеют отрицательный заряд. Однако вы можете использовать научную формулу для определения формального заряда атома.
Свойства атомов
Часто называемые «строительными блоками» всего в мире, атомы представляют собой мельчайшие частицы химического элемента, которые могут существовать; Химический элемент – это вещество, которое полностью состоит из одного типа атома. Атомы могут соединяться друг с другом, образуя молекулы, которые затем составляют объекты, известные как материя, вокруг вас. Атомы состоят из частиц, называемых протонами, электронами и нейтронами. Протоны имеют положительный электрический заряд, электроны имеют отрицательный электрический заряд, а нейтроны не имеют электрического заряда. Протоны и нейтроны слипаются в центре атома, известного как ядро, а электроны окружают ядро. Конкретный атом будет иметь равное количество протонов и электронов, а большинство атомов имеет столько же или больше нейтронов, как и протоны.
Атомный номер элемента
Атомный номер элемента, также называемый числом протонов, показывает количество протонов или положительных частиц в атоме. Нормальный атом с равным количеством положительных и отрицательных частиц имеет нейтральный заряд. Другими словами, число электронов равно атомному номеру. Ионы – это атомы с дополнительными электронами, что приводит к отрицательному заряду или отсутствию электронов, что дает атому положительный заряд.
Определить заряд атома
Если вы посмотрите на периодическую таблицу – таблицу химических элементов, расположенных в порядке атомного номера – вы увидите, что элементы на левой стороне обычно имеют положительный заряд, а элементы на правой стороне имеют отрицательный заряд. Для выработки формального заряда атома формула имеет вид:
FC = GN – UE – 1/2 BE
Где FC = формальный заряд, GN = номер группы периодической таблицы или число валентных электронов в свободном, несвязанном атоме, UE = число неразделенных электронов и BE = число электронов, общих в ковалентных связях.
Например, если вы хотите отработать заряд водорода H , найденный в верхнем левом углу периодической таблицы, он имеет один валентный электрон GN = 1 , нет неразделенных электронов UE = 0 и два общих электрона в кислороде. водородная ковалентная связь, поэтому BE = 2 .
Расчет таков:
1 – 0 – (2 ÷ 2)
что означает, что формальный заряд на атоме водорода равен 0.
Основной структурной единицей веществ атомного строения является атом.
Атом – мельчайшая, электронейтральная, химически неделимая частица вещества, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Электронная оболочка – совокупность группирующихся вокруг ядра электронов.
Электрон – одна из элементарных частиц материи, обладающая массой покоя и элементарным отрицательным зарядом.
Когда говорят о массе покоя, то подразумевают, что частица может находиться в состоянии покоя и иметь массу. Существуют частицы, которые не могут находиться в состоянии покоя, например частицы света – фотоны. В этом случае говорят, что фотон не имеет массы покоя.
Заряд электрона называется элементарным, так как это наименьший отрицательный заряд в природе. По этой причине заряд электрона условно принимают равным -1.
Атомное ядро – центральная, положительно заряженная, сложно организованная часть атома, состоящая из нуклонов, связанных между собой ядерными силами.
Нуклоны – общее название двух типов частиц, протонов и нейтронов.
С точки зрения атомной физики протон и нейтрон являются двумя состояниями одной и той же частицы – нуклона.
Нуклон – структурная единица ядра атома, которая может находиться в двух состояниях, протона и нейтрона.
Нуклоны (протоны и нейтроны) состоят из кварков.
Заряд ядра атома соответствует атомному номеру (порядковому номеру) элемента в периодической системе (Z).
Заряд ядра определяется числом протонов, следовательно:
Так как атом – электронейтральная частица, то:
Массовое число (нуклонное число) – сумма числа протонов и нейтронов в ядре данного атома.
Если в условии задания не указано массовое число, то его можно взять из таблицы Д.И. Менделеева, округлив до целой величины относительную атомную массу.
О том, что такое относительная атомная масса мы поговорим чуть позже. Пока не заостряйте на этом внимание. Где её найти в таблице Д.И. Менделеева показано на рисунке ниже.
Для расчета числа нейтронов в ядре используется формула:
Для характеристик частицы (протона, нейтрона, атома) применяют следующую запись:
Определим состав атома хлора. Порядковый номер хлора в таблице Д. И. Менделеева равен 17, следовательно заряд ядра атома хлора равен +17. Если заряд ядра равен +17, то в ядре атома хлора 17 протонов, а в электронной оболочке 17 электронов.
Чтобы определить число нейтронов в ядре атома хлора, округлим до целой величины относительную атомную массу хлора, это значение равно 36. То есть, в ядре атома хлора 36 нуклонов, 17 из них являются протонами, тогда число нейтронов равно 36-17 = 19.
Кратко это можно записать следующим образом:
Атомы отличаются друг от друга радиусом, массой, зарядом ядра, количеством электронов и другими параметрами. Заряд ядра атома – это наиболее важная его характеристика. Поэтому все атомы можно условно разделить на группы (классифицировать) по заряду их ядер. Такие абстрактные группы принято называть химическими элементами.
Химический элемент – вид атомов, с определённым зарядом ядра.
Химический элемент – одно из центральных понятий науки химии.
По предложению шведского химика Й. Берцелиуса химические элементы обозначают начальной или начальной и одной из последующих букв латинского названия элемента (1813 г).
Водород на лат. Hydrogenium (H). Ртуть на лат. Hydrargyrum (Hg) Эти буквенные обозначения называются химическими знаками или химическими символами.
Символ отдельного атома совпадает с символом соответствующего ему химического элемента. К примеру, символ S обозначает химический элемент серу или же один атом этого элемента.
Если требуется обозначить не один, а несколько атомов, то перед символом элемента ставят соответствующую цифру – коэффициент. 5S – пять атомов элемента серы.
Символы и русские названия химических элементов можно найти в таблице Д. И. Менделеева.
Несмотря на то что у ядер атомов одного и того же химического элемента одинаковый заряд, они могут отличаться друг от друга массовым (нуклонным) числом по причине разного количества нейтронов. Такие разновидности ядер атомов одного химического элемента называют изотопами.
Изотопы – ядра с одинаковым зарядом, но разным массовым числом, т.е разным числом нейтронов.
Отметим, что термин изотопы следует употреблять только во множественном числе. В единственном числе следует говорить – нуклид. Что такое нуклиды Вы узнаете чуть позже.
К примеру, химический элемент водород (H) представляет из себя смесь атомов с массовыми числами равными 1 и 2, это изотопы водорода – протий (H) и дейтерий (D). Нуклид водорода с массовым числом 3 в природе не встречается, так как его ядро чрезвычайно нестабильно и очень быстро подвергается ядерному распаду, это так называемый тритий (T).
Запишем состав изотопов водорода, пользуясь описанными выше правилами.
Мы убедились, что изотопы отличаются массовыми числами, а также количеством нейтронов в ядре. Заряд ядер изотопов одинаковый, так как они принадлежат одному химическому элементу.
Содержание изотопов в земной коре разное ввиду их разной стабильности. Чем устойчивее изотоп, тем выше его содержание.
Содержание изотопов элемента Х может быть оценено в массовых или мольных долях.
Доля – отношение части к целому.
Массовая доля (w или w%) – отношение массы части системы к массе всей системы.
О мольной доле мы поговорим позднее в соответствующей теме.
Массовая доля – величина безразмерная, её выражают в долях единицы или процентах. Для вычисления массовой доли применяются формулы:
Изотопный состав элемента водорода может быть представлен следующей схемой:
Задания по теме “Основные сведения о строении атома”
- Ядро атома некоторого элемента содержит 16 нейтронов, а электронная оболочка этого атома – 15 электронов. Назвать элемент, изотопом которого является данный атом. Привести запись его символа с указанием заряда ядра и массового числа.
- Массовое число атома некоторого элемента равно 181, в электронной оболочке атома содержится 73 электрона. Указать число протонов и нейтронов в ядре атома и название элемента.
- Укажите число протонов, нейтронов и электронов в атоме циркония.
- Укажите число протонов, нейтронов и электронов в атоме иттрия.
- Укажите число протонов, нейтронов и электронов в атоме индия.
- Укажите число протонов, нейтронов и электронов в атоме кадмия.
- Сколько нейтронов содержит ядро атома 37Cl?
- Сколько нейтронов содержит ядро атома 18O?
- Сколько нейтронов содержит ядро атома 30Si?
- Сколько нейтронов содержит ядро атома 19F?

Вспомните:
- что такое атом;
- из чего состоит атом;
- изменяется ли атом в химических реакциях?
АТОМ — это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Число электронов в ходе химических процессов может изменяться, но заряд ядра всегда остается неизменным. Зная распределение электронов в атоме (строение атома), можно предсказать многие свойства данного химического элемента, а также простых и сложных веществ, в состав которых этот элемент входит.
Содержание
- Структура Периодической системы Менделеева
- Ядро атома. Изотопы
- Распределение электронов в поле ядра атома
- Строение атома и свойства элементов
- Выводы
Структура Периодической системы Менделеева
Строение атома, т. е. состав ядра, распределение электронов вокруг ядра, несложно определить по положению элемента в Периодической системе. В Периодической системе Менделеева химические элементы располагаются в определённой последовательности. Эта последовательность тесно связана со строением атома этих элементов. Каждому химическому элементу в системе присвоен порядковый номер, кроме того, для него можно указать:
- номер периода;
- номер группы;
- вид подгруппы.
Зная точный «адрес» химического элемента, т. е. его группу, подгруппу и номер периода, можно однозначно определить строение его атома.
Период — это горизонтальный ряд химических элементов. В современной Периодической системе семь периодов. Первые три — малые, так как они содержат 2 или 8 элементов:
- 1-й период — Н, Не — 2 элемента;
- 2-й период — Li…Nе — 8 элементов;
- 3-й период — Na…Аr — 8 элементов.
Остальные периоды — большие. Каждый из них содержит 2–3 ряда элементов:
- 4-й период (2 ряда) — К…Кr — 18 элементов;
- 6-й период (3 ряда) — Сs…Rn — 32 элемента. В этот период входит ряд лантаноидов.
Группа — вертикальный ряд химических элементов. Всего групп восемь. Каждая группа состоит из двух подгрупп: главной подгруппы и побочной подгруппы (см. рис. 5).
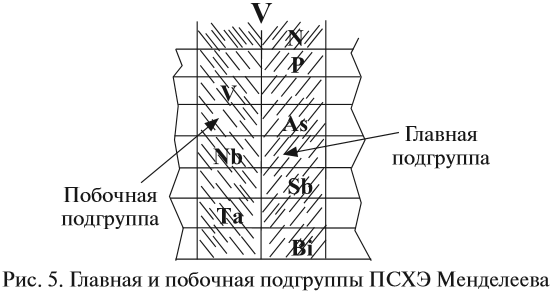
Главную подгруппу (подгруппу А) образуют химические элементы малых периодов и больших периодов. На рисунке 5 показано, что главную подгруппу пятой группы составляют элементы малых периодов (N, P) и больших периодов (As, Sb, Bi).
Побочную подгруппу (подгруппу Б) образуют химические элементы только больших периодов. В нашем случае это V, Nb, Ta.
Визуально эти подгруппы различить легко: главная подгруппа «высокая», начинается с первого или второго периода. Побочная подгруппа — «низкая», начинается с 4-го периода.
Итак, каждый химический элемент Периодической системы имеет свой адрес:
- период;
- группу;
- подгруппу;
- порядковый номер.
Например, ванадий (V) — это химический элемент 4-го периода, V группы, побочной подгруппы, порядковый номер 23.
Задание 3.1. Укажите период, группу и подгруппу для химических элементов с порядковыми номерами 8, 26, 31, 35, 54.
Задание 3.2. Укажите порядковый номер и название химического элемента, если известно, что он находится:
- в 4-м периоде, VI группе, побочной подгруппе;
- в 5-м периоде, IV группе, главной подгруппе.
Каким образом можно связать эти сведения об элементе со строением его атома?
Ядро атома. Изотопы
Атом состоит из ядра, которое имеет положительный заряд, и электронов, которые имеют отрицательный заряд. В целом атом электронейтрален.
Положительный заряд ядра атома равен порядковому номеру химического элемента.
Ядро атома — сложная частица. В ней сосредоточена почти вся масса атома. Поскольку химический элемент — совокупность атомов с одинаковым зарядом ядра, то около символа элемента указывают (рис. 6).
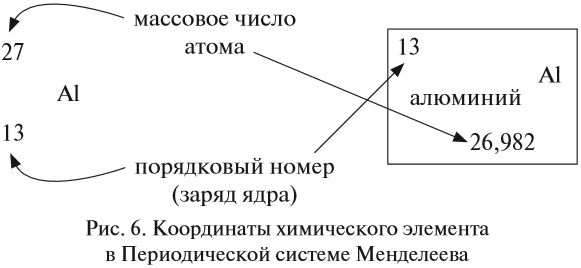
По этим данным можно определить состав ядра. Ядро состоит из протонов и нейтронов.
- Протон (р) имеет массу, равную 1 (1,0073 а. е. м.) и заряд, равный +1.
- Нейтрон (n) заряда не имеет (нейтрален), а масса его приблизительно равна массе протона (1,0087 а. е. м.).
Какие частицы определяют заряд ядра? Протоны! Причём число протонов равно (по величине) заряду ядра атома, т. е. порядковому номеру:
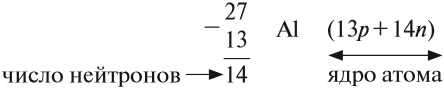
Число нейтронов определяют по разности между величинами: «масса ядра» и «порядковый номер».
Задание 3.3. Определите состав ядер атомов, если химический элемент находится в:
- 3-м периоде, VII группе, главной подгруппе;
- 4-м периоде, IV группе, побочной подгруппе;
- 5-м периоде, I группе, главной подгруппе.
Обратите внимание, что при определении массового числа ядра атома приходится округлять атомную массу, указанную в Периодической системе! Почему? Ведь массы протона и нейтрона практически целочисленны, а массой электронов можно пренебречь.
Для того,чтобы ответить на этот вопрос, нужно понять:
- Что происходит с атомом в ходе химических процессов;
- Что такое «химический элемент».
В химических процессах обязательно изменяется распределение электронов вокруг ядра или даже изменяется их число. В последнем случае атом отдаёт или принимает электроны и превращается в заряженную частицу — ион. Но в химических реакциях никогда не меняется состав ядра атома, его заряд. Поэтому заряд ядра атома является своеобразным «паспортом» химического элемента.
Химический элемент — совокупность атомов или ионов с одинаковым зарядом ядра.
Для того чтобы разобраться, попробуйте определить, какие из ядер, состав которых указан ниже, принадлежат одному и тому же химическому элементу:
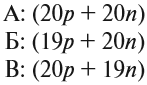
Атомам одного химического элемента принадлежат ядра А и В, так как они содержат одинаковое число протонов, т. е. заряд этих ядер одинаковый. Но ведь у них разная масса! Исследования показывают, что масса атома не оказывает существенного влияния на его химические свойства. Поэтому атомы одного и того же химического элемента (одинаковое число протонов), но с разной массой (разное число нейтронов) являются ИЗОТОПАМИ* этого элемента.
* Слово «изотоп» означает по смыслу «одно место», т. е. все изотопы данного химического элемента находятся в одной клетке ПСХЭ.
В таблице Менделеева указана средняя атомная масса всех природных изотопов данного элемента (Аr). Изотопы и их химические соединения отличаются друг от друга по физическим свойствам, но химические свойства у изотопов одного химического элемента одинаковы. Так, изотоп углерода-14 (14С) имеет такие же химические свойства, как и углерод-12 (12С), который входит в ткани любого живого организма, отличаясь от него только радиоактивностью. Поэтому изотопы применяют для диагностики и лечения различных заболеваний, для научных исследований.
Элемент «водород» встречается в природе в виде трёх изотопов:
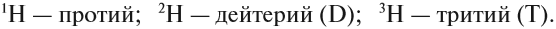
Химический элемент «кислород» также представлен тремя природными изотопами:
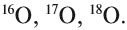
Задание 3.4. Укажите состав ядер этих изотопов водорода и кислорода.
Если разные вещества содержат атомы одного и того же химического элемента, это не означает, что эти вещества имеют одни те же свойства. Например, химический элемент «хлор» в виде атомарного хлора Cl• разрушает метан, а также атмосферный озон. Тот же элемент в виде молекулярного хлора Cl2 ядовит, активно реагирует с водой, многими металлами, а ионы хлора (химический элемент — тот же!) в составе NaCl химически инертен, а с биологической точки зрения не только безвреден, но и полезен для нас. Эти ионы являются макроэлементами нашей пищи, которые входят в состав крови, желудочного сока. Суточная потребность — до 6 граммов.
Но вернемся к описанию строения атома.

Распределение электронов в поле ядра атома
Как известно, ядро атома в химических процессах не меняется. А что меняется? Общее число электронов и распределение электронов. Общее число электронов определить несложно: оно равно порядковому номеру, т. е. заряду ядра атома:
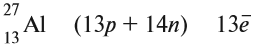
Электроны имеют отрицательный заряд –1, а масса их ничтожна: 1/1840 от массы протона.
Отрицательно заряженные электроны отталкиваются и поэтому находятся на разных расстояниях от ядра. При этом электроны, имеющие приблизительно равный запас энергии, образуют энергетический уровень.
Число энергетических уровней в атоме равно номеру периода, в котором находится химический элемент. Энергетические уровни условно обозначают так (рис. 7).
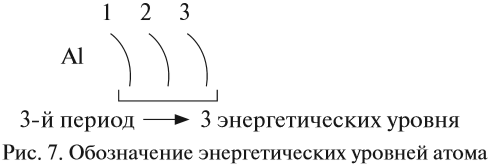
Задание 3.5. Определите число энергетических уровней в атомах кислорода, магния, кальция, свинца.
На каждом энергетическом уровне может находиться ограниченное число электронов:
- на первом энергетическом уровне не более 2 электронов;
- на втором энергетическом уровне не более 8 электронов;
- на третьем энергетическом уровне не более 18 электронов.
ЗАПОМНИТЕ ЭТИ ЧИСЛА!
Они показывают, что, например, на втором энергетическом уровне может находиться 2 или 5 или 7 электронов, но не может быть 9 или 12 электронов.
Важно знать, что, независимо от номера энергетического уровня, на внешнем (последнем) уровне не может быть больше восьми электронов. Внешний восьмиэлектронный энергетический уровень является наиболее устойчивым и называется завершённым. Такие энергетические уровни имеются у самых неактивных элементов — благородных газов.
Как определить число электронов на внешнем уровне остальных атомов? Для этого существует простое правило – число внешних электронов равно:
- для элементов главных подгрупп — номеру группы;
- для элементов побочных подгрупп — оно не может быть больше двух (рис. 8).
Например:
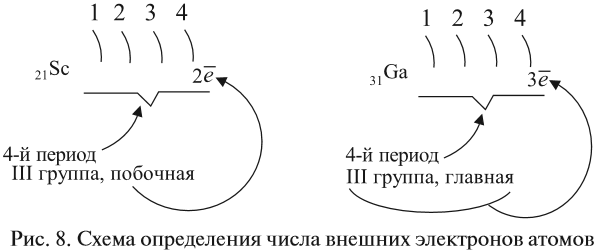
Задание 3.6. Укажите число внешних электронов для химических элементов с порядковыми номерами 15, 25, 30, 53.
Задание 3.7. Найдите в Периодической системе химические элементы, в атомах которых имеется завершённый внешний уровень.
Очень важно правильно определять число внешних электронов, так как именно с ними связаны важнейшие свойства атома. Так, в химических реакциях атомы стремятся «приобрести» устойчивый, завершённый внешний уровень (8ē). Для этого атомы, на внешнем уровне которых мало электронов, «предпочитают» их отдать.
Химические элементы, атомы которых способны только отдавать электроны, относятся к МЕТАЛЛАМ. Очевидно, что на внешнем уровне атома металла должно быть мало электронов: 1, 2, 3.
Если на внешнем энергетическом уровне атома много электронов, то такие атомы стремятся принять электроны до завершения внешнего энергетического уровня, т. е. до восьми электронов. Такие элементы относятся к НЕМЕТАЛЛАМ.
Вопрос. К каким элементам (металлам или неметаллам) относятся химические элементы побочных подгрупп? Почему?
Металлы и неметаллы главных подгрупп в таблице Менделеева отделяет линия, которую можно провести от бора к астату. Выше этой линии (и на линии) располагаются неметаллы, ниже — металлы.
Задание 3.8. Определить, к металлам или неметаллам относятся: фосфор, ванадий, кобальт, селен, висмут. Вывод сделайте, определив положение элемента в Периодической системе химических элементов и число электронов на внешнем уровне.
Для того чтобы составить распределение электрона по остальным уровням и подуровням, следует воспользоваться следующим АЛГОРИТМОМ:
- Определить общее число электронов в атоме (по порядковому номеру).
- Определить число энергетических уровней (по номеру периода).
- Определить число внешних электронов (по виду подгруппы и номеру группы).
- Указать число электронов на всех уровнях, кроме предпоследнего.
- Рассчитать число электронов на предпоследнем уровне.
Например, согласно пунктам 1…4 для атома марганца определено:

Получили распределение электронов в атоме марганца (рис. 9):
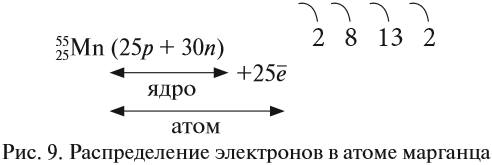
Задание 3.9. Отработайте алгоритм, составив схемы строения атомов для элементов № 16, 26, 33, 37. Укажите: металлы это или неметаллы? Ответ поясните.
Составляя вышеприведенные схемы строения атома, мы не учитывали, что электроны в атоме занимают не только определённые уровни, но и определённые подуровни каждого уровня. Вид подуровня обозначается латинской буквой: s, p, d.
Число возможных подуровней равно номеру уровня, т. е.
- первый уровень состоит из одного s-подуровня;
- второй уровень состоит из двух подуровней: s и р и т. д.
На каждом подуровне может находиться строго ограниченное число электронов:
- на s-подуровне — не больше 2ē;
- на р-подуровне — не больше 6ē;
- на d-подуровне — не больше 10ē.
Подуровни одного уровня заполняются в строго определённом порядке:
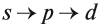
Таким образом, р-подуровнь не может начать заполняться, если не заполнен s-подуровень данного энергетического уровня и т. д. Исходя из этого правила, несложно составить электронную конфигурацию атома марганца (рис. 10).
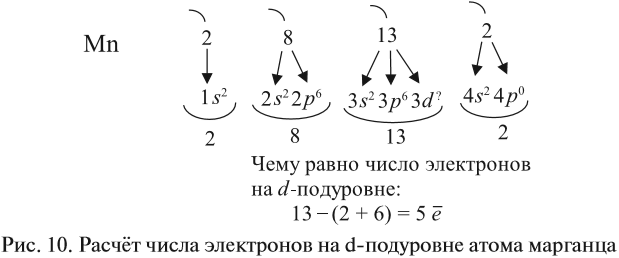
В целом электронная конфигурация атома марганца выглядит так:
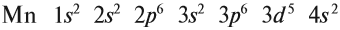
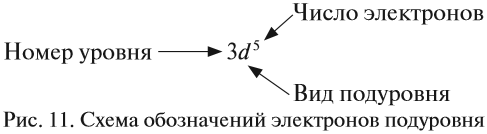
Здесь и далее приняты обозначения (рис. 11).
Задание 3.10. Составьте электронные конфигурации атомов для химических элементов № 16, 26, 33, 37.
Для чего необходимо составлять электронные конфигурации атомов? Для того чтобы определять свойства этих химических элементов!
Для этого следует помнить: в химических процессах участвуют только валентные электроны.
Валентные электроны находятся на внешнем энергетическом уровне и незавершённом d-подуровне предвнешнего уровня.
Определим число валентных электронов для марганца:

или сокращённо:
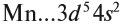

Строение атома и свойства элементов
Мы получили краткую электронную формулу атома марганца, которая отражает распределение его валентных электронов. Что можно определить по этой формуле?
1. Какие свойства — металла или неметалла — преобладают у этого элемента? Ответ: марганец — металл, так как на внешнем (четвёртом) уровне 2 электрона.
2. Какой процесс характерен для металла? Ответ: всегда только отдача электронов.
3. Какие электроны и сколько их будет отдавать атом марганца? Ответы:
- два внешних электрона (они дальше всех от ядра и слабее притягиваются им);
- семь (2+5) валентных электронов (так как в этом случае на третьем уровне атома останется восемь электронов, т. е. образуется завершённый уже внешний уровень).
Все эти рассуждения и заключения можно отразить при помощи схемы (рис. 12).
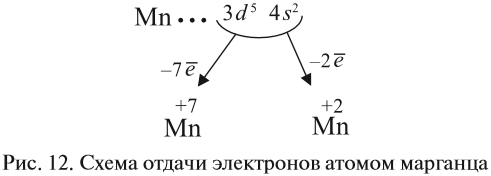
Полученные условные заряды атома называются степенью окисления.
Рассматривая строение атомов кислорода и водорода и рассуждая аналогично, можно показать, что типичными степенями окисления для кислорода является –2, а для водорода +1.
Вопрос. С каким из этих химических элементов может образовывать соединения марганец, если учесть полученные выше степени окисления его?
Только с кислородом, так как его атом имеет противоположную по заряду (знаку) степень окисления. В этом случае несложно составить формулы соответствующих оксидов марганца (здесь степени окисления соответствуют валентностям этих химических элементов):
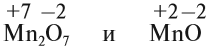
Строение атома марганца подсказывает, что большей степени окисления, чем +7, у марганца быть не может, так как в этом случае пришлось бы затрагивать устойчивый, теперь уже завершённый предвнешний уровень. Поэтому степень окисления +7 является высшей, а соответствующий оксид Мn2О7 — высшим оксидом марганца.
Для закрепления всех этих понятий рассмотрим строение атома теллура и некоторые его свойства (см. рис. 13). Этот рисунок показывает, что теллур относится к неметаллам, так как, во-первых, у него на внешнем уровне шесть электронов и, во-вторых, его символ находится в главной подгруппе выше линии В — At. Поэтому его атом может и принимать (до завершения внешнего уровня, и отдавать электроны. В результате, в отличие от металлов, неметалл теллур может проявлять низшую степень окисления (–2) и образовывать летучие водородные соединения с водородом (Н2Те). Высшая степень окисления атома теллура (+6), как и у металлов соответствует номеру группы и, находясь в этой степени окисления, теллур образует высший оксид ТеО3.

Задание 3.11. Изобразить электронные конфигурации атомов Nа, Rb, Сl, I, Si, Sn. Определить свойства этих химических элементов, формулы их простейших соединений (с кислородом и с водородом).
Сделаем выводы.
- В химических реакциях участвуют только валентные электроны, которые могут находиться только на последних двух уровнях.
- Атомы металлов могут только отдавать эти электроны (все или несколько), принимая положительные степени окисления.
- Атомы неметаллов могут принимать (недостающие до восьми) электроны, получая при этом отрицательные степени окисления, и отдавать валентные электроны (все или несколько), принимая при этом положительные степени окисления.
Возникает вопрос: как составить краткую электронную формулу (распределение валентных электронов), сразу, не составляя длинных электронных конфигураций? Для этого нужно помнить несколько простых правил.
1. Номер периода соответствует числу энергетических уровней у атомов химических элементов этого периода.
2. Номер группы, как правило, совпадает с числом валентных электронов, (исключение составляют только подгруппы меди и железа).
3. Подгруппа (главная или побочная) включает химические элементы, у которых имеется одинаковое распределение валентных электронов, причём в атомах элементов главной и побочной подгруппы электроны распределяются по-разному.
3.1. У элементов главных подгрупп все валентные электроны находятся на внешнем уровне, например:
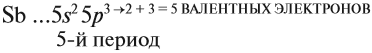
V группа, главная → 5 валентных электронов
Поэтому для всех химических элементов главной подгруппы пятой группы (пять валентных электронов) распределение этих электронов следующее:
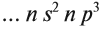
3.2. У элементов побочных подгрупп число внешних электронов не превышает двух, например:
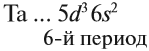
5 валентных электронов ← V группа, побочная → 2 электрона на внешнем уровне*.
* За счёт «провала электрона» число внешних электронов может быть меньше. Но число валентных электронов при этом не меняется, поэтому свойства элемента будут такими же. Эти случаи рассмотрены в Самоучителе второго уровня, часть 1.
Для большинства химических элементов побочных подгрупп, у которых на внешнем энергетическом уровне два электрона, остальные (N – 2) валентные электроны будут находиться на d-подуровне предвнешнего уровня (N – номер группы), например:
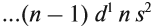
Вопрос. Для элементов какой группы составлена такая запись?
Задание 3.12. Составьте краткие электронные формулы для атомов химических элементов № 35 и 42, а затем составьте распределение электронов в этих атомах по алгоритму. Убедитесь, что ваше «предсказание» сбылось.
Сравним теперь свойства химических элементов одной подгруппы, например:
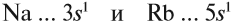
Что общего в строении атомов этих элементов? На внешнем уровне каждого атома по одному электрону — это активные металлы. Металлическая активность связана со способностью отдавать электроны: чем легче отдает электроны атом, тем сильнее выражены его металлические свойства.
Что удерживает электроны в атоме? Притяжение их к ядру. Чем ближе электроны к ядру, тем сильнее они притягиваются ядром атома, тем труднее их «оторвать».
Исходя из этого, сделаем вывод: какой элемент — Nа или Rb — легче отдает внешний электрон? Какой из них является более активным металлом? Очевидно, рубидий, так как его валентные электроны находятся дальше от ядра (и слабее удерживаются ядром).
Вывод. В главных подгруппах сверху вниз металлические свойства усиливаются, так как возрастает радиус атома и валентные электроны слабее притягиваются к ядру.
Сравним свойства:
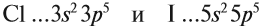
Оба химических элемента — неметаллы, так как до завершения внешнего уровня не хватает одного электрона, и эти атомы будут активно притягивать недостающий электрон. При этом, чем сильнее притягивает атом неметалла недостающий электрон, тем сильнее проявляются его неметаллические свойства (способность принимать электроны).
За счёт чего происходит притяжение электрона? За счёт положительного заряда ядра атома. Но в таком случае чем ближе электрон к ядру, тем сильнее их взаимное притяжение, тем активнее неметалл.
Сделаем вывод, у какого элемента сильнее выражены неметаллические свойства: у хлора или у йода? Очевидно, у хлора, так как его валентные электроны ближе к ядру.
Вывод. Активность неметаллов в подгруппах сверху вниз убывает, так как возрастает радиус атома и все труднее притянуть недостающие электроны.
Сравним свойства кремния и олова:

На внешнем уровне обоих атомов по четыре электрона. Тем не менее эти элементы в Периодической системе находятся по разные стороны от линии, соединяющей бор и астат (см. правило в уроке 2.1.). Поэтому:
- у кремния, символ которого находится выше линии В–At, сильнее проявляются неметаллические свойства;
- у олова, символ которого находится ниже линии В–At, сильнее проявляются металлические свойства;
Почему? Потому что в атоме олова четыре валентных электрона находятся так далеко от ядра, что присоединение недостающих четырех электронов затруднено, в то время как отдача электронов с пятого энергетического уровня происходит достаточно легко. Для кремния возможны оба процесса, причём первый (приём электронов) — преобладает.
Выводы:
- чем меньше электронов в атоме и чем дальше они от ядра, тем сильнее проявляются металлические свойства;
- чем больше внешних электронов в атоме, чем ближе они к ядру, тем сильнее проявляются неметаллические свойства.
Сравним строение атомов и свойства химических элементов одного периода:
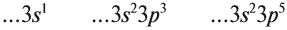
Вопрос. О каком периоде и каких элементах идёт речь?
Видно, что металлические свойства убывают, так как увеличивается число внешних электронов, а неметаллические свойства — возрастают. Если речь идёт о большом периоде, где большинство элементов имеет 2 электрона на внешнем уровне (элементы побочных подгрупп), то в этом случае главной причиной убывания металлических свойств в периоде является уменьшение радиуса атома. Дело в том, что за счёт увеличения заряда ядра в периоде увеличивается сила притяжения электронов к нему и уменьшается радиус атома:
Сравните: r (Ca) = 0,197 нм и r (Zn) = 0,139 нм
Вопрос. Какой из металлов более активен?
Основываясь на этих и других выводах, сформулированных в этой главе, можно для любого химического элемента Периодической системы составить алгоритм описания свойств химического элемента по его положению в Периодической системе.
1. Составить схему строения атома, т. е. определить состав ядра, распределение электронов по энергетическим уровням и подуровням:
- определить общее число электронов в атоме (по порядковому номеру);
- определить число энергетических уровней (по номеру периода);
- определить число внешних электронов (по виду подгруппы и номеру группы);
- указать число электронов на всех энергетических уровнях, кроме предпоследнего;
- рассчитать число электронов на предпоследнем уровне.
2. Определить число валентных электронов и число внешних электронов.
3. Определить, какие свойства — металла или неметалла — сильнее проявляются у данного химического элемента (по положению в ПСХЭ).
4. Определить число отдаваемых (принимаемых) электронов.
5. Определить высшую и низшую степени окисления химического элемента.
6. Составить для этих степеней окисления химические формулы простейших соединений с кислородом и водородом.
7. Определить характер оксида (см. урок 2.1.) и составить уравнения его реакции с водой.
8. Для указанных (пункт 6) веществ составить уравнения характерных реакций (см. урок 2).
Задание 3.13. Составить по данной схеме описания атомов серы, селена, кальция и стронция и свойства этих химических элементов. Какие общие свойства имеют их оксиды? Гидроксиды?
Если вы выполнили упражнения 3.11 и 3.12, то легко заметить, что не только атомы элементов одной подгруппы, но и их соединения имеют общие свойства и похожий состав. Это отражено в Периодическом законе Менделеева: Свойства химических элементов, а также свойства простых и сложных веществ, образованных ими, находятся в периодической зависимости от ЗАРЯДА ЯДЕР ИХ АТОМОВ.
Физический смысл Периодического закона ясен: свойства химических элементов периодически повторяются потому, что периодически повторяются конфигурации валентных электронов (распределение электронов внешнего и предпоследнего уровней).
Так, у химических элементов одной и той же подгруппы одинаковое распределение валентных электронов и, значит, похожие свойства.

Выводы
Строение атома связано с положением элемента в Периодической системе. Зная строение атома, можно предсказать свойства элемента и его соединений. Эти свойства находятся в периодической зависимости от заряда ядер атомов элементов, в соответствии с Периодическим законом Менделеева.
У этого термина существуют и другие значения, см. Атом (значения).

Сравнительный размер атома гелия и его ядра
А́том (от др.-греч. ἄτομος «неделимый[1], не разрезаемый[2]») — частица вещества микроскопических размеров и массы, наименьшая часть химического элемента, являющаяся носителем его химических свойств[1][3].
Атомы состоят из ядра и электронов (точнее, электронного «облака»). Ядро атома состоит из протонов и нейтронов. Количество нейтронов в ядре может быть разным: от нуля до нескольких десятков. Если число электронов совпадает с числом протонов в ядре, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом[1]. В некоторых случаях под атомами понимают только электронейтральные системы, в которых заряд ядра равен суммарному заряду электронов, тем самым противопоставляя их электрически заряженным ионам[3][4].
Ядро, несущее почти всю (более чем 99,9 %) массу атома, состоит из положительно заряженных протонов и незаряженных нейтронов, связанных между собой при помощи сильного взаимодействия. Атомы классифицируются по количеству протонов и нейтронов в ядре: число протонов Z соответствует порядковому номеру атома в периодической системе Менделеева и определяет его принадлежность к некоторому химическому элементу, а число нейтронов N — определённому изотопу этого элемента. Единственный стабильный атом, не содержащий нейтронов в ядре — лёгкий водород (протий). Число Z также определяет суммарный положительный электрический заряд (Z×e) атомного ядра и число электронов в нейтральном атоме, задающее его размер[5].
Атомы различного вида в разных количествах, связанные межатомными связями, образуют молекулы.

История становления понятия[править | править код]
Понятие об атоме как о наименьшей неделимой части материи было впервые сформулировано древнеиндийскими и древнегреческими философами (см.: атомизм). В XVII и XVIII веках химикам удалось экспериментально подтвердить эту идею, показав, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы с помощью химических методов. Однако в конце XIX — начале XX века физиками были открыты субатомные частицы и составная структура атома, и стало ясно, что реальная частица, которой было присвоено имя атома, в действительности не является неделимой.
На международном съезде химиков в Карлсруэ (Германия) в 1860 году были приняты определения понятий молекулы и атома. Атом — наименьшая частица химического элемента, входящая в состав простых и сложных веществ.
Модели атомов[править | править код]
- Кусочки материи. Демокрит полагал, что свойства того или иного вещества определяются формой, массой, и пр. характеристиками образующих его атомов. Так, скажем, у огня атомы остры, поэтому огонь способен обжигать, у твёрдых тел они шероховаты, поэтому накрепко сцепляются друг с другом, у воды — гладки, поэтому она способна течь. Даже душа человека, согласно Демокриту, состоит из атомов[6].
- Модель атома Томсона 1904 г. (модель «Пудинг с изюмом»). Дж. Дж. Томсон предложил рассматривать атом как некоторое положительно заряженное тело с заключёнными внутри него электронами. Была окончательно опровергнута Резерфордом после проведённого им знаменитого опыта по рассеиванию альфа-частиц.
- Ранняя планетарная модель атома Нагаоки. В 1904 году японский физик Хантаро Нагаока предложил модель атома, построенную по аналогии с планетой Сатурн. В этой модели вокруг маленького положительного ядра по орбитам вращались электроны, объединённые в кольца. Модель оказалась ошибочной.
- Планетарная модель атома Бора-Резерфорда. В 1911 году[7] Эрнест Резерфорд, проделав ряд экспериментов, пришёл к выводу, что атом представляет собой подобие планетной системы, в которой электроны движутся по орбитам вокруг расположенного в центре атома тяжёлого положительно заряженного ядра («модель атома Резерфорда»). Однако такое описание атома вошло в противоречие с классической электродинамикой. Дело в том, что, согласно классической электродинамике, электрон при движении с центростремительным ускорением должен излучать электромагнитные волны, а, следовательно, терять энергию. Расчёты показывали, что время, за которое электрон в таком атоме упадёт на ядро, совершенно ничтожно. Для объяснения стабильности атомов Нильсу Бору пришлось ввести постулаты, которые сводились к тому, что электрон в атоме, находясь в некоторых специальных энергетических состояниях, не излучает энергию («модель атома Бора-Резерфорда»). Необходимость введения постулатов Бора была следствием осознания того, что для описания атома классическая механика неприменима. Дальнейшее изучение излучения атома привело к созданию квантовой механики, которая позволила объяснить подавляющее большинство наблюдаемых фактов.
Квантово-механическая модель атома[править | править код]
Современная модель атома является развитием планетарной модели Бора-Резерфорда. Согласно современной модели, ядро атома состоит из положительно заряженных протонов и не имеющих заряда нейтронов и окружено отрицательно заряженными электронами. Однако представления квантовой механики не позволяют считать, что электроны движутся вокруг ядра по сколько-нибудь определённым траекториям (неопределённость координаты электрона в атоме может быть сравнима с размерами самого атома).
Химические свойства атомов определяются конфигурацией электронной оболочки и описываются квантовой механикой. Положение атома в таблице Менделеева определяется электрическим зарядом его ядра (то есть количеством протонов), в то время как количество нейтронов принципиально не влияет на химические свойства; при этом нейтронов в ядре, как правило, больше, чем протонов (см.: атомное ядро). Если атом находится в нейтральном состоянии, то количество электронов в нём равно количеству протонов. Основная масса атома сосредоточена в ядре, а массовая доля электронов в общей массе атома незначительна (несколько сотых процента массы ядра).
Массу атома принято измерять в атомных единицах массы (дальтонах), равных 1⁄12 от массы атома стабильного изотопа углерода 12C.
Строение атома[править | править код]
Субатомные частицы[править | править код]
Хотя слово атом в первоначальном значении обозначало частицу, которая не делится на меньшие части, согласно научным представлениям он состоит из более мелких частиц, называемых субатомными частицами. Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны.
Электрон является самой лёгкой из составляющих атом частиц с массой 9,11⋅10−31 кг, отрицательным зарядом и размером, слишком малым для измерения современными методами[8]. Эксперименты по сверхточному определению магнитного момента электрона (Нобелевская премия 1989 года) показывают, что размеры электрона не превышают 10−18 м[9][10].
Протоны обладают положительным зарядом и в 1836 раз тяжелее электрона (1,6726⋅10−27 кг). Нейтроны не обладают электрическим зарядом и в 1839 раз тяжелее электрона (1,6749⋅10−27 кг)[11].
При этом масса ядра меньше суммы масс составляющих его протонов и нейтронов из-за явления дефекта массы. Нейтроны и протоны имеют сравнимый размер, около 2,5⋅10−15 м, хотя размеры этих частиц определены плохо[12].
В стандартной модели элементарных частиц как протоны, так и нейтроны состоят из элементарных частиц, называемых кварками. Наряду с лептонами, кварки являются одной из основных составляющих материи. И первые и вторые являются фермионами. Существует шесть типов кварков, каждый из которых имеет дробный электрический заряд, равный +2⁄3 или (−1⁄3) элементарного. Протоны состоят из двух u-кварков и одного d-кварка, а нейтрон — из одного u-кварка и двух d-кварков. Это различие объясняет разницу в массах и зарядах протона и нейтрона. Кварки связаны между собой сильными ядерными взаимодействиями, которые передаются глюонами[13][14].
Электроны в атоме[править | править код]
При описании электронов в атоме в рамках квантовой механики обычно рассматривают распределение вероятности в 3n-мерном пространстве для системы n электронов.
Электроны в атоме притягиваются к ядру, между электронами также действует кулоновское взаимодействие. Эти же силы удерживают электроны внутри потенциального барьера, окружающего ядро. Для того чтобы электрон смог преодолеть притяжение ядра, ему необходимо получить энергию от внешнего источника. Чем ближе электрон находится к ядру, тем больше энергии для этого необходимо.
Электронам, как и другим частицам, свойственен корпускулярно-волновой дуализм. Иногда говорят, что электрон движется по орбитали, что неверно. Состояние электронов описывается волновой функцией, квадрат модуля которой характеризует плотность вероятности нахождения частиц в данной точке пространства в данный момент времени, или, в общем случае, оператором плотности. Существует дискретный набор атомных орбиталей, которым соответствуют стационарные чистые состояния электронов в атоме.
Каждой орбитали соответствует свой уровень энергии. Электрон в атоме может перейти на уровень с большей энергией при столкновении данного атома с другим атомом, электроном, ионом, или же поглотив фотон соответствующей энергии. При переходе на более низкий уровень электрон отдаёт энергию путём излучения фотона, либо путём передачи энергии другому электрону (безызлучательный переход, удары второго рода). Как и в случае поглощения, при излучательном переходе энергия фотона равна разности энергий электрона на этих уровнях (см.: постулаты Бора). Частота испускаемого излучения ν связана с энергией фотона E соотношением E = hν, где h — постоянная Планка.
Свойства атома[править | править код]
По определению, любые два атома с одним и тем же числом протонов в их ядрах относятся к одному химическому элементу. Атомы с одним и тем же количеством протонов, но разным количеством нейтронов называют изотопами данного элемента. Например, атомы водорода всегда содержат один протон, но существуют изотопы без нейтронов (водород-1, иногда также называемый протием — наиболее распространённая форма), с одним нейтроном (дейтерий) и двумя нейтронами (тритий)[15]. Известные элементы составляют непрерывный натуральный ряд по числу протонов в ядре, начиная с атома водорода с одним протоном и заканчивая атомом оганесона, в ядре которого 118 протонов[16] Все изотопы элементов периодической системы, начиная с номера 83 (висмут), радиоактивны[17][18].
Масса[править | править код]
Поскольку наибольший вклад в массу атома вносят протоны и нейтроны, суммарное число этих частиц называют массовым числом. Массу покоя атома часто выражают в атомных единицах массы (а. е. м.), которая также называется дальтоном (Да). Эта единица определяется как 1⁄12 часть массы покоя нейтрального атома углерода-12, которая приблизительно равна 1,66⋅10−24 г.[19] Водород-1 — наилегчайший изотоп водорода и атом с наименьшей массой, имеет атомный вес около 1,007825 а. е. м.[20] Масса атома приблизительно равна произведению массового числа на атомную единицу массы[21] Самый тяжёлый стабильный изотоп — свинец-208[17] с массой 207,9766521 а. е. м.[22]
Так как массы даже самых тяжёлых атомов в обычных единицах (например, в граммах) очень малы, то в химии для измерения этих масс используют моли. В одном моле любого вещества по определению содержится одно и то же число атомов (примерно 6,022⋅1023). Это число (число Авогадро) выбрано таким образом, что если масса элемента равна 1 а. е. м., то моль атомов этого элемента будет иметь массу 1 г. Например, углерод имеет массу 12 а. е. м., поэтому 1 моль углерода весит 12 г.[19]
Размер[править | править код]
Атомы не имеют отчётливо выраженной внешней границы, поэтому их размеры определяются по расстоянию между ядрами одинаковых атомов, которые образовали химическую связь (ковалентный радиус) или по расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома (радиус атома). Радиус зависит от положения атома в периодической системе, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин[23]. В периодической системе элементов размер атома увеличивается при движении сверху вниз по столбцу и уменьшается при движении по строке слева направо[24]. Соответственно, самый маленький атом — это атом гелия, имеющий радиус 32 пм, а самый большой — атом цезия (225 пм)[25]. Эти размеры в тысячи раз меньше длины волны видимого света (400—700 нм), поэтому атомы нельзя увидеть в оптический микроскоп. Однако отдельные атомы можно наблюдать с помощью сканирующего туннельного микроскопа.
Малость атомов демонстрируют следующие примеры. Человеческий волос по толщине в миллион раз больше атома углерода[26]. Одна капля воды содержит 2 секстиллиона (2⋅1021) атомов кислорода, и в два раза больше атомов водорода[27]. Один карат алмаза с массой 0,2 г состоит из 10 секстиллионов атомов углерода[28]. Если бы яблоко можно было увеличить до размеров Земли, то атомы достигли бы исходных размеров яблока[29].
Учёные из Харьковского физико-технического института представили первые в истории науки снимки атома. Для получения снимков учёные использовали электронный микроскоп, фиксирующий излучения и поля (field-emission electron microscope, FEEM). Физики последовательно разместили десятки атомов углерода в вакуумной камере и пропустили через них электрический разряд в 425 вольт. Излучение последнего атома в цепочке на фосфорный экран позволило получить изображение облака электронов вокруг ядра[30].
Радиоактивный распад[править | править код]
Диаграмма времени полураспада (T½) в секундах для различных изотопов с Z протонами и N нейтронами.
У каждого химического элемента есть один или более изотопов с нестабильными ядрами, которые подвержены радиоактивному распаду, в результате чего атомы испускают частицы или электромагнитное излучение. Радиоактивность возникает, когда радиус ядра больше радиуса действия сильных взаимодействий (расстояний порядка 1 фм[31]).
Существуют три основные формы радиоактивного распада[32][33]:
- Альфа-распад происходит, когда ядро испускает альфа-частицу — ядро атома гелия, состоящее из двух протонов и двух нейтронов. В результате испускания этой частицы возникает элемент с меньшим на два атомным номером.
- Бета-распад происходит из-за слабых взаимодействий, и в результате нейтрон распадается на протон, электрон и антинейтрино, во втором случае на протон, позитрон и нейтрино. Электрон и позитрон называют бета-частицами. Бета-распад увеличивает или уменьшает атомный номер на единицу. К бета-распаду относят и обратный процесс — электронный захват, когда один из протонов атомного ядра захватывает орбитальный электрон и превращается в нейтрон, испуская электронное нейтрино.
- Гамма-излучение происходит из-за перехода ядра в состояние с более низкой энергией с испусканием электромагнитного излучения. Гамма-излучение может происходить вслед за испусканием альфа- или бета-частицы после радиоактивного распада.
Каждый радиоактивный изотоп характеризуется периодом полураспада, то есть временем, за которое распадается половина ядер образца. Это экспоненциальный распад, который вдвое уменьшает количество оставшихся ядер за каждый период полураспада. Например, по прошествии двух периодов полураспада в образце останется только 25 % ядер исходного изотопа[31].
Магнитный момент[править | править код]
Элементарные частицы обладают внутренним квантовомеханическим свойством, известным как спин. Оно аналогично угловому моменту объекта вращающегося вокруг собственного центра масс, хотя строго говоря, эти частицы являются точечными и нельзя говорить об их вращении. Спин измеряют в единицах приведённой планковской постоянной (

Магнитное поле, создаваемое магнитным моментом атома, определяется этими различными формами углового момента, как и в классической физике вращающиеся заряженные объекты создают магнитное поле. Однако наиболее значительный вклад происходит от спина. Благодаря свойству электрона, как и всех фермионов, подчиняться правилу запрета Паули, по которому два электрона не могут находиться в одном и том же квантовом состоянии, связанные электроны спариваются друг с другом, и один из электронов находится в состоянии со спином вверх, а другой — с противоположной проекцией спина — в состоянии со спином вниз. Таким образом магнитные моменты электронов сокращаются, уменьшая полный магнитный дипольный момент системы до нуля в некоторых атомах с чётным числом электронов[35].
В ферромагнитных элементах, таких как железо, нечётное число электронов приводит к появлению неспаренного электрона и к ненулевому полному магнитному моменту. Орбитали соседних атомов перекрываются, и наименьшее энергетическое состояние достигается, когда все спины неспаренных электронов принимают одну ориентацию, процесс известный как обменное взаимодействие. Когда магнитные моменты ферромагнитных атомов выравниваются, материал может создавать измеримое макроскопическое магнитное поле. Парамагнитные материалы состоят из атомов, магнитные моменты которых разориентированы в отсутствие магнитного поля, но магнитные моменты отдельных атомов выравниваются при приложении магнитного поля[35][36].
Ядро атома тоже может обладать ненулевым полным спином. Обычно при термодинамическом равновесии спины ядер ориентированы случайным образом. Однако для некоторых элементов (таких как ксенон-129) возможно поляризовать значительную часть ядерных спинов для создания состояния с сонаправленными спинами — состояния называемого гиперполяризацией. Это состояние имеет важное прикладное значение в магнитно-резонансной томографии[37][38].
Энергетические уровни[править | править код]
Электрон в атоме находится в связанном состоянии; находясь на возбуждённом уровне, он обладает потенциальной энергией, которая пропорциональна его расстоянию от ядра. Эта энергия обычно измеряется в электронвольтах (эВ), и максимальное её значение равно энергии, которую надо передать электрону, чтобы сделать его свободным (оторвать от атома). По мере перехода электрона (в атоме) на более низкие уровни потенциальная энергия уменьшается, но превращается не в кинетическую, а в энергию излучаемых фотонов. Согласно квантовомеханической модели атома связанный электрон может занимать только дискретный набор разрешённых энергетических уровней — состояний с определённой энергией. Наинизшее из разрешённых энергетических состояний называется основным (потенциальная энергия равна нулю — электрон глубже падать уже не может), а все остальные — возбуждёнными[39].
Для перехода электрона с одного энергетического уровня на другой нужно передать ему или отнять у него энергию. Эту энергию можно сообщить атому путём удара другой частицей либо путём поглощения или, соответственно, испускания фотона, причём энергия этого фотона равна абсолютной величине разности энергий начального и конечного уровней электрона. Частота испускаемого излучения пропорциональна энергии фотона, поэтому переходы между разными энергетическими уровнями проявляются в различных областях электромагнитного спектра[40]. Каждый химический элемент имеет уникальный спектр испускания, который зависит от заряда ядра, заполнения электронных подоболочек, взаимодействия электронов, а также других факторов[41].

Пример линейчатого спектра поглощения
Когда излучение с непрерывным спектром проходит через вещество (например, газ или плазму), некоторые фотоны поглощаются атомами или ионами, вызывая электронные переходы между энергетическим состояниями, разность энергий которых равна энергии поглощённого фотона. Затем эти возбуждённые электроны спонтанно возвращаются на уровень, лежащий ниже по шкале энергии, снова испуская фотоны. Испущенные фотоны излучаются не в том направлении, в каком падал поглощённый, а произвольно в телесном угле 4 пи стерадиан. В результате в непрерывном спектре появляются участки с очень низким уровнем излучения, то есть темные линии поглощения. Таким образом, вещество ведёт себя как фильтр, превращая исходный непрерывный спектр в спектр поглощения, в котором имеются серии тёмных линий и полос. При наблюдении с тех углов, куда не направлено исходное излучение, можно заметить излучение с эмиссионным спектром, испускаемое атомами. Спектроскопические измерения энергии, амплитуды и ширины спектральных линий излучения позволяют определить вид излучающего вещества и физические условия в нём[42].
Более детальный анализ спектральных линий показал, что некоторые из них обладают тонкой структурой, то есть расщеплены на несколько близких линий. В узком смысле «тонкой структурой» спектральных линий принято называть их расщепление, происходящее из-за спин-орбитального взаимодействия между спином и вращательным движением электрона[43].
Взаимодействие магнитных моментов электрона и ядра приводит к сверхтонкому расщеплению спектральных линий, которое, как правило, меньше, чем тонкое.
Если поместить атом во внешнее магнитное поле, то также можно заметить расщепление спектральных линий на две, три и более компонент — это явление называется эффектом Зеемана. Он вызван взаимодействием внешнего магнитного поля с магнитным моментом атома, при этом в зависимости от взаимной ориентации момента атома и магнитного поля энергия данного уровня может увеличиться или уменьшиться. При переходе атома из одного расщеплённого состояния в другое будет излучаться фотон с частотой, отличной от частоты фотона при таком же переходе в отсутствие магнитного поля. Если спектральная линия при помещении атома в магнитное поле расщепляется на три линии, то такой эффект Зеемана называется нормальным (простым). Гораздо чаще в слабом магнитном поле наблюдается аномальный (сложный) эффект Зеемана, когда происходит расщепление на 2, 4 или более линий (аномальный эффект происходит из-за наличия спина у электронов). При увеличении магнитного поля вид расщепления упрощается, и аномальный эффект Зеемана переходит в нормальный (эффект Пашена — Бака)[44]. Присутствие электрического поля также может вызвать сравнимый по величине сдвиг спектральных линий, вызванный изменением энергетических уровней. Это явление известно как эффект Штарка[45].
Если электрон находится в возбуждённом состоянии, то взаимодействие с фотоном определённой энергии может вызвать вынужденное излучение дополнительного фотона с такой же энергией — для этого должен существовать более низкий уровень, на который возможен переход, и разность энергий уровней должна равняться энергии фотона. При вынужденном излучении эти два фотона будут двигаться в одном направлении и иметь одинаковую фазу. Это свойство используется в лазерах, которые могут испускать когерентный пучок света в узком диапазоне частот[46].
Валентность[править | править код]
Внешняя электронная оболочка атома, если она не полностью заполнена, называется валентной оболочкой, а электроны этой оболочки называются валентными электронами. Число валентных электронов определяет то, как атом связывается с другими атомами посредством химической связи. Путём образования химических связей атомы стремятся заполнить свои внешние валентные оболочки[47].
Чтобы показать повторяющиеся химические свойства химических элементов, их упорядочивают в виде периодической таблицы. Элементы с одинаковым числом валентных электронов формируют группу, которая изображается в таблице в виде столбца (движение по горизонтальному ряду соответствуют заполнению валентной оболочки электронами). Элементы, находящиеся в самом правом столбце таблицы, имеют полностью заполненную электронами внешнюю оболочку, поэтому они отличаются крайне низкой химической активностью и называются инертными или благородными газами[48][49].
Дисперсионное притяжение[править | править код]
Важным свойством атома является его склонность к дисперсионному притяжению. Происхождение дисперсионных сил было объяснено в 1930 году Ф. Лондоном. Межатомное взаимодействие возникает вследствие флуктуаций заряда в двух атомах, находящихся близко друг от друга. Поскольку электроны движутся, каждый атом обладает мгновенным дипольным моментом, отличным от нуля. Если бы флуктуации электронной плотности в двух атомах были бы несогласованными, то не было бы результирующего притяжения между атомами. Однако мгновенный диполь на одном атоме наводит противоположно направленный диполь в соседнем атоме. Эти диполи притягиваются друг к другу за счёт возникновения силы притяжения, которая называется дисперсионной силой, или силой Лондона. Энергия такого взаимодействия прямо пропорциональна квадрату электронной поляризуемости атома α и обратно пропорциональна r6, где r — расстояние между двумя атомами[50].
Деформационная поляризация атома[править | править код]
Деформационная поляризация проявляется в присущей атомам способности к упругой деформации их электронных оболочек под действием электромагнитных полей. Сегодняшнее понимание явления деформационной поляризации основано на представлениях о конечной упругости электронных оболочек атомов под действием электрического поля[51]. Снятие внешнего электрического поля приводит к восстановлению электронной оболочки атома.
Деформация электронной оболочки атома приводит к смещению электронной плотности в атоме, что сопровождается образованием наведённого электрического дипольного момента μ. Дипольный момент равен произведению величины положительного заряда q на расстояние между зарядами L и направлен от отрицательного заряда к положительному μ=qL. В относительно слабых электрических полях наведённый дипольный момент пропорционален напряжённости электрического поля E. μ =αeE, где αe — электронная поляризуемость атома. Наибольшее значение электронной поляризуемости наблюдается у атомов щелочных металлов, а минимальное у атомов благородных газов.
Ионизация атома[править | править код]
При высоких значениях напряжённости приложенного электрического поля наблюдается необратимая деформация атома, сопровождающаяся отрывом электрона.
Происходит ионизация атома, атом отдаёт электрон и превращается в положительно заряженный ион — катион. Отрыв электрона от атома требует затраты энергии, называемой потенциалом ионизации или энергией ионизации.
Энергия ионизации атома сильно зависит от его электронной конфигурации. Изменение энергии отрыва первого электрона в зависимости от порядкового номера элемента приведено на рисунке.
Наименьшей энергией ионизации обладают атомы щелочных металлов, наибольшей — атомы благородных газов.
Для многоэлектронных атомов энергия ионизации I1, I2, I3… соответствует отрыву первого, второго, третьего и т. д. электронов.
Взаимодействие атома с электроном[править | править код]
| Атом | Энергия сродства к электрону, эВ[52] |
|---|---|
| F | 3,62 ± 0,09 |
| Cl | 3,82 ± 0,06 |
| Br | 3,54 ± 0,06 |
| I | 3,23 ± 0,06 |

Атомы могут, в той или иной степени, присоединять добавочный электрон и превращаться в отрицательный ион — анион.
Энергетический эффект процесса присоединения к нейтральному атому (Э) принято называть энергией сродства к электрону:
- Э + e– → Э–.
На рисунке представлена зависимость энергии сродства к электрону атомов от порядкового номера элемента. Наибольшим сродством к электрону обладают атомы галогенов (3—4 эВ).
Электроотрицательность атома[править | править код]
Электроотрицательность атома (χ) — фундаментальное свойство атома смещать к себе общие электронные пары в молекуле. Способность атома данного элемента к оттягиванию на себя электронной плотности по сравнению с другими элементами соединения зависит от энергии ионизации атома и его сродства к электрону. Согласно одному из определений (по Малликену) электроотрицательность атома (χ) может быть выражена как полусумма его энергии ионизации (i) и сродства к электрону (F):
Имеется около двадцати шкал электроотрицательности атома, в основу расчёта значений которых положены различные свойства веществ. Полученные значения разных шкал отличаются, но относительное расположение элементов в ряду электроотрицательностей примерно одинаково.
Детальный поиск взаимосвязи между шкалами электроотрицательности позволил сформулировать новый подход к выбору практической шкалы электроотрицательностей атомов[53].

Символизм[править | править код]
С момента вхождения человечества в атомную эру атом приобрел и символический смысл. Чаще всего атом изображается в виде упрощенной модели Бора-Резерфорда. Однако встречаются и более усложненные варианты изображения. Чаще всего изображение атома символизирует атомную энергетику («мирный атом»), ядерное оружие, ядерную физику, либо науку и научно-технический прогресс в целом.
См. также[править | править код]
- Физика атомов и молекул
- Молекула
- Электрон
- Протон
- Нейтрон
Примечания[править | править код]
- ↑ 1 2 3 Большой энциклопедический словарь. Физика / Гл. ред. А. М. Прохоров. — М.: Большая Российская энциклопедия, 1998. — С. 36. — 944 с. — ISBN 5-85270-306-0.
- ↑ Большой иллюстрированный словарь иностранных слов / Ред. Е. А. Гришина. — АСТ; Астрель; Русские словари. — С. 91. — 960 с. — ISBN 5-17-008793-4.
- ↑ 1 2 Ельяшевич М. А. Атом // Большая Советская Энциклопедия. 3-е изд. / гл. ред. А. М. Прохоров. — М.: Советская энциклопедия, 1970. — Т. 2. Ангола — Барзас. — С. 389—394.
- ↑ Химический энциклопедический словарь / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1983. — С. 58. — 792 с.
- ↑ Atom Архивная копия от 4 ноября 2015 на Wayback Machine // IUPAC Gold Book
- ↑ Демокрит // Школьная энциклопедия «Руссика». История Древнего мира / А. О. Чубарьян. — М.: Olma Media Group, 2003. — С. 281—282. — 815 с. — ISBN 5-948-49307-5.
- ↑ Планетарная модель атома Архивировано 15 июня 2008 года.
- ↑ Demtröder, 2002.
- ↑ Демельт Х.«Эксперименты с покоящейся изолированной субатомной частицей» Архивная копия от 23 мая 2017 на Wayback Machine // УФН, т. 160 (12), с. 129—139, 1990
- ↑ Nobel lecture, December, 8, 1989, Hans D. Dehmelt Experiments with an isolated subatomic particle at rest Архивная копия от 10 августа 2017 на Wayback Machine
- ↑ Woan, 2000.
- ↑ MacGregor, 1992.
- ↑ The Particle Adventure. Particle Data Group. Lawrence Berkeley Laboratory (2002). Дата обращения: 3 января 2009. Архивировано 21 августа 2011 года.
- ↑ James Schombert. Elementary Particles. University of Oregon (18 апреля 2006). Дата обращения: 3 января 2007. Архивировано 21 августа 2011 года.
- ↑ Howard S. Matis. The Isotopes of Hydrogen. Guide to the Nuclear Wall Chart. Lawrence Berkeley National Lab (9 августа 2000). Дата обращения: 21 декабря 2007. Архивировано 21 августа 2011 года.
- ↑ Rick Weiss. Scientists Announce Creation of Atomic Element, the Heaviest Yet. Washington Post (17 октября 2006). Дата обращения: 21 декабря 2007. Архивировано 21 августа 2011 года.
- ↑ 1 2 Sills, 2003.
- ↑ Belle Dumé. Bismuth breaks half-life record for alpha decay. Physics World (23 апреля 2003). Дата обращения: 21 декабря 2007. Архивировано 21 августа 2011 года.
- ↑ 1 2 Mills и др. (1993).
- ↑
Chung Chieh. Nuclide Stability. University of Waterloo (22 января 2001). Дата обращения: 4 января 2007. Архивировано из оригинала 30 августа 2007 года. - ↑ Atomic Weights and Isotopic Compositions for All Elements. National Institute of Standards and Technology. Дата обращения: 4 января 2007. Архивировано 21 августа 2011 года.
- ↑ G. Audi, A. H. Wapstra, C. Thibault. The Ame2003 atomic mass evaluation (II) (неопр.) // Nuclear Physics. — 2003. — Т. A729. — С. 337—676. Архивировано 16 сентября 2008 года.
- ↑ R. D. Shannon. Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides (англ.) // Acta Crystallographica, Section A : journal. — International Union of Crystallography, 1976. — Vol. 32. — P. 751. — doi:10.1107/S0567739476001551. Архивировано 30 сентября 2007 года.
- ↑ Judy Dong. Diameter of an Atom. The Physics Factbook (1998). Дата обращения: 19 ноября 2007. Архивировано 21 августа 2011 года.
- ↑ Zumdahl, 2002.
- ↑ Small Miracles: Harnessing nanotechnology. Oregon State University (2007). Дата обращения: 7 января 2007. Архивировано из оригинала 4 декабря 2007 года. — описывает толщину человеческого волоса как 105 нм и 10 углеродных атомов по толщине как 1 нм.
- ↑ «There are 2 000 000 000 000 000 000 000 (that’s 2 sextillion) atoms of oxygen in one drop of water—and twice as many atoms of hydrogen» // Padilla et al., 2002, p. 32
- ↑ Карат равен 200 миллиграмм. По определению, углерод-12 имеет 12 грамм на моль. Постоянная Авогадро равна 6,02⋅1023 атомов на моль.
- ↑ Feynman, 1995.
- ↑ First Detailed Photos of Atoms. Inside Science News Service (14 сентября 2009). Дата обращения: 24 июня 2014. Архивировано 24 июня 2014 года.
- ↑ 1 2 Radioactivity. Splung.com. Дата обращения: 19 декабря 2007. Архивировано 21 августа 2011 года.
- ↑ L’Annunziata (2003).
- ↑ Richard B. Firestone. Radioactive Decay Modes. Berkeley Laboratory (22 мая 2000). Дата обращения: 7 января 2007. Архивировано 21 августа 2011 года.
- ↑ J. P. Hornak. Chapter 3: Spin Physics. The Basics of NMR. Rochester Institute of Technology (2006). Дата обращения: 20 марта 2011. Архивировано из оригинала 26 мая 2007 года.
- ↑ 1 2 Paul A. Schroeder. Magnetic Properties. University of Georgia (22 февраля 2000). Дата обращения: 7 января 2007. Архивировано из оригинала 18 февраля 2001 года.
- ↑ Greg Goebel. [4.3] Magnetic Properties of the Atom. Elementary Quantum Physics. In The Public Domain website (1 сентября 2007). Дата обращения: 7 января 2007. Архивировано 21 августа 2011 года.
- ↑ Lynn Yarris. Talking Pictures (неопр.) // Berkeley Lab Research Review. Архивировано 15 июня 1997 года.
- ↑ Liang, Haacke, 1999.
- ↑ Bart J. Van Zeghbroeck. Energy levels. Shippensburg University (1998). Дата обращения: 23 декабря 2007. Архивировано 15 января 2005 года.
- ↑ Fowles, 1989.
- ↑ W. C. Martin, W. L. Wiese. Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas. National Institute of Standards and Technology (май 2007). Дата обращения: 8 января 2007. Архивировано 21 августа 2011 года.
- ↑ Atomic Emission Spectra — Origin of Spectral Lines. Avogadro Web Site. Дата обращения: 10 августа 2006. Архивировано 21 августа 2011 года.
- ↑ Richard Fitzpatrick. Fine structure. University of Texas at Austin (16 февраля 2007). Дата обращения: 14 февраля 2008. Архивировано 21 августа 2011 года.
- ↑ Michael Weiss. The Zeeman Effect. University of California-Riverside (2001). Дата обращения: 6 февраля 2008. Архивировано 21 августа 2011 года.
- ↑ Beyer, 2003.
- ↑ Thayer Watkins. Coherence in Stimulated Emission. San José State University. Дата обращения: 23 декабря 2007. Архивировано 21 августа 2011 года.
- ↑ William Reusch. Virtual Textbook of Organic Chemistry. Michigan State University (16 июля 2007). Дата обращения: 11 января 2008. Архивировано 21 августа 2011 года.
- ↑ Husted Robert и др. Periodic Table of the Elements. Los Alamos National Laboratory (11 декабря 2003). Дата обращения: 11 января 2008. Архивировано 21 августа 2011 года.
- ↑ Rudy Baum. It’s Elemental: The Periodic Table. Chemical & Engineering News (2003). Дата обращения: 11 января 2008. Архивировано 21 августа 2011 года.
- ↑ Даниэльс Ф., Олберти Р. Физическая химия / под ред. К.В.Топчиевой. — М.: Мир, 1978. — С. 453. — 646 с.
- ↑ Потапов А.А. Деформационная поляризация. Поиск оптимальных моделей. — Новосибирск: “Наука”, 2004. — 511 с.
- ↑ Справочник химика. — II-ое, перераб. и доп.. — Л.-М.: ГНТИ Химической литературы, 1962. — Т. I. — С. 328. — 1072 с.
- ↑ Филиппов Г. Г., Горбунов А. И. Новый подход к выбору практической шкалы электроотрицательностей атомов. — Российский химический журнал, 1995. — Т. 39, Вып. 2. — С. 39—42.
Литература[править | править код]
- Бете Г., Солпитер Э. Квантовая механика атомов с одним и двумя электронами. — М.: Физматгиз, 1960. — 562 с.
- Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. — 532 c.
- Веселов М. Г., Лабзовский Л. Н. Теория атома: Строение электронных оболочек. — М.: Наука, 1986. — 328 с. Архивная копия от 31 июля 2013 на Wayback Machine
- Зоммерфельд А. Строение атома и спектры. Том 1 — М.: ГИТТЛ, 1956.
- Зоммерфельд А. Строение атома и спектры. Том 2 — М.: ГИТТЛ, 1956.
- Шпольский Э. В. Атомная физика. Том 2. Основы квантовой механики и строение электронной оболочки атома 4-е изд. — М.: Наука, 1974.
- На английском языке
- Michael F. L’Annunziata. Handbook of Radioactivity Analysis. — 2003. — ISBN 0-12-436603-1.
- H. F. Beyer, V. P. Shevelko. Introduction to the Physics of Highly Charged Ions. — CRC Press, 2003. — ISBN 0-75-030481-2.
- Gregory R. Choppin, Jan-Olov Liljenzin, Jan Rydberg. Radiochemistry and Nuclear Chemistry. — Elsevier, 2001. — ISBN 0-75-067463-6.
- J. Dalton. A New System of Chemical Philosophy, Part 1. — London and Manchester: S. Russell, 1808.
- Wolfgang Demtröder. Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics. — 1st ed. — Springer, 2002. — ISBN 3-540-20631-0.
- Richard Feynman. Six Easy Pieces. — The Penguin Group, 1995. — ISBN 978-0-140-27666-4.
- Grant R. Fowles. Introduction to Modern Optics. — Courier Dover Publications, 1989. — ISBN 0-48-665957-7.
- Mrinalkanti Gangopadhyaya. Indian Atomism: History and Sources. — Atlantic Highlands, New Jersey: Humanities Press, 1981. — ISBN 0-391-02177-X.
- David L. Goodstein. States of Matter. — Courier Dover Publications, 2002. — ISBN 0-48-649506-X.
- Edward Robert Harrison. Masks of the Universe: Changing Ideas on the Nature of the Cosmos. — Cambridge University Press, 2003. — ISBN 0-52-177351-2.
- Tatjana Jevremovic. Nuclear Principles in Engineering. — Springer, 2005. — ISBN 0-38-723284-2.
- James Lequeux. The Interstellar Medium. — Springer, 2005. — ISBN 3-540-21326-0.
- Z.-P. Liang, E. M. Haacke. Encyclopedia of Electrical and Electronics Engineering: Magnetic Resonance Imaging / J. G. Webster. — John Wiley & Sons, 1999. — P. 412—26. — ISBN 0-47-113946-7.
- Malcolm H. MacGregor. The Enigmatic Electron. — Oxford University Press, 1992. — ISBN 0-19-521833-7.
- Oliver Manuel. Origin of Elements in the Solar System: Implications of Post-1957 Observations. — Springer, 2001. — ISBN 0-30-646562-0.
- Robert M. Mazo. Brownian Motion: Fluctuations, Dynamics, and Applications. — Oxford University Press, 2002. — ISBN 0-19-851567-7.
- Ian Mills, Tomislav Cvitaš, Klaus Homann, Nikola Kallay, Kozo Kuchitsu. Quantities, Units and Symbols in Physical Chemistry. — 2nd ed. — Oxford: International Union of Pure and Applied Chemistry, Commission on Physiochemical Symbols Terminology and Units, Blackwell Scientific Publications, 1993. — ISBN 0-632-03583-8.
- Richard Myers. The Basics of Chemistry. — Greenwood Press, 2003. — ISBN 0-31-331664-3.
- Michael J. Padilla, Ioannis Miaoulis, Martha Cyr. Prentice Hall Science Explorer: Chemical Building Blocks. — Upper Saddle River, New Jersey USA: Prentice-Hall, 2002. — ISBN 0-13-054091-9.
- Linus Pauling. The Nature of the Chemical Bond. — Cornell University Press, 1960. — ISBN 0-80-140333-2.
- Jeremy I. Pfeffer, Shlomo Nir. Modern Physics: An Introductory Text. — Imperial College Press, 2000. — ISBN 1-860-94250-4.
- Leonid Ivanovich Ponomarev. The Quantum Dice. — CRC Press, 1993. — ISBN 0-75-030251-8.
- J. Kenneth Shultis, Richard E. Faw. Fundamentals of Nuclear Science and Engineering. — CRC Press, 2002. — ISBN 0-82-470834-2.
- Robert Siegfried. From Elements to Atoms: A History of Chemical Composition. — DIANE, 2002. — ISBN 0-87-169924-9.
- Alan D. Sills. Earth Science the Easy Way. — Barron’s Educational Series, 2003. — ISBN 0-76-412146-4.
- Boris M. Smirnov. Physics of Atoms and Ions. — Springer, 2003. — ISBN 0-38-795550-X.
- Dick Teresi. Lost Discoveries: The Ancient Roots of Modern Science. — Simon & Schuster, 2003. — P. 213—214. — ISBN 0-74-324379-X.
- Graham Woan. The Cambridge Handbook of Physics. — Cambridge University Press, 2000. — ISBN 0-52-157507-9.
- Charles Adolphe Wurtz. The Atomic Theory. — New York: D. Appleton and company, 1881.
- Marco Zaider, Harald H. Rossi. Radiation Science for Physicians and Public Health Workers. — Springer, 2001. — ISBN 0-30-646403-9.
- Steven S. Zumdahl. Introductory Chemistry: A Foundation. — 5th ed. — Houghton Mifflin, 2002. — ISBN 0-618-34342-3.
Ссылки[править | править код]
- Атом в Физической энциклопедии
- Eden Francis. Atomic Size. Clackamas Community College (2002). Дата обращения: 9 января 2007. Архивировано 21 августа 2011 года.
- Craig C. Freudenrich. How Atoms Work. How Stuff Works. Дата обращения: 9 января 2007. Архивировано 21 августа 2011 года.
- The atom. Science aid+ (2007). — A guide to the atom for teens. Дата обращения: 9 января 2007. Архивировано 21 августа 2011 года.
- Atoms and Atomic Structure. Би-би-си (3 января 2006). Дата обращения: 11 января 2007. Архивировано 21 августа 2011 года.
- Physics 2000. University of Colorado (3 января 2006). Дата обращения: 11 января 2008. Архивировано 21 августа 2011 года.
- Почему электрон не падает на ядро? Научный журнал ARI
- Украинские ученые впервые сфотографировали атом (16 сентября 2009).
- Ученые изолировали, захватили и сфотографировали атом Рубидия 85 (1 октября 2010). Дата обращения: 1 октября 2010. Архивировано 2 февраля 2012 года.
- Строение атома
- Строение атома (учебный фильм)
- Спектры атомов. Дата обращения: 10 октября 2010. Архивировано 21 августа 2011 года.
- Структура атомов, учебный фильм. Дата обращения: 10 октября 2010. Архивировано 21 августа 2011 года.


