Запрос «B12» перенаправляется сюда; см. также другие значения.
| Цианокобаламин | |
|---|---|
  |
|
 |
|
| Общие | |
| Хим. формула | С63H88CoN14O14P |
| Физические свойства | |
| Состояние | твёрдое, красного цвета |
| Молярная масса | 1355.38 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | > 300 °C |
| • кипения | > 300 °C °C |
| • вспышки | N/A °C |
| Классификация | |
| Рег. номер CAS | 68-19-9 |
| PubChem | 16212801 |
| SMILES |
NC(=O)C[C@@]8(C)[C@H](CCC(N)=O)C=2/N=C8/C(/C)=C1/[C@@H](CCC(N)=O)[C@](C)(CC(N)=O)[C@@](C)(N1[Co+]C#N)[C@@H]7/N=C(C(C)=C3/N=C(/C=2)C(C)(C)[C@@H]3CCC(N)=O)[C@](C)(CCC(=O)NCC(C)OP([O-])(=O)O[C@@H]6[C@@H](CO)O[C@H](n5cnc4cc(C)c(C)cc45)[C@@H]6O)[C@H]7CC(N)=O |
| Безопасность | |
| NFPA 704 |
1 1 0 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Витами́нами B12 называют группу биологически активных веществ, называемых кобаламинами и относящиеся к корриноидам, содержащим в структуре атом кобальта (III) и являющиеся хелатными соединениями[1][2].
В научной литературе под витамином B12 обычно подразумевают цианокобаламин, который свободно преобразуется в одну из коферментных форм в человеческом организме[3]. В форме цианокобаламина в организм человека поступает основное количество витамина B12, при этом он не является синонимом B12, несколько других соединений также обладают B12-витаминной активностью[4]. Витамин B12 также называется внешним фактором Касла[5].
В природе продуцентами этого витамина являются бактерии и археи, в растениях не синтезируется[6].
История открытия[править | править код]
Впервые влияние на развитие анемии недостатка какого-то вещества обнаружил исследователь Уильям Мёрфи в эксперименте на собаках, у которых была искусственно вызвана анемия. Подопытные собаки, которым давали в пищу большое количество печени, излечивались от анемии. Впоследствии учёные Джордж Уипл и Джордж Майнот поставили перед собой задачу выделить из печени фактор, непосредственно отвечающий за это лечебное свойство. Это им удалось, новый противоанемийный фактор получил название витамина B12, и все трое учёных в 1934 году были удостоены Нобелевской премии по медицине[7].
Молекулярную химическую структуру цианокобаламина установила Дороти Кроуфут-Ходжкин в 1956 году по данным рентгеноструктурного анализа[8].
Химическое строение[править | править код]
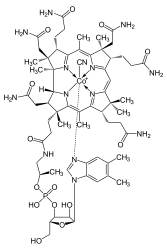
Пространственная структура цианокобаламина, отмечены: зелёным кобальт, оранжевым фосфор, синим азот, серым углерод, розовым углерод образующий корриновое кольцо, красным кислород
К кобаламинам относятся[1][9]:
- собственно цианокобаламин (Со-α-[α-(5,6-диметил-бензимидазолил)]-(Со-β-циано)кобамид; CN-Cbl; С63H89O14N14PCo) в котором с кобальтом связывается CN–-группа, наиболее устойчивое соединение, синтезируемое или образующееся при искусственном выделении из живых организмов, в естественных условиях не встречается;
- гидроксокобаламин (или оксикобаламин, или витамин B12a: Со-α-[α-(5,6-диметил-бензимидазолил)]-(Со-β-гидроксо)кобамид; OH-Cbl; С62H90O15N13PCo) в котором CN– заменена на OH–-группу, природная активная форма витамина B12 присутствующая в организмах животных, обратимо превращается в кислой среде в аквакобаламин[10];
- аквакобаламин (или витамин B12b: Со-α-[α-(5,6-диметил-бензимидазолил)]-(Со-β-аква)кобамид; aq-Cbl; С62H91O15N13PCo) продуцируется микроорганизмами, обратимо превращается в щелочной среде в гидроксокобаламин;
- нитрокобаламин (или витамин B12c) в котором CN– заменена на ONO–-группу;
- коферментные формы витамина B12: метилкобаламин и кобамамид[11];
- диаквакобинамид[12].
В природе обнаружены либо искусственно синтезированы кобаламины и с другими лигандами: сульфатокобаламин (SO3-), хлорокобаламин (Cl-), бромокобаламин (Br-), тиоцианатокобаламин (SHC-), дицианокобаламин [(RCo—CN)CN]-. Возможно образование гексаперхлората цианокобаламина. Витамин B12с образуется из витамина B12b под воздействием азотистой кислоты, также синтезируется Streptomyces griseus[en]. Все производные кобаламина проявляют биологическую активность витамина B12. При взаимодействии с CN–, производные превращаются в цианокобаламин. В кислой среде из цианокобаламина образуется биологический низкоактивный циано-13-эпикобаламин (неовитамин B12) в котором пропионамидная группа в кольце «C» (с метильной группой) коррина пространственно расположена с другой стороны. При одноэлектронном восстановлении молекулы цианокобаламина образуется устойчивый в кристаллическом состоянии витамин B12t c двухвалентным атомом кобальта, при двухэлектронном восстановлении получается витамин B12s устойчивый в водных растворах и под воздействием кислорода воздуха превращающегося в витамин B12a/B12b в зависимости от pH раствора. Для получения меченых радиоизотопных молекул цианокобаламина либо добавляют радиоактивный изотоп 60Co при культивировании микроорганизмов, либо к оксикобаламину добавляют синильную кислоту с изотопом 14С[2].
B12 имеет самое сложное по сравнению с другими витаминами химическое строение, основой которого является корриновое кольцо. Коррин во многом похож на порфирины (сложные химические структуры, входящие в состав гема, хлорофилла и цитохромов), но отличается от порфиринов тем, что два пятичленных гетероцикла в составе коррина соединены между собой непосредственно, а не метиленовым мостиком. В центре корриновой структуры располагается ион кобальта, образующий четыре координационные связи с атомами азота. Ещё одна координационная связь соединяет кобальт с диметилбензимидазольным нуклеотидом. Последняя, шестая координационная связь кобальта остаётся свободной: именно по этой связи и присоединяется цианогруппа, гидроксильная группа, метильный или 5′-дезоксиаденозильный остаток с образованием четырёх вариантов витамина B12, соответственно. Ковалентная связь углерод-кобальт в структуре цианокобаламина — единственный известный в живой природе пример ковалентной связи переходный металл-углерод.
Получение витамина B12[править | править код]
Кристаллы метилкобаламина и его водный раствор
До освоения синтеза витамина B12 он мог добываться экстракцией из печени животных. Сначала печень, а затем её экстракт использовались в лечении пернициозной анемии[13].
Химический синтез[править | править код]
Полный химический синтез цианокобаламина (англ.) (рус. впервые был осуществлён в 1972 году в результате многолетней совместной работы двух исследовательских групп (одна из которых, руководимая Робертом Вудвордом, работала в Гарварде, а другая, возглавляемая Альбертом Эшенмозером, в Швейцарском федеральном технологическом институте в Цюрихе). Первые работы над синтезом витамина В12 были начаты ещё в начале 60-х годов 20 века. На разработку общей стратегии синтеза и саму работу ушло более 10 лет. В ходе планирования синтеза, молекула была условно разделена на два основных фрагмента, синтезом которых и занимались группы, руководимые Вудвордом и Эшенмозером. Особая сложность синтеза биологически активного витамина В12 была обусловлена, в частности, наличием в корриновом кольце 9 хиральных (оптически активных) атомов углерода. В общей сложности в работах по синтезу, на протяжении ряда лет, участвовали порядка 100 учёных из примерно 20 стран, а сама разработанная схема синтеза включала 95 стадий[14][15]. Успешный полный синтез соединения столь сложной структуры явился выдающимся достижением синтетической органической химии и на практике продемонстрировал принципиальную возможность химического синтеза “любого” природного соединения, вне зависимости от сложности строения его молекулы.
Микробиологическое производство[править | править код]
Для получения препаратов витамина B12 (в основном цианокобаламина) в промышленных масштабах для нужд медицины и сельского хозяйства используется микробиологическое производство. Для производства применяют микроорганизмы и их штаммы-мутанты, такие как[9][16]:
- для медицинских препаратов — Propionibacterium[en] shermanii (штамм М-82 с выходом продукта до 58 мг/л), Propionibacterium freudenreichii[en], Pseudomonas denitrificans[en] (штамм MB 2436 с выходом продукта до 59 мг/л). Используется глубинное культивирование;
- для кормовых концентратов витамина B12 — Methanococcus[en] halophilus (с выходом продукта 16-42 мг/л, в питательные среды также добавляются пивные или кормовые дрожжи в качестве источника некоторых питательных веществ и создания благоприятной культуральной среды для метанобразующих бактерий, а также для обогащения кормов витаминами B2, B6, PP). Используется метод ферментации. При производстве так же образуются сопутствующие балластные продукты как фактор А, фактор B (предшественник витамина — кобинамид), фактор III (5-оксибензилиндазол), псевдовитамин B12 и ряд подобных.
Промышленное производство витамина B12 с помощью пропионовокислых бактерий включает следующие технологические стадии[17]:
- в течение года в железобетонных ферментерах происходит непрерывное сбраживание барды комплексом бактерий;
- полученная метановая бражка сгущается;
- сгущенная масса сушится на распылительной сушилке.
Из-за того, что витамин B12 неустойчив при тепловой обработке, особенно в щелочной среде, в метановую бражку перед выпариванием добавляют хлор до оптимального значения pH 5,0—5,3, что делает среду кислой, также добавляется сульфит натрия до оптимального содержания 0,07—0,1%[17].
Метаболизм в организме[править | править код]
В желудке желудочный сок растворяет связанный с белками пищи B12. Формы в таблетках могут проходить через желудок, но для всасывания свободного B12 (не связанного с белками пищи) желудочный сок не нужен. В желудке вырабатывается внутренний фактор Кастла (в некоторых источниках — «Касла»), необходимый для всасывания B12 в кишечнике[18]. R-протеин (другие названия — гаптокоррин и кобалофилин) — связывающий B12 белок слюны, но действовать он начинает в желудке после того, как желудочный сок высвободит B12 из белкового комплекса, тогда этот протеин связывается с ним для того, чтобы сам B12 также не был разрушен желудочным соком[19]. Затем B12 соединяется с внутренним фактором Кастла — ещё одним связывающим белком, который синтезируется париетальными клетками желудка, его выработка стимулируется гистамином, гастрином, пентагастрином и непосредственно пищей. В двенадцатиперстной кишке протеазы высвобождают B12 из комплекса с R-пептидом, затем B12 связывается с внутренним фактором, и только в таком связанном с внутренним фактором виде он распознается рецепторами поглощающих энтероцитов подвздошной кишки. Внутренний фактор защищает B12 от поедания кишечными бактериями[20].
Закись азота нарушает метаболизм витамина B12, поэтому при использовании закиси азота для анестезии (например, при стоматологических операциях) и пограничном уровне витамина B12 развивается полинейропатия, вызванная дефицитом B12[21][22]. Также в зоне риска находятся люди, постоянно работающие с закисью азота, в случае плохого уровня проветривания помещений[22]. Подобный дефицит требует терапии фолатами и B12.
Биохимические функции[править | править код]
Ковалентная связь C—Co кофермента B12 участвует в двух типах ферментативных реакций:
- Реакции переноса атомов, при которых атом водорода переносится непосредственно с одной группы на другую, при этом замещение происходит по алкильной группе, спиртовому атому кислорода или аминогруппе.
- Реакции переноса метильной группы (—CH3) между двумя молекулами.
В организме человека есть только два фермента с коферментом B12[19]:
- Метилмалонил-КоА-мутаза, фермент, использующий в качестве кофактора аденозилкобаламин и при помощи реакции, упомянутой выше в п. 1, катализирует перестановку атомов в углеродном скелете. В результате реакции из L-метилмалонил-КоА получается сукцинил-КоА. Эта реакция является важным звеном в цепи реакций биологического окисления белков и жиров.
- 5-метилтетрагидрофолат-гомоцистеин-метилтрансфераза, фермент из группы метилтрансфераз, использующий в качестве кофактора метилкобаламин и при помощи реакции, упомянутой выше в п. 2, катализирует превращение аминокислоты гомоцистеина в аминокислоту метионин.
Применение препарата в медицине[править | править код]
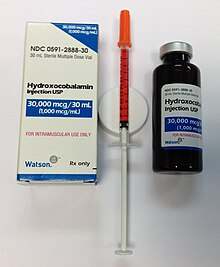
Инъекционный препарат витамина В12 набранный в шприц из ампулы
Недостаток в организме витамина В12 вследствие снижения его поступления в первую очередь из-за пониженной секреции внутреннего фактора Касла, нарушения абсорбции витамина из просвета кишечника при ряде заболеваний, при глистных инвазиях и дисбактериозах, синдроме слепой петли, реже вследствие алиментарной недостаточности из-за неполноценного питания или отсутствия транскобаламина II приводит к развитию B12-дефицитной анемии[23].
Цианокоболамин для лечебных целей выпускается промышленностью в виде растворов для парентерального введения, для целей профилактики его дефицита включается в состав ряда поливитаминных препаратов.
Оксикобаламин, кроме тех же показаний как и цианокобаламин[24], так же применяется в качестве антидота при отравлениях цианидами и при передозировке натрия нитропруссида, так как цианистое основание более тропно к кобальту в молекуле оксикоболамина, связывает цианистое основание в безвредную форму — цианокобаламин.
Фармакокинетика[править | править код]
Связь с белками плазмы — 90 %. Максимальная концентрация после подкожного и внутримышечного введения — через 1 час. Период полувыведения — 500 дней. Из печени выводится с желчью в кишечник и снова всасывается в кровь[25].
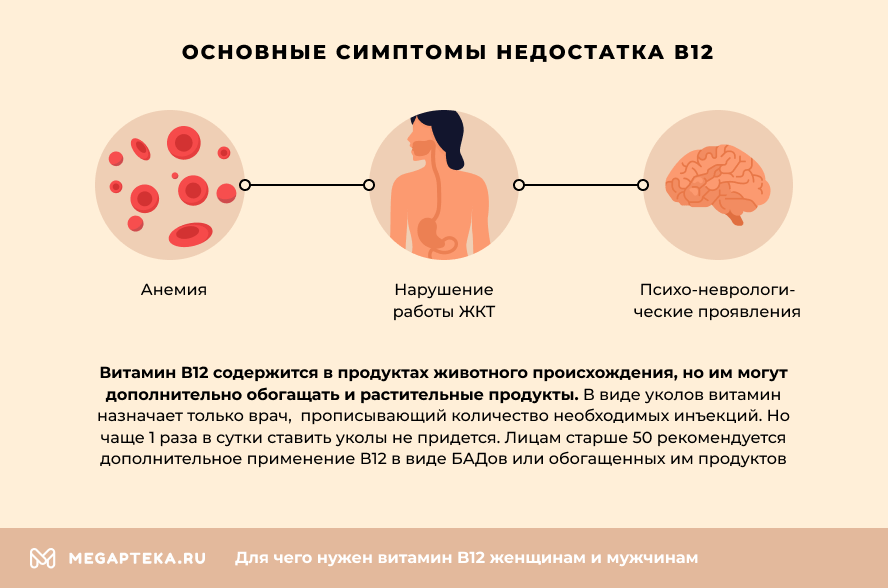
Заболевания, связанные с недостатком витамина[править | править код]
При недостатке витамина В12 развиваются некоторые неврологические состояния и заболевания, например, анемия[26], подострая комбинированная дегенерация спинного мозга (англ.) (рус.[27], полинейропатия[26].
Обычно дефицит витамина B12 лечат внутримышечными инъекциями препарата цианокобаламина. В последнее время была доказана достаточная эффективность пероральной компенсации дефицита пищевыми добавками в достаточной дозе. Суточный расход витамина B12 организмом человека оценивается примерно в 2—5 мкг[28].
Лабораторная химическая диагностика[править | править код]
Поскольку не существует золотого стандарта теста на дефицит витамина В12, для подтверждения предполагаемого диагноза проводится несколько различных лабораторных исследований.
Сывороточное значение витамина B12 является довольно неподходящим, поскольку оно изменяется поздно, а также относительно нечувствительным и неспецифичным[29].
Метилмалоновая кислота в моче или плазме крови считается функциональным маркером витамина В12, который повышается при истощении запасов витамина В12. Часто для более точной оценки наряду с метилмалоновой кислотой определяют гомоцистеин[29]. Однако повышенный уровень метилмалоновой кислоты может также указывать на часто упускаемое из виду метаболическое расстройство – комбинированную малоновую и метилмалоновую ацидурию (КМАММА) [30][31].
Самым ранним маркером дефицита витамина В12 является низкий уровень холотранскобаламина, который представляет собой комплекс витамина В12 и его транспортного белка[29].
Применение в ветеринарии[править | править код]
Обогащение кормов (включение в рацион) сельскохозяйственных животных витамином B12 способствует увеличению их продуктивности до 15 %[9].
|
|
Этот раздел статьи ещё не написан. Здесь может располагаться отдельный раздел. Помогите Википедии, написав его. (4 июля 2020) |
Источники витамина[править | править код]
| Продукт | мкг/100 г |
|---|---|
| Говяжья (или телячья) и баранья печень (приготовленные) | 70,5—88,0 |
| Бараньи почки (приготовленные) | 78,9 |
| Телячьи почки (приготовленные) | 36,9 |
| Говяжьи почки (приготовленные) | 24,9 |
| Куриная, индюшачья или свиная печень (приготовленная) | 16,8—31,2 |
| Потроха индейки (приготовленные) | 16,0 |
| Паштет из гусиной или куриной печени | 8,1—9,4 |
| Говяжий фарш (приготовленный) | 3,2—3,6 |
| Различные говяжьи обрезки (приготовленные) | 1,7—3,3 |
| Салями из говядины или свинины | 1,2—2,8 |
| Колбасные изделия | 0,5—2,6 |
| Полоски бекона (приготовленные) | 1,2—1,6 |
| Свиной паштет (приготовленный) | 1,0—1,2 |
| Ветчина (приготовленная) | 0,9 |
| Различные свиные обрезки (приготовленные) | 0,6—1,2 |
| Курица, индейка или утка (приготовленные) | 0,2—0,4 |
| Продукт | мкг/100 г |
|---|---|
| Мидии | 24,0 |
| Устрицы | 17,6—34,8 |
| Двустворчатые моллюски, за исключением устриц и мидий | 19,4 |
| Скумбрия (приготовленная) | 18,0—19,0 |
| Атлантическая сельдь (копчёная) | 18,6 |
| Икра (сырая) | 12,0 |
| Камчатский краб (приготовленный) | 11,4 |
| Обыкновенный тунец (сырой или приготовленный) | 10,9—12,4 |
| Сардины (консервированные в масле или томатном соусе) | 9,0 |
| Икра чёрная или красная | 8,0 |
| Форель (приготовленная) | 4,1—7,4 |
| Нерка (приготовленная) | 5,8 |
| Горбуша (консервированная с костями) | 4,9 |
| Атлантический лосось, дикий (приготовленный) | 3,0 |
| Тунец (серовато-розового оттенка, консервированный в воде) | 2,9 |
| Продукт | Содержание |
|---|---|
| Швейцарский сыр Эмменталь | 3,4 мкг/100 г |
| Сыры: фета, гауда, эдам, грюйер, бри, чеддер, фонтина, моцарелла, проволоне | 1,4—1,8 мкг/100 г |
| Ломтики плавленного сыра чеддер | 0,8 мкг/100 г |
| Молоко | 0,4—0,5 мкг/100 мл |
| Обезжиренное молоко | 0,5 мкг/100 мл |
| Пахта | 0,4 мкг/100 мл |
| Зернёный творог | 0,44—0,6 мкг/100 мл |
| Йогуртный напиток | 0,5 мкг/100 мл |
| Йогурт с фруктовой прослойкой на дне | 0,285—0,342 мкг/100 г |
| Греческий йогурт с фруктовой прослойкой на дне | 0,285 мкг/100 г |
| Греческий йогурт | 0,017—0,342 мкг/100 г |
| Шоколадное молоко | 0,036 мкг/100 мл |
| Йогурт | 0,028 мкг/100 г |
Витамин B12 не синтезируется в организме человека и поступает в организм вместе с пищей животного происхождения или с добавкой. Растительная пища практически не содержит витамина B12. Всасывается витамин в нижнем отделе тонкой кишки. Несмотря на то, что он вырабатывается бактериями в толстой кишке, следующей за тонкой, толстая кишка не способна его всасывать, а в тонкой бактерии практически отсутствуют[33]. Мало того, витамин B12 бактериями также поглощается, поэтому при заболеваниях, из-за которых в тонкой кишке резко увеличивается количество бактерий, у больных может возникнуть B12-ассоциированная анемия в результате соперничества в поглощении витамина между бактериями, обитающими в тонкой кишке и их носителем[34]. Непоглощённые бактериями остатки витамина B12 выводятся вместе с калом[35].
Многие травоядные животные также не могут синтезировать, и в их кишечнике не всасывается вырабатываемый обитающими там бактериями витамин B12. Однако жвачные животные, включая крупных рогатый скот, имеют специальный отдел желудка — рубец, заселённый производящими витамин B12 симбиотическими бактериями, что позволяет всасывать его в тонкой кишке[33]. После всасывания в кишечнике витамин попадает в кровь, а затем накапливается в печени и мышцах животного или попадает в молоко дойного скота[36]. Другие травоядные животные, — кролики, мыши, крысы и некоторые виды приматов для получения витамина используют копрофагию[33]. Свиньи и куры всеядны, поэтому витамин поступает к ним вместе с животной пищей, однако его содержание в сыром мясе этих животных ниже, чем в мясе жвачных животных[36].
В водоёмах витамин B12 производится бактериями и археями, поглощается фитопланктоном и попадает в зоопланктон. В конечном итоге, по пищевой цепи, витамин переносится в тела хищных рыб и его концентрация в мясе крупных рыб оказывается выше, чем в мясе мелких. Большое количество витамина B12 накапливается в печени и почках тунца и лосося[37]. При этом потери витамина в филе рыбы при различных видах кулинарного приготовления оказываются достаточно небольшими — от 2,3 % до 14, 8 %[38].
Хорошими источниками витамина B12 для человека являются говяжья, свиная и куриная печень, мясо и молоко жвачных животных, рыба, а также ферментированные молочные продукты, такие как сыр и йогурт[36]. Тем не менее при кулинарном приготовлении мяса (за исключением вакуумной обработки) значительное количество витамина разрушается[39]. Потребление же яиц практически не увеличивает содержание витамина B12 в крови[36] (из яиц усваивается менее 9 % витамина)[40]. В целом у здоровых людей из пищи усваивается лишь примерно половина содержащегося в ней витамина[41], при этом с увеличением потребления витамина B12 при приёме пищи его усвояемость уменьшается[40].
Большинству растений витамин B12 для нормальной жизнедеятельности не требуется, и они его не синтезируют[42]. Фрукты, овощи и зерновые культуры практически не содержат витамина B12[32]. Лишь небольшое количество, менее 0,1 мкг на 100 г, обнаружили в некоторых растениях: его содержат брокколи, спаржа, Белокопытник японский и пророщенный маш, что может объясняться способностью растений всасывать витамин из некоторых органических удобрений[43]. Так, исследования показали, что удобрение почвы коровьим навозом увеличивает содержание B12 в листьях шпината примерно на 0,14 мкг на 100 г[44]. Некоторое количество витамина присутствует в таких ферментированных продуктах, как темпе и натто, однако в самих соевых бобах, из которых эти продукты изготовлены, его обнаружить не удаётся[45]. Небольшое количество B12 может также накапливаться в растениях в результате взаимодействия с бактериями[41].
Витамин B12 обнаруживался и в плодовых телах высших грибов, не способных его синтезировать, что тоже может объясняться взаимодействием с бактериями[42]. Обычно в съедобных грибах содержится незначительное количество витамина B12 (менее 0,1 мкг на 100 г у сушёных грибов), однако некоторые грибы являются исключением. Так, в высушенных вороночнике рожковидном и лисичке обыкновенной содержание B12 варьируется от 1,09 до 2,65 мкг на 100 г, а в высушенном шиитаке содержится примерно 5,6 мкг на 100 г. При этом считается, что, несмотря на значительное содержание, в шиитаке витамин также попадает извне, предположительно, в результате взаимодействия с синтезирующими B12 бактериями[46].
В пищевой промышленности витамином B12 иногда обогащают такие продукты, как сухие завтраки[47], пищевые дрожжи, соевое молоко и вегетарианские заменители мяса[48].
Для веганов существуют рекомендации наладить регулярный прием препаратов кобаламина, либо употреблять пищу, обогащённую B12, так как растительная пища или не содержит в себе этот витамин, или содержит в слишком малых количествах, а организм человека синтезировать его не может. Дефицит B12 у веганов ведёт к риску развития заболеваний сердца и осложнений при беременности[49].
Нормы потребления[править | править код]
Норма потребления, установленная в США, соответствует 2,4 мкг в день для взрослого человека[50], а верхний предел пока не установлен[32]. Однако расход организма соответствует 2—5 мкг в день, что может превышать установленную суточную норму потребления. Одно из исследований показало, что потребление 6 мкг в день является достаточным для поддержания нормального уровня B12 в плазме крови[50].
| Возрастная группа | Возраст | Суточная норма потребления витамина B12, мкг (рекомендации Управления пищевых добавок (ODS) NIH)[51] |
|---|---|---|
| Младенцы | до 6 месяцев | 0,4 |
| Младенцы | 7—12 месяцев | 0,5 |
| Дети | 1—3 года | 0,9 |
| Дети | 4—8 лет | 1,2 |
| Дети | 9—13 лет | 1,8 |
| Мужчины и женщины | 14 лет и старше | 2,4 |
| Беременные женщины | Любой возраст | 2,6 |
| Кормящие женщины | Любой возраст | 2,8 |
Злоупотребление витамином B12[править | править код]
В выводах сделанных по результатам статистического анализа под руководством Theodore M. Brasky значится, что ежедневное употребление B12 как отдельного витамина в течение 10 лет в повышенных дозах >55 мкг в день увеличивает риск развития рака лёгких у мужчин на 30—40 %. Следует также обратить внимание, что существенная доля заболевших имела долгий анамнез табакокурения. У женщин данная закономерность не выявлена, хотя по результатам исследования отмечается, что в рационе исследуемых женщин витаминов группы B содержалось больше. Аналогичные же результаты выявлены и при употреблении в повышенных дозах витаминов B6 и B9[52].
Псевдовитамины B12[править | править код]
Под термином «псевдовитамин B12» подразумевают похожие на этот витамин вещества, обнаруженные в некоторых живых организмах, например, в цианобактериях (ранее известны как сине-зелёные водоросли) рода Спирулина. Такие витаминоподобные вещества не обладают витаминной активностью для организма человека[53][54]. Более того, эти вещества могут представлять определённую опасность для вегетарианцев, пытающихся с их помощью восполнить дефицит витамина, так как показано в опытах in vitro, что они блокируют метаболизм клеток молочной железы человека[54]. Также их наличие в крови показывает при анализе нормальную концентрацию витамина B12, хотя эти соединения не имеют витаминной активности, что может привести к ошибочному диагнозу и, в результате — к неправильному лечению пернициозной анемии.
Псевдовитамины B12 синтезируются бактериями в анаэробных условиях в кишечнике некоторых животных, в частности жвачных, в канализационном шламе. Не являются витаминами для животных, но являются факторами роста для некоторых бактерий, как и сами витамины B12. Структурно соответствуют цианокобаламину, но вместо 5,6-диметилбензимидазолнуклеозида содержат другие основания. К ним относятся[2]:
- «псевдовитамин B12» (или псевдовитамин B12b, циан-β-кобаламин, циан-γ-кобаламин) — 7α-аденилкобамид цианид;
- «B12-фактор» — 7α-(2-метилмеркаптоаденил)кобамид цианид;
- «Фактор III» — α-(5-оксибензимидазолил)кобамид цианид;
- «Фактор A» (или псевдовитамин B12d, псевдовитамин B12f, псевдовитамин B12m, циан-ω-кобаламин) — 7α-(2-метиладенил)кобамид цианид;
- «Фактор С» — 9β-гуанозил-5пирофосфокобинамид дицианид;
- «Фактор G» — 7α-гипоксантилкобамид цианид;
- «Фактор H» — 7α-(2-метилгипоксантил)кобамид цианид;
- α-бензимидазолилкобамид цианид;
- α-(5-метилбензимидазолил)кобамид цианид;
- 7α-гуанозилкобамид цианид.
Псевдовитамины продуцируемые микроорганизмами одновременно с витаминами и обладая схожими физико-химическими свойствами, представляют определённую трудность для очистки витаминов при промышленном производстве, в частности для этих целей может применяться электрофоретическое разделение.
См. также[править | править код]
- Кобамамид
- Витамины группы B
- CLYBL
- Гомоцистеин
Примечания[править | править код]
- ↑ 1 2 Волкова С. А., Боровков Н. Н. Основы клинической гематологии // Н. Новгород: Издательство Нижегородской государственной медицинской академии, 2013. — 400 с. (С. 36-38). ISBN 978-5-7032-0882-3.
- ↑ 1 2 3 Березовский В. М. Химия витаминов. / Изд. 2-е перераб. и доп. // М.: Пищевая промышленность, 1973 — 632 с., илл. (Стр.577-620). УДК 577.16.
- ↑ Watanabe, 2007, Introduction, p. 1266—1267.
- ↑ Herbert V. Vitamin B-12: plant sources, requirements, and assay (фр.) // The American Journal of Clinical Nutrition (англ.) (рус. : magazine. — 1988. — Vol. 48, no 3Suppl. — P. 852—858. — PMID 3046314.
- ↑ Алексеев Г. А. Касла факторы // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1979. — Т. 10 : Кабаков — Коалесценция. — 528 с. : ил.
- ↑ Cтатьи – Витамины – Витамин B12 – Электронная Медицина – Витаминные и минеральные премиксы, Микроцид и Феникс от производителя. elm.su. Дата обращения: 19 марта 2022. Архивировано 29 июня 2020 года.
- ↑ Minot, George Richards (1885-1950), physician and pathologist (англ.). American National Biography. Дата обращения: 19 марта 2022.
- ↑ Dorothy Mary Crowfoot Hodgkin, O.M. 12 May 1910–29 July 1994 on JSTOR (англ.). jstor.org. Дата обращения: 10 декабря 2018. Архивировано 11 декабря 2018 года.
- ↑ 1 2 3 Под ред. Столяровой В. А. Новый справочник химика и технолога. Часть 2: Сырьё и продукты промышленности органических и неорганических веществ // СПб.: АНО НПО «Профессионал», 2005, 2007 — 1142 с. (С. 1014-1019). ISBN 5-98371-028-1
- ↑ Ржечицкая Л. Э., Гамаюрова В. С. Пищевая химия. Часть 2: Водорастворимые витамины / Министерство образования и науки России, Казанский национальный исследовательский технологический университет // Казань: Издательство КНИТУ, 2013 – 140 с. (128-131). ISBN 978-5-7882-1499-3.
- ↑ Докучаева Е. А. Витамины // Общая биохимия / под ред. С. Б. Бокутя. — Минск: ИВЦ Минфина, 2017. — 52 с. — ISBN 978-985-7142-97-2.
- ↑ Polina N. Kucherenko, Denis S. Salnikov, Thu Thuy Bui, Sergei V. Makarov. Interaction of Aquacobalamin and Diaquacobinamide with Cyanamide / Ivanovo State University of Chemistry and Technology // Статья в журнале Macroheterocycles, 2013, № 6 (3). ISSN 1998-9539. С. 262-267, DOI: 10.6060/mhc120952m.
- ↑ I. Chanarin. Historical review: a history of pernicious anaemia (англ.) // British Journal of Haematology. — 2000. — November (vol. 111, iss. 2). — P. 407–415. — ISSN 0007-1048. — doi:10.1046/j.1365-2141.2000.02238.x. — PMID 11122079. Архивировано 14 февраля 2022 года.
- ↑ Р.Б. Вудворд. Полный синтез витамина В12 (рус.) // Успехи химии : журнал. — 1974. — Т. XLIII, № 4. — С. 727—743. Архивировано 5 июля 2020 года.
- ↑ Владимир Королев. Химики впервые полностью синтезировали мощнейший «лягушачий токсин». nplus1.ru. Дата обращения: 28 ноября 2019. Архивировано 28 ноября 2019 года.
- ↑ Под ред. Грачёвой И. М. Теоретические основы биотехнологии. Биохимические основы синтеза биологический активных веществ // М.: Элевар, 2003 — 554 с., илл. (С. 292-293). ISBN 5-89311-004-8.
- ↑ 1 2 Филимонова В. В., Тарабрин В. В. Производство витамина B12 // Молодой учёный : международный научный журнал / под ред. И. Г. Ахметова. — 2017. — 30 апреля (№ 17 (151)). — С. 9. — ISSN 2072-0297. Архивировано 3 февраля 2021 года.
- ↑ Рудакова И.П, Авакумов В.М. Цианокобаламин // Большая Медицинская Энциклопедия / под ред. Б.В. Петровского. — 3-е изд. — Т. 27. Архивная копия от 5 августа 2020 на Wayback Machine
- ↑ 1 2 Коневалова Н.Ю. Биохимия / под ред. Н.Ю. Коневаловой. — 4-е изд. — Витебск: ВГМУ, 2017. — С. 363—366. — 690 с. Архивная копия от 19 марта 2022 на Wayback Machine
- ↑ Хапалюк А.В. ВИТАМИН В12: БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ, ПАТОГЕНЕТИЧЕСКИЕ МЕХАНИЗМЫ И КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ВИТАМИННОЙ НЕДОСТАТОЧНОСТИ. — Минск: БГМУ, 2019. Архивная копия от 19 марта 2022 на Wayback Machine
- ↑ I Chanarin. Cobalamins and nitrous oxide: a review. // Journal of Clinical Pathology. — 1980-10. — Т. 33, вып. 10. — С. 909—916. — ISSN 0021-9746.
- ↑ 1 2 R. B. Layzer. Myeloneuropathy after prolonged exposure to nitrous oxide // The Lancet. — Elsevier, 1978-12-09. — Т. 2, вып. 8102. — С. 1227—1230. — ISSN 0140-6736. Архивировано 14 апреля 2019 года.
- ↑ Алексеев Г. А. Пернициозная анемия / Г. А. Алексеев, М. П. Хохлова, H. Г. Шумецкий // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1982. — Т. 19 : Перельман — Пневмопатия. — 536 с. : ил.
- ↑ Рудакова И. П. Цианокобаламин / И. П. Рудакова, В. М. Авакумов // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3-е изд. — М. : Советская энциклопедия, 1986. — Т. 27 : Хлоракон — Экономика здравоохранения. — 576 с. : ил.
- ↑ CerefolinNAC® Caplets. intetlab.com. Дата обращения: 23 ноября 2019. Архивировано 20 сентября 2018 года.
- ↑ 1 2 Мороз А. Витамины группы В. — В: Боли в спине: мифы и реальность : [арх. 20 апреля 2020] / Анна Мороз // Медфронт. — 2020. — 3 апреля.
- ↑ Azize Esra Gürsoy, Mehmet Kolukısa, Gülsen Babacan-Yıldız, Arif Çelebi. Subacute Combined Degeneration of the Spinal Cord due to Different Etiologies and Improvement of MRI Findings (англ.) // Case Reports in Neurological Medicine. — 2013. — 03 27 (vol. 2013). — ISSN 2090-6668. — doi:10.1155/2013/159649. — PMID 23607009. Архивировано 12 ноября 2020 года.
- ↑ Watanabe, 2007, Requirements of Vitamin B12 and Vitamin B12 Deficiency, p. 1270.
- ↑ 1 2 3 Wolfgang Herrmann, Rima Obeid. Causes and Early Diagnosis of Vitamin B12 Deficiency // Deutsches Ärzteblatt international. — 2008-10-03. — ISSN 1866-0452. — doi:10.3238/arztebl.2008.0680.
- ↑ NIH Intramural Sequencing Center Group, Jennifer L Sloan, Jennifer J Johnston, Irini Manoli, Randy J Chandler, Caitlin Krause, Nuria Carrillo-Carrasco, Suma D Chandrasekaran, Justin R Sysol, Kevin O’Brien, Natalie S Hauser, Julie C Sapp, Heidi M Dorward, Marjan Huizing, Bruce A Barshop, Susan A Berry, Philip M James, Neena L Champaigne, Pascale de Lonlay, Vassilli Valayannopoulos, Michael D Geschwind, Dimitar K Gavrilov, William L Nyhan, Leslie G Biesecker, Charles P Venditti. Exome sequencing identifies ACSF3 as a cause of combined malonic and methylmalonic aciduria (англ.) // Nature Genetics. — 2011-09. — Vol. 43, iss. 9. — P. 883–886. — ISSN 1546-1718 1061-4036, 1546-1718. — doi:10.1038/ng.908.
- ↑ Monique G. M. de Sain-van der Velden, Maria van der Ham, Judith J. Jans, Gepke Visser, Hubertus C. M. T. Prinsen, Nanda M. Verhoeven-Duif, Koen L. I. van Gassen, Peter M. van Hasselt. A New Approach for Fast Metabolic Diagnostics in CMAMMA // JIMD Reports, Volume 30 / Eva Morava, Matthias Baumgartner, Marc Patterson, Shamima Rahman, Johannes Zschocke, Verena Peters. — Berlin, Heidelberg: Springer Berlin Heidelberg, 2016. — Т. 30. — С. 15–22. — ISBN 978-3-662-53680-3, 978-3-662-53681-0. — doi:10.1007/8904_2016_531.
- ↑ 1 2 3 4 5 Food Sources of Vitamin B12 (англ.). www.dietitians.ca. Dietitians of Canada (2017). Дата обращения: 13 октября 2019. Архивировано из оригинала 13 октября 2019 года.
- ↑ 1 2 3 Rowley, Kendall, 2019, How do mammals acquire cobalamin?.
- ↑ Rowley, Kendall, 2019, Do humans compete with bacteria for cobalamin?.
- ↑ Rowley, Kendall, 2019, Fig 1. Cobalamin in the healthy human intestinal tract..
- ↑ 1 2 3 4 Watanabe, Bito, 2018, Vitamin B12 in animal-derived foods, p. 149.
- ↑ Watanabe, Bito, 2018, Vitamin B12 in animal-derived foods, Fish and shellfish, p. 151—153.
- ↑ Watanabe, 2007, Vitamin B12 in Animal Food : Fish, p. 1268—1269.
- ↑ Watanabe, Bito, 2018, Vitamin B12 in animal-derived foods : Meat, p. 149—150.
- ↑ 1 2 Watanabe, 2007, Abstract, p. 1266.
- ↑ 1 2 Watanabe, Bito, 2018, Conclusion, p. 155.
- ↑ 1 2 Watanabe, Bito, 2018, Vitamin B12 in plant-derived food, p. 153.
- ↑ Watanabe, 2007, Vitamin B12 in Plant Food : Vegetables, p. 1269.
- ↑ Watanabe, Bito, 2018, Vitamin B12 in plant-derived food : B12-enriched vegetables, p. 153.
- ↑ Watanabe, 2007, Vitamin B12 in Plant Food : Soybean, p. 1269—1270.
- ↑ Watanabe, Bito, 2018, Vitamin B12 in plant-derived food : Mushroom, p. 153—154.
- ↑ Watanabe, 2007, Vitamin B12 in Plant Food : Vitamin B12–Fortified Cereals, p. 1270.
- ↑ Healthdirect Australia. Foods high in vitamin B12 (англ.). www.healthdirect.gov.au (30 сентября 2019). Дата обращения: 12 октября 2019. Архивировано 12 октября 2019 года.
- ↑ What every vegan should know about vitamin B12 Архивная копия от 22 мая 2014 на Wayback Machine (англ.)
- ↑ 1 2 Watanabe, 2007, Requirements of Vitamin B12 and Vitamin B12 Deficiency, p. 1267.
- ↑ Office of Dietary Supplements – Vitamin B12. Fact Sheet for Health Professionals (англ.). National Institutes of Health. ods.od.nih.gov. Дата обращения: 18 июня 2019. Архивировано 30 ноября 2019 года.
- ↑ Theodore M. Brasky, Emily White, Chi-Ling Chen Long-Term, Supplemental, One-Carbon Metabolism–Related Vitamin B Use in Relation to Lung Cancer Risk in the Vitamins and Lifestyle (VITAL) Cohort Архивная копия от 7 февраля 2021 на Wayback Machine / Статья в «Journal of Clinical Oncology» Vol. 35, № 30, October 20, 2017, стр. 3440–3448 // American Society of Clinical Oncology, 2318 Mill Road, Suite 800, Alexandria, VA 22314
- ↑ Pseudovitamin B12 Is the Predominant Cobamide of an Algal Health Food, Spirulina Tablets. Дата обращения: 16 сентября 2010. Архивировано 8 мая 2016 года.
- ↑ 1 2 Is Vitamin B12 Available from Spirulina or Intestinal Synthesis? Дата обращения: 16 сентября 2010. Архивировано 21 сентября 2010 года.
Литература[править | править код]
- Fumio Watanabe, Tomohiro Bito. Vitamin B12 sources and microbial interaction : [англ.] // Experimental Biology and Medicine (Maywood, N.J.). — 2018. — Vol. 243, no. 2 (January). — P. 148–158. — ISSN 1535-3699. — doi:10.1177/1535370217746612. — PMID 29216732. — PMC 5788147.
- Fumio Watanabe. Vitamin B12 sources and bioavailability : [англ.] // Experimental Biology and Medicine (Maywood, N.J.). — 2007. — Vol. 232, no. 10 (November). — P. 1266–1274. — ISSN 1535-3702. — doi:10.3181/0703-MR-67. — PMID 17959839.
- Carol A. Rowley, Melissa M. Kendall. To B12 or not to B12: Five questions on the role of cobalamin in host-microbial interactions (англ.) // PLoS pathogens. — 2019. — January (vol. 15). — ISSN 1553-7374. — doi:10.1371/journal.ppat.1007479. — PMID 30605490. — PMC 6317780.
- ГОСТ Р 57201-2016 «Витамин В12 кормовой. Технические условия». // М.: Стандартинформ, 2016 г.
Ссылки[править | править код]

General skeletal formula of cobalamins |
|

Stick model of cyanocobalamin (R = CN) based on the crystal structure[1] |
|
| Clinical data | |
|---|---|
| Other names | Vitamin B12, vitamin B-12, cobalamin |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a605007 |
| License data |
|
| Routes of administration |
By mouth, sublingual, intravenous (IV), intramuscular (IM), intranasal |
| ATC code |
|
| Legal status | |
| Legal status |
|
| Pharmacokinetic data | |
| Bioavailability | Readily absorbed in distal half of the ileum. |
| Protein binding | Very high to specific transcobalamins plasma proteins. Binding of hydroxocobalamin is slightly higher than cyanocobalamin. |
| Metabolism | liver |
| Elimination half-life | Approximately 6 days (400 days in the liver). |
| Excretion | kidney |
| Identifiers | |
|
IUPAC name
|
|
| CAS Number |
|
| PubChem CID |
|
| DrugBank |
|
| ChemSpider |
|
| UNII |
|
| KEGG |
|
| ChEMBL |
|
| Chemical and physical data | |
| Formula | C63H88CoN14O14P |
| Molar mass | 1355.388 g·mol−1 |
| 3D model (JSmol) |
|
|
SMILES
|
|
|
InChI
|
Vitamin B12, also known as cobalamin, is a water-soluble vitamin involved in metabolism.[2] It is one of eight B vitamins. It is required by animals, which use it as a cofactor in DNA synthesis, and in both fatty acid and amino acid metabolism.[3] It is important in the normal functioning of the nervous system via its role in the synthesis of myelin, and in the circulatory system in the maturation of red blood cells in the bone marrow.[2][4] Plants do not need cobalamin and carry out the reactions with enzymes that are not dependent on it.[5]
Vitamin B12 is the most chemically complex of all vitamins,[6] and for humans, the only vitamin that must be sourced from animal-derived foods or from supplements.[2][7] Only some archaea and bacteria can synthesize vitamin B12.[8] Most people in developed countries get enough B12 from the consumption of meat or foods with animal sources.[2] Foods containing vitamin B12 include meat, clams, liver, fish, poultry, eggs, and dairy products.[2] Many breakfast cereals are fortified with the vitamin.[2] Supplements and medications are available to treat and prevent vitamin B12 deficiency.[2] They are taken by mouth, but for the treatment of deficiency may also be given as an intramuscular injection.[2][6]
The most common cause of vitamin B12 deficiency in developed countries is impaired absorption due to a loss of gastric intrinsic factor (IF) which must be bound to a food-source of B12 in order for absorption to occur.[9] A second major cause is age-related decline in stomach acid production (achlorhydria), because acid exposure frees protein-bound vitamin.[10] For the same reason, people on long-term antacid therapy, using proton-pump inhibitors, H2 blockers or other antacids are at increased risk.[11] The diets of vegetarians and vegans may not provide sufficient B12 unless a dietary supplement is consumed. A deficiency in vitamin B12 may be characterized by limb neuropathy or a blood disorder called pernicious anemia, a type of megaloblastic anemia, causing a feeling of tiredness and weakness, lightheadedness, headache, breathlessness, loss of appetite, abnormal sensations, changes in mobility, severe joint pain, muscle weakness, memory problems, decreased level of consciousness, brain fog, and many others.[12] If left untreated in infants, deficiency may lead to neurological damage and anemia.[2] Folate levels in the individual may affect the course of pathological changes and symptomatology of vitamin B12 deficiency.
Vitamin B12 was discovered as a result of pernicious anemia, an autoimmune disorder in which the blood has a lower than normal number of red blood cells, due to a deficiency in vitamin B12.[5][13] The ability to absorb the vitamin declines with age, especially in people over 60 years old.[14]
Definition[edit]
Vitamin B12 is a coordination complex of cobalt, which occupies the center of a corrin ligand and is further bound to a benzimidazole ligand and adenosyl group.[15] It is a deep red solid that dissolves in water to give red solutions.
A number of related species are known and these behave similarly, in particular all function as vitamins. This collection of compounds, of which vitamin B12 is one member, are often referred to as “cobalamins”. These chemical compounds have a similar molecular structure, each of which shows vitamin activity in a vitamin-deficient biological system, they are referred to as vitamers. The vitamin activity is as a coenzyme, meaning that its presence is required for some enzyme-catalyzed reactions.[10][16]
- adenosylcobalamin
- cyanocobalamin, the adenosyl ligand in vitamin B12 is replaced by cyanide.
- hydroxocobalamin, the adenosyl ligand in vitamin B12 is replaced by hydroxide.
- methylcobalamin, the adenosyl ligand in vitamin B12 is replaced by methyl.
Cyanocobalamin is a manufactured form of B12. Bacterial fermentation creates AdoB12 and MeB12, which are converted to cyanocobalamin by addition of potassium cyanide in the presence of sodium nitrite and heat. Once consumed, cyanocobalamin is converted to the biologically active AdoB12 and MeB12. The two bioactive forms of vitamin B
12 are methylcobalamin in cytosol and adenosylcobalamin in mitochondria.
Cyanocobalamin is the most common form used in dietary supplements and food fortification because cyanide stabilizes the molecule against degradation. Methylcobalamin is also offered as a dietary supplement.[10] There is no advantage to the use of adenosylcobalamin or methylcobalamin for treatment of vitamin B12 deficiency.[17][18][4]
Hydroxocobalamin can be injected intramuscularly to treat vitamin B12 deficiency. It can also be injected intravenously for the purpose of treating cyanide poisoning, as the hydroxyl group is displaced by cyanide, creating a non-toxic cyanocobalamin that is excreted in urine.
“Pseudovitamin B12” refers to compounds that are corrinoids with a structure similar to the vitamin but without vitamin activity.[19] Pseudovitamin B12 is the majority corrinoid in spirulina, an algal health food sometimes erroneously claimed as having this vitamin activity.[20]
Deficiency[edit]
Vitamin B12 deficiency can potentially cause severe and irreversible damage, especially to the brain and nervous system.[6][21] At levels only slightly lower than normal, a range of symptoms such as feeling tired, weak, feeling like one may faint, dizziness, breathlessness, headaches, mouth ulcers, upset stomach, decreased appetite, difficulty walking (staggering balance problems),[12][22] muscle weakness, depression, poor memory, poor reflexes, confusion, and pale skin, feeling abnormal sensations, among others, may be experienced, especially in people over age 60.[6][12][23] Vitamin B12 deficiency can also cause symptoms of mania and psychosis.[24][25] Among other problems, weakened immunity, reduced fertility and interruption of blood circulation in women may occur.[26]
The main type of vitamin B12 deficiency anemia is pernicious anemia.[27] It is characterized by a triad of symptoms:
- Anemia with bone marrow promegaloblastosis (megaloblastic anemia). This is due to the inhibition of DNA synthesis (specifically purines and thymidine).
- Gastrointestinal symptoms: alteration in bowel motility, such as mild diarrhea or constipation, and loss of bladder or bowel control.[28] These are thought to be due to defective DNA synthesis inhibiting replication in tissue sites with a high turnover of cells. This may also be due to the autoimmune attack on the parietal cells of the stomach in pernicious anemia. There is an association with gastric antral vascular ectasia (which can be referred to as watermelon stomach), and pernicious anemia.[29]
- Neurological symptoms: sensory or motor deficiencies (absent reflexes, diminished vibration or soft touch sensation) and subacute combined degeneration of the spinal cord.[30] Deficiency symptoms in children include developmental delay, regression, irritability, involuntary movements and hypotonia.[31]
Vitamin B12 deficiency is most commonly caused by malabsorption, but can also result from low intake, immune gastritis, low presence of binding proteins, or use of certain medications.[6] Vegans—people who choose to not consume any animal-sourced foods—are at risk because plant-sourced foods do not contain the vitamin in sufficient amounts to prevent vitamin deficiency.[32] Vegetarians—people who consume animal byproducts such as dairy products and eggs, but not the flesh of any animal—are also at risk. Vitamin B12 deficiency has been observed in between 40% and 80% of the vegetarian population who do not also take a vitamin B12 supplement or consume vitamin-fortified food.[33] In Hong Kong and India, vitamin B12 deficiency has been found in roughly 80% of the vegan population. As with vegetarians, vegans can avoid this by consuming a dietary supplement or eating B12 fortified food such as cereal, plant-based milks, and nutritional yeast as a regular part of their diet.[34] The elderly are at increased risk because they tend to produce less stomach acid as they age, a condition known as achlorhydria, thereby increasing their probability of B12 deficiency due to reduced absorption.[2]
Pregnancy, lactation and early childhood[edit]
The U.S. Recommended Dietary Allowance (RDA) for pregnancy is 2.6 µg/day, for lactation 2.8 µg/day. Determination of these values was based on the RDA of 2.4 µg/day for non-pregnant women plus what will be transferred to the fetus during pregnancy and what will be delivered in breast milk.[10][35]: 972 However, looking at the same scientific evidence, the European Food Safety Authority (EFSA) sets adequate intake (AI) at 4.5 μg/day for pregnancy and 5.0 μg/day for lactation.[36] Low maternal vitamin B12, defined as serum concentration less than 148 pmol/L, increases the risk of miscarriage, preterm birth and newborn low birth weight.[37][35] During pregnancy the placenta concentrates B12, so that newborn infants have a higher serum concentration than their mothers.[10] As it is recently absorbed vitamin content that more effectively reaches the placenta, the vitamin consumed by the mother-to-be is more important than that contained in her liver tissue.[10][38] Women who consume little animal-sourced food, or who are vegetarian or vegan, are at higher risk of becoming vitamin depleted during pregnancy than those who consume more animal products. This depletion can lead to anemia, and also an increased risk that their breastfed infants become vitamin deficient.[38][35]
Low vitamin concentrations in human milk occur in families with low socioeconomic status or low consumption of animal products.[35]: 971, 973 Only a few countries, primarily in Africa, have mandatory food fortification programs for either wheat flour or maize flour; India has a voluntary fortification program.[39] What the nursing mother consumes is more important than her liver tissue content, as it is recently absorbed vitamin that more effectively reaches breast milk.[35]: 973 Breast milk B12 decreases over months of nursing in both well-nourished and vitamin-deficient mothers.[35]: 973–974 Exclusive or near-exclusive breastfeeding beyond six months is a strong indicator of low serum vitamin status in nursing infants. This is especially true when the vitamin status was poor during the pregnancy and if the early-introduced foods fed to the still breastfeeding infant are vegan.[35]: 974–975 Risk of deficiency persists if the post-weaning diet is low in animal products.[35]: 974–975 Signs of low vitamin levels in infants and young children can include anemia, poor physical growth and neurodevelopmental delays.[35]: 975 Children diagnosed with low serum B12 can be treated with intramuscular injections, then transitioned to an oral dietary supplement.[35]: 976
Gastric bypass surgery[edit]
Various methods of gastric bypass or gastric restriction surgery are used to treat morbid obesity. Roux-en-Y gastric bypass surgery (RYGB) but not sleeve gastric bypass surgery or gastric banding, increases the risk of vitamin B12 deficiency and requires preventive post-operative treatment with either injected or high-dose oral supplementation.[40][41][42] For post-operative oral supplementation, 1000 μg/day may be needed to prevent vitamin deficiency.[42]
Diagnosis[edit]
According to one review: “At present, no ‘gold standard’ test exists for the diagnosis of vitamin B12 deficiency and as a consequence the diagnosis requires consideration of both the clinical state of the patient and the results of investigations.”[43] The vitamin deficiency is typically suspected when a routine complete blood count shows anemia with an elevated mean corpuscular volume (MCV). In addition, on the peripheral blood smear, macrocytes and hypersegmented polymorphonuclear leukocytes may be seen. Diagnosis is supported based on vitamin B12 blood levels below 150–180 pmol/L (200–250 pg/mL) in adults. However, serum values can be maintained while tissue B12 stores are becoming depleted. Therefore, serum B12 values above the cut-off point of deficiency do not necessarily confirm adequate B12 status.[2] For this reason, elevated serum homocysteine over 15 micromol/L and methylmalonic acid (MMA) over 0.271 micromol/L are considered better indicators of B12 deficiency, rather than relying only on the concentration of B12 in blood.[2] However, elevated MMA is not conclusive, as it is seen in people with B12 deficiency, but also in elderly people who have renal insufficiency,[25] and elevated homocysteine is not conclusive, as it is also seen in people with folate deficiency.[44] In addition, elevated methylmalonic acid levels may also be related to metabolic disorders such as methylmalonic acidemia.[45] If nervous system damage is present and blood testing is inconclusive, a lumbar puncture may be carried out to measure cerebrospinal fluid B12 levels.[46]
Medical uses[edit]
A vitamin B12 solution (hydroxocobalamin) in a multi-dose bottle, with a single dose drawn up into a syringe for injection. Preparations are usually bright red.
Repletion of deficiency[edit]
Severe vitamin B12 deficiency is corrected with frequent intramuscular injections of large doses of the vitamin, followed by maintenance doses of injections or oral dosing at longer intervals. In the UK, standard initial therapy consists of intramuscular injections of 1000 μg of hydroxocobalamin three times a week for two weeks or until neurological symptoms improve, followed by 1000 μg every two or three months.[47] Injection side effects include skin rash, itching, chills, fever, hot flushes, nausea and dizziness.[47]
Cyanide poisoning[edit]
For cyanide poisoning, a large amount of hydroxocobalamin may be given intravenously and sometimes in combination with sodium thiosulfate.[48][49] The mechanism of action is straightforward: the hydroxycobalamin hydroxide ligand is displaced by the toxic cyanide ion, and the resulting non-toxic cyanocobalamin is excreted in urine.[50]
Dietary recommendations[edit]
Most people in the United States and the United Kingdom consume sufficient vitamin B12.[2][9] However, proportions of people with low or marginal levels of vitamin B12 reach up to 40% in the Western world.[2] Grain-based foods can be fortified by having the vitamin added to them. Vitamin B12 supplements are available as single or multivitamin tablets. Pharmaceutical preparations of vitamin B12 may be given by intramuscular injection.[6][51] Since there are few non-animal sources of the vitamin, vegans are advised to consume a dietary supplement or fortified foods for B12 intake, or risk serious health consequences.[6] Children in some regions of developing countries are at particular risk due to increased requirements during growth coupled with diets low in animal-sourced foods.
The US National Academy of Medicine updated estimated average requirements (EARs) and recommended dietary allowances (RDAs) for vitamin B12 in 1998.[6] The EAR for vitamin B12 for women and men ages 14 and up is 2.0 μg/day; the RDA is 2.4 μg/day. RDA is higher than EAR so as to identify amounts that will cover people with higher than average requirements. RDA for pregnancy equals 2.6 μg/day. RDA for lactation equals 2.8 μg/day. For infants up to 12 months the adequate intake (AI) is 0.4–0.5 μg/day. (AIs are established when there is insufficient information to determine EARs and RDAs.) For children ages 1–13 years the RDA increases with age from 0.9 to 1.8 μg/day. Because 10 to 30 percent of older people may be unable to effectively absorb vitamin B12 naturally occurring in foods, it is advisable for those older than 50 years to meet their RDA mainly by consuming foods fortified with vitamin B12 or a supplement containing vitamin B12. As for safety, tolerable upper intake levels (known as ULs) are set for vitamins and minerals when evidence is sufficient. In the case of vitamin B12 there is no UL, as there is no human data for adverse effects from high doses. Collectively the EARs, RDAs, AIs and ULs are referred to as dietary reference intakes (DRIs).[10]
The European Food Safety Authority (EFSA) refers to the collective set of information as “dietary reference values”, with population reference intake (PRI) instead of RDA, and average requirement instead of EAR. AI and UL are defined by EFSA the same as in the United States. For women and men over age 18 the adequate intake (AI) is set at 4.0 μg/day. AI for pregnancy is 4.5 μg/day, for lactation 5.0 μg/day. For children aged 1–17 years the AIs increase with age from 1.5 to 3.5 μg/day. These AIs are higher than the U.S. RDAs.[36] The EFSA also reviewed the safety question and reached the same conclusion as in the United States—that there was not sufficient evidence to set a UL for vitamin B12.[52]
The Japan National Institute of Health and Nutrition set the RDA for people ages 12 and older at 2.4 μg/day.[53] The World Health Organization also uses 2.4 μg/day as the adult recommended nutrient intake for this vitamin.[54]
For U.S. food and dietary supplement labeling purposes the amount in a serving is expressed as a “percent of daily value” (%DV). For vitamin B12 labeling purposes 100% of the daily value was 6.0 μg, but on May 27, 2016, it was revised downward to 2.4 μg.[55][56] Compliance with the updated labeling regulations was required by 1 January 2020 for manufacturers with US$10 million or more in annual food sales, and by 1 January 2021 for manufacturers with lower volume food sales.[57][58] A table of the old and new adult daily values is provided at Reference Daily Intake.
Sources[edit]
Bacteria and archaea[edit]
Vitamin B12 is produced in nature by certain bacteria, and archaea.[59][60][61] It is synthesized by some bacteria in the gut microbiota in humans and other animals, but it has long been thought that humans cannot absorb this as it is made in the colon, downstream from the small intestine, where the absorption of most nutrients occurs.[62] Ruminants, such as cows and sheep, are foregut fermenters, meaning that plant food undergoes microbial fermentation in the rumen before entering the true stomach (abomasum), and thus they are absorbing vitamin B12 produced by bacteria.[62][63] Other mammalian species (examples: rabbits, pikas, beaver, guinea pigs) consume high-fibre plants which pass through the intestinal system and undergo bacterial fermentation in the cecum and large intestine. The first-passage of feces produced by this hindgut fermentation, called “cecotropes”, are re-ingested, a practice referred to as cecotrophy or coprophagy. Re-ingestion allows for absorption of nutrients made available by bacterial digestion, and also of vitamins and other nutrients synthesized by the gut bacteria, including vitamin B12.[63] Non-ruminant, non-hindgut herbivores may have an enlarged forestomach and/or small intestine to provide a place for bacterial fermentation and B-vitamin production, including B12.[63] For gut bacteria to produce vitamin B12 the animal must consume sufficient amounts of cobalt.[64] Soil that is deficient in cobalt may result in B12 deficiency, and B12 injections or cobalt supplementation may be required for livestock.[65]
Animal-derived foods[edit]
Animals store vitamin B12 from their diets in their livers and muscles and some pass the vitamin into their eggs and milk. Meat, liver, eggs and milk are therefore sources of the vitamin for other animals, including humans.[51][2][66] For humans, the bioavailability from eggs is less than 9%, compared to 40% to 60% from fish, fowl and meat.[67] Insects are a source of B12 for animals (including other insects and humans).[66][68] Animal-derived food sources with a high concentration of vitamin B12 include liver and other organ meats from lamb, veal, beef, and turkey; also shellfish and crab meat.[6][51][69]
Plants and algae[edit]
Natural plant and algae sources of vitamin B12 include fermented plant foods such as tempeh[70][71][72] and seaweed-derived foods such as nori and laver.[73][74][75] Other types of algae are rich in B12, with some species, such as Porphyra yezoensis,[73] containing as much cobalamin as liver.[76] Methylcobalamin has been identified in Chlorella vulgaris.[77] Since only bacteria and some archea possess the genes and enzymes necessary to synthesize vitamin B12, plant and algae sources all obtain the vitamin secondarily from symbiosis with various species of bacteria,[5] or in the case of fermented plant foods, from bacterial fermentation.[70][71]
The Academy of Nutrition and Dietetics considers plant and algae sources “unreliable”, stating that vegans should turn to fortified foods and supplements instead.[32]
Fortified foods[edit]
Foods for which vitamin B12-fortified versions are available include breakfast cereals, plant-derived milk substitutes such as soy milk and oat milk, energy bars, and nutritional yeast.[69] The fortification ingredient is cyanocobalamin. Microbial fermentation yields adenosylcobalamin, which is then converted to cyanocobalamin by addition of potassium cyanide or thiocyanate in the presence of sodium nitrite and heat.[78]
As of 2019, nineteen countries require food fortification of wheat flour, maize flour or rice with vitamin B12. Most of these are in southeast Africa or Central America.[39]
Vegan advocacy organizations, among others, recommend that every vegan consume B12 from either fortified foods or supplements.[6][34][79][80]
Supplements[edit]
A blister pack of 500 µg methylcobalamin tablets
Vitamin B12 is included in multivitamin pills; in some countries grain-based foods such as bread and pasta are fortified with B12. In the US, non-prescription products can be purchased providing up to 5,000 µg each, and it is a common ingredient in energy drinks and energy shots, usually at many times the recommended dietary allowance of B12. The vitamin can also be a prescription product via injection or other means.[2]
Sublingual methylcobalamin, which contains no cyanide, is available in 5 mg tablets. The metabolic fate and biological distribution of methylcobalamin are expected to be similar to that of other sources of vitamin B12 in the diet.[81] The amount of cyanide in cyanocobalamin is generally not a concern, even in the 1,000 µg dose, since the amount of cyanide there (20 µg in a 1,000 µg cyanocobalamin tablet) is less than the daily consumption of cyanide from food, and therefore cyanocobalamin is not considered a health risk.[81]
Intramuscular or intravenous injection[edit]
Injection of hydroxycobalamin is often used if digestive absorption is impaired,[2] but this course of action may not be necessary with high-dose oral supplements (such as 0.5–1.0 mg or more),[82][83] because with large quantities of the vitamin taken orally, even the 1% to 5% of free crystalline B12 that is absorbed along the entire intestine by passive diffusion may be sufficient to provide a necessary amount.[84]
A person with cobalamin C disease (which results in combined methylmalonic aciduria and homocystinuria) may require treatment with intravenous or intramuscular hydroxocobalamin or transdermal B12, because oral cyanocobalamin is inadequate in the treatment of cobalamin C disease.[85]
Nanotechnologies used in vitamin B12 supplementation[edit]
Conventional administration does not ensure specific distribution and controlled release of vitamin B12. Moreover, therapeutic protocols involving injection require health care people and commuting of patients to the hospital thus increasing the cost of the treatment and impairing the lifestyle of patients. Targeted delivery of vitamin B12 is a major focus of modern prescriptions. For example, conveying the vitamin to the bone marrow and nerve cells would help myelin recovery. Currently, several nanocarriers strategies are being developed for improving vitamin B12 delivery with the aim to simplify administration, reduce costs, improve pharmacokinetics, and ameliorate the quality of patients’ lives.[86]
Pseudovitamin-B12[edit]
Pseudovitamin-B12 refers to B12-like analogues that are biologically inactive in humans.[19] Most cyanobacteria, including Spirulina, and some algae, such as Porphyra tenera (used to make a dried seaweed food called nori in Japan), have been found to contain mostly pseudovitamin-B12 instead of biologically active B12.[20][87] These pseudo-vitamin compounds can be found in some types of shellfish,[19] in edible insects,[88] and at times as metabolic breakdown products of cyanocobalamin added to dietary supplements and fortified foods.[89]
Pseudovitamin-B12 can show up as biologically active vitamin B12 when a microbiological assay with Lactobacillus delbrueckii subsp. lactis is used, as the bacteria can utilize the pseudovitamin despite it being unavailable to humans. To get a reliable reading of B12 content, more advanced techniques are available. One such technique involves pre-separation by silica gel and then assessment with B12-dependent E. coli bacteria.[19]
A related concept is antivitamin B12, compounds (often synthetic B12 analogues) that not only have no vitamin action, but also actively interfere with the activity of true vitamin B12. The design of these compounds mainly involved replacement of the metal ion. These compounds have the potential to be used for analyzing B12 utilization pathways or even attacking B12-dependent pathogens.[90]
Drug interactions[edit]
H2-receptor antagonists and proton-pump inhibitors[edit]
Gastric acid is needed to release vitamin B12 from protein for absorption. Reduced secretion of gastric acid and pepsin, from the use of H2 blocker or proton-pump inhibitor (PPI) drugs, can reduce absorption of protein-bound (dietary) vitamin B12, although not of supplemental vitamin B12. H2-receptor antagonist examples include cimetidine, famotidine, nizatidine, and ranitidine. PPIs examples include omeprazole, lansoprazole, rabeprazole, pantoprazole, and esomeprazole. Clinically significant vitamin B12 deficiency and megaloblastic anemia are unlikely, unless these drug therapies are prolonged for two or more years, or if in addition the person’s dietary intake is below recommended levels. Symptomatic vitamin deficiency is more likely if the person is rendered achlorhydric (a complete absence of gastric acid secretion), which occurs more frequently with proton pump inhibitors than H2 blockers.[91]
Metformin[edit]
Reduced serum levels of vitamin B12 occur in up to 30% of people taking long-term anti-diabetic metformin.[92][93] Deficiency does not develop if dietary intake of vitamin B12 is adequate or prophylactic B12 supplementation is given. If the deficiency is detected, metformin can be continued while the deficiency is corrected with B12 supplements.[94]
Other drugs[edit]
Certain medications can decrease the absorption of orally consumed vitamin B12, including: colchicine, extended-release potassium products, and antibiotics such as gentamicin, neomycin and tobramycin.[95] Anti-seizure medications phenobarbital, pregabalin, primidone and topiramate are associated with lower than normal serum vitamin concentration. However, serum levels were higher in people prescribed valproate.[96] In addition, certain drugs may interfere with laboratory tests for the vitamin, such as amoxicillin, erythromycin, methotrexate and pyrimethamine.[95]
Chemistry[edit]
Methylcobalamin (shown) is a form of vitamin B12. Physically it resembles the other forms of vitamin B12, occurring as dark red crystals that freely form cherry-colored transparent solutions in water.
Vitamin B12 is the most chemically complex of all the vitamins.[6] The structure of B12 is based on a corrin ring, which is similar to the porphyrin ring found in heme. The central metal ion is cobalt. As isolated as an air-stable solid and available commercially, cobalt in vitamin B12 (cyanocobalamin and other vitamers) is present in its +3 oxidation state. Biochemically, the cobalt center can take part in both two-electron and one-electron reductive processes to access the “reduced” (B12r, +2 oxidation state) and “super-reduced” (B12s, +1 oxidation state) forms. The ability to shuttle between the +1, +2, and +3 oxidation states is responsible for the versatile chemistry of vitamin B12, allowing it to serve as a donor of deoxyadenosyl radical (radical alkyl source) and as a methyl cation equivalent (electrophilic alkyl source).[97] Four of the six coordination sites are provided by the corrin ring, and a fifth by a dimethylbenzimidazole group. The sixth coordination site, the reactive center, is variable, being a cyano group (–CN), a hydroxyl group (–OH), a methyl group (–CH3) or a 5′-deoxyadenosyl group. Historically, the covalent carbon–cobalt bond is one of the first examples of carbon–metal bonds to be discovered in biology. The hydrogenases and, by necessity, enzymes associated with cobalt utilization, involve metal–carbon bonds.[98] Animals have the ability to convert cyanocobalamin and hydroxocobalamin to the bioactive forms adenosylcobalamin and methylcobalamin by means of enzymatically replacing the cyano or hydroxyl groups.
The structures of the four most common vitamers of cobalamin, together with some synonyms. The structure of the 5′-deoxyadenosyl group, which forms the R group of adenosylcobalamin is also shown.
Methods for the analysis of vitamin B12 in food[edit]
Several methods have been used to determine the vitamin B12 content in foods including microbiological assays, chemiluminescence assays, polarographic, spectrophotometric and high-performance liquid chromatography processes.[99] The microbiological assay has been the most commonly used assay technique for foods, utilizing certain vitamin B12-requiring microorganisms, such as Lactobacillus delbrueckii subsp. lactis ATCC7830.[67] However, it is no longer the reference method due to the high measurement uncertainty of vitamin B12.[100] Furthermore, this assay requires overnight incubation and may give false results if any inactive vitamin B12 analogues are present in the foods.[101] Currently, radioisotope dilution assay (RIDA) with labelled vitamin B12 and hog IF (pigs) have been used to determine vitamin B12 content in food.[67] Previous reports have suggested that the RIDA method is able to detect higher concentrations of vitamin B12 in foods compared to the microbiological assay method.[67][99]
Biochemistry[edit]
Coenzyme function[edit]
Vitamin B12 functions as a coenzyme, meaning that its presence is required in some enzyme-catalyzed reactions.[10][16] Listed here are the three classes of enzymes that sometimes require B12 to function (in animals):
- Isomerases
- Rearrangements in which a hydrogen atom is directly transferred between two adjacent atoms with concomitant exchange of the second substituent, X, which may be a carbon atom with substituents, an oxygen atom of an alcohol, or an amine. These use the adoB12 (adenosylcobalamin) form of the vitamin.[102]
- Methyltransferases
- Methyl (–CH3) group transfers between two molecules. These use the MeB12 (methylcobalamin) form of the vitamin.[103]
- Dehalogenases
- Some species of anaerobic bacteria synthesize B12-dependent dehalogenases, which have potential commercial applications for degrading chlorinated pollutants. The microorganisms may either be capable of de novo corrinoid biosynthesis or are dependent on exogenous vitamin B12.[104][105]
In humans, two major coenzyme B12-dependent enzyme families corresponding to the first two reaction types, are known. These are typified by the following two enzymes:
Simplified schematic diagram of the folate methionine cycle. Methionine synthase transfers the methyl group to the vitamin and then transfers the methyl group to homocysteine, converting that to methionine.
Methylmalonyl coenzyme A mutase (MUT) is an isomerase enzyme which uses the AdoB12 form and reaction type 1 to convert L-methylmalonyl-CoA to succinyl-CoA, an important step in the catabolic breakdown of some amino acids into succinyl-CoA, which then enters energy production via the citric acid cycle.[102] This functionality is lost in vitamin B12 deficiency, and can be measured clinically as an increased serum methylmalonic acid (MMA) concentration. The MUT function is necessary for proper myelin synthesis.[4] Based on animal research, it is thought that the increased methylmalonyl-CoA hydrolyzes to form methylmalonate (methylmalonic acid), a neurotoxic dicarboxylic acid, causing neurological deterioration.[106]
Methionine synthase, coded by MTR gene, is a methyltransferase enzyme which uses the MeB12 and reaction type 2 to transfer a methyl group from 5-methyltetrahydrofolate to homocysteine, thereby generating tetrahydrofolate (THF) and methionine.[103] This functionality is lost in vitamin B12 deficiency, resulting in an increased homocysteine level and the trapping of folate as 5-methyl-tetrahydrofolate, from which THF (the active form of folate) cannot be recovered. THF plays an important role in DNA synthesis so reduced availability of THF results in ineffective production of cells with rapid turnover, in particular red blood cells, and also intestinal wall cells which are responsible for absorption. THF may be regenerated via MTR or may be obtained from fresh folate in the diet. Thus all of the DNA synthetic effects of B12 deficiency, including the megaloblastic anemia of pernicious anemia, resolve if sufficient dietary folate is present. Thus the best-known “function” of B12 (that which is involved with DNA synthesis, cell-division, and anemia) is actually a facultative function which is mediated by B12-conservation of an active form of folate which is needed for efficient DNA production.[103] Other cobalamin-requiring methyltransferase enzymes are also known in bacteria, such as Me-H4-MPT, coenzyme M methyltransferase.[107]
Physiology[edit]
Absorption[edit]
Food B12 is absorbed by two processes. The first is a vitamin B12-specific intestinal mechanism using intrinsic factor through which 1–2 micrograms can be absorbed every few hours, by which most food consumption of the vitamin is absorbed. The second is a passive diffusion process.[10] The human physiology of active vitamin B12 absorption from food is complex. Protein-bound vitamin B12 must be released from the proteins by the action of digestive proteases in both the stomach and small intestine. Gastric acid releases the vitamin from food particles; therefore antacid and acid-blocking medications (especially proton-pump inhibitors) may inhibit absorption of B12. After B12 has been freed from proteins in food by pepsin in the stomach, R-protein (also known as haptocorrin and transcobalamin-1), a B12 binding protein that is produced in the salivary glands, binds to B12. This protects the vitamin from degradation in the acidic environment of the stomach.[108] This pattern of B12 transfer to a special binding protein secreted in a previous digestive step, is repeated once more before absorption. The next binding protein for B12 is intrinsic factor (IF), a protein synthesized by gastric parietal cells that is secreted in response to histamine, gastrin and pentagastrin, as well as the presence of food. In the duodenum, proteases digest R-proteins and release their bound B12, which then binds to IF, to form a complex (IF/B12). B12 must be attached to IF for it to be efficiently absorbed, as receptors on the enterocytes in the terminal ileum of the small bowel only recognize the B12-IF complex; in addition, intrinsic factor protects the vitamin from catabolism by intestinal bacteria.[10]
Absorption of food vitamin B12 thus requires an intact and functioning stomach, exocrine pancreas, intrinsic factor, and small bowel.[10] Problems with any one of these organs makes a vitamin B12 deficiency possible. Individuals who lack intrinsic factor have a decreased ability to absorb B12. In pernicious anemia, there is a lack of IF due to autoimmune atrophic gastritis, in which antibodies form against parietal cells. Antibodies may alternately form against and bind to IF, inhibiting it from carrying out its B12 protective function. Due to the complexity of B12 absorption, geriatric patients, many of whom are hypoacidic due to reduced parietal cell function, have an increased risk of B12 deficiency.[109] This results in 80–100% excretion of oral doses in the feces versus 30–60% excretion in feces as seen in individuals with adequate IF.[109]
Once the IF/B12 complex is recognized by specialized ileal receptors, it is transported into the portal circulation. The vitamin is then transferred to transcobalamin II (TC-II/B12), which serves as the plasma transporter. Hereditary defects in production of the transcobalamins and their receptors may produce functional deficiencies in B12 and infantile megaloblastic anemia, and abnormal B12 related biochemistry, even in some cases with normal blood B12 levels. For the vitamin to serve inside cells, the TC-II/B12 complex must bind to a cell receptor, and be endocytosed. The transcobalamin II is degraded within a lysosome, and free B12 is finally released into the cytoplasm, where it may be transformed into the proper coenzyme, by certain cellular enzymes (see above).[10][110]
Investigations into the intestinal absorption of B12 point out that the upper limit of absorption per single oral dose, under normal conditions, is about 1.5 µg. The passive diffusion process of B12 absorption—normally a very small portion of total absorption of the vitamin from food consumption[10]—may exceed the R-protein and IF mediated absorption when oral doses of B12 are very large (a thousand or more µg per dose) as commonly happens in dedicated-pill oral B12 supplementation. This allows pernicious anemia and certain other defects in B12 absorption to be treated with oral megadoses of B12, even without any correction of the underlying absorption defects.[111] See the section on supplements above.
Storage and excretion[edit]
How fast B12 levels change depends on the balance between how much B12 is obtained from the diet, how much is secreted and how much is absorbed. The total amount of vitamin B12 stored in the body is about 2–5 mg in adults. Around 50% of this is stored in the liver. Approximately 0.1% of this is lost per day by secretions into the gut, as not all these secretions are reabsorbed. Bile is the main form of B12 excretion; most of the B12 secreted in the bile is recycled via enterohepatic circulation. Excess B12 beyond the blood’s binding capacity is typically excreted in urine. Owing to the extremely efficient enterohepatic circulation of B12, the liver can store 3 to 5 years’ worth of vitamin B12; therefore, nutritional deficiency of this vitamin is rare in adults in the absence of malabsorption disorders.[10] In the absence of enterohepatic reabsorption, only months to a year of vitamin B12 are stored.[112]
Synthesis[edit]
Biosynthesis[edit]
Vitamin B12 is derived from a tetrapyrrolic structural framework created by the enzymes deaminase and cosynthetase which transform aminolevulinic acid via porphobilinogen and hydroxymethylbilane to uroporphyrinogen III. The latter is the first macrocyclic intermediate common to heme, chlorophyll, siroheme and B12 itself.[113][114] Later steps, especially the incorporation of the additional methyl groups of its structure, were investigated using 13C methyl-labelled S-adenosyl methionine. It was not until a genetically engineered strain of Pseudomonas denitrificans was used, in which eight of the genes involved in the biosynthesis of the vitamin had been overexpressed, that the complete sequence of methylation and other steps could be determined, thus fully establishing all the intermediates in the pathway.[115][116]
Species from the following genera and the following individual species are known to synthesize B12: Propionibacterium shermanii, Pseudomonas denitrificans, Streptomyces griseus, Acetobacterium, Aerobacter, Agrobacterium, Alcaligenes, Azotobacter, Bacillus, Clostridium, Corynebacterium, Flavobacterium, Lactobacillus, Micromonospora, Mycobacterium, Nocardia, Proteus,
Rhizobium, Salmonella, Serratia, Streptococcus and Xanthomonas.[117][118]
Industrial[edit]
Industrial production of B12 is achieved through fermentation of selected microorganisms.[119] Streptomyces griseus, a bacterium once thought to be a fungus, was the commercial source of vitamin B12 for many years.[120] The species Pseudomonas denitrificans and Propionibacterium freudenreichii subsp. shermanii are more commonly used today.[119] These are grown under special conditions to enhance yield. Rhone-Poulenc improved yield via genetic engineering P. denitrificans.[121] Propionibacterium, the other commonly used bacteria, produce no exotoxins or endotoxins and are generally recognized as safe (have been granted GRAS status) by the Food and Drug Administration of the United States.[122]
The total world production of vitamin B12 in 2008 was 35,000 kg (77,175 lb).[123]
Laboratory[edit]
The complete laboratory synthesis of B12 was achieved by Robert Burns Woodward[124] and Albert Eschenmoser in 1972.[125][126] The work required the effort of 91 postdoctoral fellows (mostly at Harvard) and 12 PhD students (at ETH Zurich) from 19 nations. The synthesis constitutes a formal total synthesis, since the research groups only prepared the known intermediate cobyric acid, whose chemical conversion to vitamin B12 was previously reported. This synthesis of vitamin B12 is of no practical consequence due to its length, taking 72 chemical steps and giving an overall chemical yield well under 0.01%.[127] Although there have been sporadic synthetic efforts since 1972,[126] the Eschenmoser–Woodward synthesis remains the only completed (formal) total synthesis.
History[edit]
Descriptions of deficiency effects[edit]
Between 1849 and 1887, Thomas Addison described a case of pernicious anemia, William Osler and William Gardner first described a case of neuropathy, Hayem described large red cells in the peripheral blood in this condition, which he called “giant blood corpuscles” (now called macrocytes), Paul Ehrlich identified megaloblasts in the bone marrow, and Ludwig Lichtheim described a case of myelopathy.[128]
Identification of liver as an anti-anemia food[edit]
During the 1920s, George Whipple discovered that ingesting large amounts of raw liver seemed to most rapidly cure the anemia of blood loss in dogs, and hypothesized that eating liver might treat pernicious anemia.[129] Edwin Cohn prepared a liver extract that was 50 to 100 times more potent in treating pernicious anemia than the natural liver products. William Castle demonstrated that gastric juice contained an “intrinsic factor” which when combined with meat ingestion resulted in absorption of the vitamin in this condition.[128] In 1934, George Whipple shared the 1934 Nobel Prize in Physiology or Medicine with William P. Murphy and George Minot for discovery of an effective treatment for pernicious anemia using liver concentrate, later found to contain a large amount of vitamin B12.[128][130]
Identification of the active compound[edit]
While working at the Bureau of Dairy Industry, U.S. Department of Agriculture, Mary Shaw Shorb was assigned work on the bacterial strain Lactobacillus lactis Dorner (LLD), which was used to make yogurt and other cultured dairy products. The culture medium for LLD required liver extract. Shorb knew that the same liver extract was used to treat pernicious anemia (her father-in-law had died from the disease), and concluded that LLD could be developed as an assay method to identify the active compound. While at the University of Maryland she received a small grant from Merck, and in collaboration with Karl Folkers from that company, developed the LLD assay. This identified “LLD factor” as essential for the bacteria’s growth.[131] Shorb, Folker and Alexander R. Todd, at the University of Cambridge, used the LLD assay to extract the anti-pernicious anemia factor from liver extracts, purify it, and name it vitamin B12.[132] In 1955, Todd helped elucidate the structure of the vitamin, for which he was awarded the Nobel Prize in Chemistry in 1957. The complete chemical structure of the molecule was determined by Dorothy Hodgkin, based on crystallographic data in 1956, for which for that and other crystallographic analyses she was awarded the Nobel Prize in Chemistry in 1964.[133][134] Hodgkin went on to decipher the structure of insulin.[134]
Five people have been awarded Nobel Prizes for direct and indirect studies of vitamin B12: George Whipple, George Minot and William Murphy (1934), Alexander R. Todd (1957), and Dorothy Hodgkin (1964).[135]
Nobel laureates for discoveries relating to vitamin B12
Commercial production[edit]
Industrial production of vitamin B12 is achieved through fermentation of selected microorganisms.[119] As noted above, the completely synthetic laboratory synthesis of B12 was achieved by Robert Burns Woodward and Albert Eschenmoser in 1972, though this process has no commercial potential, requiring almost 70 steps and having a yield well below 0.01%.[127]
Society and culture[edit]
In the 1970s, John A. Myers, a physician residing in Baltimore, developed a program of injecting vitamins and minerals intravenously for various medical conditions. The formula included 1000 µg of cyanocobalamin. This came to be known as the Myers’ cocktail. After his death in 1984, other physicians and naturopaths took up prescribing “intravenous micro-nutrient therapy” with unsubstantiated health claims for treating fatigue, low energy, stress, anxiety, migraine, depression, immunocompromised, promoting weight loss and more.[136] However, other than a report on case studies[136] there are no benefits confirmed in the scientific literature.[137] Healthcare practitioners at clinics and spas prescribe versions of these intravenous combination products, but also intramuscular injections of just vitamin B12. A Mayo Clinic review concluded that there is no solid evidence that vitamin B12 injections provide an energy boost or aid weight loss.[138]
There is evidence that for elderly people, physicians often repeatedly prescribe and administer cyanocobalamin injections inappropriately, evidenced by the majority of subjects in one large study either having had normal serum concentrations or had not been tested prior to the injections.[139]
See also[edit]
- Adenosylcobalamin
- Cobalamin biosynthesis
- Cyanocobalamin
- Hydroxocobalamin
- Methylcobalamin
- Vitamins
Further reading[edit]
- Gherasim C, Lofgren M, Banerjee R (May 2013). “Navigating the B(12) road: assimilation, delivery, and disorders of cobalamin”. J. Biol. Chem. 288 (19): 13186–13193. doi:10.1074/jbc.R113.458810. PMC 3650358. PMID 23539619.
References[edit]
- ^ Prieto T, Neuburger M, Spingler B, Zelder F (2016). “Inorganic Cyanide as Protecting Group in the Stereospecific Reconstitution of Vitamin B12 from an Artificial Green Secocorrinoid”. Org. Lett. 18 (20): 5292–5295. doi:10.1021/acs.orglett.6b02611. PMID 27726382.
- ^ a b c d e f g h i j k l m n o p q Office of Dietary Supplements (6 April 2021). “Vitamin B12: Fact Sheet for Health Professionals”. Bethesda, Maryland: US National Institutes of Health. Archived from the original on 2021-10-08. Retrieved 24 December 2021.
- ^ Yamada K (2013). “Cobalt: Its Role in Health and Disease”. In Sigel A, Sigel H, Sigel RK (eds.). Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. Vol. 13. Springer. pp. 295–320. doi:10.1007/978-94-007-7500-8_9. ISBN 978-94-007-7499-5. PMID 24470095.
- ^ a b c Calderón-Ospina CA, Nava-Mesa MO (January 2020). “B Vitamins in the nervous system: Current knowledge of the biochemical modes of action and synergies of thiamine, pyridoxine, and cobalamin”. CNS Neurosci Ther. 26 (1): 5–13. doi:10.1111/cns.13207. PMC 6930825. PMID 31490017.
- ^ a b c Smith AG (2019-09-21). “Plants need their vitamins too”. Current Opinion in Plant Biology. 10 (3): 266–275. doi:10.1016/j.pbi.2007.04.009. PMID 17434786.
- ^ a b c d e f g h i j k “Vitamin B12“. Micronutrient Information Center, Linus Pauling Institute, Oregon State University, Corvallis, OR. 4 June 2015. Archived from the original on 29 October 2019. Retrieved 5 April 2019.
- ^ Vincenti A, Bertuzzo L, Limitone A, D’Antona G, Cena H (June 2021). “Perspective: Practical Approach to Preventing Subclinical B12 Deficiency in Elderly Population”. Nutrients. 13 (6): 1913. doi:10.3390/nu13061913. PMC 8226782. PMID 34199569.
- ^ Watanabe F, Bito T (January 2018). “Vitamin B12 sources and microbial interaction”. Exp Biol Med (Maywood). 243 (2): 148–158. doi:10.1177/1535370217746612. PMC 5788147. PMID 29216732.
- ^ a b Stabler SP (2020). “Vitamin B12”. In BP Marriott, DF Birt, VA Stallings, AA Yates (eds.). Present Knowledge in Nutrition, Eleventh Edition. London: Academic Press (Elsevier). pp. 257–272. ISBN 978-0-323-66162-1.
US survey data from the NHANES What We Eat in America 2013e16 cohort reported the median vitamin B12 consumption for all adult men of 5.1 mcg and women of 3.5 mcg.95b Using the Estimated Average Requirement (EAR) for adults for Vitamin B12 of 2 mcg,93 less than 3% of men and 8% of women in the United States had inadequate diets using this comparator. However, 11% of girls 14e18 years had intakes less than their EAR of 2.0 mcg.
- ^ a b c d e f g h i j k l m n Institute of Medicine (1998). “Vitamin B12“. Dietary Reference Intakes for Thiamin, Riboflavin, Niacin, Vitamin B6, Folate, Vitamin B12, Pantothenic Acid, Biotin, and Choline. Washington, DC: The National Academies Press. pp. 306–356. ISBN 978-0-309-06554-2. Retrieved February 7, 2012.
- ^ “Acid-Reflux Drugs Tied to Lower Levels of Vitamin B-12”. WebMD. Archived from the original on 2018-07-23. Retrieved 2018-07-23.
- ^ a b c “Vitamin B12 Deficiency Anemia”. www.hopkinsmedicine.org. 8 August 2021. Retrieved 2022-02-16.
- ^ “Pernicious anemia: MedlinePlus Medical Encyclopedia”. medlineplus.gov. Retrieved 2022-01-06.
- ^ Baik HW, Russell RM (2021-11-18). “Vitamin B12 deficiency in the elderly”. Annual Review of Nutrition. 19: 357–377. doi:10.1146/annurev.nutr.19.1.357. PMID 10448529.
- ^ Butler P, Kräutler B (2006). “Biological Organometallic Chemistry of B12”. Bioorganometallic Chemistry. Topics in Organometallic Chemistry. Vol. 17. pp. 1–55. doi:10.1007/3418_004. ISBN 3-540-33047-X.
- ^ a b Banerjee R, Ragsdale SW (July 2003). “The many faces of vitamin B12: catalysis by cobalamin-dependent enzymes”. Annual Review of Biochemistry. 72: 209–247. doi:10.1146/annurev.biochem.72.121801.161828. PMID 14527323. S2CID 37393683.
- ^ Obeid R, Fedosov SN, Nexo E (July 2015). “Cobalamin coenzyme forms are not likely to be superior to cyano- and hydroxyl-cobalamin in prevention or treatment of cobalamin deficiency”. Molecular Nutrition & Food Research. 59 (7): 1364–1372. doi:10.1002/mnfr.201500019. PMC 4692085. PMID 25820384.
- ^ Paul C, Brady DM (February 2017). “Comparative Bioavailability and Utilization of Particular Forms of B12 Supplements With Potential to Mitigate B12-related Genetic Polymorphisms”. Integr Med (Encinitas). 16 (1): 42–49. PMC 5312744. PMID 28223907.
- ^ a b c d Watanabe F, Bito T (September 2018). “Determination of Cobalamin and Related Compounds in Foods”. J AOAC Int. 101 (5): 1308–1313. doi:10.5740/jaoacint.18-0045. PMID 29669618. S2CID 4978703.
- ^ a b Watanabe F, Katsura H, Takenaka S, Fujita T, Abe K, Tamura Y, Nakatsuka T, Nakano Y (November 1999). “Pseudovitamin B(12) is the predominant cobamide of an algal health food, spirulina tablets”. J. Agric. Food Chem. 47 (11): 4736–4741. doi:10.1021/jf990541b. PMID 10552882.
- ^ van der Put NM, van Straaten HW, Trijbels FJ, Blom HJ (April 2001). “Folate, homocysteine and neural tube defects: an overview”. Experimental Biology and Medicine. 226 (4): 243–270. doi:10.1177/153537020122600402. PMID 11368417. S2CID 29053617.
- ^ Skerrett PJ (February 2019). “Vitamin B12 deficiency can be sneaky, harmful”. Harvard Health Blog. Archived from the original on 29 October 2019. Retrieved 6 January 2020.
- ^ “Vitamin B12 or folate deficiency anaemia – Symptoms”. National Health Service, England. 23 May 2019. Archived from the original on 12 August 2017. Retrieved 6 January 2020.
- ^ Masalha R, Chudakov B, Muhamad M, Rudoy I, Volkov I, Wirguin I (September 2001). “Cobalamin-responsive psychosis as the sole manifestation of vitamin B12 deficiency”. The Israel Medical Association Journal. 3 (9): 701–703. PMID 11574992.
- ^ a b Lachner C, Steinle NI, Regenold WT (2012). “The neuropsychiatry of vitamin B12 deficiency in elderly patients”. J Neuropsychiatry Clin Neurosci. 24 (1): 5–15. doi:10.1176/appi.neuropsych.11020052. PMID 22450609. S2CID 20350330.
- ^ Bennett M (March 2001). “Vitamin B12 deficiency, infertility and recurrent fetal loss”. The Journal of Reproductive Medicine. 46 (3): 209–212. PMID 11304860.
- ^ “What Is Pernicious Anemia?”. NHLBI. April 1, 2011. Archived from the original on 14 March 2016. Retrieved 14 March 2016.
- ^ Briani C, Dalla Torre C, Citton V, Manara R, Pompanin S, Binotto G, Adami F (November 2013). “Cobalamin Deficiency: Clinical Picture and Radiological Findings”. Nutrients. 5 (11): 4521–4539. doi:10.3390/nu5114521. ISSN 2072-6643. PMC 3847746. PMID 24248213.
- ^ Amarapurka DN, Patel ND (September 2004). “Gastric Antral Vascular Ectasia (GAVE) Syndrome” (PDF). Journal of the Association of Physicians of India. 52: 757. Archived (PDF) from the original on 2016-03-04.
- ^ Greenburg M (2010). Handbook of Neurosurgery 7th Edition. New York: Thieme Publishers. pp. 1187–1188. ISBN 978-1-60406-326-4.
- ^ Lerner NB (2016). “Vitamin B12 Deficiency”. In Kliegman RM, Stanton B, St Geme J, Schor NF (eds.). Nelson Textbook of Pediatrics (20th ed.). pp. 2319–2326. ISBN 978-1-4557-7566-8.
- ^ a b Melina V, Craig W, Levin S (2016). “Position of the Academy of Nutrition and Dietetics: Vegetarian Diets”. J Acad Nutr Diet. 116 (12): 1970–1980. doi:10.1016/j.jand.2016.09.025. PMID 27886704.
Fermented foods (such as tempeh), nori, spirulina, chlorella algae, and unfortified nutritional yeast cannot be relied upon as adequate or practical sources of B-12.39,40 Vegans must regularly consume reliable sources—meaning B-12 fortified foods or B-12 containing supplements—or they could become deficient, as shown in case studies of vegan infants, children, and adults.
- ^ Pawlak R, Parrott SJ, Raj S, Cullum-Dugan D, Lucus D (February 2013). “How prevalent is vitamin B(12) deficiency among vegetarians?”. Nutrition Reviews. 71 (2): 110–117. doi:10.1111/nure.12001. PMID 23356638.
- ^ a b Woo KS, Kwok TC, Celermajer DS (August 2014). “Vegan diet, subnormal vitamin B-12 status and cardiovascular health”. Nutrients. 6 (8): 3259–3273. doi:10.3390/nu6083259. PMC 4145307. PMID 25195560.
- ^ a b c d e f g h i j Obeid R, Murphy M, Solé-Navais P, Yajnik C (November 2017). “Cobalamin Status from Pregnancy to Early Childhood: Lessons from Global Experience”. Adv Nutr. 8 (6): 971–979. doi:10.3945/an.117.015628. PMC 5683008. PMID 29141978.
- ^ a b “Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies” (PDF). 2017. Archived (PDF) from the original on 2020-01-07. Retrieved 2017-08-28.
- ^ Rogne T, Tielemans MJ, Chong MF, Yajnik CS, Krishnaveni GV, Poston L, et al. (February 2017). “Associations of Maternal Vitamin B12 Concentration in Pregnancy With the Risks of Preterm Birth and Low Birth Weight: A Systematic Review and Meta-Analysis of Individual Participant Data”. Am J Epidemiol. 185 (3): 212–223. doi:10.1093/aje/kww212. PMC 5390862. PMID 28108470.
- ^ a b Sebastiani G, Herranz Barbero A, Borrás-Novell C, Alsina Casanova M, Aldecoa-Bilbao V, Andreu-Fernández V, Pascual Tutusaus M, Ferrero Martínez S, Gómez Roig MD, García-Algar O (March 2019). “The Effects of Vegetarian and Vegan Diet during Pregnancy on the Health of Mothers and Offspring”. Nutrients. 11 (3): 557. doi:10.3390/nu11030557. PMC 6470702. PMID 30845641.
- ^ a b “Map: Count of Nutrients In Fortification Standards”. Global Fortification Data Exchange. Archived from the original on 11 April 2019. Retrieved 15 April 2020.
- ^ Weng TC, Chang CH, Dong YH, Chang YC, Chuang LM (July 2015). “Anaemia and related nutrient deficiencies after Roux-en-Y gastric bypass surgery: a systematic review and meta-analysis”. BMJ Open. 5 (7): e006964. doi:10.1136/bmjopen-2014-006964. PMC 4513480. PMID 26185175.
- ^ Majumder S, Soriano J, Louie Cruz A, Dasanu CA (2013). “Vitamin B12 deficiency in patients undergoing bariatric surgery: preventive strategies and key recommendations”. Surg Obes Relat Dis. 9 (6): 1013–1019. doi:10.1016/j.soard.2013.04.017. PMID 24091055.
- ^ a b Mahawar KK, Reid A, Graham Y, Callejas-Diaz L, Parmar C, Carr WR, Jennings N, Singhal R, Small PK (July 2018). “Oral Vitamin B12 Supplementation After Roux-en-Y Gastric Bypass: a Systematic Review”. Obes Surg. 28 (7): 1916–1923. doi:10.1007/s11695-017-3102-y. PMID 29318504. S2CID 35209784.
- ^ Shipton MJ, Thachil J (April 2015). “Vitamin B12 deficiency – A 21st century perspective”. Clin Med (Lond). 15 (2): 145–150. doi:10.7861/clinmedicine.15-2-145. PMC 4953733. PMID 25824066.
- ^ Moretti R, Caruso P (January 2019). “The Controversial Role of Homocysteine in Neurology: From Labs to Clinical Practice”. Int J Mol Sci. 20 (1): 231. doi:10.3390/ijms20010231. PMC 6337226. PMID 30626145.
- ^ “Methylmalonic acidemia”. Genetics Home Reference. US National Library of Medecine. October 2015. Retrieved 10 July 2022.
- ^ Devalia V (Aug 2006). “Diagnosing vitamin B-12 deficiency on the basis of serum B-12 assay”. BMJ. 333 (7564): 385–386. doi:10.1136/bmj.333.7564.385. PMC 1550477. PMID 16916826.
- ^ a b Devalia V, Hamilton MS, Molloy AM (August 2014). “Guidelines for the diagnosis and treatment of cobalamin and folate disorders”. Br. J. Haematol. 166 (4): 496–513. doi:10.1111/bjh.12959. PMID 24942828. S2CID 5772424.
- ^ Hall AH, Rumack BH (1987). “Hydroxycobalamin/sodium thiosulfate as a cyanide antidote”. The Journal of Emergency Medicine. 5 (2): 115–121. doi:10.1016/0736-4679(87)90074-6. PMID 3295013.
- ^ MacLennan L, Moiemen N (February 2015). “Management of cyanide toxicity in patients with burns”. Burns. 41 (1): 18–24. doi:10.1016/j.burns.2014.06.001. PMID 24994676.
- ^ Dart RC (2006). “Hydroxocobalamin for acute cyanide poisoning: new data from preclinical and clinical studies; new results from the prehospital emergency setting”. Clinical Toxicology. 44 (Suppl. 1): 1–3. doi:10.1080/15563650600811607. PMID 16990188.
- ^ a b c “Foods highest in Vitamin B12 (based on levels per 100-gram serving)”. Nutrition Data. Condé Nast, USDA National Nutrient Database, release SR-21. 2014. Archived from the original on November 16, 2019. Retrieved February 16, 2017.
- ^ “Tolerable Upper Intake Levels For Vitamins And Minerals” (PDF). European Food Safety Authority. 2006. Archived (PDF) from the original on 2019-10-15. Retrieved 2016-03-12.
- ^ “Dietary Reference Intakes for Japanese 2010: Water-Soluble Vitamins” Journal of Nutritional Science and Vitaminology 2013(59):S67–S82.
- ^ World Health Organization (2005). “Chapter 14: Vitamin B12”. Vitamin and Mineral Requirements in Human Nutrition (2nd ed.). Geneva: World Health Organization. pp. 279–287. hdl:10665/42716. ISBN 978-92-4-154612-6.
- ^ “Food Labeling: Revision of the Nutrition and Supplement Facts Labels” (PDF). Federal Register. May 27, 2016. p. 33982. Archived (PDF) from the original on August 8, 2016. Retrieved August 27, 2017.
- ^ “Daily Value Reference of the Dietary Supplement Label Database (DSLD)”. Dietary Supplement Label Database (DSLD). Archived from the original on 7 April 2020. Retrieved 16 May 2020.
- ^ “Changes to the Nutrition Facts Label”. U.S. Food and Drug Administration (FDA). 27 May 2016. Retrieved 16 May 2020.
This article incorporates text from this source, which is in the public domain.
- ^ “Industry Resources on the Changes to the Nutrition Facts Label”. U.S. Food and Drug Administration (FDA). 21 December 2018. Retrieved 16 May 2020.
This article incorporates text from this source, which is in the public domain.
- ^ Fang H, Kang J, Zhang D (January 2017). “Microbial production of vitamin B12: a review and future perspectives”. Microbial Cell Factories. 16 (1): 15. doi:10.1186/s12934-017-0631-y. PMC 5282855. PMID 28137297.
- ^ Moore SJ, Warren MJ (June 2012). “The anaerobic biosynthesis of vitamin B12”. Biochemical Society Transactions. 40 (3): 581–586. doi:10.1042/BST20120066. PMID 22616870.
- ^ Graham RM, Deery E, Warren MJ (2009). “18: Vitamin B12: Biosynthesis of the Corrin Ring”. In Warren MJ, Smith (eds.). Tetrapyrroles Birth, Life and Death. New York: Springer-Verlag. p. 286. doi:10.1007/978-0-387-78518-9_18. ISBN 978-0-387-78518-9.
- ^ a b Gille D, Schmid A (February 2015). “Vitamin B12 in meat and dairy products”. Nutrition Reviews. 73 (2): 106–115. doi:10.1093/nutrit/nuu011. PMID 26024497.
- ^ a b c Stevens CE, Hume ID (April 1998). “Contributions of microbes in vertebrate gastrointestinal tract to production and conservation of nutrients”. Physiol. Rev. 78 (2): 393–427. doi:10.1152/physrev.1998.78.2.393. PMID 9562034. S2CID 103191.
- ^ McDowell LR (2008). Vitamins in Animal and Human Nutrition (2nd ed.). Hoboken: John Wiley & Sons. pp. 525, 539. ISBN 978-0470376683. Archived from the original on 2017-09-08. Retrieved 2017-01-17.
- ^ Erickson, Anna (September 3, 2019). “Cobalt deficiency in sheep and cattle”. Department of Primary Industries and Regional Development. Government of Western Australia. Archived from the original on 2015-11-11. Retrieved 2020-04-18.
- ^ a b Rooke J (October 30, 2013). “Do carnivores need Vitamin B12 supplements?”. Baltimore Post Examiner. Archived from the original on January 16, 2017. Retrieved January 17, 2017.
- ^ a b c d Watanabe F (November 2007). “Vitamin B12 sources and bioavailability”. Experimental Biology and Medicine. 232 (10): 1266–1274. doi:10.3181/0703-MR-67. PMID 17959839. S2CID 14732788.
- ^ Dossey AT (February 1, 2013). “Why Insects Should Be in Your Diet”. The Scientist. Archived from the original on November 11, 2017. Retrieved April 18, 2020.
- ^ a b “Vitamin B-12 (µg)” (PDF). USDA National Nutrient Database for Standard Reference Release 28. 27 October 2015. Archived (PDF) from the original on 26 January 2017. Retrieved 6 January 2020.
- ^ a b Liem IT, Steinkraus KH, Cronk TC (December 1977). “Production of vitamin B-12 in tempeh, a fermented soybean food”. Applied and Environmental Microbiology. 34 (6): 773–776. Bibcode:1977ApEnM..34..773L. doi:10.1128/AEM.34.6.773-776.1977. PMC 242746. PMID 563702.
- ^ a b Keuth S, Bisping B (May 1994). “Vitamin B12 production by Citrobacter freundii or Klebsiella pneumoniae during tempeh fermentation and proof of enterotoxin absence by PCR”. Applied and Environmental Microbiology. 60 (5): 1495–1499. Bibcode:1994ApEnM..60.1495K. doi:10.1128/AEM.60.5.1495-1499.1994. PMC 201508. PMID 8017933.
- ^ Mo H, Kariluoto S, Piironen V, Zhu Y, Sanders MG, Vincken JP, et al. (December 2013). “Effect of soybean processing on content and bioaccessibility of folate, vitamin B12 and isoflavones in tofu and tempe”. Food Chemistry. 141 (3): 2418–2425. doi:10.1016/j.foodchem.2013.05.017. PMID 23870976.
- ^ a b Watanabe F, Yabuta Y, Bito T, Teng F (May 2014). “Vitamin B₁₂-containing plant food sources for vegetarians”. Nutrients. 6 (5): 1861–1873. doi:10.3390/nu6051861. PMC 4042564. PMID 24803097.
- ^ Kwak CS, Lee MS, Lee HJ, Whang JY, Park SC (June 2010). “Dietary source of vitamin B(12) intake and vitamin B(12) status in female elderly Koreans aged 85 and older living in rural area”. Nutrition Research and Practice. 4 (3): 229–234. doi:10.4162/nrp.2010.4.3.229. PMC 2895704. PMID 20607069.
- ^ Kwak CS, Lee MS, Oh SI, Park SC (2010). “Discovery of novel sources of vitamin b(12) in traditional korean foods from nutritional surveys of centenarians”. Current Gerontology and Geriatrics Research. 2010: 374897. doi:10.1155/2010/374897. PMC 3062981. PMID 21436999.
- ^ Croft MT, Lawrence AD, Raux-Deery E, Warren MJ, Smith AG (November 2005). “Algae acquire vitamin B12 through a symbiotic relationship with bacteria”. Nature. 438 (7064): 90–93. Bibcode:2005Natur.438…90C. doi:10.1038/nature04056. PMID 16267554. S2CID 4328049.
- ^ Kumudha A, Selvakumar S, Dilshad P, Vaidyanathan G, Thakur MS, Sarada R (March 2015). “Methylcobalamin – a form of vitamin B12 identified and characterised in Chlorella vulgaris”. Food Chemistry. 170: 316–320. doi:10.1016/j.foodchem.2014.08.035. PMID 25306351.
- ^ Martins JH, Barg H, Warren MJ, Jahn D (March 2002). “Microbial production of vitamin B12”. Appl Microbiol Biotechnol. 58 (3): 275–285. doi:10.1007/s00253-001-0902-7. PMID 11935176. S2CID 22232461.
- ^ Mangels R. “Vitamin B12 in the Vegan Diet”. Vegetarian Resource Group. Archived from the original on December 19, 2012. Retrieved January 17, 2008.
- ^ “Don’t Vegetarians Have Trouble Getting Enough Vitamin B12?”. Physicians Committee for Responsible Medicine. Archived from the original on October 8, 2011. Retrieved January 17, 2008.
- ^ a b European Food Safety Authority (September 25, 2008). “5′-deoxyadenosylcobalamin and methylcobalamin as sources for Vitamin B12 added as a nutritional substance in food supplements: Scientific opinion of the Scientific Panel on Food Additives and Nutrient Sources added to food”. EFSA Journal. 815 (10): 1–21. doi:10.2903/j.efsa.2008.815. “the metabolic fate and biological distribution of methylcobalamin and 5′-deoxyadenosylcobalamin are expected to be similar to that of other sources of vitamin B12 in the diet”.
- ^ Lane LA, Rojas-Fernandez C (July–August 2002). “Treatment of vitamin b(12)-deficiency anemia: oral versus parenteral therapy”. The Annals of Pharmacotherapy. 36 (7–8): 1268–1272. doi:10.1345/aph.1A122. PMID 12086562. S2CID 919401.
- ^ Butler CC, Vidal-Alaball J, Cannings-John R, McCaddon A, Hood K, Papaioannou A, Mcdowell I, Goringe A (June 2006). “Oral vitamin B12 versus intramuscular vitamin B12 for vitamin B12 deficiency: a systematic review of randomized controlled trials”. Family Practice. 23 (3): 279–285. doi:10.1093/fampra/cml008. PMID 16585128.
- ^ Arslan SA, Arslan I, Tirnaksiz F (March 2013). “Cobalamins and Methylcobalamin: Coenzyme of Vitamin B12”. FABAD J. Pharm. Sci. 38 (3): 151–157. S2CID 1929961.
- ^ Thauvin-Robinet C, Roze E, Couvreur G, Horellou MH, Sedel F, Grabli D, Bruneteau G, Tonneti C, Masurel-Paulet A, Perennou D, Moreau T, Giroud M, de Baulny HO, Giraudier S, Faivre L (June 2008). “The adolescent and adult form of cobalamin C disease: clinical and molecular spectrum”. Journal of Neurology, Neurosurgery, and Psychiatry. 79 (6): 725–728. doi:10.1136/jnnp.2007.133025. PMID 18245139. S2CID 23493993.
- ^ Fidaleo M, Tacconi S, Sbarigia C, Passeri D, Rossi M, Tata AM, Dini L (March 2021). “Current Nanocarrier Strategies Improve Vitamin B12 Pharmacokinetics, Ameliorate Patients’ Lives, and Reduce Costs”. Nanomaterials. 11 (3): 743. doi:10.3390/nano11030743. PMC 8001893. PMID 33809596.
- ^ Yamada K, Yamada Y, Fukuda M, Yamada S (November 1999). “Bioavailability of Dried Asakusanori (Porphyra tenera) as a Source of Cobalamin (Vitamin B12)”. International Journal for Vitamin and Nutrition Research. 69 (6): 412–418. doi:10.1024/0300-9831.69.6.412. PMID 10642899.
- ^ Schmidt A, Call LM, Macheiner L, Mayer HK (May 2019). “Determination of vitamin B12 in four edible insect species by immunoaffinity and ultra-high performance liquid chromatography”. Food Chemistry. 281: 124–129. doi:10.1016/j.foodchem.2018.12.039. PMID 30658738. S2CID 58651702.
- ^ Yamada K, Shimodaira M, Chida S, Yamada N, Matsushima N, Fukuda M, Yamada S (2008). “Degradation of vitamin B12 in dietary supplements”. International Journal for Vitamin and Nutrition Research. 78 (4–5): 195–203. doi:10.1024/0300-9831.78.45.195. PMID 19326342.
- ^ Kräutler B (December 2020). “Antivitamins B12 -Some Inaugural Milestones”. Chemistry. 26 (67): 15438–15445. doi:10.1002/chem.202003788. PMC 7756841. PMID 32956545.
- ^ DeVault KR, Talley NJ (September 2009). “Insights into the future of gastric acid suppression”. Nat Rev Gastroenterol Hepatol. 6 (9): 524–532. doi:10.1038/nrgastro.2009.125. PMID 19713987. S2CID 25413839.
- ^ Ahmed MA (2016). “Metformin and Vitamin B12 Deficiency: Where Do We Stand?”. Journal of Pharmacy & Pharmaceutical Sciences. 19 (3): 382–398. doi:10.18433/J3PK7P. PMID 27806244.
- ^ Gilligan MA (February 2002). “Metformin and vitamin B12 deficiency”. Archives of Internal Medicine. 162 (4): 484–485. doi:10.1001/archinte.162.4.484. PMID 11863489.
- ^ Copp S (1 December 2007). “What effect does metformin have on vitamin B12 levels?”. UK Medicines Information, NHS. Archived from the original on September 27, 2007.
- ^ a b “Vitamin B-12: Interactions”. WebMD. Retrieved 21 April 2020.
- ^ Linnebank M, Moskau S, Semmler A, Widman G, Stoffel-Wagner B, Weller M, Elger CE (February 2011). “Antiepileptic drugs interact with folate and vitamin B12 serum levels” (PDF). Ann. Neurol. 69 (2): 352–359. doi:10.1002/ana.22229. PMID 21246600. S2CID 7282489.
- ^ Giedyk M, Goliszewska K, Gryko D (June 2015). “Vitamin B12 catalysed reactions”. Chemical Society Reviews. 44 (11): 3391–3404. doi:10.1039/C5CS00165J. PMID 25945462.
- ^ Jaouen G, ed. (2006). Bioorganometallics: Biomolecules, Labeling, Medicine. Weinheim: Wiley-VCH. pp. 17–25. ISBN 978-3-527-30990-0.
- ^ a b Lawrance P (March 2015). “Vitamin B12: A review of analytical methods for use in food”. LGC Limited.
- ^ O’Leary F, Samman S (March 2010). “Vitamin B12 in Health and Disease”. Nutrients. 2 (3): 299–316. doi:10.3390/nu2030299. ISSN 2072-6643. PMC 3257642. PMID 22254022.
- ^ Obeid R, ed. (2017-07-12). Vitamin B12. CRC Press. doi:10.1201/9781315119540. ISBN 978-1-315-11954-0.
- ^ a b Takahashi-Iñiguez T, García-Hernandez E, Arreguín-Espinosa R, Flores ME (June 2012). “Role of vitamin B12 on methylmalonyl-CoA mutase activity”. J Zhejiang Univ Sci B. 13 (6): 423–437. doi:10.1631/jzus.B1100329. PMC 3370288. PMID 22661206.
- ^ a b c Froese DS, Fowler B, Baumgartner MR (July 2019). “Vitamin B12, folate, and the methionine remethylation cycle-biochemistry, pathways, and regulation”. Journal of Inherited Metabolic Disease. 42 (4): 673–685. doi:10.1002/jimd.12009. PMID 30693532.
- ^ Reinhold A, Westermann M, Seifert J, von Bergen M, Schubert T, Diekert G (November 2012). “Impact of vitamin B12 on formation of the tetrachloroethene reductive dehalogenase in Desulfitobacterium hafniense strain Y51”. Appl. Environ. Microbiol. 78 (22): 8025–8032. Bibcode:2012ApEnM..78.8025R. doi:10.1128/AEM.02173-12. PMC 3485949. PMID 22961902.
- ^ Payne KA, Quezada CP, Fisher K, Dunstan MS, Collins FA, Sjuts H, Levy C, Hay S, Rigby SE, Leys D (January 2015). “Reductive dehalogenase structure suggests a mechanism for B12-dependent dehalogenation”. Nature. 517 (7535): 513–516. Bibcode:2015Natur.517..513P. doi:10.1038/nature13901. PMC 4968649. PMID 25327251.
- ^ Ballhausen D, Mittaz L, Boulat O, Bonafé L, Braissant O (December 2009). “Evidence for catabolic pathway of propionate metabolism in CNS: expression pattern of methylmalonyl-CoA mutase and propionyl-CoA carboxylase alpha-subunit in developing and adult rat brain”. Neuroscience. 164 (2): 578–587. doi:10.1016/j.neuroscience.2009.08.028. PMID 19699272. S2CID 34612963.
- ^ Marsh EN (1999). “Coenzyme B12 (cobalamin)-dependent enzymes”. Essays Biochem. 34: 139–154. doi:10.1042/bse0340139. PMID 10730193.
- ^ Allen RH, Seetharam B, Podell E, Alpers DH (January 1978). “Effect of proteolytic enzymes on the binding of cobalamin to R protein and intrinsic factor. In vitro evidence that a failure to partially degrade R protein is responsible for cobalamin malabsorption in pancreatic insufficiency”. The Journal of Clinical Investigation. 61 (1): 47–54. doi:10.1172/JCI108924. PMC 372512. PMID 22556.
- ^ a b Combs GF (2008). The vitamins: fundamental aspects in nutrition and health (3rd ed.). Amsterdam: Elsevier Academic Press. pp. 381–398. ISBN 978-0-12-183492-0. OCLC 150255807.
- ^ Al-Awami HM, Raja A, Soos MP (August 2019). “Physiology, Intrinsic Factor (Gastric Intrinsic Factor)”. StatPearls [Internet]. PMID 31536261.
- ^ Kuzminski AM, Del Giacco EJ, Allen RH, Stabler SP, Lindenbaum J (August 1998). “Effective treatment of cobalamin deficiency with oral cobalamin”. Blood. 92 (4): 1191–1198. doi:10.1182/blood.V92.4.1191. PMID 9694707.
- ^ “Vitamin B12 Deficiency – Nutritional Disorders”. MSD Manual Professional Edition. Retrieved 2022-05-24.
- ^ Battersby AR, Fookes CJ, Matcham GW, McDonald E (May 1980). “Biosynthesis of the pigments of life: formation of the macrocycle”. Nature. 285 (5759): 17–21. Bibcode:1980Natur.285…17B. doi:10.1038/285017a0. PMID 6769048. S2CID 9070849.
- ^ Frank S, Brindley AA, Deery E, Heathcote P, Lawrence AD, Leech HK, et al. (August 2005). “Anaerobic synthesis of vitamin B12: characterization of the early steps in the pathway”. Biochemical Society Transactions. 33 (Pt 4): 811–814. doi:10.1042/BST0330811. PMID 16042604.
- ^ Battersby AR (1993). “How Nature builds the pigments of life” (PDF). Pure and Applied Chemistry. 65 (6): 1113–1122. doi:10.1351/pac199365061113. S2CID 83942303. Archived (PDF) from the original on 2018-07-24. Retrieved 2020-02-20.
- ^ Battersby A (2005). “Chapter 11: Discovering the wonder of how Nature builds its molecules”. In Archer MD, Haley CD (eds.). The 1702 chair of chemistry at Cambridge: transformation and change. Cambridge University Press. pp. xvi, 257–282. ISBN 0521828732.
- ^ Perlman D (1959). “Microbial synthesis of cobamides”. Advances in Applied Microbiology. 1: 87–122. doi:10.1016/S0065-2164(08)70476-3. ISBN 9780120026012. PMID 13854292.
- ^ Martens JH, Barg H, Warren MJ, Jahn D (March 2002). “Microbial production of vitamin B12”. Applied Microbiology and Biotechnology. 58 (3): 275–285. doi:10.1007/s00253-001-0902-7. PMID 11935176. S2CID 22232461.
- ^ a b c Fang H, Kang J, Zhang D (January 2017). “Microbial production of vitamin B12: a review and future perspectives”. Microb. Cell Fact. 16 (1): 15. doi:10.1186/s12934-017-0631-y. PMC 5282855. PMID 28137297.
- ^ Linnell JC, Matthews DM (February 1984). “Cobalamin metabolism and its clinical aspects”. Clinical Science. 66 (2): 113–121. doi:10.1042/cs0660113. PMID 6420106. S2CID 27191837.
- ^ Piwowarek K, Lipińska E, Hać-Szymańczuk E, Kieliszek M, Ścibisz I (January 2018). “Propionibacterium spp.-source of propionic acid, vitamin B12, and other metabolites important for the industry”. Appl. Microbiol. Biotechnol. 102 (2): 515–538. doi:10.1007/s00253-017-8616-7. PMC 5756557. PMID 29167919.
- ^ Riaz M, Ansari ZA, Iqbal F, Akram M (2007). “Microbial production of vitamin B12 by methanol utilizing strain of Pseudomonas species”. Pakistan Journal of Biochemistry & Molecular Biology. 1. 40: 5–10.[permanent dead link]
- ^ Zhang Y (January 26, 2009). “New round of price slashing in vitamin B12 sector (Fine and Specialty)”. China Chemical Reporter. Archived from the original on May 13, 2013.
- ^ Khan AG, Eswaran SV (June 2003). “Woodward’s synthesis of vitamin B12“. Resonance. 8 (6): 8–16. doi:10.1007/BF02837864. S2CID 120110443.
- ^ Eschenmoser A, Wintner CE (June 1977). “Natural product synthesis and vitamin B12”. Science. 196 (4297): 1410–1420. Bibcode:1977Sci…196.1410E. doi:10.1126/science.867037. PMID 867037.
- ^ a b Riether D, Mulzer J (2003). “Total Synthesis of Cobyric Acid: Historical Development and Recent Synthetic Innovations”. European Journal of Organic Chemistry. 2003: 30–45. doi:10.1002/1099-0690(200301)2003:1<30::AID-EJOC30>3.0.CO;2-I.
- ^ a b “Synthesis of Cyanocobalamin by Robert B. Woodward (1973)”. www.synarchive.com. Archived from the original on 2018-02-16. Retrieved 2018-02-15.
- ^ a b c Greer JP (2014). Wintrobe’s Clinical Hematology Thirteenth Edition. Philadelphia, PA: Wolters Kluwer/Lippincott Williams & Wilkins. ISBN 978-1-4511-7268-3. Chapter 36: Megaloblastic anemias: disorders of impaired DNA synthesis by Ralph Carmel
- ^ “George H. Whipple – Biographical”. www.nobelprize.org. Archived from the original on 2017-09-13. Retrieved 2017-10-10.
- ^ “The Nobel Prize in Physiology or Medicine 1934”. NobelPrize.org. Retrieved 2023-02-23.
- ^ “Mary Shorb Lecture in Nutrition”. Archived from the original on March 4, 2016. Retrieved March 3, 2016.
- ^ Shorb MS (May 10, 2012). “Annual Lecture”. Department of Animal & Avian Sciences, University of Maryland. Archived from the original on December 12, 2012. Retrieved August 2, 2014.
- ^ Hodgkin DC, Kamper J, Mackay M, Pickworth J, Trueblood KN, White JG (July 1956). “Structure of vitamin B12”. Nature. 178 (4524): 64–66. Bibcode:1956Natur.178…64H. doi:10.1038/178064a0. PMID 13348621. S2CID 4210164.
- ^ a b Dodson G (December 2002). “Dorothy Mary Crowfoot Hodgkin, 12 May 1910 – 29 July 1994”. Biographical Memoirs of Fellows of the Royal Society. 48: 181–219. doi:10.1098/rsbm.2002.0011. PMID 13678070. S2CID 61764553.
- ^ “The Nobel Prize and the Discovery of Vitamins”. www.nobelprize.org. Archived from the original on 2018-01-16. Retrieved 2018-02-15.
- ^ a b Gaby AR (October 2002). “Intravenous nutrient therapy: the “Myers’ cocktail”“. Altern Med Rev. 7 (5): 389–403. PMID 12410623.
- ^ Gavura S (24 May 2013). “A closer look at vitamin injections”. Science-Based Medicine. Archived from the original on 11 January 2020. Retrieved 10 January 2020.
- ^ Bauer BA (29 March 2018). “Are vitamin B-12 injections helpful for weight loss?”. Mayo Clinic. Archived from the original on 27 November 2019. Retrieved 11 January 2020.
- ^ Silverstein WK, Lin Y, Dharma C, Croxford R, Earle CC, Cheung MC (July 2019). “Prevalence of Inappropriateness of Parenteral Vitamin B12 Administration in Ontario, Canada”. JAMA Internal Medicine. 179 (10): 1434–1436. doi:10.1001/jamainternmed.2019.1859. ISSN 2168-6106. PMC 6632124. PMID 31305876.
External links[edit]
- Cyanocobalamin at the U.S. National Library of Medicine Medical Subject Headings (MeSH)
- “Cyanocobalamin”. Drug Information Portal. U.S. National Library of Medicine.
- “Hydroxocobalamin”. Drug Information Portal. U.S. National Library of Medicine.
- “Methylcobalamin”. Drug Information Portal. U.S. National Library of Medicine.
- “Adenosylcobalamin”. Drug Information Portal. U.S. National Library of Medicine.
Витамин B12
Содержание страницы:
- Определение витамина B12
- Истинный витамин B12 (кобаламин)
- Химическая формула цианокобаламина
- История открытия витамина B12
- Синтез витамина B12
- Факторы Касла
- Функции витамина B12
- Формирование эритроцитов
- Витамин B12 и нервная система
- Витамин B12 и костно-мышечная система
- Витамин B12 и обмен веществ
- Суточные нормы потребления B12
- Дефицит витамина B12
- Причины дефицита витамина B12
- Проблемы с желудком
- Дисбактериоз кишечника
- Вегетарианство
- Какие лекарства влияют на витамин B12
- Курение и витамин B12
- Источники витамина B12
- Болезнь Альцгеймера, витамин B12 и микрофлора
ОПРЕДЕЛЕНИЕ ВИТАМИНА B12
Витаминами B12 называют группу кобальтсодержащих биологически активных веществ, называемых кобаламинами, относящихся к т.н. корриноидам, древним природным биокатализаторам. К ним относят собственно цианокобаламин, гидроксикобаламин и две коферментные формы витамина B12: метилкобаламин и аденозилкобаламин. В более узком смысле витамином B12 называют цианокобаламин, не упуская из вида то, что он не синоним с B12, и несколько других соединений также обладают B12-витаминной активностью. Цианокобаламин — лишь один из них. Следовательно, цианокобаламин всегда витамин B12, но не всегда витамин B12 является цианокобаламином.

Истинный витамин B12 (кобаламин)
Яркой особенностью метаболизма классических пропионовокислых бактерий является высокий уровень образования корриноидов, соединений группы витамина B12 (снизу слева представлена структура коррина – Коррин является родительской структурой корриноидов и ряда коферментов.)

В природе все корриноиды синтезируются только прокариотическими микроорганизмами – представителями обоих филогенетических доменов (империй): Bacteria и Archaea. Следовательно, все нуждающиеся в корриноидах организмы, включая человека, зависят от синтезирующих их микроорганизмов. Всю группу корриноидных соединений часто называют «витамин B12». Вместе с тем, существует понятие «истинный витамин B12», относящееся к кобаламину.
Последний характеризуется наличием «нижнего» α-лиганда атома кобальта с нуклоеотидом, специфическим основанием которого служит 5,6-диметилбензимидазол (5,6-ДМБ). Именно этот корриноид (кобаламин) функционирует в организме человека в двух коферментных формах (как аденозил- или метилкобаламин, β-лиганды), что определяет медицинский аспект изучения биохимии кобаламина. Цианокобаламин, содержащий CN-группу в качестве «верхнего» β-лиганда атома кобальта, – коммерческая форма витамина B12. Классические ПКБ синтезируют истинный витамин B12 (кобаламин) в большом количестве (500-1500 мкг/г).
В организме человека есть только два фермента с коферментами B12:
- Метилмалонил-КоА-мутаза, фермент, использующий в качестве кофактора аденозилкобаламин, катализирует перестановку атомов в углеродном скелете. В результате реакции из L-метилмалонил-КоА получается сукцинил-КоА. Эта реакция является важным звеном в цепи реакций катаболизма белков и жиров.
- 5-Метилтетрагидрофолат-гомоцистеин-метилтрансфераза, фермент из группы метилтрансфераз, использующий в качестве кофактора метилкобаламин, катализирует превращение аминокислоты гомоцистеина в аминокислоту метионин.
Химическая формула цианокобаламина: C63H88CoN14O14P
|
|
 |
ИСТОРИЯ ОТКРЫТИЯ ВИТАМИНА В12
Витамин B12 (цианокобаламин) является одним из наиболее спорных членов семьи витаминов B-комплекса. Хотя полная химическая структура витамина В12 была выявлена только в 1960-х годах, уже исследования с участием этого витамина отмечены двумя Нобелевскими премиями.
Как известно, дефицит витамина В12 приводит к развитию злокачественной анемии, которая в середине XIX века звучала, как приговор и не подлежала лечению. Способы избавления от данного заболевания были обнаружены случайно, в ходе эксперимента на собаках. Американский врач, Джордж Уиппл (George Whipple)провоцировал развитие пернициозной анемии (злокачественного малокровия) у подопытных животных, вызывая кровотечение, а затем кормил собак разнообразными продуктами с целью выявления, какая еда ускоряет выздоровление. Во время эксперимента, ученый обнаружил, что поедание печени в большом количестве быстро излечивает болезнь, вызванную потерей крови. На основании этих данных, Джордж Уиппл предположил, что ежедневный прием данного продукта ведет к устранению злокачественной анемии.
Дальнейшие клинические исследования, проводимые врачами Уильямом Мерфи (William Parry Murphy) и Джорджом Ричардс Майнотом (George Richards Minot), были направлены на изолирование «лечащего» вещества из печени. В ходе испытаний патофизиологи выявили, что лечить анемию у собак, людей способны абсолютно разные вещества печени. В результате, Мерфи и Майнот в 1926 году открыли специфический фактор, находящийся в соке печени. Это стало первым толчком в изучении «рокового» недуга.
В течение последующих 2-х лет, больным на анемию полагалось ежедневно выпивать сок и съедать «плоть» печени в большом количестве (до 3 кг). Однако, длительное употребление сырой печени вызывало отвращение у пациентов и поиск альтернативного лекарства приобрел острый характер. В 1928 году, впервые, химиком Эдвином Коном, выведен печеночный экстракт, который был в 100 раз концентрированее субпродукта животного происхождения. Полученная вытяжка стала первым действующим средством в борьбе с беспощадным заболеванием.
В 1934 году «за открытия, связанные с применением печени в лечении пернициозной анемии» три американских врача, Уильям Парри Мёрфи, Джордж Майкот, а также Джордж Уиппл, получили Нобелевскую премию. Данное событие в конечном итоге привело к появлению на свет растворимого витамина В12. Спустя 14 лет, в 1948 г. Лестер Смит (Англия), а также Эдвард Рикес и Карл Фолкерс (США) впервые получили чистый цианокобаламин в кристаллическом виде. Однако потребовалось еще несколько лет для того, чтобы методом рентгеноструктурного анализа определить его структуру, которая оказалась чрезвычайно сложной. В конце 1950 годов ученые также разработали метод получения витамина в большом количестве из бактериальных культур. Благодаря этому, смертельное заболевание того времени, под названием «злокачественная анемия», стала поддаваться лечению. В 1955 году английский химик и биохимик Дороти Кроуфут-Ходжкин (Dorothy Mary Crowfoot Hodgkin) определила пространственную конфигурацию, химическую структуру молекулы, за что в 1964 г. была удостоена Нобелевской премии.
СИНТЕЗ ВИТАМИНА В12
Витамин В12 является необычным в отношении своего происхождения. Практически все витамины могут быть извлечены из разнообразных растений или конкретных животных но, ни одно растение или животное не способно производить витамин B12. Исключительным источником этого витамина, по современным данным, являются крошечные микроорганизмы: бактерии, дрожжи, плесень и водоросли… Однако несмотря на то, что продуцируют В12 лишь немногие микроорганизмы, сам витамин требуется всему микробному сообществу благодаря своим уникальным свойствам. Подробнее об этом см. в статье: Витамин В12 – ключевое звено в регуляции метаболизма фолиевой кислоты, убихинона и метионина. Дополнительно см.:
Пропионовокислые бактерии синтезируют большое количество витамина В12, который регулирует основные обменные процессы в организме, способствуют повышению иммунного статуса организма, улучшают общее самочувствие за счет активизации белкового, углеводного и жирового обмена, повышают устойчивость к инфекционным заболеваниям, улучшает качество крови, участвует в синтезе различных аминокислот, нуклеиновых кислот. Однако синтез витамина В12 собственной кишечной флорой человека незначителен. При недостатке витамина В12 возникают желудочно-кишечные заболевания, дисбактериоз, анемия. Поэтому важную роль в профилактике и лечении этих заболеваний могут играть пробиотические продукты, содержащие пропионовокислые бактерии – продуценты витамина В12.
ПРИМ.: Следует особо отметить, что содержание витамина В12 в продуктах, ферментированных разработанными заквасками пропионовокислых бактерий в тысячи (!) раз превышает его количество в продукции на традиционных заквасках, содержащих аналогичные культуры, но с добавлением молочнокислых бактерий. Среди современных способов обогащения кисломолочных продуктов витаминами, именно такой микробный сверхсинтез витамина В12 является самым оправданным, так как последние исследования врачей и микробиологов подтвердили, что наиболее эффективно использование витаминов в коферментной (связанной с белком микробной клетки) легкоусвояемой форме. Следует при этом отметить, что витамин В12 локализуется внутри клеток ПКБ, для которых он является эндометаболитом. В пространство желудочно-кишечного тракта витамин поступает только в результате автолиза клеток ПКБ. Этот процесс достаточно выражен, т.к. определенная часть клеток (около 30%) погибает в агрессивной среде ЖКТ (усваивается В12 в основном в подвздошной кишке). Тем самым обеспечивается снабжение организма человека дополнительным витамином В12. В этом плане особое значение приобретают ферментированные ПКБ продукты, где можно увеличить накопление микробной биомассы и, соответственно, количество усвояемого витамина В12.
О ферментации см. тут: Особенности ферментирования
О синтезе см. тут: Микробиологический синтез витамина В12
См. также: Влияния хлористого кобальта на биосинтез витамина В12
ФАКТОРЫ КАСЛА
Как и большинство витаминов, В12 может существовать в различных формах и принимать различные наименования. Названия для витамина B12 содержат словоформу «кобальт», так как кобальт – минерал, найденный в центре витамина: кобринамид, кобинамид, кобамид, кобаламин, гидрокскобаламин, метилкобаламид, аквакобаламин, нитрокобаламин, и цианокобаламин.
Факторы Касла и витамин В12

Факторы Касла (Прим.: Названы в честь американского физиолога и гематолога У.Б.Касла) – это вещества, необходимые для поддержания нормального кроветворения. Витамин В12 относится к внешним факторам Касла. Внутренний же фактор Касла связывает витамин В12 и способствует его адсорбции кишечной стенкой (всасывании эпителиальными клетками подвздошной кишки). Секреция внутреннего фактора Касла может снизиться (или даже полностью прекратиться) при поражении желудочно-кишечного тракта (например, при воспалительном процессе, при атрофическом гастрите, раке), при удалении части желудка или тонкой кишки и т. д. Выделение его усиливается под влиянием инсулина и уменьшается под влиянием алкоголя. При нарушении выделения внутреннего фактора нарушается связывание и всасывание витамина B12, что приводит к развитию B12-дефицитной мегалобластной, или пернициозной, анемии.
Функции витамина В12
Витамин В12 участвует в переводе фолиевой кислоты в активную форму, в синтезе метионина, коэнзима А, антиоксиданта глутатиона, янтарной кислоты, миелина. Он контролирует синтез ДНК (следовательно, деление клеток), созревание эритроцитов, увеличивает уровень Т-супрессоров, что способствует ограничению аутоиммунных процессов. О функциях витамина В12 см. также здесь по стрелке-ссылке →
Формирование эритроцитов.

Витамин В12 и нервная система

Одной из главных задач витамина B12 является участие в процессах производства метионина – аминокислоты, которая влияет на умственную деятельность и формирование эмоционального фона человека. Витамин B12, фолиевая кислота и метионин (а также витамин С) образуют своего рода рабочую группу, которая специализируется, главным образом, на работе мозга и всей нервной системы. Эти вещества участвуют в выработке так называемых моноаминов — стимуляторов работы нервной системы, определяющих состояние нашей психики.
Также, витамин В12 и фолиевая кислота способствуют выработке холина (витамина В4), который существенно влияет на умственную деятельность и психику. В процессе обмена веществ из него в т.н. холинэргических волокнах вырабатывается нейротрансмиттер ацетилхолин – вещество, передающее нервные импульсы. Когда человеку необходимо сосредоточится, накопленный холин преобразуется в ацетилхолин, который активизирует работу мозга.
Нехватка холина грозит самым настоящим распадом психики. Холестерин при дефиците холина окисляется, соединяется с белковыми отходами и закупоривает «проходы» в клеточных мембранах, поэтому в клетку не могут попадать необходимые вещества. Мозг пытается передавать сигналы, но проходные каналы закупориваются, и человек теряет способность ясно мыслить, «впадает в депрессию». При этом сон нарушается, а клетки мозга и нервные окончания начинают быстро отмирать: чем больше холестерина накапливается в крови, тем быстрее происходит этот процесс. Поскольку при нехватке холина отмирают целые колонии холинергических нейронов, в конце концов, возникает опасность неизлечимой болезни Альцгеймера, которая сопровождается абсолютной потерей памяти и распадом личности. Современные нейрофизиологи придерживаются мнения, что значительная часть людей старше 40 лет в западных странах уже вплотную подошла к этой болезни.
См. также: Витамин В12 в лечении заболеваний нервной системы
Витамин В12 и костно-мышечная система

Витамин В12 влияет на рост мышц, поскольку участвует в процессах белкового обмена и синтеза аминокислот. Он активизирует энергообмен в организме. Немаловажно и то, что он поддерживает жизнедеятельность нервных клеток спинного мозга, через которые происходит централизованное управление мускулатурой тела.
Витамин В12 и обмен веществ
Для циркуляции по телу белков, необходимых для роста и восстановления клеток, требуется витамин В12. Многие из ключевых компонентов белка, так называемые аминокислоты, становятся недоступными для использования в отсутствие В12. Витамин В12 оказывает влияние на движение углеводов и жиров в организме.

Также, по последним данным, дефицит витамина B12 приводит к нехватке карнитина, так называемого квазивитамина (витамина Вт или В11) – вещества, являющегося кофактором метаболических процессов, обеспечивающих поддержание активности КоА. Карнитин способствует проникновению через мембраны митохондрий и расщеплению длинноцепочных жирных кислот (пальмитиновой и др.) с образованием ацетил-КоА, мобилизует жир из жировых депо. Иными словами, карнитин участвует в транспортировке молекул жира из крови в митохондрии — «энергетические станции» клеток, где жир окисляется и дает энергию всему организму. Без карнитина содержание продуктов распада в крови повышается, так как жир остается непереработанным. Также, это вещество оказывает нейротрофическое действие, тормозит апоптоз (процесс программируемой клеточной гибели), ограничивает зону поражения и восстанавливает структуру нервной ткани, нормализует белковый и жировой обмен, в т.ч. повышенный основной обмен при тиреотоксикозе, восстанавливает щелочной резерв крови, способствует экономному расходованию гликогена и увеличению его запасов в печени и мышцах.
Суточные нормы потребления витамина В12.
Физиологические потребности в витамине В12 согласно Методическим рекомендациям МР 2.3.1.2432-08 о нормах физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации:
- Верхний допустимый уровень не установлен.
- Физиологическая потребность для взрослых – 3 мкг/сутки
Водорастворимый витамин В12 не токсичен. Инъекции витамина B12 так же признаны безопасными. Поскольку витамин не токсичен, он широко используется в повышенных дозах при многих типах неизлечиваемых хронических недугах, как артриты и псориазы. Его также используют как средство, снимающее утомление, недомогания и боли. Верхний предел поглощения B12 в нормальных условиях в среднем составляет 1,5 мкг при поступлении с пищей до 50 мкг витамина. При поступлении витамина B12 выше связывающей способности избыток выводится с мочой (и калом). Прим. ред.: при некоторых патологиях витамин В12, поступивший с пищей, может вообще не поглощаться и полностью выводиться из организма – о причинах дефицита В12 будет сказано отдельно.
Таблица 1. Рекомендуемые минимальные суточные нормы потребления цианокобаламина (витамина В12) в зависимости от возраста (мкг):
|
Возраст |
Суточная потребность в витамине B12, (мкг) |
|
|
Грудные дети |
0 – 3 мес. |
0,3 |
|
4 – 6 мес. |
0,4 |
|
|
7 – 12 мес. |
0,5 |
|
|
Дети от 1 года до 11 лет |
1 — 3 |
0,7 |
|
3 — 7 |
1,5 |
|
|
7 — 11 |
2 |
|
|
Мужчины (мальчики, юноши) |
11 — 14 |
3 |
|
14 — 18 |
3 |
|
|
> 18 |
3 |
|
|
Женщины (девочки, девушки) |
11 — 14 |
3 |
|
14 — 18 |
3 |
|
|
> 18 |
3 |
|
|
Беременные и кормящие |
3,5 |
Дефицит витамина В12
Скорость изменения уровня B12 зависит от того, сколько B12 поступает из рациона, сколько выводится и сколько поглощается. У детей раннего возраста дефицит B12 может проявиться гораздо быстрее. У пожилых из-за снижения кислотности желудочного сока, снижения функции париетальных (обкладочных) клеток высок риск развития дефицита B12. При этом до 100 % B12, поступившего с пищей, может выводиться с калом.
Симптомы потенциально связанные с дефицитом витамина В12: перхоть, снижение свертывания крови, онемение ног, снижение рефлексов, красный язык, трудности при глотании, язвы языка, усталость, покалывание в ногах, нарушение менструального цикла.
Признаки дефицита витамина В12 очень разные. Его недостаточное количество проявляется как сложный синдром, который включает в себя физические, неврологические и психические расстройства. Физические расстройства проявляются как слабость, быстрая утомляемость, нарушение памяти, головные боли, тахикардия, бледность кожных покровов, головокружение, перхоть, снижение свертывания крови, онемение ног, снижение рефлексов, красный язык, трудности при глотании, язвы языка, усталость, покалывание в ногах, нарушение менструального цикла. Они также включают проблемы с пищеварением: отсутствие ощущения вкуса, потеря аппетита и в конечном итоге потеря веса. Неврологические расстройства часто появляются в первую очередь. К ним относятся:
- парестезия пальцев;
- постоянная слабость;
- нарушения чувствительности;
- мышечная слабость и понижение мышечного тонуса;
- атрофия зрительного нерва (ослабление зрение, что может закончиться слепотой);
- пирамидальный синдром.

ПРИЧИНЫ ДЕФИЦИТА ВИТАМИНА В12
Наиболее известные факторы, повышающие риск образования дефицита В12:
Уменьшенное поглощение в подвздошной кишке
- Болезнь Крона
- Резекция подвздошной кишки
- Инфекция ленточного червя
Уменьшенный внутренний фактор
- Атрофический гастрит
- Пернициозная анемия
- Постгастрэктомический синдром (включая желудочное шунтирование Roux-en-Y)
Генетика
- Дефицит транскобаламина II
Недостаточное потребление
- Злоупотребление алкоголем
- Пациенты старше 75 лет
- Веганы или строгие вегетарианцы (включая грудных детей вегетарианских / веганских матерей)
Длительное применение лекарств
- Использование гистаминовых Н2-блокаторов в течение более чем 12 месяцев
- Применение метформина более четырех месяцев
- Использование ингибитора протонной помпы более 12 месяцев.
См. дополнительно:
Причины возникновения дефицита витамина В12 у людей (Stroinski, 1987)
На рисунке: поглощение и транспортировка витамина В12
Причиной дефицита витамина В12 у 50–70% пациентов (чаще – у лиц молодого и среднего возраста, несколько чаще – у женщин) является недостаточная секреция слизистой желудка внутреннего фактора Кастла (ВФК), вызванная образованием антител к париетальным клеткам желудка, продуцирующим ВФК, или к участку связывания ВФК с витамином В12. Примерно в 20% случаев отмечается наследственная отягощенность в отношении дефицита ВФК. В этих случаях следствием дефицита витамина В12 является развитие так называемой пернициозной анемии. Кроме того, дефицит витамина В12 может быть обусловлен опухолью желудка, гастрэктомией, синдромом мальабсорбции, гельминтозами и дисбактериозом, несбалансированным питанием. К другим причинам относятся наследственные заболевания, характеризующиеся нарушением продукции белков, связывающихся с витамином В12, или дефектом образования активных форм витамина; нарушения метаболизма и/или повышенная потребность в витамине (тиреотоксикоз, беременность, злокачественные новообразования), а также длительный прием блокаторов Н2-рецепторов и ингибиторов протонной помпы. Следует отметить, что резерва витамина В12 в организме даже при ограниченном его поступлении хватает на 3–4 года.
Проблемы с желудком. Как было уже указано (см. выше), нарушения в работе желудка могут способствовать недостатку витамина В12. Это может произойти по двум причинам:
Во-первых, заболевания желудка могут вызвать нарушение функционирования клеток желудка. Клетки могут прекратить производство веществ, необходимых для поглощения B12 называемых «внутренним фактором Касла» Без внутреннего фактора витамин В12 не может всасываться из желудочно-кишечного тракта в клетки организма.
Во-вторых, недостаточная секреция желудочного сока. Отсутствие желудочного сока (состояние, которое называется гипохлоргидрия) снижает поглощение витамина В12, так как большинство B12 в продуктах питания крепится к белкам пищи, и желудочные кислоты необходимы для отделения В12 от этих белков.
В-третьих, синдром избыточного бактериального роста в тонком кишечнике (СИБР), который вызывается снижением секреции соляной кислоты в желудке и нарушением моторики тонкой кишки. При развитии СИБР различные анаэробные и факультативные грамотрицательные аэробы конкурентно утилизируют пищевой кобаламин. Внутренний фактор ингибирует утилизацию кобаламина грамотрицательной аэробной флорой, но не способен противодействовать грамотрицательной анаэробной флоре, поглощающей этот витамин.
Дисбактериоз кишечника. Об исключительной важности микрофлоры кишечника в регуляции обменных процессов в организме сегодня известно всем. Как показывает практика, основной причиной дефицита В12 является не отсутствие в рационе сбалансированного питания, а нарушения процессов всасывания микронутриентов в тонком кишечнике, которые регулируются собственной микрофлорой ЖКТ хозяина. Поэтому дисбиоз кишечника, также является одной из основных причин дефицита В12. Причины дисбаланса микрофлоры бывают разными (как правило вторичны), начиная от описанных выше заболеваний, до таких как: последствия пренесенных кишечных инфекций, вредные привычки, иные заболевания, в т.ч. стрессового характера, антибиотикотерапия и т.п. Известно, что кроме патогенных бактерий, вызывающих заболевания, существуют бактерии использующие кобаламин в своих целях, тем самым мешая его усвоению организмом человека. Исходя из вышеизложенного было бы разумным предположить, что в современных условиях пробиотикотерапия, в т.ч. с применением пропионовокислых бактерий – продуцентов В12, является эффективным инструментом в профилактике гиповитаминоза В12.
Вегетарианство. Способность строгой вегетарианской диеты на поставку достаточного количества витамина В12 является весьма спорной. Кобаламин является необычным витамином, поскольку он не вырабатывается растениями, а синтезируется исключительно бактериями и археями (Roth et al., 1996).
Хотя корриноиды в толстой кишке имеются в изобилии из-за активности кишечной микробиоты, многие факторы препятствуют приобретению человеком значительных уровней кобаламина из этого источника. Во-первых, кобаламин, вырабатываемый кишечными микробами, составляет менее 2% от общего содержания корриноидов в кале (Allen and Stabler, 2008). Кроме того, кобаламин, продуцируемый в толстой кишке, где число микроорганизмов является наивысшим, не является биодоступным, поскольку рецепторы, необходимые для поглощения витамина, находятся в тонкой кишке, выше по течению от места образования корриноидов (Seetharam and Alpers, 1982). Подробнее о микробиоме и витамине В12 см. по ссылке →.
Большинство животных, включая человека, способно накапливать и хранить витамин B12. Главным местом накопления витамина В12 в организме человека является печень, в которой содержится до нескольких миллиграммов данного витамина. В печень он поступает с животной пищей.
Какие лекарства влияют на витамин В12?
К категории препаратов, которые могут снизить поставки витамина В12 в организм, относятся: антибиотики (канамицин, неомицин), противоопухолевые препараты (метотрексат), противосудорожные средства (фенитоин, примидон), анти-подагровые препараты (колхицин), гипотензивные средства (метилдопа), препараты для лечения болезни Паркинсона (леводопа), нейролептики (аминазин), противотуберкулезные препараты (изониазид), препараты понижающие холестерин (клофибрат), хлористый калий, сазароснижающее средство метформин.
Курение и витамин B12

Однако стоит подробно описать условия исследования: мужчины, принимавшие участие в статистическом (!) исследовании ежедневно (!) в течении (!) 10 лет потребляли высокие дозы витаминных препаратов, были в возрасте от 50 до (!) 76 лет и имели долгий (!) анамнез табакокурения, что само по себе вызывает вопросы относительно достоверности данных о причинно-следственной связи повышения риска рака легких. Точку в отношении к полученным результатам поставил сам автор работы, Теодор М. Браски. Он отметил, что планирует провести второе более масштабное исследование для подтверждения результатов первого. В заключение отметим, что сама задача ежедневного многолетнего поглощения высоких доз витамина В12 вообще не ставится, т.к. без научного интереса это никому не нужно и при употреблении пищевых продуктов (даже ферментированных ПКБ) или микробиологических биодобавок (не инъекций или спецвитпрепаратов) проникновение в органы и ткани избыточного кол-ва B12 физически невозможно. Более того, водорастворимый витамин B12 не токсичен и излишки выводятся из организма (см. выше).
Источники витамина В12
Итак, что мы имеем? Человек и животные обычно обеспечивают себя витамином В12 в результате потребления продуктов питания животного происхождения и продуцирования его микрофлорой рубца (для жвачных животных). Однако, учитывая, что синтез витамина В12 кишечной флорой незначителен (и кобаламин из толстого кишечника не является биодоступным), витамин должен обязательно поступать в организм извне.
Следовательно, отличные пищевые источники витамина B12 ограничиваются лишь продуктами животного происхождения? Нет. Во-первых, не всегда можно получить достаточное количество витамина В12 из-за промышленной обработки еды. Во-вторых, разработанные технологии позволяют в настоящее время получать В12-содержащие продукты практически из любых видов пищевого сырья, в т.ч. растительного происхождения. Например, проведенные исследования показали, что при производстве хлеба из ржаной и смеси ржаной и пшеничной муки, применение концентрата закваски с пропионовокислыми бактериями способствует увеличению количества витаминов группы В, особенно витамина В12, как в ржаной закваске, так и в готовом хлебе – установлено, что при выпечке сохраняется более половины витаминов, содержащихся в полуфабрикате. (Показатели готового хлеба: В1 – 0,53-0,57 мкг/100г, В2 – 0,40-0,43 мкг/100г, В12 – 0,65-0,85 мкг/100г).
Отмечено, что пропионовокислые бактерии являются бесспорными лидерами по синтезу витамина В12, а также основными поставщиками цианокобаламина в фармакологии Ферментирование пищевого сырья с использованием пропионовокислых бактерий стало перспективным и доступным направлением в создании витаминизированных пробиотических продуктов, благодаря исследованиям проведенным в ВСГУТУ. Если конкретно говорить о еде, то идеальными, по содержанию витамина В12, являются приготовленные на наших бактериальных (пробиотических) заквасках, т.е. ферментированные именно пропионовокислыми бактериями, следующие биопродукты: кисломолочные напитки, квасные напитки, твердые сорта сыра, хлебобулочные изделия, колбасные изделия и др. продукты, как растительного так и животного происхождения. Сферы применения пробиотиков – продуцентов витаминов группы В постоянно расширяются.
На заметку
БОЛЕЗНЬ АЛЬЦГЕЙМЕРА, ВИТАМИН В12 И КИШЕЧНАЯ МИКРОФЛОРА
АЛЬЦГЕЙМЕРА БОЛЕЗНЬ, дегенеративное заболевание головного мозга, проявляющееся прогрессирующим снижением интеллекта. Впервые описанное немецким врачом А.Альцгеймером в 1907, заболевание является одной из распространенных форм приобретенного слабоумия (деменции). Только в США болезнью Альцгеймера страдают примерно 1,5 млн. человек. Из общего числа в 1,3 млн. человек, находящихся в США в домах престарелых, 30% составляют лица с болезнью Альцгеймера.
В этой же связи следует рассмотреть роль микрофлоры кишечника в развитии старческого слабоумия (болезни Альцгеймера). Как известно, деменция является одной из серьезнейших проблем пожилых людей в развитых странах, 10% людей в возрасте старше 65 лет, 20% лиц старше 75 лет и 30% пожилых людей в возрасте старше 85 лет страдают в той или иной степени этим заболеванием.
Имеются указания на взаимосвязь деменции с дефицитом витамина В12. В клетках макроорганизма витамин В12 превращается в метилкобаломин и аденозилкобаламин. Последний является коэнзимом L-метилмалонил-СоА мутазы, фермента, катализирующего первый этап метаболизма пропионовой кислоты, во время которого метилмалонил-СоА трансформируется в сукцинил-СоА. В случае дефицита витамина В12 резко возрастает количество метилмалоновой кислоты. Метилкобаломин является коэнзимом метионин-синтетазы, участвующей в превращении гомоцистеина в метионин. В отсутствие необходимого количества витамина В12 количество гомоцистеина резко возрастает. Хотя до настоящего времени нет ясности, в какой энзиматической системе или в обеих одновременно это приводит к нейрологическим нарушениям, нет сомнения, что дефицит витамина В12, и, возможно, фолиевой кислоты ответствен за болезнь Альцгеймера, а также других более легких форм неврологических нарушений (повышенной раздражительности, бессонницы и др.).
Поскольку пул витамина В12 в организме в значительной степени определяется жизнедеятельностью определенных кишечных микроорганизмов, не приходится сомневаться, что дисбаланс кишечной микрофлоры, наблюдаемый в пожилом возрасте у подавляющего большинства людей, затрагивает и те группы микроорганизмов, которые участвуют в синтезе, транспорте и метаболизме витамина В12. См. также: Пробиотики полезны для пациентов с болезнью Альцгеймера
Дополнительно см.:
Витамин B12 как модулятор микробной экологии кишечника
Связь дефицита витамина В12 и риска развития сахарного диабета
Характеристика витамина В12 и основнные продуценты при его получении
Витамин В12 в лечении заболеваний нервной системы
Мужская фертильность и витамин B12
О других витаминах:
- Тиамин (Витамин В1)
- Рибофлавин (Витамин В2)
- Ниацин (витамин В3)
- Пантотеновая кислота (Витамин В5)
- Пиридоксин (витамин В6)
- Биотин (Витамин В7)
- Фолиевая кислота (Витамин В9)
Будьте здоровы!
ССЫЛКИ К РАЗДЕЛУ О ПРЕПАРАТАХ ПРОБИОТИКАХ
- ПРОБИОТИКИ
- ПРОБИОТИКИ И ПРЕБИОТИКИ
- СИНБИОТИКИ
- ДОМАШНИЕ ЗАКВАСКИ
- КОНЦЕНТРАТ БИФИДОБАКТЕРИЙ ЖИДКИЙ
- ПРОПИОНИКС
- ЙОДПРОПИОНИКС
- СЕЛЕНПРОПИОНИКС
- БИФИКАРДИО
- ПРОБИОТИКИ С ПНЖК
- МИКРОЭЛЕМЕНТНЫЙ СОСТАВ
- БИФИДОБАКТЕРИИ
- ПРОПИОНОВОКИСЛЫЕ БАКТЕРИИ
- МИКРОБИОМ ЧЕЛОВЕКА
- МИКРОФЛОРА ЖКТ
- ДИСБИОЗ КИШЕЧНИКА
- МИКРОБИОМ и ВЗК
- МИКРОБИОМ И РАК
- МИКРОБИОМ, СЕРДЦЕ И СОСУДЫ
- МИКРОБИОМ И ПЕЧЕНЬ
- МИКРОБИОМ И ПОЧКИ
- МИКРОБИОМ И ЛЕГКИЕ
- МИКРОБИОМ И ПОДЖЕЛУДОЧНАЯ ЖЕЛЕЗА
- МИКРОБИОМ И ЩИТОВИДНАЯ ЖЕЛЕЗА
- МИКРОБИОМ И КОЖНЫЕ БОЛЕЗНИ
- МИКРОБИОМ И КОСТИ
- МИКРОБИОМ И ОЖИРЕНИЕ
- МИКРОБИОМ И САХАРНЫЙ ДИАБЕТ
- МИКРОБИОМ И ФУНКЦИИ МОЗГА
- АНТИОКСИДАНТНЫЕ СВОЙСТВА
- АНТИОКСИДАНТНЫЕ ФЕРМЕНТЫ
- АНТИМУТАГЕННАЯ АКТИВНОСТЬ
- МИКРОБИОМ и ИММУНИТЕТ
- МИКРОБИОМ И АУТОИММУННЫЕ БОЛЕЗНИ
- ПРОБИОТИКИ и ГРУДНЫЕ ДЕТИ
- ПРОБИОТИКИ, БЕРЕМЕННОСТЬ, РОДЫ
- ВИТАМИННЫЙ СИНТЕЗ
- АМИНОКИСЛОТНЫЙ СИНТЕЗ
- АНТИМИКРОБНЫЕ СВОЙСТВА
- КОРОТКОЦЕПОЧЕЧНЫЕ ЖИРНЫЕ КИСЛОТЫ
- СИНТЕЗ БАКТЕРИОЦИНОВ
- АЛИМЕНТАРНЫЕ ЗАБОЛЕВАНИЯ
- МИКРОБИОМ И ПРЕЦИЗИОННОЕ ПИТАНИЕ
- ФУНКЦИОНАЛЬНОЕ ПИТАНИЕ
- ПРОБИОТИКИ ДЛЯ СПОРТСМЕНОВ
- ПРОИЗВОДСТВО ПРОБИОТИКОВ
- ЗАКВАСКИ ДЛЯ ПИЩЕВОЙ ПРОМЫШЛЕННОСТИ
- НОВОСТИ
12.08.2017
Врачи и исследователи не перестают утверждать: наше здоровье напрямую связано с тем, что, в каких количествах и объемах мы едим. Здоровое питание – это вовсе не жесткие диеты, подразумевающие постоянные ограничения в еде, голод и чувство неудовлетворенности.
Правильный рацион состоит из питательных, богатых полезными веществами продуктов и их сбалансированного сочетания в блюдах. Такой режим не приносит дискомфорта и неудобства, а напротив – дарит радость, легкость и позитивный настрой. Стоит начать утро с сытного питательного завтрака – и заряд энергии на весь день обеспечен. Если в течение дня не забывать вовремя и в нужном объеме подкреплять себя чистой и полезной пищей, не срываться на вредные перекусы, то уже через несколько недель вы почувствуете положительные изменения.
Однако, просто употреблять богатые витаминами продукты недостаточно. Ведь сами по себе эти вещества не всегда могут полноценно усваиваться организмом, их содержание в той или иной пище различается, а некоторые соединения вообще несовместимы друг с другом. Поэтому важно знать, какие существуют группы витаминов, какое влияние они оказывают на самочувствие человека, где их найти и как грамотно принимать и сочетать с другими соединениями. В нашем блоге мы стараемся помочь читателям найти ответы на эти вопросы, получить свой рецепт здоровья, красоты и долголетия. Сегодня мы хотели бы поговорить о витамине B12. Для чего он нужен организму, к чему приводит нехватка и в каких продуктах его больше всего – расскажем в нашей статье.
Химические свойства и состав витамина В12
Если быть точными, то это не одно вещество, а несколько соединений, объединенных в одну общую группу и обозначенных буквой латинского алфавита. Эти биологические активные компоненты в своем составе содержат кобальт, необходимый для нормального функционирования многих процессов в нашем организме:
- кроветворение;
- регенерация клеток и тканей;
- предотвращение нарушений в функционировании поджелудочной железы;
- регуляция выработки гормона адреналина.
Сам витамин В12, нехватка которого может пагубно сказаться на состоянии здоровья, с точки зрения химии – это две разновидности одной и той же молекулы кобаламина. Оба варианта еще называют витамерами. Их правильное обозначение среди ученых и врачей – цианокобаламин и гидроксикобаламин.
Не все составляющие этого вещества способны благотворно повлиять на ваше здоровье и общее состояние. Пользу для человека представляют лишь его активные формы. Эти соединения образуются из витамеров – метилкобаламин и дезоксиаденозилкобаламин. Когда мы рассказываем, в каких продуктах находится витамин В12, то подразумеваем именно эти активные формы. Такие названия непросто запомнить обычному, не связанному с химией человеку, поэтому в дальнейшем, на протяжение всего текста статьи мы будем использовать привычное и знакомое всем буквенное название биологически активных веществ этой группы.
Витамин В12: показания к применению
Это вещество в определенном объеме и количестве полезно всем без исключения для нормального функционирования жизненно важных органов и систем, поддержания здорового состояния тела. Существуют и такие случаи, когда его применение не просто рекомендовано, но и необходимо для предотвращения риска развития серьезных заболеваний. Вот самые распространенные ситуации, когда нужно обязательно восполнить дефицит б12:
- болезнь Аддисона-Бирмера;
- различного рода анемии: хронические, вызванные дефицитом железа или токсическими веществами;
- заболевания печени: недостаточность, циррозы;
- лечение последствий алкоголизма
- болезни кожи: псориаз, дерматит
- неврозы;
- атеросклероз;
- артрит;
Вещество оказывает гомеопатическое и метаболическое воздействие, положительно влияет на печень, нервную систему и ускоряет регенерацию. Способно приостановить развитие указанных заболеваний и предотвратить риск возникновения осложнений. Выпускаются препараты в различных формах, в аптеках можно найти множество вариантов. Есть таблетки, жидкости и концентрированные растворы для инъекций. Каждый вид имеет свое назначение и определенные ограничения. Без совета специалиста в них сложно сориентироваться и выбрать нужный, поэтому обязательно проконсультируйтесь с вашим лечащим врачом, прежде чем начать прием. Он расскажет и подробно объяснит, какая форма вам подойдет, поможет определиться с дозировкой и даст рекомендации, как лучше применять препарат: подкожно, внутривенно или внутримышечно.
Для чего нужен организму витамин В12

Это вещество играет значимую роль во всех процессах жизнедеятельности, протекающих в нашем теле. Не зря гиповитаминоз – недостаток витаминов, считается серьезным нарушением, которое врачи советуют незамедлительно устранять. Полный список функций, которые выполняет эта группа соединений, очень велик, здесь мы перечислим лишь самые важные и основные:
- Регулирует выработку эритроцитов: способствует образованию, предотвращает их разрушение и нехватку.
- Положительно влияет на процесс кроветворения.
- Способствует полноценному усвоению белка организмом.
- Улучшает регенерацию тканей печени, почек, сердца.
- Предотвращает развитие заболеваний в этих органах.
- Защищает нервную систему от разрушений, вредного воздействия внешних и внутренних неблагоприятных факторов.
- Предотвращение возникновения анемии.
- Нормализует работу ферментов.
- Активирует деление клеток.
Особенно стоит отметить его возможность покрывать нервные клетки миелиновой оболочкой, необходимой для их полноценной и надежной защиты. Это уникальная функция витамина В12. Другие вещества не способны формировать, образовывать и поддерживать наличие этой оболочки. Это свойство В12 может стать для вас настоящим спасением, если ваша работа и образ жизни предполагают постоянное нервное напряжение и стрессы. Принимая суточную норму витамина, вы убережете себя от депрессии, подавленного состояния, раздражительности, скачков настроения и агрессии, которые так часто можно встретить у жителей современных крупных городов.
Особенно подвержены нервным расстройствам люди, работающие на руководящих должностях, находящиеся в напряжении из-за высокой степени ответственности и большого объема задач. Справедливо это и для тех, кто подвержен воздействию человеческого фактора: учителя, врачи, работники сферы обслуживания. Также не лишней будет профилактика для студентов и учеников в период сдачи экзаменов и подготовки к ним.
У нас можно купить диетические продукты:
- Хлебцы амарантовые с луком 195г
- Джем “Di&Di” вишневый 300г
- Батончики амарантовые “Умные сладости” с кокосовой начинкой, витаминизированные 110 г
Кому обязательно нужно принимать В12
Для взрослого человека стандартная суточная норма В12 составляет около 2,4 мкг. Но стоит помнить, что это количество справедливо лишь для тех, кто не подвержен нервным потрясениям и не имеет вредных привычек и чрезмерных нагрузок. Во время стресса, никотиновой зависимости, повышенной загруженности и утомляемости эта цифра может увеличиваться в диапазоне от 10 до 20%. В таких случаях мы советуем выбирать в пищу продукты, богатые витамином В12 и содержащие его в большом количестве. Мы перечислили случаи, в которых потребность в приеме вещества возрастает:
- у тех, кто активно занимается спортом, особенно касается профессиональных спортсменов;
- если ваша работа предполагает тяжелые физические нагрузки;
- проходящие реабилитацию после алкогольной зависимости;
- беременные и кормящие женщины;
- во время полового созревания у подростков
- дети в период активного роста;

Если вы относитесь к какой-либо категории из этого списка, вам стоит особенно внимательно следить, чтобы организм получал все необходимые вещества. Питание, включающее в себя полезные, богатые витаминами продукты, а также грамотный прием назначенных врачом препаратов – гарантия вашего безупречного здоровья, красоты и молодости на долгие годы.
Недостаток витамина В12: симптомы дефицита
Время от времени нехватка полезных веществ – гиповитаминоз, наступает у многих. Особенно это актуально в осенне-зимний сезон, когда источников витаминов становится меньше, повышается стрессовая нагрузка на ослабленный организм. Этого не стоит опасаться, ведь такое явления вполне естественно. Важно лишь вовремя выявить у себя его симптомы и принять меры по устранению дефицита. Тогда никаких пагубных последствий не возникнет.
О нехватке соединений группы В12 стоит задуматься, если у вас:
- Ухудшилась свертываемость крови.
- Язык приобрел неестественно красный цвет и стал сухим.
- Затруднено глотание.
- Появились зуд на коже головы, перхоть и шелушение.
- Нарушился менструальный цикл.
- Часто немеют ноги и руки, есть ощущение, будто по коже кто-то ползает.
- Наблюдается депрессия, подавленное настроение.
- Повысилась утомляемость.
- Кожные покровы стали бледными или приобрели желтоватый оттенок.
- Нарушения работы сердечно-сосудистой системы.
- Замедлен пульс.
- Ощущается сонливость и усталость.
- Диарея.
- Волосы ломкие, сильно выпадают.
- На слизистых оболочках образуются мелкие ранки и язвочки.
- Головокружение

Конечно, по отдельности эти симптомы могут являться признаками других заболеваний, но если вы наблюдаете у себя сразу несколько проявлений – возможно это и есть гиповитаминоз. С ним несложно бороться, обратившись к врачу за консультацией. Особенно внимательно нужно относиться людям, находящимся в зоне риска. У них нехватка данного витамина наблюдается чаще, чем у остальных.
В каких случаях это происходит:
- в период беременности и лактации
- при волчанке
- во время приема противозачаточных гормональных препаратов
- при наличии в организме паразитов
- злоупотребление алкоголем
- при резекции желудка
- жесткие диеты и ограничения в пище
- отказ от мяса и других продуктов животного происхождения: веганство, вегетарианство, сыроедение
- никотиновая зависимость
- при гастрите
- в преклонном возрасте
- при изменениях микрофлоры кишечника
- при Базедовой болезни
На недостаточное количество В12 могут негативно повлиять и такие факторы, как длительный прием некоторых препаратов при диабете. Вещества, содержащиеся в них, мешают усвоению. Также возможен гиповитаминоз у людей, страдающих заболеваниями желудочно-кишечного тракта. В этом случае даже если В12 поступает в организм, внутренние органы не способны его всасывать. Поговорите об этом со специалистом, который в курсе вашего состояния здоровья. Он назначит вам препараты, восполняющие нехватку В12. Их регулярный прием в совокупности с правильно подобранным рационом и сбалансированной диетой помогут вам уже через две-три недели почувствовать себя намного лучше. Если же постоянно откладывать профилактику, можно получить серьезные заболевания, лечение которых потребует гораздо больше времени, средств и усилий.
К ним относятся:
- анемия
- расстройства нервной системы
- ухудшение зрения
- болезнь Крона
- заболевания кожи
- нарушение памяти
- плохая усвояемость пищи
- потеря аппетита
- рассеянный склероз
Оградите себя и своих близких от последствий гиповитаминоза, не допускайте возникновение опасных болезней и их развитие. Профилактика, как известно, гораздо лучше, чем длительное и сложное лечение. От вас лишь требуется вовремя проходить медосмотр, обследоваться специалистов, сдавать необходимые анализы, а также следить за своим питанием и рационом членов вашей семьи. Для этого нужно знать, в каких продуктах находится и где содержится витамин В12. Мы составили для вас список, который поможет в разработке ежедневного меню, сделает ваш рацион сбалансированным и питательным.
Передозировка В12

Злоупотреблять употреблением этого вещества, конечно же, тоже не стоит. Меру нужно соблюдать даже в самых полезных продуктах и препаратах. Бесконтрольное применение нанесет лишь вред вашему организму и уж точно не будет полезным. Гипервитаминоз – передозировка, проявляет себя в следующих симптомах:
- Болит и колет слева в груди, в районе сердца
- Повышена возбудимость нервной системы
- Увеличивается количество ударов сердца в минуту
Серьезных, опасных и уж тем более смертельных последствий передозировка В12 не принесет, так как этот витамин водорастворимый. Его избыток легко покидает ваше тело вместе с мочой. Но все же на этот процесс необходимо определенное количество времени, а за этот период гипервитаминоз может навредить вашему организму. Поэтому стоит воздержаться от усиленного употребления БАДов и приема витаминных комплексов. Если покупаете препарат в аптеке, четко следуйте инструкции и точно соблюдайте дозировку. Заметив у себя побочные действия, ухудшение общего состояния и самочувствия, временно прекратите употребление комплекса и сразу же обращайтесь к врачу. Не возобновляйте курс, пока специалист не даст вам разрешение.
Где и в чем содержится витамин в 12: список продуктов на каждый день

Пользу и роль витаминосодержащих продуктов для здорового и красивого тела невозможно переоценить. Длинные шелковистые волосы, крепкие ногти, гладкая кожа, ясный ум и отличная память – все это обеспечивает нам отличное самочувствие и прекрасное настроение в любое время года и даже в самый пасмурный день. Сбалансированное и правильное питание дает прилив жизненных сил и повышает работоспособность. Человек, который не испытывает дефицит полезных веществ, соединений и витаминов, реже болеет в период обострения простудных заболеваний. Он силен, полон энергии и вынослив к физическим и умственным нагрузкам, гораздо меньше подвержен стрессам и сезонным депрессиям. К тому же, включение полезных соединений в блюда своего ежедневного рациона помогает сохранить здоровье тела, молодость и красоту даже в преклонном возрасте.
Что нужно включить в свое повседневное меню, чтобы не допустить недостаток витаминов? Чтобы ответить на этот вопрос, мы собрали для вас список самых богатых и полноценных пищевых источников В12
Мясо и субпродукты
- Говядина
- Говяжья печень
- Говяжьи почки
- Говяжий язык
- Говяжье сердце
- Нежирные части свинины
- Свиная печень
- Баранина
- Дичь
- Куриная печень
- Кролик
- Ливерная колбаса
Также В12 в большом количестве содержат куриные яйца, а если точнее – желтки.
Морепродукты
- Краб
- Осьминог
- Моллюски
- Гребешки
- Устрицы
Рыба
- Скумбрия
- Окунь
- Форель
- Кета
- Сардина
- Сельдь
Молочные продукты
- Сыр
- Молоко
- Творог
- Кефир
- Сметана
- Натуральный йогурт
- Простокваша
Растительные продукты
Большинству растений витамин B12 для нормальной жизнедеятельности не требуется, и они его не синтезируют.
Фрукты, овощи и зерновые культуры практически не содержат витамина B12.
Лишь небольшое количество, менее 0,1 мкг на 100 г, обнаружили в некоторых растениях: его содержат брокколи, спаржа, белокопытник японский и пророщенный маш, что может объясняться способностью растений всасывать витамин из некоторых органических удобрений.
Спирулина, сине-зеленая водоросль, богата витамином B12.
Важно помнить, что при ограничении потребления животной пищи, риск развития дефицита В12 усиливается. В растительных источниках он содержится в незначительном количестве и не покрывает суточную норму. Поэтому вегетарианцам стоит обратиться к специалисту, который назначит курс необходимых препаратов.
Автор: Корпорация Di&Di
Мы предлагаем диетические продукты:
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ. ВОЗМОЖНЫ ПОБОЧНЫЕ ЭФФЕКТЫ. НЕОБХОДИМА КОНСУЛЬТАЦИЯ СПЕЦИАЛИСТА.Витамины группы BСредства при гиповитаминозе
Содержание статьи
- Дефицит витамина В12
- В каких продуктах содержится витамин В12
- Витамин В12: для чего нужен женскому организму
- Витамин В12: для чего нужен мужскому организму
- Как часто можно делать уколы витамина В12
- Краткое содержание
- Задайте вопрос эксперту по теме статьи
В12 дефицитная анемия — довольно часто встречающаяся. Она появляется после 60 лет у 1 из 50 человек, а после 70 лет — у каждого 15 человека. Нехватку витамина можно профилактировать с помощью применения витамина В12, витаминных комплексов и БАДов, содержащих В12.
Мы попросили провизора Кристина Хохрина рассказать подробнее о дефиците витамина В12, о том, в каких продуктах он содержится, для чего нужен мужчинам и женщинам, а еще как часто можно делать уколы с витаминов В12.
Дефицит витамина В12
Витамин В12, или цианокобаламин, — это водорастворимый витамин, который проникает в организм из кишечника и накапливается в клетках печени. Из печени витамин уже расходуется организмом постепенно пополняя запасы вновь. Но при некоторых условиях усвоение витамина прекращается.
Рассказываем, для чего нужен витамин В12. Он участвует в синтезе ДНК, производит энергию, принимает участие в образовании кровяных клеток — эритроцитов, поддерживает нормальную работу нервной системы и обмена веществ. Витамин В12 контролирует уровень гомоцистеина, повышение которого приводит к заболеваниям сердечно-сосудистой системы и болезни Альцгеймера.
Три основных симптома недостатка витамина В12:
- анемия
- нарушение работы ЖКТ
- психо-неврологические проявления
При постановке диагноза В12-дефицитной анемии проводят ряд лабораторных исследований. Одним из них является биохимический анализ крови, в котором исследуются критерии:
- активности лактатдегидрогеназы (ЛДГ)
- свободный билирубин;
- уровень витамина В12 в крови (менее 140 пг/мл)
- уровень фолиевой кислоты в сыворотке крови (более 5 нг/мл);
У детей дефицит проявляется задержкой развития, раздражительностью, непроизвольными движениями, снижением тонуса мышц. У взрослых вред для организма от недостатка витамина б12 проявляет себя такими симптомами как:
- нарастание слабости, особенно в ногах
- отсутствие интереса и мотиваций
- невозможность выполнения физических нагрузок
- учащенное сердцебиение, боли в сердце
- расстройство работы ЖКТ: тошнота, диарея, запор и тд.
- «онемение» конечностей вплоть до полной утраты чувствительности пальцев рук
- отечность лица и отсутствие мимики
- бледно-желтый цвет кожи
- «малиновый лаковый язык»
- повышение температуры тела
- увеличение селезенки
Если вовремя не начать лечение, то прогнозы будут неутешительными. Постепенно развивается нарушение чувствительности всех мышц, снижается слух и зрение, нарушается функция тазовых органов и появляются выраженные когнитивные нарушения, поражение нервной системы туловища и конечностей.
В каких продуктах содержится витамин В12
В12 содержится в продуктах животного происхождения, а в некоторые растительные продукты его искусственно добавляют.
- мясо: говядина, свинина
- печень и почки
- морепродукты
- тунец, форель, лосось
- молоко, йогурт, сыр, яйцо
- растительные заменители молока
Средняя суточная потребность взрослого человека в витамине В12 составляет 2,4 мкг. Точное необходимое количество витамина зависит от возраста и пола человека. Для поддержания нормального уровня витамина в организме необходимо съесть, например, 2 яйца, 85 г тунца или говядины.
Витамин В12: для чего нужен женскому организму
Женскому организму витамин В12 необходим в большей степени в период беременности и лактации. Так как потребление его возрастает в 2 раза. Поэтому врач может рекомендовать дополнительный прием витаминных комплексов или обогащенных им продуктов.
Витамин В12: для чего нужен мужскому организму
В мужском организме витамин В12 отвечает за те же процессы, что и в женском. У витамина нет разделения действия по половому признаку.
Как часто можно делать уколы витамина В12
Витамин В12 в виде уколов назначает только врач, который и пропишет количество необходимых инъекций. Но чаще 1 раза в сутки ставить уколы не придется. Лицам старше 50 лет рекомендуется дополнительное применение В12 в виде БАДов или обогащенных им продуктов.
Краткое содержание
- Витамин В12 — цианокобаламин, он регулирует работу нервной системы, участвует в процессе кроветворения и поддерживает энергетические и обменные процессы организма.
- Витамин В12 содержится в продуктах животного происхождения, но им могут дополнительно обогащать и растительные продукты.
- Для женского и мужского организма действие витамина В12 одинаково.
- Ставить инъекции витаминов В12 необходимо придерживаясь рекомендаций врача, но не чаще одного раза в сутки.
Задайте вопрос эксперту по теме статьи
Остались вопросы? Задайте их в комментариях ниже – наши эксперты ответят вам. Там же Вы можете поделиться своим опытом с другими читателями Мегасоветов.
Выпускающий редактор
Эксперт-провизор
Поделиться мегасоветом
Понравилась статья? Расскажите маме, папе, бабушке и тете Гале из третьего подъезда