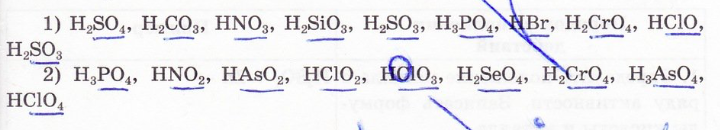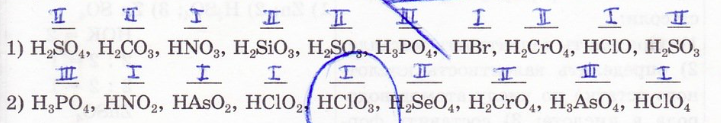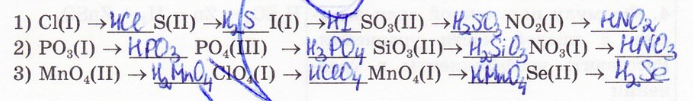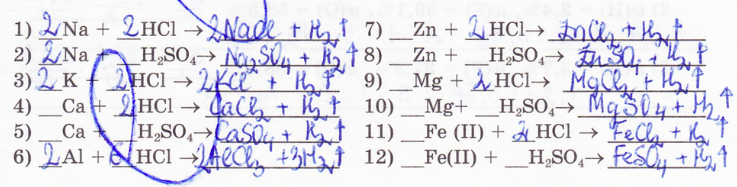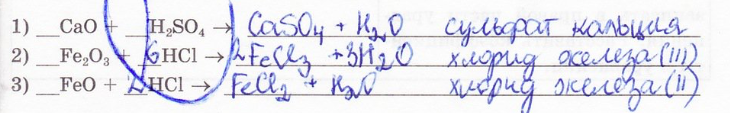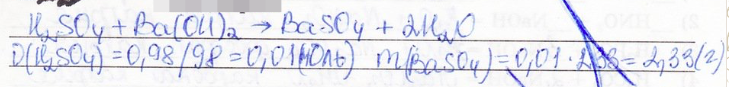1. Кислоты – это сложные вещества, состоящие из кислотных остатков и водорода, который может замещаться на атомы металлов.
2. Подчеркните кислотный остаток в молекулах кислот:
3. Валентность кислотного остатка равна числу атомов водорода, способных замещаться атомами металлов.
Определите валентность кислотных остатков следующих кислот:
4. Составьте формулы кислот по известным кислотным остаткам:
5. Составьте формулы кислот по следующим данным:
6. Составьте уравнения реакций между металлами и растворами кислот (в скобках указана валентность металла в образующейся соли):
7. Составьте уравнения возможных реакций между металлами и арстворами кислот:
8. Составьте уравнения реакций между кислотами и основными оксидами. Запишите названия образующихся солей.
9. Составьте уравнения реакций нейтрализации. Запишие названия образующихся солей.
10. Составьте уравнения реакций по следующим даным:
1) Смесь цинка и оксида цинка растворили в соляной кислоте, а образовавшихся газ пропустили над раскаленным оксидом железа (3).
2) Применяемый как примочка при ушибах ацетат свинца (ядовит) по одному из способов приготовляется дейтсвием уксусной кислоты на оксид свинца (2).
3) При паянии употребляют так называемую травленную кислоту. Приготавливают ее действием цинка на соляную кислоту.
11. Задачи:
1) Вычислите массу образующейся соли, если в реакцию вступила серная кислота массой 0,98 г и гидроксид бария.
2) Вычислите массу оксида меди (2), способного вступить в реакцию с азотной кислотой массой 12,6 г.
3) Вычислите массу оксида железа (3) способного вступить в реакцию с соляной кислотой массой 1, 825 г.
4) В лаборатории потребовалось нейтрализовать раствор, содержащий серную кислоту. Сначала для нейтрализации был прибавлен раствор гидроксида натрия, а избыток кислоты нейтрализован раствором гидроксида калия. На операцию пошло 4 г гидроксида натрия и 0,56 г гидроксида калия. Определите массу килоты, содержавшейся в растворе.
Сохраните или поделитесь с одноклассниками:
1)
ω(H) = 2,1%;
ω(N) = 29,8%;
ω(O) = 68,1%.
Из этих атомов можно составить 2 кислоты: азотную (HNO3) и азотистую (HNO2).
M(HNO3) = 1 + 14 + 48 = 63 г/моль.
ω(H) = M(H) / M(HNO3) = 1/63 = 0,016 = 1,6%
Не сходится.
M(HNO2) = 1 + 14 + 32 = 47 г/моль.
ω(H) = M(H) / M(HNO2) = 1/47 = 0,021 = 2,1%
Сходится.
Ответ: HNO2 – азотистая кислота.
2)
ω(H) = 2,4%;
ω(S) = 39,1%;
ω(O) = 58,5%.
Из этих атомов можно составить 2 кислоты: серную (H2SO4) и сернистую (H2SO3)
M(H2SO4) = 1*2 + 32 + 16*4 = 98 г/моль.
ω(H) = M(H2) / M(H2SO4) = 2/98 = 0,02 = 2%
Не сходится.
M(H2SO3) = 1*2 + 32 + 16*3 = 82 г/моль.
ω(H) = M(H2) / M(H2SO3) = 2/82 = 0,024 = 2,4%
Сходится.
Ответ: H2SO3 – сернистая кислота.
3)
ω(H)=3,7%;
ω(P)=37,8%;
ω(O)=58,5%.
Из этих атомов можно составить 2 кислоты: фосфорную (H3PO4) и фосфористую (H3PO3)
M(H3PO4) = 1*3 + 31 + 16*4 = 98 г/моль.
ω(H) = M(H3) / M(H3PO4) = 3/98 = 0,03 = 3%
Не сходится.
M(H3PO3) = 1*3 + 31 + 16*3 = 82 г/моль.
ω(H) = M(H3) / M(H3PO3) = 3/82 = 0,037 = 3,7%
Сходится.
Ответ: H3PO3 – фосфористая кислота.
Как составить химические формулы кислот соответствующих оксидам?
Ученик
(63),
закрыт
8 лет назад
Александр Титов
Гений
(50749)
9 лет назад
Просто добавить воду в формулу и записать формулу соответствующей кислоты.
На первом месте будет водород, на втором – неметалл, на третьем – кислород.
Например,
Кислотному оксиду SO3 соответствует кислота H2SO4
SO3 + H2O – всего водорода 2 атома, его на 1-е место ставим H2**, далее один атом серы – ставим его после водорода
H2S*, ещё остаётся кислород – три атома от SO3 и один от H2O – итого 4, ставим после серы и получаем H2SO4.
В случае, если атомы в молекуле можно сократить на одно и то же число – сокращаем.
Например, способом выше из N2O5 и H2O получится формально H2N2O6 – сокращаем на 2 и получаем HNO3.
Есть и особые случаи, например, оксиду P2O5 соответствует как метафосфорная (HPO3), так и ортофосфорная (H3PO4) кислота. В первом случае молекул воды условно добавили 2 штуки.
Ещё надо помнить, что не все оксиды являются солеобразующими – несолеобразующим оксидам не соответствуют никакие кислоты, таковы, например, оксиды N2O, NO, CO. Нельзя формально написать, например, H2NO2 – нет такой кислоты.
Составьте формулы кислот по следующим данным 1)w(H) = 2, 1%, w(N) = 29, 8%, w(O) = 68, 1%_______________ 2)w(H) = 2, 4%, w(S) = 39, 1%, w(O) = 58, 5%________________ 3)w(H) = 3, 7%, w(P) = 37, 8%, w(O) = 58, 5%__________________.
На этой странице сайта вы найдете ответы на вопрос Составьте формулы кислот по следующим данным 1)w(H) = 2, 1%, w(N) = 29, 8%, w(O) = 68, 1%_______________ 2)w(H) = 2, 4%, w(S) = 39, 1%, w(O) = 58, 5%________________ 3)w(H) = 3, 7%, w(P) = 37, 8%, w(O?,
относящийся к категории Химия. Сложность вопроса соответствует базовым
знаниям учеников 5 – 9 классов. Для получения дополнительной информации
найдите другие вопросы, относящимися к данной тематике, с помощью поисковой
системы. Или сформулируйте новый вопрос: нажмите кнопку вверху страницы, и
задайте нужный запрос с помощью ключевых слов, отвечающих вашим критериям.
Общайтесь с посетителями страницы, обсуждайте тему. Возможно, их ответы
помогут найти нужную информацию.