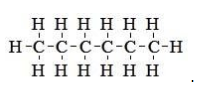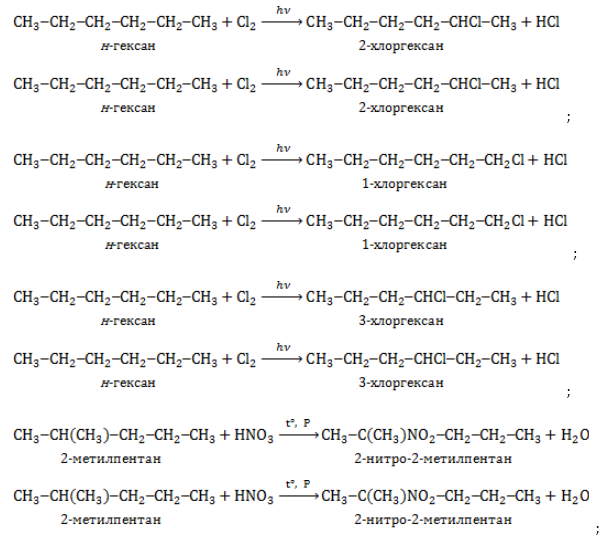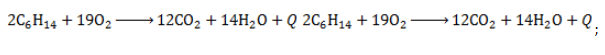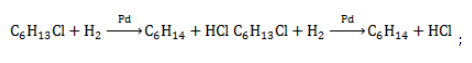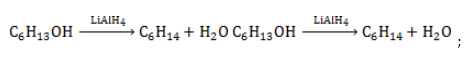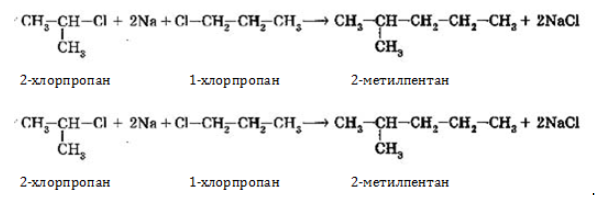Изомеры гексана
Содержание
- 1 Формула и строение гексана
- 2 Изомерия гексана
- 3 Свойства гексана
- 3.1 Физические свойства (таблица)
- 3.2 Химические свойства
- 4 Получение гексана
- 5 Применение гексана
- 6 Заключение
Гексан является шестым членом гомологического ряда алканов. Существуют различные варианты строения молекулы – изомеры гексана. Структурные различия изомеров обусловливают разные свойства.
Формула и строение гексана
Как насыщенный углеводород, гексан характеризуется максимально возможным количеством водорода в молекуле. При этом все четыре валентности углеродных атомов задействованы в простых ковалентных связях.
Молекулярная формула гексана показывает, что любой его изомер, независимо от строения, представляет собой предельное соединение с линейной (не имеющей замкнутых участков) молекулой, в которой отсутствуют кратные связи.
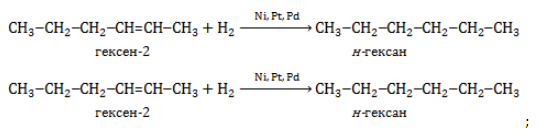
Наглядным примером может служить изомер с простейшим строением – н-гексан. Структурная формула нормального гексана имеет вид
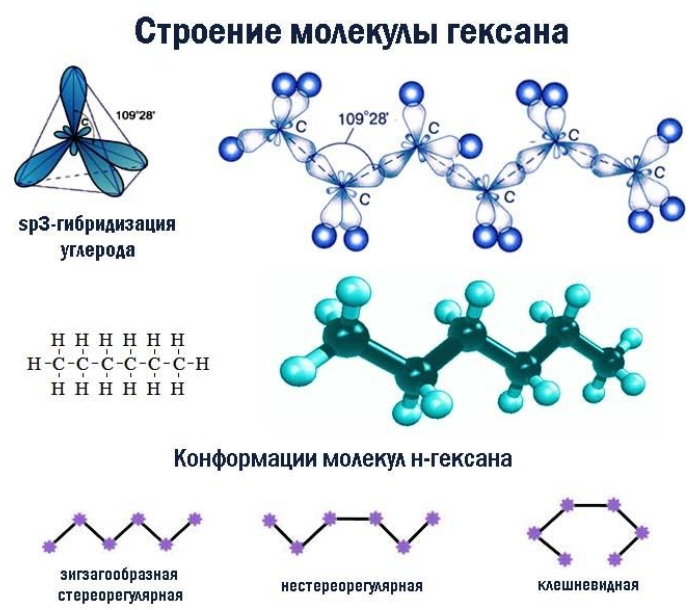
Необходимо отметить, что она не отражает зигзагообразного пространственного расположения атомов в цепи , возникающего вследствие тетраэдрических валентных углов (
)
-гибридизованного углерода.
Цепь может принимать различные конформации за счет вращения вокруг простых -связей. Изменения конформации не являются изомерами, поскольку не вызывают перестройки углеродной цепочки.
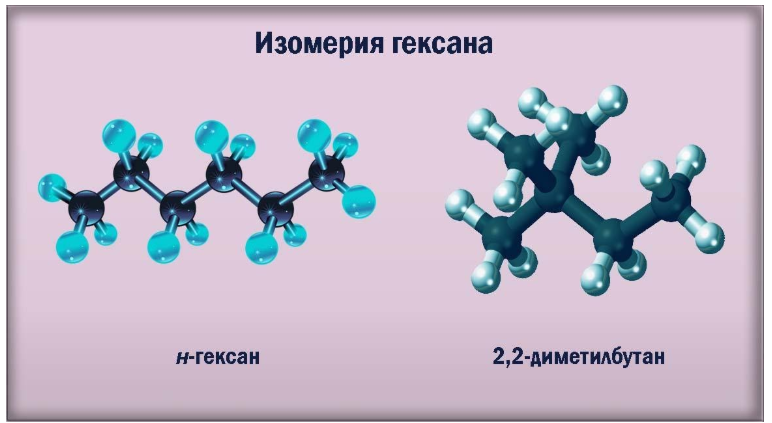
Изомерия гексана
Как представитель ряда алканов, гексан обладает структурной изомерией, обусловленной различиями в расположении звеньев углеродного скелета. Изомеры гексана отличаются друг от друга наличием или отсутствием в молекуле алкильных радикалов, их количеством и позицией.
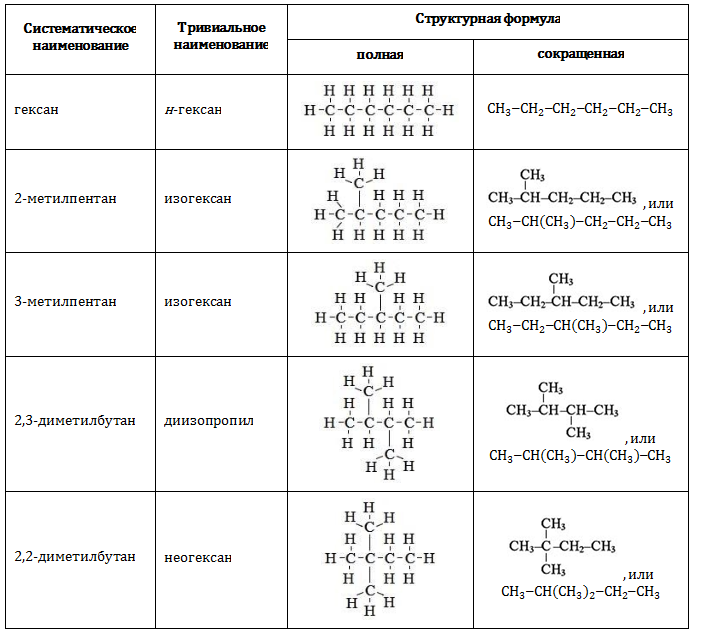
Существует всего пять изомерных соединений с составом , которые имеют распространенные тривиальные наименования помимо систематических.
В таблице представлены полные и сокращенные структурные формулы всех возможных для гексана изомеров.
Это интересно:
Изомеры пентена
Гомологи бензола
Свойства гексана
Вследствие структурных различий при одном и том же атомном составе изомеры представляют собой разные вещества, характеризующиеся неодинаковыми свойствами.
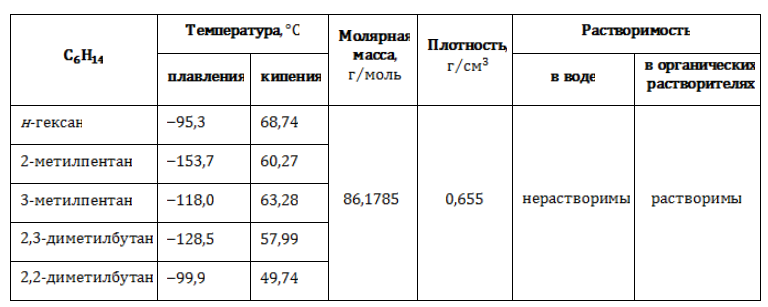
Физические свойства (таблица)
Все изомеры состава представляют собой бесцветные жидкости со слабо выраженным специфическим запахом. Изомерия оказывает влияние на термические характеристики веществ:
Химические свойства
Поскольку у алканов нет межклассовых изомеров, все вещества состава проявляют свойства, типичные для предельных углеводородов:
- неспособность к реакциям присоединения;
- участие в реакциях замещения:
- устойчивость к окислению при низких температурах;
- горючесть:
- разложение (крекинг) при энергичном термическом воздействии:
- способность к отщеплению водорода с образованием непредельных и циклических углеводородов:
Получение гексана
В промышленности гексан и его изомеры получают в процессах переработки нефтепродуктов:
- нормальный гексан – при прямой перегонке;
- изогексаны – при каталитическом разделении (крекинге).
Для лабораторных нужд используют следующие методы:
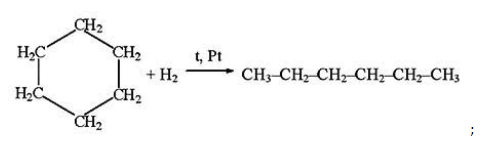
- гидрирование циклогексана:
- восстановление галогенгексана:
- восстановление спирта:
- гидрирование непредельных углеводородов:
- сшивание галогеналканов (синтез Вюрца):
Применение гексана
Различные изомеры состава находят широкое применение в топливной и химической промышленности:
- В качестве компонентов топлива используются изомеры с наиболее разветвленной цепью – диметилгексаны (н-гексан ввиду склонности к детонации, наоборот, снижает качество бензина).
- В производстве ароматических углеводородов при нефтепереработке.
- Как растворитель гексан используется в органическом синтезе, хроматографии, при экстракции из натурального сырья растительных масел, в лакокрасочном производстве и нефтедобыче.
- При обработке порошковых материалов в нанотехнологии.
Заключение
Гексан – соединение, незаменимое во многих отраслях, однако работа с ним сопряжена с риском. Гексан отличается взрывоопасностью и высокой степенью воспламеняемости, обладает негативными биологическими (наркотическими) свойствами. Это токсичное соединение относится к умеренно опасным (третий класс) веществам.
При работе с гексаном и его изомерами необходимо соблюдение техники безопасности и правильное использование средств защиты (респираторов, перчаток) и оборудования.
Оценка статьи:
Загрузка…
Как составлять изомеры
Одним из важнейших понятий в органической химии является – изомерия. Ее смысл заключается в том, что существуют вещества, различающиеся пространственным расположение своих атом или атомных групп, при этом обладающих одинаковой молекулярной массой и составом. В этом и заключается главная причина того что в природе наблюдается огромное разнообразие органических веществ.

Вам понадобится
- Как составить изомер рассмотрим на примере алкана C6H14
Инструкция
Сначала нужно составить формулу углеводородного скелета в неразветвленном виде, исходя из данных его молекулярной формулы.
С – С – С – С – С – С
Пронумеровать все атомы углерода.
1 2 3 4 5 6
С – С – С – С – С – С
Зная о том, что углерод четырехвалентен, подставить атомы водорода углеродную цепь.
1 2 3 4 5 6
СН3 – СН2 – СН2 – СН2 – СН2 – СН3
Уменьшите углеродную цепочку на один атом, расположив его в виде бокового ответвления. Важно понимать, что боковые атомы цепочки углерода не могут стать боковыми ответвлениями.
С – С – С – С – С
С
Со стороны, к которой ближе боковое ответвление начните нумерацию цепочки, а затем расставьте атомы водорода, соблюдая правила валентности.
1 2 3 4 5
СН3 – СН – СН2 – СН2 – СН3
СН3
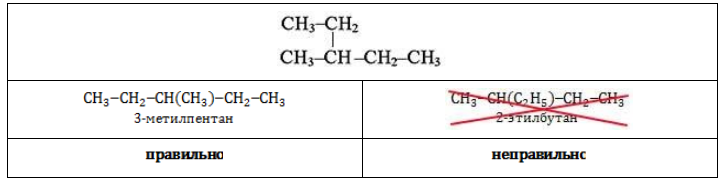
Если есть возможность чтобы расположить боковое ответвление у других атомов углеродной цепи, составьте все возможные изомеры.
1 2 3 4 5
СН3 – СН2 – СН – СН2 – СН3
СН3
Если для бокового ответвления больше нет возможностей, уменьшите изначальную цепочку углерода на один его атом, при этом расположив его как боковое ответвление. Не забывайте, что при одном атоме в углеродной цепочке находятся не больше двух ответвлений.
С
С – С – С – С
С
Пронумеруйте новую цепь атом с того же края, к которому ближе ответвление. Добавьте атомы водорода, помня о четырехвалентности атома углерода.
СН3
1 2 3 4
СН3 – С – СН2 – СН3
СН3
Проверяйте дальше можно ли расположить еще боковые ответвления к углеродной цепочке. Если можно составьте формулы изомеров. Если нельзя продолжайте уменьшать цепочку атомов углерода, постепенно на один атом, располагая его как боковое ответвление. Пронумеровав цепочку, продолжайте составлять формулы изомеров. Нумерация, в случае если боковые ответвления, находятся на одинаковом расстоянии от краев цепи, будет начинаться с края, у которого больше боковых ответвлений.
1 2 3 4
СН3 – СН – СН – СН3
СН3 СН3
Продолжайте последовательность всех действий, пока будет иметься возможность для расположения боковых ответвлений.
Видео по теме
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Опубликовано 3 года назад по предмету
Химия
от катя15197
помогите составить три изомера гексана пожалуйста
-
Ответ
Ответ дан
maria2503я знаю, что тебе там был нужен гексин, я сюда кину
-
Ответ
Ответ дан
PershinaValeryизомеры гексана
CH3-CH(CH3)-CH2-CH2-CH3 2-метилпентан
CH3-CH2-CH(CH3)-CH2-CH3 3-метилпентан
CH3-CH(CH3)-CH(CH3)-CH3 2,3-диметилбутан
Самые новые вопросы
Математика – 3 года назад
Решите уравнения:
а) 15 4 ∕19 + x + 3 17∕19 = 21 2∕19;
б) 6,7x – 5,21 = 9,54
Информатика – 3 года назад
Помогите решить задачи на паскаль.1)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти произведение всех элементов массива.2)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти сумму четных элементов массива.3)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти максимальный элемент массива.4)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти максимальный элемент массива среди элементов,
кратных 3.
География – 3 года назад
Почему япония – лидер по выплавке стали?
Математика – 3 года назад
Чему равно: 1*(умножить)х? 0*х?
Русский язык – 3 года назад
В каком из предложений пропущена одна (только одна!) запятая?1.она снова умолкла, точно некий внутренний голос приказал ей замолчать и посмотрела в зал. 2.и он понял: вот что неожиданно пришло к нему, и теперь останется с ним, и уже никогда его не покинет. 3.и оба мы немножко удовлетворим свое любопытство.4.впрочем, он и сам только еле передвигал ноги, а тело его совсем застыло и было холодное, как камень. 5.по небу потянулись облака, и луна померкла.
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Задать вопрос
Задать вопрос
Ваш вопрос
Вопрос должен состоять из 4 и более символов (не считая знаков препинания)
Подробное описание
Можно ввести 4000 cимволов
Темы
Темы обязательны для заполнения
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
Выберите причину жалобы и оставьте комментарий
Содержит грамматические или орфографические ошибкиСпамНе соответствует тематике сайтаНарушает закон РФМожет показаться обиднымНеверно указана темаПлохо сформулированДругое
Опишите, пожалуйста, подробно причину для более быстрой
обработки вашей жалобы:
Можно ввести 4000 cимволов
E-mail для обратной связи
Отправить
Нажимая кнопку «Отправить», вы принимаете условия пользовательского соглашения
Спасибо
Ваша заявка будет рассмотрена в течение 5 рабочих дней.
Гексан C6H14 – это предельный углеводород, содержащий шесть атомов углерода в углеродной цепи. Бесцветная жидкость с характерным запахом, нерастворим в воде и не смешивается с ней.
CH3-CH2-CH2-CH2-CH2-CH3
Гомологический ряд гексана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4, или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение гексана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp3:
При образовании связи С–С происходит перекрывание sp3-гибридных орбиталей атомов углерода:
При образовании связи С–H происходит перекрывание sp3-гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp3-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109о 28′ друг к другу:
Это соответствует тетраэдрическому строению.
Например, в молекуле гексана C6H14 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет имеет зигзагообразное строение.
Изомерия гексана
Структурная изомерия
Для гексана характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
Для углеводородов состава С6Н14 существуют пять изомеров углеродного скелета: н-гексан, 2-метилпентан, 3 -метилпентан, 2,2-диметилбутан, 2,3-диметилбутан
| Гексан | 2-Метилпентан |
| CH3-CH2-CH2-CH2-CH2-CH3 | CH3-CH(CH3)-CH2-CH2-CH3 |
Для пентана не характерна пространственная изомерия.
Химические свойства гексана
Гексан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для гексана характерны реакции:
- разложения,
- замещения,
- окисления.
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для гексана характерны радикальные реакции.
Гексан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Гексан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании гексана образуется смесь хлорпроизводных.
CH3-CH2-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CH2-CH2-CH2-CH2Cl + HCl
CH3-CH2-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CH2-CH2-CHCl-CH3 + HCl
CH3-CH2-CH2-CH2-CH2-CH3 + Cl2 → CH3-CH2-CHCl-CH2-CH2-CH3 + HCl
Бромирование протекает более медленно и избирательно.
С третичный–Н > С вторичный–Н > С первичный–Н
CH3-CH2-CH2-CH2-CH2-CH3 + Br2 → CH3-CH2-CH2-CH2-CHBr-CH3 + HBr
CH3-CH2-CH2-CH2-CH2-CH3 + Br2 → CH3-CH2-CHBr-CH2-CH2-CH3 + HBr
1.2. Нитрование гексана
Гексан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в гексане замещается на нитрогруппу NO2.
Например. При нитровании гексана образуются преимущественно 2-нитрогексан и 3-нитрогексан:
CH3-CH2-CH2-CH2-CH2-CH3 + HNO3 → CH3-CH2-CH2-CH2-CHNO2-CH3 + H2O
CH3-CH2-CH2-CH2-CH2-CH3 + HNO3 → CH3-CH2-CHNO2-CH2-CH2-CH3 + H2O
2. Дегидрирование гексана
Дегидрирование – это реакция отщепления атомов водорода.
В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др.
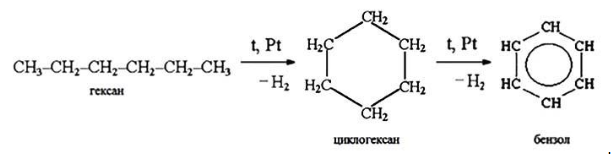
Алканы с углеродной цепью, содержащей 6 и более атомов углерода в главной цепи, при дегидрировании образуют устойчивые шестиатомные циклы, т. е. циклогексан и его гомологи, которые далее превращаются в ароматические углеводороды.
Гексан при нагревании в присутствии оксида хрома (III) в зависимости от условий может образовать циклогексан и потом бензол:
3. Крекинг
Крекинг – это реакция разложения алкана с длинной углеродной цепью на алканы с более короткой углеродной цепью и алкены.
Крекинг бывает термический и каталитический.
Термический крекинг протекает при сильном нагревании без доступа воздуха.
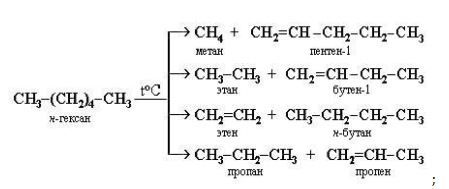
При этом получается смесь алканов и алкенов с различной длиной углеродной цепи и различной молекулярной массой.
Например, при крекинге н-гексана образуется смесь, в состав которой входят этилен, пропан, метан, бутилен, пропилен, этан и другие углеводороды.
Каталитический крекинг проводят при более низкой температуре в присутствии катализаторов. Процесс сопровождается реакциями изомеризации и дегидрирования. Катализаторы каталитического крекинга – цеолиты (алюмосиликаты кальция, натрия).
4. Окисление гексана
Гексан – слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.).
Полное окисление – горение
Гексан горит с образованием углекислого газа и воды. Реакция горения гексана сопровождается выделением большого количества теплоты.
2C6H14 + 19O2 → 12CO2 + 14H2O + Q
Уравнение сгорания алканов в общем виде:
CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O + Q
При горении гексана в недостатке кислорода может образоваться угарный газ СО или сажа С.
5. Изомеризация гексана
Под действием катализатора и при нагревании неразветвленные алканы, содержащие не менее четырех атомов углерода в основной цепи, могут превращаться в более разветвленные алканы.
Например, н-гексан под действием катализатора хлорида алюминия и при нагревании образует 2-метилпентан, 3-метилпентан и другие изомеры.
Получение гексана
1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета.
Реакция больше подходит для получения симметричных алканов.
Гексан можно получить из 1-хлорпропана и натрия:
2CH3-CH2-CH2-Cl + 2Na → CH3-CH2-CH2-CH2-CH2-CH3 + 2NaCl
2. Гидрирование алкенов и алкинов
Гексан можно получить из гексена или гексина:
При гидрировании гексена-1, гексена-2 или гексена-3 образуется гексан:
CH2=CH-CH2-CH2-CH2-CH3 + H2 → CH3-CH2-CH2-CH2-CH3
CH3-CH=CH-CH2-CH2-CH3 + H2 → CH3-CH2-CH2-CH2-CH3
При полном гидрировании гексина-1, гексина-2 или гексина-3 также образуется гексан:
CH≡C-CH2-CH2-CH2-CH3 + 2H2 → CH3-CH2-CH2-CH2-CH3
CH3-C≡C-CH2-CH2-CH3 + 2H2 → CH3-CH2-CH2-CH2-CH3
3. Синтез Фишера-Тропша
Из синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды:
nCO + (3n+1)H2 = CnH2n+2 + nH2O
Это промышленный процесс получения алканов.
Из угарного газа и водорода можно получить гексан:
6CO + 13H2 = C6H14 + 6H2O
4. Получение гексана в промышленности
В промышленности гексан получают из нефти, каменного угля, природного и попутного газа. При переработке нефти используют ректификацию, крекинг и другие способы.