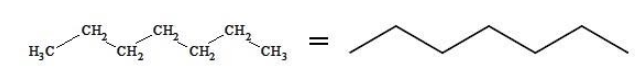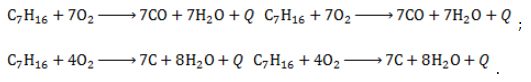Содержание
- 1 Химическое строение и формула гептана
- 2 Изомеры гептана
- 2.1 Структурная изомерия
- 2.2 Оптическая изомерия
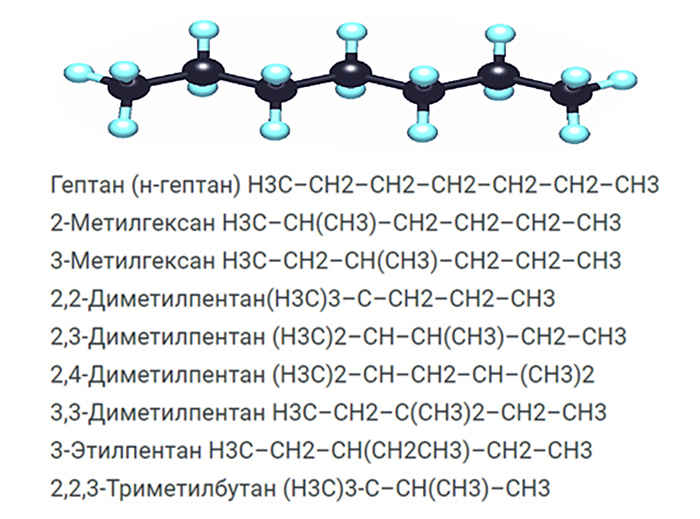
- 2.3 Список изомеров
- 3 Физические свойства
- 3.1 Свойства изомеров гептана
- 4 Химические свойства
- 5 Получение гептана и его изомеров
- 6 Применение гептана и его изомеров
- 7 Заключение
Гептан – седьмой член гомологического ряда алканов. Вследствие различий в порядке соединения и пространственного расположения атомов в молекуле гептан образует несколько изомеров, проявляющих разные свойства. Источником получения гептана служат нефть и нефтепродукты, попутный и природный газ.
Химическое строение и формула гептана
Предельные углеводороды, к числу которых относится гептан, характеризуются полным насыщением всех валентностей углерода. Располагая каждый четырьмя свободными валентностями, sp3-гибридизованные углеродные атомы в молекулах алканов образуют насыщенные водородом цепочки состава .Молекула гептана, скелет которой составлен семью атомами углерода, описывается химической формулой С7H16.
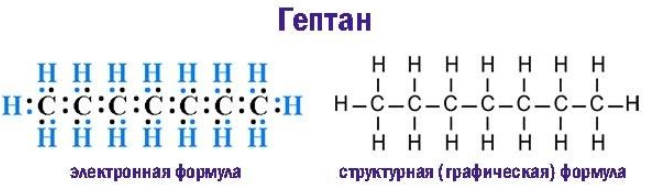
Каждая общая электронная пара, возникающая при взаимодействии атомов, соответствует одинарной (простой) ковалентной -связи. Строение молекулы графически выражают электронная и структурная формулы:
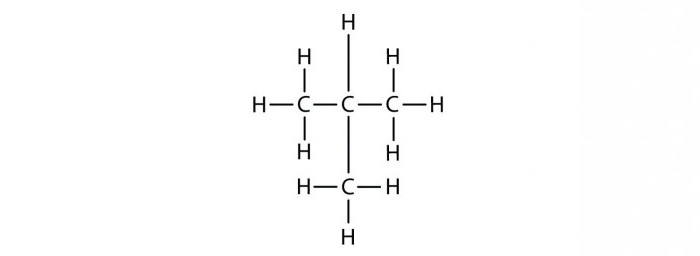
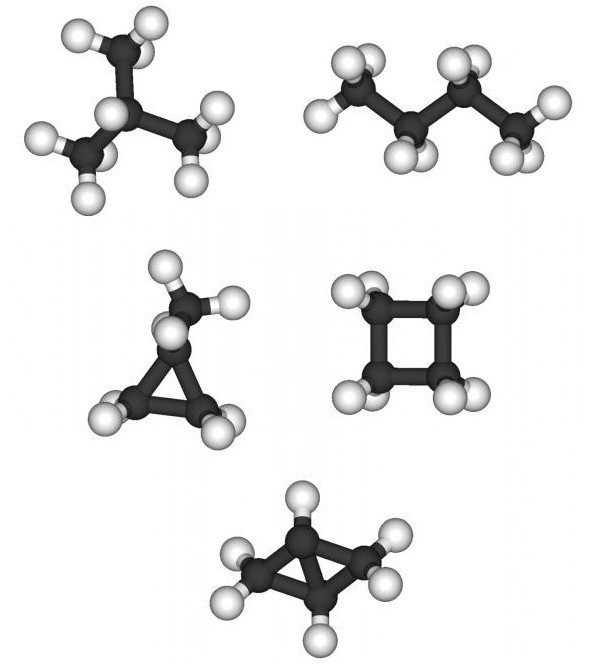
Скелетная формула представляет строение гептана в компактном виде как зигзагообразную линию. Атомы, формирующие углеродный скелет, находятся в вершинах и на концах линии; при записи их обозначения обычно опускают:
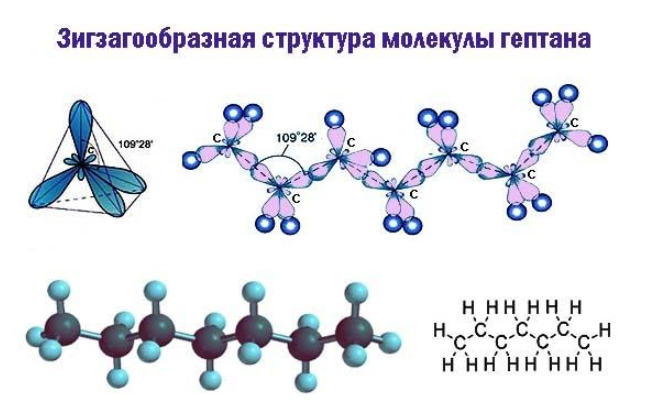
В двумерной форме зигзаг более точно показывает строение молекулы, так как ориентация связей C-C соответствует углу , который образуется между валентными орбиталями при sp3-гибридизации.
Изомеры гептана
Благодаря возможности ветвления углеродного скелета и пространственным различиям в положении одинаковых алкильных радикалов соединениям состава свойственна изомерия. Всего у гептана насчитывается 11 изомерных вариантов.
Структурная изомерия
Существует девять изомеров с химической формулой C7H16, различающихся строением молекулы. По длине главной углеродной цепочки, по типу и числу радикалов они подразделяются следующим образом:
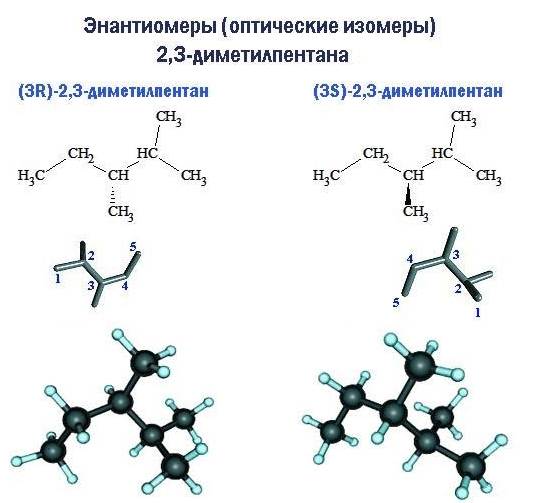
Оптическая изомерия
Если при одинаковой структуре молекулы расположение радикалов таково, что молекула не имеет зеркальной симметрии, возникает пространственная изомерия оптического типа.
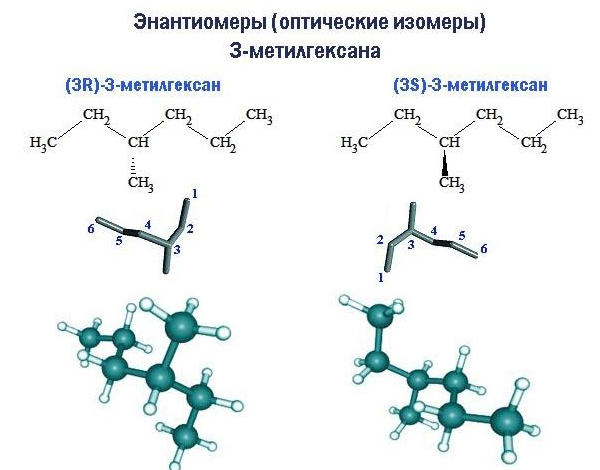
Молекулы оптических изомеров (иначе называемых энантиомерами) обладают свойством хиральности: зеркально отображая друг друга, они при вращении не становятся идентичными. Примером хиральности является отличие правой ладони от левой. Центром хиральности молекулы является тот атом углерода, к которому у энантиомеров присоединены радикалы, по-разному ориентированные в пространстве.
Хиральность свойственна двум из девяти структурных изомеров гептана. Каждое из этих соединений – 3-метилгексан и 2,3-диметилпентан – существует в форме двух энантиомеров, обозначаемых как правый (R) и левый (S) изомеры. При этом указывается номер центра хиральности в углеродной цепи.
В среде с оптической активностью или в химической реакции с другим хиральным соединением энантиомеры ведут себя различно. В других случаях их свойства одинаковы.
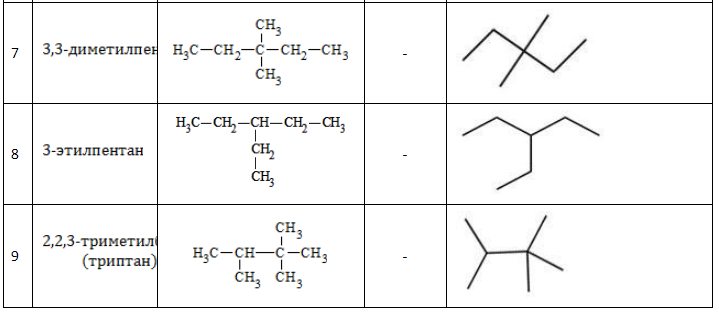
Список изомеров
Все изомеры гептана с названиями и формулами, с учетом наличия энантиомеров, перечислены в таблице:

Физические свойства
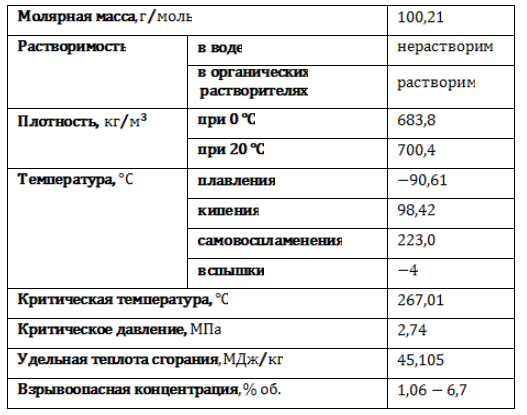
Гептан в обычных условиях представляет собой легкую подвижную жидкость с резким специфическим запахом, без цвета. Пары гептана тяжелее воздуха и образуют с ним взрывоопасную смесь. Основные физические свойства н-гептана приведены в таблице:
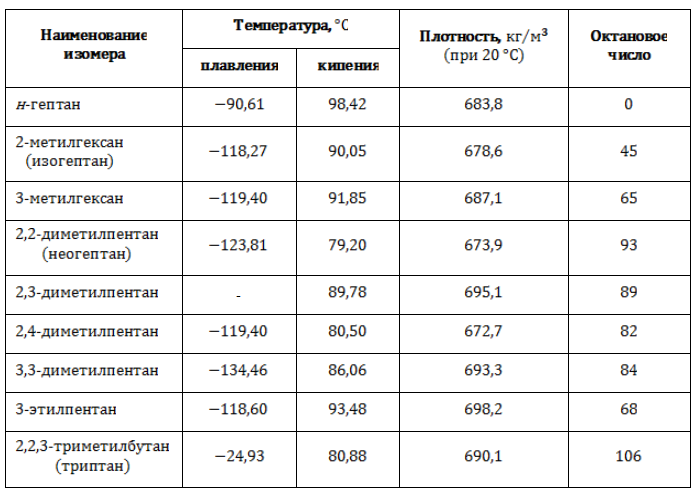
Свойства изомеров гептана
Различия в строении молекулы являются причиной неодинаковости плотностных и термических характеристик изомеров, в том числе и такой важной, как детонационные свойства.
Устойчивость горючего к взрыву при сжатии выражают через октановое число, сравнивая топливо с эталоном. В состав эталонной смеси входят н-гептан, который крайне склонен к детонации, и чрезвычайно устойчивый к ней изооктан. Процентное содержание изооктана в эталонной смеси называется октановым числом.
Существует зависимость между степенью разветвленности молекулы и стойкостью углеводорода к детонации. Чем больше алкильных радикалов и, соответственно, третичных и четвертичных углеродных атомов содержит молекула, тем выше антидетонационная характеристика и качество топлива.
Химические свойства
Гептан и его изомеры – предельные углеводороды и проявляют все химические свойства, присущие данному классу органических соединений. Вследствие насыщенного характера всех связей они вступают только в реакции, протекающие с разрывом ковалентной связи. При этом, как правило, необходимо подвергнуть реагенты нагреванию и использовать катализаторы.
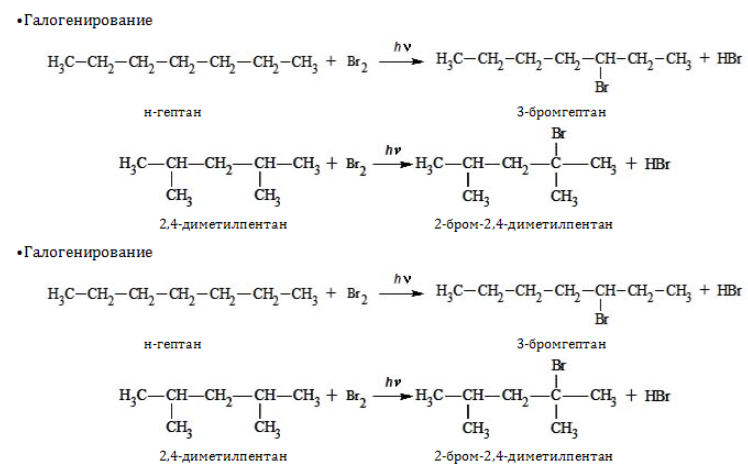
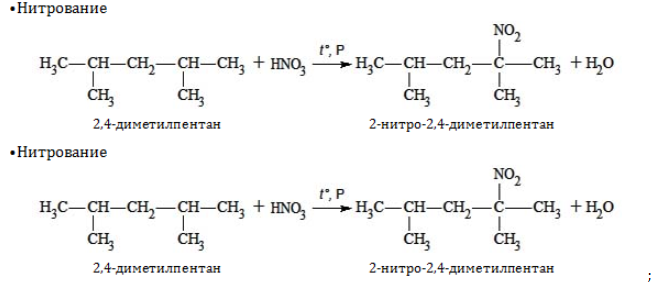
1. Замещение:
2. Окисление:
При недостатке кислорода продуктами неполного сгорания гептана являются угарный газ и сажа:
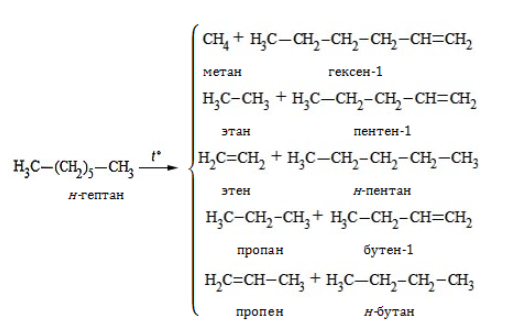
3. Разложение на низшие алканы и алкены при нагревании без доступа кислорода (крекинг):
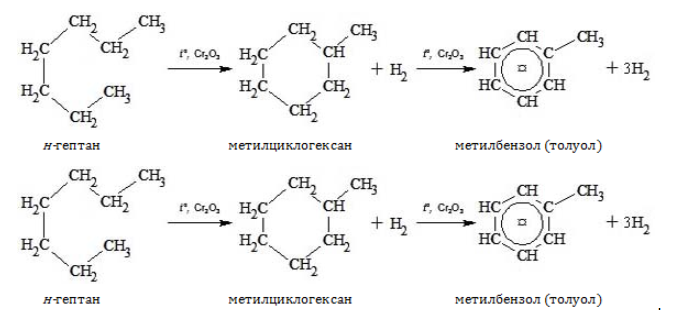
4. Дегидрирование с образованием циклического углеводорода (дегидроциклизация):
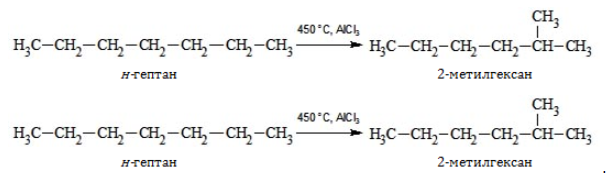
5. Изомеризация с ветвлением углеродного скелета:
Получение гептана и его изомеров
Промышленное получение соединений с химическим составом С7H16 проводится при добыче и переработке природного газа и нефти либо методом синтеза Фишера–Тропша наряду с прочими углеводородами:
В лабораторной практике гептан и изомеры синтезируются следующими способами:
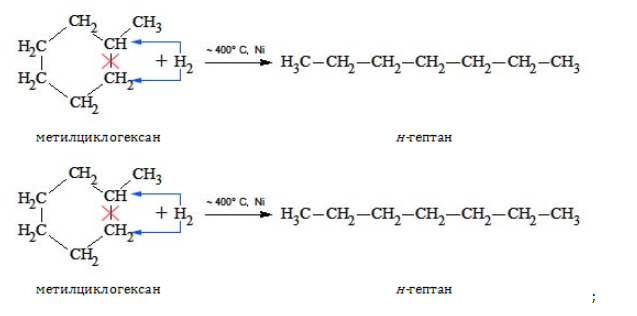
- гидрирование и дециклизация циклоалканов:
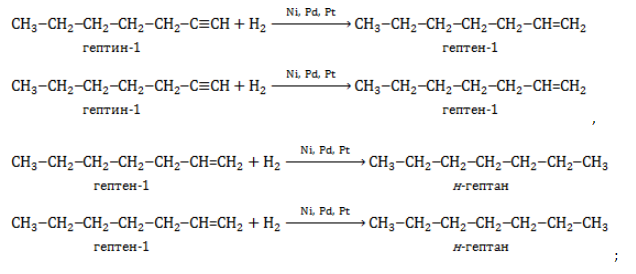
- гидрирование алкинов и алкенов:
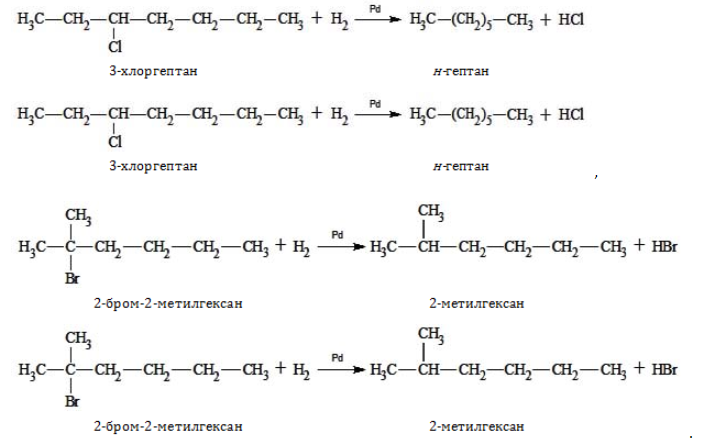
- восстановление галогенпроизводных предельных углеводородов:
Применение гептана и его изомеров
Углеводороды состава C7H16 используются в различных отраслях в зависимости от свойств.
1. В топливной промышленности находят применение:
- н-гептан – в качестве компонента эталонной смеси для определения антидетонационных качеств горючего;
- 2,2,3-триметилбутан (триптан) повышает устойчивость к детонации и добавляется в бензин как присадка.
2. В нефтепереработке и химической промышленности:
- н-гептан играет важную роль в процессах циклизации и ароматизации углеводородов, например, при получении толуола.
3. В качестве растворителя (чистый н-гептан либо в смеси с изомерами):
- для обработки склеиваемых поверхностей в производстве различных изделий из пластических масс;
- в технологиях экстрагирования растительных масел.
Это интересно:
Изомеры октана
Изомеры органических веществ
Заключение
В отношении пожаро- и взрывоопасности гептан входит в число опасных грузов III класса (легковоспламеняющиеся жидкости). Гептан оказывает раздражающее воздействие на центральную нервную систему и по шкале токсикологической опасности относится к веществам IV класса. При длительной работе с ним необходимо защищать кожные покровы и органы дыхания.
При использовании защитных средств, соблюдении герметичности тары и оборудования, вентиляции помещений работа с гептаном не представляет угрозы. Большим преимуществом гептана, как и прочих жидких углеводородов, является удобство хранения и транспортировки по сравнению с газообразными низшими алканами.
1) СH3-CH2-CH2-CH2-CH2-CH2-CH3 n-гептан
2) СH3-CH-CH2-CH-CH3
| |
CH3 CH3 2,4 ди метил пентан
3) СH3 CH3
| |
CH3 — C — CH- CH3
|
CH3 2,2,3 — триметил бутан
4)
СН3
|
CH3-CH2-C-CH2-CH3
|
CH3 3,3 диметил пентан
5) СH3-CH-CH-CH2-CH3
| |
CH3 CH3 2,3 диметил пентан
6) СH3- CH2-CH2-CН-CH2-CH3
|
CH3 3 метил гексан
7) СH3 — CH- CH2-CH2-CH2-CH3
|
CH3 2метилгексан
8)
CH3
|
СH3-C-CH2-CH2-CH3
|
CH3 2,2 диметилпентан
9)
СH2-CH3
|
CH3-CH2-C-CH2-CH3 3-этил пентан
Прежде чем анализировать, как составлять изомеры предельных углеводородов, выявим особенности данного класса органических веществ.
Насыщенные углеводороды
В органической химии выделяется множество классов CxHy. У каждого есть своя общая формула, гомологический ряд, качественные реакции, применение. Для насыщенных углеводородов класса алканов характерны одинарные (сигма) связи. Общая формула данного класса органических веществ CnH2n+2. Этим объясняются основные химические свойства: замещение, горение, окисление. Для парафинов не характерны присоединение, так как связи в молекулах этих углеводородов одинарные.
Изомерия
Такое явление, как изомерия объясняет многообразие органических веществ. Под изомерией принято понимать явление, при котором существует несколько органических соединений, имеющих одинаковый количественный состав (число атомов в молекуле), но различное расположение их в молекуле. Получаемые вещества называют изомерами. Они могут быть представителями нескольких классов углеводородов, а потому отличаются химическими свойствами. Разное соединение в молекуле алканов атомов С приводит к возникновению структурной изомерии. Как составлять изомеры алканов? Существует определенный алгоритм, согласно которому можно изобразить структурные изомеры данного класса органических веществ. Появляется подобная возможность только с четырех углеродных атомов, то есть, с молекулы бутана С4Н10.
Разновидности изомерии
Для того чтобы понять, как составлять формулы изомеров, важно иметь представление о ее видах. При наличии внутри молекулы одинаковых атомов в равном количестве, располагающихся в пространстве в разном порядке, идет речь о пространственной изомерии. Иначе ее называют стереоизомерией. В подобной ситуации применения одних только структурных формул будет явно недостаточно, потребуется использование специальных проекционных или пространственных формул. Предельные углеводороды, начиная с H3C–СН3 (этана), имеют различные пространственные конфигурации. Это обусловлено вращением внутри молекулы по связи С–С. Именно простая σ-связь создает конформационную (поворотную) изомерию.
Структурная изомерия парафинов
Поговорим о том, как составлять изомеры алканов. Класс имеет структурную изомерию, то есть, атом углерода образует разные цепи. Иначе возможность изменения положения в цепи атомов углерода называют изомерией углеродного скелета.
Изомеры гептана
Итак, как оставлять изомеры для вещества, имеющего состав C7H16? Для начала можно расположить все атомы углерода в одну длинную цепочку, добавить для каждого определенное число атомов С. Сколько? Учитывая, что валентность углерода равна четырем, у крайних атомов будет по три атома водорода, а у внутренних – по два. Полученная молекула имеет линейное строение, такой углеводород называют н – гептаном. Буква «н» подразумевает прямой углеродный скелет в данном углеводороде.
Теперь меняем расположение углеродных атомов, «укорачивая» при этом прямую углеродную цепочку в C7H16. Составить изомеры можно в развернутом либо сокращенном структурном виде. Рассмотрим второй вариант. Сначала один атом С расположим в виде радикала метил в разных положениях.
Данный изомер гептана имеет следующее химическое название: 2-метилгексан. Теперь «передвигаем» радикал к следующему углеродному атому. Полученный предельный углеводород называется: 3-метилгексан.
Если мы будем далее передвигать радикал, нумерация будет начинаться с правой стороны (ближе к началу располагается углеводородный радикал), то есть, мы получим такой изомер, который у нас уже есть. Поэтому думая над тем, как составлять формулы изомеров для исходного вещества, попробуем сделать скелет еще «короче».
Оставшиеся два углерода можно представить в виде двух свободных радикалов – метил.
Расположим сначала их у разных углеродов, входящих в главную цепь. Назовем полученный изомер -2,3 диметилпентан.
Теперь оставим один радикал на том же месте, а второй перенесем к следующему углеродному атому главной цепи. Данное вещество называется 2,4 диметилпентан.
Теперь расположим углеводородные радикалы у одного углеродного атома. Сначала у второго, получим 2,2 диметилпентан. Затем у третьего, получив 3,3 диметилпентан.
Теперь оставляем в основной цепи четыре атома углерода, оставшиеся три используем в качестве радикалов метил. Располагаем их следующим образом: два у второго атома С, один – у третьего углерода. Называем полученный изомер: 2,2, 3 триметилбутан.
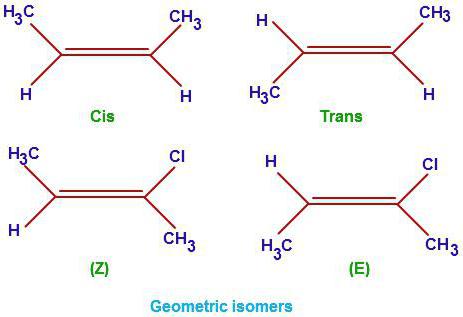
На примере гептана мы разобрали, как правильно составлять изомеры для предельных углеводородов. На фото представлены примеры структурных изомеров для бутена6 его хлорпроизводных.
Алкены
Данный класс органических веществ имеет общую формулу CnH2n. Помимо насыщенных связей С-С в данном классе есть также двойная связь. Именно она определяет основные свойства данного ряда. Поговорим о том, как оставлять изомеры алкенов. Попробуем выявить их отличия от предельных углеводородов. Помимо изомерии главной цепи (структурные формулы) для представителей данного класса органических углеводородов также характерны еще три разновидности изомеров: геометрические (цис- и трансформы), положения кратной связи, а также межклассовая изомерия (с циклоалканами).
Изомеры C6H12
Попробуем выяснить, как составить изомеры c6h12, учитывая тот факт, что вещество с данной формулой может принадлежать сразу к двум классам органических веществ: алкенам, циклоалканам.
Для начала подумаем, как составлять изомеры алкенов, если есть двойная связь в молекуле. Ставим прямую углеродную цепочку, поставим кратную связь после первого углеродного атома. Попробуем не только составить изомеры с6н12, но и назвать вещества. Данное вещество – гексен – 1. Цифрой указывается положение в молекуле двойной связи. При ее передвижении по углеродной цепочке, получаем гексен -2, а также гексен – 3
Теперь порассуждаем, как составлять изомеры для данной формулы, меняя количество атомов в главной цепи.
Для начала укоротим углеродный скелет на один углеродный атом, его будет рассматривать в качестве радикала метил. Двойную связь оставим после первого атома С. Полученный изомер по систематической номенклатуре будет иметь следующее название: 2 метилпентен – 1. Теперь передвигаем углеводородный радикал по главной цепи, оставив положение двойной связи неизменным. Данный непредельный углеводород разветвленного строения называют 3 метилпентен -1.
Возможен без изменения основной цепи и положения двойной связи еще один изомер: 4 метилпентен -1.
Для состава C6H12 можно попробовать переместить двойную связь из первого во второе положение, не преобразуя саму главную цепочку. Радикал при этом будет передвигать по углеродному скелету, начиная со второго атома С. Данный изомер имеет название 2 метилпентен-2. Кроме того, можно поместить радикал CH3 третьего атома углерода получив при этом 3 метилпентен-2
Если поместить радикал у четвертого углерода атома в данной цепи, образуется еще одно новое вещество непредельный углеводород с извилистым углеродным скелетом – 4 метилпентен-2.
При дальнейшем сокращении числа С в главной цепи, можно получить еще один изомер.
Двойную связь оставим после первого углеродного атома, а два радикала поставим к третьему атому С основной цепи, получаем 3,3 диметилутен-1.
Теперь поставим радикалы у соседних углеродных атомов, не меняя положения двойной связи, получим 2,3 диметилбутен-1. Попробуем, не меняя размер главной цепи, передвинуть двойную связь во второе положение. Радикалы при этом мы может поставить только у 2 и 3 атомов С, получив 2,3 диметилбутен-2.
Других структурных изомеров для данного алкена нет, любые попытки их придумать приведут к нарушению теории строения органических веществ А. М. Бутлерова.
Пространственные изомеры C6H12
Теперь выясним, как составлять изомеры и гомологи с точки зрения пространственной изомерии. Важно понимать, что цис- и трансформы алкенов возможны только для положения двойной связи 2 и 3.
При нахождении в одной плоскости углеводородных радикалов, образуется цис – измер гексена -2, а при расположении радикалов в разных плоскостях, транс-форма гексена – 2.
Межклассовые изомеры C6H12
Рассуждая над тем, как составлять изомеры и гомологи, нельзя забывать и о таком варианте, как межклассовая изомерия. Для непредельных углеводородов ряда этилена, имеющих общую формулу CnH2n, такими изомерами являются циклоалканы. Особенностью данного класса углеводородов является наличие циклической (замкнутой) структуры при насыщенных одинарных связях между атомами углерода. Можно составить формулы циклогексана, метилциклопентана, диметилциклобутана, триметилциклопропана.
Заключение
Органическая химия многогранна, загадочна. Количество органических веществ превышает в сотни раз число неорганических соединений. Данный факт легко объясняется существованием такого уникального явления, как изомерия. Если в одном гомологическом ряду располагаются сходные по свойствам и строению вещества, то при изменении положения атомов углерода в цепи, появляются новые соединения, названные изомерами. Только после появления теории химического строения органических веществ удалось классифицировать все углеводороды, понять специфику каждого класса. Одно из положений данной теории, непосредственно касается явления изомерии. Великий русский химик сумел понять, объяснить, доказать, что именно от расположения углеродных атомов зависят химические свойства вещества, его реакционаня активность, практическое применение. Если сравнивать количество изомеров, образуемых предельными алканами и непредельными алкенами, лидируют, безусловно, алкены. Объясняется это тем, что в их молекулах есть двойная связь. Именно она позволяет этому классу органических веществ образовывать не только алкены разного вида и строения, но и вести речь о меклассовой изомерии с циклоалканами.
Мастер
(1460),
закрыт
12 лет назад
лиза ………
Ученик
(12)
12 лет назад
Дорогие школьники! Никто за вас ваши задания не сделает. Возможно, помогут разобраться с теорией. Задавайте вопросы правильно, не “сделайте вместо меня” а “я делаю-делаю, а вот в этом месте не понимаю, почему так? ” или “где почитать про то как решать такие задачи” и т. п. Ну вы поняли
Tutti FruttiМастер (1460)
12 лет назад
Дорогая Лизанька, я не прошу “сделать мне домашнюю работу”, и теорию объяснять не надо-читала уже. Мне не понятен сам процесс составления изомеров, объяснить этот самый процесс-не значит выполнить за меня всё задания. Не можешь корректно ответить на вопрос-не суй свой нос!!!
Изомеры гептана (названия и структурные формулы)
Задание: составить 9 изомеров гептана С7Н16
Чтобы выполнить задание запишите названия изомеров гептана и их структурные формулы так, как это показано ниже.
Ответы по химии.