Радиоактивный
ряд
– это последовательность радионуклидов,
образующихся в результате
радиоактивного распада каждого
предыдущего радионуклида с образованием
в итоге стабильного элемента.
Наиболее долгоживущие изотопы называются
начальными
для каждого из радиоактивных рядов.
Существует
4
радиоактивных
ряда
и,
соответственно,
4 их
родоначальника:
1.
ториевый
ряд:
наиболее долгоживущий изотоп – торий-232
(Th-232),
Т1/2
=
1.4 × 1010
лет;
2.:
урановый
ряд
по наиболее долгоживущему изотопу –
урану-238 (U-238),
Т1/2
=
4.5 × 109
лет;
3.
урановый
ряд
по наиболее долгоживущему изотопу –
урану-235 (U-235),
T1/2
=
7 × 108
лет;
4.
нептуниевый
ряд:
наиболее долгоживущий изотоп – нептуний-237
(Np-237),
Т1/2
=
2.2 × 106
лет.
Из
сравнения периодов полураспада
родоначальников радиоактивных рядов
со временем существования Земли видно,
что в настоящий момент Th-232
почти весь сохранился, U-238
распался лишь частично, а U-235
распался большей частью (т.е., в настоящий
момент в земной коре U-238
больше, чем U-235
в 140 раз), изотоп Np-237
распался практически весь. В процессе
превращения этих элементов в качестве
промежуточных продуктов распада
образуются радиоактивные изотопы радия,
радона, полония, висмута, свинца, которые
формируют значительную дозу облучения
человека.
Радионуклиды,
не входящие в радиоактивные ряды
Эта
группа в основном состоит из 11 долгоживущих
радионуклидов (период полураспада от
107
до 1015
лет). Из них наибольший вклад в формирование
эффективной дозы вносят К-40 и Rb-87.
Калий-40
(К-40) занимает 2 место как источник
излучений, обусловливающих природный
радиоактивный фон. Ядро К-40 претерпевает
бета-распад, T1/2
– 1,32 × 109
лет. К-40 является бета- и гамма-источником
облучения биоты. В природе К-40 всегда
сопутствует стабильному К-39 (доля К-40 –
около 0,01%), формируя годовую эффективную
дозу за счет внешнего облучения 0,12 мЗв
и 0,18 мЗв за счет внутреннего облучения.
К-40
часто обусловливает активность
поверхностного слоя почвы, равную 1-2
Ки/км2.
Активность растительного покрова Земли
по К-40 равна (0,5-1) ×10-8
Ки/кг сырого веса. Активность пищевых
продуктов по К-40 составляет 10-9
Ки/кг сырых продуктов. Наибольшая
активность К-40 регистрируется в клюкве,
орехах, фасоли, картофеле.
Из
почвы К-40 поступает в растения, а затем,
с пищей – в организм животных и человека.
Радиоактивные изотопы калия поступают
в организм, главным образом, с пищей и
водой. Калий практически полностью
всасывается из желудочно-кишечного
тракта и равномерно распределяется в
органах и тканях. Тб
калия
составляет 58 суток (Тб
– время, в течение которого из организма
выводится половина введенного вещества).
Суточная
потребность человека в калии составляет
около 3 г, т.е. в организм может поступать
и значительное количество К-40. Например,
средняя активность К-40 в красном костном
мозге человека оценивается в 121 Бк/кг
(содержание калия в красном костном
мозге – 4 г/кг), в скелетных мышцах – 90
Бк/кг (содержание калия – 3 г/кг).
Рубидий-87
(Rb-87)
входит в состав продуктов деления урана
(до 6%). Ядро Rb-87
претерпевает β-превращение,
T1/2
– 4,8 × 1010
г. При пероральном поступлениипрактически
полностью всасывается из желудочно-кишечного
тракта и равномерно распределяется в
органах и тканях. Тб
из мягких тканей человека составляет
44 (от 32 до 57) суток.
Радионуклиды радиоактивных рядов,
формирующие основную дозовую нагрузку
на организм человека
Наибольшее
значение в формировании дозы внутреннего
облучения имеют радий-226, радон-222,
полоний-210, свинец-210.
Радий-226
(Ra-226)
широко распространен в природе. Ra-226
претерпевает альфа-распад с образованием
Rn-222,
T1/2
– 1620 лет. Может поступать в организм
через желудочно-кишечный тракт
(коэффициент всасывания в желудочно-кишечном
тракте – 0,2), органы дыхания и неповрежденную
кожу. Его источником для человека в
основном служат зерновые культуры и
хлеб, куриные яйца. Среднее поступление
с жидкостями и пищей – 2,3 × 10-12
г/сут. Радий, независимо от химической
формы соединения при поступлении,
депонируется в костной ткани, из которой
выводится с T6,
равным
17,13 лет.
Полоний-210
(Po-210)
подвергается альфа-распаду с образованием
стабильного Pb-206,
T1/2
– 138,38 сут., коэффициент всасывания из
желудочно-кишечного тракта – 0,2. В среднем
за сутки в организм человека с пищей
поступает 0,037-0,37 Бк Po-210
(т.н. нормальное поступление). В регионах,
где человек потребляет пищу морского
происхождения, а также питается мясом
северных оленей, наблюдается повышенное
поступление Po-210
в организм – 2,2-11,1 Бк/сут (например, в
диете японцев содержание Pb-210
в 11-18 раз превышает среднестатистические
цифры). Курение увеличивает поступление
Po-210
в организм человека: в легких курильщика,
выкуривающего 10 – 60 сигарет в сутки,
создаются концентрации Po-210
1,66 мБк/г, что в 2-9 раз выше, чем у некурящих,
и соответствует дозам 0,027-0,04 мГр/год. Из
организма человека Po-210
выводится с Тб,
равным приблизительно 80 сут.
Свинец-210
(Pb-210)
подвергается бета-превращению (электронный
распад) с образованием Bi-210,
распадается с Т1/2
– 22,3 года, коэффициент всасывания в
желудочно-кишечном тракте – 0,2 (для всех
соединений). Элемент остеотропен, связан
с обменом кальция и фосфора. Из организма
(в том числе и из костной ткани) выводится
с Тб,
равным 12 – 10000 сут. Pb-210
– один из источников появления в организме
Po-210.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Радиоакти́вные ряды́ (семейства) — группы изотопов, связанных друг с другом цепочкой радиоактивных превращений.
Выделяют три естественных радиоактивных ряда и один искусственный.
Естественные ряды:
- ряд тория (4n) — начинается с нуклида Th-232;
- ряд радия (4n + 2) — начинается с U-238;
- ряд актиния (4n + 3) — начинается с U-235.
Искусственный ряд (вымерший в природе):
- ряд нептуния (4n + 1) — начинается с Np-237.
После альфа- и бета-радиоактивных превращений ряды заканчиваются образованием стабильных изотопов.
Активности тех членов ряда, путь к которым от родительского изотопа не проходит через ветвления, при наступлении векового равновесия равны. Так, активность радия-224 в ториевых образцах через несколько десятков лет после изготовления становится практически равной активности тория-232, тогда как активность таллия-208 (образующегося в этом же ряду при α-распаде висмута-212 с коэффициентом ветвления 0,3594) стремится к 35,94 % от активности тория-232. Характерное время прихода к вековому равновесию в ряде равно нескольким периодам полураспада наиболее долгоживущего (среди дочерних) члена семейства. Вековое равновесие в ряду тория наступает достаточно быстро, за десятки лет, так как периоды полураспадов всех членов ряда (кроме родительского нуклида) не превышают нескольких лет (максимальный период полураспада T1/2 = 5,7 лет — у радия-228). В ряду урана-235 равновесие восстанавливается примерно за сто тысяч лет (наиболее долгоживущий дочерний член ряда — протактиний-231, T1/2 = 32 760 лет), в ряду урана-238 — примерно за миллион лет (определяется ураном-234, T1/2 = 245 500 лет).
Типы рядов[править | править код]
Тремя наиболее распространёнными видами радиоактивного распада являются α-распад, β±-распад и изомерный переход. В результате альфа-распада массовое число ядер всегда уменьшается на четыре, тогда как в результате бета-распадов и изомерных переходов массовое число ядра не меняется. Это приводит к тому, что все нуклиды делятся на четыре группы (ряда) в зависимости от остатка целочисленного деления массового числа нуклида на четыре (то есть родительский нуклид и его дочерний нуклид, образовавшийся в результате альфа-распада, будут принадлежать к одной группе). Во всех рядах происходит образование гелия (из альфа-частиц).
Три основных радиоактивных ряда, наблюдающихся в природе, обычно называются рядом тория, рядом радия и рядом актиния. Каждый из этих рядов заканчивается образованием различных стабильных изотопов свинца. Массовый номер каждого из нуклидов в этих рядах может быть представлен в виде A = 4n, A = 4n + 2 и A = 4n + 3, соответственно.
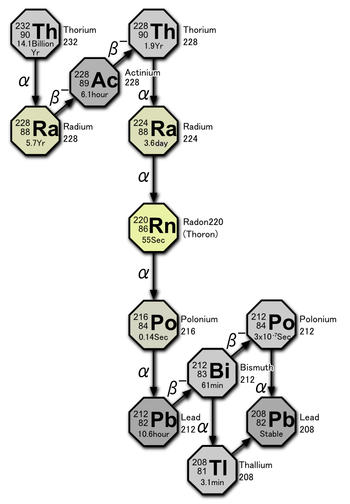
Ряд тория[править | править код]
Радиоактивный ряд нуклидов с массовым числом, представимым в виде 4n, называется рядом тория. Ряд начинается с встречающегося в природе тория-232 и завершается образованием стабильного свинца-208.
| Нуклид | Историческое обозначение | Историческое название | Вид распада | Период полураспада | Выделяемая энергия, МэВ | Продукт распада |
|---|---|---|---|---|---|---|
| 252Cf | α | 2,645 года | 6,1181 | 248Cm | ||
| 248Cm | α | 3,4⋅105 лет | 6,260 | 244Pu | ||
| 244Pu | α | 8⋅107 лет | 4,589 | 240U | ||
| 240U | β− | 14,1 ч | 0,39 | 240Np | ||
| 240Np | β− | 1,032 ч | 2,2 | 240Pu | ||
| 240Pu | α | 6561 год | 5,1683 | 236U | ||
| 236U | α | 2,3⋅107 лет | 4,494 | 232Th | ||
| 232Th | Th | Торий | α | 1,405⋅1010 лет | 4,081 | 228Ra |
| 228Ra | MsTh1 | Мезоторий 1 | β− | 5,75 лет | 0,046 | 228Ac |
| 228Ac | MsTh2 | Мезоторий 2 | β− | 6,15 ч | 2,124 | 228Th |
| 228Th | RdTh | Радиоторий | α | 1,9116 года | 5,520 | 224Ra |
| 224Ra | ThX | Торий X | α | 3,66 дня | 5,789 | 220Rn |
| 220Rn | Tn (ThEm) | Торон (эманация тория) | α | 55,6 с | 6,404 | 216Po |
| 216Po | ThA | Торий A | α | 0,145 с | 6,906 | 212Pb |
| 212Pb | ThB | Торий B | β− | 10,64 ч | 0,570 | 212Bi |
| 212Bi | ThC | Торий C | β− 64,06 % α 35,94 % |
60,55 мин | 2,252 6,208 |
212Po 208Tl |
| 212Po | ThC’ | Торий C’ | α | 299 нс | 8,955 | 208Pb |
| 208Tl | ThC” | Торий C” | β− | 3,053 мин | 4,999 | 208Pb |
| 208Pb | ThD | Торий D, ториевый свинец | стабильный |
Ряд нептуния[править | править код]
Радиоактивный ряд нуклидов с массовым числом, представимым в виде 4n + 1, называется рядом нептуния. Ряд начинается с нептуния-237 и завершается образованием стабильного таллия-205. В этой серии только два нуклида встречаются в природе — чрезвычайно долгоживущий висмут-209 и стабильный таллий-205. Однако с развитием ядерных технологий в результате ядерных испытаний и радиационных аварий в окружающую среду попали радионуклиды, такие как плутоний-241 и америций-241, которые также могут быть отнесены по массовому числу к началу ряда нептуния. Так как этот ряд был изучен недавно, его изотопы не имеют исторических названий. Слабая альфа-активность висмута-209 была обнаружена лишь в 2003 году, поэтому в более ранних работах он называется конечным (и единственным сохранившимся в природе) нуклидом ряда.
| Нуклид | Вид распада | Период полураспада | Выделяемая энергия, МэВ | Продукт распада |
|---|---|---|---|---|
| 249Cf | α | 351 год | 5,813 + 0,388 | 245Cm |
| 245Cm | α | 8500 лет | 5,362 + 0,175 | 241Pu |
| 241Pu | β− | 14,4 года | 0,021 | 241Am |
| 241Am | α | 432,7 года | 5,638 | 237Np |
| 237Np | α | 2,14⋅106 лет | 4,959 | 233Pa |
| 233Pa | β− | 27,0 д | 0,571 | 233U |
| 233U | α | 1,592⋅105 лет | 4,909 | 229Th |
| 229Th | α | 7340 лет | 5,168 | 225Ra |
| 225Ra | β− | 14,9 д | 0,36 | 225Ac |
| 225Ac | α | 10,0 д | 5,935 | 221Fr |
| 221Fr | α | 4,8 мин | 6,3 | 217At |
| 217At | α | 32 мс | 7,0 | 213Bi |
| 213Bi | β− 97,80 % α 2,20 % |
46,5 мин | 1,423 5,87 |
213Po 209Tl |
| 213Po | α | 3,72 мкс | 8,536 | 209Pb |
| 209Tl | β− | 2,2 мин | 3,99 | 209Pb |
| 209Pb | β− | 3,25 ч | 0,644 | 209Bi |
| 209Bi | α | 1,9⋅1019 лет | 3,14 | 205Tl |
| 205Tl | стабильный |
Ряд радия[править | править код]
Радиоактивный ряд нуклидов с массовым числом, представимым в виде 4n + 2, называется рядом радия (иногда называют рядом урана или урана-радия). Ряд начинается с урана-238 (встречается в природе) и завершается образованием стабильного свинца-206.
| Нуклид | Историческое обозначение | Историческое название | Вид распада | Период полураспада | Выделяемая энергия, МэВ | Продукт распада |
|---|---|---|---|---|---|---|
| 238U | UI | Уран I | α | 4,468⋅109 лет | 4,270 | 234Th |
| 234Th | UX1 | Уран X1 | β− | 24,10 сут | 0,273 | 234Pam |
| 234Pam | UX2 | Уран X2, бревий | β− 99,84 % изомерный переход 0,16 % |
1,16 мин | 2,271 0,074 |
234U 234Pa |
| 234Pa | UZ | Уран Z | β− | 6,70 ч | 2,197 | 234U |
| 234U | UII | Уран II | α | 245500 лет | 4,859 | 230Th |
| 230Th | Io | Ионий | α | 75380 лет | 4,770 | 226Ra |
| 226Ra | Ra | Радий | α | 1602 года | 4,871 | 222Rn |
| 222Rn | Rn (RaEm) | Радон (эманация радия) | α | 3,8235 д | 5,590 | 218Po |
| 218Po | RaA | Радий A | α 99,98 % β− 0,02 % |
3,10 мин | 6,115 0,265 |
214Pb 218At |
| 218At | RaAt | Астат | α 99,90 % β− 0,10 % |
1,5 с | 6,874 2,883 |
214Bi 218Rn |
| 218Rn | AtEm | эманация астата | α | 35 мс | 7,263 | 214Po |
| 214Pb | RaB | Радий B | β− | 26,8 мин | 1,024 | 214Bi |
| 214Bi | RaC | Радий C | β− 99,98 % α 0,02 % |
19,9 мин | 3,272 5,617 |
214Po 210Tl |
| 214Po | RaC’ | Радий C’ | α | 0,1643 мс | 7,883 | 210Pb |
| 210Tl | RaC” | Радий C” | β− | 1,30 мин | 5,484 | 210Pb |
| 210Pb | RaD | Радий D | β− | 22,3 года | 0,064 | 210Bi |
| 210Bi | RaE | Радий E | β− 99,99987 % α 0,00013 % |
5,013 сут | 1,426 5,982 |
210Po 206Tl |
| 210Po | RaF | Радий F, полоний | α | 138,376 сут | 5,407 | 206Pb |
| 206Tl | RaE” | Радий E” | β− | 4,199 мин | 1,533 | 206Pb |
| 206Pb | RaG | Радий G, урановый свинец | – | стабильный | – | – |
Ряд актиния[править | править код]
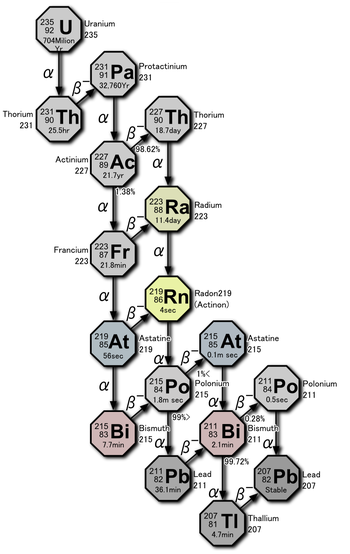
Радиоактивный ряд нуклидов с массовым числом, представимым в виде 4n + 3, называется рядом актиния или урана-актиния. Ряд начинается с урана-235 и завершается образованием стабильного свинца-207.
| Нуклид | Историческое обозначение | Историческое название | Вид распада | Период полураспада | Выделяемая энергия, МэВ | Продукт распада |
|---|---|---|---|---|---|---|
| 239Pu | α | 2,41⋅104 лет | 5,244 | 235U | ||
| 235U | AcU | Актиноуран | α | 7,04⋅108 лет | 4,678 | 231Th |
| 231Th | UY | Уран Y | β− | 25,52 ч | 0,391 | 231Pa |
| 231Pa | Pa | Протактиний | α | 32760 лет | 5,150 | 227Ac |
| 227Ac | Ac | Актиний | β− 98,62 % α 1,38 % |
21,772 года | 0,045 5,042 |
227Th 223Fr |
| 227Th | RdAc | Радиоактиний | α | 18,68 сут | 6,147 | 223Ra |
| 223Fr | AcK | Актиний K | β− 99,994 % α 0,006 % |
22,00 мин | 1,149 5,340 |
223Ra 219At |
| 223Ra | AcX | Актиний X | α | 11,43 сут | 5,979 | 219Rn |
| 219At | AcAtI | Актиноастат I | α 97,00 % β− 3,00 % |
56 с | 6,275 1,700 |
215Bi 219Rn |
| 219Rn | An (AcEm) | Актинон (эманация актиния) | α | 3,96 с | 6,946 | 215Po |
| 215Bi | β− | 7,6 мин | 2,250 | 215Po | ||
| 215Po | AcA | Актиний A | α 99,99977 % β− 0,00023 % |
1,781 мс | 7,527 0,715 |
211Pb 215At |
| 215At | AcAtII | Актиноастат II | α | 0,1 мс | 8,178 | 211Bi |
| 211Pb | AcB | Актиний B | β− | 36,1 мин | 1,367 | 211Bi |
| 211Bi | AcC | Актиний C | α 99,724 % β− 0,276 % |
2,14 мин | 6,751 0,575 |
207Tl 211Po |
| 211Po | AcC’ | Актиний C’ | α | 516 мс | 7,595 | 207Pb |
| 207Tl | AcC” | Актиний C” | β− | 4,77 мин | 1,418 | 207Pb |
| 207Pb | AcD | Актиний D, актиниевый свинец | стабильный |
См. также[править | править код]
- Атомное ядро
- Радиоактивный распад
- Вековое равновесие
Литература[править | править код]
- Lederer C. M., Hollander J. M., Perlman I. Table of Isotopes (англ.). — 6th Ed. — New York: John Wiley & Sons, 1968.
- Decay chains
- National Nuclear Data Center
РАДИОАКТИВНЫЕ РЯДЫ
РАДИОАКТИВНЫЕ РЯДЫ
(радиоактивные семейства), группы генетически связанных радионуклидов, в к-рых
каждый последующий возникает в результате а-или р-распада предыдущего (см. Радиоактивность).
Каждый радиоактивный ряд имеет родоначальника – радионуклид с наибольшим для данного
ряда периодом полураспада Т1/2. Т. к. при испускании ядром
a-частицы его массовое число уменьшается на 4 единицы, а при испускании
b–-частицы остается неизменным, в каждом радиоактивном ряду массовые числа
всех радионуклидов могут различаться на число, кратное 4. Если значения массовых
чисел членов данного радиоактивного ряда делятся на 4 без остатка, то такие массовые числа
можно выразить общей ф-лой 4n (n = 58 или 59); в тех случаях,
когда при делении массового числа ядра на 4 в остатке будет 1, 2 или 3, общие
ф-лы для массовых чисел членов таких радиоактивных рядов можно записать как 4n + 1,
4n + 2 или 4n + 3. В соответствии с этими ф-лами различают 4 радиоактивных ряда, родоначальниками к-рых являются 232Th (ряд 4n), 237Np
(ряд 4n + 1), 238U (ряд 4n + 2) и 235U (ряд
4n + 3). Обычно их называют соотв. рядами тория, нептуния, урана-238
и ура-на-235. Ряд урана-238 часто наз. также рядом урана-радия (226Rа-наиб.
устойчивый радионуклид радия), а ряд урана-235-рядом актиноурана (первонач.
название 235U).
В природе существуют ряды
тория, урана-радия и актиноурана (т.наз. естественные радиоактивные ряды). Это связано с тем,
что периоды полураспада 232Th (1,405·1010 лет), 238U
(4,468·109 лет) и 235U (7,038·108 лет) соизмеримы
с возрастом Земли. Заканчиваются естественные радиоактивные ряды изотопами 208Рb,
206Рb и 207Рb, содержание к-рых в земной коре медленно
возрастает. Для 237Np T1/2 = 2,14·106
лет, поэтому членов его радиоактивного ряда в природе нет все они полностью распались. В 40-50-х
гг. 20 в. получены искусственно члены этого радиоактивного ряда (см. Ядерные реакции).
Завершает радиоактивный ряд нептуния стабильный нуклид 209Bi.
Каждый радиоактивный ряд содержит как
долгоживущие, так и коротко-живущие радионуклиды, для к-рых T1/2
составляют минуты, секунды и доли секунды. Как бы ни был мал период полураспада
радионуклида – члена естественного радиоактивного ряда, он обязательно присутствует в природе.
Связано это с тем, что в каждом радиоактивном ряду с течением времени устанавливается т. наз.
вековое равновесие. Время достижения векового равновесия равно ~10 Т1/2
самого долгоживущего члена ряда (кроме родоначальника ряда). При вековом равновесии
числа атомов N’ и N: любых двух членов ряда и их периоды
полураспада Т’1/2 и Т:1/2 связаны соотношением:
N’ Т’1/2 = = N: T:1/2.
Поэтому чем меньше Т1/2 к.-л. промежут. члена ряда, тем
ниже его содержание в земной коре. Напр., на 1 т U в земной коре приходится
ок. 0,34 г 226Ra (T1/2 1600 лет) и всего 1,4·10-9
г 218Ро (T1/2 3,05 мин). Содержание промежут. членов
радиоактивных рядов в земной коре медленно снижается по мере распада родоначальника радиоактивного ряда,
но за человеческую жизнь практически не изменяется. Благодаря вековому равновесию
в земной коре постоянно содержатся нуклиды таких неустойчивых элементов, как
Ро, At, Rn, Fr, Ra, Ac и Pa.
Мн. члены естественных
радиоактивных рядов имеют исторически сложившиеся названия и символы. Так, 230Th
наз. ионием (символ Io), 228Th-радиоторием (RdTh), 227Тh-радиоакти-нием
(RdAc), 220Rn-Topoном (Tn), 219Rn-aктионом (An), 214Ро-радием-це-штрих
(RaC), 228Ra-мезото-рием-один (MsTh1). Эти назв. связаны
с тем, что в прошлом каждый вновь открытый член радиоактивного ряда рассматривался как новый
элемент (радиоэлемент; см. Радиохимия). Лишь с обнаружением изотопии
стало ясно, что члены радиоактивных рядов – изотопы соответствующих хим. элементов.
Нек-рые члены радиоактивных рядов распадаются
не по одному пути (a-или b-распад), а по двум (т. наз. вилка). Напр.,
член ряда актиноурана 227Ас в 988 случаях из 1000 претерпевает b–
-распад, а в 12 случаях-a-распад.
Исследования радиоактивных рядов имели
важное значение для развития учения о радиоактивности, обнаружения новых радиоактивных
элементов и их изотопов.
Лит. см. при статьях
Радиоактивность, Радиохимия.
С. С. Бердоносов.
Изотопы. Радиоактивные ряды. Искусственная радиоактивность
В данном параграфе использован текст из книги К.Хоффмана «Можно ли сделать золото»
20 лет исследований явления радиоактивности привели к открытию большого числа радиоактивных элементов, которые можно было подразделить на три ряда естественного радиоактивного распада: ряд урана — радия (продукты распада урана-238), ряд урана — актиния («актиноураном» называли изотоп урана с атомной массой 235) и ряд тория. Со времени существования Земли начальные представители этих рядов превращались во множество радиоактивных изотопов. Среди них были изотопы нескольких новых элементов.
Причем количество новых элементов всё увеличивалось, и скоро превысило количество «пустых» клеток в таблице Менделеева. Так, на вакантное место, отведенное для инертного газа, претендовали аж три элемента: радон (газообразный продукт распада радия), торон (газообразный продукт распада тория) и актинон (газообразный продукт распада актиния). Аналогичная ситуация была и с полонием, радием, актинием, торием, ураном — на их места в таблице Менделеева претендовали по нескольку элементов с совершенно одинаковыми химическими свойствами, но с разными радиоактивными свойствами и разными массами (тогда считалось, что индивидуальной характеристикой химического элемента является его масса). После открытия строения атома выяснилось, что определяющей характеристикой химического элемента является заряд его атомного ядра и количество электронов, от которого зависят и его химические свойства. Что же касается массы, то, как выяснилось, один химический элемент может иметь несколько разновидностей атомов с различными атомными массами. Эти разновидности были названы «изотопами». Это слово происходит от греческой фразы «одинаковое место» — то есть речь шла о разных видах атомов, занимающих одно и то же место в таблице Менделеева. Поэтому теперь для обозначения конкретного изотопа употребляют название элемента и после него — число, означающее атомную массу (например, уран-238, уран-235, радий-226, радон-222 и др.). Сокращенно их могут обозначать и так: 23892U. Вместо слова изотоп употребляют еще более точное понятие «нуклид» (что означает — «вид ядра»)
Прошло несколько лет упорных исследований, пока было обнаружено, что соответствующие конечные продукты радиоактивных рядов, которые вначале называли радий G, актиний D и торий D, являются не чем иным, как свинцом. Однако был ли это тот же свинец, который получают из руды на предприятиях и применяют в промышленности и технике? Появившиеся сомнения рассеялись лишь тогда, когда определили его атомную массу, а затем, с помощью масс-спектрографических исследований, подтвердили, что речь идет о различных изотопах свинца: радий G (свинец ряда урана) — свинец-206 актиний D (свинец ряда актиния) — свинец-207 торий D (свинец ряда тория) — свинец-208
Свинец естественного происхождения состоит, как и большинство элементов, из смеси нескольких изотопов. Всего только 20 химических элементов являются моноизотопными, как золото, для которого в природе существует только один устойчивый изотоп (197Au). Поэтому золото обладает относительной атомной массой, численно равной 197,0.
Естественный свинец состоит из устойчивых изотопов: 204 (1,4%), 206 (26,3%), 207 (20,8%) и 208 (51,5%) . Поэтому относительная атомная масса свинца вычисляется из различных вкладов отдельных изотопов и в среднем дает значение 207,2. В результате непрерывных радиоактивных превращений содержание свинца на Земле постоянно увеличивается. Сейчас на нашей планете свинца больше, чем было в момент ее образования. Путем измерения соотношения урана и свинца в горных породах определяют их возраст. Так определили возраст Земли, который оказался равным 4,6 миллиарда лет.
Начальный представитель ряда урана — природный изотоп 238U — распадается с периодом полураспада около 4,5 миллиардов лет. Поэтом образуются, помимо других, элементы 88 (радий), 86 (радон-эманация радия), 84 (полоний) и, наконец, 82 (свинец).
Естественный распад урана, протекающий с постоянным выделением энергии, нельзя искусственно ускорить. Должно пройти более 60 миллионов лет, чтобы из 1 кг урана в конце концов образовалось 10 г свинца. Когда физики-атомщики попытались форсировать это превращение, чтобы высвободить, быть может, огромные количества энергии в кратчайшее время, они, как известно, потерпели неудачу.
Значительно позднее, после открытия рядов радиоактивного распада, стало ясно, что и не будучи алхимиком, надо признать существование естественного распада радиоактивных элементов.
Как известно, радиоактивный распад в каждом из этих рядов бывает только двух типов — либо альфа-распад, когда заряд ядра уменьшается на две единицы, а атомная масса — на четыре единицы, либо же бета-распад, при котором заряд ядра увеличивается на единицу, а атомная масса (суммарное число протонов и нейтронов в ядре) не меняется. Как легко видеть, во время цепочки радиоактивных распадов атомная масса всех звеньев цепи может различаться на 4 единицы либо на число, кратное четырем. Поэтому, как легко понять, должно быть не три, а четыре радиоактивных ряда.
Первый — это ряд, в котором атомная масса всех продуктов распада делится на 4 (или, как его называют, 4n-ряд). Его родоначальником является торий-232, а конечным продуктом — свинец-208 (в боковой цепи радиоактивного распада может получиться и свинец-204)
Второй — это ряд, атомная масса элементов которого делится на 4 с остатком 2 (4n+2 — ряд). Его родоначальником является уран-238, в этом ряду находятся такие известные изотопы, как радий-226 и радон-222, а конечным продуктом его является свинец-206.
Третий — это ряд, атомная масса которых делится на 4 с остатком 3 (4n+3 — ряд). Его родоначальником является уран-235 («актиноуран»), а конечным продуктом распада — свинец-207.
Сложнее было с радиоактивным рядом, массы элементов которого делятся на 4 с остатком 1 (4n+1 — ряд). Был известен его конечный продукт — висмут-209 — однако ни один из членов этого ряда, ни его «родоначальник» так и не были обнаружены ни в одном из экспериментов. Вопрос решился после открытия трансурановых элементов. Родоначальником 4n+1 — ряда является нептуний-237. Он был на Земле во время ее образования, но за время существования Земли успел распасться.
Таким образом, есть 4 радиоактивных ряда, которые через цепь альфа- и бета- распадов превращаются в стабильные изотопы.
После открытия в конце 1990-х годов ХХ века элементов из так называемого «острова относительной стабильности» (элементы с атомными номерами от 110 до 118) обнаружились новые 4 радиоактивных ряда. Их условно называют «286», «287», «288» и «289» — по атомным массам входящих в эти ряды открытых и достаточно хорошо изученных элемента с атомным номером 114. После цепи альфа-распадов эти элементы превращаются в неустойчивые элементы с атомными номерами 104-109, и, распадаются путем спонтанного деления на элементы из середины таблицы Менделеева.
В начале 30-х годов казалось, что любимое занятие многих исследователей атома — поиски новых продуктов распада — уже не может дать ничего нового. Такие исследования проводились с чисто криминалистическим чутьем. Теперь ряд естественных радиоактивных элементов оказался полным. Ничего не меняло и то обстоятельство, что существование первого члена ряда актиния, актиноурана было до сих пор лишь гипотетическим. Исследователям атома и не снилось, что можно будет отыскать еще неизвестные радиоактивные элементы.
В это время между специалистами возникли очень интересные споры, а именно по поводу элемента с порядковым номером 93. Такого элемента вообще не должно было существовать на Земле. Уран, после того как он был помещен Менделеевым в периодическую систему, был признан самым последним из 92-х элементов. Так полагали все.
Однако некоторые ученые не могли расстаться с мыслью, что число элементов, возможно, превышает 92. Когда-то, в 1922 году, Нильс Бор размышлял о возможности существования благородного газа с порядковым номером 118 — как это вытекало из его теории спектров и строения атома. Многим специалистам такие представления казались пустым теоретизированием.
В апреле 1934 года Ида Ноддак большим сообщением «Периодическая система элементов и ее пустые клетки» пробудила новый интерес к этой проблеме. В докладе, который был опубликован в журнале «Ангевандте хеми» 19 мая 1934 года, она ставила провокационный вопрос: почему периодическая система вдруг обрывается после урана? В составленной ею таблице она демонстративно оставляла незанятые места от 93 до 96 для элементов, которые еще предстояло открыть. Такой шаг она обосновывала весьма оптимистично: «Нам кажется возможным, что элементы, следующие за ураном, так называемые трансураны, с возрастанием порядкового номера становятся все менее жизнеспособными, а потому все более редкими. Однако стоящие за ураном четные элементы 94 и 96 могли бы быть получены сегодняшними средствами…; следует ожидать, что как раз в этом месте системы появятся некоторые неожиданности».
Действительно, такие неожиданности не заставили себя долго ждать. Уже в начале 1934 года Ирэн Кюри, дочь Марии Кюри, вместе со своим супругом. Фредериком Жолио, сделала открытие, поразившее специалистов. Им удалось обнаружить «новый тип радиоактивности». Так называлось их сообщение в «Отчетах Парижской академии наук» от 15 января. Что же крылось за этим заголовком?
Оба исследователя бомбардировали алюминиевую фольгу альфа-частицами; при этом обнаружилась отчетливая радиоактивность алюминия, которая сохранялась также после удаления источника излучения. Такой эффект никто никогда не наблюдал. Отдельные атомы алюминия после воздействия альфа-частиц превратились в радиоактивный фосфор (Р*). Этим новым методом можно было искусственно вызвать радиоактивность. То, что Стефания Марацинеану ошибочно искала на свинцовых крышах, стало фактом — для легких элементов — пока только для них — можно искусственно индуцировать радиоактивность:
27Al + 4He = 30P + n
Радиоактивный фосфор распадается до устойчивого изотопа кремния с выделением позитрона:
30P = 30Si + e+
Исследователям атома, этим «алхимикам XX века», вновь удалось осуществить поразительное превращение элементов. Искусственным путем принудить вещества к радиоактивному распаду — это было, безусловно, новым большим шагом на пути к гигантским запасам энергии атомного ядра.
Энрико Ферми из Физического института Римского университета, новая звезда в международном семействе исследователей атома, заинтересовался открытием искусственной радиоактивности и начал систематически обстреливать нейтронами один элемент за другим. Молодой физик надеялся, что таким путем, а не только с помощью альфа-частиц ему удастся вызвать искусственную радиоактивность.
Ферми и его коллеги д’Агостино, Сегре, Амальди и Розетти подошли к этим опытам строго методически. Они начали с элемента 1, водорода, и подвергли его воздействию потока нейтронов. После того как был убран источник нейтронов — запаянная трубка с эманацией радия и порошком бериллия, ученые испытали облученный элемент на радиоактивность. Для этого был использован счетчик их собственной конструкции, работавший по принципу счетчика Гейгера — Мюллера, известного с 1928 года. Ферми вбил себе в голову испытать все элементы периодической системы вплоть до урана. Откуда же взять нужные вещества?
Физикам потребовалось некоторое время для того, чтобы обыскать запылившиеся полки институтов, химических магазинов и аптек и найти все, что им требовалось.
Многие сотрудники Римского университета находили поведение молодых физиков очень забавным: Ферми и его друзья по окончании облучения мчались, как одержимые, по длинным коридорам института, чтобы испытать свои препараты в помещении, не зараженном радиоактивностью. Ведь могло так случиться, что образовался короткоживущий радиоактивный элемент с периодом полураспада в несколько секунд.
Потом обычно можно было видеть, как они медленно возвращались с разочарованными лицами. Для первых восьми элементов физики не смогли обнаружить никакой искусственной радиоактивности. Однако на девятом элементе, фторе, счетчик вдруг защелкал. Вскоре итальянцы установили, что облучение нейтронами активизирует многие элементы. Чаще всего последние излучали бета-лучи и превращались при этом в атомы следующего элемента.
Ферми открыл «радиоактивность, индуцированную бомбардировкой нейтронами». Так назвал он статью, написанную 10 апреля и опубликованную в мае 1934 года в журнале «Нейчур»,
Источник
- http://element114.narod.ru/Education/chem2-53.html
Радиоактивные ряды
Выяснение сущности радиоактивных явлений привело к замечательному выводу, что один элемент путем распада может превратиться в другой. Если этот второй элемент радиоактивен, то, распадаясь, он превращается в третий элемент, и так далее до тех пор, пока не получится элемент, не способный разрушаться. Ряд элементов, образующихся подобным образом один из другого, называется радиоактивным рядом. Примером может служить ряд элементов, которые являются продуктами превращения радия. Как известно, при распаде радия получается радон — радиоактивный элемент, который, в свою очередь, распадается с образованием радия А. Последний тоже радиоактивен и, подвергаясь дальнейшему распаду, образует один за другим ряд новых радиоактивных элементов — радий В, радий С и т. д. Конечным продуктом этого распада является радий G, представляющий собой вполне устойчивый элемент, по химическим свойствам тождественный с обыкновенным свинцом.
Весь процесс последовательных превращений радия схематически представлен на рис. 50, где указаны атомные веса элементов, периоды их полураспада и испускаемые при каждом превращении лучи.
Рис. 50. Схема превращений радия
Кроме радия, подобным же образом распадаются уран, торий и актиний, обладающие радиоактивными свойствами. Изучение этих превращений показало, что сам радий является лишь промежуточным звеном в длинной цепи продуктов превращения урана, из которого он образуется согласно схеме, изображенной на рис. 51.
В настоящее время известны три ряда природных радиоактивных элементов; первый начинается с урана, ат. вес. 238; второй— с тория, ат. вес 232; третий — с изотопа урана — актино-урана, ат. вес 235. Эти три ряда получили название рядов распада урана, тория и актиния: первые два — по начальным членам ряда, а третий — по стоящему в ряду элементу актинию. Конечным продуктом превращений во всех трех рядах является свинец. Кроме того, в последние годы открыт еще четвертый радиоактивный ряд, начинающийся с искусственно получаемого элемента нептуния и заканчивающийся висмутом.
Присутствие в урановых рудах свинца позволяет сделать интересный вывод относительно возраста нашей планеты. Зная периоды полураспада радиоактивных элементов в ряду урана, нетрудно подсчитать, сколько времени нужно для превращения определенной части урана в свинец. Содержание свинца в урановых рудах составляет в среднем 20%. Подсчитывая отсюда время его образования из руды, получим 1500 млн. лет. Но так как сама урановая руда не может быть старше земной коры, то это же число показывает наименьший возраст земли.
57 58 59
Вы читаете, статья на тему Радиоактивные ряды
Понравилась статья поделись ей