При
графическом изображении формул веществ указывается последовательность расположения
атомов в молекуле с помощью, так называемых валентных штрихов (термин
«валентный штрих» предложил в 1858 г. А. Купер для обозначения химических сил
сцепления атомов), иначе называемых валентной чертой (каждая валентная черта,
или валентный штрих, эквивалентны одной паре электронов в ковалентных
соединениях или одному электрону, участвующему в образовании ионной связи).
Часто неправильно принимают графическое изображение формул за структурные
формулы, приемлемые только для соединений с ковалентной связью и показывающие
взаимное расположение атомов в молекуле.
Так, формула Nа—СL не является структурной, так как NаСI — ионное соединение, в его
кристаллической решетке отсутствуют молекулы (молекулы NаСL существуют только в газовой фазе).
В узлах кристаллической решетки NаСI
находятся ионы, причем каждый Nа+
окружен шестью хлорид-ионами. Это графическое изображение формулы вещества,
показывающее, что ионы натрия не связаны между собой, а с хлорид-ионами. Не
соединяются между собой и хлорид-ионы, они соединены с ионами натрия.
Покажем
это на примерах. Мысленно предварительно «разбиваем» лист бумаги на несколько
столбцов и выполняем действия согласно алгоритмам по графическому изображению
формул оксидов, оснований, кислот, солей в следующем порядке.
Графическое
изображение формул оксидов (например, Аl2O3)
III II
1. Определяем
валентность атомов элементов в Аl2O3
2.
Записываем химические знаки атомов металлов на первое место (первый столбец).
Если атомов металлов больше одного, то записываем и в один столбец и обозначаем
валентность (число связей между атомами) валентными штрихами
З.
Второе место (столбец), тоже в один столбец, занимают химические знаки атомов
кислорода, причем к каждому атому кислорода должно подходить по два валентных
штриха, так как кислород двухвалентен
lll ll l
Графическое изображение формул оснований (например Fе(ОН)3)
1.
Определяем валентность атомов элементов Fе(ОН)3
2.
На первом месте (первый столбец) пишем химические знаки атомов металла,
обозначаем их валентность Fе
З.
Второе место (столбец) занимают химические знаки атомов кислорода, которые
присоединяются одной связью к атому металла, вторая связь пока «свободна»
4.
Третье место (столбец) занимают химические знаки атомов водорода,
присоединяющихся на «свободную»
валентность атомов кислорода
Графическое
изображение формул кислот (например, Н2SO4)
l Vl ll
1. Определяем
валентность атомов элементов Н2SO4.
2.
На первом месте (первый столбец) пишем химические знаки атомов водорода в один
столбец с обозначением валентности
Н—
Н—
З.
Второе место (столбец) занимают атомы кислорода, присоединяясь одной валентной
связью к атому водорода, при этом вторая валентность каждого атома кислорода
пока «свободна»
Н—
О —
Н—
О —
4.
Третье место (столбец) занимают химические знаки атомов кислотообразователя с
обозначением валентности
5.
На «свободные» валентности атома кислотообразователя присоединяются атомы
кислорода согласно правилу валентности
Графическое
изображение формул солей
Средние
соли
(например, Fe2SO4)3) В средних солях все
атомы водорода кислоты замещены на атомы металла, поэтому при графическом
изображении их формул первое место (первый столбец) занимают химические знаки
атомов металла с обозначением валентности, а далее — как в кислотах, то есть
второе место (столбец) занимают химические знаки атомов кислорода, третье место
(столбец) — химические знаки атомов кислотообразователя, их три и они присоединяются
к шести атомам кислорода. На «свободные» валентности кислотообразователя присоединяются
атомы кислорода согласно правилу валентности
Кислые
соли (например, Ва(Н2PO4)2) Кислые соли можно рассматривать
как продукты частичного замещения атомов водорода в кислоте атомами металла,
поэтому при составлении графических формул кислых солей на первое место (первый
столбец) записывают химические знаки атомов металла и водорода с обозначением
валентности
Н—
Н—
Ва
=
Н—
Н—
Второе
место (столбец) занимают химические знаки атомов кислорода
Третье
место (столбец) — химические знаки атомов кислотообразователя, на «свободные»
валентности кислотообразователя присоединяются атомы кислорода согласно
правилу валентности
Основные
соли
(например, А1ОНSO4) Основные соли определяем, чем как
продукт частичного замещения группы ОН основания на кислотный остаток. При
составлении графических формул основных солей первое место (столбец) занимают
химические знаки атомов металлов с обозначением валентности, второе (столбец) —
химические знаки атомов металлов кислорода, третье — химические знаки атомов
водорода и кислотообразователя с обозначением соответствующей валентности. На
«свободные» валентности атома
кислотообразователя присоединяются атомы кислорода согласно правилу валентности
По
графическому изображению формул веществ можно судить об их свойствах,
определяют истинную степень окисления, например, Na+1–О-1 –О-1– Na+1
или в органических соединениях
Структурная формула Фосфата кальция
Ca3(PO4)2 Ca+23(P+5O-24)2
Как научиться писать формулы по химии?
Для составления графической (структурной) формулы вещества необходимо:
- Определить валентность всех химических элементов, образующих вещество.
- Записать знаки всех химических элементов, образующих вещество, каждый в количестве, равном числу атомов данного элемента в молекуле.
Какая формула вещества?
Химическая формула вещества — условная запись вещества, отражающая его качественный и количественный состав. Символы химических элементов показывают из каких атомов состоит вещество (его качественный состав), а индексы — число атомов химических элементов в веществе (его количественный состав).
Как правильно составить формулы солей?
Учимся называть правильно
| Формула кислоты | Название кислоты | Кислотный остаток (формула) |
|---|---|---|
| HBr | бромоводородная | Br — |
| H 2 SO 3 | сернистая | SO 3 2- |
| H 2 SO 4 | серная | SO 4 2- |
| HClO | хлорноватистая | ClO — |
•4 дек. 2021 г.
Какие бывают формулы веществ?
Систематические и тривиальные названия некоторых веществ
| Формула | Систематическое название | Тривиальное название |
|---|---|---|
| Na2CO3 | Карбонат натрия | Сода, кальцинированная сода |
| NaHCO3 | Гидрокарбонат натрия | Питьевая сода |
| CaO | Оксид кальция | Негашеная известь |
| Ca(OH)2 | Гидроксид кальция | Гашеная известь |
Как составить формулы веществ по валентности?
2. Определение валентности по формуле. Составление формулы по валентностям элементов
- Записываем известную валентность кислорода над формулой. Неизвестную валентность обозначаем буквой x: Cl x 2 O II 7 .
- Находим сумму единиц валентности каждого элемента. Для этого его валентность умножаем на число атомов: …
- Вычисляем x:
Как составить формулу оксида элемента?
0:012:48Рекомендуемый клип · 60 сек.составляем формулы оксидов — YouTubeYouTube
Как найти формулу простого вещества?
Простые вещества: молекулы состоят из атомов одного вида (атомов одного элемента). Пример: H2, O2,Cl2, P4, Na, Cu, Au. Сложные вещества (или химические соединения): молекулы состоят из атомов разного вида (атомов различных химических элементов). Пример: H2O, NH3, OF2, H2SO4, MgCl2, K2SO4.
Как сделать молекулярную формулу?
Структура формулы Молекулярная формула химического соединения состоит из символов химических элементов, а также подстрочных арабских цифр для указания их количества в этом соединении. Количество атомов всегда помещается в виде индекса справа от символа элемента, при этом число «1» не пишется.
Как образовывать соли?
- Основные соли образуются при взаимодействии щелочей с растворимыми в воде солями. …
- Основные соли образуются при взаимодействии избытка основания с кислотой. …
- Гидроксокарбонат меди(II), свинца(II), цинка и некоторых других металлов образуется при взаимодействии растворов солей этих металлов с растворами карбонатов.
Как составлять названия солей?
Названия солей составляются из названия кислотного остатка и названия металла. Главным в названии является кислотный остаток. Названия солей в зависимости от кислотного остатка показаны в таблице 8-6.
Как назвать вещество в химии?
Первая часть названия — это название элемента-неметалла с суффиксом «-ид». Вторая часть названия — это название элемента-металла в родительном падеже. Пример: Al2O3. Al2 = Алюминий; O3 = Кислород (Оксиген).
Как выглядит Молекулярная формула?
Молекулярная формула химического соединения состоит из символов химических элементов, а также подстрочных арабских цифр для указания их количества в этом соединении. Количество атомов всегда помещается в виде индекса справа от символа элемента, при этом число «1» не пишется.
Как научиться составлять формулы оксидов?
0:012:48Рекомендуемый клип · 60 сек.составляем формулы оксидов — YouTubeYouTube
Как считать валентность химических элементов?
– Большинство химических элементов обладают переменной валентностью, и ее можно определить по таблице Менделеева. В этой таблице номер группы соответствует высшей валентности элемента. Если от восьми отнять номер группы, где находится элемент, мы узнаем его низшую валентность.
Как пишется формула оксида?
Оксиды – сложные вещества, состоящие из атомов двух химических элементов, одним из которых является кислород в степени окисления -2. Общая формула оксидов: ЭхОу, где Э – атомы химического элемента; О – атомы кислорода; х, у – индексы, указывающие число атомов элементов, образующих оксид.
Какая формула у оксида?
Закономерности изменения свойств оксидов
| Формула оксида | Систематическое название | Тривиальное название |
|---|---|---|
| Оксид железа (II) | Закись железа | |
| Fe 2 O 3 | Оксид железа (III) | Окись железа |
| Оксид фосфора (V) | Фосфорный ангидрид | |
| Н 2 О 2 | Пероксид водорода |
•4 февр. 2022 г.
В чем разница химического элемента и простого вещества?
Атомы химического элемента могут входить в состав простых и сложных веществ. Можно охарактеризовать распространённость и формы нахождения химического элемента в природе, а также свойства его атомов (массу, размеры, строение). Простое вещество образовано атомами одного химического элемента.
Методическая
разработка:
«Алгоритм
составления названий и формул солей».
При изучении химии в 8
классе учащиеся сталкиваются с затруднениями в названии химических веществ и
составления формул химических соединений. Для лучшего усвоения данного
материала им помогут «Алгоритмы» – краткая запись последовательности действий.
При составлении
названий и формул солей необходимо знать состав и название кислот, и
соответственно название кислотных остатков, входящих в эти кислоты. Для
удобства, они указаны в данной разработке.
Названия
кислот и кислотных остатков этих кислот, образующих соли.
–
HCl соляная
кислота Cl хлорид
–
HF фтороводородная
кислота F фторид
–
HBr бромоводородная
кислота Br бромид
–
HI иодоводородная
кислота I иодид
2-
H2S
сероводородная кислота S сульфид
2-
H2SO3
сернистая кислота SO3
сульфит
2-
H2SO4
серная
кислота SO4
сульфат
–
HNO3
азотная кислота NO3 нитрат
–
HNO2
азотистая кислота NO2
нитрит
2-
H2CO3
угольная
кислота CO3
карбонат
2-
H2SiO3
кремниевая
кислота SiO3 силикат
3-
H3PO4
фосфорная кислота PO4
фосфат
АЛГОРИТМ
СОСТАВЛЕНИЯ НАЗВАНИЙ СОЛЕЙ.
Соли – сложные
химические соединения, состоящие из ионов металла, связанного с ионами
кислотного остатка.
При составлении
названия соли, совершаются поочередно следующие шаги:
1. Называется
кислотный остаток, который стоит в формуле соли в конце.
2. Называется
металл ( в родительном падеже). Он записан перед кислотным остатком.
3. Если
заряд металла переменный, в скобках указывается валентность металла.
ПРИМЕР:
CuSO4
сульфат меди (II) NaCl хлорид
натрия
АЛГОРИТМ
СОСТАВЛЕНИЯ ФОРМУЛ СОЛЕЙ.
1. Записываем
химические символы металла и кислотного остатка, образующих соль. Металл
записываем перед кислотным остатком.
2. Над
хим. элементами указываем заряды ионов металла и кислотного остатка.
3. Находим
Наименьшее Общее Кратное между зарядами ионов.
4. НОК
делим поочередно: на заряд металла и заряд кислотного остатка.
5. Ставим
полученные при расчете индексы справа, внизу возле химических элементов. Если
кислотных остатков несколько, заключаем его в скобки. Индекс ставиться за
скобками.
ПРИМЕР:
Нитрат железа (III)
1. Fe
NO3
2.
3+
_
Fe NO3
3.
3
3+
–
Fe NO3
4. 3
: 3 = 1 , 3 :1 = 3
5. Fe(NO3)3
Сульфат
алюминия
1. Al
SO4
2. 3+
2-
Al
SO4
3.
6
3+
2-
Al SO4
4. 6
:3 = 2 , 6 :2 = 3
5. Al2(SO4)3
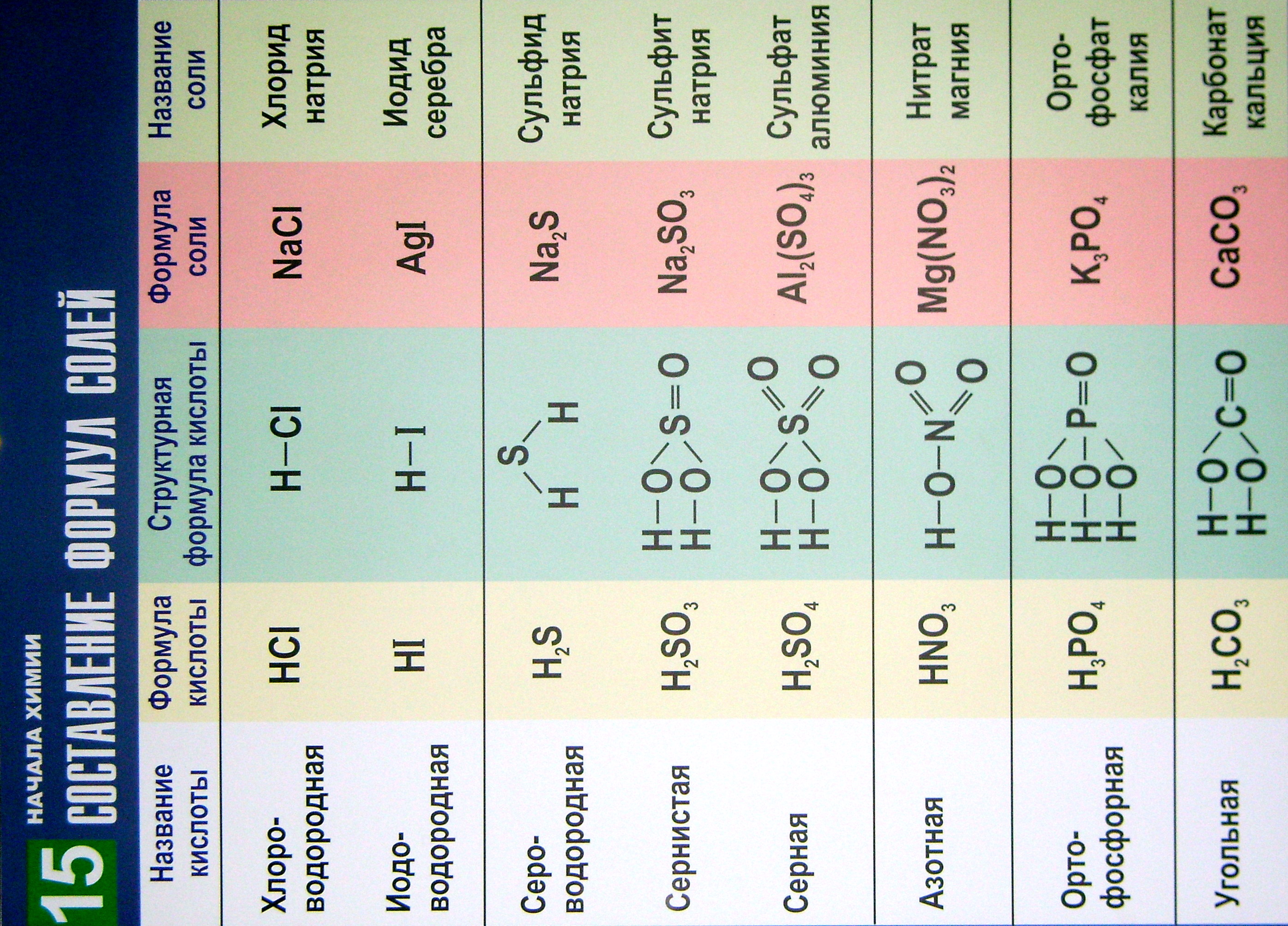
В таблице 15 приведены
названия часто встречающихся кислот,
их молекулярные и структурные формулы,
а также формульные единицы и названия
соответствующих солей.
Таблица помогает
составлять химические формулы солей
бескислородных и кислородсодержащих
кислот. Для образования химических
формул солей надо атомы водорода в
кислотах заменить на атомы металлов с
учётом их валентности.
Приведённые
названия кислот и солей соответствуют
принятой международной номенклатуре.
Название
бескислородных кислот образуются по
правилам для бинарных соединений.
Названия солей
начинаются с названия кислотного остатка
в именительном падеже. Это название
образуется из корня латинского названия
химического элемента, образующего
кислоту, и окончания “ат” или “ит”
в случае солей кислородсодержащих
кислот, для солей бескислородных кислот
– “ид”.
Затем в солях бескислородных кислот
называется металл в родительном падеже.
Причём если атом металла может иметь
разную валентность, то её отмечают
римской цифрой (в скобках) после названия
химического элемента (без пробела).
Например, хлорид железа(II) и хлорид
олова(IV).
Включение в таблицу
названий молекулярных и структурных
формул часто встречающихся кислот
позволяет легко запомнить приведённые
в ней сведения.
Названия кислот
типа HnXOm
составляют с учётом валентности (степени
окисления) центрального атома:
-
атом X
имеет высшую (или единственную)
валентность (степень окисления): H2SО4
–
серная; HNО3
–
азотная; Н2СО3
– угольная; -
атом X
имеет промежуточные степени окисления:
H2SO3
–
сернистая; HNО2
–
азотистая; НСlО – хлорноватистая.
Таблица 15
Составление химических формул солей
16. Генетическая связь классов неорганических веществ
Таблица 16 показывает
в виде схемы взаимосвязь неорганических
веществ разных классов. Изучение свойств
веществ показывает, что можно при помощи
химических реакций переходить от простых
веществ к сложным и от одних сложных
веществ к другим. Связь между веществами
разных классов, основанная на их
взаимопревращениях и отражающая единство
их происхождения, называется
генетической.
Вещества по составу
подразделяются на простые и сложные.
Среди простых веществ различают
металлы и неметаллы. Эти две группы
веществ могут образовывать многочисленные
сложные вещества. К основным классам
неорганических соединений принадлежат
оксиды, гидроксиды и соли. Связь между
этими классами веществ обозначена при
помощи стрелок.
По таблице можно
проследить переходы металлов и неметаллов
в оксиды и гидроксиды:
|
металл |
+ |
О2 |
→ |
оксид, |
оксид металла |
+ |
Н2О |
→ |
гидроксид1 |
|
|
неметалл |
+ |
О2 |
→ |
оксид, |
оксид неметалла |
+ |
Н2О |
→ |
кислород |
Эти две цепочки
превращений аналогичны и роднят металлы
и неметаллы.
Однако надо
подчеркнуть, что простое вещество металл
является родоначальником сложных
веществ, обладающих оснóвными
свойствами (оснóвных оксидов и оснований).
Простое вещество неметалл выступает в
качестве родоначальника сложных
веществ, проявляющих кислотные свойства
(кислотных оксидов и кислот).
Различие свойств
кислотных и оснóвных оксидов, а также
свойств кислот и оснований приводит к
их взаимодействию друг с другом с
образованием солей. Таким образом, соли
генетически связаны с исходными
веществами – металлами и неметаллами
– посредством
их оксидов и гидроксидов.
Так как соли
представляют собой продукты реакций
кислот и оснований, то по составу
различают средние (нормальные), кислые
и оснóвные соли. Кислые соли содержат
в своём составе атомы водорода, оснóвные
– гидроксогруппы. Названия кислых солей
складываются из названий солей с
прибавлением слова “гидро”, а
основных –
“гидроксо”.
Существуют также
двойные соли (соли двух металлов), к ним
относят, например, алюмокалиевые квасцы
KA1(SО4)2
· 12Н2О,
смешанные соли NаСl · NаF, СаВrСl, комплексные
соли Nа2[Zn(ОН)4],
К3[Fе(СN)6],
К4[Fе(СN)6],
включая кристаллогидраты СuSО4
· 5Н2О
(медный купорос), Nа2SО4
· 10Н2О
(глауберова соль)
Необходимо научиться
составлять химические формулы гидроксидов
(кислородсодержащих кислот и оснований)
для атома элемента Э с валентностью
“n”. Гидроксиды получают по реакции
присоединения воды к соответствующим
оксидам. При этом не имеет значение,
происходит ли эта реакция в реальных
условиях. Например, химическую формулу
угольной кислоты получают сложением
всех атомов по уравнению реакции
СО2
+ Н2О
= Н2СО3.
Химические формулы
метафосфорной,
пирофосфорной
и ортофосфорной
кислот составляют из формулы оксида
фосфора(V)1
и соответственно одной, двух и трёх
молекул воды:
Р2О5
+ Н2О
= 2НРО3;
Р2О5
+ 2Н2О
= Н4Р2О7;
Р2О5
+ 3Н2О
= 2Н3РО4.
Приведённая схема
взаимосвязи между классами неорганических
веществ не охватывает всего многообразия
химических соединений. В этой схеме в
качестве бинарных веществ выступают
оксиды,
Таблица 16
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
CharChem
:
Система описания химических формул для WEB.
Химические формулы для “чайников”
Научно-популярная статья о химических формулах.
Изначально сайт был задуман, как ресурс для профессиональных химиков. Содержание Структурные формулы – это просто!
Я думаю, что знакомство с формулами лучше всего начать со структурных формул органических веществ. Перед нами структурная формула метана – самого простого органического вещества. H-C-H;H|#2|H
Что мы видим? В центре латинская буква C, а от неё четыре палочки, на концах которых четыре латинских буквы H.
Структурные формулы могут слегка менять свой внешний вид.
H-C-H; H|#2|H = Все эти картинки означают одно и то же. И считаются одинаковыми формулами.
В общем, структурные формулы не являются какими-то жесткими конструкциями.
Но в химии приняты не только структурные формулы. И здесь мы познакомимся с некоторыми из них. CH4
Палочки исчезли, а вместо четырёх букв H осталась одна, но с маленькой цифрой 4, которая указывает количество атомов.
Стоит упомянуть, что метан – это природный газ, который знаком всем, у кого есть газовая плита. Углеводороды
Прежде, чем мы начнём знакомство с многочисленными органическими соединениями, хочу напомнить –
Здесь представлены органические вещества, называемые углеводородами.
Теперь посмотрим на колонку, где представлены упрощённые структурные формулы.
Некоторые функциональные группы получают собственные названия и даже специальные обозначения. Двойные и тройные связи
Итак, за короткое время мы уже разобрались, что такое структурные формулы и выяснили, что они бывают развёрнутые и упрощённые.
Представленные здесь вещества тоже относятся к углеводородам.
Кроме того, появились дополнительные названия. Тут тоже нет ничего страшного. Циклические углеводороды
Продолжим знакомство с формулами углеводородов. Они ещё не раскрыли нам всех своих секретов.
Изомеры
До сих пор мы не особенно обращали внимания на последнюю колонку, где выведены брутто-формулы.
В химии существует такое понятие как изомеры. Классическими изомерами среди углеводородов можно назвать бутан и изобутан. Посмотрим на их формулы:
Изобутан является изомером бутана. Обратите внимание, что брутто-формулы одинаковы.
Как видно, разнообразие углеводородов не перестаёт удивлять.
А у вещества декан, имеющего формулу C10H22, существует 75 изомеров.
Обратите внимание, что научное название зависит от числа звеньев в прямой цепочке, Бензол и скелетные формулы
Думаю, что пора познакомиться ещё с одним весьма примечательным представителем углеводородов.
Чем же этот бензол так примечателен? Дело в том, что это шестиугольное колечко входит в состав огромного
Конечно, скелетные формулы не так просты, как развёрнутые, но зато их гораздо легче записывать. Давайте посмотрим, как выглядят формулы других веществ, производных от бензола.
Как видите, появился ещё и смешанный вариант. Опять какой-то новый вид формул? На этот раз уже нет. А вот скелетная формула углеводорода, который называется коронен. Причём, другие варианты здесь уже использовать нет смысла. |/`/|“/|`|“|/`/“||/\/\|||`/|`//“/`\`|/`/“||/
Впечатляет? Но это далеко не самая сложная структура для органического вещества.
Скелетные формулы существуют не только для циклических молекул.
Трехмерные изображения
Иногда плоского изображения становится недостаточно.
В качестве примера посмотрим на формулы уже известных нам углеводородов:
Конечно, здесь потребуется включать воображение, чтобы представить трёхмерную структуру. Формулы с окружностью
Думаю, что стоит упомянуть ещё одну интересную конструкцию, которая нередко встречается при изображении циклических структур. /\|`//“|| <-> /=`//`-`\ <-> //||`/`\`| <-> /|`/“|_o <-> H|</H>|<H>`/<|H>`<`/H>`|<`H>/_o
Само собой, все они означают одно и то же. Но первые три отличаются только поворотом вокруг собственного центра.
Формулы бензола, где используется чередование одинарных и двойных связей называются формулами Кекуле в честь немецкого учёного,
На самом деле, среди химиков нет единого мнения по поводу того, насколько правильно использование формул с кружком. Вот пара примеров записи уже для уже знакомых нам веществ:
Знакомство с кислородом. Спирты
До сих пор мы знакомились со структурными формулами углеводородов, которые состоят только из углерода и водорода.
Кислород – очень распространённый элемент на нашей планете.
Не правда ли, что в этом есть что-то знакомое? Метан – метанол, этан – этанол, пропан – пропанол.
Все спирты можно описать в виде обобщённой формулы {R}-OH,
Конечно же стоит упомянуть, что этанол – это тот самый спирт, который входит в состав алкогольных напитков.
Ещё здесь из четырёх спиртов есть два изомера: 1-пропанол и 2-пропанол.
CH3-CH2-CH2-OH = $slope(45)CH3CH2CH2OH = CH3|CH2|CH2|OH = HO/CH2/CH2/CH3 = Поэтому первый номер – тот, который ближе к гидроксильной группе.
Все спирты, с которыми мы уже успели познакомиться, имеют в своём составе одну гидроксильную группу.
Ну и чтобы завершить знакомство со спиртами, приведу ещё формулу другого известного вещества – холестерина.
|`/`\`|<`|w>“/|<`/w$color(red)HO$color()>/`|0/`|/<`|w>|_q_q_q<-dH>:a_q|0<|dH>`/<`|wH>`|dH; Гидроксильную группу в нём я обозначил красным цветом. Карбоновые кислоты
Любой винодел знает, что вино должно храниться без доступа воздуха. Иначе оно скиснет.
Отличительной особенностью органических кислот является наличие карбоксильной группы (COOH),
Все, кто пробовал уксус, знают что он весьма кислый. Причиной этого является наличие в нём уксусной кислоты.
Карбоновые кислоты могут иметь несколько карбоксильных групп. В пищевых продуктах содержится немало других органических кислот. Вот только некоторые из них:
Название этих кислот соответствует тем пищевым продуктам, в которых они содержатся. Радикалы
Радикалы – это ещё одно понятие, которое оказало влияние на химические формулы.
Выше по тексту уже несколько раз упоминались обобщённые формулы: спирты – {R}-OH и
Если выражаться более определённо, то одновалентным радикалом называется часть молекулы, лишённая одного атома водорода.
Радикалы в химии получили собственные названия.
Думаю, что здесь всё понятно. Хочу только обратить внимание на колонку, где приводятся примеры спиртов.
Существует ещё такое явление, как свободные радикалы. Знакомство с азотом. Амины
Предлагаю познакомиться с ещё одним элементом, который входит в состав многих органических соединений. Это азот. Посмотрим, какие вещества получаются, если к знакомым нам углеводородам присоединить азот:
Как Вы уже наверное догадались из названий, все эти вещества объединяются под общим названием амины.
В общем, никаких особых новшеств здесь нет. Рациональные формулы
Не следует делать вывод о том, что неорганическая химия проще, чем органическая.
Так вот, ничего этого я рассказывать не буду. Тема моей статьи – химические формулы.
Для начала, познакомимся с ещё одним элементом – кальцием. Это тоже весьма распространённый элемент.
При первом взгляде можно заметить, что рациональная формула является чем то средним между структурной и брутто-формулой.
Кальций в чистом виде – это мягкий белый металл. В природе он не встречается. 2Ca + O2 -> 2CaO
Цифра 2 перед формулой вещества означает, что в реакции участвуют 2 молекулы. CaO + H2O -> Ca(OH2)
Получается гидроксид кальция. Если присмотреться к его структурной формуле (в предыдущей таблице), то видно,
Но и гидроксид кальция не встречается в природе из-за наличия в воздухе углекислого газа. CO2 + H2O <=> H2CO3 Знак <=> говорит о том, что реакция может проходить в обе стороны при одинаковых условиях.
Таким образом, гидроксид кальция, растворённый в воде, вступает в реакцию с угольной кислотой Ca(OH)2 + H2CO3 -> CaCO3″|v” + 2H2O
Стрелка вниз означает, что в результате реакции вещество выпадает в осадок. CaCO3 + CO2 + H2O <=> Ca(HCO3)2
Этот процесс влияет на жесткость воды.
Из карбоната кальция в значительной степени состоят мел, известняк, мрамор, туф и многие другие минералы.
Этот небольшой рассказ о круговороте кальция в природе должен пояснить, для чего нужны рациональные формулы.
Кроме того, отдельные элементы – Ca, H, O(в оксидах) – тоже являются самостоятельными группами. Ионы
Думаю, что пора знакомиться с ионами. Это слово наверняка всем знакомо.
В общем, природа химических связей обычно заключается в том, что одни элементы отдают электроны, а другие их получают. H2O <=> H^+ + OH^-
Здесь мы видим, что в результате электролитической диссоциации вода распадается на положительно заряженный H2CO3 = H^+ + HCO3^- <=> 2H^+ + CO3^2- Карбонат-ион имеет заряд 2-. Это означает, что к нему присоединились два электрона.
Отрицательно заряженные ионы называются анионы. Обычно к ним относятся кислотные остатки.
И вот здесь наверное можно полностью понять смысл рациональных формул. В них сначала записывается катион, а за ним – анион.
Вы наверное уже догадываетесь, что ионы можно описывать не только рациональными формулами. O^-|O`|/OH
Здесь заряд указан непосредственно возле атома кислорода, который получил лишний электрон, и поэтому лишился одной чёрточки. NH3 + H2O <=> NH4^+ + OH^- То же самое, но с использованием структурных формул: H|N<`/H>H + H-O-H <=> H|N^+<_(A75,w+)H><_(A15,d+)H>`/H + O`^-# -H
В правой части мы видим два иона.
2H|N^+<`/H><_(A75,w+)H>_(A15,d+)H + O^-C|O`|/O^- <=>
Но в таком виде уравнение реакции дано в демонстрационных целях. 2NH4^+ + CO3^2- <=> (NH4)2CO3 Система Хилла
Итак, можно считать, что мы уже изучили структурные и рациональные формулы.
В принципе, рациональная формула угольной кислоты вполне может считаться истинной формулой,
Вместо заключения мне хотелось бы рассказать о системе CharChem.
Зачем вообще нужна какая-то система для вывода формул?
Рациональные и брутто-формулы вполне можно изобразить при помощи текста. H H
| |
H-C-C-O-H
| |
H H
Выглядит конечно не очень красиво, но тоже осуществимо.
Настоящая проблема возникает при попытке изобразить бензольные кольца и при использовании скелетных формул.
Система CharChem позволяет хранить все формулы прямо в HTML-документе в текстовом виде. По-моему, это очень удобно.
Таким образом, для подготовки этой статьи я пользовался только текстовым редактором. Вот несколько примеров, раскрывающих секрет подготовки текста статьи:
Описания из левого столбца автоматически превращаются в формулы во втором столбце. Здесь есть гораздо более подробная документация по использованию системы CharChem. На этом разрешите закончить статью и пожелать удачи в изучении химии. Краткий толковый словарь использованных в статье терминов
|