Темы кодификатора ЕГЭ: Гидролиз солей. Среда водных растворов: кислая, основная и щелочная.
Гидролиз – взаимодействие веществ с водой. Гидролизу подвергаются разные классы неорганических и органических веществ: соли, бинарные соединения, углеводы, жиры, белки, эфиры и другие вещества. Гидролиз солей происходит, когда ионы соли способны образовывать с Н+ и ОН— ионами воды малодиссоциированные электролиты.
Гидролиз солей может протекать:
→ обратимо: только небольшая часть частиц исходного вещества гидролизуется.
→ необратимо: практически все частицы исходного вещества гидролизуются.
Для оценки типа гидролиза необходимо рассмотреть соль, как продукт взаимодействия основания и кислоты. Любая соль состоит из металла и кислотного остатка. Металлы соответствует основание или амфотерный гидроксид (с той же степенью окисления, что и в соли), а кислотному остатку — кислота. Например, карбонату натрия Na2CO3 соответствует основание — щелочь NaOH и угольная кислота H2CO3.
Обратимый гидролиз солей
Механизм обратимого гидролиза будет зависеть от состава исходной соли. Можно выделить 4 основных варианта, которые мы рассмотрим на примерах:
1. Соли, образованные сильным основанием и слабой кислотой, гидролизуются ПО АНИОНУ.
Примеры таких солей — CH3COONa, Na2CO3, Na2S, KCN.
Реакция гидролиза:
CH3COONa + HOH ↔ CH3COOH + NaOH
в ионной форме:
CH3COO— + Na+ + HOH ↔ CH3COOH + Na+ + OH—
сокращенное ионное уравнение:
CH3COO— + HOH ↔ CH3COOH + OH—
Таким образом, при гидролизе таких солей в растворе образуется небольшой избыток гидроксид-ионов OH—. Водородный показатель такого раствора рН>7.
Гидролиз солей многоосновных кислот (H2CO3, H3PO4 и т.п.) протекает ступенчато, с образованием кислых солей:
CO32- + HOH ↔ HCO32- + OH—
или в молекулярной форме:
Na2CO3 + HOH ↔ NaHCO3 + NaOH
2 ступень:
HCO3— + HOH ↔ H2CO3 + OH—
или в молекулярной форме:
NaHCO3 + HOH ↔ H2CO3 + NaOH
Продукты гидролиза по первой ступени подавляют вторую ступень гидролиза, в результате вторая ступень гидролиза протекает незначительно.
2. Соли, образованные слабым основанием и сильной кислотой, гидролизуются ПО КАТИОНУ. Пример такой соли: NH4Cl, FeCl3, Al2(SO4)3 Уравнение гидролиза:
NH4+ + HOH ↔ NH3·H2O + H+
или в молекулярной форме:
NH4Cl + HOH ↔ NH3·H2O + HCl
При этом катион слабого основания притягивает гидроксид-ионы из воды, а в растворе возникает избыток ионов Н+. Водородный показатель такого раствора рН<7.
Соли, образованные многокислотными основаниями, гидролизуются ступенчато, образуя катионы основных солей. Например:
I ступень:
Fe3+ + HOH ↔ FeOH2+ + H+
FeCl3 + HOH ↔ FeOHCl2 + HCl
II ступень:
FeOH2+ + HOH ↔ Fe(OH)2+ + H+
FeOHCl2 + HOH ↔ Fe(OH)2Cl+ HCl
III ступень:
Fe(OH)2+ + HOH ↔ Fe(OH)3 + H+
Fe(OH)2Cl + HOH ↔ Fe(OH)3 + HCl
Гидролиз по второй и, в особенности, по третьей ступени практически не протекает при комнатной температуре.
3. Соли, образованные слабым основанием и слабой кислотой, гидролизуются И ПО КАТИОНУ, И ПО АНИОНУ.
Примеры таких солей: CH3COONH4, (NH4)2CO3, HCOONH4,
Уравнение гидролиза:
CH3COO— + NH4+ + HOH ↔ CH3COOH + NH3·H2O
CH3COONH4 + HOH ↔ CH3COOH + NH3·H2O
В этом случае реакция раствора зависит от соотношения констант диссоциации образующихся кислот и оснований. В большинстве случаев реакция раствора будет примерно нейтральной, рН ≅ 7. Точное значение рН зависит от относительной силы основания и кислоты.
4. Гидролиз солей, образованных сильным основанием и сильной кислотой, в водных растворах НЕ ИДЕТ.
Сведем вышеописанную информацию в общую таблицу:
Необратимый гидролиз
Необратимый гидролиз происходит, если при гидролизе выделяется газ, осадок или вода, т.е. вещества, которые при данных условиях не могут взаимодействовать между собой. Необратимый гидролиз является химической реакцией, т.к. реагирующие вещества взаимодействуют практически полностью.
Варианты необратимого гидролиза:
- Гидролиз, в который вступают растворимые соли 2х-валентных металлов (Be2+, Co2+, Ni2+, Zn2+, Pb2+, Cu2+ и др.) с сильным ионизирующим полем (слабые основания) и растворимые карбонаты/гидрокарбонаты. При этом образуются нерастворимые основные соли (гидроксокарбонаты):
2MgCl2 + 2Na2CO3 + H2O = Mg2(OH)2CO3 + 4NaCl + CO2
2МеCl2 + 2Na2CO3 + Н2О = (МеОН)2CO3 + 4NaCl + СО2 (МеII, кроме Fe, Ca,Sr,Ba).
! Исключения: (соли Ca, Sr, Ba и Fe2+) – в этом случае получим обычный обменный процесс:
CaCl2 + Na2CO3 = CaCO3 + 2NaCl,
МеCl2 + Na2CO3 = МеCO3 + 2NaCl (Ме – Fe, Ca, Sr, Ba).
- Взаимный гидролиз, протекающий при смешивании двух солей, гидролизованных по катиону и по аниону. Продукты гидролиза по второй ступени усиливают гидролиз по первой ступени и наоборот. Поэтому в таких процессах образуются не просто продукты обменной реакции, а продукты гидролиза (совместный или взаимный гидролиз).Соли металлов со степенью окисления +3 (Al3+, Cr3+) и соли летучих кислот (карбонаты, сульфиды, сульфиты) при смешивании в растворе (взаимном гидролизе) образуют осадок гидроксида и газ (H2S, SO2, CO2):
2AlCl3 + 3K2S +6H2O = 2Al(OH)3 + 3H2S↑ + 6KCl,
2CrCl3 + 3K2CO3 + 3H2O = 2Сr(ОН)3 + 3СO2 + 6KCl,
2МеCl3 + 3Na2CO3 + 3Н2О=2Ме(ОН)3 + 6NaCl + 3СО2 (МеIII),
2МеCl3 + 3Na2SO3 + 3Н2О=2Ме(ОН)3 + 6NaCl + 3SО2 (МеIII),
2МеCl3 + 3Na2S + 3Н2О=2Ме(ОН)3 + 6NaCl + 3H2S (МеIII).
Соли Fe3+ при взаимодействии с карбонатами также при смешивании в растворе (взаимном гидролизе) образуют осадок гидроксида и газ:
2FeCl3 + 3K2CO3 + 3H2O = 2Fe(ОН)3 + 3СO2 + 6KCl
! Исключения: при взаимодействии солей трехвалентного железа с сульфидами реализуется окислительно-восстановительная реакция:
2FeCl3 + 3K2S(изб) = 2FeS + S↓ + 6KCl (при избытке сульфида калия)
При взаимодействии солей трехвалентного железа с сульфитами также реализуется окислительно-восстановительная реакция.
Полные уравнения таких реакций выглядят довольно сложно. Поначалу я рекомендую составлять такие уравнения в 2 этапа: сначала составляем обменную реацию без участия воды, затем разлагаем полученный продукт обменной реакции водой. Сложив эти две реакции и сократив одинаковые вещества, мы получаем полное уравнение необратимого гидролиза.
3. Гидролиз галогенангидридов и тиоангидридов происходит также необратимо. Галогенангидриды разлагаются водой по схеме ионного обмена (H+OH—) до соответствующих кислот (в случае водного гидролиза) и солей (в случае щелочного гидролиза). Степень окисления центрального элемента и остальных при этом не изменяется!
SO2Cl2 + 2 H2O = H2SO4 + 2 HCl,
SOCl2 + 2 H2O = H2SO3 + 2HCl,
PCl5 + 4 H2O = H3PO4 + 5HCl,
CrO2Cl2 + 2H2O = H2CrO4 + 2HCl,
PCl5 + 8NaOH = Na3PO4 + 5NaCl + 4H2O,
Галогенангидрид – это соединение, которое получается, если в кислоте ОН-группу заменить на галоген. При гидролизе галогенангидридов кислот образуются соответствующие данным элементам и степеням окисления кислоты и галогеноводородные кислоты.
POCl3 + 3H2O = H3PO4 + 3HCl
Галогенангидриды некоторых кислот:
| Кислота | Галогенангидриды |
| H2SO4 | SO2Cl2 |
| H2SO3 | SOCl2 |
| H2CO3 | COCl2 |
| H3PO4 | POCl3, PCl5 |
Тиоангидриды (сульфангидриды) — так называются, по аналогии с безводными окислами (ангидридами), сернистые соединения элементов (например, Sb2S3, As2S5, SnS2, CS2 и т. п.).
- Необратимый гидролиз бинарных соединений, образованных металлом и неметаллом:
- сульфиды трехвалентных металлов вводе необратимо гидролизуются до сероводорода и и гидроксида металла:
Al2S3 + 6H2O = 2Al(OH)3 + 3H2S
при этом возможен кислотный гидролиз, в таком случае образуются соль металла и сероводород:
Al2S3 + 6HCl = 2AlCl3 + 3H2S
- гидролиз карбидов приводит к образованию гидроксида металла в водной среде, соли металла в кислой де и соответствующего углеводорода — метана, ацетилена или пропина:
Ca+2C-12 + H2O = Ca+2(OH)2 + C-12H2
Al+34C-43 + 12H2O = 4Al+3(OH)3 + 3C-4H4,
Ca3N2 + H2O =
Ca3P2 + H2O =
Mg2Si + H2O =
- Некоторые соли необратимо гидролизуются с образованием оксосолей:
BiCl3 + H2O = BiOCl + 2HCl,
SbCl3 + H2O = SbOCl + 2HCl.
Алюмокалиевые квасцы:
KAl(SO4)2 + K2S + H2O =
MgCl2 + NaНCO3 + H2O =
ZnSO4 + CsНCO3 + H2O =
CdSO4 + RbНCO3 + H2O =
CaSO4 + Rb2CO3 + H2O =
FeCl2 + Rb2CO3 + H2O =
Количественно гидролиз характеризуется величиной, называемой степенью гидролиза.
Степень гидролиза (α) — отношение количества (концентрации) соли, подвергающейся гидролизу, к общему количеству (концентрации) растворенной соли. В случае необратимого гидролиза α≅1.
Факторы, влияющие на степень гидролиза:
1. Температура
Гидролиз — эндотермическая реакция! Нагревание раствора приводит к интенсификации процесса.
Пример: изменение степени гидролиза 0,01 М CrCl3 в зависимости от температуры:
2. Концентрация соли
Чем меньше концентрация соли, тем выше степень ее гидролиза.
Пример: изменение степени гидролиза Na2CO3 в зависимости от температуры:
По этой причине для предотвращения нежелательного гидролиза хранить соли рекомендуется в концентрированном виде.
3. Добавление к реакционной смеси кислоты или щелочи
Изменяя концентрация одного из продуктов, можно смещать равновесие реакции гидролиза в ту или иную сторону.
Пройти тест по теме Гидролиз:
Здесь вы можете потренироваться в решении тестовых заданий в формате ЕГЭ по теме Гидролиз.
Тренировочные тесты по теме «Гидролиз»( с ответами)
240
Создан на
16 января, 2022 От Admin
Тренажер задания 21
Тренажер задания 21 ЕГЭ по химии
1 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) уксусная кислота
2) метиламин
3) азотная кислота
4) гидроксид кальция
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
2 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KHCO3
2) Ba(NO3)2
3) ZnSO4
4) HCIO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
3 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2CO3
2) Н3РО4
3) Ва(NO3)2
4) Са(ОН)2
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
4 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) KF
2) LiNO3
3) (NH4)2SО4
4) H2SО4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
5 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) K2CO3
2) Cu(NO3)2
3) Li2SO4
4) НClO4
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
6 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) Na2SO4
2) Fe(NO3)2
3) K2SO3
4) HCIO3
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация (моль/л) всех растворов одинаковая.
7 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л).
1) LiIO3
2) HMnO4
3) Ca(HS)2
4) Mg(ClO4)2
Запишите номера веществ в порядке возрастания значения pH их водных растворов.
8 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) NH4Br
2) HI
3) Na2SiO3
4) KClO4
Запишите номера веществ в порядке возрастания значения рН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
9 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) CH3NH2
2) KClO4
3) Аl(NO3)3
4) Ba(OH)2
Запишите номера веществ в порядке убывания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
10 / 10
Для веществ, приведённых в перечне, определите характер среды их водных растворов.
1) C6H5OK
2) NaClO4
3) Cr(NO3)3
4) Sr(OH)2
Запишите номера веществ в порядке возрастания значения pН их водных растворов, учитывая, что концентрация всех растворов (моль/л) одинаковая.
Ваша оценка
The average score is 32%
Пособие
для учащихся «Гидролиз»
Данное пособие предназначено для учащихся 11 класса.
Тема «Гидролиз солей» вызывает некоторые затруднения у учащихся. Пособие
содержит теоретический материал по теме «Гидролиз». Представлен алгоритм
составления уравнений реакций гидролиза, разбираются примеры решения заданий
по теме «Гидролиз солей»,приведены таблицы: «Сильные и слабые электролиты»,
«Индикаторы», «Таблица растворимости».
Составлены задания для самостоятельной работы учащихся. Пособие поможет
ученикам при выполнении лабораторной работы, по выполнению домашней работы;
позволит более полно усвоить тему.
Успешное выполнение
заданий по теме: «Гидролиз солей» невозможно без знания теоретического
материала.
1.Необходимо повторить
правила пользования таблицей растворимости:
Чтобы
определить,растворима ли соль,по вертикале в таблице находим
катион,образовавший соль.По горизонтали соответствующий анион. Если на их
пересечении стоит буква Р-соль растворима,следовательно в водном растворе
диссоциирует на ионы.Если –буква Н- вещество нерастворимо,на ионы не
диссоциирует.
2.Необходимо повторить понятия :
«электролиты», «неэлектролиты», «сильные электролиты»,
«слабые электролиты»
Электролиты-это
вещества растворы или расплавы которых проводят электрический ток. NaCl,
H2SO4,
NaOH
Неэлектролиты-это
вещества, водные растворы или расплавы которых не проводят электрический
ток. Кислород O2,
азот N2,
водород H2,многие
органические вещества – спирты, глюкоза, сахароза, бензол и др.
Сильные электролиты-полность диссоциируют
на ионы
Сильные электролиты (α
→ 1 или 100%)
1) сильные кислоты (H2SO4,
HCl,
HNO3,
HClO4,
HClO3,
HBr,
HI
и др.)
2) щелочи (NaOH,
KOH,
LiOH,
Ba(OH)2,
Ca(OH)2
и др.)
3)растворимые соли
Слабые электролиты -неполность
диссоциируют на ионы
Слабые электролиты (α
→ 0)
1) cлабые
кислоты (H2S,
H2CO3,
H2SiO3,
HNO2,
H3PO4,
H2SO3,
HCN,
HF,
CH3COOH и др.)
2) нерастворимые в воде основания (Cu(OH)2,
Fe(OH)3
и др.)
3) гидроксид аммония NH4OH
3.Следует знать
цвет индикаторов в различных средах
|
Название |
Окраска индикатора в среде |
||
|
Кислая [H+]* > [OH-] |
Нейтральная [H+] = [OH-] |
Щелочная [OH-] > [H+] |
|
|
Лакмус |
красный |
фиолетовый |
синий |
|
Фенолфталеин |
бесцветный |
бесцветный |
малиновый |
|
Метилоранж |
розовый |
оранжевый |
желтый |
4.Знания о том,как
диссоциируют вещества ,относящиеся к различным классам неорганических
соединений помогут в написании уравнений гидролиза
Кислоты
– электролиты, которые при диссоциации образуют только один вид катионов –
катионы водорода Н+ Уравнение
электролитической диссоциации сильных кислот:
HCl ↔ H+ + Cl–
H2SO4 ↔ 2H+ + SO42-
Слабые
многоосновные кислоты диссоциируют ступенчато.
H2CO3
↔ H+ + HCO3– К1
> K2
HCO3–
↔ H+ + CO32-
Основания –
электролиты, которые при диссоциации образуют только один вид анионов –
гидроксид-ионы ОН Уравнение диссоциации сильных
оснований (щелочей)
NaOH ↔ Na+ +
OH–
Ba(OH)2 ↔ Ba2+
+ 2OH–
Слабые многокислотные
основания диссоциируют ступенчато.
Fe(OH)2 ↔ FeOH+
+ OH– К1
> K2
FeOH+
↔ Fe2+
+ OH–
Средние
(нормальные) соли – сильные электролиты, образующие
при диссоциации катионы металла и анионы кислотного остатка.
Al2(SO4)3
↔ 2Al3+
+ 3SO42-
Основные соли
– электролиты, которые при диссоциации образуют анионы кислотного остатка и
сложные катионы, состоящие из атомов металла и гидроксогрупп ОН-.
Fe(OH)Cl ↔ Fe(OH)+
+ Cl– (α = 1)
Fe(OH)+
↔ Fe2+
+ OH–
(α <<1)
5.Изучить
теоретический материал по теме: «Гидролиз солей»
Соли – это соединения,
образующие при диссоциации в водном растворе положительно заряженные ионы
металлов и отрицательно заряженные ионы кислотных остатков, а иногда, кроме
них, ионы водорода и гидроксид-ионы. В водном растворе эти ионы гидратированы
– окружены молекулами воды.
Водные растворы многих
солей имеют кислую или щелочную среду. Причиной этого явления является гидролиз
–это взаимодействие ионов соли с водой,приводящее к образованию слабого
электролита
Причина гидролиза –
электролитическая диссоциация соответствующих солей и воды.
По отношению к воде соли можно
разделить на 4 группы:
1.Соли,
образованные катионом сильного основания и анионом слабой кислоты.
Гидролиз такого типа
называют гидролизом по аниону. Среда раствора щелочная,лакмус синий.
Пример:гидролиз соли фосфата натрия(Na3PO4
). Соль образована сильным
основанием-гидроксидом калия и слабой кислотой-фосфорной.
Na3PO4
⇄3Na+
+ PO43-
Н2О ⇄Н+
+ ОН–
3Na+
+ PO43-
+ Н2О⇄
НРО42-+ОН– +3Na+
PO43-
+ НОН ⇄ НРО42-+ОН–
Na3PO4 + Н2О ⇄ Na2НРО4 + КОН
2.Соли,
образованные катионом слабого основания и анионом сильной кислоты.
Гидролиз такого типа
называют гидролизом катиону.Среда кислая,лакмус красный Пример: гидролиз соли
сульфата меди(2)- CuSO4
CuSO4
⇄
Cu2++
SO42-
Н2О ⇄Н+
+ ОН–
Cu2++
SO42-
+ Н2О ⇄
CuOH+
+H+
Cu+2 + НОН
⇄
CuOH+ +H+ + SO42- 2CuSO4+2H2O ⇄
(CuOH)2SO4 + H2SO4
3.Соли,
образованные катионом сильного основания и анионом сильной кислоты. Соль гидролизу не
подвергается, диссоциирует на ионы в водном
растворе. В этом случае. среда нейтральная, лакмус фиолетовый.
4.Соли,
образованные катионом слабого основания и анионом слабой кислоты.
Гидролиз
такого типа называют гидролизом по катиону и аниону. В
этом случае характер среды определяют по степени диссоциации кислоты и
основания, образовавших соль. Если степень диссоциации кислоты больше степени
диссоциации основания, то среда будет слабокислой. И ,наоборот ,если степень
диссоциации основания больше степени диссоциации кислоты, то
среда-слабощелочная.
Пример необратимого гидролиза: Al2S3
+ H2O
à
Al(OH)3¯
+ H2S
Особого внимания заслуживает совместный гидролиз.
Соли в водном
растворе полностью гидролизованы.
Пример:
2AlCl3 +3K2S +
6H2O à2Al(OH)3¯
+3H2S↑ + 6KCl
Алгоритм составления уравнений реакций гидролиза:
1.
Определить
какой по силе кислотой и каким основанием по силе образована соль.
2.
Записать
уравнение диссоциации соли,затем уравнение диссоциации молекулы воды.
3.
Выписать
формулу иона слабого электролита и написать уравнение взаимодействия его с
одной молекулой воды; в результате получится краткое ионно-молекулярное
уравнение гидролиза
4.
Записать
уравнение реакции гидролиза в молекулярном виде. Указать характер среды и цвет
индикатора лакмуса
Рассмотрим
,как пользуясь алгоритмом составления уравнения гидролиза, выполнить задание.
Пример
№1
Составить
уравнение реакции гидролиза соли, образованной сильным основанием и слабой
кислотой-сульфида натрия(Na2S)
1.Соль образована
гидроксидом натрия-сильным основанием и слабой кислотой-сероводородной.
2.Определить тип
гидролиза, среду и цвет индикатора.
Гидролиз по аниону Среда
щелочная ,лакмус синий.
3.Записать уравнение
диссоциации соли и воды
Na2 S⇄ →
2Na+ + S2-
H2O⇄ H++
OH–
4.Записать ионное
уравнение гидролиза
2Na+
+ S2-
+ H2O⇄
HS–
+2Na+
+ OH–
5.Составить молекулярное
уравнение
Na2
S+
H2O⇄
NaHS
+ Na OH
Пример №2
Составить уравнение
реакции гидролиза хлорида меди (2).
1.Рассмотрим состав
соли: соль образована слабым основанием гидроксидом меди(2) и сильной кислотой
–соляной.
2.Определить тип
гидролиза, среду и цвет индикатора.
Гидролиз по
катиону, среда кислая, лакмус красный.
3.Записать уравнение
диссоциации соли и воды
CuCl2 ⇄Cu2+
+2Cl– H2O⇄ H++
OH–
4.Записать ионное
уравнение гидролиза
Cu2+
+2Cl–
+ H2O⇄
Cu OH+
+2Cl–
+ H+
5.Составить молекулярное
уравнение
CuCl2
+ H2O⇄
Cu OHCl
+ HCl
В тестовых заданиях или в заданиях на соответствие, составленных по типу
заданий ЕГЭ встречаются обозначения среды посредством использования значений
водородного показателя. Необходимо помнить:
PH
> 7- среда щелочная, концентрация ионов гидроксогруппы больше концентрации
ионов водорода ; PH < 7- среда
кислая, концентрация ионов водорода больше концентрации гидроксид-ионов; PH
= 7- среда нейтральная; концентрация ионов водорода равна концентрации
гидроксид-ионов.
Количественно гидролиз характеризуется степенью гидролиза. Она
показывает сколько молекул вещества от общего числа молекул подвергается
гидролизу. Степень гидролиза зависит от температуры, природы вещества,
концентрации раствора. Если повысить температуру-это усилит гидролиз, так
как это эндотермическая реакция .При разбавлении водой гидролиз усиливается.
Если гидролиз по аниону-повышение концентрации гидроксид-ионов будет ослаблять
гидролиз.
Если гидролиз по катиону-повышение концентрации ионов водорода ослабит гидролиз.
Предположим
соль- хлорид меди (2).Она гидролизуется по катиону, так как образована слабым
основанием –гидроксидом меди(2) и сильной кислотой-соляной. Чтобы усилить
гидролиз этой соли ,нужно нагреть раствор; добавить воды; добавить
щелочь-раствор(делаем выбор).
Пример № 3
Определить формулу
соли, если значение PH=7 : хлорид магния,
сульфат натрия; бромид алюминия.
1.MgCl2
–соль образована слабым основанием и сильной кислотой;
гидролиз по катиону, среда кислая PH<7;
2.Na2
SO4–
соль образована сильным основанием и сильной кислотой; среда нейтральная PH=7.
3.AlBr3–
соль образована сильной кислотой и слабым основанием; гидролиз по катиону;PH<7
Задания
для самостоятельной работы :
1.Задания для закрепления знаний, умений
определять характер среды и цвет индикатора
|
Формула |
Характер |
Цвет |
|
1.хлорид |
||
|
2.сульфит |
||
|
3.силикат |
||
|
4.фосфат |
||
|
5. |
2.
|
Название |
Характер |
Тип |
|
1. сульфат |
||
|
2. фосфат |
||
|
3.хлорид |
||
|
4.карбонат |
||
|
5. нитрат |
3.
|
Формула |
Характер |
Значение PH |
|
1.Cu(NO3)2 |
||
|
2 Na2S |
||
|
3 K3PO4 |
||
|
4 K2SO3 |
||
|
5 Na2SO4 |
4.
|
Соль |
Сила |
Сила |
|
1.Cu(NO3)2 |
||
|
2 Na2S |
||
|
3 K3PO4 |
||
|
4 K2SO3 |
||
|
5 Na2SO4 |
Задания для самостоятельной домашней
работы по теме: «Гидролиз солей»
1.
Составьте
уравнения реакций гидролиза солей в молекулярном и ионном виде:
а) нитрат
меди(2); б)сульфат меди; в) карбонат калия; г)фосфат натрия;
д) сульфат
натрия; е) нитрат магния; ж) ацетат натрия; з) хлорид меди
(2);
и) нитрит
натрия; к) сульфид калия.
Определить характер
среды и цвет лакмуса.
Тест по теме: «Гидролиз солей»
Вариант
1.
1.Гидролиз-это…….
а)
окислительно-восстановительная реакция. идущая на электродах под действием
электрического тока;
б) реакция между
ионами соли и ионами воды, приводящая к образованию слабого электролита;
в) реакция, при
которой из одного сложного вещества образуется несколько простых;
г)реакция при
которой атомы простого вещества замещают атомы сложного.
2. Выберите формулу сильного электролита:
уксусная кислота ; гидроксид натрия; ацетат натрия; кремниевая кислота;
угольная кислота; сероводородная кислота; гидроксид магния.
3.Соль образована сильной кислотой и
сильным основанием. Определите характер среды: кислая, щелочная; нейтральная.
4. Дана соль-
сульфид аммония. Определите тип гидролиза:
а) гидролиз по
аниону; б) гидролиз по катиону;
в) гидролиз по
катиону и аниону; г) гидролизу не подвергается.
5. Гидролиз соли по
катиону .Каким основанием и какой кислотой по силе образована эта соль:
а)сильной кислотой
и сильным основанием; б)слабой кислотой и слабым основанием;
в)слабой кислотой и
сильным основанием; г)сильным основанием и слабой кислотой;
6.Сильный
электролит-это..
а)вещество, которое
при растворении в воде или расплавлении полностью диссоциирует на ионы
б) вещество,
которое при растворении в воде или расплавлении неполностью диссоциирует на
ионы
в)вещество, которое
не диссоциирует на ионы.
7.Водородный показатель
равен 7. Какова окраска лакмуса?
а)синяя
б)красная,
в)фиолетовая
Вариант
2.
1. Дана соль-
хлорид железа(2). Определите тип гидролиза:
а)гидролиз по
аниону; б)гидролиз по катиону;
в)гидролиз по
катиону и аниону; г)гидролизу не подвергается.
2. Выберите формулу слабого электролита:
гидроксид натрия; гидроксид бария; уксусная кислота; соляная кислота, азотная
кислота.
3. Соль образована слабой кислотой и
сильным основанием. Определите характер среды: кислая, щелочная; нейтральная.
4. Дана соль-
карбонат аммония. Определите тип гидролиза:
а)гидролиз по
аниону; б)гидролиз по катиону;
в)гидролиз по
катиону и аниону; г)гидролизу не подвергается.
5. Гидролиз соли по
катиону. Каким основанием и какой кислотой по силе образована эта соль:
а)сильной кислотой
и сильным основанием; б)слабой кислотой и слабым основанием;
в)слабой кислотой и
сильным основанием; г)сильным основанием и слабой кислотой;
6.Слабый электролит-это..
а)вещество, которое
при растворении в воде или расплавлении полностью диссоциирует на ионы
б) вещество,
которое при растворении в воде или расплавлении неполностью диссоциирует на
ионы
в)вещество, которое не диссоциирует на
ионы
7.Водородный
показатель меньше 7. Какова окраска лакмуса?
а)синяя
б)красная, в)фиолетовая
Задания на соответствие:
1.Соедините формулы из левого столбика с
окраской индикатора лакмуса в правом столбике:
K2CO3
красный
ZnCl2
фиолетовый
KCl
синий
2.Соедините формулы из левого столбика со
значением водородного показателя в правом столбике:
Na2S
PH=7
Al(NO3)3 PH>7
CuSO4 PH<7
NaBr
3.Фенолфталеин можно использовать для обнаружения
в водном растворе соли:
Нитрат
калия фенолфталеин
Сульфат алюминия
Силикат калия
4.Установите соответствие:
Нитрат
магния щелочная
Карбонат калия нейтральная
Бромид
меди(2) кислая
Сульфит калия
5.В водных растворах не подвергается
гидролизу: сульфат натрия. сульфид натрия, хлорид цинка, карбонат калия.
6.В водных растворах происходит гидролиз
по аниону:
Карбонат натрия ,нитрат магния, хлорид
натрия.
7. В водных растворах происходит гидролиз
по катиону:
Сульфит калия, хлорид цинка, бромид калия.
8. Укажите ионное уравнение реакции
хлорида меди(2):
а) СO32-
+H2
O→HCO3
+OH–
б) Cu2+ +H2O
→CuOH+
+H+
в)NH4+ +
H2O → NH3* H2O + H+
Самостоятельная работа
Вариант 1
1.Определите среду раствора солей. формулы
приведены ниже: KCl, NaF,
ZnSO4,
CrCl3,
MgSO4,
LiNO3.
2.Составьте уравнения реакций гидролиза
солей: нитрита натрия, сульфида натрия, карбоната лития, нитрата
железа(3).Определите среду и цвет индикатора.
Вариант 2
1.Определите среду раствора солей. формулы
приведены ниже: AlCl3,
Na2SO3,
Zn(NO3)2,
NaCl,
Na2
SiO3,
K2S.
2. Составьте уравнения реакций гидролиза
солей: нитрата меди(2),силиката калия, сульфата алюминия, хлорида цинка.
Вариант 3
1.Определите среду раствора солей. формулы
приведены ниже:K2S,
CuSO4,
Ba(NO3
)2 , ZnCl2,
Na3
PO4.
2. Составьте уравнения реакций гидролиза
солей: фосфата натрия ,хлорида магния, карбоната аммония, нитрита натрия.
Вариант 4
1.Определите среду раствора солей. формулы
приведены ниже: Al(NO3)3,
K2SO3,
NaCl,
K3PO4,
Na 2CO3
2.Составьте уравнения реакций гидролиза
солей: сульфида аммония, силиката натрия, бромида алюминия, нитрата меди(2).
Литература:
1.Учебник «Химия
для профессий и специальностей технического профиля «О.С.Габриэлян ;И.Г.
Остроумов-М. Академия; 2012
2.Настольная книга
учителя химии 11 класс часть 1 О.С. Габриелян, Г.Г. Лясова,А.Г.
Введенская.-М.: Дрофа,2003.-320с.
Правила составления уравнений гидролиза солей
Алгоритм написания уравнений гидролиза
Гидролиз по катиону
1. Определяем тип гидролиза. Необходимо написать уравнение диссоциации соли.
Гидролиз сульфата меди(II): CuSO4 = Cu 2+ + SO4 2–
Соль образована катионом слабого основания и анионом сильной кислоты. Гидролиз по катиону.
2. Записываем ионное уравнение гидролиза, определяем среду:
Cu 2+ + HOH CuOH + + H + ;
образуется катион гидроксомеди(II) и ион водорода, среда кислая
3. Составляем молекулярное уравнение. Из положительных и отрицательных частиц находящихся в растворе, записываются нейтральные частицы, существующие только на бумаге. В данном случае из CuOH + SO4 2– составляем (CuOH)2SO4. Для уравнивания числа ионов меди необходимо перед сульфатом меди поставить коэффициент два. Получаем:
Продукт реакции относится к группе основных солей: сульфат гидроксомеди(II).
Гидролиз
Темы кодификатора ЕГЭ: Гидролиз солей. Среда водных растворов: кислая, основная и щелочная.
Гидролиз – взаимодействие веществ с водой. Гидролизу подвергаются разные классы неорганических и органических веществ: соли, бинарные соединения, углеводы, жиры, белки, эфиры и другие вещества. Гидролиз солей происходит, когда ионы соли способны образовывать с Н + и ОН — ионами воды малодиссоциированные электролиты.
Гидролиз солей может протекать:
→ обратимо : только небольшая часть частиц исходного вещества гидролизуется.
→ необратимо : практически все частицы исходного вещества гидролизуются.
Для оценки типа гидролиза необходимо рассмотреть соль, как продукт взаимодействия основания и кислоты. Любая соль состоит из металла и кислотного остатка. Металлы соответствует основание или амфотерный гидроксид (с той же степенью окисления, что и в соли), а кислотному остатку — кислота. Например, карбонату натрия Na2CO3 соответствует основание — щелочь NaOH и угольная кислота H2CO3.
Обратимый гидролиз солей
Механизм обратимого гидролиза будет зависеть от состава исходной соли. Можно выделить 4 основных варианта, которые мы рассмотрим на примерах:
1. Соли, образованные сильным основанием и слабой кислотой , гидролизуются ПО АНИОНУ .
CH3COONa + HOH ↔ CH3COOH + NaOH
CH3COO — + Na + + HOH ↔ CH3COOH + Na + + OH —
сокращенное ионное уравнение:
CH3COO — + HOH ↔ CH3COOH + OH —
Таким образом, при гидролизе таких солей в растворе образуется небольшой избыток гидроксид-ионов OH — . Водородный показатель такого раствора рН>7 .
Гидролиз солей многоосновных кислот (H2CO3, H3PO4 и т.п.) протекает ступенчато, с образованием кислых солей:
CO3 2- + HOH ↔ HCO3 2- + OH —
или в молекулярной форме:
или в молекулярной форме:
Продукты гидролиза по первой ступени подавляют вторую ступень гидролиза, в результате вторая ступень гидролиза протекает незначительно.
2. Соли, образованные слабым основанием и сильной кислотой , гидролизуются ПО КАТИОНУ . Пример такой соли: NH4Cl, FeCl3, Al2(SO4)3 Уравнение гидролиза:
или в молекулярной форме:
При этом катион слабого основания притягивает гидроксид-ионы из воды, а в растворе возникает избыток ионов Н + . Водородный показатель такого раствора рН .
Соли, образованные многокислотными основаниями, гидролизуются ступенчато, образуя катионы основных солей. Например:
Fe 3+ + HOH ↔ FeOH 2+ + H +
FeCl3 + HOH ↔ FeOHCl2 + H Cl
FeOH 2+ + HOH ↔ Fe(OH)2 + + H +
FeOHCl2 + HOH ↔ Fe(OH)2Cl+ HCl
Fe(OH)2 + + HOH ↔ Fe(OH)3 + H +
Fe(OH)2Cl + HOH ↔ Fe(OH)3 + HCl
Гидролиз по второй и, в особенности, по третьей ступени практически не протекает при комнатной температуре.
3. Соли, образованные слабым основанием и слабой кислотой , гидролизуются И ПО КАТИОНУ, И ПО АНИОНУ .
В этом случае реакция раствора зависит от соотношения констант диссоциации образующихся кислот и оснований. В большинстве случаев реакция раствора будет примерно нейтральной, рН ≅ 7 . Точное значение рН зависит от относительной силы основания и кислоты.
4. Гидролиз солей, образованных сильным основанием и сильной кислотой , в водных растворах НЕ ИДЕТ .
Сведем вышеописанную информацию в общую таблицу:
Необратимый гидролиз
Необратимый гидролиз происходит, если при гидролизе выделяется газ, осадок или вода, т.е. вещества, которые при данных условиях не могут взаимодействовать между собой. Необратимый гидролиз является химической реакцией, т.к. реагирующие вещества взаимодействуют практически полностью.
Варианты необратимого гидролиза:
- Гидролиз, в который вступают растворимые соли 2х-валентных металлов (Be 2+ , Co 2+ , Ni 2+ , Zn 2+ , Pb 2+ , Cu 2+ и др.) с сильным ионизирующим полем (слабые основания) и растворимые карбонаты/гидрокарбонаты. При этом образуются нерастворимые основные соли (гидроксокарбонаты):
! Исключения: (соли Ca, Sr, Ba и Fe 2+ ) – в этом случае получим обычный обменный процесс:
МеCl2 + Na2CO3 = МеCO3 + 2NaCl (Ме – Fe, Ca, Sr, Ba).
- Взаимный гидролиз , протекающий при смешивании двух солей, гидролизованных по катиону и по аниону. Продукты гидролиза по второй ступени усиливают гидролиз по первой ступени и наоборот. Поэтому в таких процессах образуются не просто продукты обменной реакции, а продукты гидролиза (совместный или взаимный гидролиз). Соли металлов со степенью окисления +3 (Al 3+ , Cr 3+ ) и соли летучих кислот (карбонаты, сульфиды, сульфиты) при смешивании в растворе (взаимном гидролизе) образуют осадок гидроксида и газ (H2S, SO2, CO2):
Соли Fe 3+ при взаимодействии с карбонатами также при смешивании в растворе (взаимном гидролизе) образуют осадок гидроксида и газ:
! Исключения: при взаимодействии солей трехвалентного железа с сульфидами реализуется окислительно-восстановительная реакция:
2FeCl3 + 3K2S(изб) = 2FeS + S↓ + 6KCl (при избытке сульфида калия)
При взаимодействии солей трехвалентного железа с сульфитами также реализуется окислительно-восстановительная реакция.
Полные уравнения таких реакций выглядят довольно сложно. Поначалу я рекомендую составлять такие уравнения в 2 этапа: сначала составляем обменную реацию без участия воды, затем разлагаем полученный продукт обменной реакции водой. Сложив эти две реакции и сократив одинаковые вещества, мы получаем полное уравнение необратимого гидролиза.
3. Гидролиз галогенангидридов и тиоангидридов происходит также необратимо. Галогенангидриды разлагаются водой по схеме ионного обмена (H + OH — ) до соответствующих кислот (в случае водного гидролиза) и солей (в случае щелочного гидролиза). Степень окисления центрального элемента и остальных при этом не изменяется!
Галогенангидрид – это соединение, которое получается, если в кислоте ОН-группу заменить на галоген. При гидролизе галогенангидридов кислот образуются соответствующие данным элементам и степеням окисления кислоты и галогеноводородные кислоты.
Галогенангидриды некоторых кислот:
| Кислота | Галогенангидриды |
| H2SO4 | SO2Cl2 |
| H2SO3 | SOCl2 |
| H2CO3 | COCl2 |
| H3PO4 | POCl3, PCl5 |
Тиоангидриды (сульфангидриды) — так называются, по аналогии с безводными окислами (ангидридами), сернистые соединения элементов (например, Sb2S3, As2S5, SnS2, CS2 и т. п.).
- Необратимый гидролиз бинарных соединений, образованных металлом и неметаллом:
- сульфиды трехвалентных металлов вводе необратимо гидролизуются до сероводорода и и гидроксида металла:
при этом возможен кислотный гидролиз, в таком случае образуются соль металла и сероводород:
- гидролиз карбидов приводит к образованию гидроксида металла в водной среде, соли металла в кислой де и соответствующего углеводорода — метана, ацетилена или пропина:
- Некоторые соли необратимо гидролизуются с образованием оксосолей :
BiCl3 + H2O = BiOCl + 2HCl,
SbCl3 + H2O = SbOCl + 2HCl.
Алюмокалиевые квасцы:
Количественно гидролиз характеризуется величиной, называемой степенью гидролиза .
Степень гидролиза (α) — отношение количества (концентрации) соли, подвергающейся гидролизу, к общему количеству (концентрации) растворенной соли. В случае необратимого гидролиза α≅1.
Факторы, влияющие на степень гидролиза:
1. Температура
Гидролиз — эндотермическая реакция! Нагревание раствора приводит к интенсификации процесса.
Пример : изменение степени гидролиза 0,01 М CrCl3 в зависимости от температуры:
2. Концентрация соли
Чем меньше концентрация соли, тем выше степень ее гидролиза.
Пример : изменение степени гидролиза Na2CO3 в зависимости от температуры:
По этой причине для предотвращения нежелательного гидролиза хранить соли рекомендуется в концентрированном виде.
3. Добавление к реакционной смеси кислоты или щелочи
Изменяя концентрация одного из продуктов, можно смещать равновесие реакции гидролиза в ту или иную сторону.
Гидролиз солей
Гидролиз (от греч. – вода и – разложение) – это разложение водой. Гидролиз солей – это взаимодействие ионов соли с водой с образованием малодиссоциирующих частиц. Давая такое определение реакции гидролиза, мы подчеркиваем, что соли в растворе находятся в виде ионов и движущей силой реакции является образование малодиссоциирующих частиц (общее правило для многих реакций в растворах).
Всегда ли ионы способны образовывать с водой малодиссоциирующие частицы? Разбирая этот вопрос с учениками, отмечаем, что катионы сильного основания и анионы сильной кислоты таких частиц образовать не могут и, следовательно, в реакцию гидролиза не вступают.
Какие типы гидролиза возможны? Поскольку соль состоит из катиона и аниона, то возможны три типа гидролиза:
• гидролиз по катиону (в реакцию с водой вступает только катион);
• гидролиз по аниону (в реакцию с водой вступает только анион);
• совместный гидролиз (в реакцию с водой вступает и катион, и анион).
Гидролиз по катиону. Как катион может взаимодействовать с водой? Учитель сам должен решить, рассматривать ли ему этот вопрос в общем виде или (в менее сильном классе) на конкретном примере. Отмечаем, что катион – это положительно заряженная частица, а молекула воды полярна, условно можно представить ее состоящей из положительно заряженного атома водорода и отрицательно заряженной гидроксильной группы. Какую же часть молекулы воды оторвет и присоединит к себе катион? Ученики с удовольствием отвечают: «Гидроксильную группу!» Ответ подтверждаем записью уравнения, отмечая обратимость реакции:
M n+ + H–OH MOH (n–1)+ + H + .
Написав формулу образовавшейся частицы, тут же обсуждаем, что это за частица, будет ли она иметь заряд и какой, приходим к выводу, что, как правило, это гидроксокатион. А что останется от молекулы воды? Какую реакцию водного раствора обусловливает избыток этих частиц? Какова будет реакция индикатора? А теперь проверим нашу гипотезу (следует демонстрация опыта).
После этого школьники могут самостоятельно сделать вывод: гидролиз по катиону приводит к образованию гидроксокатионов и кислой среды раствора.
Отмечаем, что иногда (при n = 1) вместо гидроксокатионов получаем молекулы слабого основания. А может ли гидроксокатион вступить в реакцию со следующей молекулой воды? Сообщаем, что это будет вторая ступень гидролиза, что каждая следующая ступень протекает в тысячи раз слабее, чем предыдущая, что даже первая ступень протекает обычно на доли процента. Поэтому, как правило, рассматривается только первая ступень гидролиза.
Гидролиз по аниону разбираем аналогично, записывая уравнение:
An n– + H–OH HAn (n–1)– + OH – .
Подводим учеников к выводу: гидролиз по аниону приводит к образованию гидроанионов и щелочной среды раствора.
Совместный гидролиз. Из самого названия следует, что в этом случае в растворе протекают две выше рассмотренные реакции. Предлагаем школьникам проанализировать их и сделать вывод о реакции среды. Опровергаем (можно экспериментом) представление о том, что среда будет нейтральной. Одинаковое число ионов водорода и гидроксид-ионов существует только на бумаге. На самом деле здесь протекают две независимые обратимые реакции, и каких ионов в растворе окажется больше – зависит от степени протекания каждой реакции. А это, в свою очередь, зависит от того, что слабее – кислота или основание. Если слабее основание, то в большей степени будет протекать гидролиз по катиону и среда раствора будет кислой. Если слабее кислота – наоборот. Как исключение возможен случай, когда среда будет почти нейтральной, но это только исключение.
Одновременно обращаем внимание учащихся на то, что связывание гидроксид-ионов и ионов водорода в воду приводит к уменьшению их концентрации в растворе. Предлагаем вспомнить принцип Ле Шателье и подумать, как это повлияет на равновесие. Подводим их к выводу, что при совместном гидролизе степень его протекания будет значительно выше и в отдельных случаях это может привести к полному гидролизу.
Полный гидролиз. Для полного протекания гидролиза нужно, чтобы соль была образована очень слабой кислотой и очень слабым основанием. Кроме того, желательно, чтобы один из продуктов гидролиза уходил из сферы реакции в виде газа. (Малорастворимые вещества, остающиеся в контакте с раствором, вообще говоря, не уходят из сферы реакции, поскольку все равно в какой-то степени растворимы.) Поэтому полному гидролизу подвергаются обычно соли газообразных или неустойчивых кислот: сероводородной, угольной, отчасти сернистой. К ним примыкают вещества, которые в обычном понимании уже не являются солями: нитриды, фосфиды, карбиды, ацетилениды, бориды. Полностью гидролизуются также алкоголяты.
Если вернуться к обычным солям, то полностью гидролизующиеся соли (карбонаты, сульфиды алюминия, хрома(III), железа(III)) нельзя получить реакциями обмена в водных растворах. Вместо ожидаемых продуктов в результате реакции мы получим продукты гидролиза. Гидролиз осложняет протекание многих других реакций обмена. Так, при взаимодействии карбоната натрия с сульфатом меди в осадок обычно выпадает основный карбонат меди (CuOH)2CO3.
В таблице растворимости для полностью гидролизующихся солей стоит прочерк. Однако прочерк может стоять по другим причинам: вещество не изучено, разлагается в ходе окислительно-восстановительной реакции и т.п. Некоторые прочерки, иногда встречающиеся в таблице растворимости, вызывают удивление. Так, сульфид бария хорошо известен и растворим, как и сульфиды других щелочно-земельных металлов. Гидролиз этих солей протекает только по аниону.
Алгоритм написания уравнений гидролиза
Когда школьники поняли суть реакции гидролиза, даем (а лучше составляем вместе с ними) алгоритм написания уравнений гидролиза. Рассмотрим его на конкретных примерах.
Пример 1. Гидролиз сульфата меди(II)
1. Определяем тип гидролиза. На этом этапе школьники могут написать уравнение диссоциации соли:
CuSO4 = Cu 2+ + .
Можно дать им «правило цепочки»: цепочка рвется по слабому звену, гидролиз идет по иону слабого электролита.
Соль образована катионом слабого основания (подчеркиваем) и анионом сильной кислоты. Идет гидролиз по катиону.
2. Пишем ионное уравнение гидролиза, определяем среду:
Cu 2+ + H–OH CuOH + + H + .
Образуется катион гидроксомеди(II) и ион водорода, среда – кислая.
3. Составляем молекулярное уравнение. Надо учитывать, что составление такого уравнения есть некоторая формальная задача. Из положительных и отрицательных частиц, находящихся в растворе, мы составляем нейтральные частицы, существующие только на бумаге. В данном случае мы можем составить формулу (CuOH)2SO4, но для этого наше ионное уравнение мы должны мысленно умножить на два. Получаем:
2CuSO4 + 2H2O (CuOH)2SO4 + H2SO4.
Обращаем внимание, что продукт реакции относится к группе основных солей. Названия основных солей, как и названия средних, следует составлять из названий аниона и катиона, в данном случае соль назовем «сульфат гидроксомеди(II)». (Не надо приставки «ди», не говорим же мы «сульфат динатрия».) Назвать эту соль «гидроксосульфат меди», на наш взгляд, значит нарушить всю логику номенклатуры солей. Разве есть в растворе или в узлах кристаллической решетки частица «гидроксосульфат»? Нет! А катион гидроксомеди есть. В дальнейшем этот подход распространяется на номенклатуру комплексных солей.
Пример 2. Гидролиз ортофосфата рубидия
1. Определяем тип гидролиза:
Рубидий – щелочной металл, его гидроксид – сильное основание, фосфорная кислота, особенно по своей третьей стадии диссоциации, отвечающей образованию фосфатов, – слабая кислота. Идет гидролиз по аниону.
2. Пишем ионное уравнение гидролиза, определяем среду:
+ H–OH + OH – .
Продукты – гидрофосфат- и гидроксид-ионы, среда – щелочная.
3. Составляем молекулярное уравнение:
Rb3PO4 + H2O Rb2HPO4 + RbOH.
Получили кислую соль – гидрофосфат рубидия.
Пример 3. Гидролиз ацетата алюминия
1. Определяем тип гидролиза:
Соль образована катионом слабого основания и анионами слабой кислоты. Идет совместный гидролиз.
2. Пишем ионные уравнения гидролиза, определяем среду:
Al 3+ + H–OH AlOH 2+ + H + ,
CH3COO – + H–OH CH3COOH + OH – .
Учитывая, что гидроксид алюминия очень слабое основание, предположим, что гидролиз по катиону будет протекать в большей степени, чем по аниону. Следовательно, в растворе будет избыток ионов водорода, и среда будет кислая.
Не стоит пытаться составлять здесь суммарное уравнение реакции. Обе реакции обратимы, никак друг с другом не связаны, и такое суммирование бессмысленно.
3. Составляем молекулярное уравнение:
Al(CH3COO)3 + H2O AlOH(CH3COO)2 + CH3COOH.
Это тоже формальное упражнение, для тренировки в составлении формул солей и их номенклатуре. Полученную соль назовем ацетат гидроксоалюминия.
Факторы, влияющие на степень гидролиза
Поскольку гидролиз – обратимая реакция, то на состояние равновесия гидролиза влияют температура, концентрации участников реакции, добавки посторонних веществ. Если в реакции не участвуют газообразные вещества, то давление практически не влияет. Исключается из рассмотрения вода, т.к. ее концентрация в водных растворах практически постоянна
(
55 моль/л). Так, для примеров 1 и 2 выражения констант равновесия (констант гидролиза) имеют вид:
Температура. Поскольку реакция гидролиза эндотермическая, повышение температуры смещает равновесие в системе вправо, степень гидролиза возрастает.
Концентрация продуктов гидролиза. В соответствии с принципом Ле Шателье повышение концентрации ионов водорода для реакции, рассмотренной в примере 1, приведет к смещению равновесия влево, т.е. степень гидролиза будет уменьшаться. Также будет влиять увеличение концентрации гидроксид-ионов для реакции, рассмотренной в примере 2.
Концентрация соли. Рассмотрение этого фактора приводит к парадоксальному выводу: равновесие в системе смещается вправо (в соответствии с принципом Ле Шателье), но степень гидролиза уменьшается.
Понять это помогает константа равновесия. При добавлении соли, т.е. фосфат-ионов в примере 2, равновесие будет смещаться вправо, концентрации гидрофосфат- и гидроксид-ионов будут возрастать. Но из рассмотрения константы равновесия этой реакции ясно, что, для того чтобы увеличить концентрацию гидроксид-ионов вдвое, нам надо концентрацию фосфат-ионов увеличить в 4 раза! Ведь значение константы должно быть неизменным. А это значит, что степень гидролиза, под которой можно понимать отношение [OH – ]/[], уменьшится вдвое.
Разбавление. Этот фактор означает одновременное уменьшение концентрации всех частиц в растворе (не считая воды). В соответствии с принципом Ле Шателье такое воздействие приводит к смещению равновесия в сторону реакции, идущей с увеличением числа частиц. Реакция гидролиза протекает (без учета воды!) с увеличением числа частиц. Следовательно, при разбавлении равновесие смещается в сторону протекания этой реакции, т.е. вправо, степень гидролиза возрастает. К этому же выводу приведет рассмотрение константы гидролиза.
Добавки посторонних веществ могут влиять на положение равновесия в том случае, когда эти вещества реагируют с одним из участников реакции. Так, при добавлении к раствору сульфата меди в примере 1 раствора гидроксида натрия содержащиеся в нем гидроксид-ионы будут взаимодействовать с ионами водорода. В результате их концентрация уменьшится, и по принципу Ле Шателье равновесие в системе сместится вправо, степень гидролиза возрастет. Если к тому же раствору добавить раствор сульфида натрия, то равновесие сместится не вправо, как можно было бы ожидать (взаимное усиление гидролиза), а влево из-за связывания ионов меди в практически нерастворимый сульфид меди.
Практическое применение
На практике с гидролизом учителю приходится сталкиваться, например, при приготовлении растворов гидролизующихся солей, в частности ацетата свинца. Обычная методика: в колбу наливаем воду, засыпаем соль, взбалтываем. Остается белый осадок. Добавляем еще воды, взбалтываем – осадок не исчезает. Добавляем из чайника горячей воды – осадка кажется еще больше…
Причина в том, что одновременно с растворением идет гидролиз соли, и белый осадок, который мы видим, – это уже продукты гидролиза – малорастворимые основные соли. Все наши дальнейшие действия – разбавление, нагревание – только усиливают степень гидролиза.
Как же подавить гидролиз? Не нагревать, не готовить слишком разбавленных растворов и, поскольку главным образом мешает гидролиз по катиону, добавить кислоты, лучше соответствующей, т.е. уксусной.
В других случаях степень гидролиза желательно увеличить. Например, чтобы сделать щелочной моющий раствор бельевой соды более активным, мы его нагреваем – степень гидролиза карбоната натрия при этом возрастает.
Важную роль играет гидролиз в процессе обезжелезивания воды методом аэрации. При насыщении воды кислородом содержащийся в ней гидрокарбонат железа(II) окисляется до соли железа(III), значительно сильнее подвергающийся гидролизу. В результате происходит полный гидролиз, и железо отделяется в виде осадка гидроксида железа(III).
На этом же основано применение солей алюминия в качестве коагулянтов в процессах очистки воды. Добавляемые в воду соли алюминия в присутствии гидрокарбонат-ионов полностью гидролизуются, и объемистый гидроксид алюминия коагулирует, увлекая с собой в осадок различные примеси.
Гидролиз в заданиях ЕГЭ по химии
ВОПРОС А26 (2003 г.). Фенолфталеин можно использовать для обнаружения в водном растворе соли:
1) ацетата алюминия; 2) нитрата калия; 3) сульфата алюминия; 4) силиката натрия.
Фенолфталеин – индикатор на щелочную среду, в которой он принимает малиновую окраску (возможно, для многих камнем преткновения в этом вопросе стало незнание окрасок индикаторов: фенолфталеина, лакмуса, метилоранжа). В растворе соли щелочная среда может возникнуть при гидролизе по аниону.
1) ацетат алюминия рассмотрен выше, идет совместный гидролиз, среда получается слабокислая;
2) нитрат калия образован сильными кислотой и основанием, гидролиз не идет, среда нейтральная;
3) сульфат алюминия образован сильной кислотой и слабым основанием, гидролиз идет по катиону, среда получается кислая;
4) силикат натрия образован слабой кислотой и сильным основанием, гидролиз идет по аниону, среда получается щелочная:
+ H2O H + OH – .
Ответ. 4.
ВОПРОС A29 (демонстрационный вариант, 2005 г.). Среда раствора карбоната калия:
1) щелочная; 2) кислая; 3) нейтральная; 4) слабокислая.
Рассмотрение аналогичное.
Ответ. 1.
ВОПРОС B5 (демонстрационный вариант, 2005 г.). Установите соответствие между формулой соли и ионным уравнением гидролиза этой соли.
| Формула соли: | CCCCC | Ионное уравнение: |
| 1) CuSO4; | а) CH3COO – + H2O CH3COOH + OH – ; | |
| 2) K2CO3; | б) + H2O NH3•H2O + H + ; | |
| 3) CH3COONa; | в) Сu 2+ + H2O Cu(OH) + + H + ; | |
| 4) (NH4)2SO4. | г) + H2O H + OH – ; | |
| д) Сu 2+ + 2H2O Cu(OH)2 +2H + . |
Пример не слишком удачного вопроса. С одной стороны, трудно на него не ответить, исходя из простого сопоставления формул в левой и правой колонках (про гидролиз можно при этом ничего не знать). С другой стороны, оба ионных уравнения для катиона меди можно считать правильными, но уравнение д) мы бы назвали суммарным для двух стадий гидролиза и отметили бы, что степень протекания реакции по нему чрезвычайно мала. Только на основе этого мы выберем уравнение в).
Ответ. 1 – в; 2 – г; 3 – а; 4 – б.
ВОПРОС В3 (2004 г.). Установите соответствие между условиями и состоянием химического равновесия процесса гидролиза солей.
Условия смещения равновесия:
1) нагревание раствора;
2) добавление продуктов гидролиза;
3) охлаждение раствора;
4) разбавление раствора.
а) смещается влево;
б) смещается вправо;
в) не смещается.
Используем установленные выше закономерности.
Ответ. 1 – б; 2 – а; 3 – а; 4 – б.
ВОПРОС С1 (2004 г.). Как скажется на состоянии химического равновесия в системе
Zn 2+ + H2O ZnOH + + H + – Q:
2) добавление KOH;
3) нагревание раствора?
При ответе на этот вопрос надо учитывать, что добавляемые вещества – электролиты. Поставляемые ими ионы могут как непосредственно влиять на равновесие, так и взаимодействовать с одним из ионов, участвующих в обратимой реакции:
H2SO4 = 2H + + ,
повышение концентрации ионов водорода приводит по принципу Ле Шателье к смещению равновесия в системе влево;
2) добавление KOH:
гидроксид-ионы связывают ионы водорода в малодиссоциирующее вещество – воду
(H + + OH – = H2O); снижение концентрации ионов водорода приводит по принципу Ле Шателье к смещению равновесия в системе вправо;
3) нагревание раствора по принципу Ле Шателье приводит к смещению равновесия в сторону протекания эндотермической реакции, т.е. вправо.
Ответ на все три элемента вопроса оценивался в 3 балла.
Попробуйте самостоятельно ответить на следующие вопросы.
ВОПРОС А26 (2003 г.). Между собой водные растворы сульфата и фосфата натрия можно различить с помощью:
1) гидроксида натрия;
2) серной кислоты;
3) фенолфталеина;
4) фосфорной кислоты.
ВОПРОС В3 (2003 г.). Установите соответствие между названиями солей и средой их растворов.
1) нитрит калия;
2) сульфат железа(II);
3) карбонат калия;
4) хлорид алюминия.
а) кислая;
б) нейтральная;
в) щелочная.
ВОПРОС В3 (2004 г.). Установите соответствие между формулой соли и способностью этой соли к гидролизу.
Способность к гидролизу:
а) гидролиз по катиону;
б) гидролиз по аниону;
в) гидролиз по катиону и аниону;
г) гидролизу не подвергается.
ВОПРОС С1 (2003 г.). Сульфид-ион – типичный протолит. Напишите уравнение протолиза (гидролиза) сульфид-иона в водном растворе по первой ступени. Укажите среду этого раствора. Как скажется добавление гидроксида натрия на степень протолиза сульфид-ионов?
Подводя итог, отметим, что в рамках школьного курса в реакциях гидролиза солей нет ничего чрезмерно сложного для понимания школьника. Здесь используются общие правила написания ионных уравнений, общие представления о смещении химического равновесия, общий подход к номенклатуре солей, краткий и удобный алгоритм написания уравнений. Хочется надеяться, что изложенный материал поможет вам и вашим ученикам.
[spoiler title=”источники:”]
http://chemege.ru/gidroliz/
http://him.1sept.ru/article.php?ID=200501003
[/spoiler]
При растворении
веществ в воде происходит взаимодействие
растворенного вещества с молекулами
воды. Это взаимодействие приводит к
реакциям гидролиза.
Реакции обменного
разложения веществ водой называются
реакциями гидролиза.
Гидролизу
подвергаются различные вещества:
неорганические
– соли, карбиды и гидриды металлов,
галогениды неметаллов; органические
– сложные эфиры, жиры, белки, углеводы.
Гидролиз органических веществ
имеет большое
биологическое значение для живых
организмов. Из курса общей биологии
вспомните, что происходит в живых
организмах со сложными органическими
веществами? (В живых организмах происходит
ферментативный гидролиз жиров, белков
и углеводов).
Обратить
внимание:
В лабораторной работе исследовались
разные по составу соли. Разберем состав
исследуемых солей.
Nа2
CO3
NaOH
H2CO3
сильное слабая
осн-ние кислота
А1Cl3
А1(ОН)3
HCl
слабое сильная
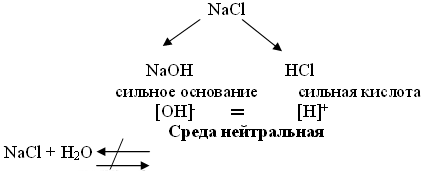
осн-ние кислота
NaСI
NaOH
HCI
сильное сильная
осн-ние кислота
Соль можно
рассматривать как продукт взаимодействия
кислоты и основания. В зависимости от
вида кислоты и вида основания выделяют
четыре типа
солей:
1.Соль, образованная
сильным основанием и слабой кислотой
2.Соль, образованная
слабым основанием и сильной кислотой
3.Соль, образованная
слабым основанием и слабой кислотой
4.Соль, образованная
сильным основанием и сильной кислотой
4. Составление уравнений гидролиза
Рассмотрим
процессы, происходящие в растворах
исследуемых солей.
1) К какому типу
солей относится карбонат натрия?
Соль,
образованная сильным основанием и
слабой кислотой.
Карбонат-ионы
прочно связывают катионы водорода, так
как угольная кислота слабая. Катионы
натрия не могут быть связаны
гидроксид-ионами, так как гидроксид
натрия – сильное основание и диссоциирует
полностью.
Уравнение
показывает, что:
-
в растворе есть
свободные гидроксид-ионы ОН–
и их концентрация больше, чем в чистой
воде, поэтому раствор соли имеет
щелочную
среду, -
в реакции с водой
участвуют анионы СО-2;
в таком случае говорят, что идет гидролиз
по аниону.
2)
К какому типу солей относится хлорид
алюминия?
Соль,
образованная слабым основанием и
сильной кислотой.
Уравнение
показывает, что:
-
в растворе есть
свободные ионы водорода Н+
и их концентрация больше чем в чистой
воде, поэтому раствор соли имеет
кислотную
среду;
-
в реакции с водой
участвуют катионы А13+;
в таком случае говорят, что идет гидролиз
по катиону.
3) К какому типу
солей относится хлорид натрия?
Соль,
образованная сильным основанием и
сильной кислотой.
ΝаCl
↔ Νа+ +
Cl
–
;
HOH
↔ H+ +
OH–
В данном случае
при диссоциации соли не образуются
слабые ионы и, следовательно, не
образуется слабый электролит. Все ионы
останутся в растворе, они не могут
объединяться, так как при этом не
образуются слабые электролиты –
гидролиз не происходит. Среда
раствора нейтральная, так как
концентрации ионов Н+
и ОН–
в растворе равны, как в чистой воде.
4) Проблемный
вопрос: А
что происходит в растворах солей,
образованных слабым основанием и
слабой кислотой?
К какому типу
солей относится ацетат аммония?
Соль,
образованная слабым основанием и слабой
кислотой.
СН3СООΝН4
↔ СН3СОО–
+ΝН4+
HOH
↔H+- +
OH-
Слабым ионом будут
катион и анион. Гидролиз будет идти
одновременно по
катиону и аниону.
СН3СООΝН4+ HOH
↔ СН3СООН+
ΝН4 ОН
среда будет слабокислая или слабощелочная
в зависимости от Кд кислоты или основания.
Константы дссоциации уксусной кислоты
и гидроксида аммония равны соответственно:
К(СН3СООН)
= 1,76×10-5
и К(NH4
ОН) = 1,79×10-5
=> среда при гидролизе этой соли
нейтральная.
Соль может
подвергаться сразу полному и необратимому
гидролизу, например, если образец соли
Al2S3
опустить в воду, моментально происходит
бурная реакция гидролиза:
Al2
S3
+
6H2O
= 2Al(OH)3
+ 3H2S
Этот гидролиз
необратим, поэтому реакцией обмена в
растворе Al2S3
получить нельзя. Вместо него образуются
продукты гидролиза.
2AlCl3
+
3Na2S
+ 6H2O
= 2Al(OH)3
+ 3H2S
+ 6NaCl
На гидролиз влияет
не только природа вещества, но и другие
факторы, например разбавление раствора
увеличение количества воды в растворе
усиливает гидролиз. При нагревании
гидролиз также усиливается.
Такие соли
подвергаются гидролизу и по катиону,
и по аниону.
Катион слабого
основания связывает ионы ОН–
из молекул воды, образуя слабое основание;
анион слабой кислоты связывает ионы
Н+
из молекул воды, образуя слабую кислоту.
Реакция растворов этих солей может
быть нейтральной, слабокислотной или
слабощелочной. Это зависит от констант
диссоциации двух слабых электролитов
– кислоты и основания, которые образуются
в результате гидролиза.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
12.08.2019203.78 Кб2Г1.doc
- #
12.08.2019986.62 Кб1Г2.doc
- #
- #
- #
- #
- #
- #
- #