Лечение рака – это всегда сотрудничество между врачом и пациентом. Чтобы правильно выполнять рекомендации онколога и эффективно бороться с заболеванием, больному нужно быть хорошо информированным. В интернете можно найти массу информации, но каждый случай индивидуален, поэтому не нужно бояться задавать вопросы лечащему врачу.
Сегодня врачи федеральной сети клиник экспертной онкологии «Евроонко» расскажут о том, какие вопросы стоит в первую очередь задать онкологу, если у вас или вашего близкого диагностировали колоректальный рак.
«У меня рак толстой или прямой кишки? В чем между ними разница?»
«Рак кишки» и «колоректальный рак» – собирательные термины. Примерно у двух третей таких пациентов злокачественная опухоль находится в толстой кишке, у трети – в прямой кишке.
Рак толстой кишки является одним из самых распространенных и в то же время одним из наиболее успешно излечимых. В большинстве случаев при I, II и III стадии можно выполнить радикальную операцию. С раком прямой кишки бороться сложнее, он чаще рецидивирует и в целом при нем хуже прогноз. Тем не менее, существуют эффективные методы лечения.
«Какие методы лечения вы планируете применять, и как они повлияют на мою жизнь?»
При I–III стадиях колоректального рака обычно основным методом лечения является хирургическое вмешательство. После него может быть проведен курс химиотерапии, лучевой терапии.
Иногда сначала применяют химиопрепараты или облучение, чтобы уменьшить злокачественное новообразование, и затем выполняют хирургическое вмешательство.
Лечение рака требует госпитализации в стационар, впоследствии придется периодически посещать клинику для проведения процедур. Пациенту нужно соблюдать некоторые рекомендации врача. В некоторых случаях накладывают временную или постоянную колостому: на кожу из кишки выводят отверстие для отхождения стула. За колостомой нужно правильно ухаживать. В целом во время лечения многие пациенты могут продолжить привычный образ жизни и заниматься многими любимыми делами.
«Какие возможны побочные эффекты?»
Если вам предстоит курс химиотерапии, то нужно понимать, что он может сопровождаться некоторыми побочными эффектами. Расспросите о них врача. Спросите, какие меры будут приняты, чтобы их предотвратить, что делать, если они всё же возникли, и о каких симптомах нужно немедленно сообщить медработникам.
«Должен ли я придерживаться специальной диеты?»
В большинстве случаев кардинальных изменений в рационе питания не требуется. Достаточно придерживаться общих рекомендаций – их нужно соблюдать любому здоровому человеку, чтобы снизить риск развития колоректального рака. Необходимо максимально сократить потребление красного и обработанного мяса, фастфуда. Основу рациона должны составлять овощи и фрукты, продукты, богатые клетчаткой.
«Поможет ли мне химиотерапия?»
Онкологи подбирают комбинации химиопрепаратов в соответствии с современными международными протоколами лечения. Их эффективность доказана в многочисленных крупных клинических испытаниях.
В процессе лечения проводят контрольные обследования, чтобы проверить, насколько эффективно работают препараты. Если химиотерапия проводится до операции, опухоль должна уменьшиться, а показателем успеха послеоперационной терапии является отсутствие рецидива.
«Какую операцию мне планируется выполнить? Как она поможет?»
При колоректальном раке проводят разные виды операций, их можно выполнять открытым (через разрез) или лапароскопическим (через проколы в брюшной стенке) способом. Рак на самых ранних стадиях можно удалить без разреза, во время колоноскопии.
Хирургические вмешательства в онкологии бывают радикальными и паллиативными. В первом случае врач стремится полностью удалить опухоль и добиться ремиссии, во втором – улучшить состояние пациента, справиться с симптомами.
«Нужно ли мне проконсультироваться с клиническим генетиком?»
Существуют наследственные формы колоректального рака, связанные с нарушениями в определенных генах. В таких случаях генетическое тестирование поможет не только больному, но и его родственникам. Они тоже могут оказаться носителями дефектного гена, и знание об этом поможет своевременно принять профилактические меры.
«Куда можно обратиться за психологической поддержкой?»
Когда человек узнаёт о том, что у него обнаружена злокачественная опухоль, он испытывает сильный стресс, эмоциональный шок. Тревожность, депрессия, навязчивые страхи и другие психоэмоциональные проблемы часто сопутствуют онкологическим заболеваниям. С ними нужно бороться. Вы можете спросить у вашего лучащего онколога, куда лучше обратиться за помощью.
В настоящее время существуют психологи, которые специализируются на работе с онкологическими больными – онкопсихологи. В России их пока еще очень мало. В клиниках «Евроонко» работает такой специалист – Ирина Валерьевна Мансурова. Записаться на приём к Ирине Валерьевне можно по телефону: 8 (800) 301-11-35
Мы написали для вас другие статьи о раке:
Рак кишечника имеет второе название – колоректальный рак. Злокачественные новообразования чаще развиваются в прямой, сигмовидной, нисходящей и восходящей кишке. Реже патологию выявляют в поперечной, слепой кишке, аппендиксе и тонком кишечнике. В Юсуповской больнице раннюю диагностику рака кишечника проводят с помощью новейших диагностических процедур и точных методов лабораторной диагностики.
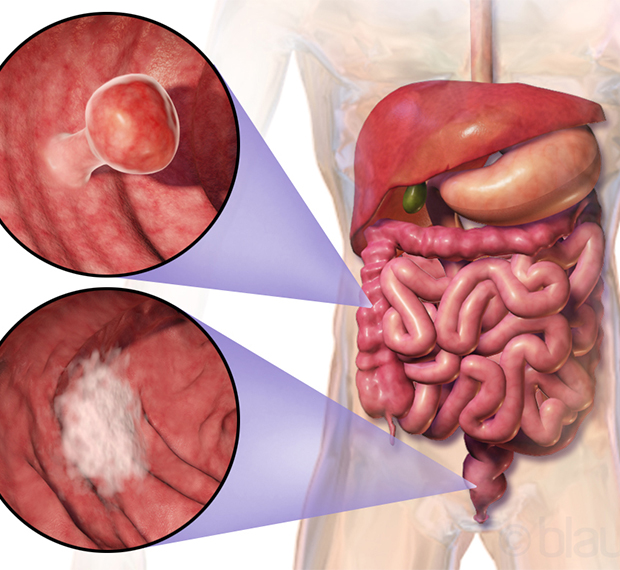
При выявлении злокачественной опухоли кишечника в виде рака в начальной стадии онкологического процесса врачи клиники онкологии проводят комплексную терапию. Она включает следующие компоненты:
- Инновационные оперативные вмешательства;
- Химиотерапию эффективнейшими лекарственными средствами, обладающими минимальным спектром побочных эффектов;
- Лучевую терапию с помощью новейшей аппаратуры, позволяющей целенаправленно воздействовать на опухоль, не повреждая окружающие ткани.
При отсутствии технической возможности провести радикальную операцию проводят паллиативные хирургические вмешательства.
Записаться на консультацию
Причины возникновения рака кишечника
Причины рака кишечника еще находятся на стадии изучения. Существуют определенные факторы, которые могут увеличивать вероятность развития раковых новообразований. Эти же факторы влияют на то, как долго развивается рак кишечника. К данным факторам относятся:
|
Причины |
Описание |
|
Наследственность |
Генетическая предрасположенность к развитию рака автоматически включает человека в группу риска. При наличии рака в семейном анамнезе человеку необходимо особенно бережно относиться к своему здоровью, вовремя лечить заболевания. |
|
Различные болезни кишечника |
Развитию рака часто предшествуют воспалительные и опухолевые заболевания слизистой оболочки кишечника: полипы, аденомы, болезни Крона, язвенный колит. Данные заболевания не являются злокачественными, но могут создавать условия для появления раковых клеток. |
|
Нерациональное питание |
Употребление в пищу слишком жирной пищи, большого количества простых углеводов, отсутствие продуктов с клетчаткой приводит к появлению запоров. Плотные каловые массы способны нарушать целостность стенок кишечника, вызывая микротрещины и нарушая его работу. Это может приводить к перерождению здоровых клеток в злокачественные. |
|
Вредные привычки |
Сигареты, алкоголь, наркотики являются канцерогенами и провоцируют перерождение клеток. |
|
Влияние окружающей среды |
Загрязненная атмосфера, постоянный контакт с вредными веществами (асбест, ртуть и др.), способны вызывать рак различных органов и систем. |
Сколько развивается рак кишечника – вопрос индивидуальный. Это будет зависеть от общего состояния здоровья человека и интенсивности влияния провоцирующего фактора.
Какой бывает рак в кишечнике
В соответствии с Международной классификацией болезней (МКБ 10), рак кишечника разделяют на следующие основные виды:

В злокачественную опухоль может переродиться доброкачественное новообразование – аденома кишечника. Она образуется у пациентов, которые страдают хроническим колитом, язвой или гастритом. В кишечнике образуются и другие доброкачественные новообразования: полипы, фибромы, липомы, ангиомы.
Стадии рака кишечника
Выделяют 4 стадии рака кишечника. Они отличаются в зависимости от степени прогрессирования заболевания и клинических проявлений. На 1-2 стадиях симптомы бывают незаметны для больного, хотя в это время онкологический процесс поражает все больше здоровой ткани. В этом и заключается сложность рака кишечника. Больной обращается к врачу на 3-4 стадиях, когда заболевание уже очень сложно вылечить.
Клиницисты выделяют 4 стадии рака кишечника:
-
На первой стадии рака заболевание не проявляется клиническими симптомами. Незначительные признаки интоксикации пациент относит к обычному недомоганию. На слизистой кишечника или под слизистой оболочкой образуется небольшое плотное образование. Метастазы в лимфатические узлы отсутствуют.
-
На второй стадии рака опухоль перекрывает просвет кишечника на треть или половину. Могут поражаться ближайшие к новообразованию лимфатические узлы, но отдалённых метастазов нет.
-
Третья стадия рака кишечника проявляется нарушением работы кишечника, которое вынуждает человека обратиться к врачу. Злокачественное новообразование перекрывает просвет кишечника полностью или на одну треть. Атипичные клетки выявляют в удалённых от опухоли лимфатических узлах. Метастазы отсутствуют.
- При четвёртой стадии рака может развиться прободение кишечника, острая кишечная непроходимость, кишечное кровотечение. Наблюдаются множественные метастазы. Выражена интоксикация организма продуктами распада опухоли.
Симптомы рака кишечника
Колоректальный рак имеет множество клинических проявлений, что иногда становится причиной диагностических ошибок. Большую роль в выявлении рака кишечника на ранней стадии играет профессионализм врачей, которые впервые сталкиваются с пациентом. Симптоматика заболевания включает появление крови в кале, боли или неприятные ощущения в области живота, диарею, потерю веса. Симптоматика развития опухоли кишечника имеет схожесть с симптомами хронического расстройства пищеварения, симптомами других заболеваний – это часто становится причиной несвоевременной постановки диагноза.
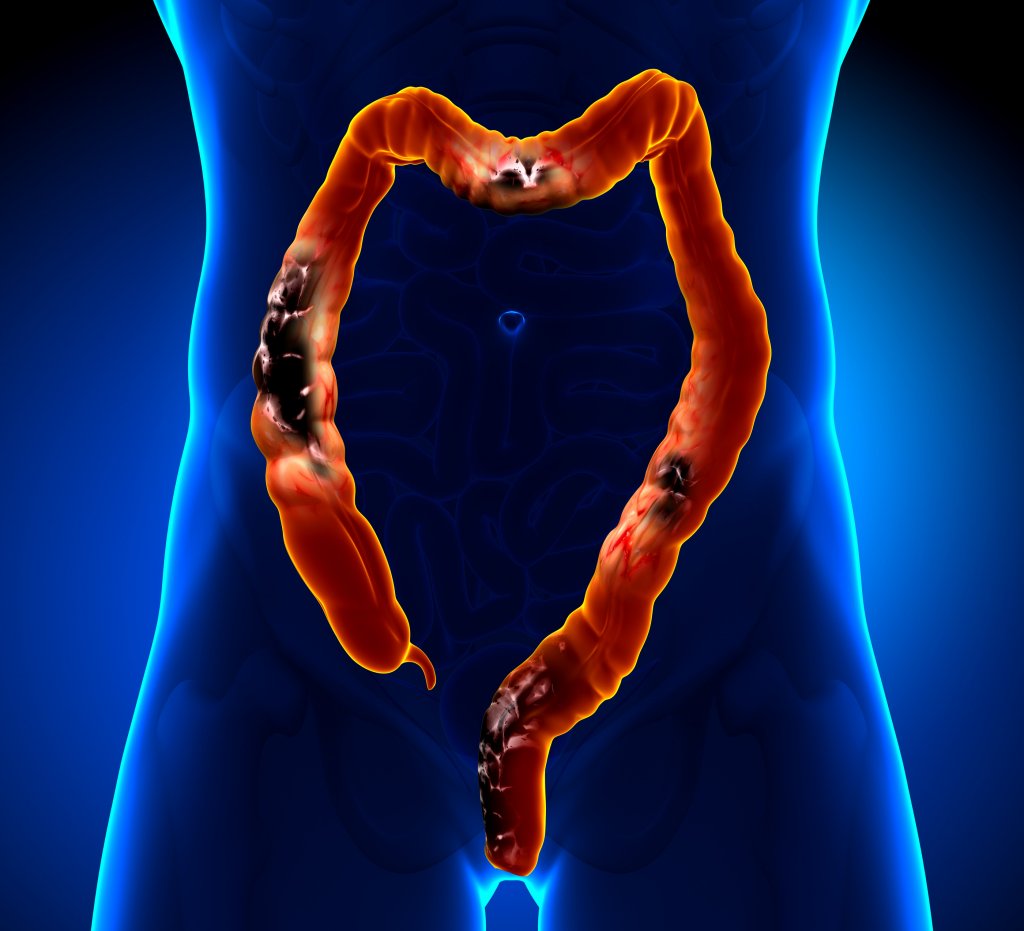
На ранней стадии заболевания пациенты предъявляют жалобы на хроническую усталость, редкие или частые позывы к дефекации. В анализе крови уменьшается количество эритроцитов и гемоглобина. Вначале терапевты не могут установить причины прогрессирующей анемии. В связи с тем, что симптоматика рака кишечника схожа с признаками других заболеваний, вызывающих хроническое расстройство пищеварения, врачи часто несвоевременно устанавливают точный диагноз. Если опухоль перекрывает просеет кишки, развивается кишечная непроходимость. Она проявляется прекращением отхождения кала и газов, вздутием кишечника. Развиваются признаки «острого живота». В этом случае хирурги выполняют ургентную операцию.
Первые признаки и симптомы рака кишечника на ранней стадии
Степень выраженности симптомов рака кишечника возрастает по мере роста и распространения опухоли. Первые признаки рака кишечника на ранней стадии почти не привлекают внимания больного, слабо выражены. Патологические признаки, которые указывают на развитие злокачественного заболевания – это появление слизи и крови в кале.
В начале проявления опухоли кровь выделяется в виде прожилок, затем количество крови в кале возрастает, появляются сгустки, иногда со зловонным запахом. Цвет кровянистых выделений – от темного окраса до почти черного цвета. Очень часто у больных раком кишечника в начальных стадиях роста опухоли развивается тахикардия.
Проявления рака кишечника в зависимости от его вида
Морфологи различают следующие гистологические виды рака кишечника:
-
Аденокарциному;
-
Карциному;
-
Лимфому;
-
Саркому.
Аденокарцинома чаще локализуется в толстой кишке. Она проявляется быстрой утомляемостью, повышением температуры тела, постоянными запорами, интенсивными болями в животе.
При наличии карциномы кишечника у пациентов возникает боль и ощущение распирания в животе, запоры или поносы. У них ухудшается аппетит, появляются слизистые и кровянистые выделения из заднего прохода.
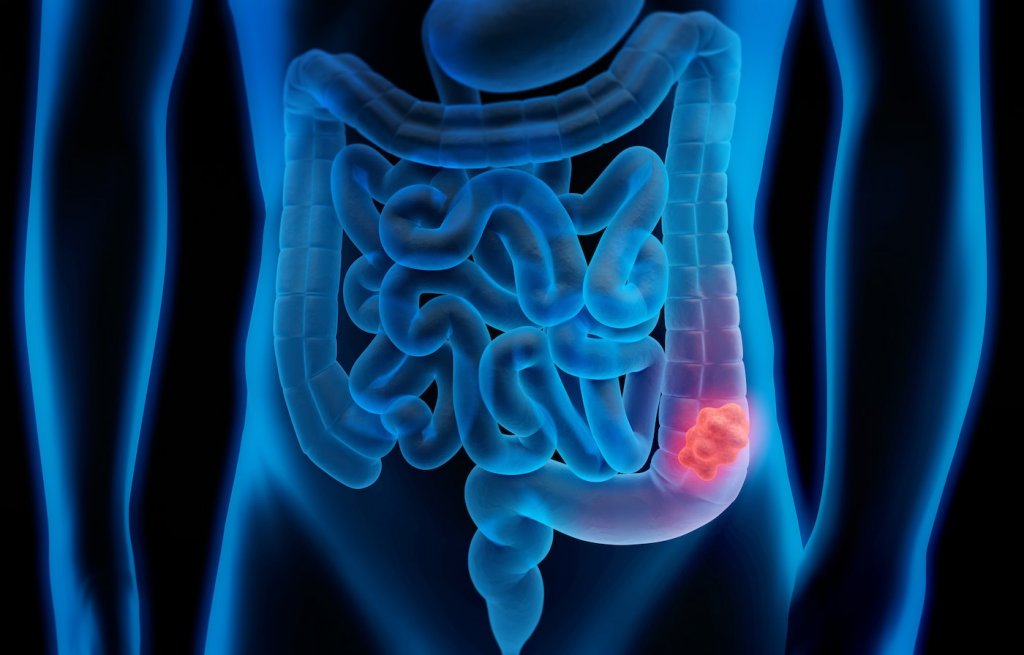
Лимфома кишечника проявляется отсутствием аппетита, тошнотой, вздутием живота, хронической усталостью. У пациентов увеличивается образование в кишечнике газов, повышается температура тела, развивается анемия.
Для саркомы характерны расстройства стула, появление изжоги, крови в кале. Пациентов беспокоит боль при прохождении каловых масс через кишечник, интенсивные боли внизу живота, периодические боли, которые возникают после принятия неудобной позы или еды.
Рак кишечника у женщин и мужчин
Признаки онкологии кишечника у мужчин и женщин встречаются одинаково часто, они совсем немного уступают раку груди у женщин и раку желудка и легких у мужчин.
Первые признаки рака кишечника у женщин
У женщин онкологи чаще выявляют рак ободочной кишки. Симптомы рака кишечника у женщин могут появиться в любом возрасте, но риск его развития возрастает после 40 лет. Самый высокий процент заболевших отмечается в возрасте от 60 лет и старше.
Наиболее частая причина рака ободочной кишки у женщин – перерождение кишечных полипов. Опухоль чаще возникает у женщин с отягощённой наследственностью, ведущих малоподвижный образ жизни, употребляющих в пищу много мяса (особенно говядины).
Симптомы заболевания появляются спустя два года от начала развития патологического процесса. Пациенток беспокоит боль в животе, вздутие, нарушение стула. При прогрессировании болезни опухоль даёт метастазы в лимфатические узлы, влагалище и другие органы.
На ранних стадиях развития рака кишечника симптомы и проявления у женщин не отличаются от симптомов заболевания раком у мужчин. Появляются запоры, боль может отдавать в область прямой кишки. Более поздние проявления рака кишечника характеризуются недержанием стула, сильными болями в области кишечника, боли могут беспокоить в области влагалища, заднепроходного отверстия.
Развивается рвота, появляются урогенитальные свищи. Метастазирование опухоли в область мочевого пузыря проявляется новыми симптомами – изменением мочи. Моча становится мутной, приобретает запах кала. Из-за постоянных кровотечений развивается анемия, может развиться тяжелая форма заболеваний мочевого пузыря и почек.
У женщин дополнительно могут возникать нарушения менструального цикла, изменение вкусовых предпочтений.
Причины и симптомы рака кишечника у мужчин
У мужчин чаще встречается рак прямой кишки. Заболевание просто диагностировать, но в связи с тем, что его симптомы напоминают признаки другой патологии кишечника, пациенты поздно обращаются за медицинской помощью. Причины визита к врачу, следующие:
-
Кровь на поверхности кала;
-
Изменение формы и консистенции каловых масс;
-
Боль в заднем проходе;
-
Поносы или запоры.
Симптомы рака кишечника у мужчин являются классическими и сочетают в себе нарушение работы ЖКТ, но при метастазировании часто поражается простата.
При пальцевом исследовании проктологи определяют опухолевидное образование. Наиболее частая причина рака кишечника у мужчин – курение, злоупотребление спиртными напитками, кулинарные предпочтения (употребление в пищу жирной, острой, жареной пищи). Рак кишечника у мужчин может развиться на фоне полипов кишечника, неспецифического язвенного колита, ожирения, нелеченного геморроя.

Метастазы
При раке кишечника чаще всего первой метастазируется печень. Это происходит на 4-ой стадии заболевания. Прогноз рака кишечника 4 стадии с метастазами будет зависеть от степени поражения тканей и органов. При прохождении лечения и соблюдении рекомендаций врача больной может прожить еще около 2-х лет.
Метастазы рака кишечника 4 стадии могут поражать забрюшинное пространство и брюшину, органы малого таза, поджелудочную железу, мочевой пузырь, легкие. Неблагоприятные симптомы метастазов в кишечнике будут следующими:
-
Прорастание опухоли в жировую клетчатку;
-
Перфорирование толстой кишки;
-
Распространение раковых клеток на соседние органы;
-
Наличие раковых клеток с низкой степенью дифференцировки.
Диагностика рака кишечника
Очень важна точная диагностика рака кишечника для составления адекватной результативной терапии. В Юсуповской больнице онкологи проводят диагностику рака кишечника с помощью современного оборудования, обладающего высокой разрешающей способностью. Обследование пациента начинают с пальцевого исследования прямой кишки. Этот простой диагностический метод позволяет выявить рак прямой кишки.
Затем гастроэнтерологи применяют рентгенологические и эндоскопические методы исследования: ректороманоскопию, колоноскопию. Во время ректороманоскопии врач проводит осмотр слизистой оболочки прямой кишки. В некоторых случаях исследуются дистальные отделы сигмовидной кишки. С помощью колоноскопии оценивают состояние толстой кишки. Во время эндоскопического исследования хирург проводит биопсию обнаруженных новообразований. Фрагменты патологически изменённых тканей отправляют на гистологическое исследование.
Для ранней диагностики рака кишечника в Юсуповской больнице определяют уровень онкомаркеров – белковых соединений, которые вырабатываются в организме при развитии опухолевого процесса:
-
СА19-9, CA 72-4, LASA – P – маркеры рака желудочно-кишечного тракта;
-
CA 125 – позволяет выявить новообразования сигмовидной кишки;
-
CYFRA 21-1 – образуется при наличии рака прямой кишки.
-
SCC – позволяет выявить плоскоклеточный рак анального канала.
-
CA 242 – определяется в случае образования рака прямой и толстой кишки.
-
АФП – образуется при опухолях прямой и сигмовидной кишки;
-
РЭА – является чувствительным маркером рака толстой кишки.
С помощью онкомаркеров можно заподозрить рак кишечника до появления клинических проявлений заболевания.
Как лечится рак в кишечнике
Лечение рака кишечника является комплексным. Оно включает оперативное вмешательство и последующую химио-, радио- или лучевую терапию, а также реабилитацию. Многолетний опыт онкологов Юсуповской больницы помогает достигать оптимального эффекта лечения даже в самых сложных случаях.
Методами лечения рака кишечника являются:
- Хирургическое вмешательство. Операция может выполняться абдоминальным (открытым) способом, а также малоинвазивными методами: эндоскопия, лапароскопия, радиохирургия (гамма-нож и кибер-нож). Выбор метода лечения будет зависеть от стадии заболевания, локализации опухоли, ее размеров. Прогноз после операции опухоли кишечника значительно улучшается, поскольку снижается вероятность метастазирования;
- Лучевая и радиотерапия терапия при раке кишечника. Назначаются для остановки роста злокачественных клеток и прогрессирования заболевания. Могут применяться до и после операции;
- Химиотерапия при раке кишечника. В лечении используется ряд препаратов, вызывающих гибель раковых клеток. Данные препараты негативно влияют и на здоровые клетки, поэтому у химиотерапии есть много неприятных побочных реакций (выпадение волос, постоянная рвота). Для поддержки организма параллельно назначают иммуностимуляторы.
Прогноз
При опухоли (аденокарцинома, карцинома, саркома) кишечника продолжительность жизни будет зависеть от масштабов развития онкологического процесса. Прогноз рака кишечника напрямую зависит от того, на какой стадии было начало лечение. На результаты терапии также могут влиять дополнительные факторы:
- Возраст пациента;
- Состояние его организма;
- Реакция на проводимое лечение;
- Сопутствующие заболевания.
Прогноз аденокарциномы кишечника и других злокачественных опухолей, которые нарушают работу желудочно-кишечного тракта и всего организма, принято считать в рамках пятилетней выживаемости после успешной терапии. В зависимости от стадии, прогноз аденокарциномы, саркомы и карциномы кишечника составляет:
- Первая стадия: 95%;
- Вторая стадия: 75%;
- Третья стадия: 50%;
- Четвертая стадия: 5%.
Методы лечения рака постоянно совершенствуются, что значительно увеличивает продолжительность жизни после проведенной терапии.
Профилактика
В настоящее время не существует препаратов, которые могли бы предотвратить рак кишечника. Профилактика злокачественных опухолей состоит из комплекса мероприятий:
-
Отказа от вредных привычек;
-
Рационального питания;
-
Умеренных физических нагрузок;
-
Контроля хронических заболеваний;
- Исключения переутомления и стрессов.
Для профилактики рецидива важно соблюдать рациональное питание при раке кишечника. Питание при онкологии кишечника должно включать все микроэлементы и витамины для нормальной работы организма. Диета при раке кишечника включает большое количество продуктов, содержащих клетчатку (фрукты, овощи, цельнозерновые злаки) для исключения застойных процессов в кишечнике. Из рациона следует исключить продукты с красителями и другими искусственными наполнителями, высоким содержанием жиров, простых углеводов. Диета при онкологии кишечника позволит наладить пищеварение, что значительно улучшит самочувствие человека.
Рекомендации по лечению рака кишечника
В Москве успешное лечение рака кишечника выполняют в Юсуповской больнице. Это многопрофильный медицинский центр, который специализируется на лечении онкологических заболеваний и выполнении реабилитации пациентов. В больнице создано специальное отделение – клиника онкологии, где работают лучшие специалисты Москвы, занимающиеся лечением рака любой локализации и стадии. Высокая квалификация и большой опыт врачей, современное оснащение позволяют выполнять лечение рака кишечника любой сложности и добиваться максимального результата.

Миф первый. Рак толстой кишки бывает только у пожилых людей, молодые люди им не болеют
Согласно статистике, частота возникновения колоректального рака увеличивается с возрастом, но даже несмотря на это, у молодых людей в 20-30 лет может развиться рак толстой кишки. Известно, что около 7% случаев заболеваемости колоректальным раком приходится на людей моложе 50 лет. У молодых людей, уже перенесших колоректальный рак, риск образования второй злокачественной опухоли кишечника значительно выше.
Поэтому, несмотря на то, что рак толстой кишки чаще всего поражает людей старше 50 лет, это заболевание может случиться и с молодыми людьми. И следует всегда помнить, что если эта болезнь выявляется на ранней стадии, ее можно полностью излечить в более, чем 90% случаев.
Миф второй. Колоректальным раком болеют в основном мужчины
Не верьте этому. Хотя существуют заболевания, которыми преимущественно болеют мужчины или женщины, колоректальный рак не из их числа. Эта болезнь, которая одинаково часто случается как у мужчин, так и у женщин. Дорогие женщины – думать, что раком толстой кишки болеют только мужчины, опасно. Вам необходимо знать и уметь выявить основные симптомы этого заболевания так же, как знаете возможные проявления рака груди или шейки матки. Необходимо включать в регулярные обследования, наряду с маммографией и мазками из влагалища, также и специальные исследования для диагностики колоректального рака.
Миф третий. В моей семье ни у кого не было рака толстой кишки, поэтому я не вхожу в группу риска
Столько много людей считают именно так, и это так печально! Действительно, если у человека несколько членов семьи предыдущих поколений имели рак толстой кишки, это приводит к значительному увеличению риска заболевания у последующих поколений. Тем не менее, необходимо понять, что около 80% больных колоректальным раком не имели случаев этого заболевания в семье. Давайте на время забудем о статистике, и поговорим о реальной жизни. Любой хирург колопроктолог подтвердит, что очень большое количество людей, у которых никто в семье никогда не болел раком толстой кишки, заболевают этим недугом и часто обращаются к врачу уже на запущенной стадии. Они не обследовались, думая, что это обследование им не нужно, так как никто в их семье не имел такого заболевания. Однако, если бы удалось диагностировать болезнь на ранней стадии, ее можно было бы вылечить без следа.
Миф четвертый. Если я чувствую себя хорошо, мне не надо волноваться, что у меня может быть рак кишечника
Это самый ужасный миф из всех. Как Вы думаете, какой самый частый симптом рака толстой кишки на ранней стадии? Думаете, это кровь в стуле или запор? Нет. На самом деле, рак ранней стадии никак себя не проявляет, у него нет особенных симптомов. Люди с колоректальным раком ранней стадии чувствуют себя хорошо, их состояние никак не меняется по сравнению с обычным самочувствием. Только когда опухоль увеличивается, она может давать о себе знать. Сейчас считается, что у обычного человека рак кишечника развивается из полипов, которые в течение длительного времени перерождаются в опухоль. Пока эта опухоль небольшая, она не приводит к появлению боли или других симптомов. Если обнаружить опухоль на ранней стадии, человека можно вылечить от рака. Не надо дожидаться симптомов заболевания, лучше проходить регулярные обследования, пока Вы чувствуете себя хорошо.
Миф пятый. Рак всегда начинается с появления крови в стуле
В основе этого мифа лежит доля правды. У всех людей появление крови в стуле вызывает страх. В большинстве случаев выделение крови из прямой кишки связано с геморроем. Да, раковые опухоли кишечника могут приводить к выделению крови из прямой кишки. Однако ее количество может быть небольшим и даже невидимым без микроскопа. В некоторых случаях при опухолях кишечника может совсем не быть крови в стуле. Если же кровотечение есть, но оно незаметное, то его проявлениями могут повышенная усталость, которая связана с анемией и недостатком железа в крови. Выявить анемию можно только, сделав общий анализ крови, при котором подсчитывается количество эритроцитов, содержание гемоглобина и гематокрит. Появление крови в стуле – это только один из возможных симптомов большой раковой опухоли толстой кишки. Помните, что небольшие опухоли на ранней стадии могут никак себя не проявлять (см. миф четвертый). При большой опухоли могут появляться характерные симптомы (см. таблицу). Могут произойти нарушения эвакуации стула из-за того, что опухоль суживает просвет кишечника, и стул не может пройти через место сужения. При этом человек может страдать от запоров, тошноты, вздутия живота, может меняться форма стула – становиться лентообразной, может быть ощущение неполного опорожнения кишечника. При более запущенных стадиях могут быть снижение аппетита, необъяснимая потеря веса. Эти симптомы возникают из-за того , что, увеличиваясь и распространяясь, опухоль выбрасывает в кровь особые вещества. Поэтому, если у Вас есть какие-либо из перечисленных симптомов, следует немедленно обратиться к врачу.
Пожалуйста, не давайте возможности этим мифам встать на пути возможного спасения Вашей или другой жизни!
Лист оценки симптомов колоректального рака
Как и большинству людей, возможно, Вам неудобно обсуждать функционирование своего кишечника. Тем не менее, Вам придется изменить свои взгляды. Если Вы сами не скажете доктору о необычных симптомах, например, изменение формы стула, он или она никогда об этом не узнают и скорее всего даже не спросят! Вот краткое перечисление того, на что нужно обращать внимание.
Пожалуйста, не пугайтесь! Большинство из этих симптомов встречаются у многих людей и не связаны с раком. Тем не менее, позвольте это решить Вашему доктору.
- Изменение режима и характера опорожнения кишки – единовременные или хронические поносы или запоры, неприятные ощущения при опорожнении кишки, изменение формы стула (тонкий, как карандаш, или тоньше, чем обычно), ощущение неполного опорожнения кишки.
- Необычные ощущение, связанные с кишечником, такие как – повышенное газообразование, боль, тошнота, вздутие живота, ощущение переполнения кишечника.
- Кровотечение (светло-красная или очень темная кровь в стуле).
- Постоянная усталость.
- Необъяснимая потеря веса.
- Необъяснимый дефицит железа.
- Необъяснимая анемия.
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Третьякова Ю.И.
1
Патрикеева М.С.
1
Меньшикова Н.С.
1
1 ФГБОУ ВО Пермский государственный медицинский университет им. ак. Е.А. Вагнера Минздрава России
В статье представлен клинический случай с описанием пациента 28 лет с агрессивным течением перстневидно-клеточного рака желудка, диагностированного на последней стадии. Из анамнеза известно, что в течение 2,5 месяцев больной наблюдался с диагнозом «гастропатия, индуцированная нестероидными противовоспалительными препаратами (НПВП), с назначением ингибиторов протонной помпы». В связи с ухудшением состояния и неэффективностью терапии пациент был госпитализирован в гастроэнтерологическое отделение клиники. На рентгенографии желудка были выявлены признаки инфильтративных изменений стенок желудка и канцероматоз брюшины. По данным фиброгастроскопии – слизистая желудка ярко гиперемирована, плотная при инструментальной пальпации. По результатам патогистологического исследования выявлен недифференцированный аденогенный рак с образованием перстневидных клеток. Больному проведен один курс полихимиотерапии в краевом онкодиспансере без положительного эффекта. Пациент скончался в связи с прогрессированием основного заболевания и развитием полиорганной недостаточности. Был поставлен заключительный патологоанатомический диагноз: Злокачественное новообразование желудка: низкодифференцированная аденогенная карцинорма G3-4 (перстневидно-клеточный вариант – гистологически) с метастазами в парааортальные, периэзофагальные лимфоузлы, легкие, надпочечники; канцероматоз плевральных полостей и брюшины рТ4N3M1b. В заключение статьи даны рекомендации по мерам профилактики онкологических заболеваний.
клинический случай
рак желудка
поздняя диагностика
перстневидно-клеточный рак
онкология.
1. Каприн А.Д., Старинский В.В., Петрова Г.В. Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2018. 250 с.
2. Абдуллаев А.Г., Аллахвердиев А.К., Бесова Н.С., Бяхов М.Ю., Горбунова В.А., Давыдов М.И., Давыдов М.М., Ибраев М.А., Карселадзе А.И., Кувшинов Ю.П., Малихова О.А., Неред С.Н., Стилиди И.С., Трякин А.А. Клинические рекомендации по диагностике и лечению больных раком желудка. Ассоциация онкологов России, 2017. 40 с.
3. Денисов И.Н., Артемьева Е.Г., Маленкова В.Ю., Бусалаева Е.И. Рак желудка. Руководство для врачей общей практики (семейных врачей). Ассоциации врачей общей практики РФ, 2015. 14 с.
4. Белковец А.В., Курилович С.А., Решетников О.В. Наследственный рак желудка (научный обзор) // Международный журнал прикладных и фундаментальных исследований. 2016. № 1-4. С. 516-522.
5. Джемал А., Паоло В., Брей Ф., Торре Л., Форман Д. Атлас современной онкологии. Издание второе. Американское онкологическое общество, 250 Williams Street, Atlanta, Georgia 30303 USA (США), 2014. 136 с.
6. Бойкова С.П., Зайратьянц О.В., Зотова Л.А. Патологическая анатомия: атлас: учеб. пособие для студентов медицинских вузов и последипломного образования. М.: “ГЭОТАР-Медиа”, 2014. 961 с.
7. Рыбакова Д.В., Давыдов М.М., Казанцев А.П., Керимов П.А., Матинян Н.В. Рак желудка у пациента 16 лет: описание клинического случая // Онкопедиатрия. 2017. Т. 2. №4. С.147–151.
8. Вашакмадзе Л.А., Филоненко Е.В., Бутенко А.В., Кириллов Н.В., Хомяков В.М. Отдаленные результаты хирургического лечения больных местнораспространенным и диссеминированным раком желудка в сочетании с интраоперационной фотодинамической терапией. // Фотодинамическая терапия и фотодиагностика. 2013. Т. 1. №2. С.3-10.
9. Каприн А.Д., Старинский В.В., Петрова Г.В. Состояние онкологической помощи населению России в 2017 году. М.: МНИОИ им. П.А. Герцена филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2018. 236 с.
10. Бойцов С.А., Чучалин А.Г., Арутюнов В.Г. Биличенко Т.Н., Бубнова М.Г., Ипатов П.В., Калинина А.М., Карпин А.Д., Марцевич С.Ю., Оганов Р.Г., Погосова Н.В., Старинский В.В., Стаховская Л.В., Ткачева О.Н., Чиссов В.И., Шальнова С.А., Шестакова М.В. Профилактика хронических неинфекционных заболеваний. Клинические рекомендации. Москва. 2013. 136 с.
Смертность от онкологических заболеваний занимает второе место после болезней сердечно-сосудистой системы. В 2017 г. в России выявлено почти 541 тыс. онкобольных, а умерло 290,7 тыс., что составило 15,9% в общей структуре смертности [1, с. 3].
В последние годы отмечается тенденция к снижению заболеваемости раком желудка (РЖ), тем не менее в структуре заболеваемости злокачественными новообразованиями населения России РЖ занимает 4-е место у мужчин (7,6%) и 5-е место у женщин (4,7%) [1, с. 9, 10]. Пик заболеваемости приходится на возраст старше 50 лет. Злокачественные новообразования желудка занимают вторую позицию в структуре смертности у мужчин и женщин. Ежегодно в РФ регистрируют около 36 тыс. новых случаев РЖ, и более 34 тыс. больных умирает от этого заболевания. Этиология заболевания до конца не выяснена [2, с. 6].
Имеется связь возникновения патологии с определенными факторами риска. Их можно разделить на немодифицируемые: пол (мужчины страдают чаще), возраст (по мере увеличения возраста увеличивается частота возникновения РЖ), генетическая предрасположенность (5–10% пациентов, страдающих РЖ, имеют отягощенный семейный анамнез); и модифицируемые: инфекция Helicobacter Pylori (HP), характер рациона, ожирение, курение, алкоголь, профессиональная деятельности [3, с. 4-6].
В настоящее время установлено, что почти 90% случаев РЖ в мире обусловлено инфицированием бактерией HP. При этом средства лечения HP-инфекции существуют, но широко не применяются из-за недостатка подтвержденных данных эффективности в профилактике рака желудка и высокой стоимости [5, с. 22]. К возникновению РЖ могут привести фоновые заболевания: хронический атрофический гиперпластический гастрит, аденоматозные полипы, пернициозная анемия, состояния после резекции желудка, болезнь Менетрие [2, с. 6]. Различают три гистологических типа РЖ (по Lauren, 1965 г.): кишечный, диффузный, смешанный. При диффузном раке опухоль представлена слабоорганизованными группами или одиночными клетками с большим содержанием муцина (перстневидные клетки). Для данного типа характерен диффузный инфильтративный рост [2, с. 7].
Перстневидно-клеточный рак желудка содержит не менее половины клеток с признаками внутриклеточного образования слизи. Скапливающаяся в цитоплазме слизь сдвигает ядро к периферии, и клетка приобретает сходство с перстнем [6, с. 589]. Согласно результатам клинических наблюдений неблагоприятный прогноз при диффузном раке желудка связывают с низкой выявляемостью на ранних стадиях, быстрым течением, более злокачественным потенциалом опухолевых клеток и ранним метастазированием [7].
Приводим случай летального исхода пациента с перстневидно-клеточным раком желудка, диагностированным на последней стадии.
Клиническое наблюдение. Пациент В., 28 лет, поступил в гастроэнтерологическое отделение клинической медико-санитарной части г. Перми 14.11.2017 г. с жалобами на постоянные боли в области правого фланка живота, преимущественно в нижней части; интенсивные боли в правом подреберье и правом боку при глубоком дыхании; тошноту, рвоту желчью, вздутие живота, Также пациента беспокоили отсутствие аппетита, отвращение к пище, жидкий стул 2–3 раза в сутки без примесей. Отмечались выраженная общая слабость, повышение температуры тела до 37,4°С. За 1 месяц больной похудел на 13 кг.
Анамнез. В начале сентября 2017 г. больной получал терапию антибактериальными и нестероидными противовоспалительными препаратами (НПВП) по назначению стоматолога (после экстракции зуба) в течение 7 дней. В начале октября 2017 г. были вновь назначены антибактериальная терапия и НПВП по поводу гайморита. На фоне приема препаратов появились боли в эпигастрии, изжога, неустойчивый стул. Больной обратился в поликлинику по месту жительства, где обследовался у участкового терапевта. 7 октября 2017 г. выполнена фиброгастродуоденоскопия (ФГДС), на которой выявлены множественные язвы желудка (6 дефектов), язва двенадцатиперстной кишки (ДПК) в стадии эпителизации, застойная гастропатия, дуоденогастральный рефлюкс. Уровень антител к HP составил 1,44. Получал терапию ингибиторами протонной помпы (ИПП), антацидами без эффекта – сохранялись тошнота и абдоминальный болевой синдром с локализацией в эпигастрии.
Участковым терапевтом дано направление на экстренную госпитализацию в терапевтическое отделение городской больницы с диагнозом: Множественные язвы желудка и язва луковицы ДПК, ассоциированные с HP. Гастринома? Синдром Золлингера–Эллиссона?, где больной находился с 12.10.2017 г. по 24.10.17 г. При обследовании в общем анализе крови (ОАК) от 13.10.2017 г.: гемоглобин – 157 г/л; умеренное повышение лейкоцитов до 11х109/л; ускоренная скорость оседания эритроцитов (СОЭ) – 40 мм/час. В биохимическом анализе крови от 13.10.2017 г. общий белок, амилаза, холестерин, печеночные тесты, электролиты крови в пределах нормальных значений. На ультразвуковом исследовании органов брюшной полости (УЗИ) от 13.10.2017 г. выявлены признаки диффузных изменений видимых участков поджелудочной железы. Кал на скрытую кровь – слабоположительный.
23.10.2017 г. выполнена повторная ФГДС: слизистая желудка диффузно гиперемирована с выраженным отеком, утолщена, сосудистый рисунок смазан. Слизистая оболочка в области привратника отечна, гиперемирована. По всем стенкам множественные точечные лимфоидные высыпания. Заключение: Диффузный катаральный гастрит выраженной степени активности. Дуоденогастральный рефлюкс. Диффузный катаральный бульбит выраженной степени активности. Косвенные признаки панкреатита. Гистологическое исследование не проводилось.
В стационаре по результатам обследований был поставлен диагноз: Язвенная болезнь желудка, луковицы ДПК. Множественные острые язвы желудка в активной стадии. НПВП-ассоциированная гастропатия. Язва луковицы ДПК в стадии эпителизации. Больной получал терапию спазмолитиками, ИПП 40 мг в сутки, антацидами.
На фоне лечения отмечалась положительная клиническая и эндоскопическая динамика в виде уменьшения болевого синдрома и эпителизации язвенных дефектов. Пациент был выписан из стационара с рекомендациями продолжить прием ИПП в дозе 40 мг в сутки и явиться на прием к участковому терапевту.
После выписки боли в эпигастрии усилились, появилась острая боль справа в боку в области ребер. Участковый терапевт назначил прием прокинетика, антацидных препаратов, НПВП внутримышечно (в/м) № 3. 4.11.2017 г. у пациента внезапно возникла острая боль в области верхнего левого фланка живота и межреберьях, связанная с дыханием. Больной обратился в приемное отделение клинической больницы, где был поставлен диагноз: Межреберная невралгия. Проведена терапия НПВП в/м, и больной был отпущен домой под наблюдение невролога и терапевта с рекомендациями приема НПВП. Далее по назначению гастроэнтеролога поликлиники принимал висмута трикалия дицитрат, спазмолитики, даларгин без эффекта – сохранялись абдоминальный болевой синдром, неустойчивый стул; также появились выраженное вздутие живота, рвота, отвращение к пище, прогрессирующее похудание. 13.11.2017 г. выполнена ректороманоскопия: стенка прямой кишки с трудом расправлялась воздухом, с эрозиями, утолщенными складками, сосудистый рисунок смазан. Заключение: эрозивно-катаральный проктосигмоидит.
14.11.2017 г. пациент был экстренно госпитализирован в гастроэнтерологическое отделение клиники для дальнейшего обследования и лечения.
Из анамнеза жизни известно, что пациент рос и развивался соответственно возрасту. Курил в течение 8 лет по 10 сигарет в день. Профессиональных вредностей не было. Со слов больного, ранее лечился по поводу мочекаменной болезни. Наследственность по заболеваниям органов пищеварения не отягощена.
При физическом исследовании обращала на себя внимание бледность кожных покровов с сероватым оттенком. Кожа чистая, отеков не отмечалось. Пульс – 92 удара в минуту, ритмичный. Тоны сердца ясные, ритм правильный. Дополнительные шумы не выслушивались. Дыхание везикулярное, ослаблено в нижних отделах, хрипы не выслушивались. Перкуторный звук несколько притуплен в нижних отделах легких. ЧДД – 16 в минуту.
Язык обложен бело-желтым налетом у корня, влажный. Живот плотный, увеличен за счет вздутия и асцита; пальпация резко болезненная в эпигастрии, в области правого фланка живота, по ходу толстой кишки. Ординаты Курлова 10х8х7 см. Стул оформленный, чередующийся с кашицеобразным, без патологических примесей, 1–2 раза в сутки. Со стороны почек и мочевого пузыря без видимой патологии.
Результаты лабораторно-инструментальных исследований представлены ниже.
ОАК: эритроциты 4,7х109/л, гемоглобин 140 г/л, среднее содержание гемоглобина (ССГ) 29%, тромбоциты 307х109/л, лейкоциты 8,4х/л, палочкоядерные нейтрофилы 7%, сегментоядерные нейтрофилы 75%, лимфоциты 15%, моноциты 3%, повышение СОЭ до 43 мм/час.
ОАМ: цвет – желтый, мутная, pH 6,0, умеренная протеинурия 0,39 г/л, лейкоциты 4–6 в поле зрения (п/з), эритроциты 0–1 в п/з, эпителий 2–3 в п/з, слизь +.
Биохимический анализ крови от 15.11.2017 г.: глюкоза 4,8 ммоль/л, Ca 2,29 ммоль/л, AСТ/АЛТ 16/18 Ед/л, ГГТП 84 Ед/л, ЩФ 285 Ед/л, общий белок 54 г/л, альбумины 27 г/л, билирубин общий 12 мкмоль/л, прямой 4,1 мкмоль/л, холестерин общий 3,7 мкмоль/л, калий 4,5 ммоль/л, натрий 134 ммоль/л, креатинин 51 ммоль/л, резкое повышение С-реактивного белка (СРБ) 105 мг/л, снижение железа сыворотки до 4,5 мкмоль/л, повышение общей железосвязывающей способности сыворотки до 75, незначительное повышение прокальцитонина до 0,2 нг/мл. При форезе белков выявлены снижение альбумина до 37,95% и повышение α1-глобулинов до 8,77%, α2-глобулинов до 13,28%, β-глобулинов до 18,5 3%, γ-глобулин 21,47%.
Коагулограмма от 15.11.2017 г.: протромбиновое время 14,9 секунд (11–15 секунд), тромбиновое время – 17,2 секунд, активированное частичное протромбиновое время – 28 секунд (24–35 секунд), резкое повышение фибриногена до 9,56 г/л.
Копрограмма от 16.11.2017 г.: консистенция жидкая, цвет темно-коричневый, переваренные мышечные волокна 0–1–2 в п/з, неизмененные мышечные волокна 0–1 в п/з, форменные элементы крови 0–1 в п/з, лейкоциты 10–20 в п/з, эпителий плоский – единичный в п/з, нейтральных жиров нет, жирных кислот нет, крахмал внеклеточно скудно, йодная флора +, детрит +++.
ФГДС от 14.11.2017 г.: складки желудка гипертрофированные, отечные. Слизистая желудка ярко гиперемирована, плотная при инструментальной пальпации, ранимая при контакте с линейными рубцами неправильной формы. Луковица ДПК деформирована, рыхлая с увеличенными эрозированными фолликулами, на верхушках – фибрин. Заключение: Болезнь Крона? Дуоденогастральный рефлюкс. Косвенные признаки панкреатита. Выполнена биопсия.
Результаты патогистологического исследования слизистой желудка (20.11.2017 г.): в слизистой оболочке пилородуоденальной области очаговое скопление крупных клеток округлой и овальной формы, со светлой слизьсодержащей цитоплазмой, периферически расположенными уплощенными ядрами, единичные клетки с гиперхромными ядрами, скудной цитоплазмой. Диагноз: недифференцированный аденогенный рак с образованием перстневидных клеток.
16.11.2017 г. выполнена КТ органов брюшной полости. Выявлен выпот в реберно-диафрагмальные синусы с обеих сторон. Желудок в области тела и антрального отдела с неравномерно утолщенными стенками до 0,8 см. Большой сальник в области эпигастрия уплотнен, с узловыми образованиями. В брюшной полости большое количество свободного выпота. Заключение: Признаки двустороннего гидроторакса, инфильтративных изменений стенок желудка. Большой сальник в эпигастральной области уплотнен с узловыми образованиями (канцероматоз брюшины). Асцит. Аденопатия гепатодуоденальных лимфатических узлов.
На рентгеноскопии пищевода, желудка, ДПК с бариевой взвесью диагностировано стойкое сужение просвета тела, синуса, выходного отдела желудка (рис. 1) с неровными фестончатыми контурами, атипичным рельефом слизистой (рис. 2). Заключение: Рентгенологические признаки инфильтративного поражения желудка.
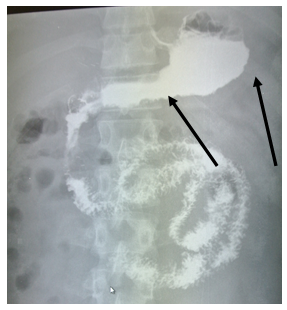
Рис. 1. Рентгенологическое исследование желудка пациента В., 28 лет: сужение просвета тела, синуса, выходного отдела желудка
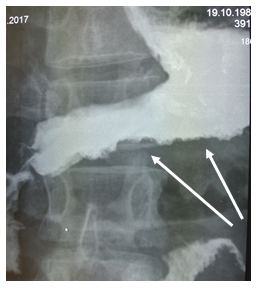
Рис. 2. Рентгенологическое исследование желудка пациента В., 28 лет: неровность и фестончатость контуров, атипичный рельеф слизистой
В условиях стационара проводилась инфузионная, антибактериальная, спазмолитическая, обезболивающая терапия. Амитриптилин 6,25–12,5 мг на ночь. Больной выписан из отделения 22.11.2017 г. с диагнозом:
Основной: Недифференцированный аденогенный рак выходного отдела желудка IV ст. Сопутствующий: Эрозивно-катаральный проктосигмоидит.
Осложнения: Канцероматоз брюшины. Аденопатия гепатодуоденальных лимфоузлов. Асцит. Двусторонний гидроторакс. Дефицит железа.
Пациенту выдано направление в онкологический диспансер. Даны рекомендации приема Амитриптилина 25 мг на ночь; Прегабалина 75 мг 1 раз в день; Нейробиона по 1 табл. 3 раза в день.
С 23.11.2017 г. по 30.11.2017 г. пациент находился в краевом онкологическом диспансере, где был подтвержден диагноз: Злокачественное новообразование желудка (ЗНО) IV ст. Т4NxMx».
Проведен 1 курс полихимиотерапии (ПХТ). После выписки, несмотря на проводимое лечение, состояние пациента прогрессивно ухудшалось. 18.12.2017 г. проведена эвакуация 10 литров асцитической жидкости в условиях стационара. 20.12.2017 г. – консультативный прием в онкологическом диспансере. Диагноз: Злокачественное новообразование желудка IV ст. Т4NxMx. Тотальное поражение. Канцероматоз брюшины. Прогрессирование. Кахексия. Асцит. Было рекомендовано продолжить симптоматическую терапию по месту жительства, а также попытка проведения гастростомии. Учитывая тяжесть состояния, ПХТ не показана.
22.12.2017 г. больной отметил появление одышки. На следующий день самостоятельно обратился в приемное отделение краевой больницы и был госпитализирован в отделение торакальной хирургии. На КТ органов грудной клетки (23.12.2017 г.) выявлен двусторонний гидроторакс. По легочным полям определялись очаги уплотнения по типу «матового стекла».
23.12.2017 г. и 25.12.2017 г. – плевральная пункция – эвакуирован 1 л серозно-геморрагического отделяемого. 26.12.2017 г. состояние больного тяжелое, с отрицательной динамикой. Появились рвота темной кровью, боли в эпигастрии, слабость, сухость во рту. На ФГДС – кровотечение интрагеморрагическое. Эрозивный эзофагит. Гемостаз системой EndoClot.
27.12.2017 г. состояние было крайне тяжелым. Сохранялась рвота темной кровью. Пациент переведен в ОРИТ, где проводилась инфузионная терапия, получал Метоклопрамид, Трамадол, Кетопрофен, Верошпирон, Транексам, Нексиум. При обследовании нарастала тромбоцитопения – 11569-41-19х109л, показатели очищения: мочевина 20,01 ммоль/л; креатинин 140,9 ммоль/л; гипопротеинемия 46,4 г/л.
27.12.2017 г. в 22:15 – асистолия. Реанимационные мероприятия в полном объеме – без эффекта.
27.12.2017 г. в 22:45 констатирована биологическая смерть. Труп В., 28 лет, был направлен на патологоанатомическое исследование с диагнозом: Перстневидноклеточный рак желудка с переходом на нижнюю треть пищевода T4NхM1. Канцероматоз плевры. Метастатическое поражение легких. Двусторонний экссудативный плеврит. Асцит. Осложнения: Кахексия. Желудочно-кишечное кровотечение. Геморрагический шок. Синдром полиорганной недостаточности.
Патологоанатомический диагноз:
Основное заболевание: Злокачественное новообразование желудка: низкодифференцированная аденогенная карцинорма G3-4 (перстневидно-клеточный вариант – гистологически) с метастазами в парааортальные, периэзофагальные лимфоузлы, легкие, надпочечники; канцероматоз плевральных полостей и брюшины рТ4N3M1b.
Осложнение основного заболевания: Отек головного мозга. Двусторонний гидроторакс (1200/1200 мл). Асцит 3500 мл. Кахексия. Венозное полнокровие и паренхиматозная дистрофия миокарда, печени, почек.
Сопутствующие заболевания: Хронический пиелонефрит, ремиссия.
Обсуждение. В структуре заболеваемости РЖ возрастает доля молодого контингента больных (до 45 лет) с преобладанием низкодифференцированных и сложных форм, характеризующихся крайне плохим прогнозом [7, 8]. В настоящее время показатели несвоевременной диагностики рака желудка (IV стадия) являются одними из лидирующих, составляя в России 39,9% [9, с. 10].
Врач первичного звена является первой линией защиты в борьбе с онкопатологией. Первичная профилактика направлена на выявление и устранение влияния неблагоприятных факторов окружающей среды (канцерогенов) на процесс возникновения злокачественной опухоли, а также на устранение модифицируемых факторов риска [10]. У описанного нами пациента к факторам риска можно отнести длительный стаж курения и инфекцию НР.
Вторичная профилактика направлена на выявление и устранение предраковых заболеваний и диагностирование злокачественного новообразования на ранней стадии процесса при помощи ряда лабораторных и инструментальных методов обследования, включая полное гистологическое и молекулярно-генетическое исследование. При этом важно помнить о «симптомах тревоги» [10]. У пациента имели место снижение массы тела и повышение СОЭ, что должно было насторожить врачей. В течение 1,5 месяцев пациента вели с диагнозом «НПВП-гастропатия» с назначением ИПП, которые могли маскировать клинику рака желудка. Кроме того, отсутствие анамнестических данных о наличии фоновых заболеваний желудка и наследственной предрасположенности, молодой возраст пациента, неспецифическая симптоматика в начале заболевания, а также несвоевременное гистологическое исследование слизистой желудка послужили причиной поздней диагностики.
Заключение. Важно помнить, что рак желудка может быть диагностирован и в молодом возрасте, имея при этом крайне агрессивное течение. Необходимо выделять группы риска и своевременно проводить скрининг онкологических заболеваний. Регулярное диспансерное наблюдение является важнейшей массовой и высокоэффективной медицинской технологией сбережения здоровья и снижения преждевременной смертности населения.
Библиографическая ссылка
Третьякова Ю.И., Патрикеева М.С., Меньшикова Н.С. ПОЗДНЯЯ ДИАГНОСТИКА РАКА ЖЕЛУДКА У ПАЦИЕНТА 28 ЛЕТ (СЛУЧАЙ ИЗ ПРАКТИКИ) // Современные проблемы науки и образования. – 2018. – № 6.
;
URL: https://science-education.ru/ru/article/view?id=28401 (дата обращения: 15.05.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Распространен и опасен: главное о колоректальном раке
12.03.2018
Колоректальный рак — «болезнь цивилизации». Наиболее часто опухоли толстой кишки диагностируют у жителей США, Западной Европы и Австралии. Почему этому заболеванию подвержено население развитых стран? Как обезопасить себя от неприятного диагноза и что делать при первом подозрении? На наши вопросы ответил к. м. н., заведующий отделением колопроктологии Московской городской онкологической больницы №62 Илья Черниковский.
Какие виды колоректального рака бывают?
Колоректальный рак (КРР) включает в себя несколько видов. Первый и самый распространенный — это рак ободочной кишки (аденокарцинома толстой кишки). Вторым по частоте является рак прямой кишки (аденокарцинома прямой кишки). И третий вид — это рак анального канала, как правило он плоскоклеточный. Значительно реже встречаются другие злокачественные опухоли прямой ободочной кишки: гастроинтестинальная стромальная опухоль, нейроэндокринный рак или карциноид — более доброкачественный вариант нейроэндокринной опухоли. И совсем редко встречаются меланомы прямой кишки и анального канала.
На каком месте по заболеваемости находится колоректальный рак?
Если брать все виды рака, которые относят к КРР, то на третьем месте в мире. Но в развитых странах процент пациентов с КРР немного больше. Скорее всего, это связано с увеличенной продолжительностью жизни и особенностями питания.
Считается, что если в популяции употребляют больше мясных продуктов и меньше растительной пищи, то вероятность возникновения колоректального рака увеличивается.

Источник: shutterstock.com
Какие виды КРР более распространены среди женщин, а какие среди мужчин?
Достоверно известно, что любым видом КРР чаще болеют женщины. Это принято связывать с тем, что женщины живут дольше, а колоректальный рак, как и большинство других видов рака, — это болезнь пожилых людей. Раньше считалось, что рак анального канала тоже чаще встречается у женщин. В 1975 году в США на 100 тыс человек им болело меньше 1% женщин и около 0,7% мужчин. А к 2007 году этот уровень увеличился в 1,7 и 3 раза соответственно. Достоверно установлена причина этого вида рака — он вызывается вирусом папилломы человека (ВПЧ) и передается между партнерами, практикующими анальный секс. Поэтому сейчас много мужчин нетрадиционной сексуальной ориентации страдают от рака анального канала, но, конечно, в зону риска входят и женщины. Если проводить массовую вакцинацию от онкогенных штаммов ВПЧ, то сложившуюся ситуацию можно было бы улучшить. Причем это работает не только при вышеуказанном заболевании, но и для других видов плоскоклеточного рака: рака шейки матки и некоторых видов опухолей головы и шеи.
Как можно понять, что у тебя повышенный риск развития колоректального рака? С какого возраста следует начинать профилактические обследования?
Очень важно помнить, что 10% случаев КРР — это наследственные формы.
В США, где скрининг развит наиболее сильно, принято выделять группы среднего, повышенного и высокого риска.
Группа среднего риска — это большинство из нас: здоровые люди, у которых нет близких родственников, которые бы болели КРР, раком желудка, раком тела матки или раком молочной железы. У них отсутствуют наследственные синдромы и хронические воспалительные заболевания кишечника, а именно неспецифический язвенный колит или синдром раздраженной кишки. В этой группе скрининговые обследования нужно проводить с 55 лет.
Группа повышенного риска — это пациенты, у которых кровные родственники (родители или бабушкидедушки) болели указанными выше видами рака. У таких людей повышен риск возникновения злокачественного новообразования, в том числе и КРР. Представителям этой группы следует начинать обследования раньше, в США советуют это делать с 45 лет.
И, наконец, есть группа высокого риска. В нее входят пациенты с доказанными наследственными синдромами: диффузным семейным полипозом, синдромом Пейтца–Егерса или синдромом Линча. Для таких людей характерно раннее возникновение полипов в кишечнике и затем развитие из них злокачественной опухоли. Также сюда относят пациентов, более 10 лет страдающих неспецифическим язвенным колитом или болезнью Крона. Этой группе нужно начинать скрининговую программу намного раньше. Например, наличие родственников с диффузным семейным полипозом сдвигает эту границу аж к 20 годам. А при синдроме Линча у пациента в 100% случаев разовьется колоректальный рак, если он до него доживет. Если у таких людей находят опухоль кишечника, то удаляют всю толстую и прямую кишку, понимая, что рано или поздно у них разовьется рак и в оставшейся части.
Первая стадия скрининга для всех групп риска — это иммунохимический анализ кала на скрытую кровь. Тест бывает количественный и качественный, но лучше выбирать количественный, он точнее. Если тест показывает наличие крови в кале, то тогда следует выполнить фиброколоноскопию, чтобы посмотреть все толстую и прямую кишку.
Какие программы скрининга действуют сейчас в России?
В России, к сожалению, вообще нет скрининговых программ, если мы говорим о популяционном скрининге. У нас есть только некоторые элементы. Например, в Санкт-Петербурге несколько лет назад проводилась программа по скринингу рака молочной железы. Женщин обследовали, поводили маммографию, специально оснащали кабинеты маммологов и прочее. Но такие программы должны финансироваться отдельно, а у нас все пытаются включить в программу диспансеризации, не совсем понимая, что диспансеризация и онкологический скрининг — разные вещи.
Всего в мире известны три опухолевые локализации, в отношении которых популяционный скрининг доказано эффективен: КРР, рак молочной железы и рак шейки матки. Все остальные вопросы, связанные со скринингом, например, рака легкого или рака предстательной железы, пока только изучаются, очевидных доказательств эффективности сегодня нет. А внедрение скрининговой программы по КРР в США помогло снизить смертность примерно на 10%, это жизнь 13,5 тысяч человек ежегодно.
Но что очень важно для популяционного скрининга, так это хороший охват групп населения. Если он меньше 50%, то затраты на скрининг превышают пользу. В такие программы должны вовлекаться не только онкологи, эпидемиологи и другие врачи, но также СМИ, медиаперсоны да и общество в целом. Это большая комплексная работа, которой сейчас нет в России.
Какие профилактические действия помогут снизить риск КРР?
Безусловно, первое, что можно сделать — отказаться от курения. Также нужно стараться употреблять больше клетчатки и меньше переработанного красного мяса. Если есть проблемы с функционированием кишечника (синдром раздраженной кишки, нарушения стула) — это нужно обязательно лечить. И, наконец, нужно понимать, что если вам стукнуло пятьдесят лет, то необходимо на всякий случай сдать кал на скрытую кровь и сделать колоноскопию. Любые жалобы: изменение стула, наличие крови — должны быть поводом для посещения врача. Нельзя махать рукой на такие обстоятельства, думая, что у тебя просто геморрой. Нужно обратиться к специалисту, который назначит правильное обследование и лечение. Для любого грамотного проктолога наличие крови в стуле — это повод назначить фиброколоноскопию.

Источник: shutterstock.com
На какие моменты нужно обратить внимание, когда тебе назначают колоноскопию?
Как и при любой другой инвазивной манипуляции, чем чаще врач ее выполняет, тем больше у него в этом опыта. Достаточно банальная истина, но нужно обращаться в учреждение с хорошим потоком пациентов. Во-вторых, нужно идти туда, где процедуру вам сделают на качественном оборудовании. И, желательно, где вам обеспечат обезболивание.
К сожалению, у нас есть проблема с отсутствием контроля качества колоноскопии. Хотя вполне объективные критерии ее выполнения существуют. К этим проблемам на западе относятся очень серьезно. Гипотетически можно делать колоноскопию всем людям, например, в городе Санкт-Петербурге. Потратить на это огромные деньги. Но если сделать ее всем и некачественно, то ценность такой процедуры теряется. Если врач пропустит 15% полипов у 15% больных, то ценность этого скрининга будет нулевая. Именно поэтому за рубежом есть четкие объективные критерии оценки качества выполненной процедуры. А у нас их пока нет.
А каковы эти критерии качества?
Самое понятное для неспециалистов — колоноскопия не должна продолжаться меньше 15 минут. Если доктор говорит, что очень быстро засунул колоноскоп, моментально осмотрел всю кишку и он молодец, то это не так.
Значит он смотрел невнимательно. А полипы бывают маленькие, например, полсантиметра-сантиметр. Если врач эти полипы пропустил, а в следующий раз человек собрался сделать колоноскопию, скажем, через 10 лет, то за это время из полипа может развиться рак.
Кстати, критерии качества хирургического вмешательства при КРР тоже важный вопрос. Ведь что такое онкологическая операция? Это операция, качество которой мы не можем определить сегодня, завтра или послезавтра. В отличии от какого-нибудь геморроя, при онкологическом заболевании у пациента, зачастую нет жалоб. Он лег на стол и чувствовал себя хорошо; встал и чувствует то же самое. Но как выполнена эта операция, мы не знаем. Мы можем это определить только через год, когда человек придет, сделает компьютерную томограмму и там действительно будет все хорошо, без признаков рецидива болезни. Но если он придет, а эти признаки будут, то поздно что-то говорить доктору. Время уже упущено.
Сегодня именно для КРР существуют вполне четкие критерии качества. Их придумали онкохирурги в развитых странах. Это, так называемая, препарат-ориентированная хирургия. На основании характеристик удаленного препарата уже через день после операции можно сказать, качественно она была выполнена или нет. Но по этим критериям в России никто не оценивает хирургов. Мы сейчас пытаемся исправить ситуацию, создаем раковый регистр. Уже охватили несколько учреждений в Питере и других городах России, которые будут участвовать в оценке качества операций. Это очень важно, поскольку качественно сделанная операция при КРР дает прибавку к выживаемости в 10%.
Нужно ли выполнять биопсию при колоноскопии?
Современная колоноскопическая техника позволяет отличить обычный доброкачественный полип от чего-то более серьезного. Но нужно понимать, что любой полип больше полусантиметра должен быть удален. Маленькие можно удалять амбулаторно, прямо во время процедуры. Но вот для крупных полипов или полипов с подозрением на злокачественный рост нужно выполнить биопсию. И если он большой, но доброкачественный, то удаляют его в стационаре — обычно это занимает не больше двух дней. А если мы получаем при изучении биопсии злокачественный результат, то тогда уже нужно проходить полное обследование, определять клиническую стадию заболевания. И в зависимости от стадии уже определяется тактика лечения: начиная от эндоскопического удаления во время колоноскопии и заканчивая применением всех методов лечения.
Расскажите, пожалуйста, поподробнее про методы лечения.
В идеале мы должны находить онкологические заболевания, в частности колоректальный рак, на таких стадиях, чтобы было достаточно небольшого вмешательства. Если бы мы всем пациентам диагностировали КРР на первой стадии, то можно было бы ограничиться эндоскопическими вмешательством во время колоноскопии. И это было бы здорово. И более того, это был бы окончательный метод лечения, который приводил бы к выздоровлению у большинства больных в 99% случаев. Но, к сожалению, пока мы далеки от этого.
Есть пациенты с опухолями побольше, но все равно вполне операбельными. В этих случаях достаточно только хирургического вмешательства, которое также приведет к полному излечению большинства больных. Не потребуется больше ничего, кроме наблюдения у онколога.
Когда пациент попадает в руки онкологов уже на третьей стадии, ему требуется использование нескольких методов лечения. Принципиально в онкологии их существует три: хирургическое лечение, лекарственное (химиотерапевтическое) лечение и лучевое воздействие на опухоль. Если мы говорим про рак прямой кишки, то на третьей стадии пациент обязательно должен получить все три составляющие. Причем начинать лечение нужно, как правило, с химиолучевой терапии, а затем уже проводить хирургическое вмешательство. В этом случае мы увеличиваем безрецидивную выживаемость на 10-15%, если сравнивать с только хирургическим лечением.

Фото из архива Ильи Черниковского
Если говорить про рак ободочной кишки, то он, как правило, не подвергается лучевому воздействию. Очень сложно облучить опухоль, которая расположена в брюшной полости. Пациент дышит, двигается, кишечник перистальтирует и нецелевые органы могут попасть под лучевое воздействие. На третьей стадии этого вида КРР уже определенно используется химиотерапия, но как профилактическое лечение после хирургического вмешательства. Она позволяет увеличить выживаемость таких пациентов примерно на 5-10%, что несомненно важно.
Так как на третьей стадии необходимо комбинированное и комплексное лечение, этим не должен заниматься стационар общего профиля. Кроме того, очень важно чтобы решение о тактике лечения принимал консилиум в составе хирурга-онколога, химиотерапевта и радиолога. Это прописано у нас в приказе Министерства здравоохранения «Об утверждении Порядка оказания медицинской помощи населению по профилю “онкология”».
Ну и наконец, самая печальная группа больных, которые обращаются к онкологам на 4 стадии заболевания с метастазами в отдаленные органы. Чтобы совсем не наводить пессимизм, можно сказать, что за последние 20 лет удалось добиться довольно существенных прорывов в лечении таких больных.
Во-первых, оказалось, что единичные метастазы в отдаленные органы очень «покладисты» в лечении КРР. Мы знаем, что примерно в 70% случаев КРР метастазирует в печень. Во вторую очередь в легкое. Сейчас появились разные способы воздействия на метастазы в печени. Помимо обычной химиотерапии и хирургического лечения, есть еще методы малоинвазивного лечения, которые сводятся к закупорке одного или нескольких кровеносных сосудов печени эмболизатом, содержащим химиопрепарат. Кроме этого, к малоинвазивным инструментам относят методы локального воздействия на метастазы в печени: криоабляцию, микроволновую абляция и радиочастотную абляцию метастатических очагов. Все вышеперечисленное позволяет использовать, комбинировать и выбирать наиболее эффективные подходы в том или ином случае. Это позволяет боротся за таких больных довольно долго и существенно продлевать им жизнь.
Во-вторых, появились новые таргетные препараты, которые дают очень хороший эффект. На фоне этих препаратов, при выполнении операции на печени, некоторые пациенты получили существенное 30-40% повышение выживаемости. Это большой прорыв.
Вышесказанное еще раз доказывает, что заниматься пациентами с КРР должны в стационарах, где работают все группы специалистов. Помимо просто хирурга, который может удалить опухоль, нужны еще грамотные химиотерапевты и радиологи, специалисты по хирургическому лечению печени и т.д. Если пациент может получить все это в одном стационаре, у него появляется шанс жить гораздо дольше.
В России такие места есть. Например, в Петербурге как минимум три таких учреждения: «Санкт-Петербургский клинический научно-практический центр специализированных видов медицинской помощи (онкологический)», «НМИЦ онкологии им. Н.Н. Петрова» и «Городской клинический онкологический диспансер». А в Москве можно выделить «Московскую городскую онкологическую больницу №62», «НМИЦ онкологии им. Н.Н. Блохина», «МНИОИ им. П.А. Герцена» и «Государственный Научный Центр Колопроктологии». Не нужно бояться названия. Пациенты часто думают, что если написано слово онкологический, то у них все плохо, мы там лечиться не будем. Ну нет же! Слово «онкологический» означает, что в клинике есть все необходимое для лечения этой сложной группы заболеваний.
Расскажите еще, пожалуйста, о влиянии локализации рака на выживаемость.
Есть данные, что при расположении первичной опухоли в левой половине ободочной кишки (то есть, в нисходящей ободочной, сигмовидной и прямой кишке) выживаемость существенно выше, чем при локализации рака в правой половине (слепой или восходящей ободочной кишке). Но пока этот вопрос на стадии изучения, и уже появляются альтернативные точки зрения.
Как правило, опухоли с левой стороны ободочной кишки диагностируются раньше. Это связано с тем, что, во-первых, в левой половине ободочной кишки опухоль часто вызывает стеноз — из-за него возникают нарушения дефекации и кровь в стуле, следовательно, пациенты раньше обращаются к врачу. Во-вторых, когда выполняют колоноскопическое исследование, иногда не могут пройти колоноскопом дальше определенного места. До левой половины добраться проще, далеко не все эндоскописты доходят до слепой кишки и тщательно рассматривают правую половину.
А это пока никто не учитывал в исследованиях. Есть мнение, что это все связано не с биологией опухоли, а лишь с такими факторами. Я сейчас ссылаюсь на нашего самого известного онкогенетика, профессора Имянитова Евгения Наумовича. Он считает, что глобальных генетических различий между правой и левой половиной опухоли нет.
Какие советы вы могли бы дать пациентам?
Первое: вы не должны бояться обследований.
Второе: если у вас подтвердился диагноз КРР, обязательно обратитесь в специализированное учреждение! Часто пациент выбирает врача по советам: говорят у него «хорошие руки». Но если руководствоваться этим принципом, то мы никогда не узнаем реального качества операции, мы увидим только шов. Дальнейшая судьба пациента хирургу, как правило, неизвестна, с рецидивом приходят уже к онкологу. Поэтому важно, чтобы пациент выбирал место лечения, специализирующееся на его заболевании. Если есть отделение в городе, где оперируют пятьсот колоректальных раков в год, то нужно идти туда. А не в клинику, где это вмешательство делают двадцать раз в год, но каждый раз говорят, что с «хорошими руками».
В развитых странах, если отделение выполняет менее пятидесяти операций в год, связанных с КРР, то его перепрофилируют. В Санкт-Петербурге совершенный разброс в этом плане. Пациенты обращаются в разные учреждения и оперируются не в профильных центрах. И дело даже не в том, что там плохие доктора, просто это не их работа. Так же, как если я начну оперировать грыжи. Да, я умею это делать, но это не моя задача. А у нас все, кому не лень, хватаются оперировать рак.
А потом министр здравоохранения приезжает и удивляется, что в Санкт-Петербурге плохая онкологическая статистика. А это все из-за того, что в Петербурге зачастую не следуют порядку оказания помощи онкологическим больным. У нас примерно половина пациентов оперируется не в профильных учреждениях на сегодняшний день. А отвечают за результаты онкологи.
Мы боремся с этим уже давно и продолжим это делать, чтобы закрепить эту простую истину: онкологические больные должны лечиться у онкологов. Это очень важно.
И третий пункт, люди мало что знают о своих правах. У нас в городе пациент, которому поставили диагноз рак, имеет право сделать все обследования, которые необходимы для определения тактики, бесплатно и в рамках одного учреждения. Что сегодня происходит с такими больными? Им ставят диагноз и начинают гонять: в одно место — сделать КТ, в другое — выполнить платно МРТ, а потом только берут на операцию в непрофильное учреждение. А после оказывается, что ему нужно делать химиотерапию. А еще желательно, перед тем как назначить лекарства, провести иммуногистохимическое и молекулярно-генетическое консультирование для более прецизионного лечения. И все это платно.
Такой бардак твориться сейчас в Санкт-Петербурге сплошь и рядом. Больные должны знать, что они могут прийти и получить весь объем исследований в одном месте, бесплатно, для того чтобы определиться с тактикой лечения. И не нужно бояться, что в государственном учреждении это займет много времени. На сегодняшний день, есть приказ комитета по здравоохранению, в котором говорится, что в течение десяти рабочих дней пациент должен быть обследован. Любой врач из поликлиники, если он заподозрил диагноз КРР, может направить человека к нам. Пациент спокойно позвонит по телефону и запишется на следующий день на консультацию. Это то, как нужно поступить в случае обнаружения колоректального рака, но, к сожалению, об этом мало кто знает.
