Нужно найти кинетическую энергию электрона и перевести ее в эВ
Знаток
(401),
закрыт
9 лет назад
Валентина Вавилова(Серкова)
Гений
(62183)
9 лет назад
Всё верно у тебя, кинетическая энергия только численно равна напряжению, но это две разные физические величины. ( разве не бывает скорость = 2м/c, и пройденный путь =2м, мы же не говорим, что они равны, просто числа одинаковые, вот и всё).
JULIANDCЗнаток (401)
9 лет назад
хорошо численно они равны, как быть с единицами измерения? не можем же просто поделив и умножив на одно и тоже (e) получить разные величины, это должно как то объясняться, значит формула не верная, т. к.
U = S(м) / t(с) и равно мс и если U*tt = все также будут мс и ничто иное. непонятно.
Условие задачи:
Электрон приобрел скорость, равную 0,98 скорости света. Найти кинетическую энергию электрона.
Задача №11.5.27 из «Сборника задач для подготовки к вступительным экзаменам по физике УГНТУ»
Дано:
(upsilon = 0,98c), (E_к-?)
Решение задачи:
Кинетическую энергию электрона (E_к), движущегося со скоростью (upsilon) относительно наблюдателя, можно найти по следующей формуле:
[{E_к} = frac{{{m_0}{c^2}}}{{sqrt {1 – frac{{{upsilon ^2}}}{{{c^2}}}} }} – {m_0}{c^2};;;;(1)]
В этой формуле (m_0) – масса покоя электрона, равная 9,1·10-31 кг, (c) – скорость света в вакууме, равная 3·108 м/с.
Так как по условию задачи электрон приобрел скорость, равную 0,98 скорости света, то есть (upsilon = 0,98c), то формула (1) примет вид:
[{E_к} = frac{{{m_0}{c^2}}}{{sqrt {1 – frac{{{{left( {0,98c} right)}^2}}}{{{c^2}}}} }} – {m_0}{c^2}]
[{E_к} = frac{{{m_0}{c^2}}}{{sqrt {1 – {{0,98}^2}} }} – {m_0}{c^2}]
[{E_к} = {m_0}{c^2}left( {frac{1}{{sqrt {1 – {{0,98}^2}} }} – 1} right)]
Посчитаем численный ответ (1 эВ = 1,6·10-19 Дж):
[{E_к} = 9,1 cdot {10^{ – 31}} cdot {left( {3 cdot {{10}^8}} right)^2} cdot left( {frac{1}{{sqrt {1 – {{0,98}^2}} }} – 1} right) = 3,3 cdot {10^{ – 13}};Дж = 2,06;МэВ]
Ответ: 2,06 МэВ.
Если Вы не поняли решение и у Вас есть какой-то вопрос или Вы нашли ошибку, то смело оставляйте ниже комментарий.
Смотрите также задачи:
11.5.26 Электрон, ускоренный электрическим полем, приобрел скорость, при которой его масса
11.5.28 Масса движущегося электрона в 11 раз больше его массы покоя. Определить кинетическую
11.5.29 Какую ускоряющую разность потенциалов должен пройти первоначально покоящийся
поделиться знаниями или
запомнить страничку
- Все категории
-
экономические
43,658 -
гуманитарные
33,653 -
юридические
17,917 -
школьный раздел
611,962 -
разное
16,905
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Теория
Бора водородоподобных атомов.
Нильс
Бор создал теорию строения атома,
способную объяснить опыты Резерфорда
и спектр излучения паров водорода.
Спектр
характеризует распределение интенсивности
излучения по шкале частот (или по шкале
длин волн).

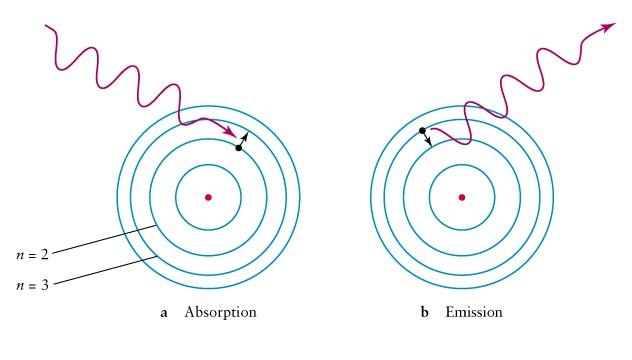
Постулаты
Бора.
1-й
постулат:
электрон
в атоме может двигаться только по
определенным стационарным орбитам,
находясь на которых, он не излучает и
не поглощает энергию. Момент импульса
электрона на этих орбитах кратен
постоянной Планка:
, (1)
me
– масса электрона,
– скорость электрона на орбите с номером
n,
rn
– радиус орбиты с номером n,
n
=1,2,3,….
Дж·с
– постоянная Планка.
2-й
постулат:
при
переходе электрона с одной стационарной
орбиты на другую излучается или
поглощается фотон, энергия которого
.
(2)
E
n1
и
E
n2
– энергия электрона в состоянии 1 и 2
(т.е. на орбитах 1 и 2),
– частота электромагнитных волн,
–
постоянная Планка.
Радиус
орбиты электрона в атоме водорода.
1-й
постулат Бора,
.
Выразим
скорость электрона:
.
(3)
Рассмотрим
круговые электронные орбиты. На электрон
с зарядом –e
со стороны ядра с зарядом +e
действует сила Кулона F,
сообщая электрону нормальное ускорение,
.
По
2-му закону Ньютона,
.
(4)
Сократим
и подставим скорость из (3):
.
Отсюда

Радиус
первой орбиты электрона (n
= 1), называется радиусом
Бора
,
=
0.53·10-10
м.
Радиус
орбиты электрона в атоме водорода
,
n
=1,2,3,…. – номер орбиты.
Энергия
электрона в атоме водорода.
Энергия
электрона представляет собой сумму
кинетической энергии
и
потенциальной
.
и
.
Потенциальная
энергия – это энергия электрона с
зарядом
в электрическом поле ядра. Из уравнения
(4) видно, что
.
Тогда
на n
–ой
орбите энергия электрона равна
=
=.
Т.е.
кинетическая энергия электрона равна
полной энергии, взятой со знаком «-».
Также
полную энергию можно записать через
потенциальную:
=
, или
.
Подставим
.
Тогда
=
.
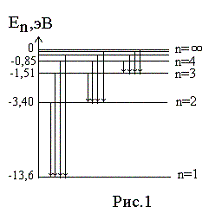
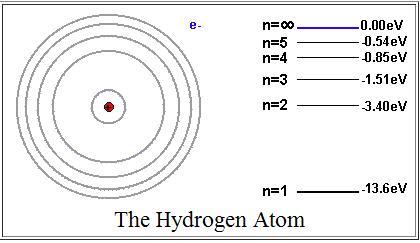
Энергия
на первой орбите (на первом энергетическом
уровне) равна
=
= -13,6 эВ.
Величину
=
13,6 эВ = 2,18∙10-18
Дж
называют
энергией ионизации
(эта энергия необходима, чтобы перевести
электрон, находящийся на первом уровне,
в свободное состояние, т.е. чтобы
ионизовать атом). Окончательно, энергия
электрона на n
–ом
энергетическом уровне (на n
–ой
орбите) записывается как
=
.
Спектр излучения водорода.
Энергия
излучаемого или поглощаемого кванта:
.
Частота
,
длина волны,
– скорость света в вакууме.
=
+
=
,
=
.
=
–
формула Бальмера,
определяет
длины волн в спектре атома водорода.
=
1,1∙107
м-1
– постоянная Ридберга.
и
– номера энергетических состояний
(номера орбит) электрона.
Переходы
электрона с возбужденных энергетических
состояний на основной энергетический
уровень (
= 1) сопровождаются излучением в УФ
области
спектра (серия линий Лаймана),
переходы
на уровень с
= 2 приводят к линиям в
видимой области
(серия Бальмера),
переходы
на уровень с
= 3, 4, 5, … приводят излучению в ИК
области.
Теория
Бора не смогла объяснить строение
сложных атомов. Для объяснения поведения
микрочастиц была развита квантовая
механика.
Она
основана на том, что любая микрочастица,
наряду с корпускулярными, обладает
также волновыми свойствами (гипотеза
де Бройля).
Для
фотона, импульс
.
По
аналогии с фотоном, любую микрочастицу
можно рассматривать как волну с длиной
волны
,
–
длина волны де Бройля.
Гипотеза
де Бройля подтверждена экспериментально
наблюдением дифракции электронов, а
затем и протонов.
Принцип
неопределенностей.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Кинетическая энергия электрона Решение
ШАГ 0: Сводка предварительного расчета
ШАГ 1. Преобразование входов в базовый блок
Атомный номер: 17 –> Конверсия не требуется
Квантовое число: 8 –> Конверсия не требуется
ШАГ 2: Оцените формулу
ШАГ 3: Преобразуйте результат в единицу вывода
-1.57574641085916E-36 Джоуль –> Конверсия не требуется
25 Структура атома Калькуляторы
Кинетическая энергия электрона формула
Энергия атома = -2.178*10^(-18)*(Атомный номер)^2/(Квантовое число)^2
EeV = -2.178*10^(-18)*(Z)^2/(nquantum)^2
Что такое теория Бора?
Теория Бора – это теория атомной структуры, в которой атом водорода (атом Бора), как предполагается, состоит из протона в качестве ядра, с одним электроном, движущимся по отдельным круговым орбитам вокруг него, каждая из которых соответствует определенному квантованному энергетическому состоянию: теория была распространена на другие атомы.