Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 2 декабря 2019 года; проверки требуют 11 правок.
| Сульфид калия | |
|---|---|
 |
|
| Общие | |
| Систематическое наименование |
калия сульфид |
| Традиционные названия | калий сернистый, сульфид калия, калия моносульфид |
| Хим. формула | K2S |
| Физические свойства | |
| Состояние | бесцветный порошок с запахом тухлых яиц |
| Молярная масса | 110,262 г/моль |
| Плотность | 1,805 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 471; 948 °C |
| Мол. теплоёмк. | 76,15 Дж/(моль·К) |
| Энтальпия | |
| • образования | −387,3 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | растворяется с образованием KSH, KOH |
| • в остальных веществах | растворяется в этаноле и глицерине |
| Структура | |
| Кристаллическая структура | кубическая сингония |
| Классификация | |
| Рег. номер CAS | 1312-73-8 |
| PubChem | 162263 |
| Рег. номер EINECS | 215-197-0 |
| SMILES |
[S-2].[K+].[K+] |
| InChI |
InChI=1S/2K.S/q2*+1;-2 DPLVEEXVKBWGHE-UHFFFAOYSA-N |
| RTECS | TT6000000 |
| ChemSpider | 142491 |
| Безопасность | |
| Пиктограммы ECB |
|
| NFPA 704 |
1 3 0 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

Калия сульфид — бинарное неорганическое химическое соединение калия с серой. Представляет собой соединение с формулой K2S[источник не указан 1008 дней].
Физические свойства[править | править код]
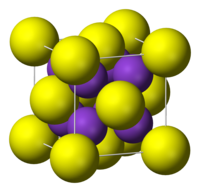
Сульфид калия K2S — бесцветные кубические кристаллы (a = 0,739 нм, Z=4; пространственная группа Fm3m). Хорошо растворимы в воде (с гидролизом). Растворим в спирте и глицерине. Гигроскопичен, образует ди- и пентагидраты.
Получение[править | править код]
Прямой синтез из элементов:
Восстановление сульфата калия водородом:
или углеродом (в промышленности — кокс):
Сульфит калия при нагревании диспропорционирует:
Химические свойства[править | править код]
На воздухе медленно окисляется:
в зависимости от условий проведения этой реакции образуются побочные продукты: коллоидная сера, полисульфиды калия.
Сульфид калия при поджигании сгорает:
Так как сероводород является слабой кислотой, то сульфид калия разлагается кислотами:
Концентрированные кислоты могут окислять выделяемый сероводород:
При кипячении раствора сульфида калия с серой или сплавления его с серой образуются полисульфиды:
для калия выделены полисульфиды вплоть до n = 6.
При пропускании через раствор сульфида калия избытка сероводорода образуется гидросульфид калия:
Реагирует, образовывая соединения с сульфидами Ag, Sn и другими.
Применение[править | править код]
Калия сульфид компонент светочувствительных эмульсий в фотографии, аналитический реагент для разделения сульфидов металлов, является компонентом входящим в состав для удаления наружного слоя шкур.
В пиротехническом деле[править | править код]
Сульфид калия образуется при сжигании пороха.
Литература[править | править код]
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
Физические свойства
Сульфид калия K2S — белое вещество, плавится без разложения. Термически устойчивый. Хорошо растворяется в воде.
Относительная молекулярная масса Mr = 110,26; относительная плотность для тв. и ж. состояния d = 1,74; tпл = 912º C.
Способ получения
1. Сульфид калия можно получить путем взаимодействия калия и серы при температуре 100 — 200º C:
2K + S = K2S
2. При взаимодействии с углеродом (коксом) сульфат калия при температуре 900º C образует сульфид калия и угарный газ:
K2SO4 + 4C = K2S + 4CO
3. При температуре 600º C в присутствии оксида железа (III) сульфат калия реагирует с водородом. Взаимодействие сульфата калия с водородом приводит к образованию сульфида калия и воды:
K2SO4 + 4H2 = K2S + 4H2O
Качественная реакция
Качественная реакция на сульфид калия — взаимодействие его с хлоридом меди, в результате реакции происходит образование черного осадка:
1. При взаимодействии с хлоридом меди, сульфид калия образует осадок сульфид меди и хлорид калия:
CuCl2 + K2S = CuS↓ + 2KCl
Химические свойства
1. Сульфид калия может реагировать с простыми веществами:
Твердый сульфид калия реагирует с кислородом при температуре выше 500º C. При этом образуется сульфат калия:
K2S + 2O2 = K2SO4
2. Сульфид калия вступает в реакцию со многими сложными веществами:
2.1. Сульфид калия способен реагировать со многими кислотами:
2.1.1. Сульфид калия реагирует с разбавленной хлороводородной кислотой. Взаимодействие сульфида калия с хлороводородной кислотой приводит к образованию хлорида калия и газа сероводорода:
K2S + 2HCl = 2KCl + H2S↑
2.1.2. Сульфид калия взаимодействует с концентрированной серной кислотой. При этом образуются гидросульфат калия, газ оксид серы, осадок сера и вода:
K2S + 3H2SO4 = 2KHSO4 + SO2↑ + S↓ + H2O
2.1.3. При взаимодействии сульфида калия с концентрированной азотной кислотой выделяются нитрат калия, газ оксид азота, сера и вода:
K2S + 4HNO3 = 2KNO3 + 2NO2↑ +S↓ + H2O
2.1.4. Взаимодействуя с насыщенной сероводородной кислотой холодный сульфид калия образует гидросульфид калия:
K2S + H2S = 2KHS
Опубликовано 3 года назад по предмету
Химия
от 79046092391
составить формул сульфида калия
-
Ответ
Ответ дан
KAMARu3CSK2S – сульфид калия – бинарное неорганическое химическое соединение калия с серой
-
Ответ
Ответ дан
ximikkkK2S соль, растворимая.
Пример получения:
K2SO4 + BaS = BaSO4↓ + K2S
Самые новые вопросы
![]()
Математика – 3 года назад
Решите уравнения:
а) 15 4 ∕19 + x + 3 17∕19 = 21 2∕19;
б) 6,7x – 5,21 = 9,54
![]()
Информатика – 3 года назад
Помогите решить задачи на паскаль.1)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти произведение всех элементов массива.2)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти сумму четных элементов массива.3)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти максимальный элемент массива.4)
дан массив случайных чисел (количество элементов
вводите с клавиатуры). найти максимальный элемент массива среди элементов,
кратных 3.
![]()
География – 3 года назад
Почему япония – лидер по выплавке стали?
![]()
Математика – 3 года назад
Чему равно: 1*(умножить)х? 0*х?
![]()
Русский язык – 3 года назад
В каком из предложений пропущена одна (только одна!) запятая?1.она снова умолкла, точно некий внутренний голос приказал ей замолчать и посмотрела в зал. 2.и он понял: вот что неожиданно пришло к нему, и теперь останется с ним, и уже никогда его не покинет. 3.и оба мы немножко удовлетворим свое любопытство.4.впрочем, он и сам только еле передвигал ноги, а тело его совсем застыло и было холодное, как камень. 5.по небу потянулись облака, и луна померкла.
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Сульфид калия – это неорганическое соединение сложного состава, состоящее из атомов калия и серы. Это бескислородная соль, которая применяется в основном в фотографии, кожевенном деле, пиротехнике, а также в химии. В органике и неорганике сульфид калия – предшественник важных веществ и ценный реагент, без которого невозможно разделение сульфидов металлов. Из-за высокой химической активности калиевый сульфид токсичен, поэтому при работе с ним требуется соблюдать осторожность.
Содержание
- Что такое сульфид калия, формула
- Физические свойства, внешний вид
- Химические свойства, реакции
- Производство и получение
- Применение
- Применение калия сульфида в химии и фотографии
- Применение калия сульфида в кожевенном производстве и других сферах
- Где купить и сколько стоит
- Перевозка, хранение, класс опасности
- Заключение
Что такое сульфид калия, формула
Сульфид калия представляет собой соль, в которой отсутствует кислород, а два атома калия связаны с серой. Химическая формула – K2S, молекула имеет особую форму куба, в которой углы занимает отрицательно заряженная сера (анион), а в центре располагаются положительно заряженные калии (катионы). Это так называемая антифлюоритовая структура – противоположность пространственной организации флюорита, в которой углы составляют катионы, а внутренние позиции – анионы.
Физические свойства, внешний вид
Сульфид калия — это мелкодисперсные кубические кристаллы, не имеющие цвета и вкуса, запах неприятный, напоминающий тухлые яйца (это связано с выделением при достаточной влажности сероводорода). Загрязнённый или технический реагент может иметь жёлто-коричневую окраску. Плотность невысокая и составляет 1,805 г/см3.
Гигроскопичен, быстро впитывает влагу и образует кристаллогидраты: дигидрат – K2S ∙ 2H2O, петагидрат – K2S ∙ 5H2O. Сульфид калия хорошо растворяется в воде, подвергается гидролизу. Растворим в органических растворителях, таких как спирт (метанол, этанол), эфиры, фенолы, глицерин. Раствор сульфида калия даёт щелочную среду (pH более 7).
Химические свойства, реакции
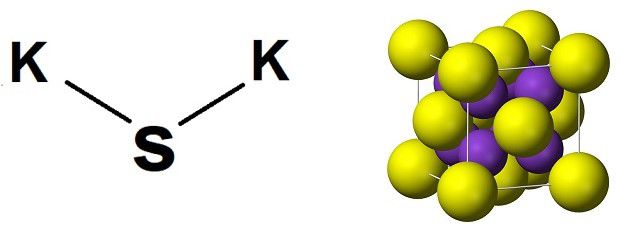
Раствор сульфида калия обладает повышенной реакционной способностью. Так, сульфид калия реагирует с кислородом, отдавая электроны. Результат может быть разным, в том числе выделение сульфата при сгорании (температура порядка 500 °С):
K2S + 2O2 → K2SO4
При медленном окислении возможен иной исход, тогда продуктом реакции выступает полисульфид и гидроксид калия:
K2S + O2 → K2S2O3 + KOH
Сульфид калия реагирует с кислотами. Так, он даёт хлорид калия и сернистый водород при взаимодействии с соляной кислотой:
K2S + 2HCl → 2KCl + H2S↑
Раствор сульфида калия реагирует с концентрированной серной кислотой, образуя коллоидную серу, кислую соль гидроксульфат калия и сернистый ангидрид:
K2S + 3H2SO4 → 2KHSO4 + SO2↑ + S↓ + 2H2O
Расплав сульфида калия подвергается электролизу при прохождении электрического тока. При этом он распадается на составные элементы:
K2S → 2K + S
Раствор сульфида калия пропускает электричество, при этом происходит образование едкого калия:
K2S → S↓ + 2KOH + H2↑
Сульфид калия реагирует с водой, при этом он разлагается, образуя новые соединения. Гидролиз вещества протекает по аниону, поскольку в образуемых им ионах присутствуют частицы слабой кислоты. Реакция обратима и приводит к выделению большого количества гидроксид-анионов, защелачивающих раствор:
K2S + H2O → KHS + K+ + OH–
Реагент подвержен реакции ионного обмена с сульфатом алюминия, которая сопровождается необратимым разложением:
3K2S + Al(SO4)2 + 6H2O → 2Al(OH)3↓ + 3H2S↑ + 3K2SO4
Раствор сульфида калия реагирует с серой в разной концентрации, в итоге образуются полсульфиды с переменной n, где n – любое натуральное число от 2 и выше:
K2S + (n-1)S → K2Sn
Производство и получение

Кристаллы сульфида калия
В лабораторных условиях проводят прямой синтез сульфида калия при 100-200 °С:
2K + S → K2S
В промышленности используют реакцию восстановления углеродом (каменноуглеродный кокс) при 900 °С:
K2SO4 + 4С → K2S + 4CO
Для восстановительной реакции можно брать водород. Взаимодействие протекает при участии катализатора (Fe2O3) и нагреве до 600 °С:
K2SO4 + 4H2 → K2S↓ + 4H2O
В качестве сырья на некоторых производствах предпочтение отдают сульфиту калия, т.к. он подвержен термолизу при 600 °С:
4K2SO3 + K2S + 3K2SO4
Промышленное получение ведётся в несколько этапов:
- Сернокислый калий предварительно высушивают, затем смешивают с жжённой магнезией (MgO) в определённых пропорциях.
- Смесь поступает специализируемую вращающуюся печь, которая разогревается до 950 °С.
- Внутрь подаётся водород, окись углерода. Образующиеся газы проходят через теплообменник, отдают тепло, охлаждаются, и отправляются на выхлоп.
- Образовавшийся в растворе осадок выщелачивают, оксид магния отфильтровывают, высушивают и переводят на повторное использование.
- Сульфид калия попадает в кристаллизатор, где перекристаллизовывается до необходимой чистоты, после подсушивается и расфасовывается в упаковочные ёмкости.
Применение
Основная сфера применения сульфида калия – химия. Он играет большую роль в реакциях синтеза многих значимых для хроматографии и металлургии веществ. Сульфид калия необходим для получения качественных кожматериалов, применение калия сульфида для удаления волос с натуральной кожи обусловлено его относительной дешевизной и доступностью. Реактив вносят в состав фотоэмульсий, пиротехнику, его используют для добычи пестицидов и дифференциации металлов.
Применение калия сульфида в химии и фотографии
Сульфид калия — это ценный реактив, который используется для синтеза сульфатов и промежуточных соединений, среди которых:
- полисульфиды, необходимые для выпуска каучуков, воронения стали, борьбы с насекомыми-вредителями;
- сернистый калий;
- каустический поташ;
- диоксид серы.
Вещество применяют для разделения и анализа сульфатов. В фотографических светоэмульсиях сульфид калия – компонент для сенсибилизации фотоматериалов – увеличения светочувствительности.
Применение калия сульфида в кожевенном производстве и других сферах
Сульфид калия способствует очищению натуральной кожи от мелких волосков, обеспечивает её прочность и долговечность, закрепление окраски, предотвращает выцветания и обветшание с течением времени. Наряду с другими средствами его включат в первичную обработку для улучшения товарного вида и внешних качеств.
Сульфид калия применяют в фейерверках для усиления яркости огня. Применение соединения отмечается в традиционных японских бенгальских огнях под названием «сенко ханаби».
Где купить и сколько стоит
Сульфид калия продаётся заводами-производителями, в интернет-магазинах. Оптовая стоимость от 75 рублей за 1 кг. Розничная цена 100 грамм – 125-170 рублей.
Перевозка, хранение, класс опасности
Сульфид калия относится к 2 классу (выскоопасные отходы), способен разъедать слизистые оболочки, оставлять глубокие ожоги. Химикат следует хранить в оригинальной герметично закрытой упаковки вдали от источников влаги при относительной влажности воздуха не более 50%. Транспортировка осуществляется всеми видами крытого транспорта, за исключением самолётов.
Заключение
Сульфид калия – это соединение, востребованное в аналитике и химической промышленности. Его высокая реактивность обусловила применение в качестве реагента для добычи различных веществ, пиротехническое и фотографическое использование. Он является компонентом составов для обработки кожевенных изделий.
Читайте также:
- Сульфид натрия: описание, реакции, получение, применение
- Оксид азота: свойства, применение, реакции
- Угольная кислота: описание, свойства и реакции, применение
- Сульфат алюминия: свойства, применение
Сайт предоставляет информацию в справочных целях, только для ознакомления. Поставить диагноз и назначить адекватное лечение может только врач! Медикаменты и народные средства должны назначаться специалистом, так как имеют противопоказания и побочные действия! Посещение и консультации квалифицированного специалиста строго обязательны!
![]() Загрузка…
Загрузка…
| Сульфид калия | |
|---|---|
 |
|
| Систематическое наименование |
калия сульфид |
| Традиционные названия | калий сернистый, сульфид калия, калия моносульфид |
| Хим. формула | K2S |
| Состояние | бесцветный порошок с запахом тухлых яиц |
| Молярная масса | 110,262 г/моль |
| Плотность | 1,805 г/см³ |
| Температура | |
| • плавления | 471; 948 °C |
| Мол. теплоёмк. | 76,15 Дж/(моль·К) |
| Энтальпия | |
| • образования | −387,3 кДж/моль |
| Растворимость | |
| • в воде | растворяется с образованием KSH, KOH |
| • в остальных веществах | растворяется в этаноле и глицерине |
| Кристаллическая структура | кубическая сингония |
| Рег. номер CAS | 1312-73-8 |
| PubChem | 14800 |
| Рег. номер EINECS | 215-197-0 |
| SMILES |
[SH-].[K+].[K+] |
| InChI |
1S/2K.H2S/h;;1H2/q2*+1;/p-1 FANSKVBLGRZAQA-UHFFFAOYSA-M |
| RTECS | TT6000000 |
| ChemSpider | 14116 |
| Пиктограммы ECB | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Калия сульфид — бинарное неорганическое химическое соединение калия с серой. Представляет собой соединение с формулой K2S.
Содержание
- 1 Физические свойства
- 2 Получение
- 3 Химические свойства
- 4 Применение
- 4.1 В пиротехническом деле
Физические свойства
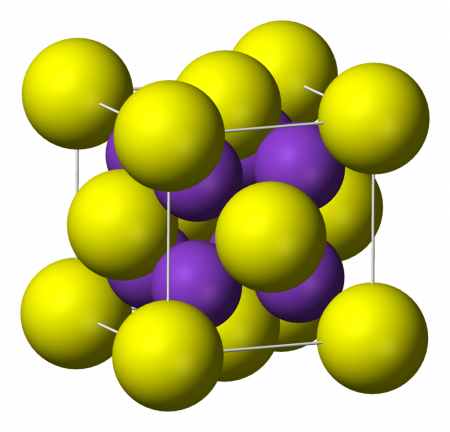
Сульфид калия K2S — бесцветные кубические кристаллы (a = 0,739 нм, Z=4; пространственная группа Fm3m). Хорошо растворимы в воде (с гидролизом). Растворим в спирте и глицерине. Гигроскопичен, образует ди- и пентагидраты.
Получение
Прямой синтез из элементов:
- 2K + S →100−200oC K2S
Восстановление сульфата калия водородом:
- K2SO4 + 4H2 →600oC,Fe2O3 K2S + 4H2O
или углеродом (в промышленности — кокс):
- K2SO4 + 4C →900oC K2S + 4CO
Сульфит калия при нагревании диспропорционирует:
- 4K2SO3 →600oC K2S + 3K2SO4
Химические свойства
На воздухе медленно окисляется:
- 2K2S + 2O2 + H2O ⟶ K2S2O3 + 2KOH
в зависимости от условий проведения этой реакции образуются побочные продукты: коллоидная сера, полисульфиды калия.
Сульфид калия при поджигании сгорает:
- 2K2S + 2O2 →>500oC K2SO4
Так как сероводород является слабой кислотой, то сульфид калия разлагается кислотами:
- K2S + 2HCl ⟶ 2KCl + H2S↑
Концентрированные кислоты могут окислять выделяемый сероводород:
- K2S + 3H2SO4 ⟶ 2KHSO4 + SO2↑ + S↓ + 2H2O
При кипячении раствора сульфида калия с серой или сплавления его с серой образуются полисульфиды:
- K2S + (n − 1)S → K2Sn
для калия выделены полисульфиды вплоть до n = 6.
При пропускании через раствор сульфида калия избытка сероводорода образуются гидросульфид калия:
- K2S + H2S ⟶ 2KHS
Реагирует, образовывая соединения с сульфидами Ag, Sn и другими.
Применение
Калия сульфид компонент светочувствительных эмульсий в фотографии, аналитический реагент для разделения сульфидов металлов, является компонентом входящим в состав для удаления наружного слоя шкур.
В пиротехническом деле
Сульфид калия образуется при сжигании пороха.











