Моль — условное количество вещества
Добавлено: 3 октября 2021 в 12:58

Химия — наука, изучающая взаимодействие веществ на атомном и молекулярном уровнях. Эти процессы значительно отличаются от привычного нам макроуровня и поэтому требуют специфических подходов, в том числе к «подсчету» и «взвешиванию».
Школьный курс химии включает понятия «моль» и «молярной массы». Они кажутся сложными, но если разобраться, то вы без труда поймете сущность этих понятий и научитесь ими пользоваться при решении задач.

Моль
Понятие «моль» попытаемся разобрать и, самое главное, понять на примере всем знакомой реакции взаимодействия кислорода и водорода. Когда одна молекула O2 соединяется с двумя молекулами H2, получается две молекулы H2O:
- O2 + 2H2 = 2H2O
То есть, чтобы максимально полно провести химическую реакцию, мы должны взять на каждую молекулу кислорода две молекулы водорода. Итак, у нас есть 100 г кислорода.
Сколько понадобится водорода для протекания процесса? И тут возникает первый вопрос: сколько молекул в 100 г кислорода? Наверное, миллиарды или даже миллиарды миллиардов? И сколько их в 100 г водорода? Уж точно в не в 2 раза меньше.
Как вообще подсчитать молекулы, ведь они бывают совершенно разными, «тяжелыми» и «легкими». Этими вопросами задавались и люди, закладывавшие основу современной химической науки.
Был найден простой выход, который помогает легко и изящно решить проблему. Химики решили взять за единицу измерения не одну молекулу, а определенное их количество, причем очень большое. Таким образом эта единица измерения приводит микроуровень к макроуровню. Она называется «моль».
Моль — это количество вещества из 6,02214076⋅1023 атомов или молекул. Оно не имеет физического смысла и изначально было привязано к массе определенного количества (12 граммов) углерода-12, но позже переопределено, как и многие другие единицы системы СИ.
В школьных расчетах количество структурных единиц в моле, которое также называется постоянной Авогадро, обычно округляют до 6,022⋅1023 и обозначают NA.
С этой величиной связано другое химическое понятие — «количество вещества», то есть количество структурных единиц в определенной его порции. Оно обозначается буквой ν (ню).
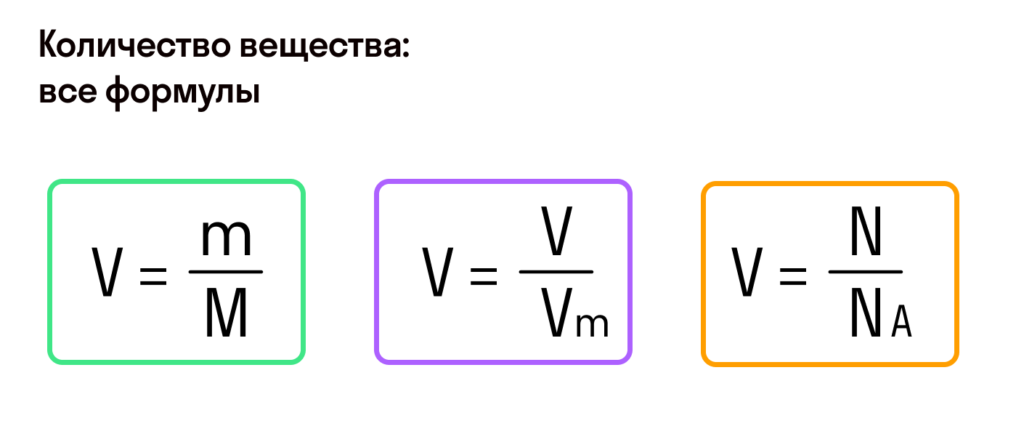
Примеры
В стакане содержится 2 моль воды. Сколько молекул воды находится в стакане?
- N = ν⋅ NA =2 ⋅ 6,022⋅1023 = 12,044⋅1023 молекул воды.
Также можно решить обратную задачу. Сколько молей вещества составляют 24,088⋅1023 молекул воды?
- ν⋅ = N / NA = 24,088⋅1023 / 6,022⋅1023 = 4 моля.

Что называется молярной массой
Итак, мы поняли, что моль — условное количество вещества, выбранное для удобства химиков. Это даже не миллиарды миллиардов, как мы предположили ранее, а миллиарды триллионов, что никак не облегчает задачу подсчета этих структурных единиц.
Как же все-таки узнать, сколько атомов или молекул в 100 граммах того или иного вещества? Теперь хорошо бы связать количество вещества и его массу, ведь это не одно и то же. Нам поможет «молярная масса» — 1 моль вещества или 6,022⋅1023 структурных единиц этого вещества.
Итак, масса вещества равна массе порции вещества m к количеству молекул ν в его порции:
- М = m / ν.
Вооружившись этим знанием, мы можем переводить граммы в число молекул и наоборот. При этом следует учесть, что молярная масса численно идентична молекулярной массе (то есть массе молекулы), выраженной в атомных единицах массы, и относительной молекулярной массе.

Пример
Найдем массу 5 моль воды.
Чтобы решить эту задачу, обратимся к формуле молярной массы и выразим из нее массу:
- m = М ⋅ ν
В этой формуле мы знаем количество вещества ν = 5 моль, а молярную массу сложной молекулы нужно определить, как сумму молярных масс составляющих ее химических элементов:
- M (H2O) = 2 ⋅M (H) + M (O)
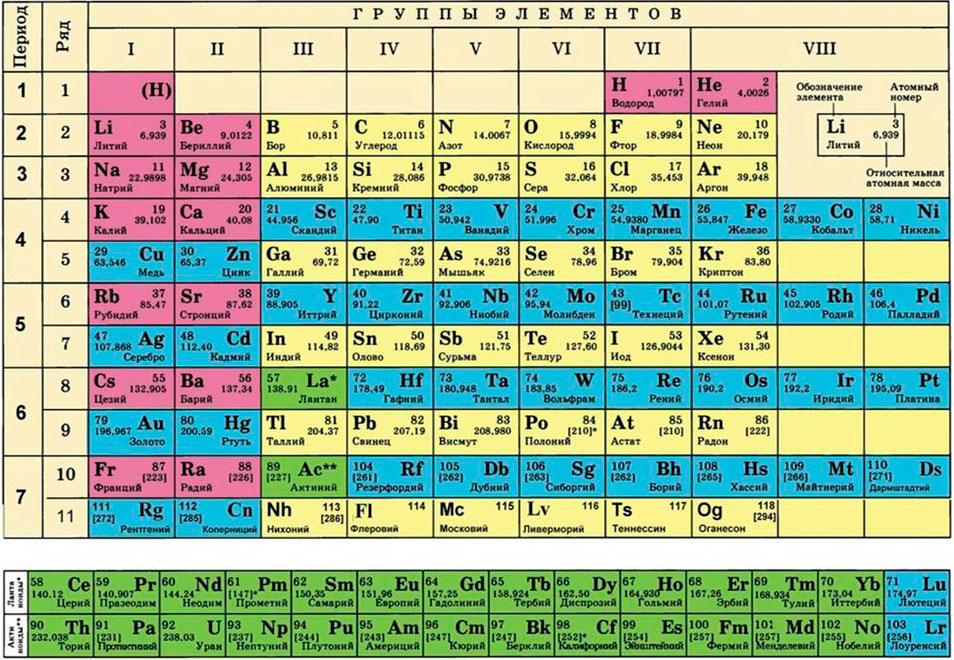
Где взять молярные массы кислорода и водорода (в соединение входит два атома водорода, поэтому его молярную массу умножаем на 2)?
Для этого нам понадобится таблица Менделеева и значение «относительной атомной массы», которая, как мы уже знаем, идентична молекулярной. Это значение приведено для каждого химического элемента и для водорода равно 1,00797 (то есть близко к 1), для углерода — близко к 6, для кислорода — около 16.
Подставим соответствующие значения в исходную формулу и получим:
- M (H2O) = 2 ⋅M (H) + M (O) = 2 ⋅ 1 + 16 = 18 г/моль.
То есть вес 1 моль воды составляет 18 граммов. Теперь можем подсчитать массу 5 моль воды:
- m = М ⋅ ν = 18 ⋅ 5 = 90 г.
Аналогичным образом мы можем подсчитать количество вещества, которое содержится в определенном образце заданной массы. Для примера возьмем оксид алюминия Al2O3 и узнаем, сколько моль в 400 граммах этого вещества. Для этого выразим количество вещества через молярную массу и подставим исходные данные:
- ν = m / М = 400 / (2 ⋅ М (Al) + 3 ⋅ (O)) = 400 / (2 ⋅ 75 + 3 ⋅ 16) = 400 / (150 + 48) = 400 / 198 ≈ 2,02 моль.
Занимайтесь на курсах ЕГЭ и ОГЭ в паре TwoStu и получите максимум баллов на экзамене:

Эксперт по подготовке к ЕГЭ, ОГЭ и ВПР
Задать вопрос
Закончил Московский физико-технический институт (Физтех) по специальности прикладная физика и математика. Магистр физико-математических наук. Преподавательский стаж более 13 лет. Соучредитель курсов ЕГЭ и ОГЭ в паре TwoStu.
Читайте также:
- Относительная атомная и молекулярная масса
- Количество вещества. Постоянная Авогадро
- Молярная масса
- Молярный объем
- Задачи
п.1. Относительная атомная и молекулярная масса
Массы атомов и молекул, из которых состоят вещества, очень малы. Поэтому их чаще измеряют не в килограммах, а используют внесистемную единицу – атомную единицу массы.
Атомная единица массы – внесистемная единица, равная 1/12 массы свободного покоящегося атома углерода (^{12}mathrm{C}), находящегося в основном состоянии. $$ 1 text{а. е. м}approx 1,66cdot 10^{-27} text{кг} $$
Относительная атомная масса – это физическая величина, показывающая, во сколько раз масса данного атома больше атомной единицы массы: $$ A_rapprox frac{m_{at}}{1,66cdot 10^{-27}} $$
Относительную атомную массу проще всего найти, пользуясь таблицей Менделеева.

Например:
(A_r(mathrm{H})=1,00797 text{а. е. м}) – относительная атомная масса водорода
(A_r(mathrm{C})=12,01115 text{а. е. м}) – относительная атомная масса углерода
(A_r(mathrm{N})=14,0067 text{а. е. м}) – относительная атомная масса азота
(A_r(mathrm{O})=15,9994 text{а. е. м}) – относительная атомная масса кислорода
На практике при решении учебных задач относительные атомные массы округляют и единицу измерения а.е.м. не пишут.
Например: $$ A_r(mathrm{H})=1, A_r(mathrm{C})=12, A_r(mathrm{N})=14, A_r(mathrm{O})=16 $$
Относительная молекулярная масса вещества – это физическая величина, показывающая, во сколько раз масса одной молекулы данного вещества больше атомной единицы массы: $$ M_rapprox frac{m_{mol}}{1,66cdot 10^{-27}} $$ Относительная молекулярная масса равна сумме относительных атомных масс всех атомов, из которых состоит данное вещество: $$ M_r=sum A_r $$
Например:
Найдем относительную молекулярную массу молекулы воды (mathrm{H_2O}), которая состоит из двух атомов водорода и одного атома кислорода $$ M_r(mathrm{H_2O})=2A_r(mathrm{H})+A_r(mathrm{O})=2cdot 1+16=18 $$
Масса молекулы вещества равна произведению относительной молекулярной массы данного вещества на величину 1 а.е.м., выраженную в килограммах: $$ m_{mol}approx 1,66cdot 10^{-27}cdot M_r (text{кг}) $$
Например:
Масса молекулы водорода $$ m(mathrm{H_2O})=approx 1,66cdot 10^{-27}cdot 18approx 2,99cdot 10^{-26} (text{кг}) $$
п.2. Количество вещества. Постоянная Авогадро
Моль – количество вещества системы, содержащей столько же структурных элементов (атомов, молекул, ионов), сколько содержится атомов в углероде-12 массой 0,012 кг.
В 1 моле любого вещества содержится одинаковое количество частиц $$ N_Aapprox 6,022cdot 10^{23} $$ Число (N_A) называют постоянной Авогадро.
Количество вещества – физическая величина, равная отношению числа однотипных структурных элементов (атомов, молекул, ионов), содержащихся в веществе, к числу Авогадро: $$ nu=frac{N}{N_A} $$ Единицей измерения количества вещества в СИ является моль.
Например:
В 5 молях углерода будет содержаться (N=5cdot N_Aapprox 6,022cdot 10^{23}approx 3,01cdot 10^{24}) атомов углерода. Причём, всё равно, будут ли эти атомы углерода образовывать уголь, графит или алмаз.
Аналогично, в 5 молях воды будет (N=5cdot N_Aapprox 3,01cdot 10^{24}) молекул воды. Причём, независимо от того, в каком агрегатном состоянии находится вода: в виде пара, жидкости или льда.
Т.е., «количество вещества» всегда говорит нам о «количестве частиц», независимо от других параметров.
п.3. Молярная масса
Молярная масса – это масса 1 моля вещества.
Из определения 1 моля вещества и относительной молекулярной массы следует, что молярная масса равна $$ mu=M_rcdot 10^{-3}frac{text{кг}}{text{моль}} $$
Например:
Молярная масса воды $$ mu(mathrm{H_2O})=M_r(mathrm{H_2O})cdot 10^{-3}=18cdot 10^{-3}frac{text{кг}}{text{моль}} $$
Алгоритм определения молярной массы вещества с помощью таблицы Менделеева
Шаг 1. По таблице Менделеева найти относительные атомные массы (A_{ri}) для всех элементов, входящих в молекулу вещества.
Шаг 2. Найти относительную молекулярную массу как сумму всех относительных атомных масс $$ M_r=sum_i A_{ri} $$ Шаг 3. Записать молярную массу в виде $$ mu=M_rcdot 10^{-3}frac{text{кг}}{text{моль}} $$
Например:
Найдем молярную массу этилового спирта begin{gather*} A_r(mathrm{C})=12, A_r(mathrm{H})=1, A_r(mathrm{O})=16\ M_r(mathrm{C_2H_5OH})= 2A_r(mathrm{C})+6A_r(mathrm{H}) +A_r(mathrm{O})=2cdot 12+6cdot 1+16=46\ mu(mathrm{C_2H_5OH})=46cdot 10^{-3}frac{text{кг}}{text{моль}} end{gather*}
п.4. Молярный объем
Молярный объем – это объем 1 моля вещества.
Молярный объем равен отношению молярной массы к плотности вещества: $$ V_{mu}=frac{mu}{rho} $$
Например:
Молярный объем воды begin{gather*} V_{mu}(mathrm{H_2O})=frac{18cdot 10^{-3} text{кг/моль}}{10^3 text{кг/м}^3}=18cdot 10^{-6}frac{text{м}^3}{text{моль}}=18frac{text{cм}^3}{text{моль}}=18frac{text{мл}}{text{моль}} end{gather*} Т.е. 1 моль воды занимает объем 18 мл (столовая ложка).
При нормальных условиях (t=0°C, ρ=1 атм) молярные объемы всех идеальных газов одинаковы и равны: $$ V_{mu text{газ}}=22,4frac{text{л}}{text{моль}} $$
Это свойство газов часто используется при изучении различных веществ и явлений в физике и химии.
п.5. Задачи
Задача 1. Масса кристалла серы равна 16 г. Сколько молекул серы (mathrm{S_8}) содержится в этом кристалле? (Ответ округлите до двух значащих цифр).
Дано:
(m=16 text{г}=16cdot 10^{-3} text{кг})
(A_r=32)
(N_A=6,022cdot 10^{23})
__________________
(N-?)
Относительная молекулярная масса одной молекулы $$ M_r=8cdot A_r=8cdot 32=256 $$ Молярная масса $$ mu=256cdot 10^{-3}frac{text{кг}}{text{моль}} $$ Количество вещества в кристалле серы: $$ nu=frac{N}{N_A}=frac{m}{mu} $$ Количество молекул в кристалле серы: $$ N=frac{m}{mu}N_A $$ $$ N=frac{1,6cdot 10^{-3}}{256cdot 10^{-3}}cdot 6,022cdot 10^{23}approx 3,8cdot 10^{22} $$ Ответ: (3,8cdot 10^{22})
Задача 2*. В кислородном генераторе на космическом корабле было получено 1,6 кг кислорода (mathrm{O_2}). Одному космонавту по норме требуется 600 литров кислорода в сутки. Считая условия для газа приблизительно нормальными, определите, на сколько часов космонавту хватит полученного кислорода.
Дано:
(m=1,6 text{кг})
(V_t=600frac{text{л}}{text{сут}}=25frac{text{л}}{text{ч}})
(A_r=16)
(V_{mu}=22,4frac{text{л}}{text{моль}})
__________________
(t-?)
Относительная молекулярная масса молекулы кислорода $$ M_r=2cdot A_r=32 $$ Молярная масса кислорода $$ mu=32cdot 10^{-3}frac{text{кг}}{text{моль}} $$ Количество вещества в полученном кислороде $$ nu=frac{m}{nu}=frac{V}{V_{mu}} $$ Объем полученного кислорода $$ V=frac{m}{mu}=V_{mu} $$ Количество часов для дыхания одного человека begin{gather*} t=frac{V}{V_t}=frac{m}{mu}frac{V_{mu}}{V_t}\[6pt] t=frac{1,6 text{кг}}{32cdot 10^{-3} text{кг/моль}}cdot frac{22,4 text{л/моль}}{25 text{л/ч}}=44,8 text{ч} end{gather*} Ответ: 44,8 ч.

Содержание
- Что такое молярная масса
- Как найти молярную массу
- Какова важность знания молярной массы вещества
Молярная масса является физическим свойством веществ. Это очень полезно при анализе, сравнении и прогнозировании других физических и химических свойств, таких как плотность, температура плавления, температура кипения и количество вещества, которое реагирует с другим веществом в системе. Существует более одного метода для расчета молярной массы. Некоторые из этих методов включают использование прямого уравнения, добавление атомных масс различных элементов в соединении и использование повышения точки кипения или понижения точки замерзания. Некоторые из этих основных методов будут кратко обсуждаться в этой статье.
Ключевые области покрыты
1. Что такое молярная масса
– определение, уравнение для расчета, объяснение
2. Как найти молярную массу
– Методы определения молярной массы
3.Какова важность знания молярной массы вещества
– Применение молярной массы
Ключевые термины: число Авогадро, точка кипения, калузиус-клапейрон, криоскопическая константа, эбуллиоскопическая константа, точка замерзания, точка плавления, молярность, молярная масса, молекулярная масса, осмотическое давление, относительная атомная масса

Что такое молярная масса
Молярная масса – это масса моля определенного вещества. Наиболее распространенной единицей измерения молярной массы вещества является гмоль-1, Однако единица СИ для молярной массы составляет кгмоль-1 (или кг / моль). Молярная масса может быть рассчитана с использованием следующего уравнения.
Молярная масса = масса вещества (кг) / количество вещества (моль)
Моль или моль – это единица измерения количества вещества. Один моль вещества равен очень большому числу, 6,023 x 1023 атомов (или молекул), из которых состоит вещество. Этот номер называется номером Авогадро. Это константа, потому что независимо от типа атома, один моль его равен этому количеству атомов (или молекул). Следовательно, молярной массе можно дать новое определение, то есть молярная масса представляет собой общую массу 6,023 х 10.23 атомы (или молекулы) конкретного вещества. Чтобы избежать путаницы, взгляните на следующий пример.
- Соединение А состоит из молекул А.
- Соединение B состоит из молекул B.
- Один моль соединения А состоит из 6,023 х 1023 молекул.
- Один моль соединения B состоит из 6,023 х 1023 молекул B.
- Молярная масса соединения А представляет собой сумму масс 6,023 х 10.23 Молекулы.
- Молярная масса соединения B представляет собой сумму масс 6,023 х 10.23 Молекулы В.
Теперь мы можем применить это для реальных веществ. Один моль Н2О состоит из 6,023 х 1023 ЧАС2О молекулы. Общая масса 6,023 х 1023 ЧАС2Молекулы O – около 18 г. Следовательно, молярная масса Н2О составляет 18 г / моль.
Как найти молярную массу
Молярная масса вещества может быть рассчитана с использованием нескольких методов, таких как;
- Используя атомные массы
- Используя уравнение для расчета молярной массы
- От точки кипения
- От замерзания депрессии
- От осмотического давления
Эти методы подробно обсуждаются ниже.
Использование атомных масс
Молярная масса молекулы может быть определена с использованием атомных масс. Это может быть сделано просто путем добавления молярной массы каждого присутствующего атома. Молярная масса элемента приведена ниже.
Молярная масса элемента = Относительная атомная масса х постоянная молярной массы (г / моль)
Относительная атомная масса – это масса атома относительно массы атома углерода-12, и она не имеет единиц измерения. Это соотношение может быть дано следующим образом.
Молекулярный вес A = масса одной молекулы A / [масса одного атома углерода-12 x (1/12)]
Давайте рассмотрим следующие примеры, чтобы понять эту технику. Далее приведены расчеты для соединений с одним и тем же атомом, комбинации нескольких разных атомов и комбинации большого количества атомов.
• Молярная масса Н2
o Типы присутствующих атомов = два атома Н
o Относительные атомные массы = 1,00794 (H)
o Молярная масса каждого атома = 1,00794 г / моль (Н)
o Молярная масса соединения = (2 х 1,00794) г / моль
= 2,01588 г / моль
• Молярная масса HCl
o Типы присутствующих атомов = один атом Н и один атом Cl
o Относительные атомные массы = 1,00794 (H) + 35,453 (Cl)
o Молярная масса каждого атома = 1,00794 г / моль (H) + 35,453 г / моль (Cl)
o Молярная масса соединения = (1 х 1,00794) + (1 х 35,453) г / моль
= 36,46094 г / моль
• Молярная масса С6ЧАС12О6
o Типы присутствующих атомов = 6 атомов C, 12 атомов H и 6 O атома Cl
o Относительные атомные массы = 12.0107 (C) + 1.00794 (H) + 15.999 (O)
o Молярная масса каждого атома = 12,0107 г / моль + 1,00794 г / моль (H) + 15,999 г / моль (O)
o Молярная масса соединения = (6 х 12,0107) + (12 х 1,00794) + (6 х 15,999) г / моль
= 180,15348 г / моль
Использование уравнения
Молярная масса может быть рассчитана с использованием уравнения, приведенного ниже. Это уравнение используется для определения неизвестного соединения. Рассмотрим следующий пример.
Молярная масса = Масса вещества (кг) / Количество вещества (моль)
- Соединение D находится в растворе. Детали даны следующим образом.
- Соединение D является сильной основой.
- Это может выпустить один H+ ион на молекулу.
- Раствор соединения D готовили с использованием 0,599 г соединения D.
- Реагирует с HCl в соотношении 1: 1
Затем определение может быть выполнено кислотно-основным титрованием. Поскольку это сильное основание, титруйте раствор сильной кислотой (например, HCl, 1,0 моль / л) в присутствии индикатора фенолфталеина. Изменение цвета указывает на конечную точку (например, при добавлении 15,00 мл HCl) титрования, и теперь все молекулы неизвестного основания титруют добавленной кислотой. Тогда молярная масса неизвестного соединения может быть определена следующим образом.
o Количество прореагировавшей кислоты = 1,0 моль / л х 15,00 х 10-3 л
= 1,5 х 10-2 моль
o Следовательно, количество прореагировавшего основания = 1,5 х 10-2 моль
o Молярная масса соединения D = 0,599 г / 1,5 х 10-2 моль
= 39,933 г / моль
o Тогда неизвестное соединение D можно предсказать как NaOH. (Но чтобы подтвердить это, мы должны сделать дальнейший анализ).
От точки кипения
Повышение температуры кипения представляет собой явление, которое описывает, что добавление соединения к чистому растворителю увеличило бы температуру кипения этой смеси до более высокой температуры кипения, чем у чистого растворителя. Следовательно, молярная масса этого добавленного соединения может быть найдена с использованием разности температур между двумя точками кипения. Если точка кипения чистого растворителя составляет Трастворитель и точка кипения раствора (с добавленным соединением) составляет ТрешениеРазница между двумя точками кипения может быть приведена ниже.
ΔT = Tрешение – Трастворитель
Используя соотношение Клаузиуса-Клапейрона и закон Рауля, мы можем получить связь между ΔT и молярностью решения.
ΔT = Kб , M
Где Кб является эбуллиоскопической константой и зависит только от свойств растворителя и М – моляльности
Из приведенного выше уравнения мы можем получить значение для моляльности решения. Поскольку количество растворителя, используемого для приготовления этого раствора, известно, мы можем найти значение для молей добавленного соединения.
Молярность = Моль добавленного соединения (моль) / Масса чистого используемого растворителя (кг)
Теперь, когда мы знаем моли соединения в растворе и массу добавленного соединения, мы можем определить молярную массу соединения.
Молярная масса = масса соединения (г) / моль соединения (моль)

Рисунок 01: Высота точки кипения и депрессия точки замерзания
От депрессии до точки замерзания
Понижение точки замерзания противоположно повышению температуры кипения. Иногда, когда соединение добавляют к растворителю, температура замерзания раствора ниже, чем у чистого растворителя. Тогда приведенные выше уравнения немного модифицируются.
ΔT = Tрешение – Трастворитель
Значение ΔT является отрицательным значением, поскольку точка кипения теперь ниже, чем начальное значение. Молярность раствора может быть получена так же, как в методе повышения температуры кипения.
ΔT = Kе , M
Здесь Кеизвестен как криоскопическая константа. Это зависит только от свойств растворителя.
Остальные расчеты такие же, как в методе повышения точки кипения. Здесь, моли добавленного соединения также могут быть рассчитаны с использованием приведенного ниже уравнения.
Молярность = Моль соединения (моль) / Масса используемого растворителя (кг)
Затем молярную массу можно рассчитать, используя значение для молей добавленного соединения и массы добавленного соединения.
Молярная масса = масса соединения (г) / моль соединения (моль)
От осмотического давления
Осмотическое давление – это давление, которое необходимо приложить, чтобы избежать попадания чистого растворителя в данный раствор посредством осмоса. Осмотическое давление может быть дано в уравнении ниже.
∏ = MRT
Где ∏ – осмотическое давление,
М – молярность раствора
R – универсальная газовая постоянная
Т – температура
Молярность решения определяется следующим уравнением.
Молярность = Моль соединения (моль) / Объем раствора (л)
Объем раствора может быть измерен, а молярность может быть рассчитана, как указано выше. Следовательно, моли соединения в растворе могут быть измерены. Тогда молярная масса может быть определена.
Молярная масса = масса соединения (г) / моль соединения (моль)
Какова важность знания молярной массы вещества
- Молярные массы различных соединений можно использовать для сравнения температур плавления и температур кипения этих соединений.
- Молярная масса используется для определения массовых процентов атомов, присутствующих в соединении.
- Молярная масса очень важна в химических реакциях для определения количества определенного реагирующего реагента или для определения количества продукта, который можно получить.
- Знание молярных масс очень важно, прежде чем будет разработана экспериментальная установка.
Резюме
Существует несколько методов для расчета молярной массы данного соединения. Самый простой способ среди них – это добавление молярных масс элементов, присутствующих в этом соединении.
Рекомендации:
1. «Крот». Энциклопедия Британника. Encyclopædia Britannica, inc., 24 апреля 2017 года. Интернет.
Загрузить PDF
Загрузить PDF
Атомы слишком малы, чтобы измерять ими массу химических веществ. Для работы с реальными количествами материи ученые ввели понятие моля. В один моль вещества входит столько же атомов, сколько содержится в 12 граммах изотопа углерод-12, что составляет примерно 6,022 x 1023 атомов. Эта постоянная величина получила название числа Авогадро.[1]
Данная константа применима для описания количества атомов или молекул любых веществ, причем масса одного моля вещества называется его молярной массой.
-

1
Ознакомьтесь с понятием молярной массы. Молярной массой какого-либо вещества называют массу (в граммах) одного моля этого вещества.[2]
Молярную массу химического элемента можно вычислить, умножив атомную массу этого элемента на коэффициент пересчета, измеряемый в граммах на моль (г/моль). -

2
Определите относительную атомную массу элемента. Относительной атомной массой какого-либо элемента называется средняя масса всех его изотопов, выраженная в атомных единицах массы (а.е.м.).[3]
Ее можно узнать из периодической таблицы Менделеева. Найдите в таблице необходимый элемент и обратите внимание на число, приведенное под символом этого элемента. Это нецелое число, имеющее знаки после десятичной запятой.- К примеру, относительная атомная масса водорода составляет 1,007, у углерода она равна 12,0107, у кислорода − 15,9994, у хлора − 35,453.
-

3
Умножьте относительную атомную массу на коэффициент пересчета, равный 0,001 килограмма, или 1 грамм на моль. Тем самым, переведя атомные единицы массы в граммы на моль, вы определите молярную массу элемента. Для водорода у вас получится 1,007 грамма на моль, для углерода − 12,0107 грамма на моль, для кислорода − 15,9994 грамма на моль, и для хлора − 35,453 грамма на моль.
- Некоторые элементы состоят из молекул, каждая из которых образована из двух или более атомов. Для того, чтобы определить молярную массу элемента, молекулы которого состоят из двух атомов (например, водорода, кислорода или хлора), следует найти его относительную атомную массу, умножить ее на коэффициент пересчета в граммы и дополнительно умножить на 2 (число атомов в одной молекуле).
- В случае H2 находим: 1,007 x 2 = 2,014 грамма на моль; для O2 получаем: 15,9994 x 2 = 31,9988 грамма на моль; для Cl2: 35,453 x 2 = 70,096 грамма на моль.
Реклама
-

1
Определите химическую формулу вещества. В этой формуле содержится информация о количестве атомов всех элементов, входящих в состав молекулы данного вещества. Химическую формулу интересующего вас вещества можно найти в справочнике по химии. Например, хлористоводородная (соляная) кислота имеет формулу HCl, а для глюкозы формула записывается как C6H12O6. По химической формуле вещества вы сможете определить число атомов каждого элемента, входящего в его состав.
- В случае HCl молекула состоит из одного атома водорода и одного атома хлора.
- Молекула глюкозы C6H12O6 состоит из 6 атомов углерода, 12 атомов водорода и 6 атомов кислорода.
-

2
Найдите относительные атомные массы всех элементов, входящих в состав данного вещества. Пользуясь периодической таблицей Менделеева, определите относительную атомную массу каждого элемента. Эта масса указана под символом соответствующего элемента. Как и в первом методе, необходимо умножить эти относительные атомные массы на 1 грамм/моль.
- Относительные атомные массы входящих в соляную кислоту водорода и хлора составляют 1,007 г/моль и 35,453 г/моль соответственно.
- Относительные атомные массы элементов, входящих в состав глюкозы, равны 12,0107 г/моль (углерод), 1,007 г/моль (водород) и 15,9994 г/моль (кислород).
-

3
Вычислите молярную массу каждого элемента, входящего в состав химического соединения. Умножьте атомную массу элемента на количество атомов этого элемента, содержащихся в одной молекуле вещества. Таким образом вы найдете относительное количество каждого элемента, входящего в состав рассматриваемого соединения.[4]
- Молярные массы элементов, входящих в состав соляной кислоты HCl, составляют 1,007 грамма на моль (водород) и 35,453 грамма на моль (хлор).
- Для элементов, входящих в состав глюкозы C6H12O6, получаем следующие молярные массы: 12,0107 x 6 = 72,0642 г/моль (углерод); 1,007 x 12 = 12,084 г/моль (водород); 15,9994 x 6 = 95,9964 г/моль (кислород).
-

4
Сложите молярные массы всех элементов, входящих в состав химического соединения. Таким образом вы определите молярную массу данного соединения. Возьмите найденные ранее молярные массы элементов и сложите их. В результате у вас получится молярная масса интересующего вас вещества.
- Для соляной кислоты находим: 1,007 + 35,453 = 36,460 г/моль. Таким образом, масса одного моля соляной кислоты составляет 36,46 грамма.
- Молярная масса глюкозы составляет 72,0642 + 12,084 + 95,9964 = 180,1446 г/моль, то есть в одном моле глюкозы содержится приблизительно 180,14 грамма.
Реклама
Советы
- Для большинства химических элементов относительные атомные массы известны с точностью до 4 знаков после запятой. В расчетах обычно учитывается только 2 знака после запятой. Поэтому, например, в лаборатории молярную массу водорода записали бы как 36,46 г/моль, а глюкозы − как 180,14 г/моль.
Реклама
Что вам понадобится
- Справочник по химии или периодическая таблица Менделеева
- Калькулятор
Похожие статьи
Об этой статье
Эту страницу просматривали 108 803 раза.
Была ли эта статья полезной?
Это отработанный пример задачи, показывающий, как рассчитать массовый процентный состав. Процентный состав указывает относительные количества каждого элемента в соединении. Для каждого элемента формула массового процента выглядит следующим образом:
% mass = (масса элемента в 1 моль соединения)/(молярная масса соединения) x 100%
или
массовый процент = (масса растворенного вещества/масса раствора) x 100%
Обычно единицы массы – граммы. Массовый процент также известен как массовый процент или мас./Мас.%. Молярная масса – это сумма масс всех атомов в одном моль соединения. Сумма всех массовых процентов должна составлять в сумме 100%. Следите за ошибками округления в последней значащей цифре, чтобы убедиться, что все проценты складываются.
Содержание
- Ключевые выводы
- Проблема массового процентного состава
- Процентный состав воды
- Массовый процент диоксида углерода
- Массовый процент раствора
- Советы по расчету массового процента
Ключевые выводы
- Состав в массовых процентах описывает относительные количества элементов в химическом соединении.
- Состав в массовых процентах также известен в процентах по массе. Он сокращенно обозначается как мас./Мас.%.
- Для раствора массовый процент равен массе элемента в одном моль соединения, деленной на молярную массу соединения, умноженную на 100%.
Проблема массового процентного состава
Бикарбонат соды (гидрокарбонат натрия) используется во многих коммерческих препаратах. Его формула – NaHCO 3 . Найдите массовые проценты (мас.%) Na, H, C и O в гидрокарбонате натрия.
Раствор
Сначала найдите атомные массы для элементов из Периодической таблицы. Атомные массы оказались следующими:
- Na = 22,99
- H = 1,01
- C – 12,01
- O – 16,00
Затем определите, сколько граммов каждого в одном моль NaHCO 3 :
- 22,99 г (1 моль) Na
- 1,01 г (1 моль) H
- 12,01 г (1 моль) C
- 48,00 г (3 моль x 16,00 грамм на моль) O
Масса одного моля NaHCO 3 составляет:
22,99 г + 1,01 г + 12,01 г + 48,00 г = 84,01 г
И масса процентное содержание элементов составляет
- масс.% Na = 22,99 г/84,01 г x 100 = 27,36%
- % масс H = 1,01 г/84,01 г x 100 = 1,20%
- % масс C = 12,01 г/84,01 г x 100 = 14,30%
- % масс O = 48,00 г /84,01 gx 100 = 57,14%
Ответ
- % масс Na = 27,36%
- % масс H = 1,20%
- массовый% C = 14,30%
- массовый% O = 57,14%
При вычислении массовых процентов всегда рекомендуется проверять, чтобы ваши массовые проценты в сумме составляли 100% (помогает отловить математические ошибки):
27,36 + 14,30 + 1,20 + 57,14 = 100. 00
Процентный состав воды
Другой простой пример – определение массового процентного состава элементов в воде, H 2 O.
Сначала найдите молярную массу воды, сложив атомные массы элементов. Используйте значения из периодической таблицы:
- H составляет 1,01 грамма на моль
- O составляет 16,00 граммов на моль
Получите молярную массу, сложив все массы элементов в соединении. Нижний индекс после водорода (H) указывает на наличие двух атомов водорода. После кислорода (O) нет индекса, что означает, что присутствует только один атом.
- молярная масса = (2 x 1,01) + 16,00
- молярная масса = 18,02
Теперь разделите массу каждого элемента на общую массу, чтобы получить массовые проценты:
масс% H = (2 x 1,01)/18,02 x 100%
масс% H = 11,19%
массовый% O = 16,00/18,02
массовый% O = 88,81%
Массовые проценты водорода и кислорода в сумме составляют 100%.
Массовый процент диоксида углерода
Какова масса процентное содержание углерода и кислорода в диоксиде углерода, CO 2 ?
Массовый процент раствора
Шаг 1: Найдите массу отдельных атомов.
Найдите атомные массы углерода и кислорода из Периодическая таблица. На этом этапе рекомендуется определиться с количеством значащих цифр, которые вы будете использовать. Атомные массы оказались следующими:
- C = 12,01 г/моль
- O = 16,00 г. /моль
Шаг 2: Найдите количество граммов каждого компонента, составляющего один моль CO. 2.
Один моль CO 2 содержит 1 моль атомов углерода и 2 моля атомов кислорода.
- 12,01 г (1 моль) C
- 32,00 г (2 моль x 16,00 грамм на моль) O
Масса одного моля CO 2 составляет:
- 12,01 г + 32,00 г = 44,01 г
Шаг 3: Найдите массовый процент каждого атома.
mass% = (масса компонента/масса всего) x 100
И массовые проценты элементов составляют
Для углерод:
- мас.% C = (масса 1 моля углерода/масса 1 моль CO 2 ) x 100
- мас.% C = (12,01 г/44,01 г) x 100
- массовый% C = 27,29%
Для кислорода:
- мас.% O = (масса 1 моля кислорода/масса 1 моль CO 2 ) x 100
- мас.% O = (32,00 г/44,01 г) x 100
- мас.% O = 72,71%
Ответ
- массовый% C = 27,29%
- массовый% O = 72. 71%
Опять же, убедитесь, что ваши массовые проценты в сумме составляют 100%. Это поможет выявить любые математические ошибки.
- 27,29 + 72,71 = 100,00
Сумма ответов составляет 100%, чего и ожидалось.
Советы по расчету массового процента
- Вам не всегда будет дана общая масса смеси или раствора. Часто вам нужно складывать массы. Это может быть неочевидно. Вам могут быть заданы мольные доли или моль, а затем потребуется преобразовать их в единицу массы.
- Следите за своими значащими цифрами.
- Всегда проверяйте сумму массовых процентов всех компонентов составляет 100%. В противном случае вам нужно вернуться и найти свою ошибку.
