Онлайн калькулятор поможет рассчитать температуру после смешивания воды, определить изменение температуры холодной и горячей жидкости при смешивании объемов в одной емкости.
Смешивание воды разной температуры – это процесс изменения температуры воды при её объединении в общий объем.
Формула определения итоговой температуры смеси: Tобщ = (Vгоряч × Tгоряч + Vхолодн × Tхолодн) / (Vгоряч + Vхолодн)
T – температура жидкости;
V – объём жидкости.
×
Пожалуйста напишите с чем связна такая низкая оценка:
×
Для установки калькулятора на iPhone – просто добавьте страницу
«На главный экран»
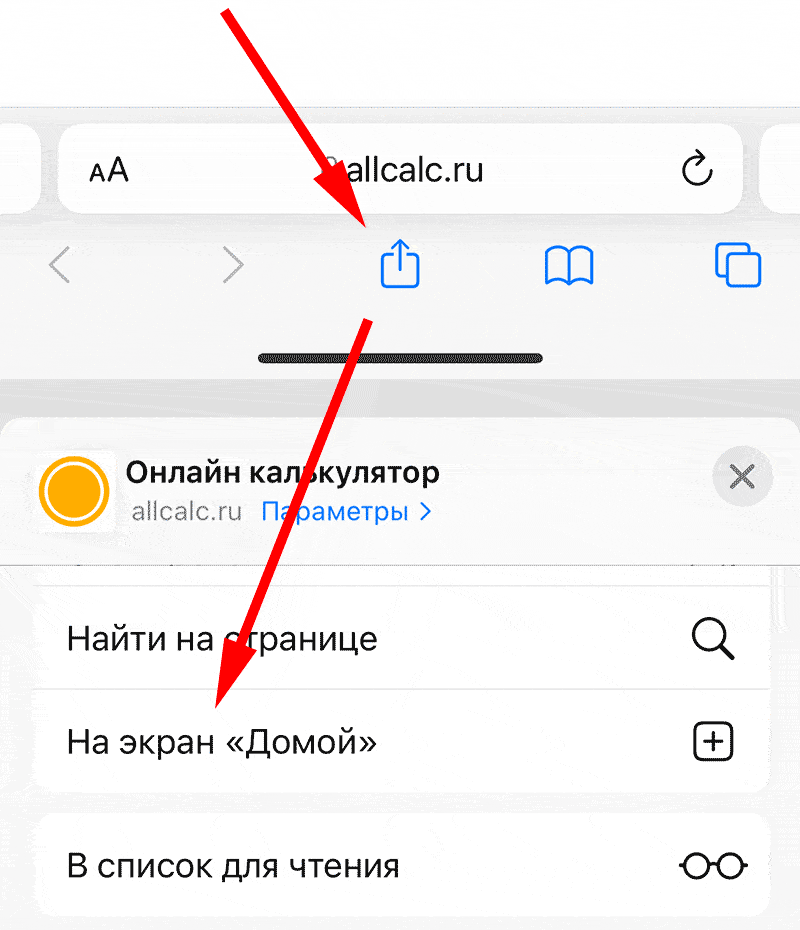
Для установки калькулятора на Android – просто добавьте страницу
«На главный экран»
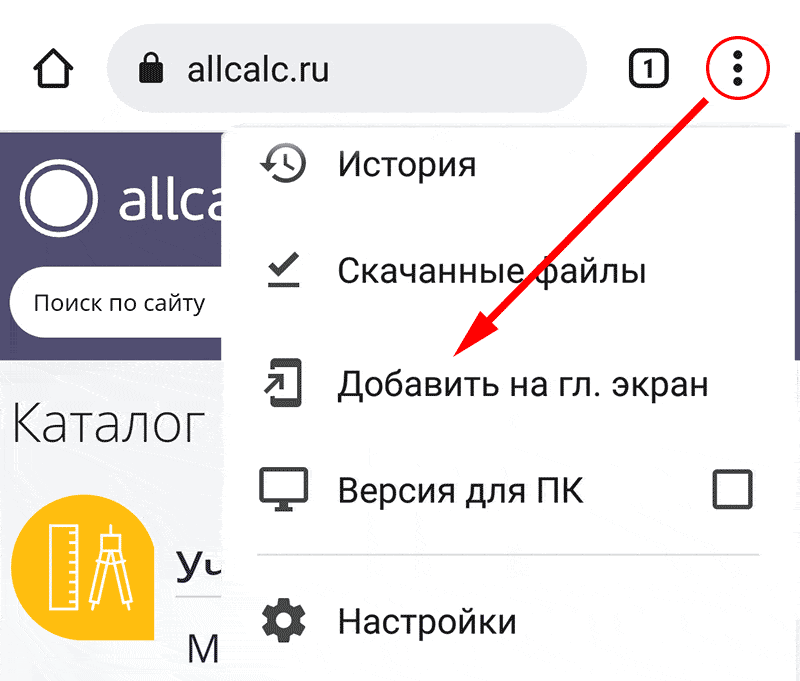
Расчет температуры смеси жидкой фазы груза
Теплота всегда
передается от более теплого тела к менее
теплому, иными словами, от тела с высокой
температурой — к телу с низкой
температурой.
Предположим, что два
вещества смешаны без образования
химической реакции, т. е. не возникает
выделения или поглощения тепла. В этом
случае можно сказать, что переданное
тепло равно теплу полученному. При этом
мы предполагаем, что передачи тепла
окружающей среде не происходит.
Теплота, которую одно
вещество передало другому в процессе
их смешивания, равна теплоте, полученной
другим веществом.
Иными словами, передача
теплоты будет происходить до тех пор,
пока температуры веществ не сравняются.
Такое определение
используется на практике при перевозке
газовой смеси сжиженных пропана и бутана
с разной теплоемкостью и разными
температурами при их смешивании на
борту судна.
В этом случае мы заранее
можем сосчитать температуру смеси
сжиженных газов, зная первоначальные
параметры каждого газа до их смешения.
А зная температуру смеси, мы можем
определить и давление в танке, и плотность
груза.
Прежде всего запишем
в виде формулы уже известное равенство
— теплота полученная равна теплоте
отданной:
m1
• C1
• ΔT1
=
т2
•
c2
•
ΔT2,
(1)
где левая половина
равенства определяет теплоту одной
жидкости, а правая — теплоту другой.
Наиболее просто это можно рассмотреть
на примере.
Пример:
Смешивают 5 кг пропана при температуре
tp
= -40°С и 8 кг бутана при температуре tb
=2°
С. Удельная теплоемкость пропана сp
= 2476 Дж/кг К, а бутана сb
= 2366 Дж/кг К. Определим температуру смеси
газов Тm.
Решение:
Ясно, что Тb
>
Тm
>
Тp
,
и можно записать для пропана
ΔTp
= (Tm-Tp),
a
для бутана ΔТb
= (Tb
—Tm),
Для нашего случая
ΔTp=
(Tm
– 233); ΔTb
= (275 – Tm).
Рассчитаем
температуру смеси по формуле (1):
mp
• cp
= ∆Tp
= mb
•cb
• ∆Tb
= 5
• 2476 • (Тm
-233) = 8 • 2366 • (275 –
Тm)
= 12380 • Тm
–
2884540 =
=
5205200 – 18928 • Тm
Отсюда 31308 • Тm
= 8089740, или
Тm
=
8089740 =
258,39 = 258,4 – 273 = -14,6°C
31308
В общем
случае расчет температуры смеси можно
выразить формулой:
ЗАКОН
ДАЛЬТОНА
Закон Дальтона можно
выразить следующим образом:
где pT
—
общее давление смеси газов; pA
+ pB
—
парциальное давление каждого газа; nА
—
количество молей газа А
в объеме; nВ
—
количество молей газа В
в объеме; R
—
универсальная газовая постоянная,
равная 8,314 Дж/(К • моль);
Т
—
абсолютная температура смеси газов; V
—
объем смеси газов, м3.
Давление смеси газов
равно сумме парциальных давлений
каждого из газов, составляющих смесь.
Парциальное давление
— это давление чистого газа (без
примесей) в данном объеме при заданной
температуре.
Для вычисления
давления смеси используют понятия
массовой концентрации газа gi
и молярной концентрации газа ri,
gi
= Gi
/ Gcm
, ri
= ni
/ ncm
,
где Gi
и
Gcm
—
масса газа и масса смеси газов; ni
и
ncm
—
количества вещества газа и смеси газов
(моль).
При перевозке смеси
сжиженных газов важно знать, какое
давление будет в танке при данной
температуре. Это требуется для определения
параметров компрессорной установки.
Рассмотрим несколько
простых методов расчета давления паров,
если известен молярный или весовой
состав смеси, погруженной на борт.
Пример: Судно должно
погрузить смесь газов, состоящую из
100 т пропана и 400 т бутана, температура
смеси составляет —8° С (см. расчет
температуры смеси газов). Давление
насыщенных паров пропана при этой
температуре, определенное по графику
или взятое из таблицы, 3,69 бара. А давление
насыщенных паров бутана при этой же
температуре 0,78 бара. Необходимо
определить давление насыщенных паров
смеси (т. е. общее давление в танке) и
процентный состав газовой фазы над
поверхностью жидкости.
Решение:
Рассчитаем молярное соотношение пропана
и бутана в составе смеси. Для этого
определим молярную массу пропана
C3H8
и
бутана C4H10.
С помощью периодической таблицы
элементов находим, что один атом углерода
имеет массу 12,01115 г/моль, а атом водорода
— 1,00797 г/моль.
Тогда молярная масса
пропана 12,01115 г/моль х 3 = 36,03345 г/моль
+
1,00797
г/моль х 8 = 8,06376 г/моль
44,09721
г/моль = 44,1 г/моль;
молярная масса бутана
12,01115 г/моль х 4 = 48,0446 г/моль
1,00797 г/моль х 10 = 10,0797
г/моль
58,1243
г/моль = 58,1 г/моль.
Теперь определим
количество молей каждого вещества в
смеси. Соотношение масс пропана и бутана
100 : 400; если использовать
не тонны, а граммы, то соотношение
останется тем же самым — 100 : 400. Рассчитаем
количество вещества (молей) из соотношения;
n
= т/Мr, где
n
— число молей; Mr
— молярная масса; m
— масса вещества.
Число молей пропана
100 г : 44,1 г/моль – 2,27 моля;
Число молей
бутана 400
г : 58,1 г/моль = 6,88 моля;
Общее число молей смеси
9,15 моля
Рассчитаем парциальное
давление пропана и бутана, используя
закон Рауля:
Молярный
состав пропана в жидкой фазе:
2,27=
0,248, или 24,8%.
9,15
Молярный состав бутана
в жидкой фазе: 6,88
= 0,752, или
75,2%.
9,15
Парциальное давление
пропана: 0,248 х 3,69 бар = 0,915 бара;
парциальное
давление бутана: 0,752
х 0,78 бар = 0,587 бара.
Давление
насыщенных паров смеси
1,502
бара,
давление в
танке (манометрическое)
≈
0,5 бара.
Состав смеси в газовой
фазе (над поверхностью жидкости) можно
рассчитать следующим образом:
содержание
пропана в газовой фазе: 0,915 бара : 1,502
бара = 0,60
→ 60,9%;
содержание
бутана в газовой фазе: 0,587 бара : 1,502
бара =
0,391 → 39,1%.
Как можно видеть, газ,
всасываемый компрессором в систему
повторного сжижения, состоит на 60,9% из
паров пропана и на 39,1% из паров бутана,
несмотря на то, что в жидкой фазе
содержится всего 24,8% пропана.
Такие
расчеты надо выполнять заранее, чтобы
определить установочное давление для
предохранительных клапанов на танках
(MARVS
— Maximum
Allowed
Relieve
Valve
Setting)
и максимально допустимое давление
конденсации смеси в системе повторного
сжижения, поскольку пропан имеет более
высокое давление конденсации, нежели
бутан.
Следует иметь в виду,
что все газы, перевозимые на судах,
фактически представляют собой смесь
целого ряда различных газов. Например,
промышленный пропан содержит от 95 до
98% пропана, 1—3% этана и около 1% бутана.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
08.02.201656.76 Кб41beklemishev1979_zool_besp.djvu
- #
- #
- #
- #
Смешиваем два объема воды с разной температурой. Как рассчитать температуру после смешивания?
Дед
Ученик
(249),
закрыт
10 лет назад
Рустам Искендеров
Искусственный Интеллект
(133392)
10 лет назад
Добавлю, хотя этого не требует автор:
Если смешиваемые жидкости разные, то t= (c1m1t1+ c2m2t2)/ (c1m1+ c2m2).
Если они растворяются друг в друге, то можно найти среднюю теплоёмкость для смеси: c= (c1m1+ c2m2)/ (m1+ m2).
Выше, понятно, подразумевается, что теплоёмкости – удельные массовые.
Полное условие задачи
Краткое условие задачи
Решение задачи
Запишем закон Дальтона для смеси газов:
Плотность смеси найдется следующим образом:
Запишем уравнение состояния идеального газа для гелия и кислорода:
Выразим массы гелия и кислорода:
Подставим массы в формулу для плотности смеси:
Из закона Дальтона имеем:
Тогда получаем:
Преобразуем последнее выражение:
Парциальное давление гелия определим через его концентрацию:
Подставляем это выражение вместо парциального давления гелия:
Подставляем данные и находим численный ответ:
Ответ: 300 К.
Как найти температуру смеси
Практическое значение имеет определение температуры смеси двух жидкостей. В этом случае рассматривается два варианта. Первый – определение температуры смеси однородных жидкостей. Для этого найдите их массы и начальные температуры, а затем рассчитайте температуру смеси. Второй – смесь разных жидкостей. Тогда для определения ее температуры найдите еще и их удельную теплоемкость.
Вам понадобится
- термометр, весы или мерный цилиндр, таблица удельных теплоемкостей веществ.
Инструкция
Температура смеси однородных жидкостейС помощью весов определите массы смешиваемых жидкостей в килограммах. В случае с водой (наиболее распространенном) можно измерить ее объем в литрах при помощи мерного цилиндра. Количество литров численно равно массе воды в килограммах. Измерьте температуру каждой жидкости в градусах Цельсия. Одна из них будет иметь большую температуру, а другая меньшую. Первая будет отдавать тепло, а другая – забирать. По окончании процесса их температуры сравняются.
Найдите произведение массы более теплой жидкости на ее температуру и сложите ее с произведением массы более холодной жидкости на ее температуру. Полученный результат поделите на сумму масс жидкостей (t=(m1•t1+m2•t2)/(m1+m2)). Результатом будет температура смеси однородных жидкостей. При практическом смешивании нужно максимально нейтрализовать влияние внешних факторов, поэтому смешивание лучше производить в калориметре.
Температура смеси различных жидкостейПеред смешиванием обязательно убедитесь, что оно возможно практически. Например, смешать воду и масло не удастся – масло окажется на поверхности воды. Найдите массы и начальные температуры жидкостей по методике, описанной в предыдущем пункте. В таблице удельных теплоемкостей найдите эти величины для жидкостей, которые смешиваете.
Далее этого произведите следующую последовательность математических действий:- найдите произведение удельной теплоемкости жидкости с большей начальной температурой на ее массу и температуру;
– найдите произведение удельной теплоемкости с меньшей начальной температурой на ее массу и температуру;
– найдите сумму чисел, полученных в пунктах 1 и 2;
– найдите произведение удельной теплоемкости жидкости с большей начальной температурой на значение этой температуры;
– найдите произведение удельной теплоемкости жидкости с меньшей начальной температурой на значение этой температуры;
– найдите сумму чисел, полученных в пунктах 4 и 5;
– поделите число, получившееся в пункте 3 на число, получившееся в пункте 6. t=(с1•m1•t1+с2•m2•t2)/(с1•m1+с2•m2).
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.

